一种四水氯化亚铁的制备方法与流程
本发明涉及一种利用盐酸洗废液制备氯化亚铁的方法,尤其是一种高纯度、大颗粒四水氯化亚铁的制备方法。
背景技术:
冶金、机械等行业在金属加工过程中,常采用强酸(盐酸或硫酸)对钢材表面进行酸洗,以去除钢材表面的氧化铁锈,酸洗外排的废液就成为酸洗废液。用盐酸清洗钢材表面氧化层,则会产生大量的盐酸洗废液,生产一吨钢材可产生酸洗废液约46~72kg。盐酸酸洗废液的主要成分为17%~22%的氯化亚铁,70%~75%的水以及3%~5%的盐酸,该废液具有严重的腐蚀性和危害性,已被列入《国家危险废物名录》代码为hw34废酸。该废液未经妥善处理而直接排放,不仅严重污染生态环境,而且造成了极大的资源浪费。
酸洗废液一般采用氢氧化钠或氢氧化钙与废液进行中和及沉淀金属离子,再经过压滤进行固液分离。该法工艺简单,但其产生了大量的金属盐泥渣,这部分泥渣处理困难,且容易对土地及地下水产生二次污染。目前,盐酸酸洗废液资源化的处理方法主要有以下几种:
(1)高温焙烧法,利用盐酸受热挥发,氯化亚铁高温氧化水解生成氧化铁和盐酸,该方法具有处理能力大,酸回收率高等优点,但其能耗高、投资大,设备维护成本高。
(2)萃取法,采用萃取剂将氯化氢从废酸液中转移到萃取剂中,再用水反萃取溶解再萃取剂中的氯化氢,从而实现盐酸和氯化亚铁的分离。该法能回收盐酸,但其产生了大量稀酸水,药剂成本较高。
(3)离子交换法,当废酸液通过阴离子交换树脂时,二价铁盐和三价铁盐被吸附并交换,然后用去离子水洗脱吸附饱和后的离子交换树脂,铁盐被交换得以再生。该法操作方便,但废酸液中酸度及金属离子含量较高,回收效果较差,树脂使用寿命低,处理成本高。
(4)膜处理法,利用选择透过性,膜在浓度差或在外界能量作用下,实现酸和金属盐从废酸中分离。但其处理量较低,膜组件易受到污染,维修费用高。
(5)结晶法,改变酸洗废液的理化性质,盐酸受热冷凝回收酸,铁盐以晶体的形式从废液中析出,从而实现酸、铁盐的分离。该法操作简便,运行费用低,可实现废酸再生利用。但传统制备四水氯化亚铁过程中,存在酸雾大、产品纯度低,结晶颗粒小,四水氯化亚铁分离回收率低等问题。
技术实现要素:
针对现有技术的不足,本发明提供一种四水氯化亚铁的制备方法,利用盐酸酸洗废液、钢铁氧化皮为原料制备四水氯化亚铁,不仅解决了环境危害问题,而且对危险废物资源实现回收利用。本发明克服了传统四水氯化亚铁工艺中产品存在纯度不高、结晶颗粒小、离心回收率低等问题的不足,提高四水氯化亚铁的纯度和回收率。本发明方法实现了酸洗废液资源化和无害化处理,同时具有良好的经济和环境效益。
一种四水氯化亚铁的制备方法,包括以下步骤:
采用盐酸酸洗废液溶解钢铁氧化皮,再与还原铁粉进行置换反应,过滤得到氯化亚铁溶液;将所述的氯化亚铁溶液依次进行蒸发浓缩、降温结晶、离心分离,获得四水氯化亚铁;
所述蒸发浓缩实施方式为采用多效蒸发器对氯化亚铁溶液进行蒸发浓缩,蒸发过程中无氯化亚铁结晶析出,蒸发出料温度为70~76.5℃,二价铁离子质量分数为20~21%。
在一个优选实施方案中,所述盐酸酸洗废液溶解钢铁氧化皮的反应条件为盐酸酸洗废液与钢铁氧化皮质量比为20:1~1.5,反应温度60~80℃,反应时间30~120min。
在一个优选实施方案中,所述置换反应中还原铁粉用量为钢铁氧化皮质量0.25~0.30倍,反应温度60~80℃,反应时间30~60min。
在一个优选实施方案中,所述氯化亚铁溶液中游离酸质量分数≤0.1%、三价铁离子质量分数≤0.01%。
在一个优选实施方案中,所述降温结晶过程中搅拌速度为50~100r/min。
在一个优选实施方案中,所述降温结晶的方式为采用冷却水对物料进行降温,降温时间为2~4h。
在一个优选实施方案中,所述降温结晶是将物料降温至12.3~30℃。
本发明的优点及积极作用有:
(1)本发明方法采用盐酸酸洗废液、钢铁氧化皮为原料制备四水氯化亚铁,不仅解决了环境危害问题,而且对危险废物资源实现回收利用,具有良好的环境和经济效益。
(2)本发明的方法通过对盐酸酸洗废液依次进行耗酸、置换还原,过滤除杂质,得到纯度高氯化亚铁溶液,并对其结晶过程进行控制,可制得纯度高、颗粒大的四水氯化亚铁成品,减少离心分离过程中产生的酸雾,产品回收率较高。
(3)本发明方法具有工艺简单、操作方便、成本费用低特点,容易实现工业化应用。
附图说明
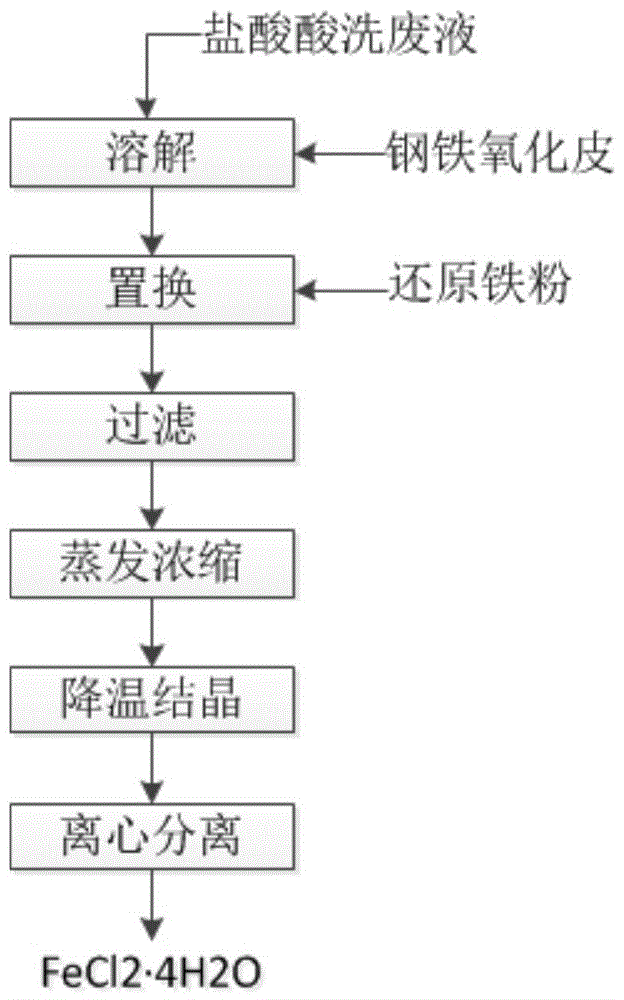
图1本发明方法工艺流程示意图。
图2氯化亚铁溶解度与温度关系示意图。
具体实施方式
用以下实施例对本发明方法的实现进行详细描述,应当理解此实施例仅用于解释本发明方法,并不用于限定本发明。
一种四水氯化亚铁的制备方法,包括以下步骤:
步骤1:采用盐酸酸洗废液溶解钢铁氧化皮,再与还原铁粉进行置换反应,过滤得到氯化亚铁溶液。
采用盐酸酸洗废液对钢铁氧化皮进行溶解,钢铁氧化皮主要成分为铁氧化物,将其与酸洗废液中盐酸进行反应,能有效降低盐酸酸洗废液中游离酸浓度,减少反应过程中酸雾产生,同时避免盐酸洗废液残留酸度过高与后续的还原铁粉反应产生氢气,消除安全隐患。
在一个实施方案中,盐酸酸洗废液溶解钢铁氧化皮的反应条件为盐酸酸洗废液与钢铁氧化皮质量比为20:1~1.5(其质量比可为20:1、20:1.25、20:1.5),反应温度为60~80℃(其温度范围应当为60、70、80℃),反应时间30~120min(即包含30、60、90、120min),溶解完全后,可得到游离酸质量分数较低的物料。
盐酸酸洗废液溶解钢铁氧化皮后,再用还原铁粉将低酸度的物料中三价铁离子充分还原为二价铁离子,并将物料中重金属离子置换出来,进一步降低游离酸浓度,提高二价铁离子的质量分数。若对盐酸酸洗废液直接进行蒸发浓缩、冷却结晶将得到金属杂质含量高、颗粒小的四水氯化亚铁,且在离心分离过程中,有大量酸雾挥发,对操作人员、环境、设备等均造成不利的影响。
在一个实施方案中,置换反应中还原铁粉用量为钢铁氧化皮质量0.25~0.30倍(其中包含0.25、0.27、0.30倍),反应温度60~80℃(其温度范围为60、70、80℃),反应时间30~60min(反应时间可为30、45、60min),过滤除去滤渣,获得游离酸质量分数低、三价铁离子含量少的氯化亚铁溶液。在一个实施方案中,氯化亚铁溶液中游离酸质量分数≤0.1%、三价铁离子质量分数≤0.01%。
步骤2:将所述的氯化亚铁溶液依次进行蒸发浓缩、降温结晶、离心分离,获得四水氯化亚铁。
形成四水氯化亚铁结晶,其结晶温度宜为12.3~76.5℃。若结晶温度较高(>76.5℃),则会形成二水氯化亚铁;结晶温度过低(<12.3℃),则形成六水氯化亚铁。在蒸发过程中,蒸发温度>76.5℃,需要控制氯化亚铁溶液的过饱和浓度,使氯化亚铁溶液不自发形成结晶,然后逐渐降温至结晶温度,析出四水氯化亚铁结晶。
在一个实施方案中,采用多效蒸发器对氯化亚铁溶液进行蒸发浓缩,蒸发过程中无氯化亚铁结晶析出,蒸发出料温度为70~76.5℃(温度可为70、72、74、76.5℃),二价铁离子质量分数为20~21%(其质量分数可为20、20.5、21%)。在该温度范围内,控制相应的氯化亚铁质量分数,避免其浓度过高析出二水氯化亚铁;氯化亚铁浓度太低,降低了四水氯化亚铁结晶产量。
在四水氯化亚铁结晶过程中,需要控制氯化亚铁的饱和度,降温速度过快,氯化亚铁饱和度过高,则析出四水氯化亚铁晶体颗粒细小。在结晶过程中,适度的搅拌能减少晶簇,避免结晶釜底部聚集成块;搅拌速度过快,破坏晶体的生长,使其颗粒度细小。
在一个实施方案中,降温结晶过程中搅拌速度为50~100r/min(搅拌速度可为50、75、100r/min)。在一个实施方案中,采用冷却水对物料进行降温,降温时间为2~4h(降温时间可为2、3、4h)。在一个实施方案中,降温结晶是将物料降温至12.3~30℃,然后进行离心分离获得四水氯化亚铁。
下面继续给出具体实施例进行详细说明。
实施例1
将1000g盐酸酸洗废液与50g钢铁氧化皮在温度为80℃下,搅拌速度为200r/min反应120min,得到降酸后酸洗液(fe:12.35%,fe2+:10.47%,hcl:0.42%);向降酸后酸洗液中加入15g还原铁粉,反应60min,过滤,获得氯化亚铁溶液(fe:13.42%,fe2+:13.41%,hcl:0.08%);对所述氯化亚铁溶液进行蒸发浓缩,出料温度为76℃,得到无氯化亚铁结晶析出氯化亚铁饱和溶液(fe:20.95%,fe2+:20.95%,hcl:0.10%),再进行搅拌降温,搅拌速度为70r/min,降温时间为3.5h,当物料温度为28℃,进行离心分离制得265g四水氯化亚铁。
实施例2
将1000g盐酸酸洗废液与75g钢铁氧化皮在温度为60℃下,搅拌速度为200r/min反应30min,得到降酸后酸洗液(fe:13.70%,fe2+:12.24%,hcl:0.42%);向降酸后酸洗液中加入18.75g还原铁粉,反应30min,过滤,获得氯化亚铁溶液(fe:14.17%,fe2+:14.17%,hcl:0.03%);对所述氯化亚铁溶液进行蒸发浓缩,出料温度为70℃,得到无氯化亚铁结晶析出氯化亚铁饱和溶液(fe:20.63%,fe2+:20.63%,hcl:0.04%),再进行搅拌降温,搅拌速度为50r/min,降温时间为2h,当物料温度为30℃,进行离心分离制得296g四水氯化亚铁。
实施例3
将1000g盐酸酸洗废液与62.5g钢铁氧化皮在温度为70℃下,搅拌速度为200r/min反应75min,得到降酸后酸洗液(fe:12.70%,fe2+:11.24%,hcl:0.42%);向降酸后酸洗液中加入16.8g还原铁粉,反应30min,过滤,获得氯化亚铁溶液(fe:13.57%,fe2+:13.57%,hcl:0.05%);对所述氯化亚铁溶液进行蒸发浓缩,出料温度为73℃,得到无氯化亚铁结晶析出氯化亚铁饱和溶液(fe:20.83%,fe2+:20.83%,hcl:0.06%),再进行搅拌降温,搅拌速度为100r/min,降温时间为4h,当物料温度为12℃,进行离心分离制得302g四水氯化亚铁。
对于本领域的技术人员来说,可根据以上技术方案以及构思,做出其他各种相应的改变以及变形,而所有的这些改变和变形都应该属于本发明权利要求的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!