一种
一种
18
f-tfb的制备方法
技术领域
1.本发明涉及药物合成技术领域,具体涉及一种正电子断层显像(pet)诊断用放射性药物的自动化合成方法。
背景技术:
2.四氟硼酸盐阴离子是碘化物的类似物,在生理条件下具有良好的相对稳定性和低毒性。
18
f-tfb用于nis的pet成像对于克服传统放射性碘和锝-99m示踪剂的许多局限性具有很大价值。
18
f-tfb已成为nis成像的一种有前途的碘类似物放射性示踪剂。早在20世纪50年代,anbar等人就报告了
18
f-tfb的放射性标记方法,并在20世纪60年代初对其与其他碘类似物的竞争结合进行了体外评估。这项开创性的研究表明了其在甲状腺成像方面的潜力。然而,这些研究是在临床pet出现之前三十年进行的,由于放射性碘和[99mtc]tco4-在spect nis成像中的应用,尽管
18
f-tfb具有潜力,但在半个世纪的文献中一直不活跃。直至2010年人们开始对
18
f-tfb进行了一系列更深入的研究,更新了标记方法、进行了动物的pet显像,
18
f-tfb的初步临床试验也已在健康人受试者和甲状腺癌患者中完成。
[0003]
在
18
f-tfb的放射化学标记方面,anbar等人发表的文章《the isotopic exchange of fluoroboric acid with hydrofuoride acid.》(anbar m,guttmann s.the j phys chem.1960;64:1896-9)最早报告了在酸性条件下使用加速器生成的[
18
f]氟化物在非放射性tfb上通过同位素交换进行放射性标记。2010年,文献《synthesis and biological evaluation of[
18
f]tetrafluoroborate:a pet imaging agent for thyroid disease and reporter gene imaging of the sodium/iodide symporter.》(jauregui-osoro m,sunassee k,weeks aj,berry dj,paul rl,cleij m,et al.eur j nucl med mol imag.2010;37:2108-16)报道更新了
18
f-tfb的放射性标记方法,其特点在于使用模块进行自动化标记,前体为四氟硼酸钠,在1.5m盐酸中加热120℃反应10分钟,用载银离子的阳离子交换柱和两个氧化铝柱进行纯化,标记用时短(39min),但存在比活度不高、放射化学产率较低(10%)的缺点。在《synthesis of[18f]tetrafluoroborate via radiofluorination of boron trifluoride and evaluation in a murine c6-glioma tumor model》(jiang h,bansal a,pandey mk,peng kw,suksanpaisan l,russell sj,et al.j nucl med.2016;57:1454-9)中报道了一种新的方法,以三氟化硼(bf3)为前体,在室温下将bf3溶液通过含有捕获的[
18
f]氟化物的qma柱时快速形成
18
f-tfb,其放射化学产率为20.0%,总合成时间为10min,但bf3为气体形态且具有毒性和腐蚀性,配制成溶液也相对复杂。《[
18
f]tetrafluoroborate as a pet tracer for the sodium/iodide symporter:the importance of specific activity》(khoshnevisan a,jauregui-osoro m,shaw k,torres jb,young jd,ramakrishnan nk,et al.ejnmmi res.2016;6:34)、《radionuclide-fluorescence reporter gene imaging to track tumor progression in rodent tumor models》(volpe a,man fa,lim ly,khoshnevisan a,blower je,blower pj,et al.j vis exp.2018;133.)报告了另一种利用bf3作为前体合成更高摩尔活性的
18
f-tfb的方法,[18f]
氟化物起始试剂呈共沸干燥的[
18
f]kf/k222/k2co3的形式,加入前体bf3·
et2o,反应在80℃下加热10分钟,经固相萃取小柱纯化后制得
18
f-tfb,但该标记方法放射化学产率亦不高(13.2%)。
技术实现要素:
[0004]
本发明要解决的技术问题是提供一种
18
f-tfb自动化的合成方法,以提升产率。
[0005]
本发明首先提供了一种
18
f-tfb的制备方法,其包括:
[0006]
1)获得
18
f-后蒸发除水,在无水条件下进行反应;
[0007]
2)将含有15-crown-5、bf3et2o的acn溶液置入反应容器中进行加热反应合成
18
f-tfb;
[0008]
3)将合成的
18
f-tfb经过固相萃取小柱进行纯化;
[0009]
其中,纯化前用无水乙醇溶液、纯水稀释后再经过氧化铝小柱进入缓冲瓶,进一步稀释后再经qma柱进行纯化。
[0010]
在根据本发明的一个实施方案中还包括:在反应前,qma上吸附的
18
f-用0.5ml生理盐水洗脱,反应在中性条件下进行。
[0011]
在根据本发明的一个实施方案中还包括:步骤3)中,在纯化前,分别稀释两次,第一次以1ml 50%的乙醇的水溶液稀释反应液,第二次以1ml纯水冲洗反应瓶,再通过氧化铝小柱,进入缓冲瓶。
[0012]
在根据本发明的一个实施方案中还包括:步骤3)中加入8ml纯水入缓冲瓶进行稀释,并将稀释溶液通过qma柱,并用4ml纯水冲洗固相萃取小柱。
[0013]
在根据本发明的一个实施方案中还包括:步骤3)中用4ml生理盐水、3ml注射用水将
18
f-tfb从固相萃取小柱洗脱。
[0014]
在根据本发明的一个实施方案中还制备过程是在fastlab2模块上进行的。
[0015]
本发明进一步提供了一种
18
f-tfb的制备方法,其包括:
[0016]
(1)将含有nabf4的hcl溶液预先置入反应容器中;
[0017]
(2)获得
18
f-后,用hcl溶液洗脱至上述反应容器中,在酸性水溶液、加热条件下进行反应合成
18
f-tfb;
[0018]
(3)将合成的
18
f-tfb经过固相萃取小柱进行纯化;
[0019]
其中,纯化前,用纯水稀释后经过silver-ion cation exchange cartridge纯化小柱及氧化铝纯化小柱进行纯化,收集溶液即可得
18
f-tfb。
[0020]
在根据本发明的一个实施方案中,步骤(1)中,在反应前,qma上吸附的
18
f-用0.45ml 2m hcl洗脱,反应在酸性水溶液条件下进行。
[0021]
在根据本发明的一个实施方案中,所述纯化前,用于稀释的纯水的体积为2-2.5ml。
[0022]
在根据本发明的一个实施方案中还包括:制备过程是在fastlab2模块上进行的。
[0023]
本发明的上述技术方案的有益效果如下:
[0024]
本发明的目的在于提供的
18
f-tfb合成方法可以在pet中心操作、安全、高效、产率高且纯度高。
附图说明
[0025]
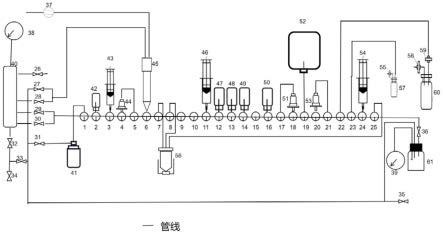
图1为本发明所用的一种装置示意图。
[0026]
图2为本发明所用的另一种装置示意图。
[0027]
图3为实施例1的分析hplc图谱。
[0028]
图4为实施例2的分析hplc图谱。
[0029]
[主要元件符号说明]
[0030]
1-25
ꢀꢀꢀꢀꢀ
第一-二十五三通阀
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
26-36
ꢀꢀꢀꢀꢀꢀ
第一-十一电磁阀
[0031]
37
ꢀꢀꢀꢀꢀꢀꢀ
18
f传输管开关
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
38-39
ꢀꢀꢀꢀꢀꢀ
第一、第二压力指示表
[0032]
40
ꢀꢀꢀꢀꢀꢀꢀ
气体缓冲瓶
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
41
ꢀꢀꢀꢀꢀꢀꢀꢀꢀ
18
o水收集瓶
[0033]
42
ꢀꢀꢀꢀꢀꢀꢀ
装载生理盐水的试剂瓶
ꢀꢀꢀꢀꢀꢀꢀ
43
ꢀꢀꢀꢀꢀꢀꢀꢀꢀ
注射器
[0034]
44
ꢀꢀꢀꢀꢀꢀꢀ
qma固相萃取小柱
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
45
ꢀꢀꢀꢀꢀꢀꢀꢀꢀ
加载
18
f离子的注射器
[0035]
46
ꢀꢀꢀꢀꢀꢀꢀ
注射器
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
47
ꢀꢀꢀꢀꢀꢀꢀꢀꢀ
装载15-crown-5、bf3et2o的乙腈溶液的试剂瓶
[0036][0037]
48
ꢀꢀꢀꢀꢀꢀꢀ
装载无水乙腈的试剂瓶
ꢀꢀꢀꢀꢀꢀꢀ
49
ꢀꢀꢀꢀꢀꢀꢀꢀꢀ
装载50%乙醇水溶液的试剂瓶
[0038]
50
ꢀꢀꢀꢀꢀꢀꢀ
装载生理盐水的试剂瓶
ꢀꢀꢀꢀꢀꢀꢀ
51
ꢀꢀꢀꢀꢀꢀꢀꢀꢀ
氧化铝固相萃取小柱
[0039]
52
ꢀꢀꢀꢀꢀꢀꢀ
水袋
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
53
ꢀꢀꢀꢀꢀꢀꢀꢀꢀ
qma固相萃取小柱
[0040]
54
ꢀꢀꢀꢀꢀꢀꢀ
注射器
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
55
ꢀꢀꢀꢀꢀꢀꢀꢀꢀ
通气滤膜
[0041]
56
ꢀꢀꢀꢀꢀꢀꢀ
带加热功能的反应器
ꢀꢀꢀꢀꢀꢀꢀꢀꢀ
57
ꢀꢀꢀꢀꢀꢀꢀꢀꢀ
缓冲瓶
[0042]
58
ꢀꢀꢀꢀꢀꢀꢀ
通气滤膜
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
59
ꢀꢀꢀꢀꢀꢀꢀꢀꢀ
无菌滤膜
[0043]
60
ꢀꢀꢀꢀꢀꢀꢀ
无菌产品瓶
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
61
ꢀꢀꢀꢀꢀꢀꢀꢀꢀ
废液瓶
[0044]1’‑
25
’ꢀ
第一-二十五三通阀
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
26
’‑
36
’ꢀ
第一-十一电磁阀
[0045]
37
’ꢀꢀꢀꢀꢀ
18f传输管开关
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
38
’‑
39
’ꢀ
第一、第二压力指示表
[0046]
40
’ꢀꢀꢀꢀꢀ
气体缓冲瓶
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
41
’ꢀꢀꢀꢀꢀꢀ
18o水收集瓶
[0047]
42
’ꢀꢀꢀꢀꢀ
装载盐酸的试剂瓶
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
43
’ꢀꢀꢀꢀꢀꢀ
注射器
[0048]
44
’ꢀꢀꢀꢀꢀ
qma固相萃取小柱
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
45
’ꢀꢀꢀꢀꢀꢀ
加载18f离子的注射器
[0049]
46
’ꢀꢀꢀꢀꢀ
注射器
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
47
’ꢀꢀꢀꢀꢀꢀ
水袋
[0050]
48
’ꢀꢀꢀꢀꢀ
silver-ion cation exchange 49
’ꢀꢀꢀꢀꢀꢀ
氧化铝固相萃取小柱
[0051]
ꢀꢀꢀꢀꢀꢀꢀꢀ
cartridge固相萃取小柱
[0052]
50
’ꢀꢀꢀꢀꢀ
注射器
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
51
’ꢀꢀꢀꢀꢀꢀꢀ
通气滤膜
[0053]
52
’ꢀꢀꢀꢀꢀ
无菌滤膜
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
53
’ꢀꢀꢀꢀꢀꢀꢀ
无菌产品瓶
[0054]
54
’ꢀꢀꢀꢀꢀ
废液瓶
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
55
’ꢀꢀꢀꢀꢀꢀꢀ
带加热功能的反应器
具体实施方式
[0055]
为使本发明要解决的技术问题、技术方案和优点更加清楚,下面将结合附图及具体实施例进行详细描述。
[0056]
实施例1
[0057]
在如图1所示的fastlab2模块上合成
18
f-tfb。如图1所示的,管路起始端设置有气
体缓冲瓶40,并设置有第一-十一电磁阀(26-34),其中,第四电磁阀29、第五电磁阀30通过管路与主管路连通,主管路依次设置有第一三通阀1、第二三通阀2、第三三通阀3、第四三通阀4、第五三通阀5、第六三通阀6、第七三通阀7、第八三通阀8、第九三通阀9、第十三通阀10、第十一三通阀11、第十二三通阀12、第十三通阀13、第十四三通阀14、第十五三通阀15、第十六三通阀16、第十七三通阀17、第十八三通阀18、第十九三通阀19、第二十三通阀20、第二十一三通阀21、第二十二三通阀22、第二十三三通阀23、第二十四三通阀24、第二十五三通阀25;第二三通阀2处连接装载生理盐水的试剂瓶42,第三三通阀3处连通注射器43,第四三通阀和第五三通阀5同时连通qma固相萃取小柱44,第六三通阀6连通加载18f离子的注射器45,注射器45同时经由第二电磁阀27和第三电磁阀28与气体缓冲瓶40连通;第七三通阀7和第八三通阀8同时连通带加热功能的反应器56,同时,带加热功能的反应器56还与第二十五三通阀25连通;
[0058]
第十一三通阀11连通装载15-crown-5、bf3et2o的乙腈溶液的试剂瓶47,第十二三通阀12连通装载无水乙腈的试剂瓶48,第十三三通阀13连通装载50%乙醇水溶液的试剂瓶49,第十六三通阀16连通装载生理盐水的试剂瓶50,第十七三通阀17和第十八三通阀18同时连通氧化铝固相萃取小柱51,第十九三通阀19连通水袋52,第二十三通阀20和第二十一三通阀21同时连通qma固相萃取小柱53,第二十二三通阀22经由无菌滤膜59连通无菌产品瓶60,同时,无菌产品瓶60还设置有通气滤膜58;第二十三三通阀23连通缓冲瓶57,所述缓冲瓶57上还设置有通气滤膜55;第二十四三通阀24连通注射器54。
[0059]
主管路的末端经由第十一电磁阀36连通废液瓶61,同时,废液瓶61还设置有第二压力指示表39,并且分别与第二电磁阀27、第三电磁阀28、第四电磁阀29、第五电磁阀30、第六电磁阀31以及第八电磁阀33通过管路连通。
[0060]
由加速器生产的含放射性
18
f-离子通过氮气传到fastlab2模块的加载18f离子的注射器(45)中,再吸附到qma固相萃取小柱(44)上,0.5ml生理盐水溶液由装载生理盐水的试剂瓶(42)将
18
f-从qma固相萃取小柱(44)上淋到带加热功能的反应器(56),由装载无水乙腈的试剂瓶(48)加入1ml乙腈共沸除水,再次加入1ml乙腈到带加热功能的反应器(56),共沸除水。
[0061]
将1ml含有24mg 15-crown-5、0.2ul bf3et2o的乙腈溶液由装载15-crown-5、bf3et2o的乙腈溶液的试剂瓶(47)加入带加热功能的反应器(56)中,加热到105℃反应10min。
[0062]
利用装载50%乙醇水溶液的试剂瓶(49)向带加热功能的反应器(56)内加入1ml的50%乙醇的水溶液,将混合液经过氧化铝固相萃取小柱(51)到缓冲瓶(57),再由水袋(52)加1ml注射用水至带加热功能的反应器(56)中冲洗残留反应液,并通过氧化铝固相萃取小柱(51)转移至缓冲瓶(57)中;再通过水袋(52)加8ml注射用水至缓冲瓶(57)稀释混合液。
[0063]
将缓冲瓶(57)中的液体转移至qma固相萃取小柱(53),并4ml水冲洗qma固相萃取小柱(53)后,操作装载生理盐水的试剂瓶(50)和水袋(52)以4ml生理盐水、3ml注射用水将
18
f-tfb从qma固相萃取小柱(53)洗脱,通过无菌滤膜(59)后收集洗脱液于无菌产品瓶(60)中。
[0064]
制备用时总计为38min,合成效率为15%。产品分析hplc结果如图3
,
保留时间为9.3min,纯度》95%。
[0065]
实施例2.
[0066]
在如图2所示fastlab2模块上合成
18
f-tfb,如图2所示的,管路起始端设置有气体缓冲瓶40',并设置有第一-十一电磁阀(26'-34'),其中,第四电磁阀29'、第五电磁阀30'通过管路与主管路连通,主管路依次设置有第一三通阀1'、第二三通阀2'、第三三通阀3'、第四三通阀4'、第五三通阀5'、第六三通阀6'、第七三通阀7'、第八三通阀8'、第九三通阀9'、第十三通阀10'、第十一三通阀11'、第十二三通阀12'、第十三通阀13'、第十四三通阀14'、第十五三通阀15'、第十六三通阀16'、第十七三通阀17'、第十八三通阀18'、第十九三通阀19'、第二十三通阀20'、第二十一三通阀21'、第二十二三通阀22'、第二十三三通阀23'、第二十四三通阀24'、第二十五三通阀25';第二三通阀2'处连接装载生理盐水的试剂瓶42',第三三通阀3处连通注射器43',第四三通阀4'和第五三通阀5'同时连通qma固相萃取小柱44',第六三通阀6'连通加载18f离子的注射器45',注射器45'同时经由第二电磁阀27'和第三电磁阀28'与气体缓冲瓶40'连通;第七三通阀7'和第八三通阀8'同时连通带加热功能的反应器55',同时,带加热功能的反应器55'还与第二十五三通阀25'连通;
[0067]
第十一三通阀11'连通装载15-crown-5、bf3et2o的乙腈溶液的试剂瓶46',第十七三通阀17'连通水袋47',
[0068]
第十八三通阀18'和第十九三通阀19'同时连通氧化铝固相萃取小柱48',第二十三通阀20'和第二十一三通阀21'同时连通qma固相萃取小柱49',第二十二三通阀22'经由无菌滤膜52'连通无菌产品瓶53',同时,无菌产品瓶53'还设置有通气滤膜51';第二十四三通阀24'连通注射器50'。
[0069]
主管路的末端经由第十一电磁阀36'连通废液瓶54',同时,废液瓶54'还设置有第二压力指示表39',并且分别与第二电磁阀27'、第三电磁阀28'、第四电磁阀29'、第五电磁阀30'、第六电磁阀31'以及第八电磁阀33'通过管路连通。
[0070]
将50μl含有1mg nabf4的2m hcl溶液加入带加热功能的反应器(55’)。由加速器生产的含放射性
18
f-离子通过氮气传到fastlab2模块的加载
18
f离子的注射器(45’),再吸附到qma固相萃取小柱(44’),0.45ml 2m hcl溶液由装载盐酸的试剂瓶(42’)加入到qma固相萃取小柱(44’)将
18
f-从qma固相萃取小柱(44’)上淋到带加热功能的反应器(55’),加热到40℃反应20min。
[0071]
由水袋(47’)向带加热功能的反应器(55’)内加入2.5ml的注射用水,将混合液silver-ion cation exchange cartridge固相萃取小柱(48’),以及氧化铝固相萃取小柱(49’)进行纯化,通过无菌滤膜(52’)后收集洗脱液于无菌产品瓶(53’)中。
[0072]
制备用时总计为27min,合成效率为45%。产品分析hplc结果如图4,保留时间为9.3min,纯度》95%。
[0073]
以上所述是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明所述原理的前提下,还可以做出若干改进和润饰,这些改进和润饰也应视为本发明的保护范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1