一种从肿节风药材中制备异秦皮啶方法与流程
本发明涉及一种异秦皮啶制备方法,属于药用活性成分提取
技术领域:
。
背景技术:
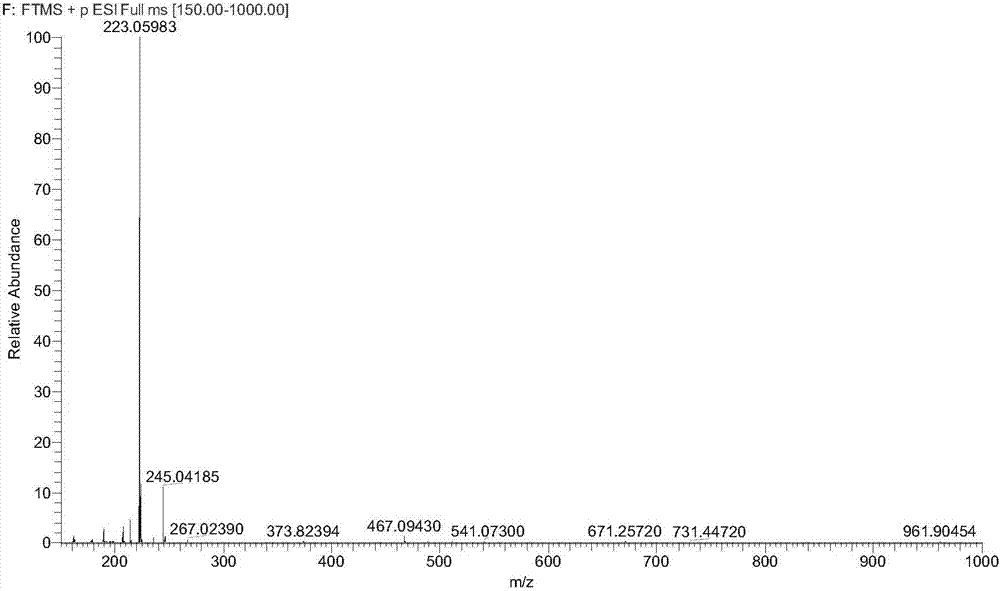
:异秦皮啶是天然香豆素类成分,具有较好的体内抗炎、镇痛、抗感染作用(xiaofengniu等,internationalimmunopharmacology.2015.24:432–439;lingliu等,immunobiology,2015,220:406–413;xiaofengniu等,internationalimmunopharmacology.2012.14:164–171),是中药肿节风、刺五加药材特征性成分,并作为药材质量控制指标性成分收载于2015版中国药典(中国药典,2015版,i部,第206、224页),用于肿节风、刺五加药材及其制剂质量控制。目前文献报道异秦皮啶的制备方法有大孔树脂色谱法(何行真,江西中医学院学报,2007,19(4):45-46)、高速逆流色谱法(江永南等,中药材,2008,31(6):913-915)。但大孔树脂分离法制备获得的香豆素粗品部位中异秦皮啶含量仅为2.59%,而采用高速逆流仪器贵重成本高、有机溶剂用量大,且制备富集部位仍为粗品,异秦皮啶得率只有3%。其它已申请发明专利的异秦皮啶制备工艺方法包括从刺五加根茎中醇提取、酸水解、1,1-二氯乙烷萃取获得异秦皮啶,但也仅为粗产品(祖元刚,一种从刺五加根茎中制备异秦皮啶的方法,专利号:201010184243.7)。迄今为止,还没有一种简单可行、制备成本相对低廉的异秦皮啶单体制备工艺公开报道。技术实现要素:本发明是克服现有技术不足,提供一种操作简单、成本低廉且所得产品纯度高的异秦皮啶制备方法。本发明目的的实现方式为:a.取肿节风药材饮片,用5-15倍原材料重量水加热取2次,每次30〜120min,合并提取滤液,过滤,滤液备用;b.滤液浓缩至适当体积,环己烷-乙酸乙酯(1:1,体积比)等体积萃取1-4次;c.环己烷-乙酸乙酯萃取相真空减压浓缩,有机溶剂复溶,1-3倍硅胶干法拌样,经5-20倍硅胶柱层析,石油醚:丙酮(15:8,体积比)洗脱,薄层分析,合并含有异秦皮啶流分;d.甲醇复溶富含异秦皮啶合并流分,经凝胶柱色谱,甲醇洗脱脱色素,再经ods柱色谱,meoh-h2o洗脱,得纯度大于85%粗品异秦皮啶,甲醇-水重结晶,即得纯度大于99%纯品。与现有技术相比,本发明的优点在于:本发明提取用原料药材来源广泛、价格低廉;对肿节风药材饮片采用水加热提取方法,大大减少了全草类药材提取液中色素类杂质;根据异秦皮啶兼有亲水、亲酯性特点,采用环己烷-乙酸乙酯混合有机溶剂萃取,能最大程度减少其它水溶性成分共萃取,降低色素干扰,从而减少后续繁琐的去除无关杂质及色素分离操作;液液萃取用有机溶剂可回收反复利用;本发明操作简单,无需用到贵重仪器设备,从而使样品制备成本大大减低。附图说明图1是异秦皮啶uv吸收光谱图。图2是异秦皮啶电喷雾(esi)正离子模式高分辨质谱图。图3是异秦皮啶氢核磁(1h-nmr,500mhz,dmso-d6)谱图。图4是异秦皮啶碳核磁(1h-nmr,125mhz,dmso-d6)谱图。图5是肿节风水提取液hplc色谱图。图6是肿节风水提取液环己烷-乙酸乙酯萃取部分hplc色谱图。图7是分离制备异秦皮啶hplc色谱图。具体实施方式实施例1.异秦皮啶提取分离取肿节风全草药材12kg(约3cm/段),置100l中药提取罐中,第一次加84l水浸润0.5小时,100℃加热煎煮2h,第二次加42l水100℃加热煎煮1.5h,,纱布滤过,浓缩至7l(相当于药材浓度约1.7g/ml),环己烷-乙酸乙酯(1:1)等体积萃取4次,合并萃取液,浓缩干燥,乙酸乙酯-甲醇溶解萃取回收可溶部分(44g),100g柱层析硅胶(100~200目)均匀拌样,室温挥去溶剂,700g柱层析硅胶(200~300目)干法装柱,石油醚ii:丙酮(15:8)梯度洗脱2个柱体积,每500ml为一个流分收集,浓缩回收有机相,得各子流分,薄层分析,石油醚ii(沸点60-90℃):丙酮(1:1)展开,石油醚ii:丙酮(15:8)洗脱第6-16瓶在紫外灯365nm下与异秦皮啶对照品相同位置显天蓝色荧光斑点。合并含异秦皮啶留分,经凝胶(sephadexlh-20)柱层析,甲醇洗脱,薄层分析,合并含有异秦皮啶子流分,再经ods柱色谱,甲醇-水(20:80®30:70)洗脱,30%甲醇洗脱部分得异秦皮啶粗品(2.9g),经甲醇-水重结晶,即得异秦皮啶纯品。2.异秦皮啶结构鉴定白色粉末(meoh),uvλmax(meoh)nm:342nm(附图1);hr-esi-ms+:m/z223.05983[m+h]++(calcdforc11h11o5+,-1.2ppm)(附图2).1h-nmr(500mhz,dmso-d6)δ:7.89(1h,d,j=9.5hz,h-4),6.22(1h,d,j=9.5hz,h-3),7.01(1h,s,h-5),3.82(3h,s,6-och3),3.81(3h,s,8-och3)。13c-nmr(125mhz,dmso-d6)δ:160.7(c-2),146.2(c-6),145.3(c-4),144.9(c-9),143.5(c-7),135.2(c-8),112.1(c-3),104.9(c-5),110.4(c-10),61.0(och3-8),56.6(och3-5),见附图3-4。以上核磁数据与文献[许旭东,胡晓茹,袁经权,杨峻山,等.草珊瑚中香豆素化学成分研究.中国中药杂志.2008,33(8),900-902]报道基本一致。3.异秦皮啶高效液相分析3.1定性分析仪器:waters2695高效分析液相,配2998pad二极管整列检测器。主要色谱条件:色谱柱:xbridgetmc18(4.6´250mm,5μm);柱温:40℃;流速0.8ml/min;检测波长:330nm;流动相:甲醇(a)-0.1%甲酸水(b)梯度洗脱条件为0-10min,20®22%a,10-30min,20®37%a,30-45min,37®42%a;进样体积:20μl。供试品溶液制备及分析:分别制备相当于肿节风药材0.2g/ml的药材水提取液、相当于萃取物10mg/ml的有机溶剂萃取部分以及从肿节风中分离制备的异秦皮啶对照品供试品溶液,进样hplc分析,色谱图见附图5-7。3.2定量分析检测波长:341nm;流动相:乙腈-0.1%磷酸水(20:80);其它条件同3.1定性分析。对照品溶液配制及标准曲线建立:异秦皮啶标准品(中检所,批次110837-201507,含量以99.2%计),十万分之一精密分析天平分别精密称取1.03、1.07mg,移取1ml甲醇,超声溶解,即得母液存储液,其中浓度为1.03mg/ml母液分别稀释2,4,6,8,16,32,64,128,256倍,进样20μl,用于标准曲线建立,浓度为1.07mg/ml稀释8倍用于质控,经仪器分析软件处理,线性方程为y=6.54e+004x-7.08e+004,r=0.9999,线性范围为3.99-510.88μg/ml。供试品溶液制备及含量测定:分别平行制备3份qc质控液、异秦皮啶粗品、异秦皮啶重结晶、肿节风全草水提液(相当于药材0.2g/ml)以及肿节风全草水提环己烷-乙酸乙酯(1:1)萃取部分(相当于萃取浸膏0.01g/ml),hplc进样分析,计算含量,测得结果见表一。表一.制备异秦皮啶及样品测定结果样品质控样品异秦皮啶粗品异秦皮啶结晶水提液萃取物含量(%)98.6±1.086.5%±0105.5±0.40.03±02.8±0.13.3结果分析从表一可知,结晶后异秦皮啶纯度可达105%,可以用于含量测定。从附图5-7可知,在同一检测波长下,肿节风水提取物中除保留时间为16.0min异秦皮啶目标成分,还有其它干扰性成分,而在肿节风水提物环己烷-乙酸乙酯(1:1)萃取部分,只有异秦皮啶一个主成分,进一步测得在其萃取物中含量是药材中含量93倍(表一),采用环己烷-乙酸乙酯液液萃取方法优势明显。本工艺流程换算成药材制备异秦皮啶得率约0.025%,制备得率较高,从而使样品制备成本大大减低。以上所述仅为本发明的较佳实施例,并不用以限制本发明,凡在本发明的精神和原则之内所作的任何修改、同等替换和改进等,均应落在本发明的保护范围之内。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1