一种肌钙蛋白I单克隆抗体磁微粒及其制备方法和检测试剂盒与流程
本发明涉及体外诊断医学检验领域。具体地说,本发明涉及一种肌钙蛋白i单克隆抗体磁微粒及其制备方法和包括其的肌钙蛋白i检测试剂盒。
背景技术:
肌钙蛋白(tn)是心肌组织的一种特有调节蛋白,严重心肌损伤时释放入血液,是反映心肌损伤的血清标志物。tn是由tni、tnt、tnc三个亚单位组成。tnc为ca2+的结合位点,肌肉收缩时活化细肌丝;tnt能结合原肌球蛋白;而tni为抑制性亚单位,可抑制肌球蛋白与肌动蛋白结合,阻止肌肉收缩。正常人血液中ctni(肌钙蛋白i)含量一般低于0.3ug/l,当肌细胞受到损伤时,游离的ctni先释放入血,随着损伤加重,导致血中ctni持续升高。
急性心肌梗死(ami)为不可逆的急性心肌细胞坏死。发病后4-6h,血清ctni水平升高,18-24h达高峰,恢复正常时间平均为99h,少数患者1周降至正常。因ctni在血中升高的时间与ck-mb相似,而持续时间较长,对急性或亚急性心肌梗塞的诊断具有重要的价值。同时ctni是溶栓治疗血管是否再通的早期敏感指标。ctni在诊断心肌梗死面积方面已有很好的相关性,对单独骨骼肌损伤、外伤、肾病均不会引起ctni升高,其敏感性和特异性优越,对判断预后有重要意义。ctni诊断ami特异性99%,而ck-mb为81%。ctni检测具有早期快速的特点,可作为ami诊断和判断预后的最敏感、最特异性的指标之一,逐渐取代ck-mb成为判断心肌损伤,特别是诊断ami的“金标准”。
血清ctni在检测不稳定性心绞痛(uap)患者轻微心肌细胞损伤方面比ck-mb更敏感,在uap检测方面有重要的预后判断价值。ctni对轻度心肌损伤是一个非常灵敏的指标。观察发现心力衰竭患者ctni轻度增高,心功能正常时ctni正常,可作为判断临床预后的指标。在病毒性心肌炎急性期患者血清ctni阳性率达88.9%。心律失常射频消融治疗的患者血清ctni可呈轻度升高,检测为弱阳性。血清ctni在心肌炎症和轻微损伤的判断上具有临床应用价值,在cabg围手术期心肌损伤的判断方面也是一个非常灵敏的指标。
目前临床上肌钙蛋白的检测方法主要有胶体金法、免疫比浊法、免疫荧光法、化学发光免疫分析法等。胶体金法的缺点在于无法准确进行定量,且批间差异较大,无法持续监控患者肌钙蛋白i的水平;免疫比浊法的缺点在于试剂灵敏度较差,对于心肌梗死的判断不利;免疫荧光法但依然存在反应时间较长,对环境要求较高,容易受空气尘埃影响,且多为96人份/盒,使用稀土标记物等缺点也使得此免疫方法无法大规模使用。化学发光免疫分析法法是一种较为先进的免疫学方法,具有反应时间短、灵敏度高、特异性好、线性范围宽、重复性好等优点,标记物稳定性好,在保证检测速度的前提下,也能达到检测高通量。根据目前肌钙蛋白i临床的应用情况,市场应用前景最好且诊断最可靠的方法学为化学发光免疫分析法。
虽然目前中国市场上已有注册批准的肌钙蛋白i化学发光免疫分析法测定试剂盒,但多为进口试剂,成本较高,且试剂盒的制备方法和相关材料均作为保密资料,未被公开,不利于肌钙蛋白i检测在社区基层医院的推广。国产肌钙蛋白i试剂盒重复性较差,批间差异难控,且灵敏度较低,交叉反应率较高,临床应用前景较差。
因此,本领域急需一种具有检测灵敏度高、特异性好、重复性高等优点的肌钙蛋白i检测试剂盒。
技术实现要素:
本发明的目的是提供一种肌钙蛋白i单克隆抗体磁微粒及其制备方法,利用所述肌钙蛋白i单克隆抗体磁微粒检测肌钙蛋白i的灵敏度大幅提高。
本发明还有一目的是提供包括上述肌钙蛋白i单克隆抗体磁微粒的肌钙蛋白i检测试剂盒。
本发明再有一目的是提供利用本发明的肌钙蛋白i单克隆抗体磁微粒或肌钙蛋白i检测试剂盒检测肌钙蛋白i的方法。
本发明公开了一种肌钙蛋白i单克隆抗体磁微粒及其制备方法和包括所述肌钙蛋白i单克隆抗体交联磁微粒的肌钙蛋白检测试剂盒。本发明采用生物素衍生物预交联磁微粒,再包被上链霉亲和素,经封闭后,与肌钙蛋白i单克隆抗体-生物素反应,洗涤后,制得肌钙蛋白i单克隆抗体磁微粒。本发明的肌钙蛋白i检测试剂盒采用链霉亲和素生物素多级放大体系,具有检测灵敏度高、特异性强、药物干扰小、结果稳定性好等优点;从而可以大规模适用于心血管疾病临床辅助诊断。
在第一方面,本发明提供一种肌钙蛋白i单克隆抗体磁微粒,所述肌钙蛋白i单克隆抗体交联磁微粒从内向外依次包括:生物素衍生物层、链霉亲和素层和肌钙蛋白i单克隆抗体-生物素层。
在具体的实施方式中,所述生物素衍生物是bsa(牛血清白蛋白)-biotin交联物、或cmo(羧甲基羟胺半盐酸盐)-biotin交联物;优选bsa-biotin交联物。
在具体的实施方式中,所述的肌钙蛋白i单克隆抗体磁微粒采用以下方法制备:1)利用生物素衍生物预交联磁微粒;2)用链霉亲和素包被步骤1)获得的生物素衍生物预交联的磁微粒;和3)封闭步骤2)获得的磁微粒,然后与肌钙蛋白i单克隆抗体-生物素反应,从而制得肌钙蛋白i单克隆抗体磁微粒。
在另一优选的实施方式中,所述bsa-biotin交联物是将bsa与biotin按照一定比例进行反应,置于2~8℃,10mmpbs透析16~24小时。
在另一优选的实施方式中,进行bsa和biotin交联时,所述bsa与biotin的反应浓度分别为1~5mg/ml、1~5mg/ml,优选2mg/ml、2mg/ml。
在另一优选的实施方式中,进行bsa和biotin交联时,所述bsa与biotin的反应的摩尔浓度比例为1:5~1:50,优选1:20。
在另一优选的实施方式中,所述磁微粒的主要成分是超顺磁性微粒,粒径为800nm~3μm,主要的活性功能基团为羧基、氨基或苯甲磺酰基。
在另一优选的实施方式中,磁微粒与bsa-biotin交联时,所述bsa-biotin的交联浓度为5~100μg/10mg磁微粒,优选40μg/10mg磁微粒。
在另一优选的实施方式中,作链霉亲和素包被时,所述链霉亲和素的包被浓度为1~5mg/ml,反应体积为20μl~100μl,优选浓度为2mg/ml,反应体积为40μl。
在另一优选的实施方式中,磁微粒经封闭后,与肌钙蛋白i单克隆抗体-生物素反应时,所述肌钙蛋白i单克隆抗体-生物素的浓度为0.5~4μg/ml,优选浓度为2μg/ml。
在第二方面,本发明提供本发明第一方面所述的肌钙蛋白i单克隆抗体磁微粒的制备方法,所述方法包括以下步骤:
1)利用生物素衍生物预交联磁微粒;
2)用链霉亲和素包被步骤1)获得的生物素衍生物预交联的磁微粒;和
3)封闭步骤2)获得的磁微粒,然后与肌钙蛋白i单克隆抗体-生物素反应,从而制得肌钙蛋白i单克隆抗体磁微粒。
在优选的实施方式中,所述的肌钙蛋白i单克隆抗体磁微粒的制备方法包括以下步骤:
a)采用生物素衍生物预交联磁微粒,再包被上链霉亲和素;
b)将步骤a)处理的磁微粒经封闭后,与肌钙蛋白i单克隆抗体-生物素反应;
c)将步骤b)处理的磁微粒经洗涤后,保存在磁微粒保存液中。
在优选的实施方式中,步骤a)中的所述生物素衍生物是bsa-biotin交联物、或cmo-biotin交联物;优选bsa-biotin交联物。
在另一优选的实施方式中,所述bsa-biotin交联物是将bsa与biotin按照一定比例进行反应,置于2~8℃,10mmpbs透析16~24小时。
在另一优选的实施方式中,进行bsa和biotin交联时,所述bsa与biotin的反应浓度分别为1~5mg/ml、1~5mg/ml,优选2mg/ml、2mg/ml。
在另一优选的实施方式中,进行bsa和biotin交联时,所述bsa与biotin的反应的摩尔浓度比例为1:5~1:50,优选1:20。
在另一优选的实施方式中,磁微粒与bsa-biotin交联时,所述bsa-biotin的交联浓度为5~100μg/10mg磁微粒,优选40μg/10mg磁微粒。
在另一优选的实施方式中,包被链霉亲和素时,所述链霉亲和素的包被浓度为1~5mg/ml,反应体积为20μl~100μl,优选浓度为2mg/ml,反应体积为40μl。
在另一优选的实施方式中,磁微粒经封闭后,与肌钙蛋白i单克隆抗体-生物素反应时,所述肌钙蛋白i单克隆抗体-生物素的浓度为0.5~4μg/ml,优选浓度为2μg/ml。
在第三方面,本发明提供本发明第一方面所述的肌钙蛋白i单克隆抗体磁微粒,或本发明第二方面所述的方法制备的肌钙蛋白i单克隆抗体磁微粒在检测肌钙蛋白i或制备肌钙蛋白i检测试剂盒中的用途。
在第三方面,本发明提供一种肌钙蛋白i检测试剂盒,所述试剂盒装有:本发明第一方面所述的肌钙蛋白i单克隆抗体磁微粒,或本发明第二方面所述的方法制备的肌钙蛋白i单克隆抗体磁微粒。
在优选的实施方式中,所述肌钙蛋白i检测试剂盒还装有:酶标记的肌钙蛋白i单克隆抗体;肌钙蛋白i定标品;化学发光底物;稀释液。
在进一步的优选实施方式中,所述肌钙蛋白i检测试剂盒还装有使用说明书和用于移液的合适器件。
在另一优选的实施方式中,所述酶标记的肌钙蛋白i单克隆抗体中的酶是碱性磷酸酶。
在另一优选的实施方式中,所述化学发光底物的主要成分为1,2-二氧杂环丁烷衍生物,为酶促化学发光底物。
在另一优选的实施方式中,所述1,2-二氧杂环丁烷衍生物为amppd(3-(2'-螺旋金刚烷)-4-甲氧基-4-(3"-磷酰氧基)苯-1,2-二氧杂环丁烷)、cdp-star。
在另一优选的实施方式中,所述的磁微粒试剂的主要成分是超顺磁性微粒,其粒径为800nm~3μm,主要的活性功能基团为羧基、氨基或苯甲磺酰基。
在第四方面,本发明提供制备肌钙蛋白i检测试剂盒的方法,所述的方法包括:将本发明第一方面所述的肌钙蛋白i单克隆抗体磁微粒,或本发明第二方面所述的方法制备的肌钙蛋白i单克隆抗体磁微粒制成肌钙蛋白i检测试剂盒。
在优选的实施方式中,所述方法包括将本发明第一方面所述的肌钙蛋白i单克隆抗体磁微粒,或本发明第二方面所述的方法制备肌钙蛋白i单克隆抗体磁微粒;酶标记的肌钙蛋白i单克隆抗体;肌钙蛋白i定标品;化学发光底物;和稀释液制成肌钙蛋白i检测试剂盒。
在另一优选的实施方式中,所述的肌钙蛋白i单克隆抗体磁微粒的制备,是将活性功能基团为羧基、氨基或苯甲磺酰基的磁微粒通过共价交联的方式与bsa-biotin预交联,再包被链霉亲和素,经封闭后,与肌钙蛋白i单克隆抗体-生物素反应,0.5~2%的bsa溶液洗涤后,制得肌钙蛋白i单克隆抗体磁微粒,最终贮存于含有0.1~1%的bsa溶液中,2~8℃保存备用。
在另一优选的实施方式中,所述的磁微粒试剂稀释液的配方为:10~100mmph7.2~7.8tris-hcl、50~300mmnacl、10~50mmcacl2、0.5~2%bsa、2~15%甘油、0.05~0.2%proclin-300。
在另一优选的实施方式中,碱性磷酸酶标记肌钙蛋白i单克隆抗体的制备方法为戊二醛偶联法,具体操作为:将碱性磷酸酶溶于终浓度5%戊二醛溶液中,室温静置过夜,生理盐水透析后,加入肌钙蛋白i单克隆抗体,50mmph9.6碳酸钠-碳酸氢钠缓冲液中透析过夜,加入甘氨酸,室温反应2小时,等体积加入饱和硫酸铵,2~8℃2小时,4000rpm离心去上清,沉淀溶于50mmph7.40磷酸缓冲液中,对其透析过夜,加入等体积甘油,置于-20℃保存。
在另一优选的实施方式中,碱性磷酸酶标记肌钙蛋白i单克隆抗体的稀释液的配方为:10~100mmph7.2~7.8tris-hcl、50~300mmkcl、0.5~2%bsa、5~15%甘油、0.05~0.5%吐温-20、0.05~0.2%proclin-300。
在另一优选的实施方式中,所述的肌钙蛋白i定标品的浓度分别为0~0.05ng/ml和15~35ng/ml。
在另一优选的实施方式中,所述的肌钙蛋白i定标品的稀释液配方为:10~100mmph7.2~7.8tris-hcl,50~300mmkcl,10~50mmcacl2、0.1~2%bsa,5~15%甘油,0.05~0.2%proclin-300。
在另一优选的实施方式中,所述的洗涤液配方为:10~100mmph7.2~7.8tris-hcl,50~300mmnacl,0.1~1%曲拉通x-100,0.05~0.2%proclin-300。
在第四方面,本发明提供一种检测肌钙蛋白i的方法,所述方法包括利用本发明第一方面所述的肌钙蛋白i单克隆抗体磁微粒,或本发明第二方面所述的方法制备的肌钙蛋白i单克隆抗体磁微粒,或本发明第三方面所述的肌钙蛋白i检测试剂盒检测离体样品中的肌钙蛋白i。
应理解,在本发明范围内中,本发明的上述各技术特征和在下文(如实施例)中具体描述的各技术特征之间都可以互相组合,从而构成新的或优选的技术方案。限于篇幅,在此不再一一累述。
附图说明
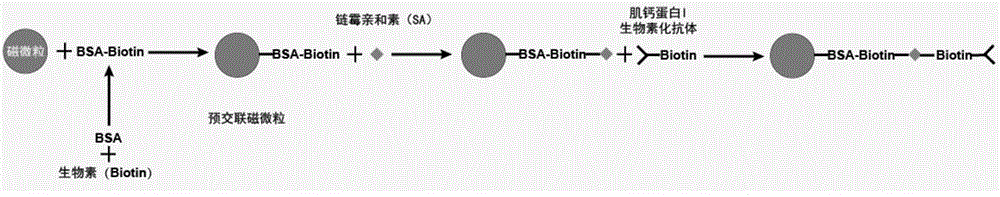
图1显示了本发明的肌钙蛋白i单克隆抗体磁微粒的制备工艺流程。
图2显示了肌钙蛋白i的反应原理。
具体实施方式
发明人在实践中发现,现有技术中将磁微粒直接交联肌钙蛋白i单克隆抗体对于肌钙蛋白i的检测灵敏度不足;将链霉亲和素化的磁微粒与生物素化的肌钙蛋白i单克隆抗体反应得到的肌钙蛋白i单克隆抗体磁微粒能在一定程度上提高检测灵敏度。然而,当发明人采用多次的“链霉亲和素+生物素”的方式制备肌钙蛋白i单克隆抗体磁微粒时,却发现得到的肌钙蛋白i单克隆抗体磁微粒的检测灵敏度不但没有进一步升高,反而显著降低。
发明人在经过广泛而深入的研究,出乎意料地发现采用生物素衍生物预交联磁微粒,再包被上链霉亲和素,经封闭后,与肌钙蛋白i单克隆抗体-生物素反应制得肌钙蛋白i单克隆抗体磁微粒,这种可以肌钙蛋白i单克隆抗体磁微粒显著提高肌钙蛋白i的检测灵敏度,同时确保试剂的特异性。在此基础上完成了本发明。
本发明的肌钙蛋白i单克隆抗体磁微粒及其制备方法
基于以上的发现,本发明提供一种肌钙蛋白i单克隆抗体磁微粒,所述生物素衍生物预交联磁微粒,再包被上链霉亲和素,经封闭后,与肌钙蛋白i单克隆抗体-生物素反应,洗涤后,制得肌钙蛋白i单克隆抗体磁微粒。
本文所用的术语“生物素衍生物”是指经亲水性分子修饰的生物素,或亲水性分子与生物素的交联物。在优选的实施方式中,所述生物素衍生物是bsa-biotin交联物、或cmo-biotin交联物;更优选bsa-biotin交联物。
相应地,本发明还提供了上文所述肌钙蛋白i单克隆抗体磁微粒的制备方法,所述方法包括以下步骤:
1)利用生物素衍生物预交联磁微粒;
2)用链霉亲和素包被步骤1)获得的生物素衍生物预交联的磁微粒;和
3)封闭步骤2)获得的磁微粒,然后与肌钙蛋白i单克隆抗体-生物素反应,从而制得肌钙蛋白i单克隆抗体磁微粒。
在具体的实施方式中,所述方法可包括:
a)采用生物素衍生物预交联磁微粒,再包被上链霉亲和素;
b)将步骤a)处理的磁微粒经封闭后,与肌钙蛋白i单克隆抗体-生物素反应;
c)将步骤b)处理的磁微粒经洗涤后,保存在磁微粒保存液中。
在具体的实施方式中,具备优异的肌钙蛋白i检测灵敏度的本发明肌钙蛋白i单克隆抗体磁微粒的制备过程中采用以下工艺参数。
在一优选的实施方式中,所述bsa-biotin交联物是将bsa与biotin按照一定比例进行反应,置于2~8℃,10mmpbs透析16~24小时。
在另一优选的实施方式中,进行bsa和biotin交联时,所述bsa与biotin的反应浓度分别为1~5mg/ml、1~5mg/ml,优选2mg/ml、2mg/ml。
在另一优选的实施方式中,进行bsa和biotin交联时,所述bsa与biotin的反应的摩尔浓度比例为1:5~1:50,优选1:20。
在另一优选的实施方式中,磁微粒与bsa-biotin交联时,所述bsa-biotin的交联浓度为5~100μg/10mg磁微粒,优选40μg/10mg磁微粒。
在另一优选的实施方式中,包被链霉亲和素时,所述链霉亲和素的包被浓度为1~5mg/ml,反应体积为20μl~100μl,优选浓度为2mg/ml,反应体积为40μl。
在另一优选的实施方式中,磁微粒经封闭后,与肌钙蛋白i单克隆抗体-生物素反应时,所述肌钙蛋白i单克隆抗体-生物素的浓度为0.5~4μg/ml,优选浓度为2μg/ml。
同样,鉴于本发明的教导和现有技术,本领域普通技术人员可以合理确定所用的磁微粒。例如,在具体的实施方式中,磁微粒的主要成分是超顺磁性微粒,粒径为800nm~3μm,主要的活性功能基团为羧基、氨基或苯甲磺酰基。
在具体的实施方式中,所述的肌钙蛋白i单克隆抗体磁微粒的制备,是将活性功能基团为羧基、氨基或苯甲磺酰基的磁微粒通过共价交联的方式与bsa-biotin预交联,再包被链霉亲和素,经封闭后,与肌钙蛋白i单克隆抗体-生物素反应,0.5~2%的bsa溶液洗涤后,制得肌钙蛋白i单克隆抗体磁微粒,最终贮存于含有0.1~1%的bsa溶液中,2~8℃保存备用。
本发明的肌钙蛋白i检测试剂盒
本发明的肌钙蛋白i单克隆抗体磁微粒可以用于检测肌钙蛋白i或制备肌钙蛋白i检测试剂盒,从而显著提高检测肌钙蛋白i时的灵敏度。因此,本发明还提供了一种肌钙蛋白i检测试剂盒,所述试剂盒装有本发明的肌钙蛋白i单克隆抗体磁微粒。
鉴于本发明的教导和现有技术,本领域普通技术人员可以确定所述肌钙蛋白i检测试剂盒中的其它组分,例如,在具体的实施方式中,本发明的肌钙蛋白i检测试剂盒还可装有:酶标记的肌钙蛋白i单克隆抗体;肌钙蛋白i定标品;化学发光底物;和稀释液及使用说明书,任选的用于移液的合适器件。
在优选的实施方式中,所述酶标记的肌钙蛋白i单克隆抗体中的酶是碱性磷酸酶。
相应地,本发明的肌钙蛋白i检测试剂盒中的所述化学发光底物的主要成分可以为1,2-二氧杂环丁烷衍生物,为酶促化学发光底物。在优选的实施方式中,所述1,2-二氧杂环丁烷衍生物为amppd(3-(2'-螺旋金刚烷)-4-甲氧基-4-(3"-磷酰氧基)苯-1,2-二氧杂环丁烷)、cdp-star。而本发明的肌钙蛋白i检测试剂盒中的磁微粒试剂的主要成分可以是超顺磁性微粒,其粒径为800nm~3μm,主要的活性功能基团为羧基、氨基或苯甲磺酰基。
本发明的肌钙蛋白i检测试剂盒可如下所示进行制备,包括:将本发明的肌钙蛋白i单克隆抗体磁微粒,或本发明方法制备的肌钙蛋白i单克隆抗体磁微粒制成肌钙蛋白i检测试剂盒。
在具体的实施方式中,将本发明的肌钙蛋白i单克隆抗体磁微粒;酶标记的肌钙蛋白i单克隆抗体;肌钙蛋白i定标品;化学发光底物;和稀释液制成本发明的肌钙蛋白i检测试剂盒。
在具体的实施方式中,所述的磁微粒试剂稀释液的配方为:10~100mmph7.2~7.8tris-hcl、50~300mmnacl、10~50mmcacl2、0.5~2%bsa、2~15%甘油、0.05~0.2%proclin-300。
在具体的实施方式中,碱性磷酸酶标记肌钙蛋白i单克隆抗体的制备方法为戊二醛偶联法,具体为:将碱性磷酸酶溶于终浓度5%戊二醛溶液中,室温静置过夜,生理盐水透析后,加入肌钙蛋白i单克隆抗体,50mmph9.6碳酸钠-碳酸氢钠缓冲液中透析过夜,加入甘氨酸,室温反应2小时,等体积加入饱和硫酸铵,2~8℃2小时,4000rpm离心去上清,沉淀溶于50mmph7.40磷酸缓冲液中,对其透析过夜,加入等体积甘油,置于-20℃保存。
在具体的实施方式中,碱性磷酸酶标记肌钙蛋白i单克隆抗体的稀释液的配方为:10~100mmph7.2~7.8tris-hcl、50~300mmkcl、0.5~2%bsa、5~15%甘油、0.05~0.5%吐温-20、0.05~0.2%proclin-300;所述的肌钙蛋白i定标品的浓度分别为0~0.05ng/ml和15~35ng/ml;所述的肌钙蛋白i定标品的稀释液配方为:10~100mmph7.2~7.8tris-hcl,50~300mmkcl,10~50mmcacl2、0.1~2%bsa,5~15%甘油,0.05~0.2%proclin-300;所述的洗涤液配方为:10~100mmph7.2~7.8tris-hcl,50~300mmnacl,0.1~1%曲拉通x-100,0.05~0.2%proclin-300。
本发明的肌钙蛋白i的检测方法
在本发明的肌钙蛋白i单克隆抗体磁微粒以及包含其的肌钙蛋白i检测试剂盒的基础上,本发明还提供一种检测肌钙蛋白i的方法,所述方法利用本发明的肌钙蛋白i单克隆抗体磁微粒,或本发明的肌钙蛋白i检测试剂盒检测离体样品中的肌钙蛋白i。
本领域技术人员知晓,本发明的肌钙蛋白i的检测方法可以用于诊断目的,但不限于诊断目的,例如,可用于科研目的等等。
本发明的优点
1)本发明的肌钙蛋白i抗体磁微粒采用链霉亲和素-生物素(biotin-sa)多级放大体系,即,通过多级放大,可以提高链霉亲和素结合生物素的量,从而显著提高单位磁微粒上交联的肌钙蛋白i单克隆抗体的量。
2)本发明使用多级放大链霉亲和素-生物素,可以增加磁微粒抗体交联物的臂长,明显改善因空间位阻造成的交联效率偏低的情况,从而显著提高单位磁微粒上交联的肌钙蛋白i单克隆抗体的量。
3)本发明的人肌钙蛋白i单克隆抗体磁微粒的试剂盒的检测灵敏度高,包含本发明肌钙蛋白i单克隆抗体磁微粒的试剂盒的最低检测限能达到0.02ng/ml;
4)本发明的试剂盒特异性强;胆红素、血红蛋白、乳糜颗粒、类风湿因子(rf)、抗核抗体(ana)、人抗鼠抗体(hama)对肌钙蛋白i测定结果均无明显干扰;
5)本发明的试剂盒受心血管药物的干扰小;对于目前市面上常见的且临床使用普遍的心血管药物,即,阿替洛尔、苯妥英钠、双氯芬酸钠、土霉素、茶碱、甲基多巴和地高辛,本发明的试剂盒对其均几乎无明显干扰;
6)本发明的试剂盒测定结果稳定性好;碱性磷酸酶更稳定、测定结果的重复性更好,1,2-二氧杂环丁烷衍生物具有较长的发光时间,发光信号可稳定超过20分钟以上;信号强度高,便于光电倍增管检测;抗干扰能力强,不易污染。
下面结合具体实施例,进一步阐述本发明。应理解,这些实施例仅用于说明本发明而不用于限制本发明的范围。下列实施例中未注明具体条件的实验方法,通常按照常规条件或按照制造厂商所建议的条件。除非另外说明,否则百分比和份数是重量百分比和重量份数。
除非另行定义,文中所使用的所有专业与科学用语与本领域熟练人员所熟悉的意义相同。此外,任何与所记载内容相似或均等的方法及材料皆可应用于本发明方法中。文中所述的较佳实施方法与材料仅作示范之用。
实施例
材料与方法
材料
以下实施例中所用的试剂均是市售可得的,例如可购自国药集团,或者碱性磷酸酶购自bbi公司,但不限于此。
1.肌钙蛋白i磁微粒试剂的制备
肌钙蛋白i磁微粒试剂稀释液配方:
将肌钙蛋白i单克隆抗体磁微粒用磁微粒稀释液稀释至0.4~0.8mg/ml,室温充分混匀至少30分钟,制得肌钙蛋白i磁微粒试剂。
2.碱性磷酸酶标记肌钙蛋白i单克隆抗体的制备
1)将碱性磷酸酶溶于终浓度5%戊二醛溶液中,使得碱性磷酸酶的浓度为10mg/ml;
2)室温静置过夜;
3)用生理盐水(体积比大于1:200)透析至少4小时;
4)取出透析后的碱性磷酸酶,按照质量1:1的比例加入肌钙蛋白i单克隆抗体,充分混匀;
5)50mmph9.6碳酸钠-碳酸氢钠缓冲液中透析过夜;
6)取出透析液,按照体积比1:1000加入1m甘氨酸溶液,混匀,终止反应2小时;
7)等体积加入饱和硫酸铵,2~8℃保存2小时;
8)4000rpm离心去上清,沉淀溶于50mmph7.40磷酸缓冲液中;
9)50mmph7.40磷酸缓冲液中透析过夜;
10)取出透析液加入等体积的甘油,制得碱性磷酸酶标记肌钙蛋白i单克隆抗体,置于-20℃保存。
3.肌钙蛋白i酶试剂的制备
肌钙蛋白i酶试剂稀释液配方:
将碱性磷酸酶标记肌钙蛋白i单克隆抗体用酶稀释液稀释至1:1000~1:5000,室温充分混匀至少30分钟,制得肌钙蛋白i酶试剂。
4.肌钙蛋白i定标品的制备
肌钙蛋白i定标品稀释液配方:
将重组心肌肌钙蛋白i抗原用定标品稀释液分别稀释至0.1ng/ml和25ng/ml,室温充分混匀至少30分钟,制得肌钙蛋白i定标品。通过多次对校准品和定标品同时测定,建立肌钙蛋白i试剂盒主曲线,并对肌钙蛋白i定标品进行赋值,即为肌钙蛋白i定标品的制备。
5.洗涤液的制备
洗涤液配方:
按配方配制洗涤液,室温充分混匀至少30分钟,制得洗涤液。
6.肌钙蛋白i的检测方法
1)加入50μl血清或血浆样本、50μl磁微粒试剂、50μl酶试剂;
2)37℃反应15分钟;
3)磁吸后去上清液,加入300μl洗涤液;
4)重复步骤3)2次;
5)磁吸后去上清液,加入300μl化学发光底物;
6)37℃下反应10分钟;
7)光电倍增管(pmt)读取相对发光单位(rlu),自动计算浓度值。
实施例1.肌钙蛋白i单克隆抗体磁微粒的制备
1)将bsa用10mmpbs溶解稀释至2mg/ml,在2mg/mlbsa溶液中按照摩尔浓度比例1:20加入2mg/mlbiotin水溶液,混匀;
2)将混合物室温反应30min,置于2~8℃,10mmpbs透析16~24小时;
3)取出透析液,用10mmpbs将bsa-biotin稀释至1mg/ml;
4)取10mg活性功能基团为羧基的1.0μm磁微粒,用50mmph6.0的mes缓冲液洗涤2次;
5)磁吸后去上清液,加入0.5ml的50mmph6.0的mes缓冲液混匀,再加入0.5ml25mg/ml碳二亚胺(edc)溶液,充分混匀,室温反应30分钟;
6)用含有50mmph7.8tris-hcl,150mmnacl,1%bsa溶液洗涤2次;
7)加入3)所得的40μgbsa-biotin,再用50mmph6.0的mes缓冲液定容至1ml,充分混匀,37℃反应过夜;
8)用含有50mmph7.8tris-hcl,150mmnacl,1%bsa溶液洗涤2次;
9)加入2ml含有50mmph7.8tris-hcl,150mmnacl,1%bsa溶液,充分混匀,37℃封闭过夜;
10)用含有50mmph7.8tris-hcl,150mmnacl,1%bsa溶液洗涤2次;
11)加入2ml含有50mmph7.8tris-hcl,150mmnacl,0.5%bsa溶液,充分混匀;
12)加入5mg/ml链霉亲和素40μl,室温反应4h;
13)用含有50mmph7.8tris-hcl,150mmnacl,1%bsa溶液洗涤2次;
14)加入2ml含有50mmph7.8tris-hcl,150mmnacl,0.5%bsa溶液,充分混匀;
15)加入2μg/ml的肌钙蛋白i单克隆抗体-生物素,室温反应4h;
16)用含有50mmph7.8tris-hcl,150mmnacl,1%bsa溶液洗涤2次;
17)加入2ml含有50mmph7.8tris-hcl,150mmnacl,0.5%bsa溶液,充分混匀;
18)2~8℃保存所制得的肌钙蛋白i单克隆抗体磁微粒。
实施例2.肌钙蛋白i单克隆抗体磁微粒的灵敏度检测
利用实施例1所得的肌钙蛋白i单克隆抗体磁微粒,如材料与方法所述进行灵敏度检测,结果如下表所示:
注:
(1)直接交联肌钙蛋白i单克隆抗体得到的磁微粒;
(2)传统链霉亲和素-生物素肌钙蛋白i单克隆抗体磁微粒;
(3)本发明的多级放大链霉亲和素-生物素肌钙蛋白i单克隆抗体磁微粒。
从上表可以看出,使用本发明的多级放大链霉亲和素-生物素肌钙蛋白i单克隆抗体磁微粒,其灵敏度(s/n值)比直接交联和传统链霉亲和素-生物素方法分别提高了1.23倍和1.89倍。此外,其检测的功能灵敏度为0.02ng/ml,远低于另外两种方法。综上所述,使用本发明的多级放大链霉亲和素-生物素肌钙蛋白i单克隆抗体磁微粒可以明显提高肌钙蛋白i的灵敏度。
实施例3.本发明所述的试剂盒分析性能
1)最低检测限:本试剂盒的最低检测限不高于0.02ng/ml。
测定空白样本20次,计算20次测定结果均值(m)和标准差(sd),m+2sd对应的浓度即为试剂盒的最低检测限。
2)准确度:本试剂盒的回收率在85%~115%之间。
3)重复性:本试剂盒的相对变异系数(cv)≤8%。
4)线性范围:本试剂盒的线性范围为0.02~50ng/ml。
将接近线性范围上限的高值样本进行系列稀释,计算实测值与理论稀释度之间的线性相关系数r,结果应大于或等于0.99。
5)批间差:本试剂盒批间的相对变异系数(cv)≤15%。
6)分析特异性:
测定以下一定浓度的干扰物质,测定结果基本无交叉反应。
7)药物干扰:
测定4种临床中常用的心血管药物,不同浓度下的药物干扰结果见下表。
8)稳定性:本试剂盒2~8℃保存12个月,试剂盒分析性能仍稳定。
实施例4.本发明所述的试剂盒与现有进口试剂盒的临床比对结果
共检测225例临床样本,同时对本发明所述的试剂盒与现有的进口肌钙蛋白i检测试剂盒(beckman公司)进行检测,通过medcalc统计软件进行相关性及一致性分析。
1)相关性分析
以现有进口试剂a的临床测定结果为x轴,本发明所述的试剂盒的临床测定结果为y轴,绘制散点图,进行相关性分析,其相关性方程为:y=0.9904x+0.0617(p<0.001);相关性系数:r=0.9933,两者的测定结果相关性良好。
2)一致性分析
采用bland-altman统计学方法对两组测定结果进行分析,以每个样本的测定结果的比值作为纵坐标,两者的测定结果的均值作为横坐标作图。计算所有比值的平均值(a)及标准差(sd),并根据公式a±1.96sd得到95%的一致性界限范围。本次临床试验中a=1.08,sd=0.675,因此95%的一致性界限范围为:0.41~1.76。上述结果显示,96.89%(218/225)的测定结果在上述范围内,两者测定结果在统计学上有着一致性。
3)总结:
现有的beckman公司的肌钙蛋白i检测试剂盒是目前临床上用于肌钙蛋白i测定市场份额最高的产品之一,其试剂盒的临床性能已被临床广泛接受。本发明所述的试剂盒在临床试验比对中,与进口试剂的结果相关性及一致性高度吻合,能满足目前市场上对肌钙蛋白i测定的需求,且生产成本远低于该试剂盒。
在本发明提及的所有文献都在本申请中引用作为参考,就如同每一篇文献被单独引用作为参考那样。此外应理解,在阅读了本发明的上述讲授内容之后,本领域技术人员可以对本发明作各种改动或修改,这些等价形式同样落于本申请所附权利要求书所限定的范围。
- 还没有人留言评论。精彩留言会获得点赞!