一种泽泻汤提取物及其合成与应用的制作方法
本发明涉及一种泽泻汤提取物。
(二)
背景技术:
泽泻汤来自东汉张仲景的《金匮要略-痰饮咳嗽病》,原文:心下有支饮,其人苦冒眩,泽泻汤主之。从此始有“泽泻汤”方名,后世多命名为“金匮泽泻汤”。张仲景同时提出,痰饮上泛是昏冒眩晕的主要病机。该方重用泽泻利水下行,以治其标;以白术健脾制水,以治其本;为临床治疗痰饮致眩之要方。后世医家在临床实践中进一步扩大了泽泻汤的主治范围,除用治“支饮冒眩”外,亦可治疗“水肿”《普济方》;“胸中痞结,坚大如盘,下则小便不利”《医灯续焰》;“咳逆难睡,其形如肿”《会约》等诸症。
目前对于泽泻和白术单味药物的研究已相当的深入。泽泻以产于福建建瓯、建阳等地者质量最佳,俗称“建泽泻”,被收载入中国道地药材“南药”中。现代药学研究证实,泽泻主要含三萜类化合物、挥发油、生物碱及利尿的有效成分泽泻醇A、B、C等,具有显著利尿等作用。白术的主要化学成分为挥发油(量为1.4%左右),还含有多糖、谷氨酸等14种氨基酸等物质;具有利尿、调节胃肠运动、提高免疫力等药理作用。但是泽泻汤整方相关化学组分的研究尚未见报道,泽泻、白术以水共煎后的成分有一定差别,因此发明人经过努力,从整方中分离出具有药效活性的新化合物。
(三)
技术实现要素:
本发明目的是提供一种泽泻汤提取物及其合成与制备预防和治疗美尼尔综合症、高血压、高血脂等药物中的应用。
本发明采用的技术方案是:
本发明提供一种泽泻汤提取物,所述提取物为下列之一:
本发明还提供一种所述泽泻汤提取物的制备方法,所述方法为:(1)将泽泻和白术混合,以8倍量水煎煮,提取液以3层纱布过滤,减压浓缩至密度1.1-1.2g·mL-1,减压过滤,获得提取物;所述泽泻和白术质量比为1:0.1~1,优选1:0.4;
(2)将提取物依次用正丁醇、乙酸乙酯和石油醚萃取,萃取物均经减压浓缩成浸膏,分别得正丁醇萃取物,乙酸乙酯萃取物,石油醚萃取物;
将乙酸乙酯萃取物进行硅胶柱层析,分别以体积比50:1~0:1的二氯甲烷与甲醇混合液进行洗脱,当洗脱液为体积比25:1的二氯甲烷:甲醇时,分别收集洗脱液总体积1/2和3/4时的流出液,获得流出液a和流出液b;将流出液a经甲醇溶解后,Sephadex LH-20葡聚糖凝胶色谱分离,甲醇洗脱,收集目标组分(首尾按各50mL流出液收集,第2至第5按约每20mL流出液,依次收集第70~90mL流出液)以LabAlliance P-24半制备液相分离,收集保留时间28-37min流出液,以Jasco制备液相分离,流动相为体积比50:50的甲醇:水,收集保留时间67-70min流出液c和保留时间75-83min的流出液d;取流出液c以Jasco制备液相分离,流动相为体积比45:55的甲醇:水,色谱柱YMC HPLC色谱柱(250x10mm),流速1.5mL·min-1,收集液相保留时间46~58min的样品,经减压干燥得提取物(1);
取流出液d以Jasco制备液相分离,流动相为体积比45:55的甲醇:水,色谱柱YMC HPLC色谱柱(250x10mm),流速1.5mL·min-1,收集液相保留时间58~66min的样品,经减压干燥得提取物(2);
取流出液b经甲醇溶解后,Sephadex LH-20葡聚糖凝胶色谱分离,甲醇洗脱,收集目标组分(首尾按各50mL流出液收集,第2至第5按约每20mL流出液,依次收集第50~70mL流出液)以Jasco制备液相分离,流动相为体积比50:50的甲醇:水,色谱柱YMC HPLC色谱柱(250x20mm),流速3mL·min-1,收集保留时间126-134min流出液,经减压干燥得提取物(3)。
此外,本发明还提供一种所述泽泻汤提取物在制备预防和治疗美尼尔综合症药物中的应用。
本发明还提供一种所述泽泻汤提取物在制备预防和治疗高血压药物中的应用。
本发明还提供一种所述泽泻汤提取物在制备预防和治疗高血脂药物中的应用。
与现有技术相比,本发明的有益效果主要体现在:
本发明化合物是一种泽泻汤提取新化合物,具有预防和治疗美尼尔综合症、高血压、高血脂等疾病的活性,其分离自经典名方泽泻汤。
(四)附图说明
图1.新化合物1的高分辨质谱。
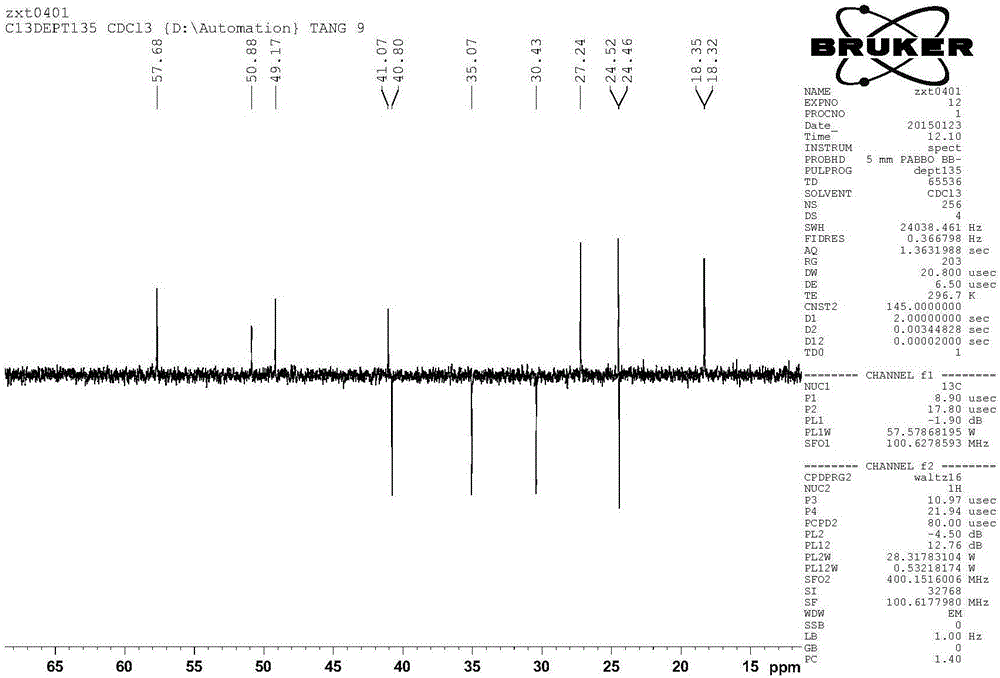
图2.新化合物1的DEPT谱。
图3.新化合物1的1H1HCOSY谱。
图4.新化合物1的HSQC谱。
图5.新化合物1的HMBC谱。
图6.新化合物1的ROESY谱。
图7.新化合物3的高分辨质谱。
图8.新化合物3的DEPT谱。
图9.新化合物3的1H1HCOSY谱。
图10.新化合物3的HSQC谱。
图11.新化合物3的HMBC谱。
图12.新化合物3的ROESY谱。
图13.新化合物2的高分辨质谱。
图14.新化合物2的DEPT谱。
图15.新化合物2的1H1HCOSY谱。
图16.新化合物2的HSQC谱。
图17.新化合物2的HMBC谱。
图18.新化合物2的ROESY谱。
图19.新化合物结构图,A为新化合物1,B为新化合物3,C为新化合物2。
图20.半制备的HPLC图,A为UV检测,B为RID检测。
图21.Jasco制备液相色谱图,A为UV检测,B为RID检测。
图22.新化合物1的HPLC图。
图23.新化合物3的HPLC图。
图24.新化合物2的HPLC图。
(五)具体实施方式
下面结合具体实施例对本发明进行进一步描述,但本发明的保护范围并不仅限于此:
核磁共振仪:Bruker AVANCE 400instrument.,1H-NMR(400MHz),13C-NMR(100MHz),各溶剂峰做内标。
质谱仪:JEOL JMS-SX 102A(EI,FAB MS),IonSpec 4.7Tesla FTMS(HRFTMS),Alliance2695Quattro Micro TM ESI(Waters,液质联用色谱仪)。
紫外分光光度计:Hitachi U-3310UV-VIS Spectrophotometer。
红外光谱仪:NICOLET 380FT-IR Spectrophotometer(Thermo Electron Corporation),KBr压片。
旋光仪:MC 241digital polarimeter(PERKIN-ELMER)。
半制备高效液相色谱仪:JASCO高效液相色谱系统(PU-2089plus,RI-2031plus,UV-2075plus);SSI Lab Alliance[TM]高效液相色谱系统(SeriesⅢpump,RI 2000,UV Model 500,Scientific Systems,Inc,USA)。
其他仪器:旋转蒸发器:SENCO R系列,上海申生科技有限公司。电子天平:BSA/24S万分之一天平(德国Sartorius)、JP/YP series百分之一天平(良平仪器)。ZF-I型三用紫外分析仪:上海顾村电光仪器厂。
实施例1
(1)化合物提取纯化
取泽泻、白术以质量比1:0.4的混合物4500g,以8倍量水分别煎煮3次,时间分别为2.5h、2.5h、2h,合并煎煮液以3层纱布过滤,减压浓缩至密度1.1-1.2g·mL-1,减压过滤,得总提取物。
将总提取物依次以正丁醇、乙酸乙酯和石油醚萃取,萃取物均经减压浓缩成浸膏,得正丁醇层萃取物52.18g,乙酸乙酯层萃取物13.77g,石油醚层萃取物2.72g。
将13.77g乙酸乙酯萃取物以20g100-200目硅胶拌样后,300-400目硅胶约250克装柱分离。分别以二氯甲烷:甲醇(50:1,v/v)1000mL、二氯甲烷:甲醇(25:1,v/v)2000mL、二氯甲烷:甲醇(10:1,v/v)2000mL、二氯甲烷:甲醇(4:1,v/v)2000mL、二氯甲烷:甲醇(1:1,v/v)1000mL、甲醇1000mL洗脱,按约每500mL 收集洗脱液经减压干燥得样品0101-0119,见表1。
表1 01系列样品重量
取样品0104(1.3016g)(即乙酸乙酯萃取物从硅胶柱色谱收集的二氯甲烷:甲醇(25:1,v/v)第2个500mL洗脱液)经10ml甲醇溶解后,Sephadex LH-20葡聚糖凝胶色谱分离,甲醇洗脱,首尾按各50mL流出液收集,第2至第5按约每20mL流出液依次收集,经减压干燥得样品0201-0206,见表2。
表2 02系列样品重量
取样品0203(0.7399g,即样品0104经Sephadex LH-20葡聚糖凝胶色谱用甲醇洗脱第70~90mL收集来的),以LabAlliance P-24半制备液相分离。半制备条件:色谱柱:YMC-Pack ODS-A(250x20mm),流动相为甲醇、水(65:35,v/v),流速3mL·min-1,紫外检测波长254nm。将0203粗分为4个部分0203-1~0203-4。半制备的HPLC见图20。
取0203-2(0.1495g,即0203经LabAlliance P-24半制备液相分离,收集液相保留时间28~37min的样品),以Jasco制备液相分离,调整流动相比例为甲醇:水(50:50,v/v),得样品0301-0305,见表3。制备液相色谱见下图21。
表3 03系列样品重量
取样品0301(0203-2经Jasco制备液相分离,收集液相保留时间67~70min的样品),以Jasco制备液相分离,流动相甲醇:水(45:55,v/v),色谱柱YMC HPLC色谱柱(250x10mm),流速1.5mL·min-1,收集液相保留时间46~58min的样品,经减压干燥得样品0401,即为提取物(1)(5.5mg)。HPLC液相图22。
取样品0303(0203-2经Jasco制备液相分离,收集液相保留时间75~83min的样品),以Jasco制备液相分离,流动相甲醇:水(45:55,v/v),色谱柱YMC HPLC色谱柱(250x10mm),流速1.5mL·min-1,收集液相保留时间58~66min的样品,经减压干燥得样品0406,即为提取物(3)(4.0mg)。HPLC液相图见图23。
表4 04系列样品重量
取样品0105(2.0381g)(乙酸乙酯萃取物从硅胶柱色谱以二氯甲烷:甲醇(25:1,v/v)洗脱第3个500mL收集来的)甲醇溶解后,Sephadex LH-20葡聚糖凝胶分离,甲醇洗脱,首尾按各50mL流出液收集,第2至第5按约每20mL流出液依次收集,经减压干燥得样品0601-0606,见表5。
表5 06系列样品重量
取样品0602(0.4500g)(0105经Sephadex LH-20葡聚糖凝胶色谱用甲醇洗脱第50~70mL收集来的),以Jasco制备液相分离,色谱柱:YMC-Pack ODS-A(250x20mm),流动相为甲醇、水(50:50),流速3mL·min-1,紫外检测波长254nm,得0801-0815。其中,收集液相保留时间126~134min的样品,经减压干燥得样品0812,即为提取物(2)(4.1mg)。HPLC液相图见图24。
表6 08系列样品重量
(2)化合物鉴定
a)化合物1为淡黄色粉末,其高分辨电喷雾质谱(HR-ESI-MS,图1)显示m/z269.1753[M+H]+,说明其分子量为268,分子式为C15H24O4(C15H24O4理论值为268.1675),具有4个不饱和度。1H-NMR谱显示有23个氢信号(1个活泼氢未出),13C-NMR谱显示有15个碳信号,结合DEPT谱(图2)可确定该化合物结构中有3个次甲基、4个亚甲基、4个甲基和2个羰基碳。一系列2D-NMR(HSQC、HMBC、COSY、ROESY,图3-图6)推测化合物结构如图19中A所示。
表7化合物1的NMR波谱数据(in CDCl3)
提取物1:C15H24O4
ROESY谱中H-1与H-5的相关,说明H-1与H-5处于同侧。经查SciFinder,提取1为新化合物,命名为1,3-dimethyl-3-(4-methyl-3-methylenepentyl)-2-oxabicyclo[2,2,1]heptane-7-carboxylic acid。
b)提取物3:
(1R,3S,4R,7R)-1,
3-dimethyl-3-(4-methyl-3-methylenepentyl)-2-oxabicyclo[2,2,1]heptane-7-carboxylic acid
表8化合物3的NMR波谱数据(in CDCl3)
化合物3为淡黄色粉末,其高分辨电喷雾质谱(HR-ESI-MS,图7)显示m/z 269.1753[M+H]+,说明其分子量为268,分子式为C15H24O4(C15H24O4理论值为268.1675),具有4个不饱和度。一系列NMR(图8-图12)数据显示化合物5的平面结构与化合物3相同,立体构型不同,图19中C。相比化合物3,-COOH的吸电子效应使化合物5的8-C化学位移向低场移动了5.9ppm,15-C化学位移向高场移动了5.7ppm,C-5的手性与化合物3不同。经查SciFinder,化合物3为新化合物,命名为(1R,3S,4R,7R)-1,3-dimethyl-3-(4-methyl-3-methylenepentyl)-2-oxabicyclo[2,2,1]heptane-7-carboxylic acid。
c)提取物2:
1-((1R,3S,3aA,4S,6aR)-4-hydroxy-3-methoxy-1,4-dimethylhexahydro-1H-cyclopenta[C]furan-1-yi)-4-methylpentan-3-one
表9化合物2的NMR波谱数据(in CDCl3)
化合物2为淡黄色粉末,其高分辨电喷雾质谱(HR-ESI-MS,图13)显示m/z285.2066[M+H]+,说明其分子量为284,分子式为C16H28O4(C16H28O4理论值为284.1988),具有3个不饱和度。1H-NMR谱显示有27个氢信号(1个活泼氢未出),13C-NMR谱显示有16个碳信号,结合DEPT谱可确定该化合物结构中有4个甲基、1个氧甲基、4个亚甲基、4个次甲基和1个羰基碳。一系列2D-NMR(HSQC、HMBC、COSY、ROESY,图14-图18)推测化合物结构如图19中C。经查SciFinder,化合物2为新化合物,命名为1-(4-Hydroxy-3-methoxy-1,4-dimethyl-hexahydro-cyclopenta[c]furan-1-yl)-4-methyl-pentan-3-one。
实施例2泽泻汤提取物应用
动物模型:选用SPF级小鼠50只,雌雄兼用,体重20±5g,釆用高脂饲料喂养法建立实验性小鼠高脂血症模型。实验前于实验室预饲养一周。所有小鼠用高脂饲料喂养四周建立实验性小鼠高脂血症模型,喂养四周后,尾部取血,测定造模小鼠空腹TC水平,小鼠TC值大于7mmol/L视为造模成功。将动物随机分成5组,每组10只,依次为新化合物(即泽泻汤提取物)高、中、低剂量组,阳性对照组、高血脂症模型组。
给药剂量:
新化合物高剂量组:灌服高剂量新化合物(剂量为5.0mg/kg.d)。
新化合物中剂量组:灌服中剂量新化合物(剂量为2.5mg/kg.d)。
新化合物低剂量组:灌服低剂量新化合物(剂量为1.0mg/kg.d)。
阳性组:灌服辛伐他汀片剂(剂量为7.0mg/kg.d)。
高脂血症模型组:灌服相同体积的蒸馏水。
灌胃给药,每天一次,四周后,禁食不禁水12小时后摘眼球取血,分离血清,测定血清TC、TG、HDL-C浓度。结果见表10。
表10血清TC、TG、HDL-C浓度
给药四周后,阳性组和新化合物高、中、低剂量组小鼠血清TC值均显著低于高脂血症模型组。与高脂血症模型组相比较,阳性组、新化合物高、中、低剂量组小鼠血清TG值均存在显著差异。阳性组小鼠血清HDL-C值、新化合物高剂量组及新化合物中剂量组与高脂血模型组比较有显著性差异,而新化合物低剂量组则无显著性差异。以上说明新化合物有降低血清中TC、TG的浓度,同时能升高血清中HDL-C浓度,高剂量的效果要比其他两个剂量效果更好,低剂量效果最差。
- 还没有人留言评论。精彩留言会获得点赞!