刺槐素的制备方法与流程
本发明涉及一种从香青兰中提取分离得到刺槐素的方法。
背景技术:
经文献检索,刺槐素的提取方法已有一些文献报道:
陈政雄(中药黄酮类的研究VIII.野菊花成分的研究(第一报)[J].药学学报,1962(06).)首次报道从野菊花分离得到刺槐素的结构,该工艺采用提取、萃取、重结晶、水解等技术联合从野菊花菊中分离得到刺槐素,操作复杂、步骤繁琐且产量低。
刺槐素的结构式为:
陈维佳(野菊花化学成分及总黄酮提取工艺研究[D].山东中医药大学,2009.)采用乙醇回流提取、萃取、硅胶柱、SephadexLH-20柱反复柱层析从6kg的野菊花中分离得到11.8mg刺槐素,工艺操作复杂且产量低。
丁智慧(飞机草中的化学成分[J].天然产物研究与开发,2001,13(5):22-24.)采用甲醇回流提取、萃取、硅胶柱反复柱层析从2.48kg的飞机草中分离得到0.318g刺槐素,该工艺操作步骤繁琐。
同时,有3篇与刺槐素提取方法有关的中国专利:
王秀敏等的发明专利(从野菊花中分离制备刺槐素单体的方法:CN,CN 103193748 A[P].)采用提取、大孔树脂柱色谱、水解、高速逆流色谱法等技术从1kg野菊花植物分离得到10mg刺槐素,该工艺采用了5种技术联合进行分离,操作复杂、成本较高、收率低。
卞毓平等的发明专利(一种从菊花中提取刺槐素的方法:CN,CN 102491964 A[P].)采用萃取、大孔树脂、聚酰胺柱层析和重结晶等技术从10kg菊花植物中分离得到1.2g的刺槐素,操作复杂、步骤繁琐。
刘晓秋等的发明专利(一种柳穿鱼黄酮及其总黄酮的制备方法和用途CN,CN 101475619 A[P].)采用回流提取、大孔树脂、聚酰胺柱层析、硅胶柱层析和SephadexLH-20柱层析等技术分离得到刺槐素,该工艺采用5种技术联合进行分离,操作复杂、步骤繁琐。
技术实现要素:
本发明的目的是提供一种从香青兰中提取分离得到刺槐素的方法。
本发明的目的是通过以下技术方案实现的:
a、将香青兰干燥的地上部分粉碎,用5~10倍量的40%~95%乙醇浸泡12~24h;
b、采用渗漉法,香青兰药材与40%~95%乙醇比例1∶30~40,流速1~6mL/min,收集渗漉液;
c、渗漉液用孔径0.1~10mm的网孔过滤1~5次,滤液合并;
d、用减压蒸馏装置,在压力:0.08~0.1Mpa,温度:30~60℃下,蒸馏除去乙醇得0.8~1.2g/mL的稠浸膏;水浴干燥后得浸膏粉;
e、将浸膏粉采用70%~100%乙醇溶解后干法拌样,上100~200目聚酰胺进行柱层析,采用20~95%乙醇梯度洗脱,并收集60~75%乙醇梯度的洗脱液,每个梯度洗脱液为4~5倍量柱体积;洗脱液用减压蒸馏装置,在压力:0.08~0.1Mpa,温度:40~60℃下蒸干得浸膏粉;
f、为了进一步纯化所得浸膏粉,滤去杂质,采用95%乙醇对浸膏粉进行重结晶,所得制备液用减压蒸馏装置,在压力:0.08~0.1Mpa,温度:40~60℃下蒸干得单体刺槐素。
有益技术效果
本专利采用聚酰胺柱层析和重结晶技术联合的方法,方法简单,步骤简短。从1kg香青兰植物中分离得到0.71g的刺槐素,转移率较高。
本发明获得的刺槐素纯度高,达到99%。
附图说明
下面将结合附图和具体实施方式对本发明的上述和其他目的、特征和优点作出进一步详细的说明。
图1为本发明提供方法的工艺流程图;
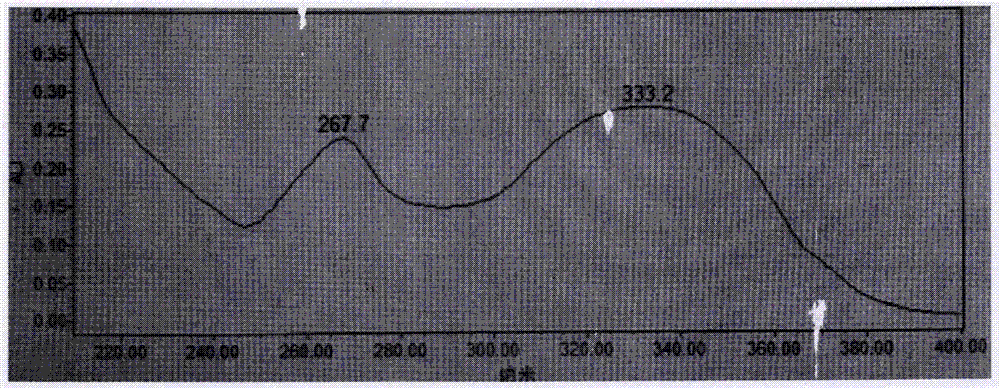
图2为根据本发明一个实施例所制备的刺槐素的紫外光谱(UV)图;
图3为根据本发明一个实施例所制备的刺槐素的红外光谱(IR)图;
图4为根据本发明一个实施例所制备的刺槐素的电喷雾质谱(ESI-MS)图;
图5为根据本发明一个实施例所制备的刺槐素的核磁共振氢谱(1H-NMR)图;
图6为根据本发明一个实施例所制备的刺槐素的核磁共振碳谱(13C-NMR)图。
具体实施方式
本发明提供的一种刺槐素的制备方法,包括获得香青兰的提取物,以及对提取物进一步纯化、层析、结晶等步骤。下面结合附图,详述本发明所提供的方法。
如图1所示,首先,将1份重量的香青兰干燥的地上部分粉碎,用15~25重量倍数的40~95vol%的醇溶液提取,例如可以选用乙醇或甲醇或丙醇或它们的任意混合物渗漉提取1~2次,每次提取6~24h。然后,将提取液浓缩,例如可以采用减压浓缩的方法,浓缩后提取液呈膏状。之后再将膏状物干燥,例如可以采用真空干燥的方法,将膏状物制成浸膏粉。
将浸膏粉用醇溶液纯化,得到溶液。纯化用的醇溶液包括,但不限于甲醇、乙醇、丙醇,以及它们的任意组合。优选乙醇,纯化的次数一般为1~2次。
将纯化后的溶液置于60℃水浴锅中拌入聚酰胺粉,不断搅拌直至溶剂挥干,聚酰胺拌入量为浸膏量的1/5。
将拌好样品,进行聚酰胺柱层析。层析的步骤可以为:加适量水于拌样聚酰胺中,使其呈混悬状上样。上柱完毕后,按梯度比例通入流动相进行洗脱。流动相采用复合洗脱剂,该复合洗脱剂由A组分和B组分构成,复合洗脱剂中A组分为乙醇且B组分为蒸馏水时,A组分与B组分的体积比为0∶100、2∶3、1∶1、3∶2、3∶1、11∶1。例如流动相可以采用乙醇-水或乙酸乙酯-乙醇,优选乙醇-水。此时刺槐素的组分主要在流动相乙醇-蒸馏水体积比为3∶2、3∶1时被洗脱。最后,合并相同组分洗脱液并浓缩,得到得到浸膏粉。
进一步地,为了提高刺槐素的收率,还可利用醇溶液,特别是95vol%的乙醇-水溶液,再对上述浸膏粉进行重结晶,即得到淡黄色粉末状结晶,为刺槐素成品,其纯度可达98%以上。经UV、IR、MS、1H-NMR、13C-NMR对所得组分的结构进行鉴定,可知其为刺槐素。
图2、图3为根据本发明的制备方法制备的刺槐素的UV图谱和IR图谱。
图4为根据本发明的制备方法制备的刺槐素的ESI-MS图谱,根据刺槐素的ESI-MS的分析可知,ESI-MS特征峰在m/z 285.20[M+](正离子),m/z 250.2[M+2OH-],m/z 302.4[M++CH3],m/z330.4[M++2OCH3-]。再结合图5、图6所示的根据本发明的制备方法制备的刺槐素的NMR图谱分析,可确定其分子量为284.2,分子式为C16H12O5,其中,1H-NMR(400MHz,DMSO)图谱中表现出典型的黄酮苷类化合物的氢谱特征,通过耦合常数及化学位移可确定每个氢的归属,δ:12.92(1H,S,5-OH),8.04(2H,d,J=8.8Hz,H-2′,6′),7.11(2H,d,J=8.8Hz,H-3′,5′),6.87(1H,d,H-3),6.50(1H,d,J=1.7Hz,H-8),6.20(1H,d,J=1.7Hz,H-6),3.86(3H,s,OCH3);13C-NMR(DMSO,400MHz)图谱中呈现出16个碳信号,为1个CH3,8个CH,7个季碳,δc表明分子中含一个羰基(δ181.78),δ:163.29(C-2),103.54(C-3),181.78(C-4),164.39(C-7),162.32(C-4′),161.46(C-9),128.34(C-2′,6′),122.84(C-1′),114.60(C-3′,5′),103.71(C-10),98.95(C-8),94.07(C-6),55.57(OCH3)。因此,可确定所得化合物为刺槐素。
下面通过具体实施例对本发明作进一步详述,以下实施例只是描述性的,不是限定性的,不能以此限定本发明的保护范围。
实施例1:从香青兰中提取分离得到刺槐素的方法,按以下步骤进行:
a、将香青兰干燥的地上部分粉碎,用10倍量的40%乙醇浸泡24h;
b、采用渗漉法,香青兰药材3.6kg与75%乙醇比例1∶40,流速6mL/min,收集乙醇渗漉液;
c、渗漉液用孔径0.5mm的网孔过滤2次,滤液合并;
d、用减压蒸馏装置,在压力:0.08Mpa,温度:30~60℃下,蒸馏除去乙醇得1.2g/mL的稠浸膏;水浴干燥后得浸膏粉500g;
e、将100g浸膏粉采用70%乙醇溶解后干法拌样,上100~200目聚酰胺进行柱层析,采用40~95%乙醇梯度洗脱,得到洗脱液共90000mL,并收集60~75%乙醇梯度的洗脱液38000mL,每个梯度洗脱液为4倍量柱体积;洗脱液用减压蒸馏装置,在压力:0.1Mpa,温度:40℃下蒸干得浸膏粉10.0g;
f、为了进一步纯化所得浸膏粉,滤去杂质,采用100倍量的95%乙醇对所述浸膏粉进行重结晶,所得制备液用减压蒸馏装置,在压力:0.08Mpa,温度:40℃下蒸干得淡黄色结晶0.51g。
一、结构鉴定:取所得样品分别对UV、IR、MS、NMR进行归峰解谱,确定实施例1所提纯的样品为刺槐素。
二、纯度鉴定:
熔点(mp)测定:263℃~265℃。
薄层色谱检测:采用两种展开体系进行检测,薄层板用聚酰胺薄膜。展开剂A为乙醇-甲酸水(体积比为1∶1),RfA为0.33;展开剂B为乙酸乙酯-95%乙醇(体积比为6∶4),RfB为0.61,紫外365nm下见黄色斑点,无杂质点。
HPLC检测:用HPLC外标法测定含量,选定260nm和330nm为检测波长。选用乙腈-0.1%磷酸水溶液(80∶20,V/V)为流动相,以刺槐素为对照品。精密称取实施例1制备的淡黄色粉末2.50mg于100mL容量瓶,用甲醇溶解并定容至刻度线。经Waters分析型高效液相色谱检测,外标法定量,其纯度为99.12%。
得率计算:
刺槐素浓度为24.78μg·mL-1,香青兰中刺槐素的量为2.88g/kg。
得率=(24.78μg·mL-1×100mL)/(2.50mg×3600g/2.56g×2.88g/kg)×100%=24.47%
经检测,实施例1提取得到的刺槐素的纯度为99.16%,得率为24.47%。
实施例2:从香青兰中提取分离得到刺槐素的方法,按以下步骤进行:
a、将香青兰干燥的地上部分粉碎,用10倍量的75%乙醇浸泡18h;
b、采用渗漉法,香青兰药材3.0kg与75%乙醇比例1∶35,流速6mL/min,收集乙醇渗漉液;
c、渗漉液用孔径0.1mm的网孔过滤1次,滤液合并;
d、用减压蒸馏装置,在压力:0.09Mpa,温度:60℃下,蒸馏除去乙醇得1.0g/mL的稠浸膏;水浴干燥后得浸膏粉410g;
e、将100g浸膏粉采用70%乙醇溶解后干法拌样,上100~200目聚酰胺进行柱层析,采用40~75%乙醇梯度洗脱得到洗脱液共75000mL,并收集60~75%乙醇梯度的洗脱液35000mL,每个梯度洗脱液为4倍量柱体积;洗脱液用减压蒸馏装置,在压力:0.1Mpa,温度:50℃下蒸干得浸膏粉9.50g;
f、为了进一步纯化所得浸膏粉,滤去杂质,采用100倍量的95%乙醇对所述浸膏粉进行重结晶,所得制备液用减压蒸馏装置,在压力:0.10Mpa,温度:40℃下蒸干得淡黄色结晶0.49g。
一、结构鉴定:取所得样品分别对UV、IR、MS、NMR进行归峰解谱,确定实施例2所提纯的样品为刺槐素。
二、纯度鉴定:
熔点(mp)测定:263℃~265℃。
薄层色谱检测:采用两种展开体系进行检测,薄层板用聚酰胺薄膜。展开剂A为乙醇-甲酸水(体积比为1∶1),RfA为0.34;展开剂B为乙酸乙酯-95%乙醇(体积比为6∶4),RfB为0.61,紫外365nm下见黄色斑点,无杂质点。
HPLC检测:用HPLC外标法测定含量,选定260nm和330nm为检测波长。选用乙腈-0.1%磷酸水溶液(80∶20,V/V)为流动相,以刺槐素为对照品。精密称取实施例2制备的淡黄色粉末2.50mg于100mL容量瓶,用甲醇溶解并定容至刻度线。经Waters分析型高效液相色谱检测,外标法定量,其纯度为99.36%,得率为22.85%。
实施例3:从香青兰中提取分离得到刺槐素的方法,按以下步骤进行:
a、将香青兰干燥的地上部分粉碎,用10倍量的40%乙醇浸泡18h;
b、采用渗漉法,香青兰药材4.0kg与70%乙醇比例1∶35,流速6mL/min,收集乙醇渗漉液;
c、渗漉液用孔径0.1mm的网孔过滤2次,滤液合并;
d、用减压蒸馏装置,在压力:0.1Mpa,温度:60℃下,蒸馏除去乙醇得1.2g/mL的稠浸膏;水浴干燥后得浸膏粉550g;
e、将100g浸膏粉采用70%乙醇溶解后干法拌样,上100~200目聚酰胺进行柱层析,采用30~75%乙醇梯度洗脱得到洗脱液共95000mL,并收集60~75%乙醇梯度的洗脱液40000mL,每个梯度洗脱液为4.5倍量柱体积;洗脱液用减压蒸馏装置,在压力:0.1Mpa,温度:50℃下蒸干得浸膏粉10.3g;
f、为了进一步纯化所得浸膏粉,滤去杂质,采用100倍量的95%乙醇对所述浸膏粉进行重结晶,所得制备液用减压蒸馏装置,在压力:0.10Mpa,温度:60℃下蒸干得淡黄色结晶0.52g。
一、结构鉴定:取所得样品分别对UV、IR、MS、NMR进行归峰解谱,确定实施例3所提纯的样品为刺槐素。
二、纯度鉴定:
熔点(mp)测定:263℃~265℃。
薄层色谱检测:采用两种展开体系进行检测,薄层板用聚酰胺薄膜。展开剂A为乙醇-甲酸水(体积比为1∶1),RfA为0.34;展开剂B为乙酸乙酯-95%乙醇(体积比为6∶4),RfB为0.61,紫外365nm下见黄色斑点,无杂质点。
HPLC检测:用HPLC外标法测定含量,选定260nm和330nm为检测波长。选用乙腈-0.1%磷酸水溶液(80∶20,V/V)为流动相,以刺槐素为对照品。精密称取实施例2制备的淡黄色粉末2.50mg于100mL容量瓶,用甲醇溶解并定容至刻度线。经Waters分析型高效液相色谱检测,外标法定量,其纯度为97.89%,得率为24.35%。
- 还没有人留言评论。精彩留言会获得点赞!