RAS蛋白的突变的片段的制作方法
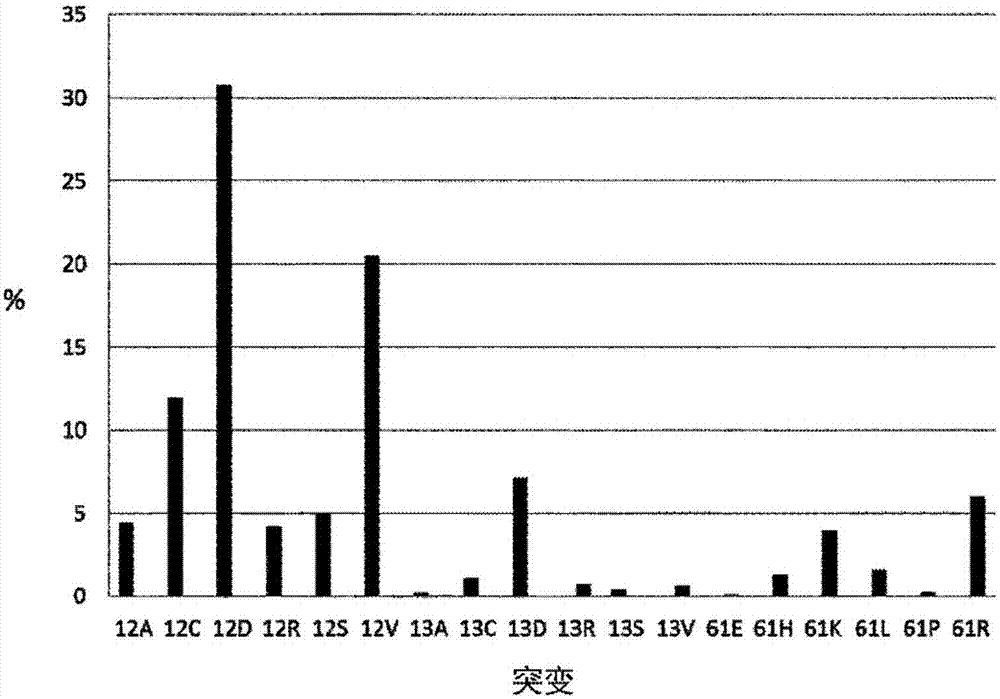
发明领域本发明提供用于引发免疫应答的ras蛋白的肽,包含用于引发免疫应答的ras蛋白的肽的肽混合物,对呈递在mhc分子上的此种肽具有特异性的t细胞,以及包含对呈递在mhc分子上的此种肽具有特异性的t细胞的t细胞混合物和t细胞制剂。本发明还涉及包含这样的肽、肽混合物、t细胞和t细胞混合物及制剂的药物制剂,这样的肽、肽混合物、t细胞和t细胞混合物及制剂用于预防和/或治疗癌症的用途,以及选择用于治疗癌症的肽、肽混合物、t细胞和t细胞混合物及t细胞制剂的方法。发明背景癌症发作的遗传背景是原癌基因、癌基因和肿瘤抑制基因的改变。原癌基因是具有变成癌基因的潜能的细胞的正常基因。所有癌基因都编码蛋白质并且通过蛋白质来行使功能。在大部分情况中,它们被证明是信号转导通路的组分。在自然中癌基因通过点突变或易位而由原癌基因产生,由此导致载有所述突变的细胞的状态转变。癌症通过涉及癌基因和肿瘤抑制细胞的若干突变事件的多步过程而发展。在其最简单的形式中,原癌基因中的单碱基置换可能导致编码的蛋白质有一个氨基酸不同。在涉及鼠肿瘤的实验模型中,已经证明细胞内“自我”-蛋白质的点突变可能产生由与正常的肽具有单个氨基酸差异的肽组成的肿瘤排斥抗原。在肿瘤细胞表面上的主要组织相容性(mhc)分子的背景中识别这些肽的t细胞能够杀死肿瘤细胞并因此将肿瘤排出宿主。(boon,t.等,cell1989,vol.58,p.293-303)在近三十年,进行了大量努力以分析人肿瘤抗原的抗体。已经表明此种抗体可以用于诊断和治疗用途两者,例如连同抗癌剂一起。一个问题是抗体仅能够结合暴露在肿瘤细胞的表面上的肿瘤抗原。因为此原因,产生基于身体免疫系统的癌症治疗的努力不如预期的成功。抗体典型地识别天然构象的游离抗原并且可以有效地识别暴露在抗原表面上几乎任何位点。相对于由b细胞产生的抗体,t细胞仅识别在mhc分子背景中的抗原,所述抗原在人中被称为hla(人白细胞抗原),并且所述识别仅在适当的抗原加工之后,所述抗原加工通常由蛋白质的蛋白水解片段化组成,其产生适配到mhc分子的沟中的肽。这使得t细胞能够识别来源于胞内蛋白质的肽。t细胞可以因此识别来源于肿瘤细胞中的任何地方的异常肽(当其被mhc分子展示在肿瘤细胞表面上时)。随后t细胞可以被激活以消灭带有异常肽的肿瘤细胞。t细胞可以通过多种机制控制癌症的发展和生长。细胞毒性t细胞,hlai类限制性cd8+和hlaii类限制性cd4+,可以直接杀死带有适当的肿瘤抗原的肿瘤细胞。需要cd4+辅助t细胞来诱导和保持细胞毒性t细胞应答以及抗体应答,并且诱导巨噬细胞和淋巴因子活化的杀伤细胞(lak细胞)杀伤。已经鉴定了很多癌基因及其蛋白质产物。此外,已经证明健康人的t细胞库(repertoire)包括对被递呈在适当的hla分子上时的来源于一种p21ras癌基因产物的合成的肽片段具有特异性的t细胞。此外,预期全部癌症中的约20%与ras癌基因的突变相关。表皮生长因子受体(egfr)抗体疗法是用于治疗癌症的一线方案。然而,已经发现,在结直肠癌中,kras基因的外显子2的密码子12和13中的点突变预示了对egfr抗体的治疗的抗性,从而egfr抗体的治疗对于具有表达这种突变的肿瘤的患者是无效的。还已经发现具有表达野生型kras密码子12和/或13的肿瘤的患者中的一半以上也对egfr抗体疗法具有抗性(vaughncp等,geneschromosomescaner,2011,50,307-12)。此外,已经报道具有任何ras突变的患者甚至可以被帕尼单抗(paitumumab)-folfox4治疗损害(douillardjy等,nengjmed2013,369,1023-34)。特别地,目前的临床指南建议,只有ras野生型肿瘤的患者应该使用与folfiri或folfox化学疗法组合的西妥昔单抗(cetuximab)或帕尼单抗(panitumumab)来治疗(vancutsem等,jco,2015jan20;国家综合癌症网络:nccn结肠癌指南(nationalcomprehensivecancernetwork:nccnguidelinescoloncancer),version2.2015)。vancutsem等(jco,印刷前在线发表于2015年1月20日)公开了评价与单独的folfiri相比,folfiri加西妥昔单抗在携带在除了kras密码子12和13以外的位置处具有ras突变的肿瘤的结直肠癌患者中的效果的研究结果。发现最常见的突变位点(kras密码子12和13之外的)位于kras外显子4内,并且向folfiri中加入西妥昔单抗没有提供对在除了密码子12和13以外的基因座中具有肿瘤ras突变的患者的治疗效力上的任何改善。然而,该文献没有公开或建议对具有ras突变的患者的任何替代治疗。sorich等(annalsofoncology,26:13-21,2015)报道了这样的研究,其评价了抗-egfrmab疗法在具有外显子2之外的nras或kras突变(称为“新”ras突变)的肿瘤的转移性结直肠癌患者中的效力。所考虑的“新”突变是外显子3(密码子59和61)或外显子4(密码子117和146)中的kras突变,或外显子2、3或4中的nras突变。发现在具有“新”ras突变的患者中不存在来自抗-egfrmab疗法的无进展生存率(pfs)或总体生存率(os)上的改善,并且与具有“新”ras突变的患者相比,具有野生型ras的患者具有显著更忧的抗-egfrmab效力。该文件进一步公开了约11%的结直肠癌患者具有“新”ras突变,并且因此可能对egfr抗体疗法具有抗性。然而,该文献没有建议egfr抗体疗法的任何替代治疗。negru等(bmjopen2014,4)公开了抗-egfrmab疗法对具有ras基因中的突变的患者是无效的,并且报道了开发和验证用于在结直肠癌患者中检测kras和nras突变的高分辨率溶解(hrm)方法的研究。该文献公开了所研究的具有野生型kras外显子2的结直肠癌患者中的15.31%在kras外显子3或4或者nras外显子2、3或4中具有突变。特别地,与对于kras和nras外显子3中的每个为1.91%相比,外显子4突变占所研究的患者中外显子2之外的ras突变中的5.3%。然而,该文献没有建议egfr抗体疗法的备选治疗,其用于具有ras突变的患者,并且特别是用于具有除了ras外显子2突变以外的ras突变的患者。在vancutsem等、sorrich等和negru等之前,并不知晓ras蛋白的外显子4中的突变与癌症相关。因此,没有提出或测试对应于ras蛋白的外显子4的肽在治疗癌症中的有用性。wo92/14756公开了引发t细胞免疫性的癌基因蛋白质产物的合成的肽和片段,其用于针对与ras相关的癌症的疫苗和用于治疗癌症的组合物。所述肽必须对应于由癌细胞呈递的癌基因的活性片段并且在对应于癌基因突变的一个或多个位置处包括突变。该文献公开了在ras蛋白的位置12、13和61处的突变并且仅具体公开了g12a、g12v、g12c、g12s、g12k、g12d、g12r、q61r、q61k、q61l、q61h、g13v和g13d突变。然而,该文献并未公开使用在除了12、13和61以外的密码子中具有突变的任何肽,并且特别是使用对应于ras外显子4的肽。此外,虽然该文献提及疫苗可以包含具有在癌基因蛋白质中发现的最常见的突变的肽的选择,但是其没有建议任何具体的组合。wo00/66153讨论了用于癌症疫苗的引发t细胞免疫性的合成的肽混合物。所述肽混合物由rasp21突变体肽组成并且该文献仅具体公开了g12a、g12c、g12d、g12r、g12s、g12v、q61h、q61k、q61l、q61r和g13d突变。该文献还公开了由肽混合物引发的免疫应答显著高于由单个肽引发的免疫应答;然而,其没有建议在除了密码子12、13或16以外具有突变的任何ras肽,或者特别是在外显子4具有突变的任何ras肽。此外,该文献没有公开可以使用除了其中具体公开的那些以外的任何其它的肽组合。gb2328689公开了能够诱导特异性细胞毒性t细胞应答(cd8+)的肽,其包含p21ras原癌基因蛋白的8至10个氨基酸(包括p21ras原癌基因蛋白的位置12和/或13或位置61)并且在位置12、13或61具有氨基酸置换。该文献还公开了所述肽可以用作癌症疫苗并且可以在用于抗癌治疗的组合物中使用。然而,没有公开除了位置12、13或61处具有突变的那些以外的肽,并且没有公开特别有用的具体肽混合物。此外,这些文献都没有讨论具体的肽如何与具体类型的癌症相关。由于以下风险,即混合物中的一些肽是免疫显性的并且因此抑制其他肽的hla呈递,所以对将肽混合物用于患者的疫苗接种存在很大的担心(pions等,blood,1999feb1;93(3):p952-62)。由体外进行的实验已知,多种突变的ras肽可以竞争结合负责向相关t细胞的呈递的hla分子,并且具有相同长度但是表现不同突变的肽可以以不同程度的效力抑制表现另一种突变的肽的结合和识别(t.gedde-dahliii等,humanimmunol.1994,33,p.266-274,以及b.h.johanssen等,scand.j.immunol.,1994,33,p.607-612)。由这些事实,免疫显性问题已被认为是突变ras肽疫苗的一个问题,但是在前述段落中提及的任何文献中均未讨论该问题。gjertsen等(int.j.cancer2001,92,p.441-450)公开了涉及用合成的突变体ras肽连同粒细胞-巨噬细胞集落刺激因子给患有胰腺的腺癌的患者进行疫苗接种的i/ii期试验。该试验使用单个肽疫苗或四种突变体肽的混合物。组合疫苗由四种在胰腺癌中发现的最常见的kras突变组成,即具有g12v、g12d、g12c或g12r突变的肽。然而,该文献没有公开可用的任何其他肽组合,没有公开与癌症相关的任何其他ras蛋白突变,没有讨论具体的肽如何与具体类型的癌症相关,并且没有讨论疫苗内免疫显性和冗余的问题。wedén等(int.j.cancer2010,128(5),p.1120-1128)报道了用合成的突变体ras肽进行疫苗接种的患有胰腺癌的患者的长期随访。所述疫苗由单个的ras肽或七种ras肽的混合物组成。特别地,用于该试验的七种ras肽具有g12a、g12c、g12d、g12r、g12s、g12v或g13d突变。然而,该文献没有讨论具体的肽如何与具体类型的癌症相关,没有公开可用的任何其他肽组合,并且没有讨论疫苗内免疫显性和冗余的问题。hunger等(exp.dermatol.2001,10:161-167)报道了以安全性作为第一终点并且以ras肽的免疫原性作为第二终点的ras肽的体内免疫原性的临床前导性研究。用具有四密码子61突变的n-ras肽(残基49-73)对黑素瘤患者进行皮内免疫。八名患者显示阳性的dth反应。然而,该文献没有讨论具体的肽如何与具体类型的癌症相关,没有公开可用的任何其他肽组合,并且没有讨论疫苗内免疫显性和冗余的问题。prior等(cancerres.2012,72(10),p.2457-2467)公开了不同类型的癌症与特定ras同种型的突变相关并且各同种型具有不同的密码子突变特征。此外,prior等公开了在ras蛋白的位置12、13和61中出现总计18种突变,每个位置出现六种突变。该综述还讨论了这些突变对ras功能的影响以及导致ras同种型突变的差异模式的潜在机制。然而,该文献没有涉及癌症的治疗或预防,或疫苗内的免疫显性和冗余的问题。此外,没有公开针对癌症的疫苗或治疗,并且该文献没有公开可用的任何其他肽组合。因此,需要提供对于egfr抗体疗法的备选治疗,其可以被施用至携带具有ras突变的肿瘤的癌症患者。特别地,需要提供对于egfr抗体疗法的备选治疗,其用于携带具有ras外显子4突变的肿瘤的患者,并且尤其用于具有结直肠癌的患者。此外,需要提供靶向特定癌症的备选治疗,其克服了免疫显性和冗余的问题,并且是成本有效的。另外,需要提供用于尽可能多的结直肠癌患者的疫苗和/或治疗。发明概述本发明提供用于解决以上讨论的问题的方案,因为现在已经发现在对应于ras基因的外显子4的密码子的氨基酸处具有点突变的肽,以及包含至少一种所述肽的肽混合物,可以用作针对与ras蛋白突变相关的癌症的疫苗和/或作为与ras蛋白突变相关的癌症的治疗。特别地,已经发现至少一些本发明的肽混合物可以用作针对超过99%的与ras蛋白突变相关的癌症的疫苗和/或用于超过99%的与ras蛋白突变相关的癌症的治疗,并且用作针对全部结直肠癌中的10%的疫苗和/或用于全部结直肠癌中的10%的治疗。特别地,当与被称为tg02的肽混合物组合考虑时(在本文中进一步讨论),本发明的肽和肽混合物可以用于治疗全部结直肠癌中的至少50%。本发明的肽和肽混合物提供了用于对egfr抗体疗法耐受的患者的替代治疗。此外,本发明的肽和肽混合物减轻了免疫显性的问题并且减少了药物组合物内的活性成分的冗余,由此使得所述肽和肽混合物成为更加成本有效的疫苗和/或治疗。此外,本发明允许靶向具体类型癌症的疫苗接种和/或治疗以及选择靶向具体类型癌症的肽混合物的方法。因此,在本发明的第一方面,提供适于引发免疫应答的肽,其中所述肽包含对应于ras蛋白的片段的区域,其中所述区域包含包括突变的位置在内的至少8个氨基酸,所述区域具有不在所述突变的位置处的与ras蛋白的相应区域相同的至少6个氨基酸残基,所述区域在所述突变的位置处具有点突变,并且所述突变的位置是ras蛋白的位置117或146。有利地,所述点突变是k117n、a146t或a146v突变。优选地,所述肽用作疫苗或药物。在本发明的第二方面,提供适于引发免疫应答的肽混合物,所述肽混合物包含第一肽和第二肽,其各自对应于ras蛋白的片段,其中:第一肽包含至少8个氨基酸的区域,所述区域包括第一突变的位置,第二肽包含至少8个氨基酸的区域,所述区域包括第二突变的位置,第一肽和第二肽的所述区域中的每个独立地具有不在所述第一突变的位置和所述第二突变的位置处的与ras蛋白的相应区域相同的至少6个氨基酸残基,第一肽和第二肽中的每个在所述第一突变的位置和第二突变的位置处具有点突变,其中所述第一突变的位置是ras蛋白的位置117或146,并且所述第二突变的位置是ras蛋白的位置12、13、61、117或146,并且其中第一突变的位置的点突变不同于第二突变的位置的点突变。有利地,第一肽的点突变选自k117n、a146t或a146v突变。方便地,第二肽的点突变选自k117n、a146t、a146v、g13a、g13c、g13d、g13r、g13s、g13v、g12a、g12c、g12d、g12r、g12s、g12v、q61e、q61h、q61k、q61l、q61p或q61r突变。优选地,第一肽在ras蛋白的位置146处具有点突变,并且第二肽在ras蛋白的位置61处具有点突变。有利地,肽混合物包含至少一种另外的肽,所述至少一种另外的肽对应于ras蛋白的片段,其中:所述至少一种另外的肽包含至少8个氨基酸的区域,所述区域包括突变的位置,所述至少一种另外的肽的所述区域具有不在所述突变的位置处的与ras蛋白的相应区域相同的至少6个氨基酸残基,所述至少一种另外的肽在所述突变的位置处具有点突变,其中所述至少一种另外的肽的所述突变的位置是ras蛋白的位置12、13、61、117或146,并且所述至少一种另外的肽的所述点突变不同于第一ras肽和第二ras肽中的每个的点突变。优选地,所述第一突变的位置是ras蛋白的位置146,并且所述第二突变的位置是ras蛋白的位置12、13或61。有利地,第一突变的位置是ras蛋白的位置146,第二突变的位置是ras蛋白的位置12,并且至少一种另外的肽的突变的位置是ras蛋白的位置13。方便地,第一突变的位置是ras蛋白的位置146,第二突变的位置是ras蛋白的位置13,并且至少一种另外的肽的突变的位置是ras蛋白的位置61。优选地,第一突变的位置是ras蛋白的位置146,第二突变的位置是ras蛋白的位置12,第一另外的肽具有的突变的位置为ras蛋白的位置13,并且肽混合物还包含第二另外的肽,所述第二另外的肽具有的突变的位置为ras蛋白的位置61。有利地,第一突变的位置是ras蛋白的位置146,第二突变的位置是ras蛋白的位置13,第一另外的肽具有的突变的位置为ras蛋白的位置13,并且肽混合物还包含第二另外的肽,所述第二另外的肽具有的突变的位置为ras蛋白的位置61。方便地,肽混合物包含具有a146t突变的第一肽,具有g13r突变的第二肽,具有g13v突变的第三肽,具有q61r突变的第四肽,具有q61k突变的第五肽,具有q61h突变的第六肽,和具有q61l突变的第七肽。优选地,肽混合物包含以下或基本上由以下组成:包含由seqidno:1或2表示的序列的第一肽,包含由seqidno:33表示的序列的第二肽,包含由seqidno:34表示的序列的第三肽,包含由seqidno:35表示的序列的第四肽,包含由seqidno:36表示的序列的第五肽,包含由seqidno:37表示的序列的第六肽,和包含由seqidno:38表示的序列的第七肽。在本发明的第三方面,提供对呈递在mhc分子上的根据上述第一或第二方面的肽具有特异性的t细胞。在本发明的第四方面,提供包含根据上述第三方面的t细胞的t细胞制剂。在本发明的第五方面,提供t细胞混合物,所述t细胞混合物包含对呈递在mhc分子上的根据上述第二方面的肽混合物之一中的每种肽具有特异性的t细胞。在本发明的第六方面,提供这样的t细胞受体或其抗原结合片段,其对呈递在mhc分子上的根据上述第一方面的肽具有特异性,或者对呈递在mhc分子上的根据本发明的第六方面使用的肽具有特异性。在本发明的第七方面,提供包含核苷酸序列的核酸,所述核苷酸序列编码根据上述第一方面的肽,根据上述第一方面使用的肽,或根据上述第六方面的t细胞受体。在本发明的第八方面,提供包含根据上述第七方面的核酸的载体。在本发明的第九方面,提供包含根据上述第八方面的载体的宿主细胞。在本发明的第十方面,提供药物组合物,所述药物组合物包含根据上述第一方面的肽,根据上述第一方面使用的肽,根据上述第二方面的肽混合物,根据上述第三方面的t细胞,根据上述第四方面的t细胞制剂,根据上述第五方面的t细胞混合物,根据上述第六方面的t细胞受体或其抗原结合片段,根据上述第七方面的核酸,根据上述第八方面的载体,或根据上述第九方面的宿主细胞,以及药用载体、稀释剂和/或赋形剂。在本发明的第十一方面,提供根据上述第一方面的肽,根据上述第一方面使用的肽,根据上述第二方面的肽混合物,根据上述第三方面的t细胞,根据上述第四方面的t细胞制剂,根据上述第五方面的t细胞混合物,根据上述第六方面的t细胞受体或其抗原结合片段,根据上述第七方面的核酸,根据上述第八方面的载体,根据上述第九方面的宿主细胞,或根据上述第十方面的药物组合物,其用于预防或治疗癌症。有利地,所述癌症是肾上腺癌、自主神经节癌、胆管癌、骨癌、乳腺癌、中枢神经系统癌、宫颈癌、结直肠癌、子宫内膜癌、造血器官(haematopoietic)癌、淋巴癌、肾癌、大肠癌、肝癌、肺癌、食管癌、卵巢癌、胰腺癌、前列腺癌、唾液腺癌、皮肤癌、小肠癌、胃癌、睾丸癌、胸腺癌、甲状腺癌、上呼吸消化道癌和尿道癌和/或恶性黑素瘤。优选地,所述癌症是结直肠癌。在本发明的第十二方面,提供治疗或预防癌症的方法,其中所述方法包括向有需要的受试者施用根据上述第一方面的肽,根据上述第一方面使用的肽,根据上述第二方面的肽混合物,根据上述第三方面的t细胞,根据上述第四方面的t细胞制剂,根据上述第五方面的t细胞混合物,根据上述第六方面的t细胞受体或其抗原结合片段,根据上述第七方面的核酸,根据上述第八方面的载体,或根据上述第九方面的药物组合物。在本发明的第十三方面,提供治疗或预防癌症的方法,其中所述方法包含:a)鉴定取自患者的样品中的ras蛋白突变;b)选择根据本发明的第一方面的肽,其包含对应于所述样品中鉴定的ras蛋白突变中的至少一个的点突变;根据本发明的第一方面使用的肽,其包含对应于所述样品中鉴定的ras蛋白突变中的至少一个的点突变;根据本发明的第二方面的肽混合物,其包含肽,所述肽包含对应于所述样品中鉴定的ras蛋白突变中的至少一个的点突变;对呈递在mhc分子上的根据本发明的第三方面的肽具有特异性的t细胞,所述肽包含对应于所述样品中鉴定的ras蛋白突变中的至少一个的点突变;根据本发明的第四方面的t细胞制剂,所述t细胞制剂包含对呈递在mhc分子上的肽具有特异性的t细胞,所述肽包含对应于所述样品中鉴定的ras蛋白突变中的至少一个的点突变;根据本发明的第五方面的t细胞混合物,所述t细胞混合物包含对呈递在mhc分子上的肽具有特异性的t细胞,所述肽包含对应于所述样品中鉴定的ras蛋白突变中的至少一个的点突变;根据本发明的第六方面的t细胞受体或其抗原结合片段,所述t细胞受体或其抗原结合片段对包含对应于所述样品中鉴定的ras蛋白突变中的至少一个的点突变的肽具有特异性;根据本发明的第七方面的核酸,所述核酸编码包含对应于所述样品中鉴定的ras蛋白突变中的至少一个的点突变的肽;根据本发明的第八方面的载体,所述载体编码包含对应于所述样品中鉴定的ras蛋白突变中的至少一个的点突变的肽;或根据本发明的第九方面的药物组合物,所述药物组合物包含肽,用作疫苗或药物的肽,包含对应于所述样品中鉴定的ras蛋白突变中的至少一个的点突变的肽混合物,或包含对呈递在mhc分子上的包含对应于所述样品中鉴定的ras蛋白突变中的至少一个的点突变的肽具有特异性的t细胞、t细胞制剂或t细胞混合物,或对包含对应于所述样品中鉴定的ras蛋白突变中的至少一个的点突变的肽具有特异性的t细胞受体或其抗原结合片段,或编码包含对应于所述样品中鉴定的ras蛋白突变中的至少一个的点突变的肽的核酸或载体,以及c)向患者施用所述肽、肽混合物、t细胞、t细胞制剂、t细胞混合物、抗体或其抗原结合片段、核酸或载体。术语“肽”,当在本文中使用时,是指作为较长的蛋白质的片段(或具有对应于较长的蛋白质的片段的序列)的氨基酸残基的聚合物。该术语还适用于这样的氨基酸聚合物,其中一个或多个氨基酸残基是修饰的残基,或非天然存在的残基,如相应的天然存在的氨基酸的人工化学拟似物,以及天然存在的氨基酸聚合物。术语“氨基酸”,当在本文中使用时,是指天然存在的氨基酸和合成的氨基酸,以及与天然存在的氨基酸类似的氨基酸类似物和氨基酸拟似物。天然存在的氨基酸是由遗传密码编码的那些氨基酸,以及在细胞中翻译后修饰的那些氨基酸(例如,羟脯氨酸、γ-羧基谷氨酸和o-磷酸丝氨酸)。短语“氨基酸类似物”是指具有相同的作为天然存在的氨基酸的基本化学结构(结合氢的α碳、羧基、氨基和r基团)但是具有修饰的r基团或修饰的主链(例如,高丝氨酸、高丝氨酸、蛋氨酸亚砜、蛋氨酸甲基锍)的化合物。术语“氨基酸拟似物”是指具有不同结构的化学化合物。两个序列之间的百分比“同一性”可以使用blastp算法版本2.2.2(altschul,stephenf.,thomasl.madden,alejandroa.jinghuizhang,zhengzhang,webbmiller,和davidj.lipman(1997),“gappedblastandpsi-blast:anewgenerationofproteindatabasesearchprograms”,nucleicacidsres.25:3389-3402)使用默认参数来确定。特别地,可以在互联网上使用urlhttp://www.ncbi.nlm.nih.gov/blast来访问blast算法。术语“免疫应答”,当在本文中使用时,在一些实施方案中是指在主要组织相容性(mhc)分子将肽呈递在细胞表面上后t细胞介导的免疫应答,并且特别地是指在肽的呈递后的t细胞的激活。术语“ras蛋白”,当在本文中使用时,是指由ras原癌基因编码的那类小gtp酶蛋白并且包括ras蛋白的全部三种同种型:hras、kras和nras。在一些实施方案中,术语“ras蛋白”是指对应于uniprotkb/swiss-prot登录号p01112.1并且如seqidno:39中所示的蛋白质,对应于uniprotkb/swiss-prot登录号p01116并且如seqidno:44中所示的蛋白质,或者对应于uniprotkb/swiss-prot登录号p01111并且如seqidno:45中所示的蛋白质。术语“ras蛋白的位置117”,当在本文中使用时,是指从n端数起,形成野生型ras蛋白的一级结构的氨基酸链中的第一百一十七个氨基酸。术语“ras蛋白的位置146”,当在本文中使用时,是指从n端数起,形成野生型ras蛋白的一级结构的氨基酸链中的第一百四十六个氨基酸。术语“ras蛋白的位置13”,当在本文中使用时,是指从n端数起,形成野生型ras蛋白的一级结构的氨基酸链中的第十三个氨基酸。术语“ras蛋白的位置12”,当在本文中使用时,是指从n端数起,形成野生型ras蛋白的一级结构的氨基酸链中的第十二个氨基酸。术语“ras蛋白的位置61”,当在本文中使用时,是指从n端数起,形成野生型ras蛋白的一级结构的氨基酸链中的第六十一个氨基酸。术语“对应于位置117的氨基酸”,当在本文中使用时,表示ras蛋白的肽中的位于所述肽的氨基酸链中在对应于ras蛋白的氨基酸序列的第一百一十七个氨基酸(从n端数起)的位置处的氨基酸。术语“对应于位置12的氨基酸”、“对应于位置13的氨基酸”、“对应于位置61的氨基酸”和“对应于位置146的氨基酸”具有相应的含义。术语“肽混合物”,当在本文中使用时,是指被混合但未化学结合的两个以上的肽。所述混合物可以作为干粉、溶液、悬浮液或胶体呈现,并且可以是均质的或异质的。术语“ras蛋白突变”,当在本文中使用时,是指在存在于取自受试者的样品中的ras蛋白中存在的一个或多个点突变。术语“点突变”,当在本文中使用时,是指蛋白质产物的多肽链中的单个氨基酸残基被不同的氨基酸残基代替。术语,例如,“g12v突变”,当在本文中使用时,是指使得野生型ras蛋白的位置12处的甘氨酸(g)被缬氨酸(v)代替的点突变。类似的定义适用于类似的术语,如k117n、a146t、g13c、g13r、q61h等。术语“核酸”或“核酸分子”,当在本文中使用时,是指多核苷酸的聚合物。核酸可以包含天然存在的核苷酸或者可以包含人工核苷酸,诸如肽核苷酸、吗啉(morpholin)和锁定(locked)核苷酸以及乙二醇核苷酸和苏糖核苷酸。术语“核苷酸”,当在本文中使用时,是指被细胞酶识别的天然存在的核苷酸或合成的核苷酸类似物。术语“药物组合物”,当在本文中使用时,表示适用于出于治疗目的而向目标人或动物受试者施用的药物制剂。附图简述图1是这样的图,其显示了结直肠癌中ras蛋白中的突变的发生率。图2是这样的图,其显示存在于所有癌症中的ras突变的发生率。图3是这样的图,其显示对应于本发明的两种肽混合物(tg02和tg03)中的肽的在所有癌症中的ras突变的相应发生率。图4是这样的图,其显示对应于本发明的两种肽混合物(tg02和tg03)中的肽的在肺癌中的ras突变的相应发生率。图5是这样的图,其显示对应于本发明的两种肽混合物(tg02和tg03)中的肽的在结直肠癌中的ras突变的相应发生率。图6是这样的图,其显示对应于本发明的两种肽混合物(tg02和tg03)中的肽的在恶性黑素瘤中的ras突变的相应发生率。图7是这样的图,其显示在健康供体中,对三轮的利用具有g13c突变的ras肽(seqidno:19)和具有g13r突变的ras肽(seqidno:27)的混合物的体外刺激的增殖的t细胞应答。apc:抗原递呈细胞(pbmc),cpm:计数/分钟。图8是这样的图,其显示在健康供体中,对三轮的利用由g13c肽(seqidno:19)、g13d肽(seqidno:20)、g12a肽(seqidno:21)、g12c肽(seqidno:22)、g12d肽(seqidno:23)、g12r肽(seqidno:24)、g12s肽(seqidno:25)、g12v肽(seqidno:26)和g13r肽(seqidno:27)组成的ras肽混合物的体外刺激的增殖的t细胞应答。apc:抗原递呈细胞(pbmc),cpm:计数/分钟。图9是这样的图,其显示在健康供体中,在利用tg02+13r的三轮体外刺激后,对g13cras肽(seqidno:19)的t细胞应答。apc:抗原递呈细胞(pbmc),cpm:计数/分钟。图10是这样的图,其显示取自用ras肽混合物(tg02;小鼠#4和#7)和tg02+viscogeltm(小鼠#24、#29和#30)接种的小鼠的脾细胞的增殖性应答。cona:伴刀豆球蛋白a(阳性对照)。图11是这样的图,其显示在用a146t肽(seqidno:1)刺激来自健康供体的血沉棕黄层(buffycoat)(棕黄5)后的t细胞增殖。图12是这样的图,其显示在用由a146t肽(seqidno:1)、g13c肽(seqidno:25)、g13d肽(seqidno:26)和q61r肽(seqidno:35)组成的肽混合物刺激来自健康供体的血沉棕黄层(棕黄5)后的肽特异性t细胞增殖。序列表简述seqidno.:1显示具有a146t突变的kras肽的氨基酸序列。seqidno.:2显示具有a146t突变的nras肽的氨基酸序列。seqidno.:3显示具有a146v突变的kras肽的氨基酸序列。seqidno.:4显示具有a146v突变的nras肽的氨基酸序列。seqidno.:5显示具有k117n突变的kras肽的氨基酸序列。seqidno.:6显示具有k117n突变的nras肽的氨基酸序列。seqidno.:7显示具有g13c突变的ras肽的氨基酸序列。seqidno.:8显示具有g13r突变的ras肽的氨基酸序列。seqidno.:9显示具有g13d突变的ras肽的氨基酸序列。seqidno.:10显示具有g13v突变的ras肽的氨基酸序列。seqidno.:11显示具有g13a突变的ras肽的氨基酸序列。seqidno.:12显示具有g13s突变的ras肽的氨基酸序列。seqidno.:13显示具有g12a突变的ras肽的氨基酸序列。seqidno.:14显示具有g12c突变的ras肽的氨基酸序列。seqidno.:15显示具有g12d突变的ras肽的氨基酸序列。seqidno.:16显示具有g12r突变的ras肽的氨基酸序列。seqidno.:17显示具有g12s突变的ras肽的氨基酸序列。seqidno.:18显示具有g12v突变的ras肽的氨基酸序列。seqidno.:19显示具有q61r突变的ras肽的氨基酸序列。seqidno.:20显示具有q61k突变的ras肽的氨基酸序列。seqidno.:21显示具有q61h突变的ras肽的氨基酸序列。seqidno.:22显示具有q61l突变的ras肽的氨基酸序列。seqidno.:23显示具有q61e突变的ras肽的氨基酸序列。seqidno.:24显示具有q61p突变的ras肽的氨基酸序列。seqidno.:25显示具有g13c突变的肽混合物的一个实施方案的ras肽的氨基酸序列。seqidno.:26显示具有g13d突变的肽混合物的一个实施方案的ras肽的氨基酸序列。seqidno.:27显示具有g12a突变的肽混合物的一个实施方案的ras肽的氨基酸序列。seqidno.:28显示具有g12c突变的肽混合物的一个实施方案的ras肽的氨基酸序列。seqidno.:29显示具有g12d突变的肽混合物的一个实施方案的ras肽的氨基酸序列。seqidno.:30显示具有g12r突变的肽混合物的一个实施方案的ras肽的氨基酸序列。seqidno.:31显示具有g12s突变的肽混合物的一个实施方案的ras肽的氨基酸序列。seqidno.:32显示具有g12v突变的肽混合物的一个实施方案的ras肽的氨基酸序列。seqidno.:33显示具有g13r突变的肽混合物的一个实施方案的ras肽的氨基酸序列。seqidno.:34显示具有g13v突变的肽混合物的一个实施方案的ras肽的氨基酸序列。seqidno.:35显示具有q61r突变的肽混合物的一个实施方案的ras肽的氨基酸序列。seqidno.:36显示具有q61k突变的肽混合物的一个实施方案的ras肽的氨基酸序列。seqidno.:37显示具有q61h突变的肽混合物的一个实施方案的ras肽的氨基酸序列。seqidno.:38显示具有q61l突变的肽混合物的一个实施方案的ras肽的氨基酸序列。seqidno.:39显示野生型hras蛋白的全长氨基酸序列。seqidno.:40显示包括ras蛋白的位置117的野生型kras肽的氨基酸序列。seqidno.:41显示包括ras蛋白的位置117的野生型nras肽的氨基酸序列。seqidno.:42显示包括ras蛋白的位置146的野生型kras肽的氨基酸序列。seqidno.:43显示包括ras蛋白的位置146的野生型nras肽的氨基酸序列。seqidno:44显示野生型kras蛋白的全长氨基酸序列。seqidno:45显示野生型nras蛋白的全长氨基酸序列。发明详述本发明总体上涉及ras蛋白的肽,其包含对应于ras蛋白的片段的区域,其中所述区域包含包括突变的位置在内的至少8个氨基酸,其中所述肽在突变的位置处具有点突变,并且其中所述突变的位置是ras蛋白的位置117或146。如上讨论的,这些肽可以用作针对癌症的疫苗和/或用于治疗癌症,并且现在首次证明这些突变的肽是免疫原性的。例如,图11显示了在ras蛋白的位置146处具有突变的肽是免疫原性的并且刺激t细胞的诱导。此外,本发明涉及肽混合物,所述肽混合物包含ras蛋白的至少第一肽和第二肽,所述第一肽和第二肽包含对应于ras蛋白的片段的区域,其中所述区域包含至少8个氨基酸,其中所述至少第一肽包括第一突变的位置且所述第二肽包括第二突变的位置,其中第一肽和第二肽中的每个在第一突变的位置和第二突变的位置处具有点突变,其中所述第一突变的位置是ras蛋白的位置117或146并且所述第二突变的位置是ras蛋白的位置12、13、61、117或146,并且其中每个突变彼此不同。图12显示了这样的肽混合物的一个实例不仅在诱导对于所述肽混合物的t细胞应答中有效,也在诱导对于肽混合物中的各个肽的t细胞应答中有效,并且这是首次已经证明包含具有位置146、13和61突变的肽的肽混合物在组合使用时是免疫原性的。本发明的肽可以是对应于hras、kras或nras中任一者的肽。全部这三种ras同种型在负责gdp/gtp结合的外显子2和3的所有区域中享有序列同一性,并且在负责gdp/gtp结合的外显子4的所有区域(即,在癌症中经历突变的区域)中享有非常高的序列同源性。例如,在以ras蛋白的位置146为中心的25个氨基酸序列的区域中,野生型hras和野生型nras二者与野生型kras都具有92%序列同源性(即,两个氨基酸的不同)。在以ras蛋白的位置117为中心的25个氨基酸序列的区域中,野生型nras与野生型kras具有92%同源性(即,两个氨基酸的不同),并且野生型hras与野生型kras具有80%同源性(即,五个氨基酸的不同)。由野生型外显子4编码的序列的差异不干扰gdp/gtp结合,并且是在此处指明的致癌突变影响gdp/gtp结合。在一些实施方案中,所述肽包含至少8个、至少9个、至少10个、至少12个、至少16个、至少17个、至少18个、至少20个、至少24个或至少30个氨基酸。在优选的实施方案中,所述肽包含至少8个氨基酸。在其它优选的实施方案中,所述肽包含至少17个氨基酸。在一些实施方案中,所述肽包含不多于30个氨基酸残基。例如,在一些实施方案中,所述肽包含不多于28、26、24、22、20、18、16、14、12、10或8个氨基酸。在一些实施方案中,所述肽作为包含与ras蛋白无关的元件的更长的多肽的部分呈递。特别地,更长的多肽可以包含与ras蛋白无关的一个或多个区域。所述肽在ras蛋白的位置117或146处具有点突变。野生型ras蛋白包含位置117处的赖氨酸(k)和位置146处的丙氨酸(a)。因此,位置117处的突变可以是从赖氨酸到任何其它氨基酸的点突变,并且位置146处的突变可以是从丙氨酸到任何其它氨基酸的点突变。然而,k117n、a146t和a146v突变已经发现是与癌症特别相关的。因此,在优选的实施方案中,肽的点突变是k117n、a146t和a146v突变中的一者。在特别优选的实施方案中,点突变是a146t或a146v突变。在甚至更优选的实施方案中,点突变是a146t突变,并且图11显示这样的肽是免疫原性的并且在诱导t细胞增殖中有效。在一些实施方案中,所述肽在不同于包括突变的位置的区域的位置处具有至少20%、至少25%、至少30%、至少37%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。在一些实施方案中,所述肽在不同于包括突变的位置的区域的位置处与seqidnos:1-6中的一者具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。在优选的实施方案中,所述肽在不同于包括突变的位置的区域的位置处与seqidnos:1-6中的一者具有至少95%序列同一性。在其它实施方案中,所述肽在不同于包括突变的位置的区域的位置处与seqidnos:1-6中的一者具有100%序列同一性。在特别优选的实施方案中,所述肽在不同于包括突变的位置的区域的位置处与seqidnos:1-4中的一者具有100%序列同一性。在甚至更优选的实施方案中,所述肽在不同于包括突变的位置的区域的位置处与seqidnos:1和2中的一者具有100%序列同一性。在上述肽混合物的一些实施方案中,第一肽和第二肽中的每个独立地包含至少8个、至少9个、至少10个、至少12个、至少16个、至少17个、至少18个、至少20个、至少24个或至少30个氨基酸。在优选的实施方案中,第一肽和第二肽中的每个包含至少8个氨基酸。在其它优选的实施方案中,第一肽和第二肽中的每个包含至少17个氨基酸。在一些实施方案中,第一肽和第二肽中的每个独立地包含不多于30个氨基酸残基。例如,在一些实施方案中,第一肽和第二肽中的每个包含不多于28、26、24、22、20、18、16、14、12、10或8个氨基酸。第一肽和第二肽可以具有相同的氨基酸数量,或者他们可以具有不同的氨基酸数量。在一些实施方案中,第一肽和第二肽中的每个在不同于包括突变的位置的区域的位置处与ras蛋白具有至少20%、至少25%、至少30%、至少37%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。在一些实施方案中,第一肽在不同于包括突变的位置的区域的位置处与seqidnos:1-6中的一者具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。在优选的实施方案中,第一肽在不同于包括突变的位置的区域的位置处与seqidnos:1-6中的一者具有至少95%序列同一性。在其它实施方案中,第一肽在不同于包括突变的位置的区域的位置处与seqidnos:1-6中的一者具有100%序列同一性。在一些实施方案中,第二肽在不同于包括突变的位置的区域的位置处与seqidnos:1-24中的一者具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。在优选的实施方案中,第二肽在不同于包括突变的位置的区域的位置处与seqidnos:1-24中的一者具有至少95%序列同一性。在其它实施方案中,第二肽在不同于包括突变的位置的区域的位置处与seqidnos:1-24中的一者具有100%序列同一性。在一些实施方案中,第一肽在不同于包括突变的位置的区域的位置处与seqidnos:1-6中的一者具有百分比序列同一性,并且第二肽在不同于包括突变的位置的区域的位置处与seqidnos:1-24中的不同的一者具有不同的百分比序列同一性。在其它实施方案中,第一肽在不同于包括突变的位置的区域的位置处与seqidnos:1-6中的一者具有百分比序列同一性,并且第二肽在不同于包括突变的位置的区域的位置处与seqidnos:1-24中的一者具有相同的百分比序列同一性。在所有实施方案中,第一肽和第二肽中的每个都能够引发免疫应答。当第一肽的突变的位置是ras蛋白的位置117时,第一肽的点突变可以是从赖氨酸(k)到任何其它氨基酸的点突变。当第一肽的突变的位置是ras蛋白的位置146时,第一肽的点突变可以是从丙氨酸(a)到任何其它氨基酸的点突变。在一些实施方案中,第一肽的点突变是k117n、a146t和a146v突变中的一者。在一些实施方案中,第一肽的点突变是a146t突变,并且在其它实施方案中,第一肽的点突变是a146v突变。在另外的实施方案中,第一肽的点突变是k117n突变。第二肽的点突变可以是从野生型氨基酸到任何其它氨基酸的点突变。例如,野生型ras蛋白在位置12和13的每个处包含甘氨酸(g),并且在位置61处包含谷氨酰胺(q)。因此,当第二肽的突变的位置是ras蛋白的位置13时,位置13处的突变可以是从甘氨酸到任何其它氨基酸的点突变。类似地,当第二肽的突变的位置是ras蛋白的位置12或61时,位置12或61处的突变可以是从甘氨酸或谷氨酰胺(视情况而定)到任何其它氨基酸的点突变。当第二肽的突变的位置是ras蛋白的位置117或146时,突变的位置处的突变可以是分别从赖氨酸或丙氨酸到任何其它氨基酸。在优选的实施方案中,第二肽的点突变是k117n、a146t、a146v、g13a、g13c、g13d、g13r、g13s、g13v、g12a、g12c、g12d、g12r、g12s、g12v、q61e、q61h、q61k、q61l、q61p或q61r突变中的任一者,独立于第一肽的点突变。在一些实施方案中,第一肽的突变的位置处的点突变是a146t突变,并且第二肽的突变的位置处的点突变是a146v、k117n、g13a、g13c、g13d、g13r、g13s、g13v、g12a、g12c、g12d、g12r、g12s、g12v、q61e、q61h、q61k、q61l、q61p或q61r突变中的任一者。在一些实施方案中,第一肽的点突变是a146t突变,并且第二肽的点突变是a146v突变。在其它实施方案中,第一肽的点突变是a146t突变,并且第二肽的点突变是k117n突变。在其它实施方案中,第一肽的点突变是a146t突变,并且第二肽的点突变是g13c、g13d或q61r突变。在其它实施方案中,第一肽的突变的位置处的点突变是a146v突变,并且第二肽的突变的位置处的点突变是a146t、k117n、g13a、g13c、g13d、g13r、g13s、g13v、g12a、g12c、g12d、g12r、g12s、g12v、q61e、q61h、q61k、q61l、q61p或q61r突变中的任一者。在一些实施方案中,第一肽的点突变是a146v突变,并且第二肽的点突变是k117n突变。在另外的其它实施方案中,第一肽的突变的位置处的点突变是k117n突变,并且第二肽的突变的位置处的点突变是g13a、g13c、g13d、g13r、g13s、g13v、g12a、g12c、g12d、g12r、g12s、g12v、q61e、q61h、q61k、q61l、q61p或q61r突变中的任一者。在本发明的备选实施方案中,肽混合物可以包含ras蛋白的至少一种另外的肽,其包含包括突变的位置在内的至少8个氨基酸的区域。至少一种另外的肽的突变的位置可以是ras蛋白的位置12、13、61、117或146,并且至少一种另外的肽在所述突变的位置处具有的点突变可以与第一肽和第二肽的点突变不同。至少一种另外的肽的突变的位置处的点突变可以是k117n、a146t、a146v、g13a、g13c、g13d、g13r、g13s、g13v、g12a、g12c、g12d、g12r、g12s、g12v、q61e、q61h、q61k、q61l、q61p或q61r突变中的任一者,独立于第一肽和第二肽的点突变。在一些实施方案中,至少一种另外的肽的突变的位置是ras蛋白的位置12、13或61,优选g13a、g13c、g13d、g13r、g13s、g13v、g12a、g12c、g12d、g12r、g12s、g12v、q61e、q61h、q61k、q61l、q61p或q61r突变,独立于第一肽和第二肽的点突变。在一些实施方案中,至少一种另外的肽的突变的位置是g13c、g13d或q61r突变,独立于第一肽和第二肽的点突变。肽混合物可以包含多于一种另外的肽。例如,肽混合物可以包含两种另外的肽,三种另外的肽,四种另外的肽,或更多种另外的肽。在肽混合物包含一种或多种另外的肽的实施方案中,另外的肽中的每个独立地具有上述至少一种另外的肽的特性。在肽混合物包含至少一种另外的肽的实施方案中,第一肽、第二肽和至少一种另外的肽中的每个独立地包含至少8个、至少9个、至少10个、至少12个、至少16个、至少17个、至少18个、至少20个、至少24个或至少30个氨基酸。在优选的实施方案中,每种肽包含至少8个氨基酸。在其它优选的实施方案中,每种肽包含至少17个氨基酸。在另外的实施方案中,每种肽包含至少18个氨基酸。在一些实施方案中,第一肽、第二肽和至少一种另外的肽中的每个独立地包含不多于30个氨基酸残基。例如,在一些实施方案中,第一肽和第二肽中的每个包含不多于28、26、24、22、20、18、16、14、12、10或8个氨基酸。通常,肽混合物中的每种肽可以包含与肽混合物中的一种或多种其它肽不同数量的氨基酸。在肽混合物包含至少一种另外的肽的实施方案中,对应于ras蛋白的突变的位置的氨基酸具有点突变。至于第二肽,突变的位置处的点突变可以是从野生型氨基酸到任何其它的氨基酸。因此,当至少一种另外的肽包含ras蛋白的位置146时,点突变可以是从丙氨酸(a)到任何其它的氨基酸。当至少一种另外的肽包含ras蛋白的位置117时,点突变可以是从赖氨酸(k)到任何其它的氨基酸。当至少一种另外的肽包含ras蛋白的位置61时,点突变可以是从谷氨酰胺(q)到任何其它的氨基酸。当至少一种另外的肽包含ras蛋白的位置13时,点突变可以是从甘氨酸(g)到任何其它的氨基酸。当至少一种另外的肽包含ras蛋白的位置12时,点突变可以是从甘氨酸(g)到任何其它的氨基酸。在至少一种另外的肽的突变的位置是ras蛋白的位置146的实施方案中,肽在除了包括位置146的区域以外的位置处与ras蛋白具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。在一些实施方案中,至少一种另外的肽在除了包括位置146的区域以外的位置处与seqidno:1-4中的一者具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。在至少一种另外的肽的突变的位置是ras蛋白的位置117的实施方案中,肽在除了包括位置117的区域以外的位置处与ras蛋白具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。在一些实施方案中,至少一种另外的肽在除了包括位置117的区域以外的位置处与seqidno:5或6中的一者具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。在至少一种另外的肽的突变的位置是ras蛋白的位置13的实施方案中,肽在除了包括位置13的区域以外的位置处与ras蛋白具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。在一些实施方案中,至少一种另外的肽在除了包括位置13的区域以外的位置处与seqidno:7-12、25、26、33和34中的一者具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。在一些实施方案中,存在多于一种另外的ras蛋白的肽,其包含包括ras蛋白的位置13的至少8个氨基酸的区域并且在对应于ras蛋白的位置13的氨基酸处具有点突变。在这样的实施方案中,具有位置13突变的肽中的每个具有不同的点突变。在至少一种另外的肽的突变的位置是ras蛋白的位置12的实施方案中,肽在除了包括位置12的区域以外的位置处与ras蛋白具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。在一些实施方案中,至少一种另外的肽在除了包括位置12的区域以外的位置处与seqidno:13-18和27-32中的一者具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。在一些实施方案中,存在多于一种另外的ras蛋白的肽,其包含包括ras蛋白的位置12的至少8个氨基酸的区域并且在对应于ras蛋白的位置12的氨基酸处具有点突变。在这样的实施方案中,具有位置12突变的肽中的每个具有不同的点突变。在至少一种另外的肽的突变的位置是ras蛋白的位置61的实施方案中,肽在除了包括位置61的区域以外的位置处与ras蛋白具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。在一些实施方案中,至少一种另外的肽在除了包括位置61的区域以外的位置处与seqidno:19-24和35-38中的一者具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。在一些实施方案中,存在多于一种另外的ras蛋白的肽,其包含包括ras蛋白的位置61的至少8个氨基酸的区域并且在对应于ras蛋白的位置61的氨基酸处具有点突变。在这样的实施方案中,具有位置61突变的肽中的每个具有不同的点突变。在一些实施方案中,肽混合物包含第一肽、第二肽和第三肽,其中第一肽的突变的位置是ras蛋白的位置146,第二肽的突变的位置是ras蛋白的位置12、13或61,并且第三肽的突变的位置是ras蛋白的位置12、13或61,其中第二肽的点突变不同于第三肽的点突变。在一些实施方案中,第一肽的突变的位置是ras蛋白的位置146,第二肽的突变的位置是ras蛋白的位置12,并且第三肽的突变的位置是ras蛋白的位置13或位置61。在一些实施方案中,第一肽的突变的位置是ras蛋白的位置146,第二肽的突变的位置是ras蛋白的位置12,并且第三肽的突变的位置是ras蛋白的位置13,而在其它实施方案中,第一肽的突变的位置是ras蛋白的位置146,第二肽的突变的位置是ras蛋白的位置12,并且第三肽的突变的位置是ras蛋白的位置61。在其它实施方案中,第一肽的突变的位置是ras蛋白的位置146,第二肽的突变的位置是ras蛋白的位置13,并且第三肽的突变的位置是ras蛋白的位置12或61。在一些实施方案中,第一肽的突变的位置是ras蛋白的位置146,第二肽的突变的位置是ras蛋白的位置13,并且第三肽的突变的位置是ras蛋白的位置61。在其它实施方案中,第一肽的突变的位置是ras蛋白的位置146,第二肽的突变的位置是ras蛋白的位置13,并且第三肽的突变的位置是ras蛋白的位置13。在其它实施方案中,肽混合物包含第一肽、第二肽和第三肽,其中第一肽的点突变是a146t突变,第二肽的点突变是a146v突变,并且第三肽的点突变是k117n突变。第一肽在除了包括位置146的区域以外的位置处与ras蛋白具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。在一些实施方案中,第一肽在除了包括位置146的区域以外的位置处与seqidno:1或2中的一者具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。第二肽在除了包括位置146的区域以外的位置处与ras蛋白具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。在一些实施方案中,第二肽在除了包括位置146的区域以外的位置处与seqidno:3或4中的一者具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。第三肽在除了包括位置117的区域以外的位置处与ras蛋白具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。在一些实施方案中,第三肽在除了包括位置117的区域以外的位置处与seqidno:5或6中的一者具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。在一些实施方案中,肽混合物由第一肽、第二肽和第三肽组成,其中第一肽的点突变是a146t突变,第二肽的点突变是a146v突变,并且第三肽的点突变是k117n突变,并且肽是如上所述的。在本发明的肽混合物中可以设想以上提及的seqidno的任意组合。在一些实施方案中,肽混合物包含ras蛋白的第四肽,其包含包括ras蛋白的突变的位置在内的至少8个氨基酸的区域。第四肽的突变的位置是ras蛋白的位置12、13、61、117或146,其独立于第一肽、第二肽和第三肽的突变的位置。第四肽在所述突变的位置处具有的点突变不同于第一肽、第二肽和第三肽中的每个的点突变。如以上关于第三肽讨论的,第四肽的点突变可以是从野生型氨基酸到任何其它的氨基酸。在优选的实施方案中,第四肽的点突变是k117n、a146t、a146v、g13a、g13c、g13d、g13r、g13s、g13v、g12a、g12c、g12d、g12r、g12s、g12v、q61e、q61h、q61k、q61l、q61p或q61r突变。在一些实施方案中,肽混合物包含如本文所述的第一肽、第二肽、第三肽和第四肽,其中第一肽的突变的位置是ras肽的位置146,第二肽的突变的位置是ras蛋白的位置12,第三肽的突变的位置是ras蛋白的位置13,并且第四肽的突变的位置是ras蛋白的位置61。独立于其它肽的点突变,第一肽的点突变可以是a146t或a146v突变,第二肽的点突变可以是g12a、g12c、g12d、g12r、g12s或g12v突变,第三肽的点突变可以是g13a、g13c、g13d、g13r、g13s或g13v突变,并且第四肽的点突变可以是q61e、q61h、q61k、q61l、q61p或q61r突变。第一肽在除了包括位置146的区域以外的位置处与ras蛋白具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。在一些实施方案中,第一肽在除了包括位置146的区域以外的位置处与seqidnos:1-4中的一者具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。第二肽在除了包括位置12的区域以外的位置处与ras蛋白具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。在一些实施方案中,第二肽在除了包括位置12的区域以外的位置处与seqidnos:13-18和27-32中的一者具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。第三肽在除了包括位置13的区域以外的位置处与ras蛋白具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。在一些实施方案中,第三肽在除了包括位置13的区域以外的位置处与seqidnos:7-12、25、26、33和34中的一者具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。第四肽在除了包括位置61的区域以外的位置处与ras蛋白具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。在一些实施方案中,第二肽在除了包括位置61的区域以外的位置处与seqidnos:19-24和35-38中的一者具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。在本发明的肽混合物中可以设想以上提及的seqidno的任意组合。在一些实施方案中,肽混合物包含如本文所述的第一肽、第二肽、第三肽和第四肽,其中第一肽的突变的位置是ras肽的位置146,第二肽的突变的位置是ras蛋白的位置13,第三肽的突变的位置是ras蛋白的位置13,并且第四肽的突变的位置是ras蛋白的位置61。独立于其它肽的点突变,第一肽的点突变可以是a146t或a146v突变,第二肽的点突变可以是g13a、g13c、g13d、g13r、g13s或g13v突变,第三肽的点突变可以是g13a、g13c、g13d、g13r、g13s或g13v突变,其中第二肽的点突变不同于第三肽的点突变,并且第四肽的点突变可以是q61e、q61h、q61k、q61l、q61p或q61r突变。第一肽在除了包括位置146的区域以外的位置处与ras蛋白具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。在一些实施方案中,第一肽在除了包括位置146的区域以外的位置处与seqidnos:1-4中的一者具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。第二肽在除了包括位置13的区域以外的位置处与ras蛋白具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。在一些实施方案中,第二肽在除了包括位置13的区域以外的位置处与seqidnos:7-12、25、26、33和34中的一者具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。第三肽在除了包括位置13的区域以外的位置处与ras蛋白具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。在一些实施方案中,第三肽在除了包括位置13的区域以外的位置处与seqidnos:7-12、25、26、33和34中的一者具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。第四肽在除了包括位置61的区域以外的位置处与ras蛋白具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。在一些实施方案中,第二肽在除了包括位置61的区域以外的位置处与seqidnos:19-24和35-38中的一者具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。在本发明的肽混合物中可以设想以上提及的seqidno的任意组合。在一些实施方案中,肽混合物包含如本文所述的第一肽、第二肽、第三肽和第四肽,其中第一肽的突变的位置是ras肽的位置117,第二肽的突变的位置是ras蛋白的位置12,第三肽的突变的位置是ras蛋白的位置13,并且第四肽的突变的位置是ras蛋白的位置61。独立于其它肽的点突变,第一肽的点突变可以是k117n突变,第二肽的点突变可以是g12a、g12c、g12d、g12r、g12s或g12v突变,第三肽的点突变可以是g13a、g13c、g13d、g13r、g13s或g13v突变,并且第四肽的点突变可以是q61e、q61h、q61k、q61l、q61p或q61r突变。第一肽在除了包括位置117的区域以外的位置处与ras蛋白具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。在一些实施方案中,第一肽在除了包括位置117的区域以外的位置处与seqidnos:5或6中的一者具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。第二肽在除了包括位置12的区域以外的位置处与ras蛋白具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。在一些实施方案中,第二肽在除了包括位置12的区域以外的位置处与seqidnos:13-18和27-32中的一者具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。第三肽在除了包括位置13的区域以外的位置处与ras蛋白具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。在一些实施方案中,第三肽在除了包括位置13的区域以外的位置处与seqidnos:7-12、25、26、33和34中的一者具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。第四肽在除了包括位置61的区域以外的位置处与ras蛋白具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。在一些实施方案中,第二肽在除了包括位置61的区域以外的位置处与seqidnos:19-24和35-38中的一者具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。在本发明的肽混合物中可以设想以上提及的seqidno的任意组合。在一些实施方案中,肽混合物包含如本文所述的第一肽、第二肽、第三肽、第四肽和第五肽,其中第一肽的突变的位置是ras肽的位置146,第二肽的突变的位置是ras蛋白的位置12,第三肽的突变的位置是ras蛋白的位置13,第四肽的突变的位置是ras蛋白的位置61,并且第五肽的突变的位置是ras蛋白的位置117。独立于其它肽的点突变,第一肽的点突变可以是a146t或a146v突变,第二肽的点突变可以是g12a、g12c、g12d、g12r、g12s或g12v突变,第三肽的点突变可以是g13a、g13c、g13d、g13r、g13s或g13v突变,第四肽的点突变可以是q61e、q61h、q61k、q61l、q61p或q61r突变,并且第五肽的点突变可以是k117n突变。第一肽在除了包括位置146的区域以外的位置处与ras蛋白具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。在一些实施方案中,第一肽在除了包括位置146的区域以外的位置处与seqidnos:1-4中的一者具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。第二肽在除了包括位置12的区域以外的位置处与ras蛋白具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。在一些实施方案中,第二肽在除了包括位置12的区域以外的位置处与seqidnos:13-18和27-32中的一者具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。第三肽在除了包括位置13的区域以外的位置处与ras蛋白具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。在一些实施方案中,第三肽在除了包括位置13的区域以外的位置处与seqidnos:7-12、25、26、33和34中的一者具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。第四肽在除了包括位置61的区域以外的位置处与ras蛋白具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。在一些实施方案中,第二肽在除了包括位置61的区域以外的位置处与seqidnos:19-24和35-38中的一者具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。第五肽在除了包括位置117的区域以外的位置处与ras蛋白具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。在一些实施方案中,第五肽在除了包括位置117的区域以外的位置处与seqidnos:5或6中的一者具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。在本发明的肽混合物中可以设想以上提及的seqidno的任意组合。在一些实施方案中(参见表6和7),肽混合物由具有a146t突变的肽、具有g12c突变的肽、具有g12d突变的肽、具有g12v突变的肽和具有g13d突变的肽组成。在所述实施方案中,肽混合物由这样的肽组成:所述肽独立地在不同于包括突变的位置的区域的位置处分别与seqidno:1或2以及seqidnos:9、14、15和18具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。在一些实施方案中,肽混合物由这样的肽组成:所述肽独立地在不同于包括突变的位置的区域的位置处与seqidno:1或2以及seqidnos:26、28、29和32具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。表6和表7显示了在这些实施方案中优选存在的肽。在一些实施方案中(参见表8和9),肽混合物由具有a146t突变的肽、具有q61r突变的肽、具有q61k突变的肽、具有q61h突变的肽和具有q61l突变的肽组成。在所述实施方案中,肽混合物由这样的肽组成:所述肽独立地在不同于包括突变的位置的区域的位置处分别与seqidno:1或2以及seqidnos:19、20、21和22具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。在一些实施方案中,肽混合物由这样的肽组成:所述肽独立地在不同于包括突变的位置的区域的位置处与seqidno:1或2以及seqidnos:35、36、37和38具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。表8和表9显示了在这些实施方案中优选存在的肽。在一些实施方案中,除在位置117处具有点突变的肽和/或在ras肽的位置146处具有点突变的肽,肽混合物还包含分别与seqidnos:25-32具有100%序列同一性的具有g13c突变的肽、具有g13d突变的肽、具有g12a突变的肽、具有g12c突变的肽、具有g12d突变的肽、具有g12r突变的肽、具有g12s突变的肽和具有g12v突变的肽,并且在ras肽的位置12或13处具有突变的肽的这种具体组合在本文中称为tg02。图3显示了在tg02中优选存在的肽。这些突变在与ras突变相关的癌症(肺癌和结直肠癌)中的发生率分别在图2、4和5中显示。用tg02接种小鼠后的脾细胞增殖测定的结果在图9中显示,并且其显示tg02对诱导免疫应答有效。在一些实施方案中,除在位置117处具有点突变的肽和/或在ras肽的位置146处具有点突变的肽,肽混合物还包含具有g13r突变的肽、具有g13v突变的肽、具有q61r突变的肽、具有q61k突变的肽、具有q61h突变的肽和具有q61l突变的肽,其中这些肽分别与seqidnos:33-38具有100%序列同一性,并且在ras肽的位置13或61处具有突变的肽的这种具体组合在本文中称为tg03。图3显示了tg03的肽。这些突变在恶性黑素瘤中的发生率在图6中显示。在一些实施方案中(参见表10和11;在本文中称为tg02+a146t),肽混合物由具有a146t突变的肽、具有g13c突变的肽、具有g13d突变的肽、具有g12a突变的肽、具有g12c突变的肽、具有g12d突变的肽、具有g12r突变的肽、具有g12s突变的肽和具有g12v突变的肽组成。在所述实施方案中,肽混合物由这样的肽组成:所述肽独立地在不同于包括突变的位置的区域的位置处分别与seqidno:1(krasa146t肽)或seqidno:2(nrasa146t肽)以及seqidnos:7、9和13-18具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。在一些实施方案中,肽混合物由这样的肽组成:所述肽独立地在不同于包括突变的位置的区域的位置处与seqidno:1(krasa146t肽)或seqidno:2(nrasa146t肽)以及seqidnos:25-32具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。表10和表11显示了在该实施方案中优选存在的肽。在一些实施方案中(参见表12和13;tg02+a146v),肽混合物由具有a146v突变的肽、具有g13c突变的肽、具有g13d突变的肽、具有g12a突变的肽、具有g12c突变的肽、具有g12d突变的肽、具有g12r突变的肽、具有g12s突变的肽和具有g12v突变的肽组成。在所述实施方案中,肽混合物由这样的肽组成:所述肽独立地在不同于包括突变的位置的区域的位置处分别与seqidno:3(krasa146v肽)或seqidno:4(nrasa146v肽)以及seqidnos:7、9和13-18具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。在一些实施方案中,肽混合物由这样的肽组成:所述肽独立地在不同于包括突变的位置的区域的位置处与seqidno:3或4以及seqidnos:25-32具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。表12和表13显示了在该实施方案中优选存在的肽。在一些实施方案中(表14和15;tg03+a146t),肽混合物由具有a146t突变的肽、具有g13r突变的肽、具有g13v突变的肽、具有q61r突变的肽、具有q61k突变的肽、具有q61h突变的肽和具有q61l突变的肽组成。在所述实施方案中,肽混合物由这样的肽组成:所述肽独立地在不同于包括突变的位置的区域的位置处分别与seqidno:1(krasa146t肽)或seqidno:2(nrasa146t肽)以及seqidnos:8、10和19-22具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。在一些实施方案中,肽混合物由这样的肽组成:所述肽独立地在不同于包括突变的位置的区域的位置处与seqidno:1(krasa146t肽)或seqidno:2(nrasa146t肽)以及seqidnos:33-38具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。表14和表15显示了在该实施方案中优选存在的肽。在一些实施方案中(参见表16和17;tg03+a146v),肽混合物由具有a146v突变的肽、具有g13r突变的肽、具有g13v突变的肽、具有q61r突变的肽、具有q61k突变的肽、具有q61h突变的肽和具有q61l突变的肽组成。在所述实施方案中,肽混合物由这样的肽组成:所述肽独立地在不同于包括突变的位置的区域的位置处分别与seqidno:3(krasa146v肽)或seqidno:4(nrasa146v肽)以及seqidnos:8、10和19-22具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。在一些实施方案中,肽混合物由这样的肽组成:所述肽独立地在不同于包括突变的位置的区域的位置处与seqidno:3(krasa146v肽)或seqidno:4(nrasa146v肽)以及seqidnos:33-38具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。表16和表17显示了在该实施方案中优选存在的肽。在一些实施方案中(参见表18和19;tg02+k117n),肽混合物由具有k117n突变的肽、具有g13c突变的肽、具有g13d突变的肽、具有g12a突变的肽、具有g12c突变的肽、具有g12d突变的肽、具有g12r突变的肽、具有g12s突变的肽和具有g12v突变的肽组成。在所述实施方案中,肽混合物由这样的肽组成:所述肽独立地在不同于包括突变的位置的区域的位置处分别与seqidno:5(krask117n肽)或seqidno:6(nrask117n肽)以及seqidnos:7、9和13-18具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。在一些实施方案中,肽混合物由这样的肽组成:所述肽独立地在不同于包括突变的位置的区域的位置处与seqidno:5(krask117n肽)或seqidno:6(nrask117n肽)以及seqidnos:25-32具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。表18和表19显示了在该实施方案中优选存在的肽。在一些实施方案中(参见表20和21;tg03+k117n),肽混合物由具有k117n突变的肽、具有g13r突变的肽、具有g13v突变的肽、具有q61r突变的肽、具有q61k突变的肽、具有q61h突变的肽和具有q61l突变的肽组成。在所述实施方案中,肽混合物由这样的肽组成:所述肽独立地在不同于包括突变的位置的区域的位置处分别与seqidno:5(krask117n肽)或seqidno:6(nrask117n肽)以及seqidnos:8、10和19-22具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。在一些实施方案中,肽混合物由这样的肽组成:所述肽独立地在不同于包括突变的位置的区域的位置处与seqidno:5(krask117n肽)或seqidno:6(nrask117n肽)以及seqidnos:33-38具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。表20和表21显示了在该实施方案中优选存在的肽。在一些实施方案中(参见表22和23;tgx3),肽混合物由具有a146t突变的肽、具有g13c突变的肽、具有g13d突变的肽和具有q61r突变的肽组成。在所述实施方案中,肽混合物由这样的肽组成:所述肽独立地在不同于包括突变的位置的区域的位置处分别与seqidno:1(krasa146t肽)或seqidno:2(nrasa146t肽)以及seqidnos:7、9和19具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。在一些实施方案中,肽混合物由这样的肽组成:所述肽独立地在不同于包括突变的位置的区域的位置处与seqidno:1(krasa146t肽)或seqidno:2(nrasa146t肽)以及seqidnos:25、26和35具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。在一些实施方案中,g13c、g13d和q61r肽分别与seqidnos:25、26和35具有100%序列同一性,并且a146t肽与seqidno:1具有100%序列同一性,并且肽的这种具体组合在本文中称为tgx3。表22显示了存在于tgx3中的肽,并且图12显示了该肽混合物在诱导对于肽混合物以及tgx3中各个肽中的每个的t细胞应答中有效。表23显示了在tgx3的备选形式中优选存在的肽,其中具有a146t突变的肽与seqidno:2具有100%序列同一性。在其它实施方案中,肽混合物由具有a146t、a146v或k117n突变的肽、具有g13c突变的肽、具有g13d突变的肽、具有g13r突变的肽、具有g12a突变的肽、具有g12c突变的肽、具有g12d突变的肽、具有g12r突变的肽、具有g12s突变的肽和具有g12v突变的肽组成。在所述实施方案中,肽混合物由这样的肽组成:所述肽独立地在除了包括位置117、146、12或13的区域以外的位置处分别与seqidnos:1-9和13-18具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。在一些实施方案中,肽混合物由这样的肽组成:所述肽独立地在除了包括位置117、146、12或13的区域以外的位置处分别与seqidnos:1-6和25-33具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。利用由seqidnos:25-33代表的肽组成的肽混合物体外刺激pmbc后的t细胞增殖测定的结果在图8中显示,并且显示t细胞被该混合物刺激。因此,ras肽混合物对诱导免疫应答有效。在一些实施方案中,肽混合物由如本文所述的第一肽、第二肽、第三肽、第四肽和第五肽组成,其中第一肽的突变的位置是ras蛋白的位置117或146。第二肽、第三肽、第四肽和第五肽中的每个的突变的位置是ras蛋白的位置13,并且第二肽、第三肽、第四肽和第五肽中的每个独立地在除了包括位置13的区域以外的位置处与ras蛋白具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。第二肽、第三肽、第四肽和第五肽中的每个可以独立地在除了包括位置13的区域以外的位置处与seqidnos:7-12、25、26、33和34中的一者具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。第二肽、第三肽、第四肽和第五肽中的每个在对应于ras肽的位置13的氨基酸处具有点突变,并且第二肽、第三肽、第四肽和第五肽中的每个具有的点突变彼此不同。在一个实施方案中,第一肽是具有a146t、a146v或k117n突变的肽,第二肽是具有g13r突变的肽,第三肽是具有g13a突变的肽,第四肽是具有g13s突变的肽,并且第五肽是具有g13v突变的肽。备选的实施方案包括包含ras蛋白的至少六种肽的肽混合物,其中所述六种肽中的每个包含对应于ras蛋白的片段的区域,其中所述区域包含包括突变的位置在内的至少8个氨基酸,如本文所述,并且其中至少六种肽中的一者的突变的位置是ras蛋白的位置117或146。所述至少六种肽中的每个独立地在不同于包括突变的位置的区域的位置处与ras蛋白具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。在一些实施方案中,肽混合物包含第一肽、第二肽、第三肽、第四肽、第五肽和第六肽,其中第一肽的突变的位置是ras肽的位置117或146,并且第二肽、第三肽、第四肽、第五肽和第六肽中的每个的突变的位置是ras蛋白的位置13。第一肽在不同于包括突变的位置的区域的位置处与seqidnos:1-6中的一者具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性,并且第二肽、第三肽、第四肽、第五肽和第六肽中的每个独立地在除了包括位置13的区域以外的位置处与seqidnos:7-12、25、26、33和34中的一者具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。第一肽具有选自a146t、a146v和k117n突变的点突变,并且第二肽、第三肽、第四肽、第五肽和第六肽中的每个在对应于ras蛋白的位置13的氨基酸处具有点突变,其独立地选自g13a、g13c、g13d、g13r、g13s或g13v突变,并且第二肽、第三肽、第四肽、第五肽和第六肽中的每个的点突变彼此不同。在一些实施方案中,第一肽具有a146t突变,在一些实施方案中,第一肽具有a146v突变。在其它实施方案中,第一肽具有k117n突变。在另一个实施方案中,适于引发免疫应答的肽混合物由ras蛋白的七种肽组成,其中每种肽包含对应于ras蛋白的片段的区域,其中所述区域包含包括突变的位置在内的至少8个氨基酸,其中第一肽的突变的位置是ras蛋白的位置117或146,并且第二肽至第七肽中的每个的突变的位置是ras蛋白的位置12。第一肽在不同于包括突变的位置的区域的位置处与ras蛋白具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性,和/或在不同于包括突变的位置的区域的位置处与seqidnos:1-6中的一者具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。第二肽至第七肽中的每个独立地在除了包括位置12的区域以外的位置处与ras蛋白具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性,和/或独立地在除了包括位置12的区域以外的位置处与seqidnos:13-18和27-32中的一者具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。第二肽至第七肽中的每个在对应于ras蛋白的位置12的氨基酸处具有点突变,其选自g12a、g12c、g12d、g12r、g12s或g12v突变,并且每种肽的点突变彼此不同。在另一个实施方案中,适于引发免疫应答的肽混合物由ras蛋白的七种肽组成,其中每种肽包含对应于ras蛋白的片段的区域,其中所述区域包含包括突变的位置在内的至少8个氨基酸,其中第一肽的突变的位置是ras蛋白的位置117或146,并且第二肽至第七肽中的每个的突变的位置是ras蛋白的位置61。第一肽在不同于包括突变的位置的区域的位置处与ras蛋白具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性,和/或在不同于包括突变的位置的区域的位置处与seqidnos:1-6中的一者具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。第二肽至第七肽中的每个独立地在除了包括位置61的区域以外的位置处与ras蛋白具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性,和/或独立地在除了包括位置61的区域以外的位置处与seqidnos:19-24和35-38中的一者具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。第二肽至第七肽中的每个在对应于ras蛋白的位置61的氨基酸处具有点突变,其选自q61e、61h、q61k、q61l、q61p或q61r突变,并且每种肽的点突变彼此不同。在进一步的实施方案中,适于引发免疫应答的肽混合物由ras蛋白的第一肽、第二肽、第三肽、第四肽和第五肽组成,其中每种肽包含对应于ras蛋白的片段的区域,其中所述区域包含包括突变的位置在内的至少8个氨基酸。第一肽的突变的位置是ras蛋白的位置117或146,第二肽、第三肽和第四肽的突变的位置是ras蛋白的位置12,并且第五肽的突变的位置是ras蛋白的位置13。第一肽在不同于包括突变的位置的区域的位置处与ras蛋白具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性,和/或在不同于包括突变的位置的区域的位置处与seqidnos:1-6中的一者具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。第二肽、第三肽、第四肽和第五肽中的每个在除了包括位置12或13的区域以外的位置处分别与ras蛋白具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性,和/或独立地在除了包括位置12或13的区域以外的位置处分别与seqidnos:7-18和25-34中的一者具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%序列同一性。第二肽、第三肽、第四肽和第五肽中的每个分别在对应于ras蛋白的所述位置12或13的氨基酸处具有点突变。在一个实施方案中,第二肽是具有g12a突变的肽,第三肽是具有g12r突变的肽,第四肽是具有g12s突变的肽,并且第五肽是具有g13c突变的肽。通常,本发明的肽,在包括位置12、13、61、117或146的8个氨基酸的区域内,分别具有不同于在位置12、13、61、117或146处的残基至少6个氨基酸残基,所述至少6个氨基酸残基与ras蛋白的相应区域相同。此外,通常,本发明的肽,在除了包括ras蛋白的位置12、13、61、117或146的区域之外的位置处独立地分别与seqidnos:1-38中的一者具有至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少66%、至少75%、至少85%、至少95%、至少99%或100%的序列同一性。在一些实施方案中,在肽混合物中存在最多12种不同的肽。在其它实施方案中,存在最多8、10、12、14或16种不同的肽。在肽混合物包含至少一种另外的肽(其包含包括ras蛋白的突变的位置的区域)的实施方案中,肽混合物包含1、2、3、4、5或6种肽,所述肽包含包括ras肽的突变的位置的至少8个氨基酸的区域并且在突变的位置处具有点突变。每种肽的突变的位置独立地是位置117、146、12、13或61,并且每种肽在突变的位置处具有不同于其它肽的点突变。在肽混合物包含至少一种另外的肽(其包含包括ras蛋白的位置12的区域)的实施方案中,肽混合物包含1、2、3、4、5或6种肽,所述肽包含包括ras肽的位置12的至少8个氨基酸的区域并且在对应于ras蛋白的位置12的位置处具有点突变。在肽混合物包含至少一种另外的肽(其包含包括ras蛋白的位置61的至少8个氨基酸的区域)的实施方案中,肽混合物包含1、2、3、4、5或6种肽,所述肽包含包括ras蛋白的位置61的区域并且在对应于ras蛋白的位置61的氨基酸处具有点突变,其中每种肽具有不同的点突变。在肽混合物包含至少一种另外的肽(其包含包括ras蛋白的位置13的至少8个氨基酸的区域)的实施方案中,肽混合物包含1、2、3、4、5或6种肽,所述肽包含包括ras蛋白的位置13的区域并且在对应于ras蛋白的位置13的氨基酸处具有点突变,其中每种肽具有不同的点突变。在一些实施方案中,包含包括ras肽的位置117的至少8个氨基酸的区域的肽包含ras蛋白的位置107至127。在备选实施方案中,包含包括ras蛋白的位置117的至少8个氨基酸的区域的肽包含ras蛋白的位置108至126,而在其它实施方案中,所述肽包含ras蛋白的位置109至125。在进一步的实施方案中,对应于ras蛋白的位置117的氨基酸在肽的c-末端。在进一步的实施方案中,对应于ras蛋白的位置117的氨基酸在肽的n-末端。通常,具有包括ras蛋白的位置117的至少8个氨基酸的区域可以由ras蛋白的包括位置117的任意8个位置组成。例如,具有包括位置117的至少8个氨基酸的区域可以由ras蛋白的位置110至位置117、位置111至位置118、位置112至位置119、位置113至位置120、位置114至位置121、位置115至位置122、位置116至位置123或位置117至位置124的氨基酸组成。在一些实施方案中,对应于ras蛋白的位置117的氨基酸在肽的中间。在一些实施方案中,包含包括ras肽的位置146的至少8个氨基酸的区域的肽包含ras蛋白的位置136至156。在备选实施方案中,包含包括ras蛋白的位置146的至少8个氨基酸的区域的肽包含ras蛋白的位置137至155,而在其它实施方案中,所述肽包含ras蛋白的位置138至154。在进一步的实施方案中,对应于ras蛋白的位置146的氨基酸在肽的c-末端。在进一步的实施方案中,对应于ras蛋白的位置146的氨基酸在肽的n-末端。通常,具有包括ras蛋白的位置146的至少8个氨基酸的区域可以由ras蛋白的包括位置146的任意8个位置组成。例如,具有包括位置146的至少8个氨基酸的区域可以由ras蛋白的位置139至位置146、位置140至位置147、位置141至位置148、位置142至位置149、位置143至位置150、位置144至位置151、位置145至位置152或位置146至位置153的氨基酸组成。在一些实施方案中,对应于ras蛋白的位置146的氨基酸在肽的中间。在肽混合物的一些实施方案中,包含包括ras肽的位置12的至少8个氨基酸的区域的肽包含ras蛋白的位置1至30。在其它实施方案中,包含包括ras蛋白的位置12的至少8个氨基酸的区域的肽包含ras蛋白的位置5至21。在备选的实施方案中,对应于ras蛋白的位置12的氨基酸在肽的c-末端。在进一步的实施方案中,对应于ras蛋白的位置12的氨基酸在肽的n-末端。通常,具有包括ras蛋白的位置12的至少8个氨基酸的区域可以由ras蛋白的包括位置12的任意8个位置组成。例如,具有包括位置12的至少8个氨基酸的区域可以由ras蛋白的位置5至位置12、位置6至位置13、位置7至位置14、位置8至位置15、位置9至位置16、位置10至位置17、位置11至位置18或位置12至位置19的氨基酸组成。在肽混合物的一些实施方案中,包含包括ras肽的位置13的至少8个氨基酸的区域的肽包含ras蛋白的位置1至30。在备选的实施方案中,包含包括ras蛋白的位置13的至少8个氨基酸的区域的肽包含ras蛋白的位置5至21。在进一步的实施方案中,对应于ras蛋白的位置13的氨基酸在肽的c-末端。在进一步的实施方案中,对应于ras蛋白的位置13的氨基酸在肽的n-末端。通常,具有包括ras蛋白的位置13的至少8个氨基酸的区域可以由ras蛋白的包括位置13的任意8个位置组成。例如,具有包括位置13的至少8个氨基酸的区域可以由ras蛋白的位置6至位置13、位置7至位置14、位置8至位置15、位置9至位置16、位置10至位置17、位置11至位置18、位置12至位置19或位置13至位置20的氨基酸组成。在肽混合物的一些实施方案中,包含包括ras肽的位置61的至少8个氨基酸的区域的肽包含ras蛋白的位置47至76。在其它实施方案中,包含包括ras肽的位置61的至少8个氨基酸的区域的肽包含ras蛋白的位置53至69。在备选的实施方案中,对应于ras蛋白的位置61的氨基酸在肽的c-末端。在进一步的实施方案中,对应于ras蛋白的位置61的氨基酸在肽的n-末端。通常,具有包括ras蛋白的位置61的至少8个氨基酸的区域可以由ras蛋白的包括位置13的任意8个位置组成。例如,具有包括位置61的至少8个氨基酸的区域可以由ras蛋白的位置54至位置61、位置55至位置62、位置56至位置63、位置57至位置64、位置58至位置65、位置59至位置66、位置60至位置67或位置61至位置68的氨基酸组成。本发明的肽混合物可以以相等或不同的比例包含所述肽。在一些实施方案中,第一肽和第二肽以肽绝对数的相等比例存在于混合物中,即各种肽构成肽混合物的肽组分中肽总数的50%。在其它实施方案中,与第二肽相比,在肽混合物中存在肽绝对数的更大比例的第一肽。例如,第一肽可以构成肽混合物的肽组分中肽总数的至少55%、至少60%、至少70%、至少80%或至少90%。在备选的实施方案中,与第一肽相比,在肽混合物中存在更大比例的第二肽。例如,第二肽可以构成肽混合物的肽组分的至少55%、至少60%、至少70%、至少80%或至少90%。在包含至少一种另外的肽的实施方案中,肽以相等比例存在于肽混合物的肽组分中。在其它实施方案中,第一肽、第二肽和至少一种另外的肽以彼此不同的比例存在。例如,第一肽、第二肽和至少一种另外的肽中的每个可以独立地构成肽混合物的肽组分的至少1%、至少5%、至少10%、至少20%至少30%、至少40%、至少50%、至少60%、至少60%、至少70%、至少80%或至少90%。在进一步的实施方案中,上述肽用作疫苗或药物。所述肽对应于ras蛋白的片段并且包含ras蛋白的包括突变的位置在内的至少8个氨基酸的区域,并且所述突变的位置是ras蛋白的位置117或146。所述至少8个氨基酸的区域具有不在所述突变的位置处的与ras蛋白的相应区域相同的至少6个氨基酸残基。用作疫苗或药物的肽在突变的位置处具有点突变,其中所述突变的位置是ras蛋白的位置117或146。在一些实施方案中,肽的点突变是k117n、a146t或a146v突变中的一者。如上讨论的,现在已经发现在位置117或146处具有点突变的ras蛋白的肽,并且特别是k117n、a146t和a146v肽,是免疫原性的并且诱导t细胞增殖。特别地,图11显示了在ras蛋白的位置146处具有突变的肽(更特别的是a146t肽)刺激t细胞的诱导。此外,图12显示了即使当肽混合物含有来源于野生型ras蛋白的不同区域的肽,也获得了对于肽混合物的免疫原性应答。因此,图12显示了混合物的肽并不竞争结合负责呈递至相关t细胞的hla分子,此种免疫显性对于本发明的肽混合物不是重要的问题。本发明的肽是对应于由mhcii分子展示在细胞表面上的ras蛋白片段的肽。因此,本发明的肽是这样的肽,其对应于由ras蛋白的细胞内蛋白水解分解产生的蛋白片段,所述片段之后可以被展示在hla分子上,并且对于所述片段,个体通常在其t细胞库中具有反应性t细胞。在本发明的另一个方面,提供t细胞和包含t细胞的t细胞制剂,所述t细胞对呈递在mhc分子上的如上所述的本发明的肽具有特异性,其中所述肽包含ras蛋白的位置117或146处的突变的位置。在本发明的另外的方面,提供t细胞混合物,所述t细胞混合物包含对本发明的肽混合物之一中的每种肽具有特异性的t细胞。所述t细胞、t细胞制剂或t细胞混合物可以通过用ras蛋白的肽或者包含ras蛋白的至少第一肽和第二肽的肽混合物刺激至少一种反应性t细胞来制备。例如,在一个实施方案中,t细胞或t细胞制剂对对应于ras蛋白的片段的肽具有特异性,其中所述肽包含包括突变的位置在内的至少8个氨基酸的区域,所述突变的位置是ras蛋白的位置117或146,其中t细胞对肽的突变的位置处的点突变具有特异性。例如,在另一个实施方案中,t细胞制剂包含对对应于ras蛋白的片段的肽具有特异性的多个t细胞,其中所述肽包含包括突变的位置在内的至少8个氨基酸的区域,所述突变的位置是ras蛋白的位置117或146,并且其中t细胞制剂中的每种t细胞对肽的突变的位置处的点突变具有特异性。例如,在另一个实施方案中,t细胞混合物包含多个t细胞,其中第一t细胞和第二t细胞分别对对应于ras蛋白的片段的第一肽和第二肽具有特异性,其中每种肽包含包括突变的位置在内的至少8个氨基酸的区域,其中第一肽的突变的位置是ras蛋白的位置117或146,并且第二肽的突变的位置是ras蛋白的位置12、13、61、117或146,并且其中第一t细胞和第二t细胞对对应于所述突变的位置的氨基酸处的点突变具有特异性,并且第一t细胞对其具有特异性的点突变不同于第二t细胞对其具有特异性的点突变。在本发明的另外的方面,提供这样的t细胞受体或其抗原结合片段,其对呈递在mhc分子上的本发明的肽或本发明的肽混合物的肽具有特异性。还提供了对ras蛋白的肽具有特异性的t细胞受体或其抗原结合片段,其中所述肽包含对应于ras蛋白的片段的区域,其中所述区域包含包括突变的位置在内的至少8个氨基酸,所述区域包含除了突变的位置以外的与ras蛋白的相应区域相同的至少6个氨基酸,其中所述突变的位置具有点突变,并且所述突变的位置是ras蛋白的位置12、13或61。t细胞受体的抗原结合片段可以包含在合适的框架区中的t细胞受体的完整可变区或其互补决定区。在本发明的另一个方面,提供了包含如上所述的至少第一t细胞受体和第二t细胞受体或其抗原结合片段的t细胞受体混合物。还提供了对ras蛋白的肽具有特异性的至少第一t细胞受体和第二t细胞受体或其抗原结合片段,其中所述肽包含对应于ras蛋白的片段的区域,其中所述区域包含包括突变的位置在内的至少8个氨基酸,所述区域包含除了突变的位置以外的与ras蛋白的相应区域相同的至少6个氨基酸,其中所述突变的位置具有点突变,并且每种肽的突变的位置独立地是ras蛋白的位置117、146、12、13或61,并且其中第一t细胞受体和第二t细胞受体中的每个或其抗原结合片段对具有不同的点突变的肽具有特异性。在一些实施方案中,t细胞受体混合物包含对任一种上述肽混合物中的每种肽具有特异性的t细胞受体或其抗原结合片段。在本发明的另一个方面,提供编码t细胞受体的mrna,所述t细胞受体对呈递在mhc分子上的本发明的肽或本发明的肽混合物的肽具有特异性。在一些实施方案中,mrna用于转染宿主细胞以在宿主细胞上展示编码的t细胞受体。在本发明的另一个方面,提供包含这样的序列的核酸,所述序列编码本发明的肽或本发明的肽混合物的肽。还提供了核酸的混合物,混合物的每种核酸包含编码本发明的肽混合物的不同肽的序列,从而核酸的混合物编码本发明的肽混合物。在一些实施方案中,核酸及其混合物用于合成本发明的肽或肽混合物。例如,本发明的肽可以通过将核酸施用至受试者来合成,由此核酸由受试者表达,因此原位地给出了本发明的肽。然后,产生的肽刺激受试者中的免疫应答。在另一个实例中,核酸可以用于通过用本发明的核酸转化或转染宿主细胞来合成本发明的肽,从而宿主细胞表达核酸以产生随后被回收并纯化的本发明的肽。在一些实施方案中,本发明的肽使用本领域中熟知的方法通过化学合成产生。在本发明的另一个方面,提供载体,所述载体包含包含这样的序列的核酸,所述序列编码本发明的肽或t细胞受体。在另外的方面,提供包含如上所述的载体的宿主细胞。所述宿主细胞被载体转染或转化,从而宿主细胞表达由载体编码的核酸。肽、肽混合物、t细胞、t细胞制剂、t细胞混合物、t细胞受体或其抗原结合片段、核酸、载体和宿主细胞被用于治疗和/或预防癌症,并且特别是与ras癌基因中的突变相关的癌症。癌症可以包括肾上腺癌、自主神经节癌、胆管癌、骨癌、乳腺癌、中枢神经系统癌、宫颈癌、结直肠癌、子宫内膜癌、造血器官(haematopoietic)癌、淋巴癌、肾癌、大肠癌、肝癌、肺癌、食管癌、卵巢癌、胰腺癌、前列腺癌、唾液腺癌、皮肤癌、小肠癌、胃癌、睾丸癌、胸腺癌、甲状腺癌、上呼吸消化道癌和尿道癌和恶性黑素瘤,并且本发明的肽混合物、肽、t细胞混合物、t细胞制剂、核酸、载体和宿主细胞可以用于预防和/或治疗这些类型的癌症中的多于一种。在一些实施方案中,本发明的肽(其中肽具有a146t、a146v或k117n突变)、本发明的肽混合物(其中第一肽具有a146t、a146v或k117n突变)、本发明的t细胞(其中t细胞对具有a146t、a146v或k117n突变的肽具有特异性)、本发明的t细胞制剂(其中t细胞对具有a146t、a146v或k117n突变的肽具有特异性)、本发明的t细胞混合物(其中第一t细胞对具有a146t、a146v或k117n突变的肽具有特异性)、本发明的t细胞受体或其抗原结合片段(其对具有a146t、a146v或k117n突变的肽具有特异性)、本发明的核酸(其包含编码具有a146t、a146v或k117n突变的肽或者对具有a146t、a146v或k117n突变的肽具有特异性的t细胞受体或其抗原结合片段的序列)、本发明的载体(其包含核酸,所述核酸编码具有a146t、a146v或k117n突变的肽或者对具有a146t、a146v或k117n突变的肽具有特异性的t细胞受体或其抗原结合片段)或本发明的宿主细胞(其包含载体,所述载体包含核酸,所述核酸编码具有a146t、a146v或k117n突变的肽或者对具有a146t、a146v或k117n突变的肽具有特异性的t细胞受体或其抗原结合片段)用于预防和/或治疗癌症。所述t细胞受体或其抗原结合片段可用于工程改造转基因t细胞、例如嵌合抗原受体t细胞(cart)。所述cart可以用于个人化的癌症疗法,例如通过静脉输注。在这样的实施方案中,优选的是,所述癌症是结直肠癌、肺癌和胰腺癌中的一种或多种。在一些实施方案中,所述癌症是结直肠癌。特别地,已经发现,当选自本发明的肽或肽混合物时,可以治疗99%的与ras蛋白中突变相关的癌症。更特别地,已经发现,包含具有a146t突变的肽、具有g13r突变的肽、具有g13v突变的肽、具有q61r突变的肽、具有q61k突变的肽、具有q61h突变的肽和具有q61l突变的肽的肽混合物可以用于治疗全部结直肠癌中的10%,无论他们是否与ras中的突变相关。此外,已经发现,可以用上述肽混合物或者用包含具有g13c突变的肽、具有g13d突变的肽、具有g12a突变的肽、具有g12c突变的肽、具有g12d突变的肽、具有g12r突变的肽、具有g12s突变的肽和具有g12v突变的肽的肽混合物(例如,tg02)来治疗全部结直肠癌中的至少50%。因此,本发明的肽和肽混合物提供用于增加的数量的结直肠癌患者的疫苗和/或治疗。还提供包含如上所述的肽、肽混合物、t细胞、t细胞混合物、t细胞制剂或核酸的药物组合物。所述药物组合物还可以包含至少一种药用载体、稀释剂和/或赋形剂。在一些实施方案中,所述药物组合物还包含一种或多种另外的活性成分和/或佐剂。在某些实施方案中,所述药物组合物可以还包含一种或多种对相同的疾病适应症具有治疗有效性的成分。在一个实施方案中,本发明的药物组合物可以还包含一种或多种另外的化疗剂、一种或多种抗体、一种或多种小分子和/或一种或多种免疫刺激剂(例如,细胞因子)。在一些实施方案中,所述肽、肽混合物、t细胞、t细胞制剂、t细胞混合物、核酸或药物组合物可以与其他形式的免疫疗法联合使用。已经发现某些类型的癌症与ras蛋白的某些突变相关,并且近来已经发现a146t、a146v和k117n突变与癌症相关,并且如图1所示特别是与结直肠癌相关。因此,有可能使肽、肽混合物、t细胞、t细胞制剂、t细胞混合物和t细胞受体或其抗原结合片段、核酸、载体和宿主细胞适于靶向某些类型的癌症。本发明的肽、肽混合物或药物组合物可以通过本领域技术人员已知的任何合适的递送技术施用至受试者。例如,其它技术中,肽混合物、肽或药物组合物可以以溶液的形式、以脂质体的形式或以干燥的形式(例如,以包衣颗粒的形式等)通过注射施用至受试者。在一些实施方案中,所述肽或肽混合物与免疫刺激剂(诸如gm-csf)施用。在使用gm-csf的实施方案中,这可以是任何gm-csf。在一些实施方案中,肽混合物、肽或药物组合物可以以例如1μg至1g的每种肽的量,每三天一次、每周一次、每月一次、每三个月一次、每四个月一次或每六个月一次施用。本发明的t细胞、t细胞混合物和t细胞制剂可以通过静脉内注射和/或输注施用,并且可以以例如106至1012个的对肽混合物的肽或肽具有特异性的各种t细胞的量,每月一次、每两个月一次、每三个月一次、每六个月一次或每年一次的量施用。优选地,所述剂量每月一次地施用2至5个月,并且随后以较低的频率施用。本发明的核酸和核酸的混合物可以通过肌肉内注射和/或皮下注射施用。将本发明的肽或肽混合物施用至受试者刺激了对肽或肽混合物的免疫应答,特别是t细胞介导的免疫应答。肽或者肽混合物中的每种肽由抗原呈递细胞(apc)加工并在mhc分子上呈递。t细胞通过t细胞受体结合由apc呈递于mhc分子上的肽而激活,因此导致针对肿瘤细胞的免疫应答,所述肿瘤细胞具有这样的突变,其对应于在施用的肽中存在的突变。将本发明的t细胞或t细胞混合物施用至患有与相应ras突变相关的癌症的受试者刺激了经由施用的t细胞针对肿瘤细胞的免疫应答。特别地,并且如上提及的,t细胞识别来源于细胞内蛋白质的肽,从而施用的t细胞可以当通过mhc分子在肿瘤细胞的表面上展现时识别肿瘤细胞的突变的ras蛋白。如上所提及的,不同类型的癌症与ras蛋白的不同突变相关的发现意味着疫苗和治疗可以靶向具体癌症。因此,在本发明的另一个方面,提供用于包括癌症的诊断和合适治疗的选择的方法的肽、肽混合物、t细胞、t细胞混合物、t细胞制剂、核酸和/或载体。所述方法包括以下步骤:a)鉴定存在于取自患者的样品中的ras蛋白点突变,和b)选择如上所述的肽,选择包含肽的如上所述的肽混合物,选择如上所述的t细胞,选择包含对肽具有特异性的t细胞的如上所述的t细胞混合物,选择包含对肽具有特异性的t细胞的如上所述的t细胞制剂,选择包含编码肽的序列的如上所述的核酸,和/或选择编码核酸(所述核酸包含编码肽的序列)的如上所述的载体,所述肽包含对应于样品中鉴定的至少一种ras蛋白点突变的点突变。例如,如果发现取自受试者的样品含有具有a146t突变的ras蛋白,则将选择肽,包含肽的肽混合物,包含对肽具有特异性的t细胞的t细胞、t细胞混合物和/或制剂,包含编码肽的序列的核酸,和/或编码核酸(所述核酸包含编码肽的序列)的载体,所述肽包含a146t突变。在样品含有例如包含a146t突变和g13c突变的ras蛋白的情况中,选择含有包含a146t突变的肽和包含g13c突变的肽的肽混合物,包含对包含a146t的肽具有特异性的t细胞和对包含g13c突变的肽具有特异性的t细胞的t细胞混合物,包含编码具有a146t突变的肽的序列的核酸和包含编码具有g13c突变的肽的序列的核酸,和/或编码包含编码具有a146t突变的肽的序列的核酸的载体和编码包含编码具有g13c突变的肽的序列的核酸的载体。所述方法还可以包括将包含所选的肽混合物、肽、t细胞、t细胞混合物、t细胞制剂、核酸和/或载体的药物组合物施用至患者的步骤。因此,在一些实施方案中,所述方法包括施用表6-23中所示和本文中称为tg02和tg03的肽混合物中的一者的步骤。在其它实施方案中,所述方法包括以下步骤:施用包含对表6-23、tg02和tg03中的一者的肽混合物具有特异性的t细胞的t细胞混合物、编码表6-23、tg02和tg03中的一者的肽混合物的核酸,和/或编码包含编码表6-23、tg02和tg03中的一者的肽混合物的序列的核酸的载体。在特别优选的实施方案中,肽混合物是tg02、tg03、表14的混合物和表15的混合物中的一者。在本发明的另外的方面,提供试剂盒,所述试剂盒包含如本文所述的肽、肽混合物、t细胞、t细胞混合物、t细胞制剂、核酸、核酸混合物、t细胞受体、t细胞受体混合物、载体、宿主细胞和/或mrna。所述肽、肽混合物、t细胞、t细胞混合物、t细胞制剂、核酸、核酸混合物、t细胞受体、t细胞受体混合物载体、宿主细胞和/或mrna可以原样地存在于试剂盒中,或所述肽、肽混合物、t细胞、t细胞混合物、t细胞制剂、核酸、核酸混合物、t细胞受体、t细胞受体混合物、载体、宿主细胞和/或mrna可以作为药物制剂存在于试剂盒中。在一些实施方案中,所述肽、肽混合物、t细胞、t细胞混合物、t细胞制剂、核酸、核酸混合物、t细胞受体、t细胞受体混合物、载体、宿主细胞和/或mrna可以被包装在例如小瓶、瓶、烧瓶中,所述小瓶、瓶、烧瓶可以被进一步包装,例如,被包装在箱子、封套或袋子中。在一些实施方案中,所述试剂盒包含肽混合物、t细胞混合物、核酸混合物和/或t细胞受体混合物,其中肽、t细胞、核酸和/或t细胞受体被提供在分开的容器中,以使得由使用者来混合肽、t细胞、核酸和/或t细胞受体。表表1.seqidnos:1-4的位置146突变的ras肽表2.seqidnos:5和6的位置117突变的ras肽表3.seqidnos:7-12的位置13突变的ras肽表4.seqidnos:13-18的位置12突变的ras肽表5.seqidnos:19-24的位置61突变的ras肽表6.本发明的肽混合物的一个实施方案中含有的肽表7.本发明的肽混合物的一个实施方案中含有的肽表8.本发明的肽混合物的一个实施方案中含有的肽表9.本发明的肽混合物的一个实施方案中含有的肽表10.本发明的肽混合物的一个实施方案中含有的肽(tg02+krasa146t)表11.本发明的肽混合物的一个实施方案中含有的肽(tg02+nrasa146t)表12.本发明的肽混合物的一个实施方案中含有的肽(tg02+nrasa146v)表13.本发明的肽混合物的一个实施方案中含有的肽(tg02+krasa146v)表14.本发明的肽混合物的一个实施方案中含有的肽(tg03+krasa146t)表15.本发明的肽混合物的一个实施方案中含有的肽(tg03+nrasa146t)表16.本发明的肽混合物的一个实施方案中含有的肽(tg03+krasa146v)表17.本发明的肽混合物的一个实施方案中含有的肽(tg03+nrasa146v)表18.本发明的肽混合物的一个实施方案中含有的肽(tg02+krask117n)表19.本发明的肽混合物的一个实施方案中含有的肽(tg02+nrask117n)表20.本发明的肽混合物的一个实施方案中含有的肽(tg03+krask117n)表21.本发明的肽混合物的一个实施方案中含有的肽(tg03+nrask117n)表22.本发明的肽混合物的一个实施方案中含有的肽(tgx3)表23.本发明的肽混合物的一个实施方案中含有的肽(tgx3的备选形式)实施例实施例1在该实施例中,自4名正常人供体收集血沉棕黄层(buffycoat)(棕黄1、棕黄2、棕黄3和棕黄4)并在体外培养。利用单个ras肽或ras肽的混合物刺激体外pbmc,并进行t细胞增殖测定。结果显示在图7-9中。方法设备/试剂-hettichrotina420(半径210)或同等物-kojairsilverlineblueseries层流罩或同等物-co2培养器,formascientificmodel3111或同等物-水浴37℃-kovaglasstic载玻片(目录号87144e,hycorbiomedicalinc,gardengrove,usa)-topcount,微板闪烁计数器(packardinstrumentcompany,meriden,usa)-cellharvesterfiltermate196harvester,(packardinstrumentcompany,meriden,usa)-unifiltergf/c(目录号6-005174,nerliensmeszansky,oslo,norway)或同等物-microscint-0闪烁液(scintillationliquid)(目录号6013611,nerliensmeszansky,oslo,norway)或同等物-topseal-a(目录号6005185,nerliensmeszansky,oslo,norway)或同等物-3h-胸苷(目录号art178-d,nerliensmeszansky,oslo,norway)或同等物-cellgrodc培养基(目录号0020801-0500,cellgenixgmbh,freiburg,germany)或同等物-rpmi-1640(目录号:e15-840)paalabs,linz,austria)或同等物-二甲亚砜(dmso)(目录号:d5879-500ml,sigma-aldrichnorwayas,oslo,norway)或同等物-易咳净(mucomyst)(目录号019249,medaas,asker,norway)或同等物-重组人白介素-2(il-2,),(chirontherapeutics,emeryville,usa)或同等物-4-(2-羟乙基)-1-哌嗪乙磺酸(hepes)缓冲液1m(目录号s11-001,fisherscientificas,oslo,norway)或同等物-il-7(目录号207-il-025,r&dsystemseuropeltd,abingdon,uk)或同等物-庆大霉素40mg/ml(目录号sanofiaventisnorgeas,lysaker,norway)或同等物-人血清白蛋白20%,(目录号sw2g0013,baxteras,oslo,norway)或同等物-24孔组织培养板(目录号734-1605,vwrinternationalas,oslo,norway)或同等物-96孔圆底微板(目录号734-1797,vwrinternationalas,oslo,norway)或同等物-葡萄球菌肠毒素c型(sec-3)(目录号ct333,toxintechnologyinc,sarasota,usa)。用于培养的完全cellgrodc培养基:将以下各项添加至500ml的cellgrodc培养基中达终浓度:庆大霉素50μg/ml(添加630μl的40mg/ml储液至500ml培养基)易咳净1.6mg/ml(添加4ml的200mg/ml储液至500ml培养基)hepes缓冲液0.01m(添加5ml的1m储液至500ml的培养基)过程a.解冻冷冻的pbmc必须在室温进行该过程直至第5点。所有对细胞的开放性操作在直立式层流罩中进行。1.快速转移小瓶至37℃水浴,各小瓶具有来自血沉棕黄层(棕黄1、棕黄2、棕黄3和棕黄4)的冷冻的pbmc。2.以有规律的间隔(约2-3分钟)手动晃动小瓶并且在尚有些许冰存在时将其从水浴中移出。3.当所有冰融化后,将1ml的cellgrodc培养基逐滴转移至细胞悬液中。4.将细胞悬液转移至盛有20ml的cellgrodc培养基的50ml管中。5.将细胞以500g在室温离心5min。6.将细胞重悬在5mlcellgrodc培养基中。7.使用bürker小室或kovagalsstic载玻片对存活的细胞的数目进行计数并在完全cellgrodc培养基(见配方)中将细胞浓度调整至2x106细胞/ml。总细胞数:棕黄1-45x106,棕黄2-27.5x106,棕黄3-40.5x106,棕黄4-40.5x106个细胞。b.大体积培养以增加ras肽反应性t细胞的数目1.将1ml解冻的pbmc(2x106个细胞/ml,在dc培养基中)转移至24孔板的各个孔中。表24.再刺激:利用肽混合物刺激的孔的数目.2.添加20μl的13c和13r肽中的一种或20μl13r和60μltg02-混合物至孔中,终浓度为每种肽10μm。3.在加湿的培养器中以37℃/5%co2培养细胞达3天4.第3天:添加终浓度为20iu/ml的重组人白介素-2(ril-2)(即取1000iu/ml的储液50μl)和终浓度为5ng/ml的重组人il-7(即取500μg/ml的储液10μl)至细胞培养物并以37℃/5%co2继续温育。如果细胞生长良好,则此步骤是任选的。5.第4-6天:在显微镜下有规律地检查细胞并在需要时分细胞(从各孔中取出500μl并用500μl补充有40iu/mlil-2和il-7的新鲜cellgrodc培养基代替)。6.第7-14天:每天检查细胞并将细胞生长缓慢的孔混合在一起。c.i)3天t细胞增殖测定1.将来自步骤b.的大体积培养的t细胞收集、洗涤并计数;表25:t细胞总数2.将5x104个来自大体积培养的t细胞转移到圆底96孔板的每个孔中。3.将1小瓶在cellgrodc培养基中的自体pbmc样品解冻。照射pbmc(30gy),计数并添加5x104个细胞至各孔并用dc培养基调节至200μl/孔的总体积。4.根据平板布置,一式三份地制备以下样品:-阴性对照:仅t细胞来自各个时间点的t细胞+照射的pbmc-阳性对照:来自各个时间点的t细胞+照射的pbmc+1μg/mlsec-3.-试验样品:来自各个时间点的t细胞+照射的pbmc(10μm的各种肽):i)对于用13c+13r刺激的大体积培养物:13c+13r混合物或单一g13c肽ii)对于用tg02+13r刺激的大体积培养物:tg02+13r、13c+13r混合物或单一g13c肽将细胞在37℃/5%co2温育48小时。5.添加20μl的3h-胸苷(3.7x104bq)。6.在37℃/5%co2温育17小时。7.使用filtermate196harvester收获细胞至unifilters并在45℃干燥滤器直至完全干燥(通常这在1.5小时后实现,但是这之后在45℃放置的小时数不重要,因此平板可以在60小时后计数)。8.用粘性覆盖物(与unifilters一起递送的)覆盖unifilters的底部并向各孔添加25μl微闪烁液。用topseal覆盖平板并将滤器放置在topcountpackard微板闪烁β计数器中。进入测定向导程序。选择方案/程序3h胸苷,一式三份。进入报告定义和ascii文件输出。在目录下,选择数据文件夹(每个使用者应当具有单独的文件夹)。为要保存的实验文件选择名称。叠式存储器开启或关闭(如果超过一个平板,使用叠式存储器)。开始测定程序。ii)大体积培养物的第二次刺激将剩余的细胞(1-2x106个t细胞/孔)用自体pbmc(1百万个/孔)和肽混合物再刺激一次(如步骤b.中所述)。表26:刺激–用肽混合物刺激的孔的数目1.将细胞在加湿的培养器中在37℃/5%co2培养3天(如步骤b.中所述)。2.第17天:添加终浓度为40iu/ml的重组人白介素-2和终浓度为5ng/ml的重组人il-7至细胞培养物并且在37℃/5%co2继续培育。在显微镜下规律地检查细胞并且在需要时分细胞。3.第19-21天:从各孔中取出500μl并且用500μl补充有40iu/mlil-2和il-7的新鲜cellgrodc培养基代替。4.第22-27天:每天有规律地检查细胞,并且将t细胞生长缓慢的孔混合在一起(如步骤b.中)。d.i)3天t细胞增殖测定1.将大体积培养物中的t细胞收集、洗涤和计数。表27:细胞总数2.将来自大体积培养物的5x104个t细胞转移到圆底96孔板的每个孔中。3.将1小瓶在cellgrodc培养基中的自体pbmc样品解冻。照射pbmc(30gy),计数并添加5x104个细胞至各孔并用dc培养基调节至200μl/孔的总体积(如步骤c.i)中所述)。ii)第27-42天:大体积培养物的第三次刺激将剩余的细胞(1-2百万个t细胞/孔)用自体pbm(1百万个/孔)和肽混合物再刺激一次(如步骤b.中所述)表28:刺激–刺激的孔的数目e)3天t细胞增殖测定1.将大体积培养物中的t细胞收集、洗涤并计数。表29:细胞总数2.将来自大体积培养物的5x104个t细胞转移到圆底96孔板的每个孔中。3.将1小瓶的在cellgrodc培养基中的自体pbmc样品解冻。照射pbmc(30gy),计数并将5x104个细胞添加至各孔中并用dc培养基调节至200μl/孔的总体积(如步骤c.i)中所述)。结果大体积培养物的三轮刺激后的利用肽混合物的t细胞增殖测定的结果分别显示在表30-32和图7-9中。表30-32显示每次重复的每分钟计数(cpm),以及每名供体的平均cpm。表30:用由13c和13r肽组成的肽混合物刺激后的每分钟计数(cpm)。在大体积培养物的三轮体外刺激期间,用tg02+13r肽混合物来刺激供体#3,而用13c+13r肽混合物来刺激供体#4。表31:用由13c、13d、12a、12c、12d、12r、12s、12v和13r(即tg02+13r)肽组成的肽混合物进行刺激后的每分钟计数(cpm)。在大体积培养物的三轮体外刺激期间,用tg02+13r肽混合物来刺激供体#3。表32:用13c肽刺激后的每分钟计数(cpm)。在大体积培养物的三轮体外刺激期间,用tg02+13r肽混合物来刺激供体#3。阳性对照的结果被确认但是由于比例大小原因没有被包括在图7-9中。如可见的,肽混合物和单一肽二者都可以诱导t细胞增殖,表明所述肽和肽混合物能够在人中诱导免疫应答。实施例2在该实施例中,用tg02在皮下重复接种小鼠,以便分析免疫应答。在接种后,收获脾细胞,并测量脾细胞的增殖性反应。结果显示在图10中。方法试验项表征名称:tg02产品:tg02由等量(重量)的8种不同的肽(12a、12c、12d、12r、12s、12v、13c、13d)组成批次号:12a:批号1034804;12c:批号1034803;12d:批号1034801;12r:批号1034802;12s:批号1034805;12v:批号1034800;13c:批号1050468;13d:批号1034806治疗适应证:癌症物理状态:粉末颜色:白色纯度:每个小瓶净80mg肽(每种肽净10mg)存储条件:-15℃–-20℃并且避光有效期限:31.12.2014安全预防:常规卫生程序足以保证个人健康和安全。载体1的表征名称:viscogel批次号:vg14056治疗适应证:癌症物理状态:凝胶颗粒颜色:无色水含量:99%存储条件:2-8℃有效期限:01.06.2015安全预防:常规卫生程序足以保证个人健康和安全。载体2的表征该研究中使用的载体2将是注射用水(aquaadinjectionem)。以下列出由供应商提供的说明:名称:注射用水物理状态:液体存储条件:室温安全预防:常规卫生程序足以保证个人健康和安全。试验项的制备将5ml注射用水添加至一小瓶tg02(80mg)并且轻柔地转动(避免泡沫形成)从而获得16mgtg02/ml的均质储液。对于第1组的动物(见表28),用注射器抽取1mltg02储液并将其与1ml注射用水混合从而获得8mg/ml的终浓度。对于第2组和第3组的动物(参见表28),用注射器抽取1mltg02储液并将其与1mlviscogeltm混合从而获得8mg/ml的终浓度。认为试验项制剂在2-8℃稳定达6h。试验体系物种/品系:健康的balb/c小鼠(完全屏障)balb/canncrl来源:charlesriver,97633sulzfeld,德国性别:雌性治疗期开始时的年龄:约6-8周龄动物数:30(每组10只动物)动物来源于受控的保持完全屏障的繁育系统(spf)。根据德国关于动物福利的法案的第9.2条,第7项(art.9.2,no.7ofthegermanactonanimalwelfare),所述动物的繁育是出于实验目的。圈养和喂饲条件-有空调的房间中的完全屏障。-温度:22±3℃。-相对湿度:55±10%。-人造光,顺序为12小时亮,12小时暗。-换气:10x/小时。-自由接近用于大鼠和小鼠的altromin1324维持饮食。-自由接近自来水,硫酸化至约2.8的ph(饮用水,城市残余物控制、规律间隔的微生物控制)。-将动物以每笼5只动物成组地保持在ivc笼,iil型,聚砜笼中,在altromin锯纤维垫上。-食物、水和垫子的证书在bslbioservice处提交。-在实验室条件下的足够的适应期(至少5天)。动物的分配和识别将在给药前显示病理征候的动物从研究中排除。提供来自同一递送的补充动物作为交换。用耳标记给每只动物做标记以用于个体识别。实验过程用3组进行研究,每组包含10只雌性balb/c小鼠。研究的开始分两天进行,在这两天每组中的5只动物被处理。因此,将所述组分成部分i和部分ii。在不同时间点皮下处理动物(表30)。在给药期间,每天准确地观察动物的毒性征候。在最后一次给药后48小时将动物安乐死,进行宏观检查并且准备脾以用于进一步的分析。剂量在所有组中,在重复的时间点(表33)通过颈背和肩之间的皮下注射来施用试验项。所有组的施用体积都为0.1ml(0.80mgtg02)。表33:处理和动物识别临床观察在整个24天的处理期期间观察所有动物的临床征候。每天进行至少一次总体临床观察,优选地在每天的同一时间,并且考虑用药后的预期效应的峰值期。记录动物的健康状况。对每只动物进行包括皮毛、眼睛和粘膜的变化的总体临床观察,优选在每天的同一时间进行,并且考虑用药后的预期效应的峰值期。同样检查呼吸系统、循环系统、自主和中枢神经系统和躯体运动活性和行为模式。特别注意观察过敏反应、瘫痪、震颤、抽搐、流延、腹泻、昏睡、睡眠和昏迷的征候。此外,注意注射位点。病理学-总体验尸最后一次给药后48小时(研究的第24天)通过断颈将动物处死并且对其进行详细的总体尸检,包括认真地检查身体的外表面、所有孔口以及颅腔、胸腔和腹腔及其内含物。细胞培养和脾细胞刺激将所有动物的脾取出,转移到细胞培养基(补充有10%fcs,100u/ml青霉素,100μg/ml链霉素,2mml-谷氨酰胺和50μmβ-巯基乙醇的rpmi1640培养基)并在冰上保存。无菌地进行所有步骤并将细胞保持在冰上。使用细胞过滤器来生成脾细胞的单细胞悬液。在离心(350g,5min,5±3℃)后,将上清移除并将细胞沉淀重悬在ack缓冲液中并在室温温育5min。添加10ml细胞培养基。将样品在试验台上放置5min以使细胞碎片沉淀。将细胞碎片上方的悬液转移到另一个管中并离心(350g,5min,5±3℃)。将上清移除并将细胞沉淀重悬在10ml细胞培养基中。在给细胞计数后,将0.2mio细胞接种到96孔板中(180μl/孔;1,1*106个细胞/ml)。对于每个脾在每个板上铺板9个重复样。(1)1块板用于在24小时后收集用于细胞因子测量的上清(结果未示)(2)1块板用于在48小时后收集用于细胞因子测量的上清(结果未显示)。(3)1块板用于增殖测定进行以下刺激:-3个重复样:未刺激的(添加20μl细胞培养基)-3个重复样:用10μmtg02(8种肽,每种肽的终浓度为10μm,添加在20μl细胞培养基中)刺激-3个重复样:用1μg/200μlcona(伴刀豆球蛋白a)(将1μgcona添加在20μl细胞培养基中)刺激在37℃和5%co2孵育24h(1)、48h(2)或5天(3)。将剩余的细胞离心(350g,5min,5±3℃),转移至1.5ml管中,再次离心(350g,5min,5±3℃),将上清完全移除,并将细胞沉淀在≤-70℃冷冻。(1)在24h后,将相应的板离心(350g,室温)并收集150μl上清并将其在≤-70℃冷冻。(2)在48h后,将相应的板离心(350g,室温)并收集150μl上清并将其在≤-70℃冷冻。增殖测定(3)在5天后,将1μci/孔3h-胸苷添加至样品中,然后将其在37℃和5%co2孵育18h。然后将平板在≤-20℃冷冻。在室温将平板解冻。在洗涤收集器后,使用收集器将样品转移至过滤板,之后使用水进行5个洗涤步骤。将过滤板在室温过夜干燥。将金属箔粘至过滤板的底部并将20μl闪烁液添加至孔中。室温孵育1小时后,使用topcountnxt测量样品并计算刺激指数(si)。si=刺激的样品的cpm/对照样品的cpm。结果表34和图10显示脾细胞增殖测定的结果。表34显示各重复样的cpm以及每只小鼠的平均cpm。如可见的,用tg02刺激的脾细胞显示与未刺激的脾细胞相比增加的cpm,表明tg02诱导免疫应答。表34:用tg02刺激后的每分钟计数(cpm).实施例3在该实施例中,自三名正常人供体收集血沉棕黄层(棕黄5、棕黄6和棕黄7)以测试对于反映ras中外显子2、3和4突变的所选肽的t细胞应答。使用kras肽接种(tg01)的临床研究中用于监测t细胞应答的标准操作程序(sop)被用于测试肽混合物tgx3和各个肽。方法试验肽表35.在肽混合物tgx3中的肽肽氨基酸序列seqidno:a146tgipfietstktrqrved1g13cklvvvgagcvgksalti25g13dklvvvgagdvgksalti26q61rldildtagreeysard35肽混合物tgx3是等摩尔量的a146t+g13c+g13d+q61r的混合物。设备/试剂-hettichrotina420(半径210)或同等物-kojairsilverlineblueseries层流罩或同等物-co2培养器,formascientificmodel3111或同等物-水浴37℃-kovaglasstic载玻片(目录号87144e,hycorbiomedicalinc,gardengrove,usa)-topcount,微板闪烁计数器(packardinstrumentcompany,meriden,usa)-cellharvesterfiltermate196harvester,(packardinstrumentcompany,meriden,usa)-unifiltergf/c(目录号6-005174,nerliensmeszansky,oslo,norway)或同等物-microscint-0闪烁液(scintillationliquid)(目录号6013611,nerliensmeszansky,oslo,norway)或同等物-topseal-a(目录号6005185,nerliensmeszansky,oslo,norway)或同等物-3h-胸苷(目录号art178-d,nerliensmeszansky,oslo,norway)或同等物-cellgrodc培养基(目录号0020801-0500,cellgenixgmbh,freiburg,germany)或同等物-rpmi-1640(目录号:e15-840)paalabs,linz,austria)或同等物-二甲亚砜(dmso)(目录号:d5879-500ml,sigma-aldrichnorwayas,oslo,norway)或同等物-易咳净(mucomyst)(目录号019249,medaas,asker,norway)或同等物-重组人白介素-2(il-2,),(chirontherapeutics,emeryville,usa)或同等物-4-(2-羟乙基)-1-哌嗪乙磺酸(hepes)缓冲液1m(目录号s11-001,fisherscientificas,oslo,norway)或同等物-il-7(目录号207-il-025,r&dsystemseuropeltd,abingdon,uk)或同等物-庆大霉素40mg/ml(目录号sanofiaventisnorgeas,lysaker,norway)或同等物-人血清白蛋白20%,(目录号sw2g0013,baxteras,oslo,norway)或同等物-24孔组织培养板(目录号734-1605,vwrinternationalas,oslo,norway)或同等物-96孔圆底微板(目录号734-1797,vwrinternationalas,oslo,norway)或同等物用于培养的完全cellgrodc培养基:将以下各项添加至cellgrodc培养基中至500ml培养基以达到终浓度:庆大霉素50μg/ml(储液为40mg/ml,添加630μl的储液至500ml培养基)易咳净1.6mg/ml(储液为200mg/ml,添加4ml的储液至500ml培养基)hepes缓冲液0.01m(储液为1m,添加5ml的储液至500ml的培养基)实验过程a).从血沉棕黄层分离pbmc该过程在室温进行。所有对细胞的开放性操作在直立式层流罩中进行。1.从blodbanken,ous,norway订购3个血沉棕黄层2.根据方法c001-003(血小板降低(platelet-low))分离pbmc。3.使用kovagalsstic载玻片对存活的细胞的数目进行计数并在完全cellgrodc培养基(见配方)中将细胞浓度调整至4x106细胞/ml。总细胞数:棕黄5-585x106,棕黄6-360x106,和棕黄7-405x106个细胞。b).第一次刺激-大体积培养以增加tgx3和肽反应性t细胞的数目1.将1ml不同的pbmc(4x106个细胞/ml,在dc培养基中)转移至24孔板的各个孔中。表36.第一次刺激:大体积培养中的细胞数目.细胞总数tgx3混合物肽a146t棕黄5120x1061010棕黄6120x1061010棕黄7120x10610102.添加tgx3-混合物/单个肽至每个孔中,终浓度为每种肽10μm。3.在加湿的培养器中以37℃/5%co2培养细胞达3天4.第3天:添加终浓度为20iu/ml的重组人白介素-2(ril-2,b#77)和终浓度为5ng/ml的重组人il-7(b#25)至细胞培养物并以37℃/5%co2继续温育。这取决于细胞生长的速度有多快,并且需要由具备t细胞培养经验的受过培训的人员来决定(根据培训清单,细胞疗法部分)。5.第4-12天:在显微镜下有规律地检查细胞并在需要时分细胞(从各孔中取出500μl并用500μl补充有20iu/mlil-2和5ng/mlil-7的新鲜cellgrodc培养基代替),并将细胞生长缓慢的孔混合在一起。c)大体积培养的第二次刺激(第14天)1.第14天:将来自6.2的大体积培养的t细胞收集、洗涤并计数;表37:培养中的t细胞总数tgx3-混合物肽a146t棕黄58.1x1064x106棕黄65.4x1064x106棕黄713.5x1066.8x106大体积培养细胞(约2x106个t细胞/孔)用自体照射(30gy)的apc(约2x106个apc/孔)加其相应的肽再一次进行再刺激(如上述步骤b)中所述的)。2.在加湿的培养器中以37℃/5%co2培养细胞达3天3.第二次刺激后的第3天(即,该过程的第17天):添加终浓度为20iu/ml的重组人白介素-2(ril-2,b#77)和终浓度为5ng/ml的重组人il-7(b#25)至细胞培养物并以37℃/5%co2继续温育(如上步骤b)中所述的)。4.第18-26天:在显微镜下有规律地检查细胞并在需要时分细胞(从各孔中取出500μl并用500μl补充有20iu/mlil-2和5ng/mlil-7的新鲜cellgrodc培养基代替),并将细胞生长缓慢的孔混合在一起(参见上述步骤b))。d)第三次刺激(第19天)并测试在3天t细胞增殖测定-大体积培养中的特异性1.第19天:将来自6.3的大体积培养的t细胞收集、洗涤并计数;表38:t细胞总数tgx3-混合物肽a146t棕黄512.6x10610.8x106棕黄69x10612.6x106棕黄723.4x10614.4x1062.将5x104个来自大体积培养的t细胞转移到圆底96孔板的每个孔中。3.将1-2小瓶在cellgrodc培养基中的自体pbmc样品解冻。照射pbmc(30gy),计数并添加5x104个细胞至各孔并用其相应的肽进行刺激。4.将5x104个t细胞加至其相应的孔(参见表39)表39:增殖测定布置棕黄5、6、7apc*-照射的pbmc(第23天)5.第三次刺激:剩余细胞(约2x106个t细胞/孔)用照射的自体apc(约2百万个/孔)加其相应的肽再刺激一次(如6.2所述)。6.第21天:添加20μl的3h-胸苷(3.7x104bq)。7.在37℃/5%co2温育17小时。8.第22天:使用filtermate196harvester收获细胞至unifilters并在45℃干燥滤器直至完全干燥(通常这在1.5小时后实现,但是这之后在45℃放置的小时数不重要,因此平板可以在60小时后计数)。9.用粘性覆盖物(与unifilters一起递送的)覆盖unifilters的底部并向各孔添加25μl微闪烁液。用topseal覆盖平板并将滤器放置在topcountpackard微板闪烁β计数器中。进入测定向导程序。选择方案/程序3h胸苷,一式三份。进入报告定义和ascii文件输出。结果利用肽混合物的t细胞增殖测定的结果显示在图11和12中。特别地,图11显示了ras蛋白的位置146处具有突变的肽是免疫原性的并且刺激t细胞的诱导。图12显示了肽混合物tgx3可有效诱导t细胞应答(不仅对肽混合物,而且还对肽混合物中的各个肽)。因此,图12首次显示了包含各自具有位置13、位置61或位置146点突变的肽的肽混合物可以诱导t细胞应答。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1