Ф6内部对照组合物、设备和方法与流程
公开了用于核酸扩增方法的包含ф6噬菌体的组合物。还公开了被进行配置以执行核酸扩增方法的样品处理设备和试剂盒,其中所述设备和/或试剂盒包含ф6内部对照组合物。
发明背景
已经开发了各种用于扩增核酸的方法,包括聚合酶链反应(pcr)、连接酶链反应、聚合酶连接酶链反应、缺口-lcr、修复链反应(repairchainreaction)、3sr、nasba、链置换扩增(sda)、转录介导的扩增(tma)和qβ-扩增。这些方法中的每一种都涉及一系列复杂且敏感的步骤,并且准确、定性和/或定量测定需要仔细控制在每个步骤的可变性。对控制标准进行精确校准并且它们可以经受住测定程序的苛刻行为也是关键的。
生物样品中核酸的定性检测是关键的,例如,对于识别个体的感染,且因此应将假阴性和假阳性结果减至最小。因此,将定性内部对照核酸添加到检测混合物中。此外,定量生物样品中的病毒核酸序列是用于评估患者的病毒量(即,在一个时间点在给定患者内病毒颗粒的总量的量度)的重要工具。在慢性感染中,病毒量是病毒复制和免疫介导的宿主清除的高度动态平衡的函数。病毒量可用于评估诊断时病毒复制的程度,其提供对患者进展和预后的评估。它还可用于在病程早期监控抗病毒药疗法的效果,并快速评估改变抗病毒药疗法的效果。
与临床诊断相关的许多核酸是核糖核酸,例如,来自rna病毒的核酸,如例如,人免疫缺陷病毒(hiv)、丙型肝炎病毒(hcv)、西尼罗病毒(wnv)、人乳头瘤病毒(hpv)、日本脑炎病毒(jev)、圣·路易脑炎病毒(slev)、流感病毒、诺如病毒(norovirus)等。因此,使用由rna组成的内部对照核酸以反映样品中靶核酸的性质可以是有利的。因为rna由于其对诸如碱性ph、核糖核酸酶等的影响的固有敏感性而比dna更易于降解,所以由rna制备的内部对照核酸通常作为被壳的颗粒提供。被壳的rna®(arna)技术通过将核酸包装在保护性噬菌体蛋白外壳中来稳定和保护核酸免于核酸酶降解。(被壳的rna由ambion,inc.和cenetrondiagnosticsllc开发,两者均是德克萨斯州奥斯汀的,并且在美国专利5,677,124、5,919,625和5,939,262下保护)。这些arna构建体在测定中被完全加工,它们在环境温度是热稳定的,并且它们是相对rna酶抗性的。然而,在高温,arna构建体迅速降解,从而导致测定失败。为了延长包含这些构建体的产品的贮存期限,产品于4℃运输和储存,这是昂贵的。因此,需要一种用于定性和/或定量核酸检测方法的耐热的、核糖核酸酶抗性rna标准物。
发明概述
本文提供了用于定性和/或定量核酸检测方法的耐热的、核糖核酸酶抗性rna标准制剂。本文所述的组合物于30℃热稳定达最多到110天,且特别是于45℃达最多到28天。因此,本公开内容提供了包含悬浮于在7-9的ph的适合于核酸扩增反应的缓冲液中的ф6噬菌体的组合物,其包含螯合剂和防腐剂,并且任选地包含一种或多种选自bsa、明胶、聚rarna、甘油、氨基酸、海藻糖、酪蛋白或聚乙二醇的额外组分。
在一个方面,提供了包含悬浮于在7-9的ph的适合于核酸扩增反应的缓冲液中的ф6的组合物,其包含螯合剂和防腐剂。在一些实施方案中,所述缓冲液选自柠檬酸缓冲液、甘氨酸缓冲液、n-(三(羟甲基)甲基)甘氨酸(tricine)缓冲液、pipes或hepes。在某些实施方案中,所述缓冲液是n-(三(羟甲基)甲基)甘氨酸缓冲液。在一些实施方案中,组合物进一步包含一种或多种选自bsa、明胶、聚rarna、甘油、氨基酸、海藻糖、酪蛋白或聚乙二醇的额外组分。在一些实施方案中,所述一种或多种额外组分选自0-25mg/mlbsa、0-1.0%明胶、0-20mg/l聚rarna或0-40%甘油。在特定实施方案中,所述一种或多种额外组分包含最多到40%的甘油。在一些实施方案中,所述ф6以最多到4e5拷贝/ml的浓度存在。在一些实施方案中,所述螯合剂选自edta和egta。在某些实施方案中,该组合物包含0.01-1.0mmedta。在特定实施方案中,该组合物包含0.10mmedta。在一些实施方案中,所述防腐剂选自叠氮化钠和proclin300。在某些实施方案中,该组合物包含0.01-1.0mm叠氮化钠。在特定实施方案中,该组合物包含0.05%叠氮化钠。
在一些实施方案中,组合物包含:
(a)在10mmtris,ph8.0,0.1mmedta,0.05%叠氮化钠和25mg/mlbsa中最多到4e5cp/ml的ф6;或
(b)在10mmtris,ph8.0,0.1mmedta,0.05%叠氮化钠和1%明胶中最多到4e5cp/ml的ф6;或
(c)在10mmtris,ph8.0,0.1mmedta,0.05%叠氮化钠和20mg/l聚rarna中最多到4e5cp/ml的ф6;或
(d)在10mmtris,ph8.0,0.1mmedta,0.05%叠氮化钠,20mg/l聚rarna和40%甘油中最多到4e5cp/ml的ф6。
在一些实施方案中,该组合物于45℃热稳定达最多到28天。在一些实施方案中,该组合物于30℃热稳定达最多到110天。在一些实施方案中,在第0天的∆ct于45℃<5-7达最多到28天。在一些实施方案中,在第0天的∆ct在一个或多个冻融循环后<5-7。
在另一个方面,提供了一种用于核酸扩增的方法,包括:
-提供含有至少一种可扩增的靶核酸序列的核酸样品;
-使所述核酸样品与上述任一实施方案的组合物接触;和
-使用能够起始扩增反应的酶扩增所述靶核酸序列。
在一些实施方案中,所述核酸样品是rna,并且该方法进一步包括
-使用能够起始逆转录的酶逆转录所述靶核酸序列。
在一些实施方案中,使用能够起始逆转录和/或扩增反应的酶的组合或使用能够起始逆转录和扩增反应的酶来进行逆转录和扩增所述靶核酸序列。在一些实施方案中,ф6噬菌体在定性和/或定量核酸检测中作为rna标准物被逆转录和/或扩增。在一些实施方案中,ф6噬菌体在与靶核酸相同的反应中被逆转录和/或扩增。在一些实施方案中,核酸样品中靶核酸序列的量基于测定的ф6噬菌体的量来确定。在一些实施方案中,用于核酸扩增的方法是聚合酶链反应(pcr)。在一些实施方案中,用于核酸扩增的方法是偶联逆转录和聚合酶链反应(rt-pcr)。在一些实施方案中,所述核酸样品衍生自血浆、全血、尿、粪便材料、粘液及其组合。在一些实施方案中,用于核酸扩增的方法是病毒量分析。在某些实施方案中,用于核酸扩增的方法是病毒量分析,其中样品是rna病毒。在某些实施方案中,rna病毒是人免疫缺陷病毒(hiv)、丙型肝炎病毒(hcv)、西尼罗病毒(wnv)、人乳头瘤病毒(hpv)、日本脑炎病毒(jev)、圣·路易脑炎病毒(slev)、流感病毒或诺如病毒。
在另一个方面,提供了一种设备,其被进行配置以在样品中进行核酸分析,所述设备包括
(a)适合于接收样品等分试样的样品引入端口;
(b)内部对照区室,其包含上述任一实施方案的组合物;和
(c)核酸分析区域,其包括一个或多个另外的区室,每个区室被进行配置以进行所述核酸分析的一个或多个步骤,包括试剂制备、靶富集、抑制剂去除、核酸提取、逆转录、扩增和实时检测。
在一些实施方案中,核酸分析是或包括聚合酶链反应(pcr)。在一些实施方案中,用于核酸扩增的方法是或包括偶联逆转录和聚合酶链反应(rt-pcr)。在一些实施方案中,所述样品包括血浆、全血、尿、粪便材料、粘液及其组合。在一些实施方案中,将样品悬浮在通用运送培养基(utmtm)中。在一些实施方案中,所述分析是病毒量分析。在某些实施方案中,所述分析是病毒量分析,其中样品是rna病毒。在某些实施方案中,rna病毒是人免疫缺陷病毒(hiv)、丙型肝炎病毒(hcv)、西尼罗病毒(wnv)、人乳头瘤病毒(hpv)、日本脑炎病毒(jev)、圣·路易脑炎病毒(slev)、流感病毒或诺如病毒。在具体的实施方案中,提供了一种设备,其被进行配置以在样品中进行病毒量分析,其中所述设备包括适合于接收样品等分试样的样品引入端口;内部对照区室,其包含如本文所述的组合物;和pcr分析区域,其包括一个或多个另外的区室,每个区室被进行配置以进行pcr分析的一个或多个步骤,包括试剂制备、靶富集、抑制剂去除、核酸提取、扩增和实时检测。
还提供了ф6噬菌体在定性和/或定量核酸检测方法中作为rna标准物的用途。在本文中,提供了ф6噬菌体在定性和/或定量核酸检测方法中作为rna标准物的用途,其中将ф6噬菌体悬浮于在7-9的ph的适合于核酸扩增反应的缓冲液中,包含螯合剂和防腐剂。还提供了缓冲液选自柠檬酸缓冲液、甘氨酸缓冲液、n-(三(羟甲基)甲基)甘氨酸缓冲液、pipes或hepes,特别是n-(三(羟甲基)甲基)甘氨酸缓冲液。还提供了所述缓冲液进一步包含一种或多种选自bsa、明胶、聚rarna、甘油、氨基酸、海藻糖、酪蛋白或聚乙二醇的额外组分。还提供了所述一种或多种额外组分选自0-25mg/mlbsa、0-1.0%明胶、0-20mg/l聚rarna或0-40%甘油,特别是所述一种或多种额外组分包含最多到40%的甘油。还提供了ф6以最多到4e5拷贝/ml的浓度存在。还提供了螯合剂选自edta和egta。还提供了该组合物包含0.01-1.0mmedta,特别是0.10mmedta。还提供了防腐剂选自叠氮化钠和proclin300。还提供了该组合物包含0.01-1.0mm叠氮化钠,特别是0.05%叠氮化钠。还提供了所述缓冲液包含:
(a)在10mmtris,ph8.0,0.1mmedta,0.05%叠氮化钠和25mg/mlbsa中最多到4e5cp/ml的ф6;或
(b)在10mmtris,ph8.0,0.1mmedta,0.05%叠氮化钠和1%明胶中最多到4e5cp/ml的ф6;或
(c)在10mmtris,ph8.0,0.1mmedta,0.05%叠氮化钠和20mg/l聚rarna中最多到4e5cp/ml的ф6;或
(d)在10mmtris,ph8.0,0.1mmedta,0.05%叠氮化钠,20mg/l聚rarna和40%甘油中最多到4e5cp/ml的ф6。
附图简述
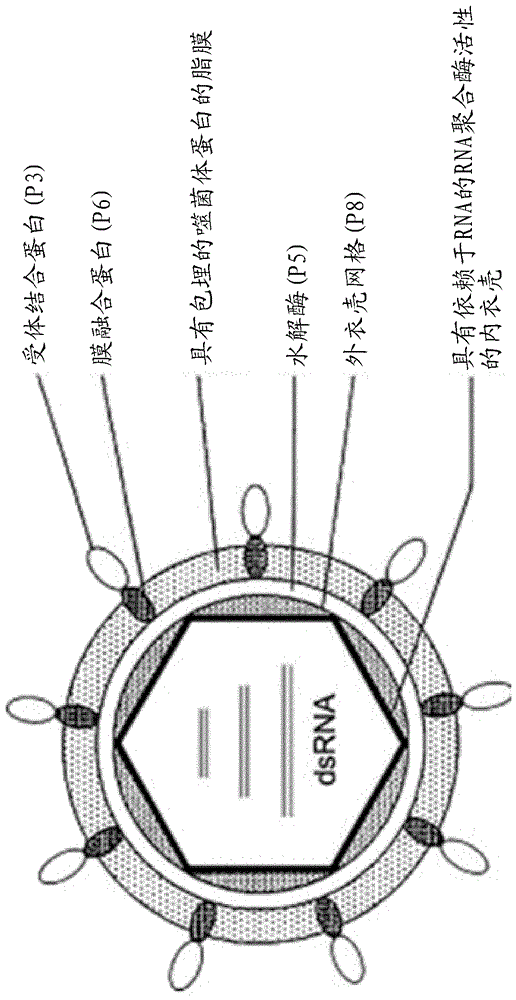
图1显示了ф6噬菌体的结构。
图2显示了可与本文所述组合物一起使用的样品处理设备。
图3举例说明了被壳的rna组合物在升高的温度随时间的过去的降解。
图4a-4b显示了各种ф6组合物在升高的温度随时间的过去的热稳定性。
详述
定义
除非本文另有定义,否则本文使用的科学和技术术语都具有本领域普通技术人员通常理解的含义。此外,除非上下文另有要求,否则单数术语包括复数,并且复数术语包括单数。本文使用的冠词“一(a)”和“一个(an)”是指该冠词的一个或多于一个(即,至少一个)语法对象。作为例子,“要素”表示一个要素或多于一个要素。
术语“检测(detect)”、“检测(detecting)”、“检测(detection)”和类似术语在本申请中用于广泛地指过程或发现或确定某事物存在或不存在,以及程度、量或水平,或发生的概率。例如,当关于靶核酸序列使用时,术语“检测”可以表示发现或确定所述序列存在、不存在、水平或量,以及存在或不存在的概率或可能。要理解的是,表述“检测存在或不存在”、“存在或不存在的检测”和相关表达包括定性和定量检测。
术语“核酸”、“多核苷酸”和“寡核苷酸”是指核苷酸(例如,核糖核苷酸或脱氧核糖核苷酸)的聚合物,并且包括天然存在的(腺苷、胍、胞嘧啶、尿嘧啶和胸苷)、非天然存在的和修饰的核酸。该术语不受聚合物长度(例如,单体数)的限制。核酸可以是单链或双链的,并且将通常含有5'-3'磷酸二酯键,尽管在一些情况下,核苷酸类似物可以具有其他键。单体一般称为核苷酸。术语“非天然核苷酸”或“修饰的核苷酸”是指含有修饰的含氮碱基、糖或磷酸基团的核苷酸,或在其结构中掺入非天然部分的核苷酸。非天然核苷酸的实例包括双脱氧核苷酸、生物素化的、胺化的、脱氨基的、烷基化的、苄化的和荧光团标记的核苷酸。
核酸扩增的一种方法是聚合酶链反应(pcr),其公开于连同其他参考文献一道的美国专利nos.4,683,202、4,683,195、4,800,159和4,965,188中。pcr一般使用两种或更多种寡核苷酸引物,其与选择的核酸模板(例如,dna或rna)结合。用于核酸分析的引物包括能够作为靶核酸的核酸序列内的核酸合成的起始点的寡核苷酸。可以通过常规方法从限制酶切消化液中纯化引物,或者可以合成生产引物。引物优选是单链的以用于最大的扩增效率,但引物可以是双链的。首先使双链引物变性,即,处理以分离链。使双链核酸变性的一种方法是通过加热。“热稳定聚合酶”是一种热稳定的聚合酶,即,它是这样的酶,其催化形成与模板互补的引物延伸产物,并且当经受升高的温度达引起双链模板核酸变性所需的时间时不会不可逆地变性。通常,合成在每个引物的3'端起始,并沿着模板链以5'至3'方向进行。例如,热稳定聚合酶已分离自黄栖热菌(thermusflavus)、红栖热菌(t.ruber)、嗜热栖热菌(t.thermophilus)、水生栖热菌(t.aquaticus)、乳栖热菌(t.lacteus)、红色栖热菌(t.rubens)、嗜热脂肪芽孢杆菌(bacillusstearothermophilus)和炽热甲烷嗜热菌(methanothermusfervidus)。尽管如此,在pcr测定中也可使用不热稳定的聚合酶,只要补足酶。
如果模板核酸是双链的,则在其用作pcr中的模板前必须将两条链分离。链分离可以通过任何合适的变性方法完成,包括物理、化学或酶促方法。分离核酸链的一种方法包括加热核酸直至其多数变性(例如,大于50%、60%、70%、80%、90%或95%变性)。用于变性模板核酸所必需的加热条件将取决于例如缓冲盐浓度和变性的核酸的长度和核苷酸组成,但取决于反应的特征如温度和核酸长度,一般范围从约90℃到约105℃达一段时间。变性一般进行达约5秒至9分钟。为了不将相应的聚合酶暴露于如此高的温度达太长时间并因此冒丧失功能酶的风险,优选使用短的变性步骤。在具体实施方案中,变性步骤最多到30秒,例如最多到20秒、最多到10秒、最多到5秒,且特别是约5秒。
如果双链模板核酸通过加热变性,则允许反应混合物冷却至促进每个引物与靶核酸上的其靶序列退火的温度。用于退火的温度优选约35℃至约70℃,进一步优选约45℃至约65℃;进一步优选约50℃至约60℃,进一步优选约55℃至约58℃。退火时间可为约10秒至约1分钟(例如,约20秒至约50秒;约30秒至约40秒)。在这种情况下,使用不同的退火温度以增加相应测定的包容性(inclusivity)可以是有利的。简而言之,这意味着在相对低的退火温度,引物也可以与具有单个错配的靶结合,从而也可以扩增某些序列的变体。如果例如某种生物具有已知或未知的也应该被检测到的遗传性变型,则这是所期望的。另一方面,相对高的退火温度具有提供更高特异性的优点,这是因为在更高的温度,引物结合到不完全匹配的靶序列的概率连续降低。为了得益于这两种现象,在本发明的一些实施方案中,优选上述方法包括在不同温度的退火,优选首先在较低温度,然后在较高温度。例如,如果第一次温育在55℃发生约5个循环,则可以(预)扩增非完全匹配的靶序列。这后面可以是例如在58℃的约45个循环,从而在整个实验的主要部分期间提供更高的特异性。这样,潜在重要的遗传性变型不会被遗漏,而特异性仍然相对高。
然后将反应混合物调节至促进或最优化聚合酶活性的温度,即,足以从退火的引物发生延伸以产生与待分析的核酸互补的产物的温度。温度应足以从每个与核酸模板退火的引物合成延伸产物,但不应高得足以使延伸产物从其互补模板变性(例如,延伸温度通常范围从约40°到80℃(例如,约50℃至约70℃;约60℃)。延伸时间可为约10秒至约5分钟,优选约15秒至2分钟,进一步优选约20秒至约1分钟,进一步优选约25秒至约35秒。新合成的链形成双链分子,其可用于随后的反应步骤。可以如所需要的那样经常重复链分离、退火和延伸的步骤,以生产对应于靶核酸的所期望量的扩增产物。反应中的限制因子是反应中存在的引物、热稳定酶和核苷三磷酸的量。循环步骤(即,变性、退火和延伸)优选重复至少一次。为了用于检测,循环步骤的数目将取决于例如样品的特性。如果样品是核酸的复杂混合物,则将需要更多循环步骤来扩增足以进行检测的靶序列。通常,循环步骤重复至少约20次,但可重复多达40、60或甚至100次。
可以进行pcr测定,其中退火和延伸的步骤在相同步骤(一步pcr)或者在分开的步骤(两步pcr)中进行。一起且因而在相同的物理和化学条件下,使用合适的酶(如例如z05dna聚合酶)进行退火和延伸,具有节省每个循环中用于额外步骤的时间的优点,并且还消除了对退火和延伸之间的额外温度调节的需要。因此,一步pcr降低了相应测定的总体复杂性。
通常,总体扩增的较短时间是优选的,这是因为到结果的时间(time-to-result)减少并且导致可能的更早诊断。
可包括使用本文所述标准物的其他优选核酸扩增方法包括,但不限于,连接酶链反应(lcr;wud.y.和wallacer.b.,genomics4(1989)560-69;和baranyf.,proc.natl.acad.sci.usa88(1991)189-193);聚合酶连接酶链反应(baranyf.,pcrmethodsandapplic.1(1991)5-16);缺口-lcr(wo90/01069);修复链反应(ep0439182a2),3sr(kwohd.y.等人,proc.natl.acad.sci.usa86(1989)1173-1177;guatellij.c.等人,proc.natl.acad.sci.usa87(1990)1874-1878;wo92/08808)和nasba(us5,130,238)。此外,本文描述的标准物还可以用于以下方法:链置换扩增(sda)、转录介导的扩增(tma)和qb-扩增(关于综述,参见,例如,whelena.c.和persingd.h.,annu.rev.microbiol.50(1996)349-373;abramsonr.d.和myerst.w.,curropinbiotechnol4(1993)41-47)。
术语“引物”是指短核酸(寡核苷酸),其充当在合适的条件下通过核酸聚合酶的多核苷酸链合成的起始点。多核苷酸合成和扩增反应一般包括合适的缓冲液、dntps和/或rntps,以及一种或多种任选的辅因子,并且在合适的温度进行。引物一般包含至少一个靶杂交区域,其至少基本上与靶序列互补。这个区域的长度一般为约15至约40个核苷酸。“引物对”是指正向引物和反向引物(有时称为5'和3'引物),其与靶序列的相反链互补并设计用于扩增靶序列。正向和反向引物排列在靶序列上彼此可扩增的距离内,例如约10-5000个核苷酸,或约25-500个核苷酸。
如本文所用的,“探针”意指能够选择性结合特别预期的靶生物分子(例如,待被探针结合、捕获或杂交的目标核酸序列)的任何分子。
词语“互补”或“互补性”是指多核苷酸中的核酸与第二多核苷酸中的另一核酸形成碱基对的能力。例如,序列5'-a-g-t-3'(rna的5'-a-g-u-3')与序列3'-t-c-a-5'(rna的3'-u-c-a-5')互补。互补性可以是部分的,其中仅一些核酸根据碱基配对匹配,或完全的,其中所有核酸都根据碱基配对匹配。如果探针或引物与靶序列至少部分互补,则认为该探针或引物“特异于”所述靶序列。取决于条件,与靶序列的互补程度对于较短的核酸(例如引物)一般比对于较长序列的更高(例如,大于80%、90%、95%或更高)。
术语“扩增条件”或类似表达是指核酸扩增反应(例如,pcr扩增)中的条件,其允许引物的杂交和模板依赖性延伸,如上文所述的。术语“扩增子”是指核酸分子,其含有靶核酸序列的全部或片段,并且作为通过任何合适的扩增方法的体外扩增产物形成。pcrstrategies(innis等,1995,academicpress,sandiego,ca)第14章;pcrprotocols:aguidetomethodsandapplications(innis等人,academicpress,ny,1990)中描述了各种pcr条件。
术语“样品”或“生物样品”是指含有或假定含有来自个体的核酸的任何组合物。该术语包括细胞、组织或血液的纯化或分离的组分,例如dna、rna、蛋白质、无细胞部分或细胞裂解物。在一个实施方案中,样品是全血样品。如本文所用的,“全血样品”包括从身体抽出的血液,其中尚未去除诸如血浆或血小板的成分。通常,除了存在抗凝剂之外,样品是未修饰的。样品还可以指其他类型的生物样品,例如血浆、血清、血液组分(暗黄覆盖层(buffycoat))和干血点(driedbloodspots)。样品还可包括从个体获得的细胞的体外培养物的成分和组分,包括细胞系。生物样品的具体另外的实例包括粪便、粘膜拭子、组织抽吸物、组织匀浆、细胞培养物和细胞培养物上清液(包括真核细胞和原核细胞的培养物)、尿、唾液、痰和脑脊样品。
本文所述的内部对照组合物可充当“定量标准核酸”,其是用于确定靶核酸的量的参考。为此目的,定量标准核酸与靶核酸一起经历所有可能的样品制备步骤。此外,在整个测定方法期间,在相同反应混合物中处理定量标准核酸。它必须在存在或不存在靶核酸的情况下直接或间接产生可检测的信号。为此目的,必须在每次测试中最优化定量标准核酸的浓度,以不干扰灵敏度,但是也例如在非常高的靶浓度产生可检测的信号。就各个测定的检测极限(lod,参见下文)而论,“定量标准核酸”的浓度范围是20-5000xlod,特别是20-1000xlod,且具体是20-5000xlod。反应混合物中定量标准核酸的最终浓度取决于完成的定量测量范围。
“检测极限”或“lod”是指样品中核酸的最低可检测量或浓度。低“lod”对应于高灵敏度,且反之亦然。“lod”通常通过单位“cp/ml”表示,特别是如果核酸是病毒核酸的话,或表示为iu/ml。“cp/ml”表示“每毫升拷贝数”,其中“拷贝”是相应核酸的拷贝。iu/ml代表“国际单位/ml”,参考who标准。
如果组合物能够在没有显著的循环阈值(ct)丧失的情况下经受住中等的热(例如37-60℃的温度)达最多到200天,则该组合物是“热稳定的”。在实时pcr中,通过荧光信号的累积检测阳性反应,并且ct值定义为荧光信号穿过阈值所需的循环数,此时信号超过背景水平。ct与样品中靶核酸的量成反比。∆ct对应于目标序列的ct与内部对照的ct之间的差。在一个实施方案中,如本文所述的内部对照组合物的∆ct于45℃≤1-3达最多到28天,且更具体地,∆ct于45℃≤1达最多到28天。此外,本文所述的组合物在-80℃至4℃的一个或多个冻融循环后是热稳定的。
组合物
φ6噬菌体(ф6)是具有分节段基因组的有包膜双链rna病毒。与单链rna基因组(如arna)不同,ф6具有两个保护性被壳的层:蛋白质衣壳和脂膜。这在图1中举例说明。
ф6可以配制在适合用于核酸扩增测定的任何介质中。在一个实施方案中,将最多到约4e5拷贝/ml的冻干的ф6悬浮于ph为7-9的合适的缓冲液中,例如基于柠檬酸的、基于甘氨酸的、基于n-(三(羟甲基)甲基)甘氨酸的缓冲液,以及pipes和hepes。对于核酸扩增方法,应避免使用基于磷酸的缓冲液。在具体实施方案中,缓冲液是tris-hcl,例如浓度为5-20mm,具体是8-12.5mm,且特别是10mm,且ph为7-9,且具体是ph8。
制剂还可包含螯合剂,例如edta或egta,和防腐剂,例如nan3或proclin300。在具体实施方案中,制剂包含edta和nan3。在一个实施方案中,螯合剂为0.01-1.0mmedta,例如0.1mmedta且防腐剂为0.01-1.0mm叠氮化钠,例如0.05%nan3。
制剂中可包含一种或多种额外组分,包括但不限于0-25mg/ml牛血清清蛋白(bsa),0-3%明胶,0-100mg/l聚rna,0-40%甘油,0-25mg/ml氨基酸,例如谷氨酰胺等,海藻糖,酪蛋白,5-40%聚乙二醇(peg)等。
在具体实施方案中,内部对照的原液可包含1000至1,000,000拷贝/ml冻干的ф6,且更具体地,100,000至750,000拷贝。表1提供了合适的ф6制剂的非限制性实例组:
表1.
ф6组合物于45℃稳定达最多到28天,于50℃稳定达最多到14天,且于30℃稳定达最多到110天。此外,制剂耐受一个或多个冻融循环,例如在-80℃至4℃之间。
测定系统和样品处理设备
本文所述的对照材料可用于任何手动扩增测定方法或自动核酸扩增系统或样品制备系统。在一个实施方案中,对照材料可用于任何合适的可商购的pcr仪器和/或样品制备系统,包括但不限于cobas®6800/8800系统,cobas®4800系统,cobas®ampliprep仪器,cobas®liat®系统,cobas®p630仪器,cobas®s201系统,cobas®taqman®48分析仪,cobas®taqman®分析仪,lightcycler®1536系统,lightcycler®2.0系统,lightcycler®480系统,lightcycler®96系统,magnapure96系统,magnapurecompact系统,magnapurelc2.0系统或flow解决方案(solution)(参见,例如,www.molecular.roche.com/systems)。
在具体实施方案中,本文所述的组合物用于被进行配置以进行核酸扩增技术的样品处理设备中。可以通过使用上文描述的任何方法扩增核酸来进一步处理从生物样品中提取的核酸。在具体实施方案中,从生物提取的核酸是rna,并且它们的处理包括使用酶的组合的偶联逆转录和聚合酶链反应(rt-pcr),所述酶例如tth聚合酶和taq聚合酶或逆转录酶和taq聚合酶。在一些实施方案中,带切口的环状核酸探针可以使用t4dna连接酶或ampligasetm和指导核酸环化,后面是在体外选择过程后检测闭环探针的形成。这种检测可以使用本领域技术人员已知的酶通过pcr、tma、rca、lcr、nasba或sdar进行。在示例性实施方案中,可以通过使用荧光标记的核酸探针或dna嵌入染料以及分子分析仪中的光度计或电荷耦合设备以检测在核酸扩增期间荧光的增加,来实时检测核酸的扩增。这些荧光标记的探针使用本领域技术人员众所周知的检测方案(即,taqmantm,分子信标tm,荧光共振能量转移(fret)探针,scorpiontm探针)并且通常使用荧光猝灭以及猝灭释放或荧光能量从一个报道分子到另一个报道分子的转移以检测具体核酸的合成或存在。
在一个实施方案中,本文公开的组合物用于包括自携式微尺度到大尺度通道、室、储蓄器、检测和处理区域的设备中。该设备可以是药筒、设备、容器或袋,例如,如美国专利nos.6,440,725;6,783,934;6,818,185;6,979,424;8,580,559和8,940,526中所述的,以及诸如可从cepheidcorp.、idahotechnology,inc.和/或biofirediagnostics,inc.获得的那些的设备。
例如,设备可以是自携式核酸分析袋,其包括细胞裂解区、核酸制备区、第一阶段扩增区、第二阶段扩增区,如美国申请公开no.201000056383的图1中所示的。袋包括各种尺寸的多种通道和泡,并且这样布置以使样品通过系统和各个区流动并相应地进行处理。样品处理发生在位于袋内的各种泡中。提供许多通道以在处理区内和处理区之间移动样品,而提供其他通道以将流体和试剂递送到样品或从样品去除这种流体和试剂。袋内的液体通过压力(例如气动压力(pneumaticpressure))在泡之间移动。在这个具体实施方案中,本文所述的组合物提供在内部对照区室中,所述内部对照区室被进行配置以容纳组合物并与一个或其他通道和泡流体连通,从而使得组合物可以掺入样品处理工作流程(workflow)中并相应地进行处理。
在备择的例子中,设备可以是自携式核酸分析药筒,如美国专利no.9,322,052的图3-5和9中所示的。药筒尤其包括多个室,所述多个室包括用于容纳通过入口端口引入的流体样品的样品室、用于容纳洗涤溶液的洗涤室、用于容纳裂解试剂的试剂室、裂解室、用于接收用过的样品和洗涤溶液的废物室、用于容纳中和剂的中和剂室和用于容纳主混合物(例如,扩增试剂和荧光探针)并用于将试剂和探针与从流体样品分离的分析物混合的主混合室、反应容器和检测室。在这个实施方案中,本文所述的组合物提供在内部对照区室中,所述内部对照区室被进行配置以容纳组合物并与一个或其他通道和泡流体连通,从而使得组合物可以掺入样品处理工作流程中并相应地进行处理。
在具体实施方案中,本文所述的方法在样品处理设备中进行,例如美国专利no.7,718,421中所述的样品处理设备。分节设备,例如美国专利no.7,718,421中描述的那些,提供了用于接收、存储、处理和/或分析生物样品的方便容器。在某些实施方案中,分节设备便于涉及多个处理步骤的样品处理规程。在某些实施方案中,可以将样品收集在样品设备中,且然后将该设备置于分析仪中,该分析仪操作该设备及其内容物以处理样品。
特定实施方案包括柔性设备,该柔性设备已通过易碎密封装置分节成区室。各个节段可含有用于处理样品的各种试剂和缓冲液。夹子和调节器可以以各种组合和各种时间控制应用于设备,以引导流体的移动并使易碎密封装置破裂。这种易碎密封装置的破裂可能留下内部设备表面,该内部设备表面基本上没有流体流动的障碍。在一个实施方案中,随着处理的进展,生物样品的流动可以被引导向设备的远端,而废物的流动可能不得不在相反的方向移动,朝向设备的开口,样品在那里最初输入。这个样品入口可以通过具有锁定机构的盖可能永久地密封,并且废物室可以位于盖中以接收废物用于储存。这个方法的显著益处是处理的样品不与已被未处理的样品接触的表面接触。因此,可能涂覆设备壁的存在于未处理的样品中的痕量反应抑制剂不太可能污染处理的样品。
样品处理设备在图2中示出并且可包括透明柔性设备10,其能够被配置成多个节段,例如16、110、120、130、140、150、160、170、180和/或190,并且通过压缩基本上变平。在一个实施方案中,设备可以具有至少两个节段。在一个实施方案中,设备可以具有至少三个节段。柔性设备可提供约2-105℃之间的操作功能(functionality),与样品、靶和试剂的相容性,低透气性,最小荧光性质和/或在重复压缩和弯曲循环期间的弹性。该设备可以由多种材料制备,其实例包括但不限于:聚烯烃,例如聚丙烯或聚乙烯,聚氨基甲酸酯,聚烯烃共聚物和/或提供合适特征的其他材料。
在示例性实施方案中,一种或多种试剂可以作为干物质和/或作为液体溶液储存在设备节段中。在试剂可以以干形式储存的实施方案中,液体溶液可以储存在毗邻的节段中以促进试剂溶液的重构。典型试剂的实例包括:裂解试剂、洗脱缓冲液、洗涤缓冲液、dna酶抑制剂、rna酶抑制剂、蛋白酶抑制剂、螯合剂、中和试剂、离液盐溶液、去污剂、表面活性剂、抗凝剂、萌发剂溶液、异丙醇、乙醇溶液、抗体、核酸探针、肽核酸探针和硫代磷酸酯(phosphothioate)核酸探针。在其中一种试剂是离液盐溶液的实施方案中,优选的组分是异氰酸胍或盐酸胍或其组合。在一些实施方案中,试剂相对于输入样品的开口可以存储在设备中的顺序反映了试剂可以在利用管的方法中使用的顺序。在优选的实施方案中,试剂包含能够特异性结合样品的预选组分的物质。例如,物质可以特异性结合核酸,或核酸探针可以特异性结合具有特定碱基序列的核酸。
通过使用连接到块例如块490的传感器492(图2),例如光度计、分光计、ccd,可以实现对来自设备节段的信号的实时检测。在示例性实施方案中,可以通过调节器392在设备节段190上施加压力以适当地限定设备节段的形状。信号的形式可以是一定波长的光的强度,例如荧光、光谱和/或图像,例如细胞或诸如量子点(quantumdots)的人造元素的图像。对于荧光检测,可以使用来自光学系统的光的激发来照射反应,并且可以通过光度计检测发射光。为了检测具有具体波长的多个信号,可以通过专用检测通道或分光计串联或并联检测不同波长信号。
试剂盒
在一些实施方案中,本文描述的组合物包括在试剂盒或其组件中。本文预期的试剂盒可包括任何制品(例如,包装或容器),包括至少一种用于特异性扩增、捕获、标记/转化或检测如本文所述的靶核酸序列的设备,其中本文所述的组合物包括在设备中或作为单独的试剂盒组件、小瓶或容器提供。试剂盒可以进一步包括使用说明书、补充试剂、对照材料和/或在本文所述的扩增方法或其步骤中使用的组件或模块。一个或多个试剂盒组件可以作为单独的组件包括在试剂盒中,例如,在一起包装的单独的小瓶或容器中,或者一个或多个试剂盒组件可以在相同小瓶或容器中包括在试剂盒中。
这种试剂盒可包括可在样品制备程序过程中使用的组件,例如,96-孔或384-孔形式的微量滴定板或例如由eppendorf,hamburg,德国制造的普通反应管和用于使用本文描述的对照材料进行核酸扩增的所有其他试剂。试剂盒还可包括对核酸具有亲和力的固体支持体,例如具有二氧化硅表面的材料。在一个实施方案中,固体支持体包括例如磁性玻璃颗粒。该试剂盒可以进一步或另外包含蛋白酶试剂和允许细胞裂解的含有例如离液剂、去污剂或醇或其混合物的裂解缓冲液。试剂盒的这些组件可以分别提供在管或储存容器中。取决于组件的特性,这些可以提供在单个管或储存容器中。
试剂盒可以进一步或另外包含洗涤溶液,该洗涤溶液适合于当核酸结合时磁性玻璃颗粒的洗涤步骤。这个洗涤溶液可以在如上所述具有酸性ph的不含乙醇和/或离液剂的一种或多种缓冲的溶液中含有乙醇和/或离液剂。洗涤溶液或其他溶液经常作为母液提供,其在使用前必须稀释。试剂盒可以进一步包含洗脱剂或洗脱缓冲液,即,溶液或缓冲液(例如10mmtris,1mmedta,ph8.0)或纯水,以洗脱与磁性玻璃颗粒结合的核酸。此外,可以存在另外的试剂或缓冲的溶液,其可以用于核酸的纯化。
在具体实施方案中,试剂盒含有具有5'至3'外切核酸酶活性的聚合酶。该试剂盒还可含有具有逆转录酶活性的酶。在另一个实施方案中,试剂盒含有具有5'至3'外切核酸酶活性和逆转录酶活性的聚合酶。
方法和用途
本文所述的组合物可用于分析任何病毒病原体,包括但不限于人免疫缺陷病毒(hiv)、丙型肝炎病毒(hcv)、西尼罗病毒(wnv)、人乳头瘤病毒(hpv)、日本脑炎病毒(jev)、圣·路易脑炎病毒(slev)、流感病毒、诺如病毒等。该组合物还可用于检测其他形式的rna,例如,来自非病毒生物(例如,人、细菌等)的mrna或mirna。在具体实施方案中,所述组合物可用于检测任何hiv致病株,包括hiv-1和hiv-2,及其任何组或亚型,以及肝炎或巨细胞病毒。例如,组合物可以用于分析hiv-1组m、n、o、p及其组合的测定方法。在具体实例中,组合物用于分析hiv-1组m和/或o,以及任选地一个或多个另外的hiv-1组。组合物还可用于分析hiv-1的一个或多个亚型,包括但不限于亚型,a、a1、a2、crf19、b、c、d、f、g、crf02_ag、h、crf04_cpx、j、k及其组合。此外,该方法还可用于检测hiv-2,组a-h,且特别是hiv-2组a和b。此外,还可以使用本文所述的组合物分析肝炎,包括但不限于,甲型肝炎、乙型肝炎或丙型肝炎,且特别地,可以使用本文所述的组合物分析乙型肝炎或丙型肝炎。
实施例
实施例1.在样品处理设备中从全血进行病毒rna分离和检测
rna分离和rna序列检测可以在管1(图2)中完成,包括具有由可剥离密封装置隔开的九个节段并含有预装试剂的柔性设备和具有在其中容纳的废物储蓄器的盖。如本文所述的,通过选择性地接合可操作地连接在设备的一个或多个节段或分段内的一个或多个调节器和夹子来控制从设备的一个节段或分段到另一个节段或分段的流体流动。该设备的第一节段可以接收全血样品。设备的额外节段按以下顺序包含以下组分:
表2.
对于病毒rna分离和检测,将100ul全血加样到第1节段中。然后可以通过盖封闭该设备并将其插入cobas®liat®分析仪(可从rochemolecularsystems,pleasanton,ca获得)中。样品处理可包括以下步骤。
(1)样品裂解。在设备上除第一个夹子外,所有夹子都闭合。与第1段可操作地连接的调节器用于调节血液的体积以在所述节段中保持约100ul,且然后使用关联的节段夹子闭合第1节段。与第2节段可操作地连接的调节器全部或部分地压缩第2节段的第一分段以破坏可剥离密封装置并将对照材料与样品混合。可操作地与第一分段连接的调节器可以交替地压缩所述分段以将对照与样品混合。通过将关联的调节器和夹子接合在该节段/分段中,将样品移动到第3节段,在第3节段上面关闭夹子以防止样品与下游样品混合,且然后移动到第4节段以将裂解缓冲液与样品混合。将第3和第4节段中的混合物于50℃温育2分钟。
(2)核酸捕获。在裂解温育后,调节器交替地压缩它们各自的节段以在室温搅拌并温育混合物达2分钟以促进dna与颗粒的结合。然后,通过该节段附近的磁源产生磁场,以捕获悬浮液中的颗粒。调节器可以交替地压缩节段以捕获颗粒。序贯打开和关闭调节器和夹子以将未结合的样品和废物移动到废物储蓄器。
(3)洗涤。在捕获过程后面是洗涤过程,以从将用于进一步样品处理的颗粒和节段去除残留的碎片和反应抑制剂。使用利用乙醇洗涤缓冲液的基于稀释的洗涤,并且使用利用mes洗涤缓冲液的基于薄层流动的洗涤。首先打开夹子和调节器,且然后调节器关闭以将乙醇缓冲液移动到第5节段,后面是关闭夹子。磁场被去除;调节器和至少一个相邻的调节器交替地靠着它们各自的节段压缩,以产生流动以重悬浮颗粒。然后打开磁场以捕获基本上所有的颗粒,并将液体移动到废物储蓄器中。在完成第一次洗涤之后,将mes洗涤缓冲液从一个节段移动到另一个节段,并且使用相应的调节器和夹子的序贯施加和释放来操作缓冲液,以确保洗涤缓冲液通过流动通道的基本上层流。当洗涤完成时,调节器和夹子关闭,并且基本上所有废物都被移动到废物储蓄器中。
(4)核酸洗脱。使用如前所述的类似方法将洗脱缓冲液从第7节段移动。可以去除磁场并且在第四和第五节段之间的流动下将颗粒重悬浮在洗脱缓冲液中。将颗粒悬浮液于95℃在稳流或搅拌条件下温育2分钟。打开磁场并且基本上所有颗粒都被固定,并且通过序贯地打开和关闭调节器和夹子,可以将洗脱的核酸溶液移动到第7节段。调节器可压缩第7节段以将洗脱的核酸溶液的体积调节至40ul,且夹子然后可靠着设备关闭以完成dna提取过程。
(5)核酸扩增和检测。然后可将核酸溶液转移至第8节段,混合,并与ung280于37℃温育1分钟,以降解可能已存在于生物样品中的任何污染物pcr产物。温育后,可将温度升至95℃以使核酸和ung变性2分钟。然后可将核酸溶液转移至第9节段,并于65℃与rt-pcr试剂混合10分钟,后面是在60℃温育以起始热启动pcr。通过将第8节段设置在95℃并且将第9节段设置在60℃,并通过关闭和打开关联的调节器交替地在节段之间转移反应混合物,可以进行50个循环的95℃达2秒和60℃达15秒的典型2-温度扩增测定。通过将第7节段设置在95℃、将第8节段设置在72℃且将第9节段设置在60℃,并通过关闭和打开关联的调节器交替地在节段中转移反应混合物,可以进行50个循环的95℃达2秒、60℃达10秒和72℃达10秒的典型3-温度扩增测定。光学连接到第9室的检测传感器,例如光度计,可以监控来自报道染料通过设备壁的一部分的实时荧光发射。测定完成后,报告测试结果。
实施例2.使用lightcycler480在样品中进行病毒rna分离和检测
使用lightcycler480(rochemolecularsystems)分析hiv-1m样品(50000cp/ml,roche)。对于样品制备,使用以下试剂作为稀释剂:reservcyt(可从thinprep获得)和k3edta血浆(plasma),pcrneg.(可从roche获得)。
将样品在k3edta血浆中稀释至终浓度为100cp/ml并储存过夜(血浆稀释在-60至-90℃,preservcyt稀释在2-8℃)。
将样品(500ul)和稀释剂(350ul)手动移液到深孔板中,并将分开的样品等分试样加入三个不同的孔中进行三重分析。手动添加内部对照核酸(ф6对照制剂:在10mmtris,ph8.0,0.1mmedta,0.05%叠氮化钠,20mg/l聚rarna,40%甘油中最多到~4e5cp/ml新鲜培养的ф6)的50ul等分试样。样品制备在hamiltonstar(hamilton,bonaduz,ch)上进行,遵循使用以下试剂的根据美国专利no.8,609,340(其公开内容整体引入本文作为参考)的图1中描绘的方案的工作流程:
表3.
在最后的步骤之后,hamiltonstar装置的处理头将各自含有扩增试剂的主混合物(mmxs)添加到每个孔中(例如,美国专利no.8,609,340中公开的mmxs),将含有分离的核酸的流体与mmx混合并将每个得到的混合物转移到微孔板的相应孔中,在其中进行扩增。
为了扩增和检测,用自动板密封器密封微孔板,并将板转移到lightcycler480。使用以下pcr概况:
表4
表5
pcr循环分为两次测量,其中两次测量均应用一步配置(组合退火和延伸)。于55℃的前5个循环通过预扩增略微错配的靶序列而允许增加的包容性,而第二次测量的45个循环通过使用58℃的退火/延伸温度提供增加的特异性。
实施例3.被壳的rna的热稳定性评价
为了测试被壳的rna(arna)的热稳定性,对各批pef070arna进行了应激测试(测试了以下批次:pd6701;rd4675;rd4676;和sv6610)。将预定浓度的每批的等分试样在一定温度范围(4-45℃)储存达延长的时间段。结果示于图3中。在第0天,所有四个批次显示出大约32.5的ct,并且随着时间的过去和增大的温度,可测量的ct迅速下降并且在于45℃截止4周测试的4个批次中的3个中完全丧失。
实施例4.ф6组合物的热稳定性评价
为了测试ф6的热稳定性,对不同缓冲液中纯化的ф6的培养物进行了应激测试。简言之,将预定浓度的全部方法对照的等分试样在一定温度范围(4-45℃)储存达延长的时间段并评价性能(拷贝数维持)。通过qpcr中的ct和幅度测量来测量性能。
为了确立浓度,将ф6连续稀释以产生动态范围,并在cobas®liat®分析仪上计算ct和幅度(n=3)。引物-探针序列和热循环参数的举例说明性实例提供如下:
表6.
表7.
使用约29.5-30.0的ct,将ф6连续稀释到表1中提供的每种缓冲制剂中。将ф6在每种缓冲液中稀释至用于基于rna的cobas®测定的ct范围后,对每种缓冲液条件制备一次性使用的无菌等分试样。然后将这些一次性使用的等分试样储存在设置为4℃、30℃、37℃和45℃的温度监控的培养箱中。
结果示于图4(a)中(下图是ct,且上图是幅度)。结果表明,当使用tris-缓冲液时,ф6噬菌体大大比目前的标准arna稳定得多。此外,添加最多到40%的甘油进一步提高了ф6制剂在研究的加速贮存期限内的热稳定性(参见图4(b))。
序列表
<110>rochediagnosticsgmbh
f.hoffmann-larocheag
rochemolecularsystems,inc.
<120>ф6内部对照组合物、设备和方法
<130>p33787-wo-hs
<150>62/406,166
<151>2016-10-10
<160>3
<170>patentinversion3.5
<210>1
<211>24
<212>dna
<213>人工序列
<220>
<221>来源
<223>/注释=“人工序列描述:合成的探针”
<400>1
tgcgatccgtgtccaagggttcgc24
<210>2
<211>20
<212>dna
<213>人工序列
<220>
<221>来源
<223>/注释=“人工序列描述:合成的引物”
<400>2
gcatttctggagcagtgcat20
<210>3
<211>19
<212>dna
<213>人工序列
<220>
<221>来源
<223>/注释=“人工序列描述:合成的引物”
<400>3
gactgccaaggtgccatta19
- 还没有人留言评论。精彩留言会获得点赞!