6–羟甲基-17α-乙酰氧基-19-去甲孕甾-4,6-二烯-3,20-二酮合成法的制作方法
本发明涉及药物合成领域,具体地,本发明涉及一种6–羟甲基-17α-乙酰氧基-19-去甲孕甾-4,6-二烯-3,20-二酮的合成方法。
背景技术
6–羟甲基-17α-乙酰氧基-19-去甲孕甾-4,6-二烯-3,20-二酮是新型高效口服孕激素诺美孕酮醋酸酯的类似物,也是合成诺美孕酮醋酸酯的工艺中可能出现的另外一个杂质(杂质b)。诺美孕酮醋酸酯作为第四代避孕药具有避孕效果好、毒副作用小、使用方便、安全等特点,已经广泛在欧洲国家应用于避孕、激素替代治疗、子宫内膜异位症、月经异常等各种妇科不适症chinesepharmacologicalbulletin2004,20(11),1215-7;chinesejournalofnewdrugs2011,20(19),1880-1885)。由于6–羟甲基-17α-乙酰氧基-19-去甲孕甾-4,6-二烯-3,20-二酮是诺美孕酮合成中可能产生的杂质,对其需要进行工艺控制和最终产品的检测。由于这个杂质在最终产品中的含量很低,其结构没有被报道,属于新化合物。因此,研究开发一条简单的制备6–羟甲基-17α-乙酰氧基-19-去甲孕甾-4,6-二烯-3,20-二酮的方法、解决其来源作为标准对照品非常重要。
技术实现要素:
本发明的发明目的是提供一种6–羟甲基-17α-乙酰氧基-19-去甲孕甾-4,6-二烯-3,20-二酮的合成方法,解决6–羟甲基-17α-乙酰氧基-19-去甲孕甾-4,6-二烯-3,20-二酮作为标准对照品。
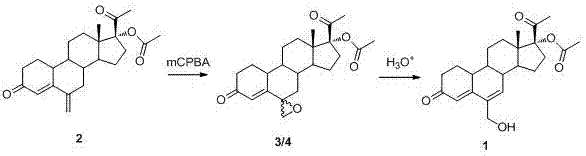
参照图1,本发明的6–羟甲基-17α-乙酰氧基-19-去甲孕甾-4,6-二烯-3,20-二酮的合成方法,包括以下步骤:
1、将6–亚甲基-17α-乙酰氧基-19-去甲孕甾-4-烯-3,20-二酮(2)加入到反应瓶中,加入二氯甲烷使其溶解,再加入间氯过氧苯甲酸,搅拌反应直到原料完全消失,得到环氧化合物3和4混合物,其中,反应物6–亚甲基-17α-乙酰氧基-19-去甲孕甾-4-烯-3,20-二酮和间氯过氧苯甲酸的摩尔比例为1:1~1:5,反应温度为0~40℃。
2、将中间体环氧化合物3和4混合物溶解于thf中,搅拌下加入稀硫酸,直到中间体完全消失,脱水得到产物1,其中,加入的硫酸的浓度为0.1~1n,硫酸和环氧化物的摩尔比例为0.01:1~0.5:1,反应温度为0~50℃。
本发明提供了一种6–羟甲基-17α-乙酰氧基-19-去甲孕甾-4,6-二烯-3,20-二酮的合成方法,6–羟甲基-17α-乙酰氧基-19-去甲孕甾-4,6-二烯-3,20-二酮是诺美孕酮醋酸酯的结构类似物,可能具有相关孕激素类活性,也是合成诺美孕酮工艺中可能带进的杂质。另外,此化合物属于新化合物,文献没有报道。经hplc检测,使用本发明合成的6–羟甲基-17α-乙酰氧基-19-去甲孕甾-4,6-二烯-3,20-二酮,纯度高达99.77%。
附图说明
图1为6–羟甲基-17α-乙酰氧基-19-去甲孕甾-4,6-二烯-3,20-二酮的合成路线反应式。
图2为6–羟甲基-17α-乙酰氧基-19-去甲孕甾-4,6-二烯-3,20-二酮检测结果。
具体实施方式
实施例1
将6–亚甲基-17α-乙酰氧基-19-去甲孕甾-4-烯-3,20-二酮(1.0g,2.7mmol)加入到25ml反应瓶中,加入二氯甲烷(5ml),搅拌溶解,在0℃下加入mcpba(1.0g,5.8mmol)的二氯甲烷(5ml)溶液,升至室温搅拌过夜,将反应液倒入冰水中,二氯甲烷萃取,分别用10%亚硫酸钠水溶液、10%碳酸氢钠水溶液洗涤,无水硫酸镁干燥,抽滤,减压浓缩除去有机溶剂,柱层析分离,得到环氧化产物(0.35g,产率33.3%)。
将上述环氧化合物(0.35g,0.9mmol)加入到10ml的反应瓶中,加入四氢呋喃(5ml),搅拌溶解,降温至0℃左右,加入0.4n硫酸(1ml,0.2mmol),室温搅拌过夜,将反应液倒入冰水中,用二氯甲烷萃取、饱和碳酸氢钠水溶液洗涤、无水硫酸镁干燥,过滤,减压除去有机溶剂,柱层析分离得到白色固体产物6–羟甲基-17α-乙酰氧基-19-去甲孕甾-4,6-二烯-3,20-二酮(0.12g,纯度99.73%@290nm),产率34%,m.p.℃。1hnmr(cdcl3,ppm):δ6.36(s,1h),6.01(s,6.01),4.32-4.33(d,1h),2.96-3.03(dt,1h),2.55-2.59(dd,1h),2.30-2.35(m,3h),2.16-2.22(m,1h),2.09(s,3h),2.06(s,3h),1.93-2.02(m,4h),1.55-1.68(m,4h),1.10-1.47(m,3h),0.72(s,3h)。dept-13cnmr(cdcl3,ppm):δ139.79(c-7),121.43(c-4),62.71(6-ch2-oh),48.54(c-14),45.33(c-9),41.01(c-10),40.89(c-8),37.39(c-2),30.99(c-12),30.30(c-16),26.85(c-1),26.44(c-21),24.93(c-11),23.18(c-15),21.18(17-ococh3),14.19(c-18)。ms(esi):387.3(m+h)。
实施例2
将6–亚甲基-17α-乙酰氧基-19-去甲孕甾-4-烯-3,20-二酮(1.0g,2.7mmol)加入到25ml反应瓶中,加入二氯甲烷(5ml),搅拌溶解,室温下加入mcpba(2.0g,11.6mmol)的二氯甲烷(5ml)溶液,室温搅拌1小时,加热回流反应2小时,将反应液倒入冰水中,二氯甲烷萃取,分别用10%亚硫酸钠水溶液、10%碳酸氢钠水溶液洗涤,无水硫酸镁干燥,抽滤,减压浓缩除去有机溶剂,得到环氧化产物粗品后直接加入到10ml的反应瓶中,溶解于四氢呋喃(10ml),降温至0℃,加入1n硫酸(0.5ml),升至室温搅拌1小时,加热至50℃反应3小时,将反应液倒入冰水中,用二氯甲烷萃取、饱和碳酸氢钠水溶液洗涤、无水硫酸镁干燥,过滤,减压除去有机溶剂,柱层析分离得到白色固体产物6–羟甲基-17α-乙酰氧基-19-去甲孕甾-4,6-二烯-3,20-二酮(0.37g,纯度99.5%@290nm),两步总产率35%。
实施例3
将6–亚甲基-17α-乙酰氧基-19-去甲孕甾-4-烯-3,20-二酮(1.0g,2.7mmol)加入到25ml反应瓶中,加入二氯甲烷(5ml),搅拌溶解,室温下加入mcpba(0.5g,2.9mmol)的二氯甲烷(5ml)溶液,搅拌加热回流过夜,将反应液倒入冰水中,二氯甲烷萃取,分别用10%亚硫酸钠水溶液、10%碳酸氢钠水溶液洗涤,无水硫酸镁干燥,抽滤,减压浓缩除去有机溶剂,得到环氧化产物粗品后直接加入到10ml的反应瓶中,溶解于四氢呋喃(10ml),降温至0℃,加入0.1n硫酸(2ml),室温搅拌1小时候,在35-40℃下反应2小时,将反应液倒入冰水中,用二氯甲烷萃取、饱和碳酸氢钠水溶液洗涤、无水硫酸镁干燥,过滤,减压除去有机溶剂,柱层析分离得到白色固体产物6–羟甲基-17α-乙酰氧基-19-去甲孕甾-4,6-二烯-3,20-二酮(0.29g,纯度98.8%@290nm),两步总产率28%。
实施例4
将6–亚甲基-17α-乙酰氧基-19-去甲孕甾-4-烯-3,20-二酮(1.0g,2.7mmol)加入到25ml反应瓶中,加入二氯甲烷(5ml),搅拌溶解,室温下加入mcpba(1.5g,8.7mmol)的二氯甲烷(5ml)溶液,室温下搅拌反应1小时,加热回流反应2小时,将反应液倒入冰水中,二氯甲烷萃取,分别用10%亚硫酸钠水溶液、10%碳酸氢钠水溶液洗涤,无水硫酸镁干燥,抽滤,减压浓缩除去有机溶剂,得到环氧化产物粗品后直接加入到10ml的反应瓶中,溶解于四氢呋喃(10ml),降温至0℃,加入0.6n硫酸(2ml),室温搅拌1小时候,加热回流搅拌2小时,将反应液倒入冰水中,用二氯甲烷萃取、饱和碳酸氢钠水溶液洗涤、无水硫酸镁干燥,过滤,减压除去有机溶剂,柱层析分离得到白色固体产物6–羟甲基-17α-乙酰氧基-19-去甲孕甾-4,6-二烯-3,20-二酮(0.33g,纯度99.3%@290nm),两步总产率32%。
- 还没有人留言评论。精彩留言会获得点赞!