特异性检测氰根的试剂及其合成方法和应用与流程
本发明涉及一种特异性检测氰根的试剂及其合成方法和应用。
背景技术
氰阴离子在阴离子识别领域受到广泛关注,因为它对人体健康非常有害,可以通过口腔,呼吸道或皮肤吸收到体内,导致惊厥,呕吐,意识丧失和最终死亡。氰化物的主要中毒机制是氰化物进入人体血液循环后,与细胞色素氧化酶fe3+发生络合作用,导致fe3+传递电子,阻断呼吸链,导致缺氧所致的死亡。值得注意的是氰化物离我们不远。它有各种来源,如生产事故,药品,火灾烟雾,甚至一些食物。然而,氰化物在许多领域中被广泛使用。例如,氰化物广泛用于冶金工业中的金矿开采和电镀。此外,氰化物在合成农药和农药等重要原料时也是不可或缺的。因此,开发一种快速高效的氰化物检测方法对环境监测和食品分析非常重要。
目前,大部分荧光探针使用荧光增强型实现氰根的检测,检测限较高。因此研究开发一种信号响应明显且检测限低的、可以在细胞浓度水平上检测氰根的试剂显得尤为重要。
技术实现要素:
本发明的目的是提供一种操作方便、选择性好、灵敏度高的检测氰根的bodipy衍生物及其制备方法。在本发明中,合成了一种基于bodipy的化合物,通过氰根和化合物在亲核加成反应前后荧光强度的比率变化,实现氰根的特异性检测。
本发明提供了一种氟硼二吡咯(bodipy)衍生物,结构式为:
本发明还提供了上述氟硼二吡咯(bodipy)衍生物的合成方法,包括以下步骤:将摩尔比为1:2的对甲氧基苯甲醛和2,4-二甲基吡咯溶于无水二氯胺,再加三氟乙酸(tfa),搅拌混合物,之后加入二氯二氰基苯醌并继续搅拌,然后加入三乙胺,后滴加三氟化硼乙醚,反应得到粗产物;所述粗产物通过柱色谱法纯化以获得第一化合物;向所述第一化合物在四氢呋喃(thf)/水中的溶液中滴加二氯二氰基苯醌溶液,其中四氢呋喃与水的体积比为100:1,在氩气保护下,将溶液在0℃下储存4小时后,将反应混合物的温度缓慢升至室温,将反应混合物放置过夜,通过加入水骤冷,所得混合物用二氯甲烷萃取并用水洗涤,使用柱色谱法进一步纯化,用乙酸乙酯/石油醚的混合物洗脱得到第二化合物,其中乙酸乙酯与石油醚的体积比为1:6;将第二化合物和1,3,3-三甲基-3h-吲哚鎓盐溶于苯中,在氩气保护下搅拌并回流,反应后,过滤,用乙醇洗涤,干燥得到黑色固体,为氟硼二吡咯(bodipy)衍生物。
本发明还提供了上述氟硼二吡咯(bodipy)衍生物在氰根检测中的应用。
本发明还提供了一种检测氰根的方法,包括以下步骤:(1)、配制ph=7.4、浓度为10mm的pbs缓冲溶液,并用二甲基亚砜配制2mm(e)-2-(2-(5,5-二氟-10-(4-甲氧基苯基)-1,7,9三甲基-5h-4λ4,5λ4二吡咯并[1,2-c:2',1'-f][1,3,2]二氮杂硼砂-3-基)乙烯基)-1-乙基-3,3-二甲基-3h-吲哚-1-鎓的二甲基亚砜溶液;(2)、按体积比1:1将pbs缓冲溶液和乙腈溶液加到2ml荧光比色皿中,在荧光分光光度仪上检测,随着待测样的加入,646nm处的荧光强度的逐渐降低,伴随着542nm荧光强度显著增强;(3)、用蒸馏水配制20mm的氰根溶液,按体积比1:1将pbs缓冲溶液和乙腈溶液加到2ml荧光比色皿中,逐渐加入氰根溶液的体积为0、3、6、9、12、15、18μl,同时在荧光光谱仪上测定542nm处与646nm处相对荧光强度的比值i542/i646为0.705、1.970、4.134、11.263、32.964、76.852、97.833,以氰根浓度为横坐标,以相对荧光强度比值i542/i646为纵坐标绘制图,得到氰根浓度c的工作曲线;线性回归方程为:f542/f646=2.45c+1.25,c的单位为10-5mol/l;(4)、测定样品溶液时,将测得的荧光强度代入线性回归方程,即可求得氰根浓度c。
与现有技术相比,本发明具有如下优点和效果:
1、所述bodipy衍生物的合成简单,操作方便;
2、所述检测方法能实现氰根的特异性检测,显示了高的灵敏性和极好的选择性;
3、检测手段简单,只需要借助荧光光谱仪即可实现;
4、检测信号明显,为比率型荧光。
附图说明
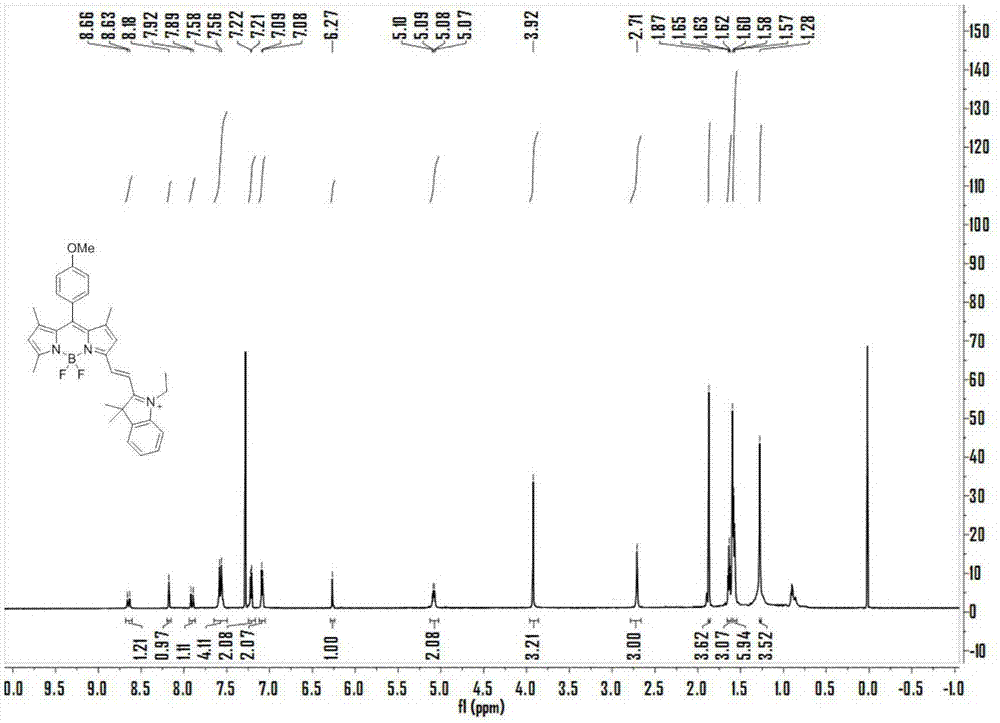
图1示出了实施例1制备的探针1的核磁氢谱图。
图2示出了实施例1制备的探针1的核磁碳谱图。
图3示出了实施例1制备的探针1的质谱图。
图4示出了实施例2中的探针1与氰根作用的荧光发射图。
图5示出了实施例3中的探针1与各种分析物的荧光柱状图。
图6示出了实施例4中的探针1测定氰根的工作曲线。
图7示出了实施例5中的探针1测定样品的荧光发射图。
图8示出了实施例6中的细胞成像图。
具体实施方式
下面结合实施例和附图对本发明做进一步说明,但本发明不受下述实施例的限制。
本发明提供的一种bodipy衍生物,中文名称为1-(4-叠氮基苄基)-4-(5,5-二氟-1,3,7,9四甲基-5h-4λ4,5λ4二吡咯并[1,2-c:2',1'-f]的[1,3,2]二氮杂硼砂-10-基)吡啶-1-鎓,英文名称为1-(4-azidobenzyl)-4-(5,5-difluoro-1,3,7,9-tetramethyl-5h-4λ4,5λ4-dipyrrolo[1,2-c:2',1'-f][1,3,2]diazaborinin-10-yl)pyridin-1-ium,命名为探针1。结构式为:
探针1的合成方法,步骤为:
1)将摩尔比为1:2的对甲氧基苯甲醛和2,4-二甲基吡咯溶于无水二氯胺,再加三氟乙酸(tfa),搅拌混合物。加入二氯二氰基苯醌(ddq)并继续搅拌,然后加入三乙胺,后滴加三氟化硼乙醚。粗产物通过柱色谱法纯化以获得橙色结晶固体化合物1。向化合物2在四氢呋喃(thf)/h2o(v/v=100/1)中的溶液滴加溶于thf的ddq溶液,在氩气保护下。将溶液在0℃下储存4小时后,将反应混合物的温度缓慢升至室温,将反应混合物放置过夜,通过加入水骤冷。所得混合物用二氯甲烷萃取并用水洗涤。使用柱色谱法进一步纯化粗产物,用(乙酸乙酯/石油醚v/v=1:6)混合物洗脱得到化合物2,为橙色固体。
2)将化合物2和1,3,3-三甲基-3h-吲哚鎓盐溶于苯中,在氩气保护下搅拌并回流,反应后,过滤,用乙醇洗涤,干燥得到黑色固体,为所需产物探针1。
本发明还提供了一种检测氰根的方法,步骤为:
(1)、配制ph=7.4、浓度为10mm的pbs缓冲溶液,并用二甲基亚砜(dmso)配制2mm(e)-2-(2-(5,5-二氟-10-(4-甲氧基苯基)-1,7,9三甲基-5h-4λ4,5λ4二吡咯并[1,2-c:2',1'-f][1,3,2]二氮杂硼砂-3-基)乙烯基)-1-乙基-3,3-二甲基-3h-吲哚-1-鎓的dmso溶液;
(2)、按体积比1:1将pbs缓冲溶液和乙腈溶液加到2ml荧光比色皿中,在荧光分光光度仪上检测,随着待测样的加入,646nm处的荧光强度的逐渐降低,伴随着542nm荧光强度显著增强;
(3)、用蒸馏水配制20mm的氰根(由nacn配置)溶液,按体积比1:1将pbs缓冲溶液和乙腈溶液加到2ml荧光比色皿中,逐渐加入氰根溶液的体积为0、3、6、9、12、15、18μl,同时在荧光光谱仪上测定542nm处与646nm处相对荧光强度的比值i542/i646为0.705、1.970、4.134、11.263、32.964、76.852、97.833,以氰根浓度为横坐标,以相对荧光强度比值i542/i646为纵坐标绘制图,得到氰根浓度c的工作曲线;线性回归方程为:f542/f646=2.45c+1.25,c的单位为10-5mol/l;
(4)、测定样品溶液时,将测得的荧光强度代入线性回归方程,即可求得氰根的浓度。
实施例1
探针1的制备和表征
将摩尔比为1:2.175的对甲氧基苯甲醛(0.545g,4mmol)和2,4-二甲基吡咯(0.833g,8.7mmol)溶于无水二氯胺(300ml),再加三氟乙酸(tfa)(1ml),搅拌混合物。加入二氯二氰基苯醌(0.98g,4mmol)并继续搅拌4h,然后加入三乙胺(9ml),15min后滴加三氟化硼乙醚(9ml)。粗产物通过柱色谱法纯化以获得橙色结晶固体化合物1。向化合物1(142mg,0.4mmol)在8mlthf/h2o(v/v=100/1)中滴加溶于thf的ddq溶液(360mg,1.58mmol),在氩气保护下。将溶液在0℃下储存4小时后,将反应混合物的温度缓慢升至室温,将反应混合物放置过夜,通过加入水(20ml)骤冷。所得混合物用二氯甲烷萃取并用水洗涤。使用柱色谱法进一步纯化粗产物,用(乙酸乙酯/石油醚v/v=1:6)混合物洗脱得到化合物2,为橙色固体。
2)将化合物2(80mg,0.22mmol)和1,3,3-三甲基-3h-吲哚鎓盐(70mg,0.22mmol)溶于20ml苯中,在氩气保护下搅拌并回流反应4h后,过滤,用乙醇洗涤,干燥得到黑色固体,为所需产物探针1。
1hnmr(600mhz,cdcl3):δ8.66(d,j=18hz,1h),8.18(s,1h),7.92(s,j=18hz,1h),7.58(d,j=12hz,4h),7.22(d,j=6hz,2h),7.09(d,j=6hz,2h),6.27(s,1h),5.10(m,j=18hz,2h),3.92(s,3h),2.71(s,3h),1.87(s,3h),1.65(m,j=18hz,3h),1.60(m,j=18hz,6h),1.28(s,3h)(图1).13cnmr(150mhz,cdcl3):δ180.1,165.8,160.8,149.8,143.6,143.1,142.3,140.6,130.9,129.6,128.8,125.7,125.3,122.7,115.0,114.2,113.2,55.4,51.9,44.2,29.7,27.1,22.7,19.2,15.7,15.4,14.5,14.1(图2).esi-msm/z:[m]+calcdfor538.2836;found538.2837(图3)。
实施例2
配制ph=7.4、浓度为10mm的pbs缓冲溶液,并用dmso配制2mm探针1溶液;把20μl探针1的dmso溶液加入到2mlmecn:pbs(10mm,ph=7.4,1:1,v/v)的荧光比色皿中,取氰根溶液,逐渐用微量进样器加到此比色皿中,边加样边在荧光分光光度仪上检测,随着氰根的加入,646nm处荧光强度降低,并伴随着542nm处荧光强度逐渐增强。荧光发射图见图4。
实施例3
配制ph=7.4、浓度为10mm的pbs缓冲溶液,并用dmso配制2mm的探针1溶液;在20个荧光比色皿中,各加入2ml的mecn:pbs(10mm,ph=7.4,1:1,v/v)溶液和20μl探针1的dmso溶液,再分别加入3摩尔当量氰根,以及30摩尔当量的各种分析物:cys,hcy,gsh,f-,cl-,br-,no3-,n3-,hso3-,aco-,co32-,hco3-,s2-,scn-,clo4-,so42-,hpo42-,h2po42-,no2-在荧光分光光度仪上检测,绘制不同分析物对应的542nm处和646nm处相对荧光强度比值的柱状图,(见图5)。氰根使得探针1在542nm处和646nm的荧光强度明显变化,其它的分析物基本没有引起明显的荧光变化。
实施例4
配制ph=7.4、浓度为10mm的pbs缓冲溶液,用蒸馏水配制20mm的氰根溶液,分别将2mlmecn:pbs(10mm,ph=7.4,1:1,v/v)溶液加到在7个比色皿中,逐渐加入氰根溶液的体积为0、5、10、15、20、25、30μl,同时在荧光光谱仪上测定542nm处与646nm处相对荧光强度的比值i542/i646为0.705、1.970、4.134、11.263、32.964、76.852、97.833,以氰根浓度为横坐标,以相对荧光强度比值i542/i646为纵坐标绘制图,得到氰根浓度c的工作曲线;线性回归方程为:f542/f646=2.45c+1.25,c的单位为10-5mol/l;见图6。
实施例5
配制ph=7.4、浓度为10mm的pbs缓冲溶液,并用dmso配制2mm探针1溶液;把20μl探针1的dmso溶液加入到2mlmecn:pbs(10mm,ph=7.4,1:1,v/v)溶液的荧光比色皿中,取氰根的溶液24μl,用微量进样器加到此比色皿中,同时在荧光光谱仪上测定542nm和646nm处荧光强度为1249和21,542nm处与646nm处相对荧光强度的比值(i542/i646)为49.476,通过实施例4的线性回归方程,求得c=23.8×10-5mol/l。偏差为0.8%。见图7。
实施例6
用dmso配制2mm的探针1dmso溶液;将探针dmso溶液加入hepg-2细胞培养液中,使得其浓度为10μm,与hepg-2细胞在37℃下孵育30分钟。此时体系在共聚焦显微镜红色通道中显示出红色荧光,而绿色通道只有很微弱的绿色荧光。分别将50μm、100μm、150μm氰根溶液与上述预处理过的hepg-2细胞再孵育30分钟后,此时体系在共聚焦显微镜绿色通道显示强烈的绿色荧光,而红色通道的荧光基本消失,见图8。
本领域技术人员应理解,以上实施例仅是示例性实施例,在不背离本申请的精神和范围的情况下,可以进行多种变化、替换以及改变。
- 还没有人留言评论。精彩留言会获得点赞!