多代减数分裂雌核发育团头鲂的遗传多样性鉴定方法及试剂与流程
本发明属于鱼类养殖领域,更具体地,本发明涉及多代减数分裂雌核发育团头鲂的遗传多样性鉴定方法及试剂。
背景技术:
人工雌核发育是一种有效的产生纯系的手段,而且在鱼类染色体操作、遗传分析以及性别控制等方面具有潜在的应用价值。迄今为止,各国学者已先后在鲤科、鲑科、鲽科、鳅科和鲷科等近百种重要经济鱼类开展雌核发育研究并获得成功,在一些重要水生模式动物如青鳉和斑马鱼等也有成功先例。
团头鲂“浦江1号”是养殖性能优良的草食性鱼类首例选育良种,为使该良种的优良性状基因进一步纯化、巩固和发展,自1999年以来,上海海洋大学水产种质资源研究室先后对团头鲂“浦江1号”选育系f5和f6进行了人工雌核发育(抑制第二次成熟分裂)的研究,成功地生产了一定数量的雌核发育鱼(g1);随后,他们又通过抑制一次雌核发育鱼(g1)卵子的第二次成熟分裂成功地诱导出两次雌核发育鱼(g2),在g2的基础上,用同样的方法诱导得到连续3次减数分裂雌核发育鱼(g3)。近几年的养殖实践证明,这些雌核发育团头鲂(g1、g2、g3)及其后代具有很好的生长优势,其生长速度超过了团头鲂选育系。但是,在实际的育种过程中,不同雌核发育世代团头鲂群体的遗传纯合度的具体指标如何,是否能达到遗传育种和遗传分析所需要的纯合度?此外,在雌核发育过程中可能由于经过辐射处理的异源精子的某些未失活遗传物质的影响、物理隔离的不完善等因素而影响雌核发育鱼群体的遗传纯合性。因此,在将培育的雌核发育群体应用于育种实践前,需要用各种技术在分子水平上对其基因组进行精确的遗传学分析,以确定雌核发育类型鱼类群体的遗传纯合度是否能达到遗传育种的要求。另外,由于雌核发育团头鲂在形态上和普通团头鲂完全一致,从外形上无法鉴别普通团头鲂与雌核发育团头鲂(g1、g2、g3),这导致这几种鱼(团头鲂“浦江1号”、g1、g2、g3)在养殖生产和选育过程中极易混杂,为下一步的纯系选育工作埋下了隐患。
鉴于此,找到合适的评估不同雌核发育团头鲂群体的遗传多样性和遗传纯合度的工具,开发出能够有效区分不同团头鲂群体(团头鲂“浦江1号”、g1、g2、g3)的特异性分子标记已成为迫切需要解决的问题。
技术实现要素:
本发明的目的在于提供了多代减数分裂雌核发育团头鲂的遗传多样性鉴定方法及试剂。
在本发明的第一方面,提供一种特异性鉴定团头鲂(megalobramaamblycephala)连续2~3次减数分裂雌核发育鱼的方法,所述方法包括:以特异性的引物作为分子标记,对待测鱼样品进行pcr扩增,根据扩增产物的dna片段大小确定团头鲂连续2~3次减数分裂雌核发育鱼;其中,所述的特异性引物选自:seqidno:3(s3)、seqidno:19(s40)、seqidno:24(s58)、seqidno:32(71)、seqidno:36(s75)。
在本发明的另一方面,提供分子标记的应用,用于特异性鉴定团头鲂连续2~3次减数分裂雌核发育鱼,或用于制备特异性鉴定团头鲂连续2~3次减数分裂雌核发育鱼的试剂盒;其中,所述的分子标记包括选自下组的引物或其组合:seqidno:3、seqidno:19、seqidno:24、seqidno:32、seqidno:36。
在另一优选例中,所述的方法或应用中,若以seqidno:3为引物且扩增产物中存在136bp片段,则该待测鱼为团头鲂连续3次减数分裂雌核发育鱼。
在另一优选例中,所述的方法或应用中,若以seqidno:3为引物且扩增产物中不存在797bp片段,则该待测鱼为团头鲂连续3次减数分裂雌核发育鱼。
在另一优选例中,所述的方法或应用中,若以seqidno:19为引物且扩增产物中存在780bp片段,则预期该待测鱼为团头鲂连续3次减数分裂雌核发育鱼;较佳地,可进一步通过seqidno:3为引物的扩增来进一步确定。
在另一优选例中,所述的方法或应用中,若以seqidno:24为引物且扩增产物中不存在439bp片段,则预期该待测鱼为团头鲂连续3次减数分裂雌核发育鱼;较佳地,可进一步通过seqidno:3为引物的扩增来进一步确定。
在另一优选例中,所述的方法或应用中,若以seqidno:36为引物且扩增产物中不存在313bp片段,则预期该待测鱼为团头鲂连续3次减数分裂雌核发育;较佳地,可进一步通过seqidno:3为引物的扩增来进一步确定)。
在另一优选例中,所述的方法或应用中,若以seqidno:32为引物且扩增产物中不存在504bp片段,则预期该待测鱼为团头鲂连续2次减数分裂雌核发育鱼。
在另一优选例中,所述的待测鱼为团头鲂“浦江1号”选育系f9,其连续1次减数分裂雌核发育鱼g1,连续2次减数分裂雌核发育鱼g2,连续3次减数分裂雌核发育鱼g3。
在另一优选例中,所述的待测鱼样品为来自活鱼的组织样品,或为鱼类加工产物,如食品、保健品。
在本发明的另一方面,提供用于特异性鉴定团头鲂连续2~3次减数分裂雌核发育鱼的分子标记,包括选自下组的引物或其组合:seqidno:3、seqidno:19、seqidno:24、seqidno:32、seqidno:36。
在本发明的另一方面,提供一种用于特异性鉴定团头鲂连续2~3次减数分裂雌核发育鱼的试剂盒,该试剂盒中包括:容器,以及分装于容器中的所述的分子标记。
在另一优选例中,所述试剂盒中还包括选自以下的试剂:dna提取试剂,pcr缓冲液,dna聚合酶,和/或说明特异性鉴定团头鲂连续2~3次减数分裂雌核发育鱼的方法的使用说明书。
在本发明的另一方面,提供一种对团头鲂及其减数分裂雌核发育鱼进行遗传分析(包括群体内或群体间的遗传分析)的方法,所述方法包括:以特异性的引物组分别对待测鱼样品进行pcr扩增,获取扩增产物,对扩增产物进行群体内或群体间遗传变异分析,从而确定团头鲂及其减数分裂雌核发育鱼的遗传变异情况;其中,所述的特异性引物组包括seqidno:1~seqidno:39的引物。
在另一优选例中,所述的遗传变异分析包括选自下组的参数:多态位点数、多态位点比例、shannon信息指数、遗传相似系数、遗传距离、遗传分化指数。
在另一优选例中,所述的遗传变异情况包括:遗传多样性水平,平均遗传相似情况,遗传纯度,遗传分化水平。
在本发明的另一方面,提供用于对团头鲂及其减数分裂雌核发育鱼进行遗传分析的特异性引物组,包括seqidno:1~seqidno:39的引物。
在本发明的另一方面,提供用于对团头鲂及其减数分裂雌核发育鱼进行遗传分析的特异性引物组的试剂盒,包括:容器,以及分装于容器中的所述的引物组。
在另一优选例中,所述试剂盒中还包括选自以下的试剂:dna提取试剂,pcr缓冲液,dna聚合酶,和/或说明对团头鲂及其减数分裂雌核发育鱼进行遗传分析的方法的使用说明书。
在本发明的另一方面,提供所述的引物组或所述的试剂盒的用途,用于对团头鲂及其减数分裂雌核发育鱼进行遗传分析。
本发明的其它方面由于本文的公开内容,对本领域的技术人员而言是显而易见的。
附图说明
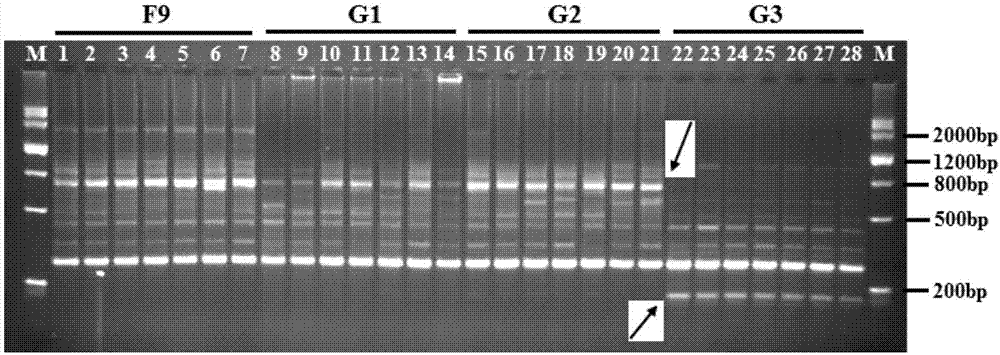
图1、引物s3在4个群体中的扩增图谱(箭头示特异dna片段)。其中,m:markerⅲ(200bp,500bp,800bp,1200bp,2000bp,3000bp,4500bp)。
图2、引物s40在4个群体中的扩增图谱(箭头示特异dna片段)。其中,m:markerⅲ(200bp,500bp,800bp,1200bp,2000bp,3000bp,4500bp)。
图3、引物s58在4个群体中的扩增图谱(箭头示特异dna片段)。其中,m:markerⅲ(200bp,500bp,800bp,1200bp,2000bp,3000bp,4500bp)。
图4、引物s71在4个群体中的扩增图谱(箭头示特异dna片段)。其中,m:markerⅲ(200bp,500bp,800bp,1200bp,2000bp,3000bp,4500bp)
图5、引物s75在4个群体中的扩增图谱(箭头示特异dna片段)。其中,m:markerⅲ(200bp,500bp,800bp,1200bp,2000bp,3000bp,4500bp)。
图6、基于群体间遗传距离的4个团头鲂群体间nj聚类图(a)和upgma聚类图(b)。
具体实施方式
为评估不同雌核发育团头鲂群体(g1、g2、g3)的遗传多样性和遗传纯合度,鉴别不同团头鲂群体(团头鲂g1、g2、g3),本发明以普通团头鲂(团头鲂“浦江1号”选育系f9)群体作为对照,对连续三代人工雌核发育团头鲂群体(g1,g2,g3)进行基因组分析。确定了不同雌核发育团头鲂群体的遗传多样性和遗传纯合度,进而从分子水平评估连续多代人工减数分裂雌核发育的效果;同时,获得了区分不同团头鲂育种群体(团头鲂“浦江1号”选育系f9、g1、g2、g3)的稳定的分子遗传标记。基于此建立了团头鲂雌核发育群体的分子鉴别技术。
分子标记
尽管团头鲂基因组较为复杂,但是本发明人通过大量比较和反复分析验证,以及对与团头鲂接近的其它物种在基因层面的比较和筛选,获得了一系列可用于对团头鲂及其减数分裂雌核发育鱼进行遗传分析的引物,构成进行遗传分析的特异性引物组。同时,本发明人还获得了特异性地鉴定团头鲂连续2~3次减数分裂雌核发育鱼的分子标记。
一个方面,本发明提供了特异性地鉴定团头鲂连续2~3次减数分裂雌核发育鱼的分子标记,包括选自下组的引物或其组合:seqidno:3、seqidno:19、seqidno:24、seqidno:32、seqidno:36。其中,seqidno:3、seqidno:19、seqidno:24、seqidno:36可被单独或组合应用,鉴定出团头鲂连续3次减数分裂雌核发育鱼;seqidno:32的引物,可被应用于鉴定出团头鲂连续2次减数分裂雌核发育鱼。
另一个方面,本发明提供了对团头鲂及其减数分裂雌核发育鱼进行遗传分析的特异性引物组,包括seqidno:1~seqidno:39的引物。这些引物的组合应用,可确定团头鲂及其减数分裂雌核发育鱼的遗传变异情况,进行遗传多样性水平,平均遗传相似情况,遗传纯度,遗传分化水平等方面的分析。
根据鉴定方法的需要,本发明的上述引物还可以用放射性同位素、生物素、酶、荧光素或其他化学发光物质进行标记。
鉴定方法
基于本发明人的新发现,本发明提供了一种特异性鉴定团头鲂连续2~3次减数分裂雌核发育鱼的方法,包括:以特异性的引物作为分子标记,对待测鱼样品进行pcr扩增,根据扩增产物的dna片段大小,鉴定出团头鲂连续2~3次减数分裂雌核发育鱼;其中,所述的特异性引物选自:seqidno:3、seqidno:19、seqidno:24、seqidno:32、seqidno:36。
具体地,若以seqidno:3为引物且扩增产物中存在136bp片段,则该待测鱼为团头鲂连续3次减数分裂雌核发育鱼;若以seqidno:3为引物且扩增产物中不存在797bp片段,则该待测鱼为团头鲂连续3次减数分裂雌核发育鱼;若以seqidno:19为引物且扩增产物中存在780bp片段,则预期该待测鱼为团头鲂连续3次减数分裂雌核发育鱼;若以seqidno:24为引物且扩增产物中不存在439bp片段,则预期该待测鱼为团头鲂连续3次减数分裂雌核发育鱼;若以seqidno:36为引物且扩增产物中不存在313bp片段,则预期该待测鱼为团头鲂连续3次减数分裂雌核发育鱼;和/或,若以seqidno:32为引物且扩增产物中不存在504bp片段,则预期该待测鱼为团头鲂连续2次减数分裂雌核发育鱼。
利用本发明的选自seqidno:3、seqidno:19、seqidno:24、seqidno:32、seqidno:36的引物,只需进行pcr反应和/或琼脂糖凝胶电泳,就可以准确、快速地判断待测样品团头鲂连续2~3次减数分裂雌核发育鱼,灵敏度非常高。
在本发明的具体实施例中,结果表明,5条引物在群体间产生了特异dna片段,其中,4条引物(s3、s40、s58和s75)可区分g3群体和其它3个群体(f9、g1和g2),引物s3的鉴别可靠性最高;仅1条引物(s71)可区分g2群体和其它3个群体(f9、g1和g3)。
本发明还提供了一种对团头鲂及其减数分裂雌核发育鱼进行遗传分析的方法,包括:以特异性的引物组分别对待测鱼样品进行pcr扩增,获取扩增产物,对扩增产物进行群体内或群体间遗传变异分析,从而确定团头鲂及其减数分裂雌核发育鱼的遗传变异情况;其中,所述的特异性引物组包括seqidno:1~seqidno:39的引物。
获取待测样品的dna的方法是本领域技术人员所熟知的技术,例如可采取传统的酚/氯仿/异戊醇法,或者可采用一些商购的dna提取试剂盒,这类试剂盒是本领域技术人员熟知的。
聚合酶链反应(pcr)技术是本领域技术人员熟知的技术,其基本原理是体外酶促合成特异dna片段的方法。本发明的方法可采用常规的pcr技术进行。
本发明的方法针对的待测鱼样品没有特别的限制,可以为来自团头鲂活鱼的组织样品,或为鱼类加工产物,如食品、保健品。
在本发明的具体实施例中,39条引物在f9、g1、g2和g3群体中扩增条带总数分别为213条、202条、200条和190条,f9、g1、g2和g3群体的多态位点比例分别为36.15%、35.64%、27.00%和26.84%,f9、g1、g2和g3群体的shannon信息指数分别为0.2079、0.1857、0.1461和0.1383。3个雌核发育群体的遗传多样性水平(多态位点比例、shannon信息指数)均明显低于对照组f9群体,随着雌核发育世代数的增加,遗传多样性水平呈现逐代降低的趋势,即:g1>g2>g3。4个群体的群体内个体间的平均遗传相似系数为0.8285~0.9060,3个雌核发育群体的群体内个体间平均遗传相似系数均明显高于对照组f9群体;群体内个体间的平均遗传相似系数呈现随雌核发育世代数的增加而升高的趋势,即:g3>g2>g1。群体间成对fst值为0.2692~0.4195,经置换检验得到的fst值的p值为0.0000~0.0090,均达到极显著水平(p<0.01),表明4个群体间存在极显著的遗传分化。
本发明结果表明,连续多代的人工减数分裂雌核发育诱导已对团头鲂育种群体产生如下两个方面的影响:一方面,遗传多样性明显降低,并呈现逐代降低的趋势;另一方面,遗传纯度明显升高,并呈现逐代升高的趋势。连续多代减数分裂雌核发育能显著加快团头鲂基因的纯合速度,雌核发育三代群体(g3)已经是一个遗传一致性较高的高纯品系。
试剂盒
本发明还提供了一种用于特异性鉴定团头鲂连续2~3次减数分裂雌核发育鱼的试剂盒,包括:容器,以及分装于容器中的所述的分子标记,即选自seqidno:3、seqidno:19、seqidno:24、seqidno:32、seqidno:36的引物。
本发明还提供了一种用于对团头鲂及其减数分裂雌核发育鱼进行遗传分析的特异性引物组的试剂盒,包括:容器,以及分装于容器中的所述的特异性引物组包括seqidno:1~seqidno:39的引物。
此外,所述的试剂盒还可含有其它辅助试剂,包括如(但不限于):
(a)各种pcr反应用试剂,例如但不限于:pcr缓冲液,dntps,dna聚合酶等;或
(b)各种提取dna(即制备pcr反应模板)所需的试剂,例如但不限于:酚、氯仿、异戊醇、nacl等;或
(c)提取dna的试剂盒。
此外,所述的试剂盒中还可含有说明特异性鉴定团头鲂连续2~3次减数分裂雌核发育鱼的方法的使用说明书和/或标准操作程序;或说明对团头鲂及其减数分裂雌核发育鱼进行遗传分析的方法的使用说明书和/或标准操作程序。本发明所述的试剂盒可实现快速检测、批量检测团头鲂的目的。
下面结合具体实施例,进一步阐述本发明。应理解,这些实施例仅用于说明本发明而不用于限制本发明的范围。下列实施例中未注明具体条件的实验方法,通常按照常规条件如j.萨姆布鲁克等编著,分子克隆实验指南,第三版,科学出版社,2002中所述的条件,或按照制造厂商所建议的条件。
i.材料与方法
生物材料
对照组团头鲂选育系群体样本为“浦江1号”选育系f9群体,试验组为团头鲂一代雌核发育群体(g1)、团头鲂连续两代雌核发育群体(g2)和团头鲂连续三代雌核发育群体(g3),每群体各采集35尾,每尾剪取少许鳍条于95%酒精中保存备用,所有样本均采自上海海洋大学鱼类种质研究试验站(上海市浦东新区新场镇)。设计rapd引物为10碱基引物,由上海生工生物工程技术服务有限公司合成。
基因组dna的提取
基因组dna提取采用常规的“酚-氯仿”方法进行。
基因组dna的rapd分析
pcr扩增反应在eppendorfmastercyclergradientpcr仪上进行,每一样品的反应总体积25μl,含2.5μl10×扩增缓冲液[含100mmol/ltris-hcl(ph9.0),500mmol/lkcl,15mmol/lmgcl2,1%(质量浓度)明胶,1%(体积分数)tritonx-100,最后调节ph值至8.0]。2μldntp混合液(每种dntp的终浓度0.2mmol/l),引物2μl(终浓度0.2μmol/l),2μl基因组dna(约50~150ng),0.5μltaqdna聚合酶(1.25单位),16μl无菌重蒸水,最后加入30μl石腊油。
pcr的扩增程序为:94℃预变性5min,接下来进行45个循环,每个循环包括94℃45s,36℃45s,72℃90s;最后一次循环结束后在72℃延伸5min。
取10μl扩增产物经1.5%琼脂糖凝胶电泳,电泳缓冲液为0.5×tbe,电压为5v/cm,采用的分子量标准为markerⅲ[天根生化科技(北京)有限公司产品]。电泳结束后,电泳凝胶经溴化乙锭染色,用syngene凝胶成像分析系统进行扫描摄像,并用genetools软件相对于分子量标准markerⅲ对每个引物扩增条带的分子量大小进行估算。每个引物至少被重扩一次以保证结果的准确性。
数据处理与分析
首先对照扩增图谱分别统计特异性条带在群体间的出现频率。随后进行遗传多样性数据统计,仅记录清晰且重复性好的dna条带。根据markerⅲ各带的迁移率确定扩增产物各带的迁移率,同一引物对不同个体扩增出的条带,只要迁移率相同都视为同一类型(性状)记为1,缺乏此带的记为0;以此类推,将所有个体的条带转换成二元数据矩阵。采用popgene1.31软件包计算以下遗传变异参数:
(1)多态位点比例(p):p=(多态位点数/位点总数)×100%。
(2)shannon信息指数(s):
其中pi为某一座位上第i个等位基因在某一群体中出现的频率,㏑pi为pi的自然对数,r为等位基因数目。
(3)群体内个体间nei’s标准遗传距离(ds)和nei’s遗传相似系数(i)按照nei(1978)的方法计算:
式中,xij、yij分别为个体x、y第j座位第i个等位基因频率,r为基因座数目,m为等位基因数目。
(4)群体间nei’s标准遗传距离(ds)和nei’s遗传相似系数(i)按照nei(1978)的方法计算:
式中,xij、yij分别为群体x、y第j座位第i个等位基因频率,r为群体中的基因座数目,m为等位基因数目。
用arlequin3.01软件估测群体间成对fst值,并利用置换检验法(permutationtest)进行显著性检验(重复次数为1000)。
采用分子方差分析(analysisofmolecularvariance,amova)估算各群体间和群体内的遗传变异及分化水平。通过3种分子遗传变量进行分析:fst为群体内个体之间(amongindividualswithinpopulations)的遗传变异;fsc为组内各群体间(amongpopulationswithingroups)的变异程度;fct为不同组别之间(amonggroups)的遗传变异程度。并用置换检验法(permutationtest)进行1000次重复模拟计算,以上运算在arlequin3.01软件中完成。
利用mega4.0软件包根据群体间nei’s标准遗传距离(ds),用upgma法(unweightedpairgroupmethodwitharithmeticmeans)和nj法(neighbour-joiningmethod)构建群体间聚类图。
采用lsd-t检验比较群体间遗传多样性参数(多态位点比例和shannon信息指数),bonferroni校正p值,检验水准定为α=0.05,在spss19.0软件上完成运算。
ii.具体实施例
实施例1、pcr扩增结果
本发明人对减数分裂雌核发育团头鲂的遗传多样性分析,结合研究经验和实验论证,从大量的引物中筛选出39条pcr扩增产物电泳条带清晰、重复性好、扩增效果稳定的引物,这些引物列于表1中,并对清晰可计数位点进行统计,各引物所产生的条带数见表2。单条引物扩增的条带数为2~10条,扩增片段长度集中在200~2000bp。39条引物在f9、g1、g2和g3群体中扩增条带总数分别为213条、202条、200条和190条,呈现出随雌核发育世代数增加而减少的趋势。单条引物在f9、g1、g2和g3群体中扩增条带数的范围分别为2~10、2~9、2~9和2~10。这些引物经过多次重复的扩增和电泳实验,确定为稳定性、再现性良好。
表1、本发明使用的39条引物序列及编号
实施例2、群体内遗传变异分析
1、多态位点比例和shannon信息指数
39条引物在f9、g1、g2和g3群体中的多态位点数、多态位点比例和shannon信息指数见表2。39条引物在f9、g1、g2和g3群体中扩增到的多态位点数分别为77、72、54和51,单条引物在f9、g1、g2和g3群体中扩增到的多态位点数范围分别为0~7、0~4、0~5和0~7。f9、g1、g2和g3群体的多态位点比例分别为36.15%、35.64%、27.00%和26.84%,f9群体的多态位点比例最高,g3群体的多态位点比例最低,3个雌核发育群体的多态位点比例均明显低于对照组f9群体;随着雌核发育世代数的增加,多态位点比例呈现逐代降低的趋势,即:g1>g2>g3。f9、g1、g2和g3群体的shannon信息指数为0.1383~0.2079,f9群体的shannon信息指数最高,g3群体的shannon信息指数最低,3个雌核发育群体的shannon信息指数均明显低于对照组f9群体;shannon信息指数随雌核发育世代数的增加而降低,即:g1>g2>g3。
群体间多态位点比例和shannon信息指数的lsd-t检验结果显示(表3),在α=0.05显著性水平上,群体间多态位点比例差异不显著(p=0.261~1.000),群体间shannon信息指数差异不显著(p=0.312~1.000)。
总体而言,3个雌核发育群体的遗传多样性水平均明显低于对照组f9群体,随着雌核发育世代数的增加,遗传多样性水平呈现逐代降低的趋势,即:g1>g2>g3。
表2、4个群体的扩增位点数、多态位点数和shannon信息指数(s)
表3、4个团头鲂群体间多态位点比例(对角线上)和shannon信息指数(对角线下)lsd-t检验p值
2、群体内个体间的遗传相似系数和遗传距离
f9、g1、g2和g3群体内个体间的遗传相似系数和遗传距离见表4。4个群体的群体内个体间的平均遗传相似系数为0.8285~0.9060,g3群体内个体间的平均遗传相似系数最高(0.9060),f9群体内个体间的平均遗传相似系数最低(0.8285),3个雌核发育群体的群体内个体间平均遗传相似系数均明显高于对照组f9群体;群体内个体间的平均遗传相似系数呈现随雌核发育世代数的增加而升高的趋势,即:g3>g2>g1。
4个群体的群体内个体间的平均遗传距离为0.0991~0.1908,g3群体内个体间的平均遗传距离最低(0.0991),f9群体内个体间的平均遗传距离最高(0.1908),3个雌核发育群体的群体内个体间平均遗传距离均明显低于对照组f9群体;群体内个体间的平均遗传距离呈现随雌核发育世代数的增加而降低的趋势,即:g1>g2>g3。
总体而言,3个雌核发育群体的遗传纯度(遗传相似系数)均明显高于对照组f9群体,随着雌核发育世代数的增加,雌核发育群体内的遗传纯度呈逐代上升的趋势,即:g3>g2>g1。
表4、群体内个体间的遗传相似系数和遗传距离
实施例3、群体间遗传变异分析
1、群体间rapd特异片段分析
在39条扩增稳定、多态性丰富的引物中,本发明人又进一步筛选出5条引物,它们在群体间产生了特异dna片段,这5条引物分别是s3、s40、s58、s71和s75(表5)。其中,引物s3扩增出一条长约136bp片段,该片段在g3群体中出现频率达100%,而在其它3个群体中的出现频率均为0(图1);同时,引物s3扩增出另一条长约797bp片段,该片段在g3群体中的出现频率为0,而在其它3个群体中的出现频率均为100%(图1)。由此可见,引物s3产生的rapd图谱及其特异片段(136bp和797bp)可以作为区分g3群体和其它3个群体(f9、g1和g2)的分子遗传标记。
如图2所示,引物s40扩增出一条长约780bp片段,该片段在g3群体中的出现频率为100%,而在其它3个群体中的出现频率仅为5.71%~14.29%,笔者认为,该片段在g3群体中的高出现频率可作为区分g3群体与其它3个群体(f9、g1和g2)的重要依据。
如图3所示,引物s58扩增出一条长约439bp片段,该片段在g3群体中的出现频率为0,而在其它3个群体(f9、g1和g2)中的出现频率高达71.43%~100%,由此可以认为,引物s58产生的特异片段(439bp)可作为区分g3群体和其它3个群体(f9、g1和g2)的分子遗传标记。
如图4所示,引物s71扩增出一条长约504bp片段,该片段在g2群体中的出现频率为0,而在其它3个群体(f9、g1和g3)中的出现频率高达71.43%~85.71%,因此,引物s71产生的特异片段(504bp)可作为区分g2群体和其它3个群体(f9、g1和g3)的分子遗传标记。
如图5所示,引物s75扩增出一条长约313bp片段,该片段在g3群体中的出现频率为0,而在其它3个群体(f9、g1和g2)中的出现频率高达85.71%~100%,鉴于此,引物s75产生的特异片段(313bp)可作为区分g3群体和其它3个群体(f9、g1和g2)的分子遗传标记。
综上所述,4条引物(s3、s40、s58和s75)可用于区分g3群体和其它3个群体(f9、g1和g2),其中,使用引物s3的进行群体鉴别的可靠性最高。仅1条引物(s71)能用于区分g2群体和其它3个群体(f9、g1和g3)。尚未找到能有效区分f9群体和g1群体的引物。
表5、5个引物在4个群体间扩增出的特异dna片段及其出现频率
2、群体间遗传相似系数、遗传距离和遗传分化
4个群体间遗传相似系数和遗传距离见表6。群体间遗传相似系数为0.8404~0.9204,g1群体和g3群体间遗传相似系数最低(0.8404),f9群体和g2群体间遗传相似系数最高(0.9204)。群体间遗传距离为0.0829~0.1739,f9群体和g2群体间遗传距离最小(0.0829),g1群体和g3群体间遗传距离最大(0.1739)。
4个群体间的遗传分化指数(成对fst值)见表7。群体间成对fst值为0.2692~0.4195,f9群体和g2群体间fst值最小(0.2692),g2群体和g3群体间fst值最大(0.4195)。经1000次置换检验得到的fst值的p值为0.0000~0.0090,均达到极显著水平(p<0.01),据此可推测,4个群体间存在极显著的遗传分化。
表6、4个群体间的遗传相似系数(对角线上)和遗传距离(对角线下)
表7、4个群体间的遗传分化指数(成对fst值)(对角线上)及其p值(对角线下)
3、分子方差分析(analysisofmolecularvariance,amova)
本发明对4个团头鲂群体进行分组(1个组、2个组、3个组),从不同角度对群体遗传变异进行分子方差分析(amova)。结果显示(表8),在任何一种分组条件下,fst值都达到了极显著水平(p<0.01),说明群体内个体间的遗传分化极显著。当把所有群体分成2个组或3个组时,fsc值均达到极显著水平(p<0.01),表明群体间存在极显著的遗传分化。这证实了群体间遗传分化指数(fst值)的分析结果。当把所有群体分成2个组或3个组时,在任何一种分组条件下,fct值均未达到显著水平(p>0.05),表明组别之间不存在显著的遗传分化。
表8、4个团头鲂群体间遗传差异的分子方差分析(amova)
注:*表示p<0.05,**表示p<0.01,ns表示“无显著性”(p>0.05)。
4、聚类分析
基于群体间nei’s标准遗传距离构建的4个团头鲂群体间nj聚类图和upgma聚类图如图6所示。因聚类方法的差异,2种聚类图显示了各自的特点,很难说哪种聚类图最能反映真实的群体间遗传关系。但2种聚类图(图6a和图6b)均显示,f9、g2和g3群体可被聚为一类,g1群体和其它3个群体(f9、g2、g3)间聚类关系较远,这也验证了前文中群体间遗传距离的结果。
讨论
连续多代减数分裂雌核发育效果分析
在传统的育种方法中,建立一个遗传纯系或选育系一般需要通过连续数代的近亲交配来完成。同时还会因近交衰退及繁育条件限制对部分个体的淘汰造成育种材料的丢失,因而这是一项长期、大量而严密的工作。而采用人工诱导雌核发育的方法可加速纯化过程。人工诱导鱼类雌核发育的方式有两种:一种是通过抑制第二极体释放来诱导产生雌核发育二倍体,称为减数分裂雌核发育;另一种是通过抑制第一次卵裂来诱导产生雌核发育二倍体,称为卵裂雌核发育。一次卵裂雌核发育相当于8~10代同胞兄妹交配,一次卵裂雌核发育加一次减数分裂雌核发育就可以获得纯系。
理论上,抑制第二极体释放诱导雌核发育二倍体时,如果不发生重组,子代都应成为完全的纯合体,但由于鱼类的染色体一般都发生一次交叉,因此距离着丝粒近的基因位点为纯合体,距离着丝粒远的基因位点,杂合体的比率根据基因位点在染色体上的位置而变化,范围为0~1.0。在实际的雌核发育育种实践中,连续多代诱导减数分裂雌核发育,将快速地提高遗传相似系数。虽然是杂合子,但是亲本的遗传特征已被固定,其子代个体数量性状表现一致,个体之间差异较小,可以作为良种选育的一种有效方法。许多研究显示,人工诱导多代减数雌核发育大大加速了鱼类基因纯合速度。
团头鲂“浦江1号”是农业部公告推广的鱼类良种,鉴于没有永远的良种的理念和推陈出新的时代要求,借助人工雌核发育技术,在“浦江1号”良种的基础上,快速培育出性状更加优良且遗传稳定的品系具有十分重要的意义。上海海洋大学水产种质资源研究室多年前开展了团头鲂减数分裂雌核发育的诱导,并陆续获得了第一代减数分裂雌核发育群体和连续两代减数分裂雌核发育群体。为使团头鲂雌核发育家系的遗传纯合度得到更显著的提升,本发明人对连续两代雌核发育团头鲂雌鱼卵子再进行减数分裂雌核发育诱导,成功培育出连续三代减数分裂雌核发育团头鲂群体,并应用于良种选育实践。本发明选择到39条引物对雌核发育一代群体(g1)、雌核发育二代群体(g2)和雌核发育三代群体(g3)基因组进行rapd分析,结果显示,g1、g2和g3群体的多态位点比例分别为35.64%、27.00%和26.84%,远低于鲤(c.carpiol.)、双棘黄姑鱼(nibeadiacanthus)和唐鱼(tanichthysalbonubeslin)等鱼类养殖群体的相应参数。而且,多态位点比例随雌核发育世代数的增加而降低,即:g1>g2>g3,其中,g2比g1降低了24.24%,g3又比g2降低了0.59%,平均每代降低12.42%。g1、g2和g3群体的shannon信息指数分别为0.1857、0.1461和0.1383,远低于鲤(c.carpiol.)、草鱼(ctenopharyngodonidellus)和双棘黄姑鱼(nibeadiacanthus)等鱼类养殖群体的相应参数。而且,shannon信息指数随雌核发育世代数的增加而降低,即:g1>g2>g3,其中,g2比g1降低了21.32%,g3又比g2降低了5.34%,平均每代降低13.33%。多态位点比例和shannon信息指数的结果一致表明,连续多代的人工减数分裂雌核发育诱导已使团头鲂育种群体的遗传多样性明显降低,并呈现逐代降低的趋势。g1、g2和g3群体内个体间的平均遗传相似系数分别为0.8538、0.8968和0.9060,呈现随雌核发育世代数的增加而升高的趋势,即:g3>g2>g1,其中,g2比g1升高了5.04%,g3又比g2升高了1.03%,平均每代升高3.04%。表明连续多代的人工减数分裂雌核发育诱导已使团头鲂育种群体的遗传纯度明显升高,并呈现逐代升高的趋势。以上结果表明,连续多代减数分裂雌核发育能显著加快团头鲂基因的纯合速度,使控制优良性状的基因快速纯合化;所培育的雌核发育群体,尤其是雌核发育三代群体已经是一个遗传一致性较高的高纯品系。此外,g3群体与对照组(f9群体)间成对fst值为0.3661,经1000次置换检验得到的fst值的p值为0.0000,已达到极显著水平(p<0.01),显示g3群体与对照组(f9群体)间已经发生了极显著的遗传分化。这也说明连续的雌核发育是快速建立具有特定遗传特征品系的有效途径。本发明为连续多代人工诱导减数分裂雌核发育育种实践提供了新的依据。
群体间鉴别标记的发现及其成因分析
人工诱导雌核发育是使团头鲂良种重要经济性状基因快速纯化和固定的主要途径。但在实际的雌核发育育种实践中,因雌核发育子代与普通团头鲂在形态上极其相似,故使用传统的形态学方法难以准确区分雌核发育团头鲂与普通团头鲂群体。
本发明从许多引物中筛选到5条在群体间产生特异dna片段的引物,根据这些引物扩增到的特异dna片段在群体内的出现频率,可以将它们分成两类,第一类特异dna片段在某个雌核发育群体中出现频率为0,在对照组和其它雌核发育群体中出现频率很高(71.43%~100%)。如,引物s3扩增出的一条长约797bp片段在g3群体中的出现频率为0,而在其它3个群体中的出现频率均为100%(图1)。引物s58扩增出的一条长约439bp片段在g3群体中的出现频率为0,而在其它3个群体(f9、g1和g2)中的出现频率高达71.43%~100%(图3)。引物s71扩增出的一条长约504bp片段在g2群体中的出现频率为0,而在其它3个群体(f9、g1和g3)中的出现频率高达71.43%~85.71%(图4)。引物s75扩增出的一条长约313bp片段在g3群体中的出现频率为0,而在其它3个群体(f9、g1和g2)中的出现频率高达85.71%~100%(图5)。第二类特异dna片段在某个雌核发育群体中出现频率为100%,而在对照组和其它雌核发育群体中出现频率很低(0~14.29%)。如,引物s3扩增出的一条长约136bp片段在g3群体中出现频率达100%,而在其它3个群体中的出现频率均为0(图1);引物s40扩增出的一条长约780bp片段在g3群体中的出现频率为100%,而在其它3个群体中的出现频率仅为5.71%~14.29%(图2)。
在本发明提及的所有文献都在本申请中引用作为参考,就如同每一篇文献被单独引用作为参考那样。此外应理解,在阅读了本发明的上述讲授内容之后,本领域技术人员可以对本发明作各种改动或修改,这些等价形式同样落于本申请所附权利要求书所限定的范围。
序列表
<110>上海海洋大学
<120>多代减数分裂雌核发育团头鲂的遗传多样性鉴定方法及试剂
<130>186991
<160>39
<170>siposequencelisting1.0
<210>1
<211>10
<212>dna
<213>引物(primer)
<400>1
gtttcgctcc10
<210>2
<211>10
<212>dna
<213>引物(primer)
<400>2
tgatccctgg10
<210>3
<211>10
<212>dna
<213>引物(primer)
<400>3
catccccctg10
<210>4
<211>10
<212>dna
<213>引物(primer)
<400>4
ggactggagt10
<210>5
<211>10
<212>dna
<213>引物(primer)
<400>5
ggtgacgcag10
<210>6
<211>10
<212>dna
<213>引物(primer)
<400>6
ctgctgggac10
<210>7
<211>10
<212>dna
<213>引物(primer)
<400>7
agggaacgag10
<210>8
<211>10
<212>dna
<213>引物(primer)
<400>8
acccccgaag10
<210>9
<211>10
<212>dna
<213>引物(primer)
<400>9
caggcccttc10
<210>10
<211>10
<212>dna
<213>引物(primer)
<400>10
tgccgagctg10
<210>11
<211>10
<212>dna
<213>引物(primer)
<400>11
aatcgggctg10
<210>12
<211>10
<212>dna
<213>引物(primer)
<400>12
aggggtcttg10
<210>13
<211>10
<212>dna
<213>引物(primer)
<400>13
gtgacgtagg10
<210>14
<211>10
<212>dna
<213>引物(primer)
<400>14
gggtaacgcc10
<210>15
<211>10
<212>dna
<213>引物(primer)
<400>15
gtgatcgcag10
<210>16
<211>10
<212>dna
<213>引物(primer)
<400>16
tcggcgatag10
<210>17
<211>10
<212>dna
<213>引物(primer)
<400>17
cagcacccac10
<210>18
<211>10
<212>dna
<213>引物(primer)
<400>18
aggtgaccgt10
<210>19
<211>10
<212>dna
<213>引物(primer)
<400>19
gttgcgatcc10
<210>20
<211>10
<212>dna
<213>引物(primer)
<400>20
tgagcggaca10
<210>21
<211>10
<212>dna
<213>引物(primer)
<400>21
ggtctacacc10
<210>22
<211>10
<212>dna
<213>引物(primer)
<400>22
agcgccattg10
<210>23
<211>10
<212>dna
<213>引物(primer)
<400>23
agggcgtaag10
<210>24
<211>10
<212>dna
<213>引物(primer)
<400>24
gagagccaac10
<210>25
<211>10
<212>dna
<213>引物(primer)
<400>25
acccggtcac10
<210>26
<211>10
<212>dna
<213>引物(primer)
<400>26
ccgcatctac10
<210>27
<211>10
<212>dna
<213>引物(primer)
<400>27
gaacggactc10
<210>28
<211>10
<212>dna
<213>引物(primer)
<400>28
gtcccgacga10
<210>29
<211>10
<212>dna
<213>引物(primer)
<400>29
tggaccggtg10
<210>30
<211>10
<212>dna
<213>引物(primer)
<400>30
ctcaccgtcc10
<210>31
<211>10
<212>dna
<213>引物(primer)
<400>31
agggccgtct10
<210>32
<211>10
<212>dna
<213>引物(primer)
<400>32
aaagctgcgg10
<210>33
<211>10
<212>dna
<213>引物(primer)
<400>33
tgtcatcccc10
<210>34
<211>10
<212>dna
<213>引物(primer)
<400>34
aagcctcgtc10
<210>35
<211>10
<212>dna
<213>引物(primer)
<400>35
ggatgagacc10
<210>36
<211>10
<212>dna
<213>引物(primer)
<400>36
gacggatcag10
<210>37
<211>10
<212>dna
<213>引物(primer)
<400>37
cacactccag10
<210>38
<211>10
<212>dna
<213>引物(primer)
<400>38
ttccccccag10
<210>39
<211>10
<212>dna
<213>引物(primer)
<400>39
tgagtgggtg10
- 还没有人留言评论。精彩留言会获得点赞!