盐酸小檗碱与乳酸共晶、其制备方法和应用与流程
本发明属于药物共晶技术领域,具体涉及盐酸小檗碱与乳酸共晶、其制备方法和应用。
背景技术:
在药物开发过程中,药物活性成分(api)的难溶性、难分散性、低生物利用度及稳定性等问题仍是困扰医药工业的发展,更制约着药物的开发和临床应用。药物溶出速率小导致药物生物利用度的降低,这一问题对于固体剂型药物来说显得尤为突出,因此,提高难溶性药物溶出度仍是药物开发急需解决的问题,也是药物研发者越来越关注的问题,更是api新固体型态的药物研发中的一个重要方面。
盐酸小檗碱c20h18clno4(式ⅰ)是一种异喹啉生物碱,通常以二水合物的形式存在,主要用于治疗胃肠炎、细菌性痢疾等肠道感染、眼结膜炎、化脓性中耳炎等,还有阻断α受体的抗心律失常作用。由于盐酸小檗碱水溶性差,导致其生物利用度低,从而极大地限制其临床药物开发。因此,改善盐酸小檗碱的水溶性和溶出度仍是盐酸小檗碱药物制剂亟待解决的问题。
近年来,利用超分子化学和晶体工程学制备药物共晶已经成为化学和医药学领域的研究热点,药物共晶由于其独特的物理化学性质而倍受青睐。药物共晶是指药物活性组分(activepharmaceuticalingredient,api)与其他生理上可接受的酸、碱或非离子化合物等共晶形成物(co-crystalformer,ccf),通过氢键、范德华力、π-π堆积作用、卤键等非共价键作用力结合而成的晶体。
技术实现要素:
本发明的目的在于提供一种盐酸小檗碱的新固体形态,即盐酸小檗碱与乳酸共晶,为由一分子盐酸小檗碱、一分子乳酸和一分子水为基本结构单元形成的共晶化合物,该共晶化合物可显著降低盐酸小檗碱的吸湿性,改善盐酸小檗碱的溶解度和溶出度,增强盐酸小檗碱的制药和医疗应用。
本发明还提供盐酸小檗碱与乳酸共晶的制备方法,该制备方法简单易控,适于工业化生产,且成本低廉。
为实现上述目的,本发明的技术方案为:盐酸小檗碱与乳酸共晶,以盐酸小檗碱为活性药物成分,以乳酸作为前驱体,形成的共晶;为三斜晶系,空间群为p-1,晶胞参数为:
盐酸小檗碱与乳酸共晶的pxrd在衍射角2θ为8.43°±0.2、14.82°±0.2、15.26°±0.2、18.86°±0.2、19.99°±0.2、24.93°±0.2、25.71°±0.2、26.33°±0.2处有特征峰。
盐酸小檗碱与乳酸共晶的红外谱图在1029±5cm-1、1279±5cm-1、1585±5cm-1、1711±5cm-1、3301±5cm-1处具有特征峰。
盐酸小檗碱与乳酸共晶的结构式为c20h18clno4·c3h6o3·h2o,由一分子盐酸小檗碱、一分子乳酸和一分子水通过卤键、氢键形成盐酸小檗碱与乳酸共晶的基本结构单元,盐酸小檗碱分子的氯原子分别与乳酸分子的羟基氢原子和水分子的氢原子通过非共价结合,在盐酸小檗碱分子与乳酸分子间、盐酸小檗碱分子与水分子间分别形成卤键;乳酸分子中羧基氧原子作为氢键供体,水分子中氧原子作为氢键受体,在乳酸分子与水分子间形成氢键。
本发明采用研磨法或者混悬法制备盐酸小檗碱与乳酸的药物共晶。研磨法通过机械作用力使得化合物分子之间产生卤键、氢键或其他分子间作用力形成共晶,研磨法包括干磨法和加液辅助研磨法。混悬法是将活性药物成分与共晶形成物或者前驱体在溶剂中混合后,充分混悬作用使得化合物分子间产生卤键、氢键或其它分子间作用力形成共晶。
盐酸小檗碱与乳酸共晶的制备方法,盐酸小檗碱与乳酸共混研磨析晶。
盐酸小檗碱与乳酸的摩尔比为1:0.9~3,优选为1:1~1.5,更优选为1:1。
研磨的方法包括手工研磨、球磨法或者机械研磨。
研磨的速度为10~800r/min,优选为200~400r/min。
研磨的温度为15℃~35℃,优选为室温。
或者,制备方法还包括:在共混研磨前,向盐酸小檗碱与乳酸中加入溶剂,即溶剂辅助研磨。
溶剂辅助研磨时,盐酸小檗碱和乳酸的总质量与溶剂的用量比为2~15g/ml,优选为5~7g/ml,更优选为6g/ml。所述溶剂包括甲醇、乙醇、异丙醇、正丙醇或丙酮等。研磨形成共晶的同时,甲醇、乙醇、异丙醇、正丙醇或丙酮等溶剂亦挥发,利于共晶的析出。
还包括,研磨后静置析晶,静置析晶过程中,甲醇、乙醇、异丙醇、正丙醇或丙酮等溶剂挥发,易于共晶饱和析出。静置析晶的温度为15℃~35℃,优选为室温。
或者,制备方法还可以为:盐酸小檗碱加入乳酸中至饱和,或者盐酸小檗碱与乳酸均达到饱和的混合溶液,混悬析晶。
具体的,向甲醇中加入盐酸小檗碱与乳酸至两者均达到饱和,形成盐酸小檗碱与乳酸均达到饱和的混合溶液。
混悬作用力(搅拌等机械作用力或者声波等物理作用力)使得盐酸小檗碱与乳酸之间产生卤键、氢键等作用力形成共晶,混悬过程中溶剂同时挥发,利于共晶饱和析出。
混悬析晶的方式为搅拌或者超声等。
混悬析晶的温度为15℃~35℃,优选为室温。
混悬析晶的时间为3~8小时,优选为4~8小时,更优选为6小时。
本发明制备的盐酸小檗碱与乳酸共晶,降低盐酸小檗碱的吸湿性,便于制剂成型过程中的环境参数、工艺步骤及工艺参数的控制,利于制剂成型,提高制剂成型后的稳定性。
本发明制备的盐酸小檗碱与乳酸共晶可用于制备药物制剂,该药物制剂中含有盐酸小檗碱与乳酸共晶活性成分。
所述药物制剂还含有任意一种或多种药学上可接受的辅料,所述药学可接受的辅料有载体、赋形剂、崩解剂、调味剂、润滑剂、粘合剂等。
所述药物制剂,根据需要制备成具有预防和/或治疗作用的药学上可接受的任意剂型。药学上可接受的剂型有液体制剂、固体制剂或者半固体制剂等。固体制剂包括但不限于颗粒剂、胶囊剂、片剂或者粉剂;液体制剂包括但不限于注射液、混悬液或冲剂;片剂包括但不限于糖衣片剂、薄膜衣片剂或肠溶衣片剂;胶囊剂包括但不限于硬胶囊剂和软胶囊剂。
相对于现有技术,本发明的有益效果为:
(1)本发明制备的盐酸小檗碱与乳酸共晶,可降低盐酸小檗碱的吸湿性,增强盐酸小檗碱的稳定性;改善盐酸小檗碱的溶解度和溶出度,提高其生物利用度,改善吸湿性,提高盐酸小檗碱的制剂成型性和稳定性;提高盐酸小檗碱的制药和医疗应用。
(2)本发明盐酸小檗碱共晶的制备工艺简单易控,产率高达90%~93%,纯度高达91%~96%,产率和纯度高,成本低廉,适于工业化生产。
附图说明
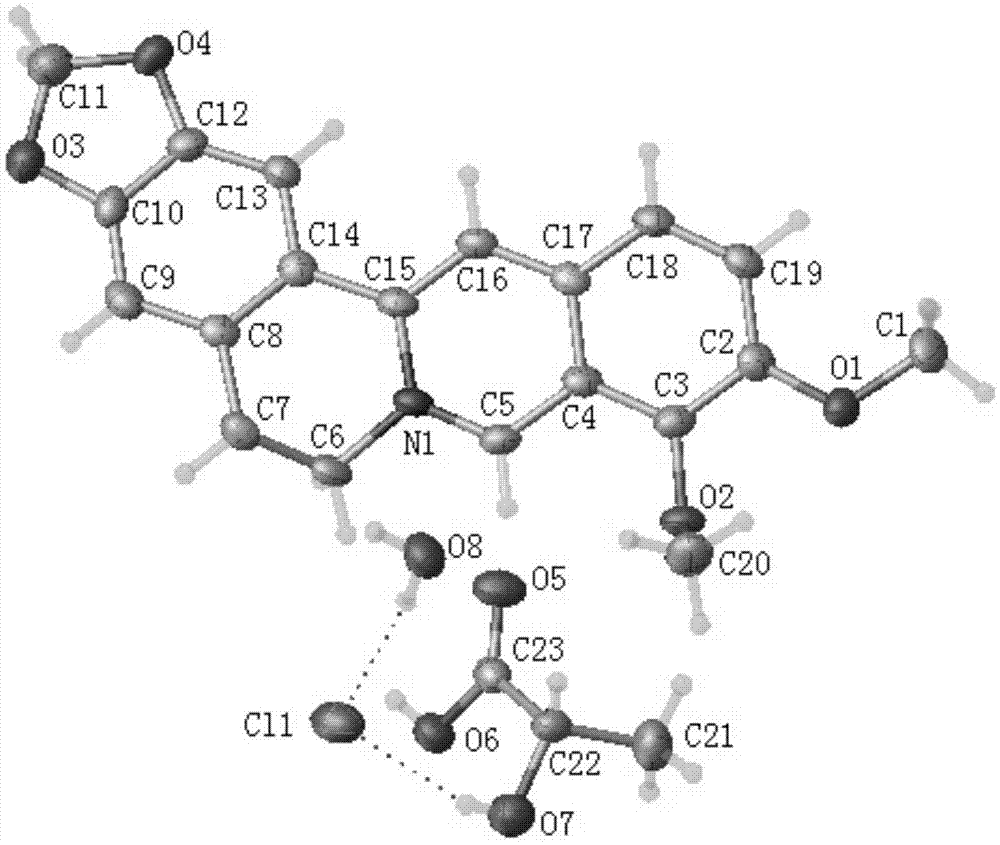
图1为本发明盐酸小檗碱与乳酸共晶化合物的分子结构示意图。
图2为盐酸小檗碱与乳酸共晶化合物、盐酸小檗碱与乳酸共晶模拟粉末、盐酸小檗碱二水化合物的pxrd谱图。
图3为盐酸小檗碱二水合物(a)、实施例1制备的盐酸小檗碱与乳酸共晶(b)的红外谱图。
图4为盐酸小檗碱二水合物(a)、实施例1制备的盐酸小檗碱与乳酸共晶(b)的tga曲线图。
图5为盐酸小檗碱二水合物(a)、实施例1制备的盐酸小檗碱与乳酸共晶(b)的dsc曲线图。
图6为实施例1制备的盐酸小檗碱与乳酸共晶、盐酸小檗碱二水化合物(api)的溶出度曲线。
图7为室温下盐酸小檗碱二水合物(api)的动态水分吸附曲线(a)、盐酸小檗碱二水合物(api)的动态水分解吸附曲线(b)、实施例1制备的盐酸小檗碱与乳酸共晶的动态水分吸附曲线(c)、实施例1制备的盐酸小檗碱与乳酸共晶的动态水分解吸附曲线(d)。
具体实施方式
本发明在室温条件下分别采用研磨法和混悬法制备盐酸小檗碱与乳酸的药物共晶,分子结构图如图1所示,以盐酸小檗碱作为药物活性成分(api),以乳酸(式ⅱ)作为前驱体,通过分子间卤键、氢键将一分子盐酸小檗碱、一分子乳酸和一分子水结合在一起形成盐酸小檗碱与乳酸药物共晶的晶体学不对称单元,其中,盐酸小檗碱分子中的氯原子分别与乳酸分子的羟基氢原子和水分子的氢原子通过非共价作用,在盐酸小檗碱分子与乳酸分子间、盐酸小檗碱分子与水分子间分别形成卤键;乳酸分子的羧基氧原子作为氢键供体,水分子中氧原子作为氢键受体,在乳酸分子与水分子间形成氢键。具体实施方式如下所示:
实施例1
溶液辅助研磨:准确称取408mg盐酸小檗碱二水合物(1mmol)和100mg乳酸(质量浓度90%,1mmol),按照摩尔比=1:1投料,置于玛瑙研钵中,然后向盐酸小檗碱二水合物和乳酸中滴加1~2滴乙醇(约0.05~0.1ml),室温条件下,充分研磨,制备盐酸小檗碱与乳酸共晶固体粉末,产率90.5%,纯度96.2%。在此过程中,辅助溶液挥发,利于共晶析出。研磨中滴加的辅助溶液除了乙醇之外,还可以是甲醇、正丙醇、丙酮或异丙醇。
实施例2
混悬法:准确称取408mg盐酸小檗碱二水合物(1mmol)溶入10ml乳酸(质量浓度90%)中,制成过饱和盐酸小檗碱乳酸溶液,充分搅拌6小时,直至析出淡黄色固体,形成盐酸小檗碱与乳酸共晶。
实施例3
干磨法:准确称取408mg盐酸小檗碱二水合物(约1mmol)和100mg乳酸(质量浓度90%,1mmol),按照摩尔比=1:1投料,置于玛瑙研钵中,室温条件下,充分研磨,制备盐酸小檗碱与乳酸共晶固体粉末,产率90%,纯度93%。
实施例4
在室温条件下,将100mg乳酸(质量浓度90%,1mmol)和408mg盐酸小檗碱二水合物(1mmol)加入10ml甲醇中,得到乳酸和盐酸小檗碱均达到饱和的混合溶液,在室温条件下搅拌,至析出盐酸小檗碱与乳酸共晶,产率93%,纯度91%。
上述实施例制备的盐酸小檗碱与乳酸共晶通过pxrd表征各自的衍射图谱,通过红外、dsc/tg、dvs进行各自的单晶结构分析,并分别进行不同溶液(水、甲醇、乙醇)溶解度、水中溶出度测定。具体过程如下:
(1)盐酸小檗碱与乳酸共晶的pxrd(粉末x射线衍射法)鉴定
仪器:x射线衍射仪(德国bruker公司,d2型);
检测条件:cu-ka靶,管电压30kv,管电流10ma,扫描范围θ为5°—45°,扫描速度为8°/min,步宽0.015。
实施例1制备的盐酸小檗碱与乳酸共晶、盐酸小檗碱与乳酸共晶模拟粉末、盐酸小檗碱二水化合物的pxrd谱图如图2所示,实施例1制备的盐酸小檗碱与乳酸共晶在衍射角2θ为8.43°±0.2、14.82°±0.2、15.26°±0.2、18.86°±0.2、19.99°±0.2、24.93°±0.2、25.71°±0.2、26.33°±0.2处有特征峰。盐酸小檗碱二水合物在衍射角2θ为8.64°±0.2、9.09°±0.2、12.98°±0.2、16.31°±0.2、25.40°±0.2、26.26°±0.2、26.86°±0.2、30.20°±0.2处有特征峰。
由图2可知,相对于盐酸小檗碱二水化合物,盐酸小檗碱与乳酸共晶的特征衍射峰及衍射峰强度均发生显著变化,说明盐酸小檗碱与乳酸之间发生反应,生成了新的物相,并在25.71°处出现盐酸小檗碱与乳酸共晶的特征峰。
实施例2至实施例4制备的盐酸小檗碱与乳酸共晶的pxrd衍射角2θ特征峰与实施例1相同。说明干磨法、混悬法同样可促使盐酸小檗碱与乳酸之间发生反应,生成新的物相。
(2)盐酸小檗碱与乳酸共晶的晶胞参数测试
共晶结构由x-射线单晶衍射仪(brukersmartapexiidiffractometer)测定,mo-ka在173k温度下扫描。
实施例1制备的盐酸小檗碱与乳酸共晶的晶体结构为三斜晶系,空间群为p-1,晶胞参数为:
实施例2至实施例4制备的盐酸小檗碱与乳酸共晶的晶胞参数与实施例1相同。
(3)盐酸小檗碱与乳酸共晶的红外表征
仪器:傅里叶变换红外光谱仪(德国bruker公司,equinox55型);
检测条件:扫描波段为4000~400cm-1,样品采用kbr固体压片,分辨率:1cm-1。
盐酸小檗碱二水合物(a)、实施例1制备的盐酸小檗碱与乳酸共晶(b)的红外谱图如图3所示,盐酸小檗碱二水合物至少在约3421cm-1、1621cm-1、1504cm-1、1028cm-1处有特征峰,盐酸小檗碱与乳酸共晶至少在约3301cm-1、1711cm-1、1585cm-1、1279cm-1、1029cm-1处具有特征峰。由图3可知,相对于盐酸小檗碱二水合物,盐酸小檗碱与乳酸共晶的红外特征峰发生了显著变化,说明盐酸小檗碱与乳酸之间发生反应,生成了新的物相。
实施例2至实施例4制备的盐酸小檗碱与乳酸共晶的红外谱图特征峰与实施例1相同。
(4)盐酸小檗碱与乳酸共晶的dsc/tg(差示扫描量热法/热重法)测试
仪器:dsc/tga同步热分析仪(sdt-600q系列dsc/tga/dta同步热分析仪);
检测条件:氮气气氛,气体流速:10ml/min,升温速率为10℃/min,测试温度区间:室温~250℃。
盐酸小檗碱二水合物(a)和实施例1制备的盐酸小檗碱与乳酸共晶(b)的tga谱图如图4所示。盐酸小檗碱二水合物(a)在99.6℃时损失质量为8.9%,与盐酸小檗碱二水合物中两分子水的理论质量8.8%相吻合,说明所用原料盐酸小檗碱为二水合物;盐酸小檗碱与乳酸共晶(b)在67.1℃时,有3.9%的质量损失,与理论计算的一个水分子含量(3.8%)相吻合,说明盐酸小檗碱-乳酸共晶里含有一个结晶水。
盐酸小檗碱二水合物(a)和实施例1制备的盐酸小檗碱与乳酸共晶(b)的dsc谱图如图5所示。盐酸小檗碱与乳酸共晶(b)在67.1℃有一个吸收峰,说明盐酸小檗碱-乳酸共晶里含有水分;在210℃处有一个尖锐的放热峰,对应该共晶化合物的热分解温度。
实施例2至实施例4制备的盐酸小檗碱与乳酸共晶的dsc/tg测试结果与实施例1相同。
(5)盐酸小檗碱与乳酸共晶的溶解度测定
ⅰ.最佳吸收波长的确定
盐酸小檗碱与乳酸共晶的溶解度测定采用标准曲线法,仪器:agilent-1260s高效液相色谱仪;检测条件:agilent-c18色谱柱(4.6mm×150nm,5μm),流动相:甲醇-0.4%磷酸溶液梯度洗脱,流速:1ml/min,检测波长:230nm,柱温为30℃,进样量10μl。
盐酸小檗碱二水合物在230nm处出现较强的吸收峰,因此,选定230nm波长处进行盐酸小檗碱与乳酸共晶的溶解度和溶出度测定。
ⅱ.hplc的洗脱程序
ⅲ.标准曲线绘制
精密称取盐酸小檗碱二水合物适量,分别配制0.0196mg/ml、0.0492mg/ml、0.0983mg/ml、0.1966mg/ml、0.2949mg/ml、0.3932mg/ml、0.4915mg/ml、0.5898mg/ml标准液,标准溶液经0.45μl滤膜过滤,分别进样,按照上述hplc检测条件,测定峰面积,线性方程为y=40044x+20.191,相关r2=1>0.995,说明盐酸小檗碱质量浓度在0.0196~0.5898mg/ml范围内线性关系良好。
ⅳ.盐酸小檗碱与乳酸共晶的溶解度测定
盐酸小檗碱二水合物(api)、实施例1制备的盐酸小檗碱与乳酸共晶在25℃时的溶解度测定结果如表1所示,37℃时的溶解度测定结果如表2所示。
表125℃时的盐酸小檗碱二水合物(api)、盐酸小檗碱与乳酸共晶溶解度结果(单位mg/ml)
表237℃时的盐酸小檗碱二水合物(api)、盐酸小檗碱与乳酸共晶溶解度结果(单位mg/ml)
由表1和表2的结果可知,随着温度的升高,盐酸小檗碱、盐酸小檗碱与乳酸共晶在溶剂(水、甲醇和乙醇)中的溶解度均增大,相同温度、相同溶剂(水、甲醇和乙醇)条件下,盐酸小檗碱与乳酸共晶的溶解度大于盐酸小檗碱。盐酸小檗碱、盐酸小檗碱与乳酸共晶在水、甲醇和乙醇的溶解度大小次序相同,次序如下:s甲醇>s水>s乙醇。
实施例2至实施例4制备的盐酸小檗碱与乳酸共晶的溶解度测试结果与实施例1相似。
ⅴ.盐酸小檗碱与乳酸共晶的溶出度测定
精确称取盐酸小檗碱二水化合物109mg(含盐酸小檗碱100mg)、盐酸小檗碱与乳酸共晶129mg(其中盐酸小檗碱的量为100mg),照溶出度与释放度测定法,以900ml水为溶出介质,采用浆法,设置转速为50r/min,测量温度为37℃,投料时开始计时,分别在5min、10min、15min、20min、30min、45min、60min、90min、120min直至原料全部溶解完全取相同体积的溶出介质,即5ml,每次取完之后补充相同体积的溶出介质,将取出的溶出介质用水系滤膜过滤,滤液移至液相小瓶内,按照上述hplc检测条件测定含量,盐酸小檗碱与乳酸共晶的累积溶出度曲线如图6所示。
由图6可知,在水中达到完全溶解时,盐酸小檗碱二水化合物(api)所用时间为90min,实施例1制备的盐酸小檗碱与乳酸共晶所用时间为30min,盐酸小檗碱与乳酸形成共晶后,大大改善了盐酸小檗碱的溶出度。
实施例2至实施例4制备的盐酸小檗碱与乳酸共晶的溶出度测试结果与实施例1相似。
(6)盐酸小檗碱与乳酸共晶的动态蒸汽吸附法(dvs)测定
在smsdvs仪器上(表面测量系统,英国)进行了dvs实验。首先对盐酸小檗碱二水合物粉末、盐酸小檗碱与乳酸共晶粉末干燥,在氮气流中干燥几小时以建立平衡干重,相对湿度范围为0%—95%—0%,并且以10%rh增量,温度在25℃保持不变,进行的动态水分吸/脱附测试。
盐酸小檗碱二水合物(api)分子内含有两分子水,其动态水分吸附曲线和解吸附曲线如图7所示。动态水分吸附过程中,在10%~70%相对湿度范围内,盐酸小檗碱二水合物相对质量变化微小,基本保持平稳;当相对湿度升至70%以上,盐酸小檗碱开始吸收水分;当相对湿度达到95%时,盐酸小檗碱分子内再增加两分子水,此时,盐酸小檗碱含有四分子水。含四分子水的盐酸小檗碱比较稳定,在动态水分解吸附过程中,只有当相对湿度小于20%时,含四分子水的盐酸小檗碱才开始失水,当相对湿度降至0%时,盐酸小檗碱内水分含量只有1%左右。
由图7盐酸小檗碱二水合物的动态水分吸/脱附曲线可知,盐酸小檗碱二水合物在相对湿度10%~95%范围内,存在水分吸附滞后圈,盐酸小檗碱二水合物呈现吸湿滞后性,盐酸小檗碱二水合物同水分子的亲和力强,吸湿性高。
盐酸小檗碱与乳酸共晶分子内含有一分子水,实施例1制备的盐酸小檗碱与乳酸共晶的动态水分吸附曲线和解吸附曲线如图7所示。动态水分吸附过程中,随湿度增加,盐酸小檗碱与乳酸共晶缓慢吸收水分,当相对湿度升至70%,盐酸小檗碱与乳酸共晶开始逐渐大幅吸收水分;当湿度达到95%时,盐酸小檗碱与乳酸共晶分子再吸收8%的水分。在动态水分解吸附过程中,相对湿度从95%下降至70%的过程中,盐酸小檗碱与乳酸共晶迅速失去两分子水;相对湿度从70%下降至20%以下时,盐酸小檗碱与乳酸共晶的相对质量变化缓慢,盐酸小檗碱与乳酸共晶内的水分基本保持不变;相对湿度下降至20%以下时,再次迅速失水。由图7盐酸小檗碱与乳酸共晶的动态水分吸/脱附曲线可知,说明盐酸小檗碱与乳酸共晶同水分子的亲和力显著减弱,吸湿性显著降低。
盐酸小檗碱与乳酸以共晶形式结合后,显著改善了盐酸小檗碱或者盐酸小檗碱二水合物的吸湿性,便于制剂成型过程中的环境参数、工艺步骤及工艺参数的控制,提高制剂成型后的稳定性及生物利用度。
实施例2至实施例4制备的盐酸小檗碱与乳酸共晶的动态蒸汽吸/脱附测试结果与实施例1相似。
上述对实施例的描述是为便于该技术领域的普通技术人员能理解和使用发明。熟悉本领域技术的人员显然可以容易地对这些实施例做出各种修改,并把在此说明的一般原理应用到其他实施例中而不必经过创造性的劳动。因此,本发明不限于上述实施例,本领域技术人员根据本发明的揭示,不脱离本发明范畴所做出的改进和修改都应该在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!