CACYBP及其编码mRNA在肝癌诊断、治疗和预后判断中的应用的制作方法
本发明涉及生物技术和医学
技术领域:
,特别是涉及一种cacybp及其编码mrna在肝癌诊断、治疗和预后判断中的应用。
背景技术:
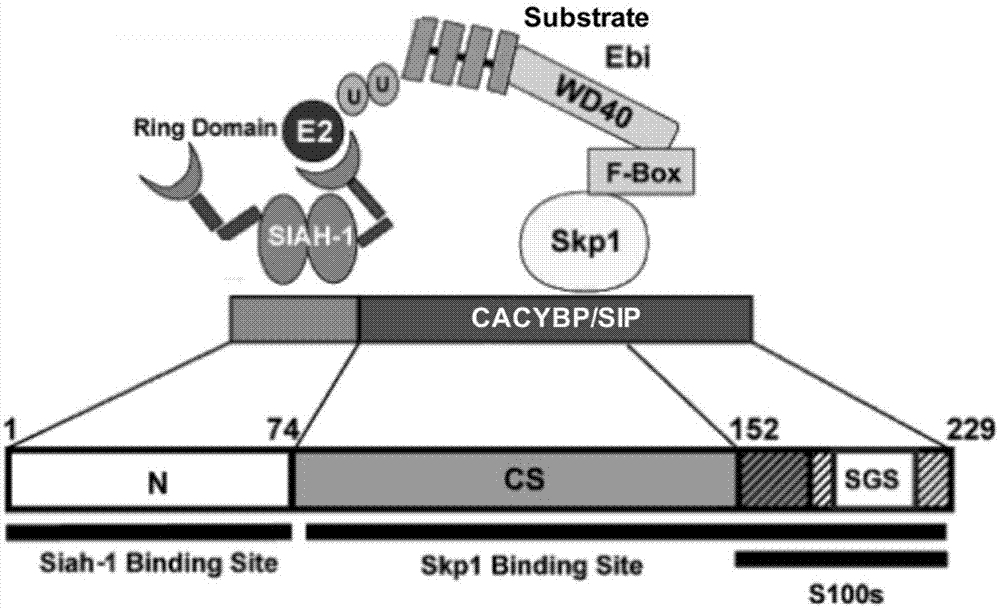
:与全球癌症总体死亡率持续下降成鲜明对比,肝癌发病和死亡逐年上升,最新癌症调查数据显示,肝癌年发病为78.2万,死亡74.5万,平均5年生存率低于5%,总体生存时间大约10个月;我国肝癌发病占了全球55%,一直是全球肝癌发生和死亡最多的国家。肝癌治疗常用手段有手术(肿瘤切除和肝移植)、局部治疗(射频消融、微波、粒子、肝动脉化疗栓塞tace)、全身用药;手术治疗被认为是肝癌的根治性手段,五年存活率可达60-75%,但术后每年复发率有25%,三年有50%,五年达70%,一旦复发,预后较差。同时,75%患者首次诊断时已经到了肝癌中晚期,没有手术机会,只能采用局部治疗如tace或者药物治疗,tace治疗后的复发转移高,副作用大,药物治疗的肿瘤控制率低且价格昂贵。这些瓶颈问题说明目前缺乏有效的肝癌治疗措施,其根本原因在于肝癌发生和疾病进展机制的多样性、复杂性、多重基因变异性,而目前用临床指标(如tnm分级、bclc分期、肝硬化程度)和单个分子指标(如afp、gpc3、pivka-ii)预测肝癌复发转移已经具有明显的局限性,这些临床指标或者病理类型相似的患者的临床结局通常存在很大差异。因此,用临床指标或者单独的分子标记来预测或评价患者难以取得满意的效果;这些因素直接影响早期诊断和准确的预后评估。因此,深入探索新的肝癌相关基因通路、开发新型有效的肝癌诊断及预后预测的方法是改善肝癌临床结局的关键。技术实现要素:基于此,有必要针对上述问题,提供一种cacybp及其编码mrna在肝癌诊断、治疗和预后判断中的应用,开发新型有效的肝癌诊断、预后判断试剂盒,并为肝癌治疗药物提供有效靶点。本发明公开了一种生物样本中cacybp及其编码mrna在诊断、治疗和/或预后评估肝癌中的应用。cacybp/sip(calcyclin-bindingprotein/siah-1interactingprotein)最初在埃里希腹水瘤细胞中被描述为与siah-1相结合的蛋白,其核苷酸编码序列如seqidno.3所示,其氨基酸序列如seqidno.4所示,cacybp/sip蛋白分子大小约为26.5kda,分为三个区域:n段区(氨基酸残基1-77)、cs区(氨基酸残基74-178)、c区(氨基酸残基152-229),不同的区域作为不同蛋白的配体发挥不同的功能,其中较为经典的组合是cacybp作为e3泛素连接酶与siah-1蛋白、接头蛋白skp1、骨架蛋白tbl组合成为scftbl1复合物,促进底物β-catenin的泛素化(如图1所示)。本发明人为了探索肝癌发生进展的未知基因和信号通路,利用生物信息大数据作为启动研究和探索的工具,利用生物信息学方法,从癌症相关数据库中,通过数据挖掘发现cacybp可能在肝癌发生发展中扮演着非常重要的角色,随后针对cacybp进行全方位的深入研究,具有高度的合理性和探索性。最终通过深入研究后发现,cacybp在肝癌组织中呈强阳性表达,而在正常组织中几乎不表达;且肝癌组织中cacybpmrna水平显著高于癌周非癌组织;而cacybp高表达是肝癌患者预后较差的独立危险因素,且cacybp高表达可加快肝癌细胞的生长,增强癌细胞的侵袭能力,有助于肝癌的转移,具有预测肝癌不良预后,尤其是复发和转移的有效指标。同时,研究结果还提示阻断cacybp可活化泛素化通路rnf41,促进癌基因降解,最后抑制肝癌细胞生长。综上所述,cacybp作为指标物,可以辅助诊断肝癌发生,也可预测患者治疗后的无癌生存期和总生存期;同时,cacybp还可以作为肝癌治疗新靶点,研究开发针对抑制肝癌细胞生长的药物。本发明公开了一种生物样本中cacybp及其编码mrna作为标志物在开发和/或制备具有肝癌诊断和/或预后评估用途的产品中的应用。可以理解的,上述产品可以是试剂盒,也可以是一体化检测设备。本发明公开了一种检测生物样本中cacybp及其编码mrna的试剂在制备肝癌诊断试剂或诊断设备中的应用。上述试剂可以是针对生物样本中cacybp及其编码mrna检测所设计的特异性试剂,也可以是能够实现检测生物样本中cacybp及其编码mrna的常规试剂和/或上述特异性试剂的组合。本发明公开了一种生物样本中cacybp及其编码mrna作为靶点在制备用于治疗肝癌的药物中的应用。本发明通过基因敲除和过表达技术的体外肝癌细胞模型,发现cacybp可以促进肝癌细胞生长和侵袭,提示cacybp的在肝癌中的强烈致癌作用。还通过蛋白组学和免疫沉淀实验发现,肝癌组织中cacybp与rnf41结合提示cacybp可能干扰了rnf41-e3泛素连接酶降解其下游癌基因底物的作用。据此,可将cacybp及其编码mrna作为靶点,设计针对该靶点的新型药物或治疗方式。本发明公开了一种cacybp抑制剂及cacybp编码mrna失活剂在制备用于治疗肝癌的药物中的应用。可以理解的,将cacybp及其编码mrna作为靶点,可通过cacybp抑制剂阻断cacybp,活化泛素化通路rnf41,促进癌基因降解,最后达到抑制肝癌细胞生长的作用,该cacybp抑制剂可以是小分子化合物或抗体药物等,仅需能够达到阻断cacybp活性即可。对于以cacybp编码mrna(即cacybp-mrna)作为靶点,可设计其互补序列使其编码翻译蛋白功能失效等,同样能够达到阻断cacybp的目的。本发明公开了一种检测生物样本中cacybp的试剂盒,其特征在于,包括有检测生物样本中cacybp的试剂。上述试剂盒可用于检测生物样本中cacybp的表达量,从而辅助肝癌判断或进行预后评估用。在其中一个实施例中,生物样本包括:获取自检测对象的新鲜组织、福尔马林固定或石蜡包埋组织、血液、细胞中的至少一种。优先为新鲜组织、福尔马林固定或石蜡包埋组织。这些样品可为切片、涂片、悬液、溶液、rna提取物等适用于本检测的多种形式存在。在其中一个实施例中,该试剂盒包括免疫组化反应试剂。以免疫组化的方式检测cacybp,具有直观、准确的效果。在其中一个实施例中,所述免疫组化反应试剂包括cacybp单克隆或多克隆抗体。在其中一个实施例中,该试剂盒还包括对照样本,所述对照样本中含有预定量的cacybp,作为判断cacybp高表达或低表达的对照。通过含有预定量的cacybp的对照样本的使用,便于病理学检视人员判断评估,区分cacybp的低表达和高表达;并且,根据不同的评估目的,例如作为辅助诊断,或者作为预后评估,再或者作为不同分型的肝癌预后评估,所预设的对照样本中cacybp含量是不同的,需要根据对照目的和区分场景进行调整。本发明公开了一种检测生物样本中cacybp编码mrna的试剂盒,包括有检测生物样本中cacybp编码mrna的试剂。上述试剂盒可用于检测生物样本中mrna的含量,该检测可以为定量检测、半定量检测或定性检测均可,用以辅助肝癌判断或进行预后评估用。在其中一个实施例中,该试剂盒采用定量逆转录pcr法检测。在其中一个实施例中,所述定量逆转录pcr法中,采用以下引物对进行qpcr反应:正向序列:ctcccattacaacgggctatac(seqidno.1);反向序列:gaactgccttccacagagatg(seqidno.2)。在其中一个实施例中,还包括以下内参gapdhqpcr引物对:正向引物:ggagcgagatccctccaaaat(seqidno.7)反向引物:ggctgttgtcatacttctcatgg(seqidno.8)。与现有技术相比,本发明具有以下有益效果:本发明对136例肝癌手术切除标本进行检测,与对应的癌周非癌组织比较,cacybp在癌组织中显著升高;对该136例随访8年,并分析cacybp与临床肿瘤学资料的相关性,结果进一步证实cacybp水平与无瘤生存率和总体生存率呈负相关。并且通过基因敲除和过表达技术的体外肝癌细胞模型,发现cacybp可以促进肝癌细胞生长和侵袭,提示cacybp的在肝癌中的强烈致癌和促进肿瘤进展的作用。还通过蛋白组学和免疫沉淀实验发现,肝癌组织中cacybp与rnf41结合提示cacybp可能是抑制rnf41-e3泛素连接酶降解其下游癌基因底物的作用。上述研究发现表明cacybp及其编码mrna可作为标志物或靶标在肝癌诊断、治疗和预后判断中的应用,开发新型有效的肝癌诊断、预后判断试剂盒,并为肝癌治疗药物提供有效靶点。附图说明图1为cacybp与e3泛素连接酶相互作用的结构示意图;图2为肝癌组织石蜡切片中cacybp的表达情况;图3为136例肝癌患者的无癌生存率分析曲线;图4为136例肝癌患者的总生存率分析曲线;图5为癌组织中cacyby-mrna水平显著高于非癌组织示意图;图6表示利用sk-hep-1细胞株和huh7细胞株各构建了敲低cacybp基因两个位点的细胞株;图7表示利用sk-hep-1细胞株和huh7细胞株各构建了过表达cacybp的细胞株;图8为不同基因位点灭活cacybp表达的细胞株mtt实验;图9为不同基因位点灭活cacybp表达的细胞株mtt实验;图10为cacybp敲减株的平板克隆实验;图11为cacybp敲减株的平板克隆实验;图12为cacybp敲减株的transwell实验;图13为cacybp敲减株的transwell实验示意图;图14为串联亲和纯化技术和蛋白质谱图;图15为蛋白质谱结果示意图;图16为肝癌细胞株sk-hep-1过表达带有flag标签cacybp基因构建成功示意胶图;图17为cacybp与蛋白rnf41免疫共沉淀实验示意胶图。具体实施方式为了便于理解本发明,下面将参照相关附图对本发明进行更全面的描述。附图中给出了本发明的较佳实施例。但是,本发明可以以许多不同的形式来实现,并不限于本文所描述的实施例。相反地,提供这些实施例的目的是使对本发明的公开内容的理解更加透彻全面。除非另有定义,本文所使用的所有的技术和科学术语与属于本发明的
技术领域:
的技术人员通常理解的含义相同。本文中在本发明的说明书中所使用的术语只是为了描述具体的实施例的目的,不是旨在于限制本发明。本文所使用的术语“和/或”包括一个或多个相关的所列项目的任意的和所有的组合。以下数据样本来自于广州市某三甲医院136例肝癌手术切除标本。以下试验基本实验材料来源如下:1、所用的细胞株:sk-hep-1,人肝癌细胞株,来源于中国科学院细胞库/干细胞库(上海);huh7,人肝癌细胞株,来源于中国科学院细胞库/干细胞库(上海)。2、主要实验试剂和设备:opi-men,美国gibco公司;realtimepcr引物,北京睿博兴科生物有限公司;dmem,美国gibico公司;胎牛血清,美国gibico公司;0.25%胰酶,美国gibico公司;逆转录试剂盒,美国promega公司;cellcountingkit,日本东仁化学;dapi,美国lifesciences;ecl发光液,美国milipore公司;depc水,美国sigmaaldrich公司;pvdf膜,美国milipore公司;matrigelmatrix,美国corning公司;trizol,美国sigmaaldrich公司;bca蛋白检测试剂盒,美国thermofisherscientific;rnaasefreeep管,美国axygen公司;pcr仪,德国eppendorf公司;realtimepcr仪,美国roche公司;western曝光仪,美国proteinsimple公司;兔二抗,美国thermofisherscientific;鼠二抗,美国thermofisherscientific;lipofectamine2000,美国lifesciences;3、使用的抗体:表1.抗体信息一抗名称westernblot免疫组化种属分子量公司cacybp1:10001:400rabbit30kdaproteintechtubublin1:2000无rabbit55kdaproteintech实施例1免疫组化技术对cactby基因分布水平的鉴定。1、方法:利用肝组织石蜡切片对cacybp蛋白进行免疫组化检测。(1)脱蜡:烘箱拷片,60℃,30min;二甲苯浸泡溶蜡,2缸,10min/次,共2次;(2)水化:100%酒精浸泡,2缸,10min/次,共2次;梯度酒精浸泡,95%、90%、80%、70%、60%每缸,5min/次,共5次;ddh2o浸泡,1缸,5min/次(3)除去内源性过氧化物酶:3%浓度的h2o2浸泡,1缸,10min;(4)抗原修复:配制ph8.0edta,先煮沸,然后浸泡其中,放到高压锅煮沸修复2-5min;(5)取出片子,甩干,用免疫组化笔对组织切片画圈,快速插入准备好的pbst,浸泡1min后取出,轻轻甩干,加入一抗(cacybp一抗,抗体货号proteintech,#11745-1-ap,浓度1:400),4℃过夜孵育;(6)室温平衡30min,甩掉一抗;pbst浸泡,2~3次,5min/次;(7)加通用二抗,37℃孵育30min,pbst浸泡,2~3次,5min/次(8)dab染色(时间控制在1-5min内),甩掉染色液,pbst浸泡终止染色;(9)苏木素染核浸泡1.5min,自来水洗掉苏木素,苏木素回收;(10)盐酸-酒精浸泡,1-2s,快速取出浸泡于ddh2o中,缓水流慢慢冲洗冲完甩干37℃烘干;(11)用中性树脂封片,通风橱中吹干,完成制片。2、结果。结果如图2所示,该图为肝癌组织石蜡切片中cacybp的表达情况,图中,nt为包含癌周非癌组织和癌组织交界处(比例尺为500μm),n为非癌组织示意图(比例尺为100μm),t为癌组织示意图(比例尺为100μm);图中深色(黄色、棕色和深褐色)显示为cacybp阳性表达;从图中可以看出,cacybp在癌组织(t)中显著高表达,而在癌周非癌组织(nt)中低表达(400x)。上述结果表明,cacybp在癌组织中呈现强阳性表达,而在正常组织中几乎不表达。实施例2cacybp对肝癌预后的预测。具体的,由两位独立的病理学医师对上述免疫组化结果进行评判,把136例病人分为两组:高cacybp评分组(cacybp-h,n=65)和低cacybp评分组(cacybp-l,n=71),进行临床肿瘤学指标的相关性分析以及生存分析。一、方法。1、免疫组化采用双盲评分,采用表达面积×表达强度作为总评分,阳性信号的表达面积分为5个等级:0分(<5%),1分(5%-25%),2分(25%-50%),3分(50%-75%),4分(75%以上)。表达强度分为4个等级:0分(无表达),1分(低强度,信号为浅黄色),2分(中强度,信号为棕色),3分(高强度,信号为深褐色)。最后根据总评分取中位数,标本评分高于中位数的为cacybp高表达,即上述高cacybp评分组(cacybp-h);小于或等于中位数的标本为cacybp低表达,即上述低cacybp评分组(cacybp-l)。2、比较两组中cacybp评分与临床肿瘤学指标的相关性,结果发现cacybp-h组肝癌病人与肝硬化、无包膜肿瘤、较大肿瘤、高胆红素水平、多个肿瘤、白蛋白水平较低、ast较高、饮酒史密切相关(表2)表2:肝癌患者中cacybp评分与临床肿瘤学指标的相关性注:*表示经统计学分析,p值≤0.05。3、把cacybp评分纳入临床肿瘤学指标范围,进一步分析生存相关的临床肿瘤学因素。3.1单因素分析(1)方法:以连续变量以“均数±标准差”表示,分类变量以个数或者百分比表示;连续变量采用t检验或者mann-whitneyu检验进行分析,分类变量采用chi-square检验或者fisher'sexacttest检验进行分析。p值≤0.05为具有显著的统计学意义,所有数据分析采用spsssoftware,version15(spssinc.chicago,il)。(2)结果:结果提示:无包膜、肿瘤越大、多个肿瘤、肿瘤转移、肿瘤复发、肝硬化、癌栓、腹水、高afp、低白蛋白、高谷草转氨酶、高胆红素、较高tnm分期、cacybp-h评分与病人较低生存时间密切相关。3.2多因素分析(1)方法:采用cox回归模型分析肝癌患者预后的相关因素,采用thekaplan-meiermethod评估患者无癌生存与总生存时间的相关因素,危险比(95%可信区间)和p值使用spsssoftware,version15(spssinc.chicago,il)计算分析,p值≤0.05为具有显著的统计学意义。(2)结果:结果提示:肿瘤越大、低白蛋白水平、高tnm分期、高胆红素水平、cacybp-h评分是肝癌病人生存率较低的独立相关因素,具体如下表所示。表3.影响肝癌患者预后的单因素及多因素分析上述多因素分析证实cacybp是肝癌生存率的独立相关因素。4、描绘生存率与cacybp水平的相关性。该136例肝癌病人随访时间为8年(随访终点为手术后8年或者死亡/肿瘤复发),比较cacybp-h和cacybp-l两组病人无癌生存率和总生存率的差异。结果如图3-4所示,图3为136例肝癌患者的无癌生存率分析曲线,图4为136例肝癌患者的总生存率分析曲线;从图中可以看出,cacybp-h评分组患者的无癌生存率显著低于cacybp-l评分组(p=0.0022,图3);同样的,cacybp-h评分组患者的总生存率显著低于cacybp-l评分组(p=0.0011,图4)。上述结果表明,cacybp高表达病人生存显著低于cacybp低表达者。综合上述3和4的结果,证实cacybp具有预测肝癌临床结局的价值,可作为肝癌预后的预测指标。实施例3逆转录技术对肝癌组织及癌旁组织中cacybp-mrna水平进行检测。1、方法。1.1提取冰冻或新鲜肝组织中的mrna。(1)将肝癌及癌旁组织分别放入rnase-freeep管中,每管加入trizol700ml后各放入一颗磁珠,在组织研磨器中匀浆5~10min,转速为40000r/min;(2)将细胞悬液移入ep管中,做好标记,每管分别加入三氯甲烷140μl,震荡15s,室温放置2~3min;(3)4℃离心,12000r/min,15min;(4)吸取上清,计量体积,加入1.5倍体积的无水乙醇,混合均匀后取700μl混合液加入至mirneasyminikit中,以8500g转速离心15s,弃废液;重复加液直至加完以上混合物样品;(5)将700μlrwt加入样品,8500g转速离心15s,弃废液;继续加入rpe700μl,以8500g转速离心15s,弃去液;更换套管,空离心约1min;更换为有盖1.5mlep管,加入rnase-free水30~40μl,8500g转速离心1min;此时ep管中即为总rna,测定浓度,于-80℃保存。2、cacybp逆转录qpcr检测2.1mrna逆转录:mix-1体系:mix-1条件:70℃,5min后立即冰上2min。反转录完毕,此cdna即为mrna定量pcr使用的模板,2.2qpcr扩增。mix-2体系:cacybpqpcr引物序列如下:正向:ctcccattacaacgggctatac;(seqidno.1)反向:gaactgccttccacagagatg;(seqidno.2)gapdhqpcr(内参)引物序列如下:正向:ggagcgagatccctccaaaat;(seqidno.7)反向:ggctgttgtcatacttctcatgg。(seqidno.8)上述gapdh是甘油醛-3-磷酸脱氢酶(glyceraldehyde-3-phosphatedehydrogenase),该酶基因为管家基因,几乎在所有组织中都高水平表达,在同种细胞或者组织中的蛋白质表达量一般是恒定的,故被广泛用作抽提totalrna,poly(a)+rna,westernblot等实验操作的标准化的内参。在本实验中以其作为cacybpmrna鉴定的内参。3、结果。检测结果如下表和图5所示。图5为同一样本的癌组织和非癌组织中cacybpmrna含量。表4.癌组织和非癌组织中mrna水平上述共33例患者组织,癌(t)和癌旁(nt)中cacybp相对于gapdh的表达值如表中所示。从上述结果中可以看出,癌组织中cacyby-mrna水平显著高于非癌组织。通过上述实施例的结果可以看出,cacybp高表达是肝癌患者预后较差的独立危险因素,可预测患者治疗后的无癌生存期和总生存期;也可以辅助诊断肝癌发生。实施例4cacybp促进肝癌细胞生长和增殖实验研究。一、慢病毒制备过表达cacybp质粒。为了进一步探究cacybp促进肝癌生长的生物学功能,我们选取了肝癌细胞株huh7和sk-hep-1,利用逆转录病毒系统各构建了两株cacybpshrna稳定低表达或不表达cacybp的细胞系(shcacybp#1和shcacybp#2,以及shhuh7#1和shhuh7#2)以及稳定高表达cacybp的细胞系(flag-cacybp)。1、质粒构建:(1)瞬时过表达对照质粒:pcdna3.1(+)(购买自invitrogen公司,货号v79020)为一种过表达对照质粒,其参数如下:载体:pcdna3.1(+)载体长度:5428bp抗性:amp+稳定筛选标记:g418报告基因:无启动子:cmv(2)慢病毒制备过表达cacybp质粒:为市售慢病毒制备过表达cacybp质粒(购自clontech公司,货号632152),其参数如下:载体:plvx-dsred-monomer-n1质粒长度:8799bp抗性:amp+稳定筛选标记:puromycin报告基因:无启动子:cmv基因序列:无(3)慢病毒制备敲低cacybp质粒:为市售慢病毒制备敲低cacybp质粒(购自sigma),其参数如下:载体:plko.1质粒长度:7086bp抗性:amp+稳定筛选标记:puro报告基因:无启动子:u62、成功构建两株cacybpshrna稳定表达的细胞系如图6所示为cacybp基因敲除的sk-hep-1和shhuh7细胞系的cacybp表达凝胶电泳示意图,图7所示为稳定高表达cacybp(flag-cacybp)的sk-hep-1和shhuh7细胞系的cacybp表达凝胶电泳示意图。图6中,shnc表示cacybp基因未敲除的阴性对照,shcacybp#1和shcacybp#2分别表示cacybp基因被成功敲除的两株细胞株;图7中,dsred表示红色荧光蛋白,用作对照,flag-cacybp-dsred表示过表达cacybp的质粒,带有flag标签和dsred,可以用flag抗体检测,tubulin表示微管蛋白,在本实验中作为内参;二、cacybp的促癌功能研究实验。1、cacybp促进肝癌细胞增殖。(1)采用mtt法检测。将5x103个sk-hep-1细胞和huh7细胞分别铺入6个96孔板并培养过夜,次日转染对照shnc-sk-hep-1和shnc-huh7,以及cacybp基因敲除细胞株shcacybp#1-sk-hep-1、shcacybp#2-sk-hep-1、shcacybp#1-huh7、shcacybp#2-huh7,并于转染后1、3、5、7天检测细胞生长情况。具体操作:弃去培养上清,换入100μl含mtt0.5mg/ml的新鲜培养基,随后37℃孵育4小时,最后换入100μldmso并震荡10分钟,最终吸光度使用570nm波长检测。(2)结果:结果如图8-9所示,细胞内沉默cacybp表达(基因敲除)时,细胞的生长速度显著低于对照组,图中*表示具有统计学差异p<0.05。2、cacybp促进肝癌细胞克隆形成。利用软琼脂克隆形成实验检测沉默cacybp基因表达对肿瘤细胞非锚定依赖性生长能力的影响。(1)方法。软琼脂培养法常用检测肿瘤细胞和转化细胞系。按照常规方法进行,基本步骤包括:(a)取对数生长期细胞,用0.25%胰蛋白酶消化并轻轻吹打,使之成为单细胞,作活细胞计数,用含20%胎牛血清的dmem培养液调整细胞密度至1×106细胞/l。然后根据实验要求作梯度倍数稀释。(b)用蒸馏水分别制备出1.2%和0.7%两个浓度的低溶点琼脂糖液,高压灭菌后,维持在40℃中不会凝固。(c)按1:1比例使1.2%的琼脂糖和2×dmem培养基(含有2×抗生素和20%的小牛血清)混合后,取3ml混合液注入直径6cm平皿中(10cm平皿加7~10ml),冷却凝固,可作底层琼脂置co2温箱中备用。(d)按1:1比例让0.7%的琼脂糖和2×dmem培养基在无菌试管中相混以后,再向管中加入0.2ml的细胞悬液,充分混匀,注入铺有1.2%琼脂糖底层平皿中,逐形成双琼脂层。待上层琼脂凝固后,置入37℃5%co2温箱中培养10~14天。(e)把平皿放置在倒置显微镜下,观察细胞克隆数。计算形成率。(2)结果。结果如下表和图10-11所示,灭活cacybp表达能显著降低肝癌细胞的非锚定依赖性生长能力,图中*表示具有统计学差异p<0.05。图10中:以sk-hep-1细胞进行克隆形成实验,图a(上图)从左到右分别为用作对照的cacybp基因无效敲除、cacybp基因敲除1号、cacybp基因敲除2号的克隆形成实验结果的代表图;图b(下图)是重复3次的克隆形成实验的的均数,并进行统计学分析。结果提示:cacybp基因敲除1号(shcacybp#1)和cacybp基因敲除2号(andshcacybp#2)的肝癌细胞形成克隆的能力显著降低。图11中:以huh7细胞进行克隆形成实验,图a(上图)从左到右分别为用作对照的cacybp基因无效敲除、cacybp基因敲除1号、cacybp基因敲除2号的克隆形成实验结果的代表图;图b(下图)是重复3次的克隆形成实验的的均数,并进行统计学分析。结果提示:cacybp基因敲除1号(shcacybp#1)和cacybp基因敲除2号(andshcacybp#2)的肝癌细胞形成克隆的能力显著降低。表5:cacybp对肝癌细胞克隆形成的影响上表表示分别使用sk-hep-1及huh7两种细胞进行克隆形成实验,每组三个复孔的数据。3、cacybp促进肝癌细胞侵袭和迁移实验。利用小室浸润实验(transwellassay,boydenchambercoatedbymatrigel)进行cacybp促进肝癌细胞侵袭和迁移能力考查。(1)方法。按照常规方法进行实验:(a)取对数生长细胞,调密度至5x105个细胞/毫升,取细胞悬液100ul接种在24孔transwell板(孔径为8um)上室,加入600ul培养基于下室;(b)上室加入80ulmatrigel胶(使用培养液与胶8:1稀释),在37摄氏度培养箱中孵育4小时,下室加600ul新鲜培养液;(c)将上述24孔板放置37摄氏度,5%co2的培养箱培养24-48小时;(d)取出小室,行结晶紫甲醛染色;(e)在200x光镜下随机选择5个视野进行拍照并记录迁移到小室背面的细胞数,再取其平均值进行数据分析。(2)结果。实验结果如图12-13所示,图12中,图a(上图)从左到右分别为用作对照的cacybp基因无效敲除、cacybp基因敲除1号的克隆形成实验结果的代表图;图b(下图)是重复3次的克隆形成实验的的均数,并进行统计学分析。结果提示:cacybp基因敲除1号(shcacybp#1)的肝癌细胞侵袭和转移的能力显著降低。图13中,图a(上图)从左到右分别为用作对照的cacybp基因无效敲除、cacybp基因敲除2号的克隆形成实验结果的代表图;图b(下图)是重复3次的克隆形成实验的的均数,并进行统计学分析。结果提示:cacybp基因敲除2号(andshcacybp#2)的肝癌细胞侵袭和转移的能力显著降低。上述结果表示,cacybp基因敲除细胞穿过小室的数量明显低于对照组,图中*表示具有统计学差异p<0.05。表5:cacyby对肝癌细胞侵袭和转移的作用上表表示分别使用shcacybp#1及#2两条shrna与shcontrol对照进行transwell实验每组三个复孔的数据。以上实验结果表示,cacybp高表达可加快肝癌细胞的生长,增强癌细胞的侵袭能力,有助于肝癌的转移,具有预测肝癌不良预后,尤其是复发和转移的有效指标;因此,阻断cacybp可显著降低癌细胞的侵袭和转移。实施例5cacybp对rnf41降解下游癌基因通路的潜在调控作用研究。为了进一步研究cacybp的下游效应基因,我们构建了带有标签的cacybp过表达质粒,利用质粒转染技术使cacybp在293t细胞中过表达,利用串联亲和纯化技术和蛋白质谱实验分析,查找与cacybp亲和性较强的蛋白。具体实验步骤如下:先在293t细胞中表达外源sfb-cacybp蛋白,收集过表达细胞裂解后的裂解液,取细胞裂解液与streptavidinsephrose(gehealthcare,17-5113-01)孵育后用biotin(来源:sgima,b4639)洗脱,收集洗脱液后再与s-proteinbeads(来源:novagen,69704)孵育,孵育完成后将珠子离心收集,加入1xloadingbuffer,金属浴煮沸将与珠子结合的蛋白洗脱后上样跑sds-page,考染出条带后将其用干净刀片割(示意图红框部分)下送质谱检测。质谱结果如图14-15所示,结果显示有6条uniquepeptieds可以比对上rnf41,提示rnf41能够与sfb-cacybp共沉淀。图14中,表示未处理蛋白液(input)泳道在55kd(cacybp与sfb标签融合后约为55kd)处有较浅的条带,说明cacybo-sfb在293t细胞中成功表达;“strepbeads”泳道55kd处条带较弱,说明biotin洗脱较为干净;“s-proteinbeads”泳道55kd处有较重的条带,推测应为cacybp-sfb主条带,另在该条带其他大小位置也可以观察到与cacybp相互作用的候选蛋白条带。图15为质谱检测发现rnf41特征肽段。将图14中“s-proteinbeads”泳道红框所示胶条切下进行maldi-tof/tof质谱检测,结果发现rnf41的6个特征肽段(特征肽段在氨基酸序列下用线条进行标记)。这个结果提示了rnf41可能是cacybp的一个结合蛋白。对实验数据进行分析后发现,如图15所示,蛋白rnf41(其核苷酸编码序列如seqidno.5,所示,氨基酸序列如seqidno.6所示)与cacybpp结合存在较大的可能性。进一步,我们构建带有标签的过表达质粒ha-rnf41,联同flag-cacybp过表达质粒,进行免疫共沉淀实验,结果如图16-17所示,cacybp能和蛋白rnf41结合。图16中体现:肝癌细胞株sk-hep-1过表达cacybp基因构建成功,该过表达基因带有flag标签(即flag-cacybp条带),可同时用cacpby抗体和flag抗体检测。图17中体现:进行免疫共沉淀实验,结果进一步验证了cacybp与rnf41蛋白结合。以上结果表明:cacybp通过与rnf41结合发挥生物学作用,rnf41是泛素-蛋白酶体系统(ubiquitin-proteasomesystem,ups)中的e3连接酶,ups是介导细胞内蛋白降解的主要途径,广泛影响细胞生长发育的各个环节,包括增殖、细胞周期、分化、凋亡等细胞生物学活动。rnf41可有效降解一系列促癌基因,从而维持细胞的正常功能;然而,若cacybp与rnf41结合病阻断rnf41降解其下游癌基因底物的作用,则有助于癌肿形成或癌细胞转移。这些研究结果提示阻断cacybp可活化泛素化通路rnf41,促进癌基因降解,最后抑制肝癌细胞生长,为潜在的肝癌治疗新靶点开发奠定了坚实的科学基础。以上所述实施例的各技术特征可以进行任意的组合,为使描述简洁,未对上述实施例中的各个技术特征所有可能的组合都进行描述,然而,只要这些技术特征的组合不存在矛盾,都应当认为是本说明书记载的范围。以上所述实施例仅表达了本发明的几种实施方式,其描述较为具体和详细,但并不能因此而理解为对发明专利范围的限制。应当指出的是,对于本领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干变形和改进,这些都属于本发明的保护范围。因此,本发明专利的保护范围应以所附权利要求为准。序列表<110>璞晞(广州)生物免疫技术有限公司<120>cacybp及其编码mrna在肝癌诊断、治疗和预后判断中的应用<150>201811330524.1<151>2018-11-09<160>8<170>siposequencelisting1.0<210>1<211>22<212>dna<213>人工序列(artificialsequence)<400>1ctcccattacaacgggctatac22<210>2<211>21<212>dna<213>人工序列(artificialsequence)<400>2gaactgccttccacagagatg21<210>3<211>687<212>dna<213>cacybp蛋白(cacybpcalcyclin-bindingprotein)<400>3atggcttcagaagagctacagaaagatctagaagaggtaaaggtgttgctggaaaaggct60actaggaaaagagtacgtgatgcccttacagctgaaaaatccaagattgagacagaaatc120aagaacaagatgcaacagaaatcacagaagaaagcagaacttcttgataatgaaaaacca180gctgctgtggttgctcccattacaacgggctatacggtgaaaatcagtaattatggatgg240gatcagtcagataagtttgtgaaaatctacattaccttaactggagttcatcaagttccc300actgagaatgtgcaggtgcatttcacagagaggtcatttgatcttttggtaaagaatcta360aatgggaagagttactccatgattgtgaacaatctcttgaaacccatctctgtggaaggc420agttcaaaaaaagtcaagactgatacagttcttatattgtgtagaaagaaagtggaaaac480acaaggtgggattacctgacccaggttgaaaaggagtgcaaagaaaaagagaagccctcc540tatgacactgaaacagatcctagtgagggattgatgaatgttctaaagaaaatttatgaa600gatggagacgatgatatgaagcgaaccattaataaagcctgggtggaatcaagagagaag660caagccaaaggagacacggaattttga687<210>5<211>228<212>prt<213>cacybp蛋白(cacybpcalcyclin-bindingprotein)<400>5metalaserglugluleuglnlysaspleuglugluvallysvalleu151015leuglulysalathrarglysargvalargaspalaleuthralaglu202530lysserlysilegluthrgluilelysasnlysmetglnglnlysser354045glnlyslysalagluleuleuaspasnglulysproalaalavalval505560alaproilethrthrglytyrthrvallysileserasntyrglytrp65707580aspglnserasplysphevallysiletyrilethrleuthrglyval859095hisglnvalprothrgluasnvalglnvalhisphethrgluargser100105110pheaspleuleuvallysasnleuasnglylyssertyrsermetile115120125valasnasnleuleulysproileservalgluglyserserlyslys130135140vallysthraspthrvalleuileleucysarglyslysvalgluasn145150155160thrargtrpasptyrleuthrglnvalglulysglucyslysglulys165170175glulysprosertyraspthrgluthraspprosergluglyleumet180185190asnvalleulyslysiletyrgluaspglyaspaspaspmetlysarg195200205thrileasnlysalatrpvalgluserargglulysglnalalysgly210215220aspthrgluphe225<210>6<211>954<212>dna<213>rnf41蛋白(rnf41protein)<400>6atggggtatgatgtaacccgtttccagggggatgttgacgaagatcttatctgccctatt60tgcagtggagtcttggaggagccagtacaggcacctcattgtgaacatgctttctgcaac120gcctgcatcacccagtggttctctcagcaacagacatgtccagtggaccgtagtgttgtg180acggtcgcccatctgcgcccagtacctcggatcatgcggaacatgttgtcaaagctgcag240attgcctgtgacaacgctgtgttcggctgtagtgccgttgtccggcttgacaacctcatg300tctcacctcagcgactgtgagcacaacccgaagcggcctgtgacctgtgaacagggctgt360ggcctggagatgcccaaagatgagctgcccaaccataactgcattaagcacctgcgctca420gtggtacagcagcagcagacacgcatcgcagagctggagaagacgtcagctgaacacaaa480caccagctggcggagcagaagcgagacatccagctgctaaaggcatacatgcgtgcaatc540cgcagtgtcaaccccaaccttcagaacctggaggagacaattgaatacaacgagatccta600gagtgggtgaactcccttcagccagcaagagtgacccgctggggagggatgatctcgact660cctgatgctgtgctccaggctgtaatcaagcgctccctggtggagagtggctgtcctgct720tctattgtcaacgagctgattgaaaatgcccacgagcgtagctggccccagggtctggcc780acactagagactagacagatgaaccgacgctactatgagaactacgtggccaagcgcatc840cctggcaagcaggctgttgtcgtgatggcctgtgagaaccagcacatgggggatgacatg900gtgcaagagccaggccttgtcatgatatttgcgcatggcgtggaagagatataa954<210>7<211>317<212>prt<213>rnf41蛋白(rnf41protein)<400>7metglytyraspvalthrargpheglnglyaspvalaspgluaspleu151015ilecysproilecysserglyvalleuglugluprovalglnalapro202530hiscysgluhisalaphecysasnalacysilethrglntrppheser354045glnglnglnthrcysprovalaspargservalvalthrvalalahis505560leuargprovalproargilemetargasnmetleuserlysleugln65707580ilealacysaspasnalavalpheglycysseralavalvalargleu859095aspasnleumetserhisleuseraspcysgluhisasnprolysarg100105110provalthrcysgluglnglycysglyleuglumetprolysaspglu115120125leuproasnhisasncysilelyshisleuargservalvalglngln130135140glnglnthrargilealagluleuglulysthrseralagluhislys145150155160hisglnleualagluglnlysargaspileglnleuleulysalatyr165170175metargalaileargservalasnproasnleuglnasnleugluglu180185190thrileglutyrasngluileleuglutrpvalasnserleuglnpro195200205alaargvalthrargtrpglyglymetileserthrproaspalaval210215220leuglnalavalilelysargserleuvalgluserglycysproala225230235240serilevalasngluleuilegluasnalahisgluargsertrppro245250255glnglyleualathrleugluthrargglnmetasnargargtyrtyr260265270gluasntyrvalalalysargileproglylysglnalavalvalval275280285metalacysgluasnglnhismetglyaspaspmetvalglnglupro290295300glyleuvalmetilephealahisglyvalglugluile305310315<210>7<211>21<212>dna<213>人工序列(artificialsequence)<400>7ggagcgagatccctccaaaat21<210>8<211>23<212>dna<213>人工序列(artificialsequence)<400>8ggctgttgtcatacttctcatgg23当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1