生物催化制备(S)-4-癸醇的方法与流程
本发明属于生物制药和生物化工技术领域,具体涉及一种酶法不对称还原制备对映体纯的(s)-4-癸醇的方法。
背景技术:
(s)-4-癸醇(如式ii所示)是一种常见且应用广泛的手性醇。由于手性醇的手性中心接有一个活泼的羟基官能团,使得该类物质成为合成许多重要手性药物、农用化学品和天然产品的关键手性中间体。例如,(s)-4-癸醇是制备一种抑制星形胶质细胞激活药物的重要手性中间体,其化学及光学纯度决定了该手性药物的最终质量,因此其制备方法的改进十分重要。
目前,在制备(s)-4-癸醇的方法(包括传统化学法和生物酶催化法)中,仅有一种通过格氏试剂的化学合成方法获得单一构型的手性癸醇。
相关文献(organicprocessresearchanddevelopment,2005,9(6),774-781)报道,描述了以(r)-1,2-环氧辛烷作为反应底物,加入格氏试剂(etmgbr或etmgcl)在溶剂四氢呋喃中对环氧化物进行开环反应形成(s)-4-癸醇。具体来说,加入格氏试剂etmgbr的反应以氰化亚铜和氯化锂作为催化剂在-10~0℃下需反应2小时;加入格氏试剂etmgcl以氯化铜作为催化剂在-40℃惰性气体中需反应3.5小时。以上所述化学法制备(s)-4-癸醇反应条件相对严苛,需要在低温下进行。
另有相关文献(tetrahedronasymmetry,2012,23(8),583-586)报道,以1-乙烯乙酯为底物,脂肪酶为手性催化剂,对消旋体4-癸醇进行手性拆分。反应在30℃下进行16小时,最终所得产品转化率仅为51%,其中s型占33%。该方法虽采用脂肪酶作为催化剂,反应条件温和,但转化率和立体选择性均不理想。
此外,通过4-癸酮经酶催化还原制备高光学纯度的(s)-4-癸醇的生物制备方法,目前仍没有相关文献报道。
技术实现要素:
本发明所要解决的技术问题在于,提供一种高收率高手性纯度的(s)-4-癸醇的制备方法,主要解决现有制备方法工艺条件复杂,难以得到光学纯度高的手性产品,难以实现大规模制备手性纯度高的(s)-4-癸醇的技术问题。
为解决上述技术问题,本发明提供一种生物催化制备(s)-4-癸醇的方法,是以4-癸酮(式i化合物)为原料,在氢源和辅酶存在的条件下,通过酶催化反应制备(s)-4-癸醇(式ii化合物);其中,
所述酶催化反应所用的酶选自酮还原酶、醛酮还原酶、羰基还原酶或醇脱氢酶中的至少一种;
所述酶催化反应的ph为6~8,反应温度为15~50℃;
所述氢源选自异丙醇,或葡萄糖,或异丙醇与葡萄糖的混合物;
所述辅酶选自nad、nadh、nadp或nadph中的至少一种。
具体反应式为:
优选的,所述酶催化反应所用酶为酮还原酶。更优选的,所述酮还原酶为购自合全药业的试剂编号为r308055、r130709、r113020、r103014、或r103022的还原酶。
优选的,所述酶催化反应所用酶的用量为原料质量的0.002~10倍;更优选的,酶的用量为原料质量的0.02~1倍。
优选的,所述氢源的用量为原料质量的0.5~10倍;更优选的,所述氢源中还可以添加葡萄糖脱氢酶(gdh);所述葡萄糖脱氢酶(gdh)的用量为原料质量的0.01~1倍。
优选的,所述辅酶为nad和nadp的组合物。其中,nad的用量为原料质量的0.001~0.1倍,nadp的用量为原料质量的0.001~0.1倍。
优选的,所述酶催化反应的ph为6.2~7.5,反应温度为20~40℃。
具体的,所述酶催化的反应溶剂为水,或水与有机溶剂的混合物。优选的,所述水为纯水或磷酸盐缓冲水溶液;所述磷酸盐缓冲水溶液为含有磷酸盐浓度在0.1~2mmol/l、ph范围为7.0~9.0的kh2po4-k2hpo4或nah2po4-na2hpo4缓冲液。更优选的,所述磷酸盐浓度为0.2mol/l,ph=6.2~7.5。
具体的,所述酶催化反应通过向反应体系中加入缓冲液或碱液进行ph控制。所述缓冲液包括kh2po4-k2hpo4或nah2po4-na2hpo4缓冲液,常用的碱液包括koh或naoh溶液。
具体的,制备方法中,还包括以常规方法进行后处理分离出产物式ii所述的对映体。常规分离方法包括有机溶剂进行萃取、离子交换或层析等。其中,优选使用溶剂萃取法分离所述式ii的对映体。例如,反应结束后,使用二氯甲烷或甲基叔丁基醚等有机溶剂萃取,分层后,分离得有机层,即为粗产品溶液;将粗产品溶液用无水硫酸钠干燥、过滤后,直接在不高于45℃的条件下减压浓缩干,最终得到无色至淡黄色液体,即为对映体过量值不低于97%、纯度不低于95%的产品(s)-4-癸醇。
在本发明的制备方法中,所述反应在ph范围为6~8的条件下进行。当ph小于6时,酶的催化活力显著降低。当ph大于8时,酶活亦有降低。优选的反应ph为6.2~7.5。通过向反应溶剂中加入缓冲液或碱液进行ph控制。
在本发明的制备方法中,所述反应在温度为15~60℃的条件下进行。当温度低于15℃时,反应速度较慢。但温度高于60℃时,酶会不可逆失活。出于保证反应稳定、高效进行的目的,优选的反应温度为20~40℃。
在本发明的制备方法是通过酶催化反应对4-癸酮进行不对称还原来制备(s)-4-癸醇。在本发明的制备方法中,通过酶催化反应能够以高转化率获得高光学纯度的(s)-4-癸醇产品。然后经过常规的后处理操作,即可高收率的制备得到化学纯度高、光学纯度高的手性产物(s)-4-癸醇。
本发明的有益效果在于,以本发明的酶催化方法制备的(s)-4-癸醇,对映体过量值不低于97%,纯度不低于95%。相比于传统方法利用酯或环氧化物等作为原料且反应条件相对苛刻的工艺,通过一种新型酶催化技术高效生产对映体纯的(s)-4-癸醇具有重要意义。该方法操作简单易行,经后处理得产品的产率高,选择性好,适用于大规模工业生产。
附图说明
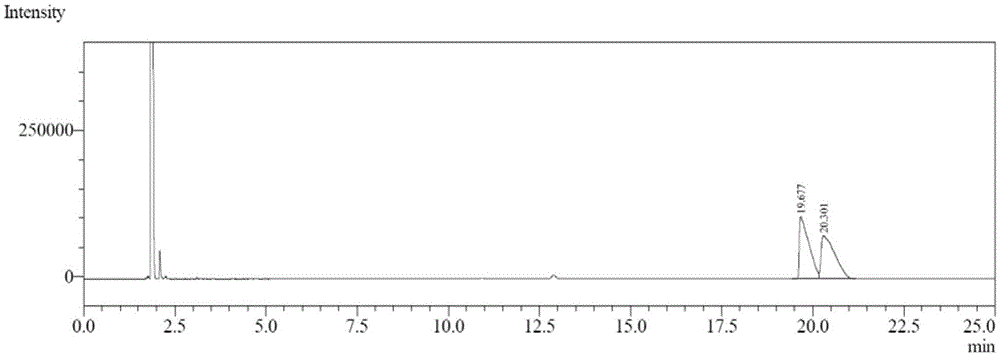
图1为4-癸醇的外消旋物的高效气相色谱法图谱。
图2为按照本发明实施例6的方法转化后的4-癸醇的手性高效气相色谱法图谱,其中12.286min处的峰为原料4-癸酮,19.299min处的峰为目标化合物(s)-4-癸醇。
图3是按照本发明实施例2的方法转化后的4-癸醇的手性高效气相色谱法图谱,其中19.821min处的峰为目标化合物(s)-4-癸醇。
图4是按照本发明实施例1的方法转化后的(s)-4-癸醇的氢谱核磁图谱。1hnmr(400mhz,cdcl3)δppm0.82-0.96(m,6h)1.21-1.51(m,15h)3.54-3.64(m,1h)。
具体实施方式
下面将对本发明的技术方案进行清楚、完整的描述,显然,所描述的实施例是本发明的一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动的前提下所获得的所有其他实施例,都属于本发明保护的范围。
本发明中所使用试剂和原料均市售可得。
实施例1
在50ml玻璃夹套反应瓶中,加入20ml水,0.212gkh2po4和0.557gk2hpo4,搅拌直至固体溶清;加入氢氧化钾调节ph值到6.2-7.5;向反应液中加入3g葡萄糖、1g酮还原酶(商品试剂,购自合全药业,试剂编号r308055),0.02gnadp和0.2ggdh,搅拌后加入2g4-癸酮;调整并控制反应液温度25℃,ph7.0,连续搅拌24小时。
用16ml甲基叔丁基醚萃取反应液,收集有机相,加入少量无水硫酸钠除水后过滤,在30℃减压蒸馏浓缩。所得淡黄色液体即产品(s)-4-癸醇,粗收率为92.7%,经高效气相色谱法分析,转化率99.4%,对映体过量值97.6%。分析条件:岛津气相色谱仪,agilentcyclosil-b(30×0.25mm,0.25μm)手性色谱柱,恒温110℃25min,载气为氮气,载气流速30ml/min,稀释剂为甲基叔丁基醚。产品的核磁图谱见图4。
酶催化反应结束后,通过简单的萃取、分液、浓缩操作即可以高收率高纯度的得到(s)-4-癸醇产品。
通过分析萃取的有机相可知,酶催化反应结束后,以高转化率制备得到了高光学纯度的(s)-4-癸醇。
实施例2
在50ml玻璃夹套反应瓶中,加入20ml水,0.212gkh2po4和0.557gk2hpo4,搅拌直至固体溶清;加入氢氧化钾调节ph值到6.2-7.5;向反应液中加入2g葡萄糖、0.02g酮还原酶(商品试剂,购自合全药业,试剂编号r130709),0.02gnadp和0.1ggdh,搅拌后加入1g4-癸酮;调整并控制反应液温度25℃,ph7.0,连续搅拌24小时。
用16ml甲基叔丁基醚萃取反应液,收集有机相,加入少量无水硫酸钠除水后过滤,在30℃减压蒸馏浓缩。所得淡黄色液体即产品(s)-4-癸醇,粗收率为94.5%,经高效气相色谱法分析,转化率100%,对映体过量值100%。分析条件同实施例1。产品的气相色谱法图谱见图2。
酶催化反应结束后,通过简单的萃取、分液、浓缩操作即可以高收率高纯度的得到(s)-4-癸醇产品。
实施例3
在50ml玻璃夹套反应瓶中,加入20ml水,0.212gkh2po4和0.557gk2hpo4,搅拌直至固体溶清;加入氢氧化钾调节ph值到7.5;向反应液中加入3g异丙醇、1g酮还原酶(商品试剂,购自合全药业,试剂编号r130709)和0.02gnad,搅拌后加入2g4-癸酮;调整并控制反应液温度25℃,ph7.0,连续搅拌24时。
用16ml甲基叔丁基醚萃取反应液,收集有机相,加入少量无水硫酸钠除水后过滤,在30℃减压蒸馏浓缩。所得淡黄色液体即产品(s)-4-癸醇,粗收率为96.2%,经高效气相色谱法分析,转化率100%,对映体过量值100%。分析条件同实施例1。
酶催化反应结束后,通过简单的萃取、分液、浓缩操作即可以高收率高纯度的得到(s)-4-癸醇产品。
实施例4
在50ml玻璃夹套反应瓶中,加入20ml水,0.212gnah2po4和0.557gna2hpo4,搅拌直至固体溶清;加入氢氧化钾调节ph值到7;向反应液中加入3g异丙醇、1g酮还原酶(商品试剂,购自合全药业,试剂编号r308055),0.02gnadp,搅拌后加入2g4-癸酮;调整并控制反应液温度37℃,ph7.0,连续搅拌24小时。
用20ml二氯甲烷萃取反应液,收集有机相,加入少量无水硫酸钠除水后过滤,在30℃减压蒸馏浓缩。所得淡黄色液体即产品(s)-4-癸醇,粗收率为90.1%,经高效气相色谱法分析,转化率96.2%,对映体过量值97.1%。分析条件同实施例1。
酶催化反应结束后,通过简单的萃取、分液、浓缩操作即可以高收率高纯度的得到(s)-4-癸醇产品。
实施例5
在50ml玻璃夹套反应瓶中,加入20ml水,0.212gkh2po4和0.557gk2hpo4,搅拌直至固体溶清;加入氢氧化钾调节ph值到6;向反应液中加入4g葡萄糖、1g酮还原酶(商品试剂,购自合全药业,试剂编号r308055),0.02gnad和1ggdh,搅拌后加入2g4-癸酮;调整并控制反应液温度25℃,ph6.0,连续搅拌24小时。
用22ml甲基叔丁基醚萃取反应液,收集有机相,加入少量无水硫酸钠除水后过滤,在30℃减压蒸馏浓缩。所得淡黄色液体即产品(s)-4-癸醇,粗收率为90.1%,经高效气相色谱法分析,转化率94.7%,对映体过量值97.1%。分析条件同实施例1。
酶催化反应结束后,通过简单的萃取、分液、浓缩操作即可以高收率高纯度的得到(s)-4-癸醇产品。
实施例6
在1l玻璃夹套反应瓶中,加入500ml水,5.3gkh2po4和13.9gk2hpo4,搅拌直至固体溶清;加入氢氧化钾调节ph值到7.0;向反应液中加入30克异丙醇,25g酮还原酶(商品试剂,购自合全药业,试剂编号r308055)和500mgnad,搅拌后加入50g4-癸酮;调整并控制反应液温度25℃,ph7.0,连续搅拌24小时。
反应结束后向反应液中分别加入400ml和300ml二氯甲烷及50g硅藻土搅拌2h,萃取两次过滤分层后取下层有机相。另用100ml二氯甲烷洗涤硅藻土滤饼,重复以上操作后合并有机相。在40℃减压蒸馏浓缩有机相,所得淡黄色液体即产品(s)-4-癸醇,粗收率为81.7%,经高效气相色谱法分析,转化率99.9%,对映体过量值97.5%。分析条件:岛津气相色谱仪,agilentcyclosil-b(30×0.25mm,0.25μm)手性色谱柱,恒温110℃25min,载气为氮气,载气流速30ml/min,稀释剂为乙醇。产品的气相色谱法图谱见图3。
综上所述,上述各实施例仅为本发明的较佳实施例而已,并不用以限定本发明的保护范围,凡在本发明的精神和原则之内,所做的任何修改、等同替换、改进等,皆应包含在本发明的保护范围内。
- 还没有人留言评论。精彩留言会获得点赞!