一种检测加热不燃烧卷烟总粒相物细胞毒性的方法与流程
本发明属于烟草制品的安全性生物学效应评价技术领域,特别涉及一种检测加热不燃烧卷烟总粒相物细胞毒性的方法。
背景技术:
中性红细胞毒性法和噻唑蓝法(mtt)具有简便、快捷、灵敏等特点,是目前应用较多的两种毒理学检测细胞毒性的方法。国际烟草科学研究合作中心coresta组织于2002年成立了卷烟烟气体外毒理测试工作组,经过大量的文献调研及研究工作,该工作组推荐采用中性红细胞毒性试验对卷烟烟气冷凝物潜在的细胞毒性进行检测,该检测方法目前已经被国内外烟草公司广泛采用。
烟草监管立法的日趋严格以及吸烟与健康研究的深入,导致了烟草公司寻求风险更低、无环境烟气的新型烟草制品。加热非燃烧型卷烟,其特征在于加热烟草而非燃烧烟草,向消费者提供一定的烟草特征感受。加热不燃烧卷烟制品避免了传统卷烟制品燃烧时产生的复杂混合物所带来的危害,现阶段已成为国外烟草公司从传统卷烟制品转向的新方向之一。
检测对象的改变导致样品的前处理方法、检测用细胞、检测剂量等出现很大差异,这些差异会对试验结果的准确性产生较大影响,现有的用于检测卷烟烟气细胞毒性的中性红细胞毒性法已经不能满足加热不燃烧卷烟制品细胞毒性检测的需要。目前,国内外研究机构及烟草公司尚未有针对加热不燃烧卷烟制品的细胞毒性的准确有效的检测方法。
技术实现要素:
本发明的目的是提供一种检测加热不燃烧卷烟总粒相物细胞毒性的方法,其以加热不燃烧卷烟总粒相物作为检测基础,能够增强检测结果的准确性,进而更为有效地评价加热不燃烧卷烟制品的安全性。
本发明中所使用的rpmi1640细胞培养基购买于市场任何可购买到的商品公司。
一种检测加热不燃烧卷烟总粒相物细胞毒性的方法,包括以下步骤:
(1)样品前处理:采用直线型吸烟机,在抽吸容量为55.0ml,持续时间3s,抽吸频率为30s的抽吸条件下,连续抽吸10口,用直径为44mm的剑桥滤片捕集,分别于抽吸前、抽吸后称量烟气捕集器的质量,按照公式(1)计算加热不燃烧卷烟总粒相物的质量mtpm;
mtpm=m1-m0(1)
式中:
m0——抽吸前烟气捕集器的质量,单位为毫克(mg);
m1——抽吸后烟气捕集器的质量,单位为毫克(mg);
捕集完毕后,将捕集后的剑桥滤片放入50ml的三角瓶中,加入二甲基亚砜,使加热不燃烧卷烟总粒相物在二甲基亚砜中的浓度为40mg/ml;将此三角瓶置于超声仪上超声30min;再用无菌滤纸过滤收集二甲基亚砜萃取液,分装至1ml的冻存管中,-80℃保存待用;
(2)人鼻腔上皮细胞单细胞悬浮液的制备:人鼻腔上皮细胞rpmi2650复苏后,接种到25cm2细胞培养瓶中,加入10mlrpmi1640细胞培养基,置于37℃、5%co2培养箱中培养,倒置显微镜观察培养细胞的汇合和形态情况,待细胞长至70%~90%的汇合率时,移除培养瓶中的rpmi1640细胞培养基,用磷酸缓冲液洗两次,弃洗液;加入1ml0.25%(w/v)的胰蛋白酶溶液单层孵育1~2min,用rpmi1640细胞培养基悬起,形成单细胞悬浮液;
(3)人鼻腔上皮细胞单细胞悬浮液的细胞浓度计算:用血球计数板计数法对步骤(2)所得人鼻腔上皮细胞单细胞悬浮液的细胞浓度进行计算,得到每毫升单细胞悬浮液的活细胞数;
(4)人鼻腔上皮细胞单细胞悬浮液的接种:将步骤(3)计数后的人鼻腔上皮细胞单细胞悬浮液用rpmi1640细胞培养基稀释至2.0×105个/ml,再按接种量为200μl/孔接种到96孔细胞培养板中,然后将96孔细胞培养板置于37℃、5%co2培养箱内培养24h;
(5)受试物分组:将受试物分为四组:空白组、细胞对照组、阳性对照组和检测样品组;各组的构成为:空白组不种植人鼻腔上皮细胞,只加rpmi1640细胞培养基;细胞对照组种植人鼻腔上皮细胞并加rpmi1640细胞培养基;阳性对照组加入200μg/ml的十二烷基硫酸钠200μl;检测样品组加入步骤(1)所得待测液并加rpmi1640细胞培养基;
(6)受试物检测剂量的设定:步骤(1)所得待测液的最终浓度为10个非零剂量,分别为:60μg/ml、120μg/ml、180μg/ml、240μg/ml、300μg/ml、360μg/ml、420μg/ml、480μg/ml、540μg/ml、600μg/ml;
(7)受试物培养品的制备:移除步骤(4)中96孔细胞培养板内的培养基,再按步骤(5)进行分组,用rpmi1640细胞培养基将细胞培养板中每孔的液体体积补足至200μl/孔;做8孔平行,为了避免边缘效应,数据统计时去除边缘2孔采用中间6孔的数据;
(8)孵育受试物:将步骤(7)加样后的96孔细胞培养板置于37℃、5%co2培养箱中孵育24h;
(9)染料孵育:将步骤(8)孵育后的空白组、细胞对照组、阳性对照组和检测样品组中加入浓度为5mg/ml的mtt溶液,20μl/孔,再置于37℃、5%co2培养箱中孵育4h后移除96孔细胞培养板中的液体,加入dmso溶液200μl/孔,置于微板振荡器内振荡10min;
(10)测定吸光值:将步骤(9)染料孵育后的空白组、细胞对照组、阳性对照组和检测样品组,用酶标仪在490nm波长下检测吸光值;
(11)计算细胞存活率:根据所得吸光值,按照下列公式计算细胞存活率:
式中:
x——细胞存活率;
odn——检测样品组多孔平均的吸光值;
odo——空白组多孔平均的吸光值;
odc——细胞对照组多孔平均的吸光值;
(12)绘制细胞存活率曲线:
根据10个非零剂量及0剂量对应的细胞存活率绘制曲线,即可确定所检测的加热不燃烧卷烟总粒相物的细胞毒性。
本发明有益效果:
本发明综合考察了加热不燃烧卷烟的使用特点和作用方式,且根据加热不燃烧卷烟作用靶细胞选取人鼻腔上皮细胞rpmi2650作为细胞毒性试验检测用细胞,并确定了样品检测剂量,形成了适合加热不燃烧卷烟的细胞毒性试验检测方法。本发明对样品检测剂量的优化设定以及靶细胞的正确选择,使得本方法能够准确有效的检测加热不燃烧卷烟总粒相物的细胞毒性。
附图说明
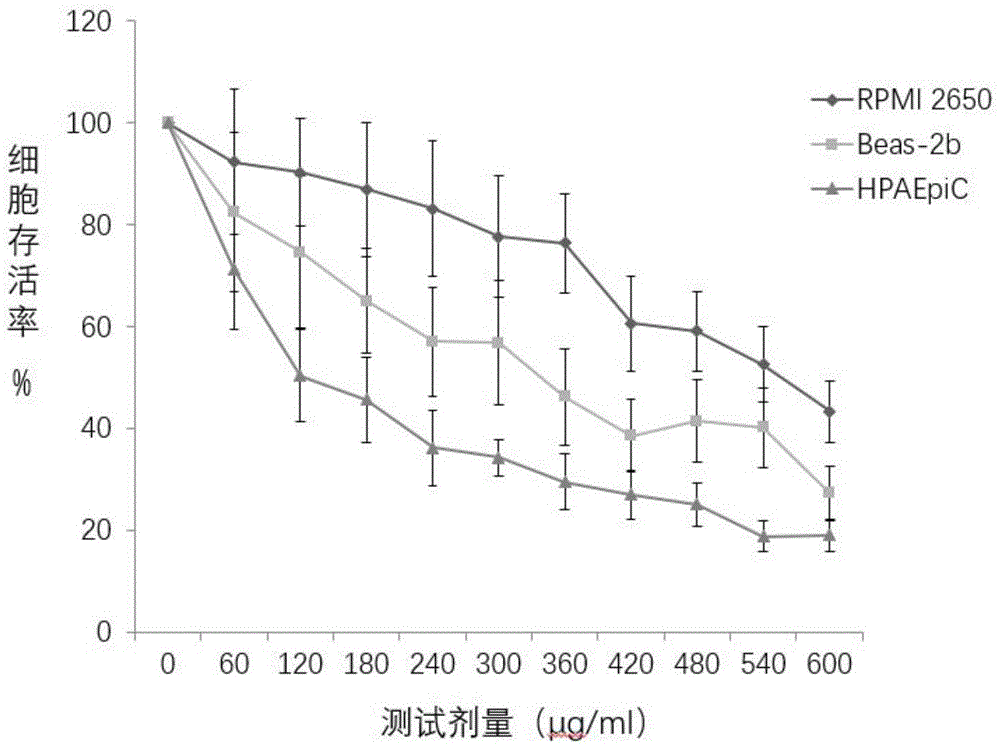
图1是实施例1检测加热不燃烧卷烟总粒相物对三种细胞毒性的细胞存活率曲线图。
图2是实施例1中使用的三种受试细胞的细胞倍增时间图。
具体实施方式
下面将结合具体实例对本发明做详细描述,但并不限制本发明。
实施例1
以剑桥滤片捕集的加热不燃烧卷烟总粒相物作为样品,分别以人鼻腔上皮细胞(rpmi2650)、人支气管上皮细胞(beas-2b)、人肺泡上皮细胞(hpaepic)检测其细胞毒性。
具体检测过程,包括以下步骤:
(1)样品前处理:采用直线型吸烟机,在抽吸容量为55.0ml,持续时间3s,抽吸频率为30s的抽吸条件下,连续抽吸10口,用直径为44mm的剑桥滤片捕集,分别于抽吸前、抽吸后称量烟气捕集器的质量,按照公式(1)计算加热不燃烧卷烟总粒相物的质量mtpm;
mtpm=m1-m0(1)
式中:
m0——抽吸前烟气捕集器的质量,单位为毫克(mg);
m1——抽吸后烟气捕集器的质量,单位为毫克(mg);
捕集完毕后,将捕集后的剑桥滤片放入50ml的三角瓶中,加入二甲基亚砜,使加热不燃烧卷烟总粒相物在二甲基亚砜中的浓度为40mg/ml;将此三角瓶置于超声仪上超声30min;再用无菌滤纸过滤收集二甲基亚砜萃取液,分装至1ml的冻存管中,-80℃保存待用;
(2)单细胞悬浮液的制备:人鼻腔上皮细胞(rpmi2650)、人支气管上皮细胞(beas-2b)、人肺泡上皮细胞(hpaepic)复苏后,接种到25cm2细胞培养瓶中,加入10mlrpmi1640细胞培养基,置于37℃、5%co2培养箱中培养,倒置显微镜观察培养细胞的汇合和形态情况,待细胞长至70%~90%的汇合率时,移除培养瓶中的rpmi1640细胞培养基,用磷酸缓冲液洗两次,弃洗液;加入1ml0.25%(w/v)的胰蛋白酶溶液单层孵育1~2min,用rpmi1640细胞培养基悬起,形成单细胞悬浮液;
(3)单细胞悬浮液的细胞浓度计算:用血球计数板计数法对步骤(2)所得单细胞悬浮液的细胞浓度进行计算,得到每毫升单细胞悬浮液的活细胞数;
(4)单细胞悬浮液的接种:将步骤(3)计数后的单细胞悬浮液用rpmi1640细胞培养基稀释至2.0×105个/ml,再按接种量为200μl/孔接种到96孔细胞培养板中,然后将96孔细胞培养板置于37℃、5%co2培养箱内培养24h;
(5)受试物分组:将受试物分为四组:空白组、细胞对照组、阳性对照组和检测样品组;各组的构成为:空白组不种植人鼻腔上皮细胞,只加rpmi1640细胞培养基;细胞对照组种植人鼻腔上皮细胞并加rpmi1640细胞培养基;阳性对照组加入200μg/ml的十二烷基硫酸钠200μl;检测样品组加入步骤(1)所得待测液并加rpmi1640细胞培养基;
(6)受试物检测剂量的设定:步骤(1)所得待测液的最终浓度为10个非零剂量,分别为:60μg/ml、120μg/ml、180μg/ml、240μg/ml、300μg/ml、360μg/ml、420μg/ml、480μg/ml、540μg/ml、600μg/ml;
(7)受试物培养品的制备:移除步骤(4)中96孔细胞培养板内的培养基,再按步骤(5)进行分组,用rpmi1640细胞培养基将细胞培养板中每孔的液体体积补足至200μl/孔;做8孔平行,为了避免边缘效应,数据统计时去除边缘2孔采用中间6孔的数据;
(8)孵育受试物:将步骤(7)加样后的96孔细胞培养板置于37℃、5%co2培养箱中孵育24h;
(9)染料孵育:将步骤(8)孵育后的空白组、细胞对照组、阳性对照组和检测样品组中加入浓度为5mg/ml的mtt溶液,20μl/孔,再置于37℃、5%co2培养箱中孵育4h后移除96孔细胞培养板中的液体,加入dmso溶液200μl/孔,置于微板振荡器内振荡10min;
(10)测定吸光值:将步骤(9)染料孵育后的空白组、细胞对照组、阳性对照组和检测样品组,用酶标仪在490nm波长下检测吸光值;
(11)计算细胞存活率:根据所得吸光值,按照下列公式计算细胞存活率:
式中:
x——细胞存活率;
odn——检测样品组多孔平均的吸光值;
odo——空白组多孔平均的吸光值;
odc——细胞对照组多孔平均的吸光值;
(12)绘制细胞存活率曲线:
根据10个非零剂量及0剂量对应的细胞存活率绘制曲线,即可确定所检测的加热不燃烧卷烟总粒相物的细胞毒性。
由图1可以看出,加热不燃烧卷烟对受试的三种细胞的存活率与检测剂量间存在剂量效应关系,加热不燃烧卷烟总粒相物对不同细胞的细胞毒性有显著差异(p<0.05)。
不同的受试细胞对相同的样品测试结果定性结果一致,样品间相对定量趋势一致,以上候选细胞均能用于溶剂的生物学效应测试。不同的受试细胞对溶剂的耐受性存在显著差异,当受试剂量相同时,人鼻腔上皮细胞(rpmi2650)耐受性较高,人支气管上皮细胞(beas-2b)次之,人肺泡上皮细胞(hpaepic)较低。图2为检测用细胞的细胞倍增时间,在24h的测试周期内,rpmi2650细胞的增殖较快。
综上所述,本发明综合考察了加热不燃烧卷烟制品的暴露途径,作用方式,建立了加热不燃烧卷烟制品前处理方法,且根据测试细胞的耐受性高和细胞倍增时间短的特点,选取了人鼻腔上皮细胞rpmi2650作为加热不燃烧卷烟制品细胞毒性试验检测用细胞,并确定了样品检测剂量,形成了适合加热不燃烧卷烟制品的细胞毒性试验检测方法。样品的有效处理、检测剂量的优化设定以及靶细胞的正确选择,使得本方法能够准确有效的检测加热不燃烧卷烟总粒相物细胞毒性。
- 还没有人留言评论。精彩留言会获得点赞!