改进的转座酶多肽及其用途的制作方法
本发明涉及具有增加的溶解度的改进的转座酶多肽。本发明的所述酶是基于睡美人(sb)转座酶开发的。本发明还提供了编码或含有所述改进的转座酶的核酸、载体和重组细胞,以及转座酶系统。此外,提供了本发明所述的转座酶用于基因递送的医学和非医学用途。本发明特别可用作在基于遗传修饰细胞的用于治疗各种疾病的治疗方法中进行基因递送的工具。
发明背景
dna转座子是遍布生命树的离散遗传实体,其可以在基因组内和基因组之间移动。它们是促进基因组重塑、进化变化、抗生素抗性决定子的传递以及新生物学功能如适应性免疫的发展的重要进化力。由于dna转座子的天然特性,dna转座子已被成功地用作转基因和功能基因组学中的人工基因载体和插入诱变剂。
通过从鲑鱼的基因组中重建睡美人(sb)转座子来首次实现将dna转座子用于脊椎动物中的基因组操作。应用的sb转座子系统由转座子和转座酶蛋白组成,所述转座子由侧翼为特异性sb反向重复(ir)的目的基因(遗传货物)组成,所述转座酶蛋白由单独的质粒或基因座表达。转座酶能特异性结合ir,从供体基因座切割转座子,并将其整合到新的基因组位置。sb在脊椎动物基因组中具有异常高的插入效率,这允许其发展成为一种成功地应用于高等生物的转基因、干细胞生成和癌症基因发现的主要遗传工具。
重要的是,sb现在也被用作许多临床试验中的非病毒基因递送载体,其中五个临床试验旨在通过掺入针对恶性肿瘤特异性抗原的嵌合抗原受体(car)来离体修饰t细胞。在这些研究中,sb转座酶将来自供体质粒的携带car基因的转座子插入到患者来源的t细胞的基因组中,随后将所述细胞再输注到癌症患者中。所引入的car为t细胞提供了新的特异性,以区别性地靶向癌细胞,并在遇到抗原时引发效应子功能。最成功的car-t疗法靶向在恶性b细胞中过表达cd19抗原。这种疗法在急性和慢性白血病的治疗中已显示出前所未有的响应率(70%-90%),并且在接下来的几年将可能进入对许多b细胞恶性肿瘤的主流护理。然而,对于大量患者的治疗,迫切需要提高制造可行性和安全性,这也是一般基因治疗的关键要求。
因为sb是简单的二元合成系统,所以它比病毒载体便宜,能更容易和更快速地生产和实施。这尤其为一次性使用和个性化应用提供了特别的优势。非病毒sb载体的使用还降低了患者中不期望的免疫应答激活的风险,这构成了与在一般基因治疗应用和癌症免疫疗法(即car-t细胞疗法)中使用病毒载体相关的主要安全问题。此外,与优先插入活性转录区或调控区的γ-逆转录病毒和慢病毒载体相比,sb呈现了近乎随机的基因组整合模式,从而降低了插入诱变和基因毒性的风险。与基因组编辑核酸酶如锌指、talen和cas9不同,sb转座酶直接且精确地将其货物整合到染色体中,而不会在靶基因座处产生潜在有害的双链断裂。因此,sb的插入率和安全性不依赖于靶细胞中修复机构的效率。这些优势使得sb成为临床试验中用于car-t细胞工程的唯一非病毒基因递送载体,这在最近几年引发了对sb系统的相当大的商业兴趣。
虽然sb系统通常具有比病毒载体低的基因转移效率,但新策略-如改进其组分的设计和递送方法,以及car阳性细胞的选择性增殖-最近将sb介导的t细胞工程的成功增加到类似于病毒方法的水平。尽管有了这些改进,但仍然存在重要的问题。特别地,长期的转座酶表达可导致不受控制的进行性转座,这可能导致转基因重新活动、不期望的插入事件、基因组不稳定性和细胞毒性。此外,从表达载体插入sb转座酶基因(例如通过同源重组)可导致无数的转座酶产生,并且转座酶启动子的意外获得可引起致癌基因的激活或破坏靶细胞中的基因调节网络。这引起了对当前sb系统的安全性的关注,并突出了对减少或减轻这些风险的技术进步的需要。
为了避免这些风险,非常期望直接递送sb转座酶蛋白,因为它可以帮助实现更高的效率/时间控制并提高基于转座的细胞工程的安全性,尤其是用于治疗应用。然而,迄今为止,生产足够数量和质量的活性重组sb转座酶具有挑战性。
在第一方面,通过转座酶多肽解决了上述问题,与转座酶的参照氨基酸序列-如非突变但人工转座酶或野生型酶相比,所述转座酶多肽包含至少一个突变的氨基酸残基,其中所述至少一个突变的氨基酸残基位于转座酶的催化结构域内。催化结构域优选在例如sb100x(seqidno:2)的残基150与250的氨基酸序列内。根据本发明的参照转座酶优选为野生型酶或者基因工程酶如sb10、sb11或sb100x的sb转座酶。
与现有技术的sb100x酶相比,转座酶多肽具有几个令人惊讶的优势。与现有技术中的酶相比,本发明在实施例部分中显示,本发明的转座酶在重组蛋白表达中具有较高的蛋白产量,增加的溶解度,这有利于经由电穿孔递送蛋白(更好地溶于电穿孔缓冲液中),该酶较为稳定,不易于蛋白降解,以及特别是较为热稳定的,这在电穿孔过程中也是有利的。
本发明提供了经由直接递送突变的转座酶变体来实现哺乳动物细胞的有效、稳定和受控的基因工程的安全且有效的策略。本发明的新转座酶变体适合大规模重组蛋白生产和转染,其允许成功地工程化一系列哺乳动物细胞系和制备嵌合抗原受体(car)t-细胞。被称为“sbprotact”的本发明策略提供了一种减轻安全问题,并且使得能够在临床应用中最大程度地控制转座酶系统的新方法。最后,本发明的转座酶被证明在相同的转基因比率下每个细胞产生较少的插入,因此允许严格受控的基因递送。
本文使用的术语“转座酶”是指这样的酶,其是能够转座的功能性核酸-蛋白复合物的组分,并介导转座。术语“转座酶”也指来自逆转录转座子或逆转录病毒来源的整合酶。本文使用的“转座反应”是指转座子插入靶核酸的反应。转座反应中的主要组分是转座子和转座酶或整合酶。例如,根据本发明的转座酶系统优选是所谓的“睡美人(sb)”转座酶。在某些方面,转座酶是具有改善的特性如增强的酶功能的工程化酶。工程化sb转座酶的一些具体实例包括但不限于sb10、sb11或sb100×sb转座酶(参见,例如,mates等人,nat.gen.2009,通过引用并入本文)。可以使用其它转座系统,例如ty1((devine和boeke,1994以及wo95/23875)、tn7(craig,1996)、tn10和is10(kleckner等人,1996)、mariner转座酶(lampe等人,1996)、tc1(vos等人,1996)、tn5(park等人,1992)、p元件(kaufman和rio,1992)和tn3(ichikawa和ohtsubo,1990)、细菌插入序列((ohtsubo和sekine,1996)、逆转录病毒(varmus和brown1989)和酵母的逆转录转座子(boeke,1989)。
在本发明的优选实施方案中,转座酶是睡美人(sb)转座酶,优选为sb100x(seqidno:2)或衍生自sb100x的酶。
因此,根据本发明的转座酶多肽是具有转座酶活性的多肽,其中至少一个突变的氨基酸残基是位于sb转座酶(优选sb100x转座酶)的氨基酸150至250的残基。
在一些实施方案中,优选地,所述至少一个突变的氨基酸残基是至少两个突变的氨基酸残基,或者至少3个、4个、5个或更多个氨基酸。优选地,当本发明的转座酶多肽的序列与sb转座酶,优选sb100x的序列比对时,本发明的转座酶多肽在氨基酸170至180和/或207至217中的任一个中突变。更优选地,所述至少一个突变的氨基酸残基选自sb转座酶,优选sb100x的氨基酸176和/或212。最优选地,所述至少一个突变的氨基酸残基被突变为丝氨酸残基,并且优选为c176s、或c176s和i212s。
在其它实施方案中,本发明的转座酶多肽还包含与seqidno:1(hssb)所示的残基150至250的氨基酸序列具有至少60%、70%、80%、90%、95%、96%、97%、98%、99%,最优选100%序列同一性的氨基酸序列。与seqidno:2的序列相比,优选转座酶多肽包含至少c176突变,优选c176s。甚至更优选地,转座酶多肽还包含在i212位的突变,优选i212s。
在一些实施方案中,本发明的转座酶多肽包含与seqidno:1或3(hssb)所示的全长氨基酸序列具有至少60%、70%、80%、90%、95%、96%、97%、98%、99%,最优选100%序列同一性的氨基酸序列。优选地,虽然在一些实施方案中序列同一性的程度低于100%,但上述至少一个突变应存在于本发明的转座酶多肽中。
如本文所用,术语“相同的”或“同一性”百分比,当在本文中在两个或更多个核酸或蛋白质/多肽序列的上下文中的任何地方使用时,是指这样的两个或更多个序列或子序列:其为相同的或者具有(或至少具有)指定百分比的相同的(即,当相对比较窗口或指定区域,针对最大一致性进行比较和比对时,相对指定区域-优选相对其全长序列-具有或至少约60%同一性,优选具有或至少65%、70%、75%、80%、85%、90%、91%、92%、93%或94%同一性,以及更优选具有或至少约95%、96%、97%、98%、99%或更高同一性)氨基酸残基或核苷酸,如使用序列比较算法,或者通过手动比对和目测(参见,例如,ncbi网站)测量的。在特定的实施方案中,例如当将本发明的转座酶的蛋白质或核酸序列与例如参照(未突变的转座酶)进行比较时,可以通过ncbi中提供的blast搜索来确定同一性百分比;特别是对于氨基酸同一性,使用具有以下参数的blastp2.2.28+的那些:矩阵:blosum62;空位罚值:存在:11,延伸:1;相邻词阈值(neighboringwordsthreshold):11;多命中窗口(windowformultiplehits):40。
此外,在一些实施方案中,与参照未突变的转座酶多肽相比,本发明的转座酶多肽具有增加的溶解度,优选地,其中所述参照未突变的转座酶多肽是sb100x转座酶,优选如seqidno:2(未突变的sb100x)所示。
在本发明的另一个方面,提供了包含编码本文以上描述的转座酶多肽的核酸序列的多核苷酸,优选地,其中所述多核苷酸是rna或dna。例如,rna可以以信使rna(mrna)的形式提供,如果将mrna导入生物细胞,则该mrna允许直接翻译成本发明的转座酶多肽。
本发明的另一方面涉及包含本发明的多核苷酸的载体。还提供了表达构建体,其包含编码本发明转座酶多肽的可表达多核苷酸和启动子元件,其中所述启动子元件与所述可表达多核苷酸可操作地连接以允许所述多核苷酸的表达。
还提供了重组细胞,其包含本发明的转座酶多肽、本发明的多核苷酸、或者本发明的载体和/或表达构建体。
重组细胞优选为适于重组蛋白表达的细胞,优选适于本发明转座酶多肽的重组蛋白表达的细胞。如细菌细胞或真核细胞,最优选细菌细胞,如大肠杆菌或昆虫细胞,如果蝇s2细胞或哺乳动物细胞,如hek293t细胞。
又一方面涉及转座子系统,其包含:
(a)转座子单元,其含有反向末端重复(itr)或同向末端重复(dtr),所述反向末端重复(itr)或同向末端重复(dtr)位于待插入靶细胞基因组中的目标序列的侧翼;以及
(b)如本文以上描述的转座酶多肽、多核苷酸、载体和/或表达构建体。
在本文中,术语“转座子单元(transposonunit)”是指核酸构建体,其包含转座子基因序列和待导入靶细胞基因组中的靶序列。通常转座子单元是核酸,并且可以是适于转座的任何形式的载体。
如本文所用,术语“反向末端重复”是指位于转座子单元的一端的序列,当与位于载体或转座子单元的相对端的互补序列组合使用时,该序列可以被转座酶多肽切割。该对反向末端重复涉及本公开内容的转座子单元的转座子的转座活性,特别涉及目标dna的dna添加或去除以及切除和整合。在一个实例中,至少一对反向末端重复似乎是质粒中转座活性所需的最小序列。在另一个实例中,本公开内容的转座子单元可以包括至少两对、三对或四对反向末端重复。如本领域技术人员所理解的,为了促进容易克隆,必需的末端序列可以尽可能短,从而含有尽可能少的反向重复。因此,在一个实例中,本公开内容的转座子单元可以包含不超过一对、不超过两对、不超过三对或不超过四对的反向末端重复。在一个实例中,本公开内容的转座子单元可以仅包括一个反向末端重复。尽管不希望受到理论的束缚,但设想具有多于一个反向末端重复可能是不利的,因为它可能导致非特异性转座酶结合多个反向末端重复,并导致除去期望序列或插入不期望的序列。本公开内容的反向末端重复可以形成完美的反向末端重复(或可互换地称为“完美反向重复”)或不完美的反向末端重复(或可互换地称为“不完美反向重复”)。如本文所用,术语“完全反向重复”是指以相反方向放置的两个相同的dna序列。以上对具有itr的转座子单元的描述也适用于具有dtr的转座子单元。
可以与本发明的本发明转座子多肽/核酸一起使用的转座子系统例如公开于wo2017/050448a1中,将其通过引用包括在本公开内容中。
根据本发明的转座子系统是优选的,其中(a)的所述转座子单元呈微环的形式。然而,转座子单元可以是其它核酸系统。但是,在t细胞工程的背景下,微环是优选的。
在优选的实施方案中,本发明的转座子系统是sb转座子系统。
此外,本发明的另一方面涉及如所述的转座子系统用于基因递送至靶细胞中。基因递送优选是离体基因递送至靶细胞中,如选自以下的靶细胞:干细胞,如造血干细胞或胚胎干细胞、t细胞、b细胞或中国仓鼠卵巢(cho)细胞。最优选的是用于产生cart细胞的本发明的系统或化合物。
如本文所用,术语“嵌合抗原受体”(car)是指与细胞(如t细胞或nk-92细胞)的细胞内信号传导结构域融合的细胞外抗原结合结构域。
还提供了用于将基因递送至靶细胞的方法,其包括以下步骤:
(a)使所述转座子系统与靶细胞接触;
(b)在允许培养所述靶细胞的条件下培养所述靶细胞。
在另一方面,提供了药物组合物,其包含转座酶多肽、多核苷酸、载体和/或表达构建体,以及药学上可接受的载体和/或赋形剂。
此外,另一方面涉及试剂盒,其包含:
(a)转座子单元,其含有反向末端重复(itr)或dtr,所述反向末端重复(itr)或dtr位于待插入靶细胞基因组中的目标序列侧翼;以及
(b)如本文所述的本发明的转座酶多肽、多核苷酸、载体和/或表达构建体。
本发明的化合物和系统可以优选地应用于医学。因此,本发明的这些化合物和系统优选用于疾病的治疗。这种疾病可以是增殖性疾病,如癌症。对于癌症治疗,本发明可以用于产生修饰的免疫细胞的背景中。例如,本发明可以用于将t细胞受体(tcr)或car或其它免疫分子引入免疫细胞中,以增强和靶向患者针对癌细胞的免疫系统。可以被修饰的免疫细胞可以选自人t淋巴细胞或b细胞。可以从本发明获益的其它疾病为遗传性疾病,其特征在于基因功能丧失。在此类疾病中,可以用本发明修饰细胞以包括疾病相关基因的健康拷贝。在本发明的上下文中优选使用的其它靶细胞是干细胞,如例如胚胎干细胞或成体干细胞,如造血干细胞。
以下附图、序列表和实施例仅用于说明本发明,而不应被解释为将本发明的范围限制于在实施例中描述的本发明的特定实施方案。本文引用的所有参考文献据此通过引用以其整体并入。
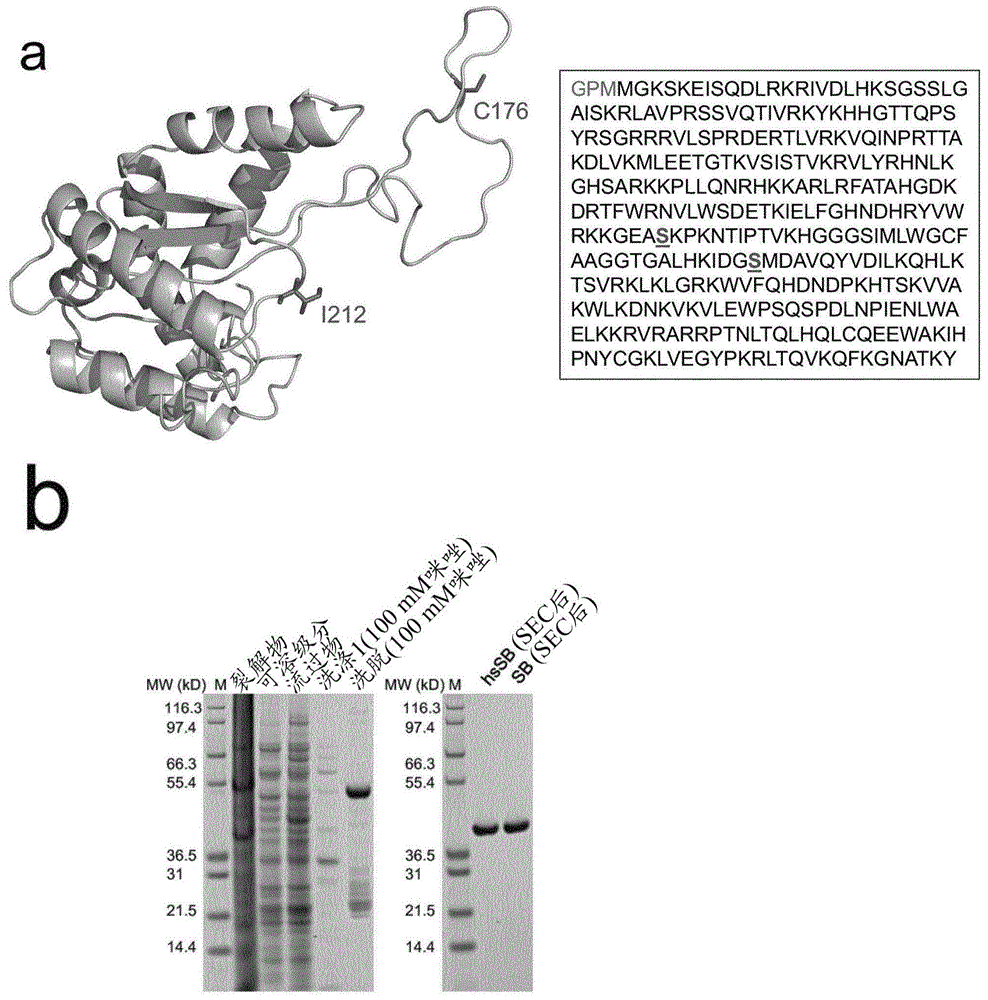
图1:sb100x转座酶的合理诱变。
图2:sbprotact工程程序的示意图。
图3:由转染的hssb转座酶的转座活性驱动转基因(新霉素)插入。
图4:通过对来自11个分离的新霉素阳性hela细胞克隆的新霉素基因座进行序列分析得到的插入位点。sbir的插入准确地发生在ta二核苷酸处。
图5:通过蛋白质或质粒递送hssb。(a):作为蛋白质或由质粒dna表达的hssb递送至hela细胞的保留;(b)和(c):当使用以质粒(b)或以蛋白质(c)递送的hssb转座酶时,hela细胞中的代表性转座测定显示出相当的转基因(新霉素抗性)插入率。误差柱条表示来自2次独立实验(n=2)的平均值的标准误差;(d)和(e):用携带venus的转座子质粒和(a)hssb质粒转染或(b)通过电穿孔递送hssb至hela细胞的荧光活化细胞分选(facs)的代表性流式细胞术分析。转染后2天分选获得转座子质粒的细胞;21天后通过facs分析来定量转座效率。
图6:sbprotact工程程序的示意图,其中通过细胞分选进行定量。
图7:用携带venus的转座子质粒转染并且用hssb转座酶电穿孔的hela细胞的代表性流式细胞术分析。
图8:用携带venus的转座子质粒转染并且用hssb转座酶电穿孔的中国仓鼠卵巢(cho)细胞的流式细胞术分析。
图9:直接递送hssb转座酶蛋白的mesc的基因工程。
图10:通过流式细胞术分析定量的sbprotact系统在不同细胞系中的转基因效率。误差表示为标准差(n=2)。
seqidno:1(hssb)
mgkskeisqdlrkrivdlhksgsslgaiskrlavprssvqtivrkykhhgttqpsyrsgrrrvlsprdertlvrkvqinprttakdlvkmleetgtkvsistvkrvlyrhnlkghsarkkpllqnrhkkarlrfatahgdkdrtfwrnvlwsdetkielfghndhryvwrkkgeaskpkntiptvkhgggsimlwgcfaaggtgalhkidgsmdavqyvdilkqhlktsvrklklgrkwvfqhdndpkhtskvvakwlkdnkvkvlewpsqspdlnpienlwaelkkrvrarrptnltqlhqlcqeewakihpnycgklvegypkrltqvkqfkgnatky
seqidno:2(未突变的sb100x)
mgkskeisqdlrkrivdlhksgsslgaiskrlavprssvqtivrkykhhgttqpsyrsgrrrvlsprdertlvrkvqinprttakdlvkmleetgtkvsistvkrvlyrhnlkghsarkkpllqnrhkkarlrfatahgdkdrtfwrnvlwsdetkielfghndhryvwrkkgeackpkntiptvkhgggsimlwgcfaaggtgalhkidgimdavqyvdilkqhlktsvrklklgrkwvfqhdndpkhtskvvakwlkdnkvkvlewpsqspdlnpienlwaelkkrvrarrptnltqlhqlcqeewakihpnycgklvegypkrltqvkqfkgnatky
seqidno:3(用于重组表达的hssb)
gpmmgkskeisqdlrkrivdlhksgsslgaiskrlavprssvqtivrkykhhgttqpsyrsgrrrvlsprdertlvrkvqinprttakdlvkmleetgtkvsistvkrvlyrhnlkghsarkkpllqnrhkkarlrfatahgdkdrtfwrnvlwsdetkielfghndhryvwrkkgeaskpkntiptvkhgggsimlwgcfaaggtgalhkidgsmdavqyvdilkqhlktsvrklklgrkwvfqhdndpkhtskvvakwlkdnkvkvlewpsqspdlnpienlwaelkkrvrarrptnltqlhqlcqeewakihpnycgklvegypkrltqvkqfkgnatky
(带下划线的是突变的或待突变的残基。粗体和斜体是为了重组蛋白表达而引入的残基)
实施例
实施例1:sb100x转座酶的合理诱变。
在图1中,(a)左侧显示了sb100x转座酶(下文称为sb)催化结构域的晶体结构。突变为丝氨酸以产生hssb变体的残基显示为洋红色的条。右侧:用于重组蛋白产生的全长hssb转座酶变体的氨基酸序列。洋红色的加粗加下划线字符表示丝氨酸分别取代sb100x序列中的c176和i212。在n-末端引入蓝色残基用于重组蛋白产生。
图1(b)显示了本发明的hssb蛋白质的重组产生。提供了纯化的hssb蛋白变体的sds-page分析。hssb在大肠杆菌中大量重组产生(与n-末端纯化和可溶性标签融合)。在标签去除和尺寸排阻色谱法(sec)之后,hssb是高纯度的。hssb的纯化产量显示在图1c中。尺寸排阻色谱法显示,与sb相比,hssb以显著更高的产量(大约两倍的量)重组产生,表明hssb变体的溶解度改善。hssb在电穿孔缓冲液中的高溶解度显示在图1d中。hssb可以浓缩多达50倍(对应于20mg/ml),而sb在高于7mg/ml的浓度下经历沉淀。hssb在低盐r缓冲液(用于电穿孔)中是高度可溶的,甚至在高蛋白浓度下亦如此。虽然在浓缩时观察到一些沉淀,但绝大多数hssb保留在可溶性级分中。在37℃温育后纯化的sb蛋白质的sds-page分析显示在图1e中。即使在生理温度下短时间温育,sb也表现出降解(星号表示降解产物),而hssb则不表现出降解。而且,如图1f所示,hssb比sb更为热稳定的。在接近生理(200mmnacl,ph7.5)缓冲条件下的两种蛋白质的cd测量。然而,如左图所示,hssb具有与sb相同的折叠。尽管如此,hssb的热稳定性显著更高;其在95℃下仍无法完全展开(右图)。考虑到电穿孔加热样品,这种特性对于蛋白质转染是非常有利的。最后,在长期存储时,hssb比sb更好地保存(图1g)。左图:纯化的sb蛋白质在-80℃长期储存后的sds-page分析,显示sb在冷冻后经历显著降解,而hssb则不会(右图)。左边的蓝色框和星号所示的条带的质谱分析证实了这些条带对应于sb蛋白质的降解产物。
实施例2:使用hssb转座酶将基因递送至hela细胞中
基因递送的策略描述在图2中。由转染的hssb转座酶的转座活性驱动转基因(新霉素抗性基因)插入(图3)。上图:hela细胞中的代表性转座测定。新霉素抗性菌落的数目显示在括号中。下图:hela细胞中转座测定的定量。误差柱条表示标准误差(n=3)。
图4显示了通过对来自分离的新霉素阳性hela细胞的新霉素基因座进行序列分析得出的插入位点。sbir的插入准确地发生在ta二核苷酸处。
图5(a)显示了以蛋白质或由质粒dna表达的hssb递送至hela细胞的hssb的保留。蛋白质印迹分析显示了电穿孔后48小时递送的hssb蛋白几乎完全丢失,而用hssb表达质粒转染的细胞在转染后24小时至5天持续产生高水平的蛋白。对来自用0.5μgpsbter(tpn)转染以及用10μghssb蛋白电穿孔或用0.5μghssb表达质粒转染的hela细胞的裂解物进行蛋白质印迹。在指定的时间点取样,通过电泳分离20μg-s的总裂解物,并将其转移到硝化纤维膜上。用抗sb抗体检测sb。内部上样对照是用抗gapdh抗体检测的甘油醛3-磷酸脱氢酶(gapdh)。条带强度的测量允许随时间定量hela细胞中的hssb持久性(如左侧图表所示)。
图5(b)至5(e)显示了由在表达质粒上提供的hssb或通过电穿孔直接作为蛋白质递送的hssb在hela细胞中的基因工程效率的比较。如图所示,基因工程效率不依赖于转染方法,尽管蛋白质电穿孔在较短的时间段内更有效,而质粒转染产生转座酶的长期表达。
图6显示了通过细胞分选进行定量的sbprotact工程程序的示意图。图7显示了用携带venus的转座子质粒转染并且用hssb转座酶电穿孔的hela细胞的代表性流式细胞术分析。在转染后3周鉴定venus阳性细胞,以便选择转座阳性细胞。电穿孔的hssb蛋白量在每个图表上方显示。y轴:碘化丙啶(pi)染色以选择活细胞。x轴:来自venus的绿色荧光。nt:未转染的。
实施例3:在cho细胞和小鼠胚胎干细胞(mesc)中使用hssb转座酶的基因递送
图8显示了用携带venus的转座子质粒转染并且用hssb转座酶电穿孔的中国仓鼠卵巢(cho)细胞的代表性流式细胞术分析。在转染后3周鉴定venus阳性细胞,以便选择转座阳性细胞。电穿孔的hssb蛋白量在每个图表上方显示。y轴:碘化丙啶(pi)染色以选择活细胞。x轴:来自venus的绿色荧光。nt:未转染的。
图9显示了通过直接递送hssb转座酶蛋白对mesc进行基因工程。(a):小鼠胚胎干细胞(mesc)中的代表性转座测定,表明转染的hssb转座酶的有效转基因(新霉素抗性)插入。(b):用携带venus的转座子质粒转染并用hssb转座酶电穿孔的mesc的代表性流式细胞术分析。在转染后3周鉴定venus阳性细胞,以便选择转座阳性细胞。电穿孔的hssb蛋白量在每个图表上方显示。y轴:碘化丙啶(pi)染色以选择活细胞。x轴:来自venus的绿色荧光。nt:未转染的。(c)oct4染色证实了工程化的mesc保持其多能状态。
图10中显示了sbprotact系统在不同细胞系中的转基因效率,如通过流式细胞术分析所定量的。误差表示为标准差(n=2)。
图11(a)显示了小鼠胚胎干细胞(mesc)中的代表性转座测定,表明转染的hssb转座酶的有效转基因(新霉素)插入。在(b)中,提供了用携带venus的转座子质粒转染并且用hssb转座酶电穿孔的mesc的代表性流式细胞术分析。在转染后3周鉴定venus阳性细胞,以便选择转座阳性细胞。电穿孔的hssb蛋白量在每个图表上方显示。y轴:活细胞的碘化丙啶(pi)染色。x轴:来自venus的绿色荧光。nt:未转染的。在图11(c)中,oct4染色证实了工程化的mesc保持其多能状态。
在进一步的实验中,本申请的发明人寻求量化转座效率。通过流式细胞术分析来定量sbprotact系统在不同细胞系中的转基因效率。结果提供在图12中,误差表示为标准差(n=2)。
总之,新的转座酶变体和转染策略(即sbprotact)基于纯化的转座酶蛋白的使用建立了用于细胞工程的新一代sb转座子系统,这在迄今为止是前所未有的。在标准的基于sb的应用中,sb转座酶的表达可通过递送至靶细胞中的表达质粒或编码蛋白质的信使rna实现的。在正在进行的临床基因治疗试验中,表达质粒专门用作sb转座酶的来源。与转座酶基因递送相比,sbprotact中的直接hssb蛋白递送提供了:
a)在不同细胞类型中相当的转基因比率。
b)没有转座酶-基因或-启动子整合的风险,避免了靶细胞中不受控的长期转座和不期望的(例如致癌基因的)转录激活。
c)不需要在靶细胞中转录和翻译。这将sb介导的工程适用性扩展至其中蛋白质过表达困难和/或损害细胞活力的细胞。
d)因为hssb蛋白在递送48小时内降解,所以实现了快速的细胞工程和迅速的蛋白周转。因此,hssb蛋白以命中即跑(hit-and-run)的方式起作用,使脱靶活性最小化(参见下文)。
e)由于转座的时间窗口有限,因此降低了细胞毒性,减少了插入诱变和转基因重新活动的风险。
f)在相同转基因比率下每个细胞的插入数目较少,使基因组扰动最小化。
g)剂量依赖性效率。通过改变转染的hssb蛋白的浓度,可以严格控制阳性克隆的数目。
h)插入事件的离散和可调的数目。hssb介导的工程产生每个基因组具有离散数目插入的克隆,其可以通过改变蛋白质剂量来调节。相比之下,来自表达质粒的不受控的转座水平和时间导致不均一的多拷贝克隆。
此外,对于car-t细胞的产生,已经探索了使用mrna作为sb转座酶的替代来源,但是mrna的不稳定性引起了质量控制问题,这会阻碍广泛用于治疗。与mrna递送相比,hssb蛋白递送提供了以下几种优势:
i)与细胞翻译效率和调控无关。
j)甚至更严格和更直接地控制转座效率,因为sb转座酶在转染后立即起作用而无需翻译。
k)在应用之前在体外评估蛋白质质量和活性的可能性(在出版物中描述并在本文的图1h中示出的测定)。这对于商业或临床环境中的质量控制程序是特别相关的。
迄今为止,仅对于piggybac转座酶实现了用于高效哺乳动物细胞工程的活性转座酶的递送,但需要将蛋白质掺入慢病毒颗粒中。因此,sbprotact首次提供了用于在医学相关的环境中有效递送转座酶蛋白的完全无病毒的系统,从而避免了与病毒载体的使用和生产有关的所有安全问题和财务限制。
总之,我们的发明sbprotact系统为在基因工程应用中实现sb转座的最大控制开创了新的可能性,使sb成为一种更加安全的遗传工具。hssb蛋白的直接递送允许从细胞中快速清除转座酶,避免了长期转座的不期望的影响。此外,直接提供转座的活性因子,活性转基因插入的比率和时间范围可以被精细地调节,并且不依赖于细胞机构中转座酶表达(来自质粒)或翻译(来自mrna)的时间线和随机事件,从而也避免了靶细胞的适应成本。
目前,sb是当前在临床试验中用于制备cart细胞的唯一非病毒基因递送工具,并且已经在临床开发中取得了相当大的进展。在保留当前sb系统的所有优势(包括简单、简便和低成本)的同时,本发明的sbprotact提供了一种新的方法来克服关于在临床应用中使用当前sb系统的安全性问题。
序列表
<110>欧洲分子生物学实验室(europeanmolecularbiologylaboratory)
<120>改进的转座酶多肽及其用途
<130>e31909wo
<140>ep17187128.8
<141>2017-08-21
<160>34
<170>patentinversion3.5
<210>1
<211>340
<212>prt
<213>人工的(artificial)
<220>
<223>hssb
<400>1
metglylysserlysgluileserglnaspleuarglysargileval
151015
aspleuhislysserglyserserleuglyalaileserlysargleu
202530
alavalproargserservalglnthrilevalarglystyrlyshis
354045
hisglythrthrglnprosertyrargserglyargargargvalleu
505560
serproargaspgluargthrleuvalarglysvalglnileasnpro
65707580
argthrthralalysaspleuvallysmetleuglugluthrglythr
859095
lysvalserileserthrvallysargvalleutyrarghisasnleu
100105110
lysglyhisseralaarglyslysproleuleuglnasnarghislys
115120125
lysalaargleuargphealathralahisglyasplysaspargthr
130135140
phetrpargasnvalleutrpseraspgluthrlysilegluleuphe
145150155160
glyhisasnasphisargtyrvaltrparglyslysglyglualaser
165170175
lysprolysasnthrileprothrvallyshisglyglyglyserile
180185190
metleutrpglycysphealaalaglyglythrglyalaleuhislys
195200205
ileaspglysermetaspalavalglntyrvalaspileleulysgln
210215220
hisleulysthrservalarglysleulysleuglyarglystrpval
225230235240
pheglnhisaspasnaspprolyshisthrserlysvalvalalalys
245250255
trpleulysaspasnlysvallysvalleuglutrpproserglnser
260265270
proaspleuasnproilegluasnleutrpalagluleulyslysarg
275280285
valargalaargargprothrasnleuthrglnleuhisglnleucys
290295300
glngluglutrpalalysilehisproasntyrcysglylysleuval
305310315320
gluglytyrprolysargleuthrglnvallysglnphelysglyasn
325330335
alathrlystyr
340
<210>2
<211>340
<212>prt
<213>人工的(artificial)
<220>
<223>未突变的sb100x
<400>2
metglylysserlysgluileserglnaspleuarglysargileval
151015
aspleuhislysserglyserserleuglyalaileserlysargleu
202530
alavalproargserservalglnthrilevalarglystyrlyshis
354045
hisglythrthrglnprosertyrargserglyargargargvalleu
505560
serproargaspgluargthrleuvalarglysvalglnileasnpro
65707580
argthrthralalysaspleuvallysmetleuglugluthrglythr
859095
lysvalserileserthrvallysargvalleutyrarghisasnleu
100105110
lysglyhisseralaarglyslysproleuleuglnasnarghislys
115120125
lysalaargleuargphealathralahisglyasplysaspargthr
130135140
phetrpargasnvalleutrpseraspgluthrlysilegluleuphe
145150155160
glyhisasnasphisargtyrvaltrparglyslysglyglualacys
165170175
lysprolysasnthrileprothrvallyshisglyglyglyserile
180185190
metleutrpglycysphealaalaglyglythrglyalaleuhislys
195200205
ileaspglyilemetaspalavalglntyrvalaspileleulysgln
210215220
hisleulysthrservalarglysleulysleuglyarglystrpval
225230235240
pheglnhisaspasnaspprolyshisthrserlysvalvalalalys
245250255
trpleulysaspasnlysvallysvalleuglutrpproserglnser
260265270
proaspleuasnproilegluasnleutrpalagluleulyslysarg
275280285
valargalaargargprothrasnleuthrglnleuhisglnleucys
290295300
glngluglutrpalalysilehisproasntyrcysglylysleuval
305310315320
gluglytyrprolysargleuthrglnvallysglnphelysglyasn
325330335
alathrlystyr
340
<210>3
<211>343
<212>prt
<213>人工的(artificial)
<220>
<223>用于重组表达的hssb
<400>3
glyprometmetglylysserlysgluileserglnaspleuarglys
151015
argilevalaspleuhislysserglyserserleuglyalaileser
202530
lysargleualavalproargserservalglnthrilevalarglys
354045
tyrlyshishisglythrthrglnprosertyrargserglyargarg
505560
argvalleuserproargaspgluargthrleuvalarglysvalgln
65707580
ileasnproargthrthralalysaspleuvallysmetleugluglu
859095
thrglythrlysvalserileserthrvallysargvalleutyrarg
100105110
hisasnleulysglyhisseralaarglyslysproleuleuglnasn
115120125
arghislyslysalaargleuargphealathralahisglyasplys
130135140
aspargthrphetrpargasnvalleutrpseraspgluthrlysile
145150155160
gluleupheglyhisasnasphisargtyrvaltrparglyslysgly
165170175
glualaserlysprolysasnthrileprothrvallyshisglygly
180185190
glyserilemetleutrpglycysphealaalaglyglythrglyala
195200205
leuhislysileaspglysermetaspalavalglntyrvalaspile
210215220
leulysglnhisleulysthrservalarglysleulysleuglyarg
225230235240
lystrpvalpheglnhisaspasnaspprolyshisthrserlysval
245250255
valalalystrpleulysaspasnlysvallysvalleuglutrppro
260265270
serglnserproaspleuasnproilegluasnleutrpalagluleu
275280285
lyslysargvalargalaargargprothrasnleuthrglnleuhis
290295300
glnleucysglngluglutrpalalysilehisproasntyrcysgly
305310315320
lysleuvalgluglytyrprolysargleuthrglnvallysglnphe
325330335
lysglyasnalathrlystyr
340
<210>4
<211>27
<212>dna
<213>智人(homosapiens)
<400>4
tgtatatatatatatacagttgaagtc27
<210>5
<211>27
<212>dna
<213>智人(homosapiens)
<400>5
gacacatacatacatacagttgaagtc27
<210>6
<211>27
<212>dna
<213>智人(homosapiens)
<400>6
ctgttggatgcctctacagttgaagtc27
<210>7
<211>27
<212>dna
<213>智人(homosapiens)
<400>7
gatatatacatatgtacagttgaagtc27
<210>8
<211>27
<212>dna
<213>智人(homosapiens)
<400>8
gtactgagtgtatgtacagttgaagtc27
<210>9
<211>27
<212>dna
<213>智人(homosapiens)
<400>9
ctttcaggaacaaatacagttgaagtc27
<210>10
<211>28
<212>dna
<213>智人(homosapiens)
<400>10
tcaacttcagaaatgtacagttgaagtc28
<210>11
<211>28
<212>dna
<213>智人(homosapiens)
<400>11
ggacacatacatacatacagttgaagtc28
<210>12
<211>27
<212>dna
<213>智人(homosapiens)
<400>12
gtactgagtgtatgtacagttgaagtc27
<210>13
<211>26
<212>dna
<213>智人(homosapiens)
<400>13
tttcaggaacaaatacagttgaagtc26
<210>14
<211>27
<212>dna
<213>智人(homosapiens)
<400>14
actctcctatgatatacagttgaagtc27
<210>15
<211>27
<212>dna
<213>智人(homosapiens)
<400>15
actctcctatgatatacagttgaagtc27
<210>16
<211>27
<212>dna
<213>智人(homosapiens)
<400>16
aataatgctagttatacagttgaagtc27
<210>17
<211>27
<212>dna
<213>智人(homosapiens)
<400>17
atggcgagttaacatacagttgaagtc27
<210>18
<211>27
<212>dna
<213>智人(homosapiens)
<400>18
tattccatggcatatacagttgaagtc27
<210>19
<211>27
<212>dna
<213>智人(homosapiens)
<400>19
tatagctaacaatatacagttgaagtc27
<210>20
<211>26
<212>dna
<213>智人(homosapiens)
<400>20
gcaagtcctgtcatacagttgaagtc26
<210>21
<211>27
<212>dna
<213>智人(homosapiens)
<400>21
ttaaatggaataattacagttgaagtc27
<210>22
<211>27
<212>dna
<213>智人(homosapiens)
<400>22
gacacatacatacatacagttgaagtc27
<210>23
<211>27
<212>dna
<213>智人(homosapiens)
<400>23
aaagcaatagcacatacagttgaagtc27
<210>24
<211>27
<212>dna
<213>智人(homosapiens)
<400>24
ttgtataaatcatatacagttgaagtc27
<210>25
<211>27
<212>dna
<213>智人(homosapiens)
<400>25
tatagctaacaatatacagttgaagtc27
<210>26
<211>27
<212>dna
<213>智人(homosapiens)
<400>26
cctaatcatctacttacagttgaagtc27
<210>27
<211>27
<212>dna
<213>智人(homosapiens)
<400>27
ttgtataaatcatatacagttgaagtc27
<210>28
<211>27
<212>dna
<213>智人(homosapiens)
<400>28
catgtcacatgaagtacagttgaagtc27
<210>29
<211>27
<212>dna
<213>智人(homosapiens)
<400>29
agtgaggtttaacatacagttgaagtc27
<210>30
<211>27
<212>dna
<213>智人(homosapiens)
<400>30
ctattttggaaacatacagttgaagtc27
<210>31
<211>54
<212>dna
<213>智人(homosapiens)
<400>31
catgtcacatgaagtacagttgaagtcgacttcaactgtacattaggtaaccac54
<210>32
<211>55
<212>dna
<213>智人(homosapiens)
<400>32
attgtataaatcatatacagttgaagtcgacttcaactgtatctacatattcata55
<210>33
<211>54
<212>dna
<213>智人(homosapiens)
<400>33
tcttttgttgcatatacagttgaagtcgacttcaactgtatgtatgcatttctg54
<210>34
<211>54
<212>dna
<213>智人(homosapiens)
<400>34
ccctctcctacacatacagttgaagtcgacttcaactgtacattatactactaa54
- 还没有人留言评论。精彩留言会获得点赞!