检测阿留申病毒的CPA引物组、试剂、试剂盒及检测方法和应用与流程
本发明涉及病毒分子生物学技术领域,具体而言,涉及一种检测阿留申病毒的cpa引物组、试剂、试剂盒及检测方法和应用。
背景技术:
阿留申病毒(amdoparvovirus)归属细小病毒科(parvoviridae)、细小病毒亚科(parvovirinae)、阿留申病毒属。阿留申病毒主要感染鼬科动物、臭鼬科和小熊猫科等广泛的宿主,阿留申病毒是水貂、雪貂、水獭和臭鼬和小熊猫等的阿留申病的病原,也是犬科动物狐属和貉等的潜在病原。阿留申病毒属可能存在新病毒种类,感染更广泛的宿主。其中阿留申水貂病病毒(aleutianminkdiseasevirus,amdv)会导致水貂阿留申病,对水貂养殖业危害严重。
目前常用的检测阿留申病毒的方法主要有常规的pcr检测、ciep检测和elisa检测。常规的病毒pcr检测,需要提取核酸,提供精确反应条件,电泳检测核酸扩增特异条带,主要在专门的实验室完成,耗时、实验条件要求高,在现场应用受限。ciep通过检测抗体间接确定病毒感染,不能直接检测病毒。elisa检测定量病毒的抗体需要专业精密仪器,试剂成本较高,在现场应用上有很大限制。
有鉴于此,特提出本发明以解决上述技术问题中的至少一个。
技术实现要素:
本发明的目的在于提供用于检测阿留申病毒的cpa引物组、试剂、试剂盒及检测方法,以解决现有技术中缺少一种快速简便、结果准确、成本低和适合现场检测阿留申病毒的检测方法。
为了实现本发明的上述目的,特采用以下技术方案:
第一方面,本发明提供了一种检测阿留申病毒的cpa引物组,包括剥离引物对和单交叉引物对;
所述剥离引物对的核苷酸序列包括:
bl-f:5’-ctgtmacagaaaccaaccaaggta-3’(seqidno.1);
bl-r:5’-ttgaatgttaggrtatctgttgta-3’(seqidno.2);
所述单交叉引物对的核苷酸序列包括:
jc-f:5’-gttggtttggttgctctccaaggactccagctgcgccgttgg-3’(seqidno.3);
jc-r:5’-actccagctgcgccgttggttggtttggttgctctccaagga-3’(seqidno.4)。
第二方面,本发明提供了一种检测阿留申病毒的试剂,包括所述的检测阿留申病毒的cpa引物组。
第三方面,本发明提供了检测阿留申病毒的cpa试剂盒,包括所述的检测阿留申病毒的cpa引物组或所述的检测阿留申病毒的试剂。
进一步,在本发明提供的技术方案的基础上,所述cpa试剂盒还包括释放剂、dna聚合酶、缓冲液、dntps和显色剂;
优选地,所述cpa试剂盒还包括阳性对照模板;
优选地,所述阳性对照模板为包含所述剥离引物扩增区段的质粒。
进一步,在本发明提供的技术方案的基础上,所述释放剂包括a和b两种试剂;所述a试剂包括koh0.4~0.6mol/l和tritonx-1000.1%(v/v);所述b试剂包括hcl0.4~0.6mol/l;
优选地,所述dna聚合酶为bst2.0warmstartdna聚合酶;
优选地,所述显色剂为sybrgreeni。
第四方面,本发明提供了一种阿留申病毒的检测方法,应用所述的cpa引物组或所述的试剂或所述的cpa试剂盒,以待测样品处理后的dna为模板,进行恒温扩增,检测阿留申病毒。
进一步,在本发明提供的技术方案的基础上,所述待测样品包括液体待测样品或固体待测样品;所述液体待测样品包括血液、血清或尿液;所述固体待测样品包括组织或粪便。
进一步,在本发明提供的技术方案的基础上,液体待测样品的处理包括以下步骤:每1~2μl液体待测样品与2.5~3.5μla试剂混匀,作用8~10min,再加入2.0~3.0μlb试剂混合得到模板dna;
优选地,固体待测样品的处理包括以下步骤:将固体待测样品与水混合后冻融2~3次匀浆后静置得到上清液,取1~2μl上清液与2.5~3.5μl释放剂a混匀,作用8~10min,再加入2.0~3.0μl释放剂b混合得到模板dna;
优选地,所述固体待测样品与水的质量体积比(g/ml)为1:(3~5)。
进一步,在本发明提供的技术方案的基础上,所述恒温扩增的条件包括:温度59~64℃,反应时间50~70min;
优选地,恒温扩增的条件包括:温度62~64℃,反应时间50~60min。
第五方面,本发明提供了所述检测阿留申病毒cpa引物组或所述检测阿留申病毒的试剂或所述检测阿留申病毒的cpa试剂盒或所述阿留申病毒检测方法在检测阿留申病毒中的应用。
与现有技术相比,本发明的有益效果为:
(1)本发明提供的检测阿留申病毒的cpa引物,特异性好,灵敏度高,扩增结果稳定可靠,能有效检测阿留申病毒。
(2)本发明提供的检测阿留申病毒的cpa试剂盒,检测快速、灵敏,检测下限可以低至1.82×102copies/μl,可实现对阿留申病毒的快速定性检测,并且生产成本低,操作简便,适合在实验室或其它地点进行快速筛查和检测,扩大了适用范围。
(3)本发明提供的阿留申病毒的检测方法,该检测方法简便、快速、高效,扩增与检测时均不需要复杂仪器设备,扩增反应后可通过加入可视化显色剂观察颜色变化来判断病毒的存在与否,非常适合基层与现场快速检测。同时,该检测方法简化了检测过程,降低了对操作人员的专业要求,使得非专业人员也可以顺利完成检测工作,具有较大的应用前景。
附图说明
为了更清楚地说明本发明具体实施方式或现有技术中的技术方案,下面将对具体实施方式或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图是本发明的一些实施方式,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
图1为实施例1和实施例3的cpa扩增产物的琼脂糖凝胶电泳图;
图2为实施例2的cpa扩增产物的琼脂糖凝胶电泳图;
图3为实施例3的普通pcr扩增产物的琼脂糖凝胶电泳图。
具体实施方式
下面将结合实施例对本发明的实施方案进行详细描述,但是本领域技术人员将会理解,下列实施例仅用于说明本发明,而不应视为限制本发明的范围。实施例中未注明具体条件者,按照常规条件或制造商建议的条件进行。所用试剂或仪器未注明生产厂商者,均为可以通过市售购买获得的常规产品。
本发明中,如果没有特别的说明,本文所提到的所有实施方式以及优选实施方法可以相互组合形成新的技术方案。
本发明中,如果没有特别的说明,本文所提到的所有技术特征以及优选特征可以相互组合形成新的技术方案。
本发明中,如果没有特别的说明,百分数(%)或者份指的是相对于组合物的体积百分数。
本发明中,如果没有特别的说明,所涉及的各组分或其优选组分可以相互组合形成新的技术方案。
本发明中,除非有其他说明,数值范围“a~b”表示a到b之间的任意实数组合的缩略表示,其中a和b都是实数。例如数值范围“6~22”表示本文中已经全部列出了“6~22”之间的全部实数,“6~22”只是这些数值组合的缩略表示。
本发明所公开的“范围”以下限和上限的形式,可以分别为一个或多个下限,和一个或多个上限。
本发明中,除非另有说明,各个反应或操作步骤可以顺序进行,也可以不按照顺序进行。优选地,本文中的反应方法是顺序进行的。
除非另有说明,本文中所用的专业与科学术语与本领域熟练人员所熟悉的意义相同。此外,任何与所记载内容相似或均等的方法或材料也可应用于本发明中。
根据本发明的第一个方面,提供了一种检测阿留申病毒的cpa引物组,包括剥离引物对和单交叉引物对;
剥离引物对的核苷酸序列包括:
bl-f:5’-ctgtmacagaaaccaaccaaggta-3’(seqidno.1);
bl-r:5’-ttgaatgttaggrtatctgttgta-3’(seqidno.2)。
其中剥离引物对中的bl-f,使用兼并碱基m,表示该位点是腺嘌呤a或胞嘧啶c均可;剥离引物对中的bl-r,使用兼并碱基r,表示该位点是腺嘌呤a或胞嘧啶g均可。
单交叉引物对的核苷酸序列包括:
jc-f:5’-gttggtttggttgctctccaaggactccagctgcgccgttgg-3’(seqidno.3);
jc-r:5’-actccagctgcgccgttggttggtttggttgctctccaagga-3’(seqidno.4)。
交叉引物恒温扩增技术(crossprimingamplification,cpa)是一种新型的恒温核酸扩增方法,针对靶基因设计特异性引物,利用链置换dna聚合酶在恒温条件下反应一定时间即可完成核酸扩增反应。通过标记特异性探针使其扩增产物可用一次性核酸检测装置进行检测,有效防止扩增产物带来的污染,减少假阳性结果。
cpa技术作为一种基础方法,在应用到具体检测对象时,需要针对检测对象基因序列的特点,针对性地选择靶基因及扩增位点,合理设计交叉引物及剥离引物以提高方法的特异性与灵敏度。
剥离引物是指位于单交叉引物后方的短链引物,其作用是在链置换dna聚合酶的作用下,将扩增的延伸链从模板上剥离。
单交叉引物是指用于交叉扩增的主要引物,其中正向引物的5’末端序列与反向引物的互补序列相同,而反向引物的5’末端序列与正向引物的互补序列相同,因此在扩增过程中这两条引物互相引入对方的互补序列,增加引物的杂交位点,促进扩增反应。
上述检测阿留申病毒的cpa引物,包括了剥离引物对和单交叉引物对,cpa引物组的特异性好,灵敏度高,扩增结果稳定可靠,能有效检测阿留申病毒。
根据本发明的第二个方面,提供了一种检测阿留申病毒的试剂,包括上述的检测阿留申病毒的cpa引物组。
对检测阿留申病毒的试剂的具体种类不进行限定,包括上述的cpa引物组中剥离引物和单交叉引物即可,可以用于检测阿留申病毒。上述阿留申病毒的试剂由于含有上述cpa引物组,因此具有特异性好,灵敏度高,扩增结果稳定可靠的优点。
根据本发明的第三个方面,提供了一种检测阿留申病毒的cpa试剂盒,包括上述的cpa引物组或上述检测阿留申病毒的试剂。
该检测阿留申病毒的cpa试剂盒,能够检测除灰狐阿留申病毒外已发现的6个阿留申病毒种,不仅适用水貂阿留申病毒(amdv)、貉、狐阿留申病病毒(rfav)的检测,也可用于检测新宿主的其它种阿留申病毒感染。
上述检测阿留申病毒的cpa试剂盒,检测快速、灵敏,检测下限可以低至1.82×102copies/μl,可实现对阿留申病毒的快速定性检测,并且生产成本低,操作简便,适合在实验室或其它地点进行快速筛查和检测,扩大了适用范围。
在一种优选地实施方式中,检测阿留申病毒的cpa试剂盒还包括释放剂、dna聚合酶、缓冲液、dntps和显色剂。
释放剂中a试剂提供强碱性环境,可以裂解细胞和病毒的结构蛋白,从而充分释放核酸;释放剂中b试剂为酸,在a试剂作用后加入b试剂可以中和a试剂的碱性,经释放剂简单处理样品可使核酸释放适用于作cpa反应模板。
dna聚合酶是dna恒温扩增过程中重要的工具酶,催化dna合成。此处dna聚合酶需要满足以下条件:具有5’→3’的聚合酶活性和强链置换活性,但没有5’→3’核酸外切酶活性。对dna聚合酶的种类不进行限定,能够满足上述条件即可,优选bst2.0warmstartdna聚合酶。
缓冲液的作用是使恒温扩增的反应体系溶液的ph更稳定,减少ph变化对恒温扩增反应的影响。
显色剂可以与恒温扩增后的dna结合,加入可视化显色剂可以在可见光下显色,通过直接肉眼观察颜色变化来判断靶基因是否充分扩增;或利用本领域常规的实验手段观察是否存在靶基因。对显色剂的种类不进行限定,优选可以与dna结合在可见光下直接显色的显色剂,进一步优选sybrgreeni。
优选检测阿留申病毒的cpa试剂盒中dna聚合酶和显色剂的种类,可以使cpa试剂盒检测阿留申病毒更快速和灵敏,且操作更方便。
采用cpa扩增技术,针对阿留申病毒特异设计4条引物组合,将释放试剂、恒温扩增试剂和反应结果可视化判定指示剂组合成试剂盒,实现样品的核酸提取的简化、反应温度条件易得和结果判定可视化,可以满足现场易用,可检测大部分阿留申病毒。
在一种优选地实施方式中,上述cpa试剂盒还包括阳性对照模板。
对阳性对照模板的具体种类不进行限定,只要满足可以经cpa反应后能够明显且准确的检测到阿留申病毒即可。优选阳性对照模板为包含剥离引物扩增区段的质粒,如检测水貂阿留申病毒(amdv),阳性对照模板优选包含剥离引物扩增区段的amdv-g836bp片段的质粒。
在cpa试剂盒中加入阳性对照模板可以使样品的检测结果与阳性对照的检测结果进行明显的比对,方便使用者更好地鉴别待测样品中是否存在阿留申病毒。优选阳性对照模板可以使阳性结果更稳定可靠,提高cpa试剂盒的准确性。
在一种优选地实施方式中,上述释放剂包括a和b两种试剂;所述a试剂包括koh0.4~0.6mol/l和tritonx-1000.1%(v/v);所述b试剂包括hcl0.4~0.6mol/l。
a试剂中,koh的浓度典型但非限制性的例如为0.4mol/l、0.5mol/l或0.6mol/l;b试剂中,hcl的浓度典型但非限制性的例如为0.4mol/l、0.5mol/l或0.6mol/l。
需要说明的是,使用释放剂处理样品时,a试剂中koh与b试剂中hcl的浓度相同。
优选释放剂可以使待测样品处理过程中,样品的核酸更容易释放,且减少对核酸的损伤,提高样品的检测准确性。
在一种优选地实施方式中,1×缓冲液包括如下组分:18~22mmtris-hcl、8~12mm(nh)2so4、2~3.5mmol/lmgso4、tween-200.1%(v/v)和0.35~0.45mol/lbetaine,缓冲液的ph8.8。
优选缓冲液的组分和浓度,可以使缓冲液的缓冲效果更好,保持反应体系的ph稳定,使cpa试剂盒的检测更快速、灵敏和准确。
根据本发明的第四个方面,提供了一种阿留申病毒的检测方法,应用上述的cpa引物组或上述的试剂或上述的cpa试剂盒,以待测样品处理后的dna为模板,进行恒温扩增,检测阿留申病毒。
优选地,待测样品包括液体待测样品或固体待测样品,其中,液体待测样品包括血液、血清或尿液;固体待测样品包括组织或粪便。
该阿留申病毒检测方法简便、快速、高效,扩增与检测时均不需要复杂仪器设备,非常适合基层与现场快速检测。
在一种优选地实施方式中,阿留申检测方法包括以下几个步骤:处理待测样品、配制cpa反应体系、cpa反应和结果鉴定。
处理待测样品
优选液体待测样品的处理,包括以下步骤:每1~2μl液体待测样品与2.5~3.5μla试剂混匀,作用8~10min,再加入2.0~3.0μlb试剂混合得到模板dna;
优选固体待测样品的处理,包括以下步骤:将固体待测样品与水混合后冻融2~3次匀浆后静置得到上清液,取1~2μl上清液与2.5~3.5μla试剂混匀,作用8~10min,再加入2.0~3.0μlb试剂混合得到模板dna;优选固体待测样品与水的质量体积比(g/ml)为1:(3~5)。
处理待测样品时,优选b试剂的加入量比a试剂少0.5μl,可以使释放剂发挥更好的效果。
需要说明的是,液体待测样品或固体待测样品处理过程中,可以根据实际需要和参照上述样品和释放剂的比例及作用时间进行合理的调整,不局限于上述比例和作用时间。
配制cpa反应体系
优选cpa反应体系包括:剥离引物对各0.12~0.28μmol/l、单交叉引物对各0.32~0.64μmol/l、bst2.0dna聚合酶7.5~8.5u、10×缓冲液2.5~3.5μl和dntps0.3~0.5mmol/l,模板dna,加水至体积为30μl并混匀。
10×缓冲液指的是上述1×缓冲液各组分浓度扩大了10倍。
cpa反应体系中,各剥离引物的浓度典型但非限制性的例如为0.14μmol/l、0.16μmol/l、0.18μmol/l、0.2μmol/l、0.23μmol/l、0.25μmol/l或0.28μmol/l;各单交叉引物的浓度典型但非限制性的例如为0.32μmol/l、0.38μmol/l、0.4μmol/l、0.45μmol/l、0.5μmol/l、0.55μmol/l、0.6μmol/l或0.64μmol/l;dna聚合酶的浓度典型但非限制性的例如为7.5u、7.8u、8u、8.2u或8.5u;10×缓冲液的体积典型但非限制性的例如为2.5μl、2.8μl、3μl、3.2μl或3.5μl;dntps的浓度典型但非限制性的例如为0.3mmol/l、0.4mmol/l或0.5mmol/l。
优选cpa反应体系中,剥离引物对和单交叉引物对的浓度比为(2~2.4):1;进一步优选各剥离引物的浓度为0.2μmol/l,各单交叉引物的浓度为0.4μmol/l。
需要说明的是,为了证明实验结果的准确性,cpa反应体系还可以增加水为模板作为阴性对照和阿留申病毒的dna为模板作为阳性对照。
cpa反应
优选恒温扩增(cpa反应)的温度为59~64℃,时间为50~70min;进一步优选恒温扩增的温度为62~64℃,时间为50~60min。
恒温扩增的温度典型但非限制性的例如为59℃、60℃、61℃、62℃、63℃或64℃;恒温扩增的时间典型但非限制性的例如为50min、55min、60min、65min或70min。
cpa反应可以在保温杯或恒温水浴锅中进行,或其它能够提供上述温度的设备中进行,简便快捷,无需复杂设备,非常适合基层与现场快速检测。
结果鉴定
cpa反应完成后,加入显色剂,混合均匀后观察显色结果。
cpa反应扩增生成dna后,优选加入可视化显色剂,如sybrgreeni,该显色剂加入dna后,经过瞬时离心混合后即可进行肉眼观察结果,阴性为橙色,阳性为绿色。扩增反应后,可通过加入可视化显色剂观察颜色变化来判断病毒的存在与否,非常适合基层与现场快速检测。
需要说明的是,加入显色剂sybrgreeni肉眼观察的变色反应的下限为1.82×102copies/μl。
此外,cpa反应扩增生成dna后,也可以加入其它显色剂进行琼脂糖凝胶电泳实验,通过紫外照射观察检测结果,或其它可以显示结果的本领域常用的技术手段。
该阿留申病毒的检测方法简便、快速、高效,扩增与检测时均不需要复杂仪器设备,扩增反应后可通过加入可视化显色剂观察颜色变化来判断病毒的存在与否,非常适合基层与现场快速检测。同时,该检测方法简化了检测过程,降低了对操作人员的专业要求,使得非专业人员也可以顺利完成检测工作,具有较大的应用前景。
一种优选地采用上述cpa试剂盒检测阿留申病毒的方法,包括以下步骤:
(a)样品处理:每1~2μl液体待测样品与2.5~3.5μla试剂混匀,作用8~10min,再加入2.0~3.0μlb试剂混合得到模板dna;
或,固体待测样品的处理包括以下步骤:将固体待测样品与水混合后冻融2~3次匀浆后静置得到上清液,取1~2μl上清液与2.5~3.5μla试剂混匀,作用8~10min,再加入2.0~3.0μlb试剂混合得到模板dna;固体待测样品与水的质量体积比(g/ml)为1:(3~5);
(b)配制pca反应体系:剥离引物对各0.12~0.28μmol/l、单交叉引物对各0.32~0.64μmol/l、bst2.0dna聚合酶7.5~8.5u、10×缓冲液2.5~3.0μl和dntps0.3~0.5mmol/l,模板dna,加水至体积为30μl并混匀;
(c)恒温扩增:反应体系在59~64℃反应50~70min,得到反应产物;
(d)结果鉴定:在步骤(c)得到的反应产物中加入显色剂,混合均匀后观察显色结果。
该阿留申病毒的检测方法采用上述cpa试剂盒,清楚地限定了检测过程中的具体操作方法、步骤和反应条件等,优化了各引物浓度比例以及反应体系中其他物质的浓度,优化了反应条件,使检测结果更快速和准确。
根据本发明的第五个方面,提供了上述cpa引物组或上述试剂或上述cpa试剂盒或上述检测方法在检测阿留申病毒中的应用。
为了使本发明的发明目的、技术方案及其有益技术效果更加清晰,以下实施例和对比例,对本发明进行进一步详细说明。应当理解的是,本说明书中描述的实施例仅是为了解释本发明,并非为了限定本发明。本发明涉及的各原料均可通过商购获取。
实施例1阿留申病毒cpa引物设计及检测
1、引物设计
参考比对amdv基因序列(nc_001662),设计和筛选出amdv的vp2基因为靶标的cpa引物组,包括剥离引物对和单交叉引物对,其序列分别如下:
剥离引物对的核苷酸序列包括:
bl-f:5’-ctgtmacagaaaccaaccaaggta-3’(seqidno.1);
bl-r:5’-ttgaatgttaggrtatctgttgta-3’(seqidno.2);
单交叉引物对的核苷酸序列包括:
jc-f:5’-gttggtttggttgctctccaaggactccagctgcgccgttgg-3’(seqidno.3);
jc-r:5’-actccagctgcgccgttggttggtttggttgctctccaagga-3’(seqidno.4)。
2、cpa扩增反应
以amdv基因组dna为阳性模板,amdv模板量分别为5.38×101copies/μl、5.38×102copies/μl、5.38×103copies/μl、5.38×104copies/μl、5.38×105copies/μl、5.38×106copies/μl和5.38×107copies/μl,ddh2o为阴性对照进行cpa扩增反应。
cpa反应体系(30μl):剥离引物对各0.2μmol/l、单交叉引物对各0.48μmol/l、bst2.0dna聚合酶8u、10×缓冲液3μl和dntps0.4mmol/l,模板dna,加水至体积为30μl并混匀。
cpa反应条件为:63℃,60min扩增终止反应。
3、结果鉴定
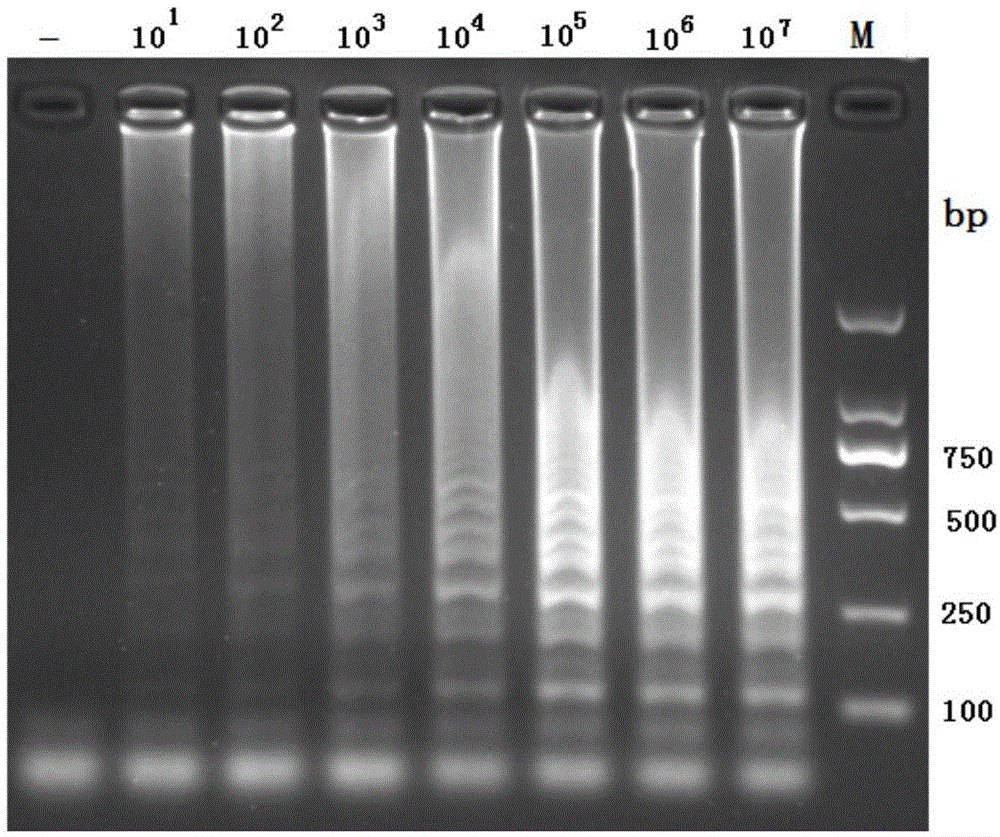
(1)分别取10μl扩增产物进行琼脂糖凝胶电泳,图1的电泳图中,m代表dl2000marker,101、102、103、104、105、106和107分别代表amdv模板量为5.38×101copies/μl、5.38×102copies/μl、5.38×103copies/μl、5.38×104copies/μl、5.38×105copies/μl、5.38×106copies/μl和5.38×107copies/μl的阳性对照,—代表阴性对照。
图1的电泳结果显示,阴性对照无明显条带,各阳性模板的产物呈现cpa特有的梯形条带。
(2)采用简便的目视检测来判断反应结果:在扩增产物中加入sybrgreeni,结果显示阴性管呈橙色,各阳性管呈绿色。
实施例2cpa引物组特异性测试
1、选择犬腺病毒、犬细小病毒、犬瘟热病毒和水貂肠炎病毒的dna,以及水貂、蓝狐和乌苏里貉组织的dna作为dna模板,以amdv为阳性模板,ddh2o为阴性对照,利用实施例1所述的扩增体系和方法进行cpa扩增反应,再进行琼脂糖凝胶电泳,结果见图2。
2、结果鉴定
图2的琼脂糖电泳图中,m代表dl2000marker,1~4分别代表模板为犬腺病毒、犬细小病毒、犬瘟热病毒和水貂肠炎病毒的dna,5~7分别代表模板为水貂、蓝狐和乌苏里貉组织的dna,+代表阳性对照,—代表阴性对照;
图2的琼脂糖电泳结果证明,只有加入amdv阳性对照模板的有cpa特有的梯形条带,说明上述cpa引物和检测方法的特异性好。
实施例3cpa引物组灵敏度测试
1、测试amdv基因组提取液的dna浓度为5.4×107copies/μl,逐级稀释10倍,至稀释浓度为5.4×102copies/μl,作为普通pcr的模板。
2、cpa反应体系跟实施例1相同,普通pcr反应条件如下所示:
30μl反应体系:1μl模板、1×pcr缓冲液、剥离引物各自0.3~0.6μm、hotstartaqtm聚合酶2~3u至30μl混匀。
反应程序:95℃预变性3min,95℃变性30sec、55℃退火30sec、72℃延伸30sec,进行35个循环,最后72℃延伸5min。
3、结果鉴定
取10μl普通pcr产物进行琼脂糖凝胶电泳,图3的电泳图中,m代表dl2000marker,102、103、104、105和106分别代表amdv模板量为5.4×102copies/μl、5.4×103copies/μl、5.4×104copies/μl、5.4×105copies/μl和5.4×106copies/μl的阳性对照,—代表阴性对照,+代表amdv模板量为5.4×106copies/μl。
如图3所示:普通pcr产物产物条带约为223bp,普通pcr在模板浓度约为5.4×102copies/μl时,电泳条带已十分微弱。
图1中cpa琼脂糖凝胶电泳结果,cpa在模板浓度为5.38×102copies/μl时仍可见扩增条件,可见本发明的阿留申病毒的cpa检测法的敏感性显著高于普通pcr。
实施例4cpa检测试剂盒的建立
1、一种检测amdv的cpa检测试剂盒,该试剂盒中含有以下各试剂:cpa引物组、释放剂、bst2.0warmstartdna聚合酶、10×缓冲液、10mmdntps、sybrgreeni(×60)和5×103copies/μlamdv-g836bp质粒。
释放剂:koh0.5mol/l,tritonx-1000.1%(v/v)和hcl0.5mol/l;
10×缓冲液:200mmtris-hcl、100mm(nh)2so4、20mmol/lmgso4、1%tween-20和4mol/lbetaine,缓冲液ph8.8。
实施例5采用cpa试剂盒检测阿留申病毒的方法
采用实施例4的cpa试剂盒对阿留申病毒进行检测,具体检测方法包括以下步骤:
(1)样品处理:将1~2μl血液与2.5~3.5μla试剂混匀,作用8~10min,再加入2.0~3.0μlb试剂混合,得到模板dna;
(2)配制30μlpca反应体系:剥离引物对各0.2μmol/l、单交叉引物对各0.48μmol/l、bst2.0dna聚合酶8u、10×缓冲液3μl和dntps0.4mmol/l,模板dna,加水至体积为30μl并混匀;
(3)恒温扩增:反应体系在63℃反应60min,得到反应产物;
(4)结果鉴定:在步骤(3)得到的反应产物中加入1μlsybrgreeni,混合均匀后观察显色结果,阴性为橙色,阳性为绿色。
尽管已用具体实施例来说明和描述了本发明,然而应意识到,在不背离本发明的精神和范围的情况下可以作出许多其它的更改和修改。因此,这意味着在所附权利要求中包括属于本发明范围内的所有这些变化和修改。
sequencelisting
<110>中国农业科学院特产研究所
<120>检测阿留申病毒的cpa引物组、试剂、试剂盒及检测方法和应用
<160>4
<170>patentinversion3.5
<210>1
<211>24
<212>dna
<213>人工序列
<400>1
ctgtmacagaaaccaaccaaggta24
<210>2
<211>24
<212>dna
<213>人工序列
<400>2
ttgaatgttaggrtatctgttgta24
<210>3
<211>42
<212>dna
<213>人工序列
<400>3
gttggtttggttgctctccaaggactccagctgcgccgttgg42
<210>4
<211>42
<212>dna
<213>人工序列
<400>4
actccagctgcgccgttggttggtttggttgctctccaagga42
- 还没有人留言评论。精彩留言会获得点赞!