一种冰酒的制备及采用橡木桶保藏的方法与流程
本发明属于冰酒制备及保藏方法,具体涉及一种橡木桶装冰酒的制备和保藏方法。
背景技术:
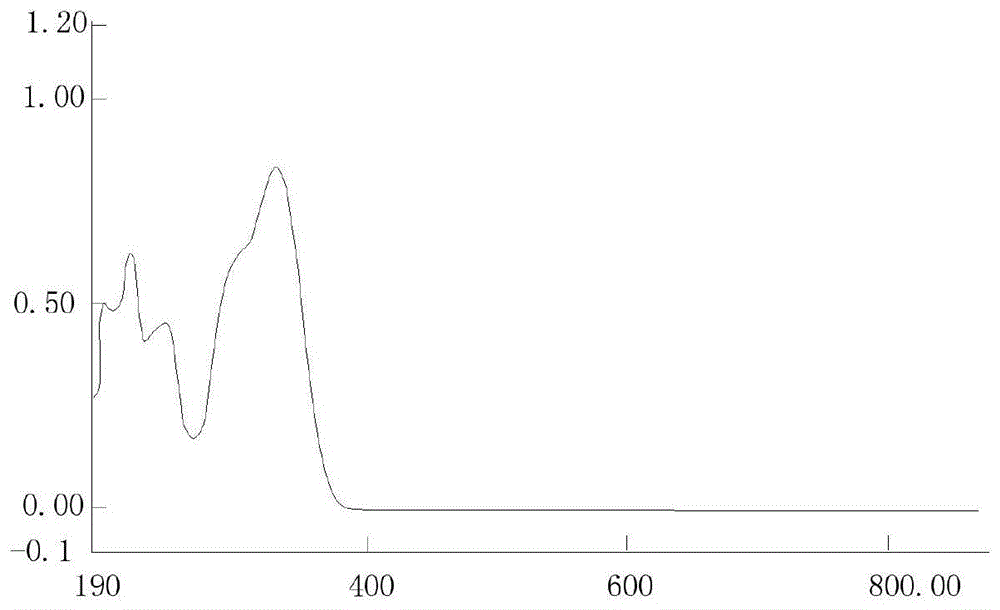
:冰酒因其香气芳香四溢,口感甜润奇佳,深深吸引着众多消费者。冰酒是指将葡萄推迟采收,当气温低于-7℃使葡萄在树枝上保持一定时间,结冰,采收,在结冰状态下压榨,发酵,酿制而成的葡萄酒(在生产过程中不允许外加糖源)。冰酒按颜色分为红冰葡萄酒和白冰葡萄酒。在世界范围内,加拿大安大略省的尼亚加拉地区是目前世界上最著名的冰酒产区,其次是德国、澳大利亚以及法国、匈牙利等国。近年来,我国辽宁省桓仁满族自治县桓龙湖山地成为国内重要的冰葡萄生产基地。桓龙湖山地依山傍水,海拔低,平均海拔380m,由地形、河流、湖泊、植被、土质等形成了适宜种植冰葡萄种植的独特的区域冷湿小气候。桓龙湖山地冬季寒冷但不干燥,最热月(7月和8月)平均气温为23.1℃,年均气温、年均降雨量、土质、平均相对湿度等均达到冰葡萄生长、生产所需的理想条件,是全球范围内不多见的适合冰葡萄种植的区域。正是因为桓龙湖山地得天独厚的生态、地理、气候优势,现在辽宁省桓仁满族自治县的冰葡萄酒年产量达到840吨,占世界总产量的30%左右,居世界首位。传统的冰葡萄酒酿造工艺中,通常采用冰葡萄推迟采收的方式,gb/t25504-2010冰葡萄酒中记载“当气温低于-7℃使葡萄在树枝上保持一定时间,结冰,采收”,但是,在我国东北地区,这样制备方式会导致冰葡萄落粒较多,且葡萄树枝容易冻伤,影响下一年的产量。因此,该方法并不适用于我国东北地区。橡木桶是冰葡萄酒最好的陈酿容器。橡木组织具有多孔性的特点,可以缓慢地加速葡萄酒的陈酿过程,同时橡木中含有的丹宁、木质素、香兰素、橡木内酯、丁子香酚等化合物质会溶解于葡萄酒中,这些物质可以使葡萄酒的颜色更为稳定、口感更为柔和、香味更为协调。此外,橡木桶壁因具备通透性,因而可提高葡萄酒的澄清度。橡木的品种、树龄、生长环境、加工过程中的烘烤程度、橡木桶的使用时间长短和使用次数等因素均影响葡萄酒的陈酿效果。原料品质和成熟度优良的葡萄经良好酿造工艺酿造出的葡萄酒,再经橡木桶的陈酿,会变得更加柔和、圆润、肥硕。但是本领域对橡木桶装冰酒品质变化相关研究较少,尤其是橡木桶用于冰酒陈酿方面的研究鲜有报道。技术实现要素:为弥补现有技术的不足,本发明在冰酒的酿造过程中,将vidal(威代尔)冰葡萄经挑选、清洗、精选及破冰榨汁、酶解、榨汁、接种、发酵、倒酒、下胶、过滤、陈酿、过滤、精滤、橡木桶贮存,提出了一种冰葡萄品质保持和提升的方法,同时优化了冰葡萄酒的酿造和陈酿工艺,从活性成分检测、风味口感等多角度改进冰葡萄酒的酿造技术。为实现上述目的,本发明采用如下技术方案,(1)冰葡萄采收当葡萄园夜间温度低于-7℃时,将冰葡萄果穗连带一段枝条剪下,就近悬挂在葡萄架上,当夜间温度达到-10℃—-15℃时,在夜间采摘葡萄果穗,并在2个小时内运抵冰葡萄加工车间进行精选;(2)冰葡萄精选及破冰榨汁冰葡萄精选车间的温度为-5℃—-10℃,进行人工颗粒精选,并立即进行带冰冷榨,从冰冻果实的裂缝中得到浓缩果汁并过滤,得到含糖量高达410-420g/l的冰葡萄汁;(3)酵母菌活化由于冰葡萄汁中含糖量太高,发酵反应很难启动,因此需对酵母进行活化。20℃下将山葡萄汁和冰葡萄汁以2:1的比例混匀,接种0.4-0.5g/l酵母菌进行活化,活化时间为48h,活化液中酵母菌细胞数要达到108个/l。(4)低温发酵,地窖贮存以步骤(3)所得活化液作为发酵液,按5%(v/v)的比例接种到冰葡萄汁中进行主发酵,发酵温度为15℃,主发酵时间为2-3个月,当冰葡萄汁中含糖量降低到180-190g/l时转入10℃条件下进行后发酵,实行24小时监控,当糖度不再下降时发酵结束,冷稳合格后,将冰酒原汁注入地窖中的法国维卡(vicard)橡木桶里;优选225升法国维卡橡木桶。为达到最佳的口感,本发明还采用下述方法对冰酒提质,具体步骤为:将步骤(4)中制备的冰酒原汁在地下窖藏陈酿9年后,将其分装在橡木桶中,在10℃条件下贮存1个月后即可饮用,橡木桶可以反复使用2-3次。进一步的,所述步骤(2)中人工颗粒精选指的是将饱满、坚硬、没有受到任何损伤、颜色一致且棕红色的葡萄颗粒精选出来。进一步的,所述提质步骤中的橡木桶为2升法国维卡(vicard)橡木桶。本发明的有益效果是:(1)本发明采取的是当葡萄园夜间温度低于-7℃时,将冰葡萄果穗连带一段枝条剪下,就近悬挂在葡萄架上的方法,该采收方法可以有效避免传统采收方法导致冰葡萄落粒较多,且葡萄树枝容易冻伤,影响下一年的产量等不良效果。(2)传统工艺中由于冰葡萄汁中含糖量太高,发酵反应很难启动,因此生产上不仅需要价格昂贵的酵母菌,而且添加量是普通葡萄酒的3倍以上,造成较高的生产成本。本发明采取酵母菌先行活化的方式,不仅使发酵反应容易启动,而且使酵母的使用量减少90%以上,生产成本显著降低。(3)采用2升法国产橡木桶为窖藏年份冰葡萄酒精准提质。经过多项科学实验和感官品评实验,提出用2升法国产橡木桶在10℃条件下贮存1个月,以提升窖藏年份冰葡萄酒陈酿潜质,而且提出橡木桶可以反复使用2-3次的陈酿方法。该冰葡萄酒精准提质方法简单易行,科学有效。且采用该橡木桶提质的冰葡萄酒具有冰葡萄固有的香味和橡木的清香,橡木桶装冰葡萄酒可显著提高抗氧化能力,脂溶性抗氧化能力和水溶性抗氧化能力比普通冰葡萄酒分别提高2.2倍和2.0倍。橡木桶装2010年窖藏年份冰葡萄酒含有丰富的钾、纳、钙、铁、锌、铜、锰、镁、硒等矿物元素,尤其是硒含量比普通冰葡萄酒高出300倍。本发明具有显著的社会和经济效益。附图说明图1绿原酸标准品在190-900nm波长条件下全波长扫描谱图。图2冰酒不同贮藏阶段脂溶性抗氧化能力和水溶性抗氧化能力比较。具体实施方式下面结合具体实施例对本发明的技术方案作进一步的说明,但本发明不以任何形式受限于实施例内容。实施例中所述试验方法如无特殊说明,均为常规方法;如无特殊说明,所述试剂和生物材料,均可从商业途径获得。实施例11.冰葡萄采收:当葡萄园夜间温度低于-7℃时,将冰葡萄果穗连带一段枝条剪下,就近悬挂在葡萄架上,当夜间温度达到-10℃—-15℃时,在夜间采摘葡萄穗,2个小时内运抵冰葡萄加工车间进行精选。2.冰葡萄精选及破冰榨汁:精选车间的温度为-5℃—-10℃,进行人工颗粒精选,将饱满、坚硬、没有受到任何损伤、颜色一致(棕红色)的葡萄颗粒精选出来,并立即进行带冰冷榨,从冰冻果实的裂缝中得到浓缩果汁并过滤。得到含糖量高达410-420g/l的冰葡萄汁。3.酵母菌活化:20℃下将山葡萄汁和冰葡萄汁以2:1的比例混匀,接种0.4-0.5g/l酵母菌进行活化,活化时间为48h,活化液中酵母菌细胞数要达到108个/l。4.低温发酵,地窖贮存:以上述活化液作为发酵液,按5%(v/v)的比例接种到冰葡萄汁中进行主发酵,发酵温度为15℃,主发酵时间为2-3个月,当冰葡萄汁中含糖量降低到180-190g/l时转入10℃条件下进行后发酵,实行24小时监控,当糖度不在下降时发酵结束,冷稳合格后,注入地窖中的法国百年橡木桶里,在微透氧状态下,使酒慢慢成熟、日臻完善,各种矿物质、微量元素得到有效充分缔结,浑然天成,使产品特殊的花香、果香、蜜香、木香,优雅芬芳沁人心脾。5.橡木桶提质:上述冰酒原汁在地下窖藏陈酿9年后,为了进一步提高酒的品质,衬托该窖藏年份冰葡萄酒陈酿潜质,将其分装在2升法国产橡木桶中,在10℃条件下贮存1个月后饮用,该橡木桶可以反复使用2-3次。本发明成品质量检测1冰葡萄酒中绿原酸的提取与含量的测定(一)实验原理采用体积比为1:1的乙酸乙酯和氯仿的混合溶液进行萃取,经过减压旋转蒸发法提纯,乙醇溶解提取物。根据紫外分光光度计法确定最适提取液乙醇的浓度,全波长扫描法确定样品的最高吸收峰。采用高效液相色谱法测定提取物中绿原酸的含量。(二)涉及的仪器设备与试剂如下:(1)仪器设备:lc-10a高效液相色谱仪;spd-m10a二极管阵列检测器;sil-10a自动进样器;lc-10a高压输液泵,日本岛津公司;hypersil-c18色谱柱(5μm,250mm,4.6mm),大连依利特科学仪器有限公司;pl203型精密电子天平,上海梅特勒-托利多仪器有限公司;旋转蒸发仪,德国ika公司;超声;uv-2600紫外可见分光光度计,日本岛津公司。(2)试剂:威代尔(vidal)冰葡萄汁,辽宁五女山米兰酒业有限公司;绿原酸标准品;乙醇、乙酸乙酯、氯仿、磷酸分析纯;乙腈色谱纯。(三)测定步骤(1)对照品溶液制备:精密称取绿原酸标准品10mg,置于10ml容量瓶中,加50%乙醇,溶解定容至刻度,制成1mg/ml的绿原酸对照品储备液。取储备液0.2、0.4、0.6、0.8、1.0ml加入50%乙醇定容至5ml,制成40、80、120、160、200、400μg/ml的对照样品溶液。(2)供试品溶液的制备:分别取威代尔冰葡萄酒原酒以及采用实施例1所述方法进行橡木桶贮藏一个月、两个月、三个月的冰酒20g,加入40ml氯仿-乙酸乙酯的混合溶液(1︰1),摇晃15min,静置分层;取上层溶液旋转蒸发,至无溶剂蒸出停止。加入适量的50%乙醇洗圆底烧瓶定容至5ml;混匀,经微孔滤膜(0.45μm)过滤,即得。(3)色谱条件①测定波长的确定:采用紫外-可见分光光度计在190~900nm进行全波长扫描,绿原酸对照品在330nm波长处出现最大吸收峰,见图1,故确定检测波长为330nm。②测定绿原酸含量:色谱条件色谱柱:hypersil-c18(5μm,250mm,4.6mm);流动相为乙腈-0.5%磷酸溶液10:90;流速1.0ml/min;柱温:室温;进样量:20μl;检测波长330nm。(四)结果计算以标准峰面积(或峰高)为纵坐标,标准绿原酸浓度(μg/ml)为横坐标,制作标准曲线。(五)冰葡萄酒中绿原酸的含量的测定结果表1冰葡萄酒中绿原酸的含量(μg/g)(六)结论随着原酒在橡木桶中贮存时间的延长,绿原酸含量略有减少。2.冰葡萄酒酒精度测定(密度瓶法)(一)原理以蒸馏法去除样品中的不挥性物质,用密度瓶法测定馏出液的密度。根据馏出液(酒精水溶液)的密度,查附录a,求得20℃时乙醇的体积分数,即酒精度,%(体积分数)表示。(二)仪器分析天平:感量0.0001g;全玻璃蒸馏器:500ml;恒温水浴:精度±0.1℃;附温度计密度瓶:25ml或50ml。(三)试样的制备用一洁净、干燥的100ml容量瓶准确量取100ml样品(液温20℃)于500ml蒸馏瓶中,用50ml水分三次冲洗容量瓶,洗液全部并入蒸馏瓶中,再加几颗玻璃珠,连接冷凝器,以取样用的原容量瓶作接收器(外加冰浴)。开启冷却水,缓慢加热蒸馏。收集馏出液接近刻度,取下容量瓶,盖塞。于20.0℃±0.1℃水浴中保温30min,补加水至刻度,混匀,备用。(四)分析步骤(1)蒸馏水质量的测定a)将密度瓶洗净并干燥,带温度计和侧孔罩称量。重复干燥和称量,直至恒重(m)。b)取下温度计,将煮沸冷却至15℃左右的蒸馏水注满恒重的密度瓶,插上温度计,瓶中不得有气泡。将密度瓶浸入20.0℃±0.1℃的恒温水浴中,待内容物温度达20℃,并保持10min不变后,用滤纸吸去侧管溢出的液体,使侧管中的液面与侧管管口齐平,立即盖好侧孔罩,取出密度瓶,用滤纸擦干瓶壁上的水,立即称量(m1)。(2)试样质量的测量将密度瓶中的水倒出,用试样(三)反复冲洗密度瓶3次~5次,然后装满,按(1)中b)同样操作,称量(m2)。(五)结果计算样品在20℃时的密度按式(1)计算,空气浮力校正值按式(2)计算。式中:——样品在20℃时的密度,单位为克每升(g/l);m——密度瓶的质量,单位为克(g);m1——20℃时密度瓶与水的质量,单位为克(g);m2——20℃时密度瓶与试样的质量,单位为克(g);ρ0——20℃时蒸馏水的密度(998.20g/l);a——空气浮力校正值;ρu——干燥空气在20℃、1013.25hpa时的密度值(≈1.2g/l);997.0——在20℃时蒸馏水与干燥空气密度值之差,单位为克每升(g/l)。根据试样的密度查附录a,求得酒精度。所得结果表示至一位小数。(六)精密度在重复性条件下获得的两次独立测定结果的绝对差值不得超过算术平均值的1%。(七)冰酒酒精度的测定结果表2冰酒酒精度的测定结果3.冰葡萄酒总糖测定(直接滴定法)(一)原理利用费林溶液与还原糖共沸,生成氧化亚铜沉淀的反应,以次甲基蓝为指示液,以样品或经水解后的样品滴定煮沸的费林溶液,达到终点时,稍微过量的还原糖将蓝色的次甲基蓝还原为无色,以示终点。根据样品消耗量求得总糖或还原糖的含量。(二)试剂和材料1、盐酸溶液(1+1)2、氢氧化钠溶液(200g/l)3、葡萄糖标准溶液(2.5g/l):称取在105℃~110℃烘箱内烘干3h并在干燥器中冷却的无水葡萄糖2.5g(精确至0.0001g),用水溶解并定容至1000ml。4、费林溶液(ⅰ、ⅱ)a)配制:按gb/t603配制b)标定预备试验:吸取费林溶液ⅰ、ⅱ各5.00ml于250ml三角瓶中,加50ml水,摇匀,在电炉上加热至沸,在沸腾状态下用葡萄糖标准溶液滴定,当溶液的蓝色消失呈红色时,加2滴次甲基蓝指示液,继续滴定蓝色消失,记录消耗葡萄糖标准溶液的体积。正式试验:吸取费林溶液ⅰ、ⅱ各5.00ml于250ml三角瓶中,加50ml水和比预备试验少1ml的葡萄糖标准溶液,加热至沸,并保持2min,加2滴次甲基蓝指示液,在沸腾状态下于1min内用葡萄糖标准溶液滴至终点,记录消耗葡萄糖标准溶液的总体积(v)。c)计算费林溶液ⅰ、ⅱ各5ml相当于葡萄糖的克数按式(3)计算:式中:f——费林溶液ⅰ、ⅱ各5ml相当于葡萄糖的克数,单位为克(g);m——称取无水葡萄糖的质量,单位为克(g);v——消耗葡萄糖标准溶液的总体积,单位为毫升(ml)。(三)试样的制备准确吸取一定量的样品(v1)[液温20℃]于100ml容量瓶中,使之所含总糖量为0.2g~0.4g,加5ml盐酸溶液,加水至20ml,摇匀。于(68±1)℃水浴上水解15min,取出,冷却。用氢氧化钠溶液中和至中性,调温至20℃,加水定容至刻度(v2),备用。(四)分析步骤以试样代替葡萄糖标准溶液,按b)同样操作,记录消耗试样的体积(v3),结果按式(4)计算。(五)结果计算除干葡萄酒、半干葡萄酒以外的其它葡萄酒总糖的含量按式(4)计算。式中:f——费林溶液ⅰ、ⅱ各5ml相当于葡萄糖的克数,单位为克(g);v1——吸取样品的体积,单位为毫升(ml);v2——样品稀释后或水解定容的体积,单位为毫升(ml);v3——消耗试样的体积,单位为毫升(ml);x——葡萄酒总糖的含量,单位为克每升(g/l)。所得结果表示至一位小数。(六)精密度在重复性条件下获得的两次独立测定结果的绝对差值不得超过算术平均值的2%。(七)冰酒总糖的测定结果表3冰酒总糖的测定结果4.冰葡萄酒干浸出物测定(一)原理用密度瓶法测定样品或蒸出酒精后的样品的密度,然后用其密度值查附录c,求得总浸出物的含量。再从中减去总糖的含量,即得干浸出物的含量。(二)仪器瓷蒸发皿:200ml;恒温水浴:精度±0.1℃;附温度计密度瓶:25ml或50ml。(三)试样的制备用100ml容量瓶量取100ml样品(液温20℃),倒入200ml瓷蒸发皿中,于水浴上蒸发至约为原体积的三分之一取下,冷却后,将残液小心地移入原容量瓶中,用水多次荡洗蒸发皿,洗液并入容量瓶中,于20℃定容至刻度。也可使用2.1(三)中蒸出酒精后的残液,在20℃时以水定容至100ml。(四)分析步骤吸取试样,按2.1中(四)同样操作,并按2.1(五)计算出脱醇样品20℃时的密度ρ1。以ρ1×1.00180的值,查附录c,得出总浸出物含量(g/l)。式中:ρ1——脱醇样品在20℃时的密度,单位为克每升(g/l);m——密度瓶的质量,单位为克(g);m1——20℃时密度瓶与水的质量,单位为克(g);m2——20℃时密度瓶与试样的质量,单位为克(g);ρ0——20℃时蒸馏水的密度(998.20g/l);a——空气浮力校正值;ρu——干燥空气在20℃、1013.25hpa时的密度值(≈1.2g/l);997.0——在20℃时蒸馏水与干燥空气密度值之差,单位为克每升(g/l)。——20℃时密度瓶体积的修正系数。根据ρ1×1.00180的值,查附录c,求得总浸出物含量(g/l)。所得结果表示至一位小数。(五)精密度在重复性条件下获得的两次独立测定结果的绝对差值不得超过算术平均值的2%。(六)冰酒干浸出物的测定结果表4冰酒干浸出物的测定结果5.冰葡萄酒总酸测定(指示剂法)(一)原理利用酸碱滴定原理,以酚酞作指示剂,用碱标准溶液滴定,根据碱的用量计算总酸含量。(二)试剂和材料氢氧化钠标准滴定溶液[c(naoh)=0.05mol/l]:按gb/t601配制与标定,并准确稀释。酚酞指示液(10g/l):按gb/t603配制。(三)分析步骤吸取样品2ml(液温20℃;取样量可根据酒的颜色深浅而增减),置于250ml三角瓶中,加入50ml水,同时加入2滴酚酞指示液,摇匀后,立即用氢氧化钠标准滴定溶液滴定至终点,并保持30s内不变色,记下消耗氢氧化钠标准滴定溶液的体积(v1)。同时做空白试验。(四)结果计算样品中总酸的含量按式(7)计算。式中:x——样品中总酸的含量(以酒石酸计),单位为克每升(g/l);c——氢氧化钠标准滴定溶液的浓度,单位为摩尔每升(mol/l);v0——空白试验消耗氢氧化钠标准滴定溶液的体积,单位为毫升(ml);v1——样品滴定时消耗氢氧化钠标准滴定溶液的体积,单位为毫升(ml);v2——吸取样品的体积,单位为毫升(ml);75——酒石酸的摩尔质量的数值,单位为克每摩尔(g/mol)。所得结果表示至一位小数。(五)精密度在重复性条件下获得的两次独立测定结果的绝对差值不得超过算术平均值的5%。(六)冰酒总酸的测定结果表5冰酒总酸的测定结果6.冰葡萄酒挥发酸测定(一)原理以蒸馏的方式蒸出样品中的低沸点酸类即挥发酸,用碱标准溶液进行滴定,再测定游离二氧化硫和结合二氧化硫,通过计算与修正,得出样品中挥发酸的含量。(二)试剂与溶液氢氧化钠标准滴定溶液[c(naoh)=0.05mol/l]:按gb/t601配制与标定,并准确稀释。酚酞指示液(10g/l):按gb/t603配制。盐酸溶液:将浓盐酸用水稀释4倍。碘标准滴定溶液按gb/t601配制与标定,并准确稀释。碘化钾淀粉指示液(5g/l):称取5g淀粉于500ml水中,加热至沸,并持续搅拌10min。再加入200g氯化钠,冷却后定容至1000ml。硼酸钠饱和溶液:称取5g硼酸钠(na2b4o7·10h2o)溶于100ml热水中,冷却备用。(三)分析步骤1、实测挥发酸:安装好蒸馏装置。吸取10ml样品(v)[液温20℃]在该装置上进行蒸馏,收集100ml馏出液。将馏出液加热至沸,加入2滴酚酞指示液,用氢氧化钠标准滴定溶液滴定至粉红色,30s内不变色即为终点,记下消耗氢氧化钠标准滴定溶液的体积(v1)。2、测定游离二氧化硫:于上述溶液中加入1滴盐酸溶液酸化,加入2ml淀粉指示液和几粒碘化钾,混匀后用上术碘标准溶液滴定,得出碘标准滴定溶液消耗的体积(v2)。3、测定结合二氧化硫:在上述溶液中加入上述硼酸钠饱和溶液,至溶液显粉红色,继续用碘标准滴定溶液滴定,至溶液呈蓝色,得到碘标准滴定溶液消耗的体积(v3)。(四)结果计算样品中实测挥发酸的含量按式(8)计算。式中:x1——样品中实测挥发酸的含量(以乙酸计),单位为克每升(g/l);c——氢氧化钠标准滴定溶液的浓度,单位为摩尔每升(mol/l);v1——消耗氢氧化钠标准滴定溶液的体积,单位为毫升(ml);60——乙酸的摩尔质量的数值,单位为克每摩尔(g/mol);v——吸取样品的体积,单位为毫升(ml)。若挥发酸含量接近或超过理化指标时,则需进行修正。修正时,按式(9)换算:式中:x——样品中真实挥发酸(以乙酸计)含量,单位为克每升(g/l);x1——实测挥发酸含量,单位为克每升(g/l);c2——碘标准滴定溶液的浓度,单位为摩尔每升(mol/l);v——吸取样品的体积,单位为毫升(ml);v2——测定游离二氧化硫消耗碘标准滴定溶液的体积,单位为毫升(ml);v3——测定结合二氧化硫消耗碘标准滴定溶液的体积,单位为毫升(ml);32——二氧化硫的摩尔质量的数值,单位为克每摩尔(g/mol);1.875——1g游离二氧化硫相当于乙酸的质量,单位为克(g);0.9375——1g结合二氧化硫相当于乙酸的质量,单位为克(g);所得结果表示至一位小数。(五)精密度在重复性条件下获得的两次独立测定结果的绝对差值不得超过算术平均值的5%。(六)冰酒挥发酸的测定结果表6冰酒挥发酸的测定结果7.游离二氧化硫(氧化法)(一)原理在低温条件下,样品中的游离二氧化硫与过氧化氢过量反应生成硫酸,再用碱标准溶液滴定生成的硫酸。由此可得到样品中游离二氧化硫的含量。(二)试剂和材料a)过氧化氢溶液(0.3%):吸取1ml30%过氧化氢(开启后存于冰箱),用水稀释至100ml。使用当天配制。b)磷酸溶液(25%):量取295ml85%磷酸,用水稀释至1000ml。c)氢氧化钠标准滴定溶液[c(naoh)=0.01mol/l]:准确吸取100ml氢氧化钠标准滴定溶液,以无二氧化碳水定容至500ml。存入在橡胶塞上装有钠石灰管的瓶中,每周重配。d)甲基红-次甲基蓝混合指示液:按gb/t603配制。(三)仪器a)二氧化硫测定装置。b)真空泵(四)分析步骤1.将二氧化硫测定装置连接妥当,i管与真空泵相接,直管冷凝管通入冷却水。取下梨形瓶和气体洗涤器,在梨形瓶中加入20ml过氧化氢溶液、气体洗涤器中加入5ml过氧化氢溶液,各加3滴混合指示剂后,溶液立即变为紫色,滴入氢氧化钠标准溶液,使其颜色恰好变为橄榄绿色,然后重新安装妥当,将短颈球瓶浸入冰浴中。2.吸取20.00ml样品(液温20℃),从c管上口加入a瓶中,随后吸取10ml磷酸溶液,亦从通气管上口加入短颈球瓶中。3.开启真空泵,使抽入空气流量1000ml/min~1500ml/min,抽气10min。取下梨形瓶,用氢氧化钠标准滴定溶液滴定至重现橄榄绿色即为终点,记下消耗的氢氧化钠标准滴定溶液的体积数。以水代替样品做空白试验,操作同上。一般情况下,气体洗涤器中溶液不应变色,如果溶液变为紫色,也需用氢氧化钠标准滴定溶液测定至橄榄绿色,并将所消耗的氢氧化钠标准滴定溶液的体积与梨形瓶消耗的氢氧化钠标准滴定溶液的体积相加。(五)结果计算样品中游离二氧化硫的含量按式(10)计算。式中:x——样品中游离二氧化硫的含量,单位为毫克每升(mg/l);c——氢氧化钠标准滴定溶液的浓度,单位为摩尔每升(mol/l);v——测定样品时消耗的氢氧化钠标准滴定溶液的体积,单位为毫升(ml);v0——空白试验消耗的氢氧化钠标准滴定溶液的体积,单位为毫升(ml);32——二氧化硫的摩尔质量的数值,单位为克每摩尔(g/mol);20——吸取样品的体积,单位为毫升(ml);所得结果表示至一位小数。(六)精密度在重复性条件下获得的两次独立测定结果的绝对差值不得超过算术平均值的10%。(七)冰酒游离二氧化硫的测定结果表7冰酒游离二氧化硫的测定结果8.冰酒和橡木金属矿物质元素含量(一)实验原理利用氩等离子体产生的高温使用试样完全分解形成激发态的原子和离子,由于激发态的原子和离子不稳定,外层电子会从激发态向低的能级跃迁,因此发射出特征的谱线。通过光栅等分光后,利用检测器检测特定波长的强度,光的强度与待测元素浓度成正比。(二)仪器设备与试剂(1)仪器设备:prodigy美国leemanlabs公司(2)试剂:hno3分析级;h2o2分析级(三)测定步骤(1)橡木粉样品处理分别称取0.5g橡木粉于消解罐中,加入5ml的浓hno3和2ml的h2o2,拧紧盖,置于微波炉中消解10min,冷却至室温后,转移至50ml容量瓶中,用超纯水水定容,摇匀待测。(2)冰酒样品处理分别称取五女山冰酒原酒、橡木桶-1、橡木桶-2、橡木桶-3橡木桶-4、橡木桶-5各5g,旋转蒸发至干,加入10ml的浓hno3和2ml的h2o2,超声15min,转移至100ml的容量瓶中,用超纯水定容,待测。(3)仪器操作参数高频发生器功率1100w;冷却气流量20l/min;雾化气压40psi;辅助气流量0.5l/min;溶液提取量1.5ml/min;积分时间15s(四)结果计算按仪器操作参数测定各元素标准溶液和样品溶液,若样品溶液浓度超出标准曲线,需将样品溶液进行稀释,再进行测定。按下列公式(11)计算样品中各元素含量:其中:x—样品中各元素含量,μg/g;c—由标准曲线查得的样品溶液浓度,μg/ml;v—样品溶液体积,ml;n—稀释倍数;w—试样质量,g。(五)冰酒和橡木金属矿物质元素含量测定结果表8五女山冰酒和橡木金属矿物质元素含量(μg/g)注:---表示未检出9.冰酒中微生物指标的检测(一)测定方法1.微生物指标(1)细菌总数:gb4789.2-2016食品安全国家标准食品微生物学检验菌落总数测定(2)酵母菌总数:gb4789.15-2016食品安全国家标准食品微生物学检验霉菌和酵母计数(3)大肠菌群:gb4789.3-2016食品安全国家标准食品微生物学检验大肠菌群计数(4)金黄色葡萄球菌:gb4789.10-2016食品安全国家标准食品微生物学检验金黄色葡萄球菌检验(5)沙门氏菌:gb4789.4-2016食品安全国家标准食品微生物学检验沙门氏菌检验2.参考的其他标准(1)gb4789.1-2016食品安全国家标准食品微生物学检验总则。(2)gb4789.25-2003食品安全国家标准食品微生物学检验酒类检验。(3)gb2758-2012食品安全国家标准发酵酒及其配制酒。(二)测定结果表9五女山冰酒微生物指标检测结果10.五女山冰酒品评评酒员:胡文忠、冮洁、邹宇、姜爱丽、王艳颖、陈晨、田密霞表10冰酒品评打分标准11.冰酒抗氧化能力的测定(一)实验原理:(1)采用化学发光法来测定样品中的抗氧化物质的含量。在紫外光(uv)照射下,光敏剂(发光氨l)与o2反应,产生中间产物[l*o2],该中间产物再次与o2相互作用,生成超氧阴离子自由基o2·-和发光氨阳离子自由基。其自由基反应公式如下:l+hv(uv)+o2→[l*o2]→l·++o2·-这些自由基中,有一部分与样品中的抗氧化物反应,当所有抗氧化物被自由基消耗完后,剩下的超氧阴离子基o2·-继续与发光氨阳离子自由基反应,产生激发态的酞酸胺阴离子ap*2-,由于激发态的酞酸胺阴离子不稳定,要回到基态而发光(蓝色光),发射光被光电倍增管检测。其检测反应公式如下:o2·-+l·+→n2+ap*2-→ap2-+hv(blueluminescence)这里,发光氨有两个作用:光敏剂和检测剂。(2)发光信号强度通过光电倍增管在预定的时间内被连续的检测。在水溶性物质抗氧化能力测定方法中,自由基与抗氧化物反应,直到抗氧化物被消耗完之前的一段时间是不发光的,我们定义这段时间为滞后时间(lag-time)。当抗氧化物被消耗完后,自由基继续反应,随着反应的持续,发光信号强度不断增加,直到最大值(v),滞后时间的长短取决于样品中抗氧化物的含量。在acw测量中,滞后时间是这样定义的:由测量曲线的一阶导数算出曲线的拐点,拐点的切线与x轴的交点即是滞后时间(lag-time)。滞后时间有pcl软件自动计算出来。(二)仪器设备与试剂(1)仪器设备:德国耶拿公司产抗氧化剂和自由基分析仪。(2)试剂:脂溶性物质抗氧化能力实验所需试剂试剂包试剂名称reagent1:甲醇reagent2:反应缓冲剂reagent3:ps-1储备液(反应光敏剂和检测剂),250μl/瓶reagent4:标准试剂(以相当于多少nmol的trolox(维生素e)来表示脂溶性物质的抗氧化性)水溶性物质抗氧化能力实验所需试剂试剂包试剂名称reagent1:样品溶剂reagent2:反应缓冲剂reagent3:ps-1储备液(反应光敏剂和检测剂),250μl/瓶reagent4:标准试剂(以相当于多少nmol的抗坏血酸来表示水溶性物质的抗氧化性)(三)测定步骤1.水溶性物质抗氧化能力测定方法(1)方法参数由于只要计算出测量曲线的拐点,即可算出滞后时间,所以测量过程中,只要信号达到最高点并开始下降时,就可点击“stop”手动停止。没有必要等到acw方法规定时间停止测量。(2)空白测量首先执行清洗3次,点击“purge→cleaner1”,然后测量空白“blank”至少2次,空白值的rsd不得超过5%,直到获得稳定值,不平行的空白值应该删除。当空白测量稳定时,系统才达到稳定。(3)标准测量用50μl的移液枪分别移取5μl、10μl、20μl、30μlreagent4工作溶液(100nmol/l),相当于0.5nmol、1.0nmol、2.0nmol和3.0nmol的工作曲线系列溶液。由于抗坏血酸容易被氧化,加reagent4时间应尽可能短,同时加reagent3和4时间,混匀时间和插到进样口时间尽量保持一致,这样可以得到较好的重复性。另外,每次测量前,先加入reagent1和reagent2,预先混合好,然后,快速加入reagent3和reagent4工作溶液,简单混匀后,插到进样口测量。(4)样品制备和测量用acw方法测量的物质必须是水溶液或水溶性的物质。如果样品的含量超过标注曲线范围,需要用reagent1稀释后才能测量,保证在曲线范围内。2.脂溶性物质抗氧化能力测定方法(1)方法参数由于需要计算出测量曲线的积分值,所以在一个测量系列中,空白测量、标样测量和样品测量时间必须一致的。(2)空白测量首先执行清洗3次,点击“purge→cleaner2+1”,然后测量空白“blank”至少3次,空白值的rsd最好不超过5-10%,否则,空白需继续测量,直到获得稳定值。不平行的空白值应该删除。当空白测量稳定时,系统才达到稳定。(3)标准测量用50μl的移液枪分别移取5μl、10μl、20μl、30μlreagent4工作溶液(100nmol/l),相当于0.5nmol、1.0nmol、2.0nmol和3.0nmol的工作曲线系列溶液。由于torlox容易被氧化,加reagent4时间应尽可能短,同时加reagent3和4时间,混匀时间和插到进样口时间尽量保持一致,这样可以得到较好的重复性。另外,每次测量前,先加入reagent1和reagent2,预先混合好,然后快速加入reagent3和reagent4工作溶液,简单混匀后,插到进样口测量。(4)样品制备和测量用acl方法测量的物质必须是溶于甲醇的物质。当然也适用于能溶于其他有机溶剂的物质,最好是这种有机溶剂能和甲醇互溶。然而,值得注意的是:有些有机溶剂会溶解样品管(塑料的),这样也会有一定的抗氧化性,造成错误的测量结果。所以当使用其他溶剂时,为了排除这种错误结果的可能性,需要执行一次控制分析(即除了样品外,加有机溶剂或稀释剂到样品中)。如果样品的含量超过标注曲线范围,需要用reagent1或选择的其他溶剂稀释后才能测量,保证在曲线范围内。如果样品中有颗粒物存在,需用0.45μm有机膜过滤或离心除掉。(四)结果计算1.水溶性物质抗氧化能力结果计算其中:quantity:nmol(以抗坏血酸计)dilution:稀释倍数m:摩尔质量(抗坏血酸176.13g/mol)pipettedvolume:用移液枪移取的体积(μl)2.脂溶性物质抗氧化能力结果计算采用上述公式(12)、(13)计算其中:quantity:nmol(以trolox计)dilution:稀释倍数m:摩尔质量(trolox250.3g/mol)pipettedvolume:用移液枪移取的体积(μl)(五)测定结果:(1)冰酒及葡萄酒抗氧化能力测定结果表11冰酒抗氧化能力研究结果表明:与原酒相比,加入橡木桶中的冰酒的抗氧化能力显著增强,橡木桶中存放1个月的冰酒的脂溶性抗氧化能力和水溶性抗氧化能力分别是原酒的2.197倍和2.027倍,但橡木桶中存放的冰酒,其抗氧化能力并不随着贮藏时间的延长而增加,从贮藏1个月到3个月这段过程中,橡木桶装冰酒的脂溶性抗氧化能力和水溶性抗氧化能力基本保持不变。12.冰葡萄酒中多酚类物质的测定(一)原理冰葡萄酒中的多酚类物质经有机溶剂提取,用甲醇和乙酸做流动相,高效液相色谱仪反相色谱法进行检测,外标法进行计算。(二)仪器和试剂(1)高效液相色谱仪,紫外检测器(2)超声清洗仪(3)旋转蒸发仪(4)甲醇:色谱纯;乙酸,乙酸乙酯、石油醚(30-60℃):优级纯(5)儿茶素、表儿茶、榭皮素、香豆酸、对羟基苯甲酸、咖啡酸、阿魏酸、单宁酸、香草酸、丁香酸标准品:sigma。(三)色谱条件c18色谱柱(4.6mm×25cm),流动相为甲醇和乙酸,流速:1ml/min,进样量:20μl,检测波长为280nm和320nm。(四)实验步骤(1)标准溶液配制分别称取一定量多酚标准品,用甲醇溶解,配成浓度为1mg/ml的标准溶液。分别从表1的标准溶液中取出一定量的标准溶液于5ml容量瓶中,用甲醇定容,配成不同浓度的混合标准溶液,摇匀,过0.45μm膜。表12不同多酚标准溶液浓度(2)样品处理a)冰葡萄酒多酚物质的提取准确量取冰葡萄酒样品10.00ml于50ml容量瓶中,加入10ml石油醚+乙酸乙酯(1+1)振荡萃取2min,分液,重复3次,合并有机相转入蒸馏瓶中,40℃减压旋转蒸发至干,残渣溶于5.00ml中,经0.45μm滤膜过滤,用于分析。b)测定按上述色谱条件测定标准对照品和样品溶液。c)计算按下列公式(14)计算冰葡萄酒中各多酚成分含量:其中:w—冰葡萄酒中各多酚含量,μg/ml;c—由标准曲线查得的样品溶液浓度,μg/ml;v1—样品溶液体积,ml;v2—试样体积,ml。(五)分析检测结果表13冰葡萄酒各多酚含量测定结果(μg/ml)样品名称冰葡萄酒原酒橡木桶-1个月橡木桶-2个月橡木桶-3个月香豆酸11.3616.6714.2710.35咖啡酸4.134.252.963.21阿魏酸1.571.521.171.30对羟基苯甲酸2.363.702.141.87单宁酸192.38310.72270.36317.86儿茶素8.538.168.629.16香草酸21.2017.6717.3817.52榭皮素2.131.591.511.59表儿茶114.82117.22104.40112.46丁香酸16.2017.0513.8316.43以上所述,仅为本发明创造较佳的具体实施方式,但本发明创造的保护范围并不局限于此,任何熟悉本
技术领域:
的技术人员在本发明创造披露的技术范围内,根据本发明创造的技术方案及其发明构思加以等同替换或改变,都应涵盖在本发明创造的保护范围之内。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1