一种水中诺如病毒的检测方法与流程
本发明涉及水中病毒的检测方法,特别涉及一种水中诺如病毒的检测方法。
背景技术:
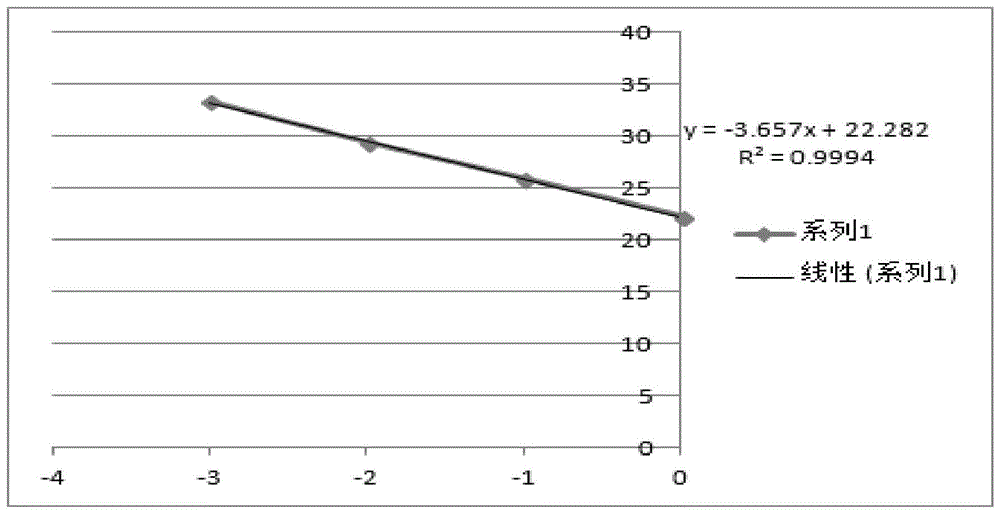
:诺如病毒属于人类杯状病毒科,诺如病毒属,诺如病毒基因组是单股正链rna,基因组全长约7kb~7.5kb。诺如病毒共可分为gⅰ~gⅴ5个基因型,其中感染人的主要是gⅰ型和gⅱ型。诺如病毒感染性腹泻在全世界范围内均有流行,全年均可发生感染,感染对象主要是成人和学龄儿童,寒冷季节呈现高发。美国每年在所有的非细菌性腹泻暴发中,60-90%是由诺如病毒引起。荷兰、英国、日本、澳大利亚等发达国家也都有类似结果。在中国5岁以下腹泻儿童中,诺如病毒检出率为15%左右,血清抗体水平调查表明中国人群中诺如病毒的感染亦十分普遍。目前,国内针对水中诺如病毒的检测报道较少,诺如病毒在水中虽然比较稳定但无法增值,导致难以检测,所以,开发一种准确、稳定的检测水样品中诺如病毒的方法尤为重要。技术实现要素:本发明提供了一种水中诺如病毒的检测方法,该方法可以对水中的诺如病毒进行准确、定量的检测。为解决上述技术问题,本发明提供了以下的技术方案:一种水中诺如病毒的检测方法,包括以下步骤:(1)水样处理与诺如病毒的富集;(2)诺如病毒rna的提取,得到纯化的病毒核酸溶液;(3)配置rt-pcr反应液;(4)荧光定量pcr仪检测;所述荧光定量pcr仪检测的程序为:50℃30min;95℃5min;95℃15s、60℃30s采集信号;65℃30s,循环45次;荧光通道检测选择fam、vic通道。进一步地,所述水样处理与诺如病毒的富集的步骤为:取水样,加入mgcl2溶液使其浓度达到0.03~0.05mol/l,调节水样使ph至3.0~5.0,使水样通过混合硝酸纤维素膜,用牛肉膏-甘氨酸洗脱液震荡洗脱滤膜;去除滤膜,调节洗脱液ph至6.0~8.0,向洗脱液中加入peg8000溶液放置过夜,离心保留沉淀;加入无rna酶的超纯水溶解沉淀,离心后上清液为病毒粗提取物。进一步地,所述诺如病毒rna的提取步骤为:取病毒粗提取物,加入裂解液,充分混匀,然后漂洗液漂洗数次,加入洗脱液,离心后得到纯化的病毒核酸溶液。进一步地,所述mgcl2溶液的浓度为2.5mol/l。进一步地,所述牛肉膏-甘氨酸洗脱液的配置方法为:将30.0g牛肉膏和3.75g甘氨酸搅拌溶解于超纯水中,调节ph至9.5,用超纯水定容至1000ml,分装,121℃高压灭菌15min。进一步地,所述水样处理与诺如病毒的富集的步骤中,洗脱液与peg8000溶液的体积比为1:0.25。进一步地,所述peg8000溶液的配置方法为:将peg8000400.0g和氯化钠87.0g搅拌溶解于超纯水中,用超纯水定容至1000ml,分装,121℃高压灭菌15min。进一步地,所述病毒粗提取物加入裂解液的体积为600μl。与现有技术相比,本发明的水中诺如病毒的检测方法的有益效果为:本发明的水中诺如病毒的检测方法,使用荧光定量pcr仪进行检测,灵敏性和准确度较高,并可定量分析。附图说明下面结合附图中的具体实施例对本发明的技术方案做进一步的详细说明,但不构成对本发明的任何限制。图1为本发明实施例中病毒提取过程控制的rna标准曲线图。具体实施方式实施例1水中诺如病毒的检测方法,包括以下步骤:(1)水样处理与诺如病毒的富集取水样,加入2.5mol/lmgcl2溶液使其浓度达到0.03~0.05mol/l,用1mol/l盐酸调节水样使ph至3.0~5.0,采用真空抽滤使之通过孔径为0.22μm的混合硝酸纤维素膜,然后用10ml牛肉膏-甘氨酸洗脱液震荡洗脱滤膜20~30min;去除滤膜,用1mol/l盐酸调节洗脱液ph至6.0~8.0,向洗脱液中加入0.25倍体积的peg8000溶液,上下颠倒离心管以充分混匀。将离心管及样液一起在4℃放置过夜。然后在4℃下,10000g离心5min,弃去上清,保留沉淀。然后加入200μl无rna酶的超纯水,60℃加热5min充分溶解沉淀。4℃,10000g离心3min,取上清,得到病毒粗提产物。另取一水样加入10μl过程控制病毒,摇匀,同法操作,作为过程控制1。(2)诺如病毒rna的提取:按照病毒核酸提取试剂盒(购自江苏硕世生物科技有限公司)说明:取200μl含有病毒的液体,加入600μl裂解液,充分混匀,室温放置5分钟,期间颠倒管子数次帮助裂解。加入600μl缓冲液到裂解好的样本溶液中,充分混匀。转移650μl混合液到套有接液管的亲和柱内,13000rpm离心30秒,弃掉过滤液,重复此操作直到滤完剩下的液体。加入500μl漂洗液到亲和柱内,13000rpm离心30秒,弃掉过滤液,重复此步骤一次。将亲和柱重新套入到rnase-free的离心管中,向亲和柱底部吸附膜的中心部位加入50μl洗脱液,室温放置2分钟,13000rpm离心2分钟收获纯化的病毒核酸溶液。(3)配置rt-pcr反应液按照诺如病毒(gi/gii)核酸检测试剂盒(rt-pcr探针法)说明操作配制诺如病毒gi/gii反应体系。按照ms2过程控制试剂盒(rt-pcr探针法)说明操作配制ms2反应体系。另取20μlms2过程控制,于95℃加热5min后在冰上冷却至室温,按照1:9的比例进行梯度稀释,用于制作过程控制标准曲线。其中,诺如病毒(gi/gii)核酸检测试剂盒购自江苏硕世生物科技有限公司,ms2过程控制试剂盒购自北京良润生物科技有限公司。按照表1的方法设置过程控制与外加扩增控制。根据反应体系、上机样品管数计算各试剂所需用量如表3和表4所示。表1往pcr管中分装反应液,每管20μl;在各管中加入相应的反应模板,反应液与模板混匀,立即进行pcr反应。(4)荧光定量pcr仪检测使用lightcycler96型荧光定量pcr仪进行检测。反应程序为:50℃30min;95℃5min;95℃15s、60℃30s采集信号;65℃30s,循环45次。荧光通道检测选择:fam、vic通道。试验例1.溶液的配置(1)peg8000溶液:将400.0gpeg8000、87.0g氯化钠,搅拌溶解于超纯水中,用超纯水定容至1000ml,分装,121℃高压灭菌15min,备用。(2)2.5mol/lmgcl2溶液:将238.0g氯化镁(mgcl2)搅拌溶解于超纯水中,用超纯水定容至1000ml,分装,121℃高压灭菌15min,备用。(3)牛肉膏-甘氨酸洗脱液(含3%牛肉膏,0.05mol/l甘氨酸,ph9.5)将30.0g牛肉膏和3.75g甘氨酸搅拌溶解于超纯水中,调节ph至9.5,用超纯水定容至1000ml,分装,121℃高压灭菌15min,备用。2.样品处理和病毒富集取水样两瓶,每瓶500ml,分别加入10ml的2.5mol/lmgcl2溶液,使其浓度达到0.03~0.05mol/l。然后用1mol/l盐酸调节水样使ph至3.0~5.0,其中一瓶加入10μl过程控制病毒,摇匀,作为过程控制1。采用真空抽滤使之通过孔径为0.22μm的混合硝酸纤维素膜,然后用10ml牛肉膏-甘氨酸洗脱液震荡洗脱滤膜20~30min;去除滤膜,用1mol/l盐酸调节洗脱液ph至6.0~8.0,向洗脱液中加入0.25倍体积的peg8000溶液,上下颠倒离心管以充分混匀。将离心管及样液一起在4℃放置过夜。然后在4℃下,10000g离心5min,弃去上清,保留沉淀。然后加入200μl无rna酶的超纯水溶解沉淀,60℃加热5min充分溶解沉淀。4℃,10000g离心3min,取上清液(v1),得到病毒粗提产物。3.rna的提取按照病毒核酸提取试剂盒说明取200μl(v2)含有病毒的液体,进行裂解。加入600μl核酸沉淀剂到裂解好的样本溶液中,充分混匀。转移650μl混合液到套有接液管的亲和柱内,13000rpm离心30秒,弃掉过滤液,重复此操作直到滤完剩下的液体。加入500μltris缓冲盐溶液到亲和柱内,13000rpm离心30秒,弃掉过滤液,重复此步骤一次。将亲和柱重新套入到rnase-free的离心管中,向亲和柱底部吸附膜的中心部位加入50μl(v3)去rna酶水,室温放置2分钟,在13000rpm的转速下离心2分钟得到纯化的病毒核酸溶液。4.配置rt-pcr反应液4.1将诺如病毒(gi/gii)核酸检测试剂盒(rt-pcr探针法)和ms2过程控制试剂盒(rt-pcr探针法)从-20℃冰箱取出,放在冰盒上解冻。解冻后振荡混匀数秒,3000转离心数秒。4.2取20μlms2过程控制,于95℃加热5min后在冰上冷却至室温。按照1:9的比例进行梯度稀释,做3个稀释梯度,一共4个浓度,用于制作过程控制标准曲线(过程控制2-5)按照表2的方法设置过程控制与外加扩增控制。表2根据反应体系、上机样品管数计算各试剂所需用量如表3和表4所示。表3诺如病毒gi/gii反应体系反应液名称加入量(μl)/每反应nov预混液(无ms2)17.5酶混合液2.5总体积20表4ms2反应体系反应液名称加入量(μl)/每反应ms2预混液17.5酶混合液2.5总体积20按照以上顺序依次加入试剂至干净的离心管中,涡旋振荡混匀后,放冰盒上待用,整个配置过程,需在冰盒上操作。取出干净的pcr八联管固定在pcr管盒上,将冰盒上的反应液短暂离心后,轻轻打开盖子,往pcr管中分装反应液,每管20μl,管中尽量避免气泡。在各管中加入相应的反应模板,加模板顺序为阴性对照→待检样品→扩增控制→过程控制→阳性对照,管中尽量避免气泡存在,盖好管盖。轻轻敲打pcr管盒,使反应液与模板混匀,并以3000rpm的转速离心数秒,立即进行pcr反应。5.荧光定量pcr检测使用lightcycler96型荧光定量pcr仪进行检测。反应程序为:50℃30min;95℃5min;95℃15s、60℃30s采集信号;65℃30s,循环45次。荧光通道检测选择:fam、vic通道。6.实验数据各个过程的pcr检测数据如表5所示。表5pcr检测数据6.1标准曲线以病毒提取过程控制2-5的rna浓度lg值为x轴,以其ct值为y轴建立标准曲线,标注曲线如图1所示。得到的标准曲线为y=-3.657x+22.282,r2=0.9994,大于等于0.98。未稀释过程控制病毒rna浓度为1,梯度稀释过程控制rna浓度分别为10-1、10-2、10-3。6.2提取效率将病毒提取过程控制1的ct值代入标准曲线,计算经过病毒提取等步骤后的过程控制病毒rna浓度。提取效率计算公式:提取效率计算所得:过程控制1,e=12%,满足过程控制要求。6.3.抑制指数通过外加扩增控制rna,计算扩增抑制指数,作为扩增控制。抑制指数=(扩增控制1)ct值-(扩增控制3)ct值。如抑制指数≥2.00,需比较10倍稀释食品样品的抑制指数,即抑制指数=(扩增控制2)ct值-(扩增控制3)ct值。计算所得:抑制指数=25.04-25.22=-0.18,满足扩增控制要求。其中,需满满足以下质量控制要求,检测方有效。空白对照阴性,阴性对照阴性,阳性对照阳性。过程控制需满足:提取效率≥1%,如提取效率<1%,需重新检测,但如提取效率<1%,检测结果为阳性,也可酌情判定为阳性。扩增控制需满足:抑制指数<2.00;如抑制指数≥2.00,需比较10倍稀释食品样品的抑制指数;如10倍稀释食品样品扩增的抑制指数<2.00,则扩增有效,且需采用10倍稀释食品样品rna的ct值作为结果;10倍稀释食品样品扩增的抑制指数也≥2.00时,扩增可能无效,需要重新检测;但如抑制指数≥2.00,检测结果为阳性,也可酌情判定为阳性。检测样品:待测样品的ct值大于等于45时,判定为诺如病毒阴性;待测样品的ct值小于等于38时,判定为诺如病毒阳性;待测样品的ct值大于38,小于45时,应重新检测;重新检测结果大于等于45时,判定为诺如病毒阴性;小于等于38时,判定为诺如病毒阳性。本发明使用荧光定量pcr仪进行检测,灵敏性和准确度较高,实验数据处理简单,大大节省了检测效率。以上所述为本发明的优选实施方式,并不限制于本发明。对本领域技术人员来说,在不脱离本发明原理的前提下做出的若干改进和变型,也应视为本发明的保护范围。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1