Glu-Leu-Phe-Tyr-Val五肽,其合成,活性和应用的制作方法
本发明涉及glu-leu-phe-tyr-val五肽,涉及它的制备方法,涉及它的抗炎活性,涉及它的抗肿瘤活性,涉及它的抗血栓活性及涉及它的溶血栓活性,因而本发明涉及它在制备抗炎药,抗肿瘤药物,抗血栓药物,溶血栓药物中的应用。本发明属于生物医药领域。
背景技术:
发明抗肿瘤,抗血栓,溶血栓和抗凝血作用寡肽是发明人长期关注的领域。虽然发明人发明公开过一系列具有这些活性的寡肽,但是集这些活性为一体的寡肽一直没有得到。发明人发现,glu-leu-phe-tyr-val五肽是集抗炎作用,抗肿瘤作用,抗血栓作用和溶血栓作用为一体的肽。根据这些发现发明人提出本发明。.
技术实现要素:
本发明的第一个内容是提供序列为glu-leu-phe-tyr-val的五肽。
本发明的第二个内容是提供glu-leu-phe-tyr-val五肽的合成方法,该方法包括:
(1)在dcc和hobt的催化下按照标准方法制备boc-tyr-val-obzl;
(2)boc-tyr-val-obzl在浓度为4n的氯化氢-乙酸乙酯溶液中,0℃脱boc,转化成tyr-val-obzl;
(3)在dcc和hobt的催化下制备boc-leu-phe-obzl;
(4)boc-leu-phe-obzl在h2,pd/c催化下,转化成boc-leu-phe;
(5)在dcc和hobt的催化下制备boc-leu-phe-tyr-val-obzl;
(6)boc-leu-phe-tyr-val-obzl在浓度为4n的氯化氢-乙酸乙酯溶液中,0℃脱boc,转化成leu-phe-tyr-val-obzl;
(7)在dcc和hobt的催化下制备boc-glu(obzl)-leu-phe-tyr-val-obzl;
(8)boc-glu(obzl)-leu-phe-tyr-val-obzl在pd/c催化下氢解boc-glu-leu-phe-tyr-val;
(9)boc-glu-leu-phe-tyr-val在浓度为4n氯化氢-乙酸乙酯溶液中,0℃脱boc转化成glu-leu-phe-tyr-val。
本发明的第三个内容是评价glu-leu-phe-tyr-val五肽的抗炎作用。
本发明的第四个内容是评价glu-leu-phe-tyr-val五肽的抗肿瘤作用。
本发明的第五个内容是评价glu-leu-phe-tyr-val五肽的抗血栓作用。
本发明的第六个内容是评价glu-leu-phe-tyr-val五肽的溶血栓作用。
附图说明
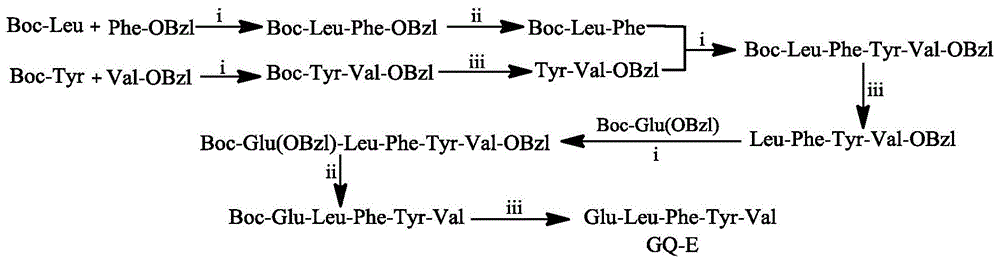
图1glu-leu-phe-tyr-val的合成路线.i)二环己基碳二亚胺(dcc),1-羟基苯并三唑(hobt),n-甲基吗啉(nmm),四氢呋喃(thf);ii)h2,pd/ciii)4nhcl/ea,0℃。
具体实施方式
为了进一步阐述本发明,下面给出一系列实施例。这些实施例完全是例证性的,它们仅用来对本发明进行具体描述,不应当理解为对本发明的限制。
实施例1制备boc-tyr-val-obzl
冰浴下,2.81g(10mmol)boc-tyr溶解于少量无水四氢呋喃(thf)中,加入1.36g(10mmol)hobt,加入2.47g(12mmol)dcc与少量无水thf的溶液,活化30分钟,加入2.07g(10mmol)val-obzl,用nmm调节ph=9,反应结束后过滤除去二环己基脲(dcu)。滤液减压浓缩,残留物用乙酸乙酯溶解,再次过滤dcu,滤液用nahco3饱和溶液洗3遍,用nacl饱和溶液洗3遍,5%的khso4溶液洗3遍,nacl饱和溶液洗3遍,5%的nahco3溶液萃洗3遍,nacl饱和溶液萃洗3遍,乙酸乙酯层用无水na2so4干燥12小时,滤除na2so4,滤液减压浓缩,得到4.02g(85.5%)标题化合物,为无色粉末。esi+-ms(m/e):472[m+h]+。
实施例2制备tyr-val-obzl
冰浴下将4.7g(10mmol)boc-tyr-val-obzl用尽少量干燥过的乙酸乙酯溶解,搅拌10min,加入50ml氯化氢-乙酸乙酯溶液(4n)反应4h,原料点消失。反应混合物减压浓缩至干,残留物加40ml干燥过的乙酸乙酯溶解,得到的溶液减压浓缩至干。残留物按该操作重复3次。残留物加无水乙醚,用塑料铲研磨,减压浓缩除去乙醚。残留物按该操作重复3次。得到3.97g(99%)标题化合物,为无色粉末。esi+-ms(m/e):372[m+h]+。
实施例3制备boc-leu-phe-obzl
按照实施例1的方法,2.31g(10mmol)boc-leu和2.55g(10mmol)phe-obzl得到3.98g(81.6%)标题化合物,为无色油状物。esi+-ms(m/e):470[m+h]+。
实施例4制备boc-leu-phe
将4.88g(10mmol)boc-leu-phe-obzl用甲醇溶解,加入488mg的10%的pd/c。连接三通,减压抽除茄瓶中的空气后,反应瓶中充满h2,按该操作重复3次。反应20h后原料点消失。滤除pd/c,旋干甲醇。得到3.67g(97%)标题化合物,为无色粉末。esi+-ms(m/e):380[m+h]+。
实施例5制备boc-leu-phe-tyr-val-obzl
按照实施例1的方法,3.78g(10mmol)boc-leu-phe和3.7g(10mmol)tyr-val-obzl得到4.23g(57.9%)标题化合物,为无色粉末。esi+-ms(m/e):732[m+h]+。
实施例6制备leu-phe-tyr-val-obzl
按照实施例2的方法,从7.3g(10mmol)boc-leu-phe-tyr-val-obzl得到6.1g(98%)标题化合物,为无色粉末。esi+-ms(m/e):632[m+h]+。
实施例7制备boc-glu(obzl)-leu-phe-tyr-val-obzl
按照实施例1的方法,3.37g(10mmol)boc-glu(obzl)和6.3g(10mmol)leu-phe-tyr-val-obzl得到3.35g(35.3%)标题化合物,为无色粉末。esi+-ms(m/e):951[m+h]+;1h-nmr(300mhz,dmso-d6):δ/ppm=9.14(s,1h),8.23(d,1h),7.95(m,2h),7.71(d,1h),7.34(m,10h),7.16(m,5h),7.12(m,3h),6.63(d,2h),5.13(s,2h),5.08(s,2h),4.60(m,1h),4.40(m,1h),4.25(m,2h),3.92(m,1h),2.90(m,2h),2.51(m,2h),2.33(m,2h),2.10(m,1h),1.80(m,2h),1.54(m,1h),1.30(s,11h),0.81(s,12h)。
实施例8制备boc-glu-leu-phe-tyr-val
按照实施例4的方法,从950mg(1mmol)的boc-glu-leu-phe-tyr-val-obzl得到750mg(95.2%)标题化合物,为无色粉末。esi+-ms(m/e):771[m+h]+。
实施例9制备glu-leu-phe-tyr-val(gq-e)
按照实施例2的方法,从769mg(1mmol)boc-glu-leu-phe-tyr-val-obzl得到650mg(95.1%)标题化合物,为无色粉末。esi+-ms(m/e):671[m+h]+;mp166.2~167.8℃.
实施例10评价glu-leu-phe-tyr-val的抗炎活性
体重20±雄性小鼠口服1μmol/kgglu-leu-phe-tyr-val(gq-e)或1200μmol/kg阿司匹林或0.2ml/20g生理盐水30分钟后,往小白鼠的左耳外廓涂二甲苯(0.04ml),2小时后将小白鼠颈椎脱臼处死。将小鼠的左,右耳剪下,用直径7mm的打孔器在两耳的相同位置,取圆形耳片,分别称重,求出两圆耳片的重量差作为肿胀度。(肿胀度=左耳原片重量-右耳原片重量)以肿胀度表示化合物的活性。本实验数据统计均采用t检验和方差分析,肿胀度以(x±sdmg)表示。结果表明,glu-leu-phe-tyr-va治疗小鼠的耳肿胀度与生理盐水治疗小鼠的耳肿胀度相比具有显著性差异。表明化合物具有确切的抗炎活性。
表1glu-leu-phe-tyr-val(gq-e)的抗炎活性
a)与生理盐水比p<0.05;n=14.
实施例11评价glu-leu-phe-tyr-val的抗肿瘤活性
无菌条件下取接种于icr小鼠7-10天的s180肉瘤,加入适量生理盐水配制成瘤细胞悬液,细胞数为2×107/ml,接种于健康雄性icr小鼠前肢腋皮下,每只小鼠注射0.2ml。肿瘤接种24h后,小鼠每日腹腔注射0.2mlglu-leu-phe-tyr-val(gq-e)的生理盐水溶液,连续给药10天,剂量为1μmol/kg/天;或小鼠每日腹腔注射0.2ml阿霉素的生理盐水溶液,连续给药10天,剂量为2μmol/kg/天;或小鼠每日腹腔注射0.2ml生理盐水,连续给药10天。实验进行至第11天,称小鼠体重,乙醚麻醉剖取各组小鼠的肿瘤,称重并以瘤重表示化合物的活性,数据列入表2。结果表明1μmol/kg/天glu-leu-phe-tyr-val治疗小鼠的瘤重明显小于生理盐水治疗小鼠的瘤重,而与剂量为2μmol/kg/天的阿霉素治疗小鼠的瘤重无显著性差异。glu-leu-phe-tyr-val显示确切的抗肿瘤活性。
表2glu-leu-phe-tyr-val(gq-e)对s180荷瘤小鼠瘤重的影响
a)与生理盐水比p<0.01,与阿霉素比p>0.05;n=15.
实施例12评价glu-leu-phe-tyr-val的抗血栓活性
1)将聚乙烯管拉成一端为斜口的细管,定长为10.0cm,分别为右经静脉(管径较粗)及左颈动脉(管径较细)插管;中段聚乙烯管定长为8.0cm,血栓线压在颈动脉插管方向,插管前需在管中充满肝素。
2)体重250±雄性大鼠口服1μmol/kgglu-leu-phe-tyr-val(gq-e)或167μmol/kg阿司匹林或0.3ml/100g生理盐水30分钟后,腹腔注射20%的乌拉坦进行麻醉。仰卧位将大鼠固定于鼠板上,剪开颈部皮肤,分离右颈总动脉及左颈静脉,血管下压线,结扎远心端,静脉靠远心端处剪一小口,进行静脉端插管,注射肝素,系线固定,再用动脉夹夹住动脉近心端,靠近远心端方向剪一小口,进行动脉端结扎,系线固定后松开动脉夹,建立体外循环旁路。循环15分钟后先剪断静脉端观察血液循环是否正常,若正常从动脉端取出血栓线,在纸上沾干浮血后称重,以栓重表示化合物的活性,数据列入表3。结果表明,glu-leu-phe-tyr-val(gq-e)治疗大鼠的血栓重明显小于生理盐水治疗大鼠的血栓重,显示确切的抗血栓活性。
表4glu-leu-phe-tyr-val(gq-e)对大鼠栓重的影响
a)与生理盐水比p<0.01;n=12.
实施例13评价glu-leu-phe-tyr-val的溶栓活性
将大鼠静息饲养一天,随机分组,每组10只,禁食不禁水。
1)将体重250±雄性sd大鼠用20%乌拉坦溶液进行麻醉(6ml/kg腹腔)。麻醉后的大鼠固定于鼠板上,分离右侧颈总动脉,于近心端夹动脉夹,近心端和远心端分别传入手术线,在远心端插取血管,松开动脉夹取约1ml动脉血。迅速将动脉血注射入垂直的造栓管(长16mm,内径2.5mm,外径5mm,管底用1mlep管底座)中,(注意不可有气泡)每个造栓管中注入0.1ml大鼠动脉血液,往管内迅速插入血栓固定螺栓(长20mm,),血液凝固40min,用针灸针取出血栓,称取血栓重量。
2)旁路插管由三部分组成,其中中段为聚乙烯胶管,长60mm,内径3.5mm,两端为相同的聚乙烯管,长100mm,内径1mm,外景2mm,该管的一段拉成尖管,另一端的外部套一段长7mm,外径3.5mm的聚乙烯管。三段管的内壁均为硅烷化。
3)将血栓包裹的血栓固定螺栓置于中段的聚乙烯胶管内,胶管的两端分别与两根聚乙烯的加粗端相套,用注射器通过尖管端注满肝素生理盐水溶液。将充满肝素钠的生理盐水溶液一端插入左侧静脉,另一端用注射器加入准确量的肝素钠抗凝后,拔掉肝素钠的注射器,插入动脉端。用头皮针将生理盐水(3ml/kg)或者尿激酶的生理盐水溶液(20000iu/kg)或glu-leu-phe-tyr-val(gq-e)的生理盐水溶液(1μmol/kg)通过旁路管的中段,刺入远离血栓固定螺栓的近静脉处,打开动脉夹,使血流通过旁路管道从动脉流入静脉的时刻为循环起始时间,缓慢的将注射器中的液体注入到血液中(约6min),使生理盐水,尿激酶,arg-leu-val-cys-val通过血液循环,按静脉-心脏-动脉的顺序作用到血栓上。60min后取出附有血栓的螺栓,蘸去浮血,记录重量。以血栓减重代表溶栓活性。数据列入表4。结果表明,glu-leu-phe-tyr-val(gq-e)治疗大鼠的血栓减重明显大于生理盐水治疗大鼠的血栓减重,显示确切的溶血栓活性。
表4glu-leu-phe-tyr-val(gq-e)的溶栓活性
a)与生理盐水比p<0.01;n=10。
- 还没有人留言评论。精彩留言会获得点赞!