一种以TS为荧光团的小分子荧光探针及其制备方法与应用与流程
本发明涉及荧光成像分子探针领域,尤其是涉及一种利用荧光成像技术检测铜离子的探针,具体涉及一种分子探针、其制备方法及应用。
背景技术:
在生命体中,铜离子是仅次于铁离子和锌离子之后的第三大必须微量元素,一定含量的铜离子在植物和动物的基本生理活动过程中起着至关重要的作用。然而,过量的铜离子能产生活性氧类,打乱细胞新陈代谢的平衡,成为生物体系中的有毒物质。例如,摄取过量的铜离子可能导致肠胃、肾脏和肝脏的严重损害;一些难以治疗的疾病,包括阿尔茨海默病、肌萎缩性脊髓侧索硬化症、门克斯综合征、威尔逊疾病也和过量的铜离子存在着某些关联。更多的是,在当今社会,随着矿物的开采和工业污染的日渐严重,铜离子成为一种污染环境的主要的重金属离子,由其在饮用水方面,其毒性仅次于汞离子。因此,为了保护环境和人类健康,精确有效的检测环境中的微量铜离子是相当有意义的。
检测铜离子的分析方法有很多,包括原子吸收光谱法、电感耦合等离子质谱法、电感耦合等离子体原子发射光谱法和荧光光谱法等。在这些方法中,荧光光谱法具有高的灵敏度高选择性,响应迅速,比其他分析方法更经济简便的特点,因此,用于检测铜离子的荧光探针得到广泛的研究。然而,大多数早期报道的经典的铜离子荧光探针存在一些缺陷。例如,只能在纯的或含少量水的有机溶剂中进行检测,需要特别的反应条件,对铜离子的响应灵敏度不高。更多的是,相对其他的金属离子,一些探针对铜离子的选择性不理想。因此,发展新的高灵敏度高选择性的铜离子荧光探针仍然具有重要的研究意义。
近年来,报道了许多具有良好性能的基于不同检测机理的铜离子荧光探针。主要包括以下几种:基于分子内电荷转移(ict)过程的铜离子荧光探针;基于光诱导的电子转移(pet)过程的铜离子荧光探针;基于荧光共振能量转移(fret)过程的铜离子荧光探针以及基于激发态分子内质子转移(esipt)过程的铜离子荧光探针等。基于ict过程的荧光探针,其结构特点是荧光基团与识别基团共轭连接。这种类型的荧光探针是一种在荧光基团上连着强拉电子基和供电子基的电子推-拉体系。当探针分子被光激发后,分子内电荷从电子供体转移到电子受体的过程会增加。但是当与客体发生识别过程后,探针分子内的电荷转移会受到影响,从而其紫外和荧光光谱发生变化。基于这种机理的荧光分子探针可以实现对检测物的比率检测,避免检测误差。
技术实现要素:
针对现有技术存在的不足,本发明的目的在于提供一种高选择性和高灵敏度的铜离子识别荧光探针。
为实现上述目的,本发明提供一种以ts为荧光团的小分子荧光探针,所述分子探针分子式为c26h21n3o2,其结构式为:
本发明还提供上述以ts为荧光团的小分子荧光探针的制备方法,具体包括如下步骤:
将4-二苯胺基苯甲醛溶解在乙醇溶液中,并在室温下加入水杨酸酰肼搅拌,室温搅拌反应4-24h,反应得到绿色固体并用乙醇洗涤干燥得到目标产物。
作为本发明的进一步改进,原料的摩尔比为:
1~2份4-二苯胺基苯甲醛;
1~2份水杨酸酰肼。
本发明还提供上述以ts为荧光团的小分子荧光探针在检测、识别环境中或生物样品中铜离子的应用。
作为本发明的一种应用方式,通过紫外分光光度法,在200nm~650nm的波长范围内测定铜离子溶液的吸光度;在最大吸收波长372nm下识别环境中或生物样品中铜离子。
作为本发明的一种应用方式,通过荧光分光光度法,以370nm为激发波长,在380nm到650nm的波长范围内测定铜离子溶液的荧光强度;在最大发射波长476nm下识别环境中或生物样品中的铜离子。
作为本发明的一种应用范围,所述小分子荧光探针利用荧光成像检测正常细胞和癌细胞中外源性的铜离子的应用。
作为本发明的一种应用范围,所述以ts为荧光团的小分子荧光探针在制备细胞体外铜离子检测试剂盒中的应用。
本发明另一方面在于提供小分子荧光探针检测离子的方法,其具体步骤如下:
步骤一、制备小分子荧光探针母液:将纯化后的以ts为荧光团的小分子荧光探针溶解在1ml二甲亚砜中,得到探针母液;
步骤二、将母液稀释稀释得到探针工作液,滴加待测检测液,通过紫外光谱设备在特定紫外光波长下检测吸光度,或者通过荧光光谱设备在特定荧光波长下检测荧光强度;
其中紫外光谱法:将母液稀释得到10μm的探针工作液,其稀释液为去离子水,在200nm~650nm的波长范围内测定铜离子溶液的吸光度;在最大吸收波长372nm下识别环境中或生物样品中铜离子,待检测液的最大浓度限值为:1mm,紫外比色皿为1ml;
其中荧光光谱法:稀释探针母液得到5μm的探针工作液,其稀释液为去离子水,在476nm处测定荧光值。
本发明具有如下优点:本发明的两种小分子荧光探针分别以三苯胺(ts)为荧光团和水杨酰肼为基础,具有很强共轭π电子,其中水杨酰肼和醛基缩合作为金属离子的螯合位点,小分子荧光探针结合铜离子后能荧光发生淬灭,小分子荧光探针在铜离子的存在下阻碍了探针分子内的电子转移,使得其荧光从有到无,紫外吸收峰红移移,在波长为398nm出现新的吸收,且随着铜离子浓度增加,吸收峰也逐渐增加并转移,说明金属离子与探针发生了很强的结合,实现荧光技术精确检测铜离子,并且可以检测活细胞内外源性的铜离子。因此在铜离子检测方面具有良好的应用前景。同时,本发明的合成方法简单、操作方便,不需要苛刻的条件。
附图说明
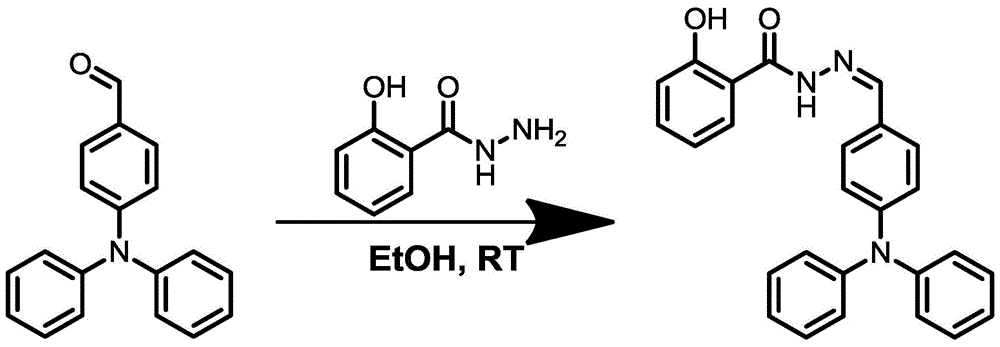
图1为实施例1中小分子荧光探针合成的路线模式图;
图2为实施例1中小分子荧光探针产物的核磁氢谱图;
图3为实施例1中小分子荧光探针产物的核磁碳谱图;
图4为实施例1中合成小分子探针产物的质谱图
图5a、b分别为实施例2中小分子荧光探针对铜离子识别的紫外光谱和荧光光谱;
图6为实施例3中小分子荧光探针对铜离子的选择性和竞争性,其中6(a)为不同金属离子与荧光探针结合后的荧光强度,其中6(b)为铜离子与荧光探针结合后再加入其他金属离子后荧光强度的变化值,其中6(c)为荧光探针对铜离子响应的时间分析,其中图6(d)为不同ph值条件下的铜离子与荧光探针结合后的荧光强度变化;
图7为实施例4中小分子荧光探针对铜离子识别的密度泛函理论计算;
图8为实施例5中小分子荧光探针在hepg2细胞中检测外源性的铜离子;
图9为实施例6中小分子荧光探针在a549细胞中检测外源性的铜离子;
图10为实施例7中小分子荧光探针在hela细胞中检测外源性的铜离子。
具体实施方式
下面将结合实施例和效果例对本发明做进一步的详述,而非限制本发明的范围。
实施例1合成小分子荧光探针
合成以ts为荧光团的小分子荧光探针:将4-二苯胺基苯甲醛(500mg,1.83mmol)溶解在30ml乙醇溶液中,并在室温下加入水杨酸酰肼(278mg,1.83mmol)搅拌,室温搅拌反应20h,反应得到绿色固体并用乙醇洗涤干燥。小分子荧光探针用无水乙醇重结晶便可得到纯度更高的样品,最终样品的产率为:80%,合成小分子荧光探针的路线图如图1所示,图1表示合成小分子荧光探针的路线图,其中etoh为乙醇,rt为室温。
通过质谱、核磁以及光谱学方法可以确定该产物即为目标小分子荧光探针,其质谱和核磁氢谱图谱如图2-4所示,
探针质谱:
hrms(esi)m/z[m+1]+:calcdforc26h22n3o2,408.1707,found,408.1704;
探针核磁氢谱:
1hnmr(600mhz,dmso)δ11.93(s,1h),11.73(s,1h),8.35(s,1h),7.87(d,j=7.5hz,1h),7.59(d,j=8.5hz,2h),7.41(t,j=7.4hz,1h),7.33(t,j=7.7hz,4h),7.11(t,j=7.4hz,2h),7.07(d,j=7.8hz,4h),6.98–6.89(m,4h);
探针核磁碳谱:
13cnmr(151mhz,dmso)δ164.15,158.71,148.72,148.08,146.01,133.29,129.30,128.08,127.89,126.64,124.61,123.64,120.71,118.41,116.82,115.25。
实施例2小分子荧光探针对铜离子响应的紫外和荧光光谱
制备1.0ml小分子荧光探针(1.0×10-5mol/l)的dmso/h2o(v/v=1:1)溶液。0.5倍当量浓度的铜离子溶液滴加到探针溶液中,如图5(a)所示,在ts探针溶液中加入铜离子后,在298nm和372nm处的吸收带逐渐减少,400nm~500nm处有一个新的吸收峰,并在398nm处出现最大吸收峰,其吸光强度随离子浓度逐渐增加,最终两者化学计量比为2:1。
在荧光滴定实验中,制备3.0ml小分子探针(5.0×10-6mol/l)的dmso/h2o(v/v=1:1)溶液。0.5倍当量浓度的铜离子溶液滴加到探针溶液中,对于ts探针以370nm为激发波长测量探针从380nm到650nm的荧光值,实验结果见图5(b)。可观察到探针的荧光强度随铜离子浓度增加而减弱,最大发射波长都在476nm左右,当两者浓度比例为2:1时,荧光强度完全淬灭。
实施例3验证小分子荧光探针对铜离子选择性和竞争性。
制备5.0ml分子探针(5.0×10-6mol/l)的dmso/h2o(v/v=1:1)溶液。通过将相应的盐溶于去离子水制备各种阳离子溶液[fe(iii),al(iii),cr(iii),zn(ii),ni(ii),co(ii),mg(ii),ca(ii),cd(ii),mn(ii),ag(i),k(i)和na(i)](1.0×10-3mol/l)。随后,将同等当量的金属离子溶液加入到探针溶液中。通过荧光光谱进行检测,实验结果见图6(a)。取荧光最大吸收波长进行对比,如图6(b)所示,离子包括fe(iii),al(iii),cr(iii),zn(ii),ni(ii),co(ii),mg(ii),ca(ii),cd(ii),mn(ii),ag(i),k(i)和na(i)。除cu(ii)外,这些金属离子对探针的荧光都没有产生明显变化。在加入cu(ii)后,ts荧光探针在476nm处的荧光强度完全淬灭,而且在探针结合铜离子后,再加入其它金属离子,其它金属离子对体系的荧光强度也不产生干扰,可以判定探针和铜离子具有很强的结合能力。同时,检测了探针对铜离子响应的时间动力学研究和不同ph值条件下的荧光强度变化,实验结果见图6(c、d)可以看出荧光探针对铜离子有很快的响应,且ts结合铜离子荧光淬灭的时间是100s。在ph为2-10之间,探针以及探针与铜离子的复合物荧光都能够保持好现有的荧光强度。
实施例4小分子荧光探针识别铜离子的密度泛函理论计算
在探针单独存在下和结合铜离子后荧光从有到无的一个变化过程,其中具体产生变化的原因通过计算结合前后分子荧光探针的能级跃迁,计算两者跃迁时所需的能量是否有差别,从本质上来解释这种情况。实验结果见图7。
如图7所示,在ts探针单独存在下,分子探针的最高占据轨道(homo)的能量为-0.19,最低空轨道(lumo)的能量为-0.05,而两者的能量差为:0.14,而在结合铜离子后的homo值为-0.16,以及luno值为-0.07,其中两个轨道的能级差为:0.09,而且数据分析再结合离子后两者跃迁的能级差变小,使得跃迁变得更加容易。
实施例5小分子荧光探针的在人的肝癌细胞(hepg2)中成像效果
在hepg2细胞成像体系中,设立对照组(单独5μm探针处理细胞)和实验组(探针处理后再加入2.5μm铜离子处理),最后通过荧光成像系统中的蓝色通道进行拍照记录。实验结果见图8。如图8所示,在有铜离子和没有铜离子存在情况下,探针单独处理的hepg2细胞中发现荧光出现非常明显,而且ts探针在蓝色通道呈现出很强的荧光,而随着铜离子加入,探针在细胞中的荧光消失不见,说明探针可以检测hepg2细胞体内外源性的铜离子。
实施例6小分子荧光探针的在人的肺癌细胞(a549)中成像效果
在a549细胞成像体系中,设立对照组(单独5μm探针处理细胞)和实验组(探针处理后再加入2.5μm铜离子处理),最后通过荧光成像系统中的蓝色道进行拍照记录。实验结果见图9。如图9所示,在有铜离子和没有铜离子存在情况下,探针单独处理的a549细胞中发现荧光出现非常明显,而且ts探针在蓝色通道呈现出很强的荧光,而随着铜离子加入,探针在细胞中的荧光消失不见,说明探针可以检测a549细胞体内外源性的铜离子。
实施例7小分子荧光探针的在海拉细胞(hela)中成像效果
在hela细胞成像体系中,设立对照组(单独5μm探针处理细胞)和实验组(探针处理后再加入2.5μm铜离子处理),最后通过荧光成像系统中的蓝色通道进行拍照记录。实验结果见图10。如图10所示,在有铜离子和没有铜离子存在情况下,探针单独处理的hela细胞中发现荧光出现非常明显,而且ts探针在蓝色通道呈现出很强的荧光,而随着铜离子加入,两种探针在细胞中的荧光都消失不见了,说明探针可以检测hela细胞体内外源性的铜离子。
本发明所述的小分子荧光探针可通过荧光光谱技术检测溶液中的铜离子。
该小分子荧光探针在铜离子存在下,紫外吸收峰发生红移约26nm,同时荧光迅速从有到无,产生非常明显的荧光淬灭。
本发明具有如下优点:通过本发明所述制备方法合成小分子荧光探针,还可以实现紫外和荧光光谱法精确传感铜离子,并且可以快速、准确的检测多种癌细胞中的铜离子。因此在铜离子检测方面具有良好的应用前景。同时,本发明的合成方法简单、操作方便,不需要苛刻的条件。
以上仅是本发明的优选实施方式,本发明的保护范围并不仅局限于上述实施例,凡属于本发明思路下的技术方案均属于本发明的保护范围。应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理前提下的若干改进和润饰,这些改进和润饰也应视为本发明的保护范围。
- 还没有人留言评论。精彩留言会获得点赞!