一种产蔗糖磷酸化酶的大肠杆菌的制作方法
本发明涉及一种产蔗糖磷酸化酶的大肠杆菌,属于微生物技术领域。
背景技术:
蔗糖磷酸化酶(ec2.4.1.7,sucrosephosphorylase,以下简称spase)主要能够催化两种类型反应:一种是以磷酸化的葡萄糖当作供体转移到不同的物质,如以d-果糖为受体合成蔗糖;另外的一种催化方式是把蔗糖磷酸化酶分解蔗糖得到的葡萄糖基转移至不同类型的受体,如无机磷酸,含酚羟基、醇羟基及羧基的物质,催化合成多种糖苷。
蔗糖磷酸化酶主要分布在细菌中。根据文献报道该酶主要存在于肠膜明串珠菌leuconostocmesenteroides、变异链球菌stococcusmutans、嗜糖假单胞菌pseudomonassaccharophila、长双歧杆菌bifidobacteriumlongum、青春双歧杆菌bifidobacteriumadolescentis等微生物中。leuconostocmescnteroides可以合成蔗糖磷酸化酶[goedlc.,schwarza.,minaina.,etal.recombinantsucrosephosphorylasefromleuconostocmesenteroides:characterization,kineticstudiesoftransglucosylation,andapplicationofimmobilisedenzymeforproductionofd-glucose1-phosphate[j].journalofbiotechnol,2007,129(1):77-86.]。
目前,蔗糖磷酸化酶主要分布在细菌微生物中,植物细胞中有少量分布,该酶主要通过生物发酵获得,野生型菌株中的复杂代谢调控机制使得蔗糖磷酸化酶的产量较低,仅通过野生型菌株发酵生产蔗糖磷酸化酶,难以满足工业应用的要求。目前,在大肠杆菌、枯草芽孢杆菌中异源表达蔗糖磷酸化酶均有文献报道,但存在表达量不高,酶活力不高等问题。
因此,提供一种产蔗糖磷酸化酶的大肠杆菌,对于蔗糖磷酸化酶的工业生产具有重要的应用价值。
技术实现要素:
本发明的第一个目的是提供一株大肠杆菌(escherichiacoli),分类命名为escherichiacolispl0224,已于2019年5月24日保藏于中国典型培养物保藏中心,保藏编号为cctccno:m2019389,保藏地址为中国武汉,武汉大学。
本发明的第二个目的是提供含有上述大肠杆菌spl0224的微生物制剂。
在本发明的一种实施方式中,所述微生物制剂中含有活菌数不低于106cfu/g或106cfu/ml的大肠杆菌spl0224细胞。
在本发明的一种实施方式中,所述大肠杆菌细胞包括大肠杆菌spl0224干菌体或湿菌体。
本发明的第三个目的是提供一种生产蔗糖磷酸化酶的方法,是利用上述大肠杆菌spl0224进行发酵。
在本发明的一种实施方式中,以tb培养基为发酵培养基。
在本发明的一种实施方式中,将大肠杆菌spl0224单菌落接种于lb液体培养基中,于35-39℃,200-220r/min培养8-12h后,按1-5%接种量接入到tb液体培养基中,于35-39℃,200-220r/min培养至菌密度od600达到0.5-0.7后,加入iptg诱导剂于23-27℃,200-220r/min诱导20-30h后收集菌液,离心收集菌体,重悬后破碎菌体,离心收集上清,即为蔗糖磷酸化酶粗酶液。
在本发明的一种实施方式中,将大肠杆菌spl0224单菌落接种于含kana的lb液体培养基中,于37℃,200r/min过夜培养后,按1%接种量接入到含kana的tb液体培养基中,于37℃,200r/min培养至菌密度od600达到0.6后,加入iptg诱导剂于25℃,200r/min诱导24h后收集菌液。将菌液于4℃,7000r/min的低温冷冻离心机中离心15min,收集菌体。菌体用50mmol/lk2hpo4/kh2po4缓冲液(ph6.5)洗两次后收集菌体。将收集好的湿菌体加入50mmol/lk2hpo4/kh2po4缓冲液(ph6.5)缓冲液制成菌悬液,放在冰上并固定好,然后用超声波破碎菌体。超声波破碎仪工作时间:2s,间歇时间:4s,总时间:30min。将破碎后的液体于4℃,7000r/min的低温冷冻离心机下离心30min收集上清即为蔗糖磷酸化酶粗酶液。
本发明的第四个目的是提供上述大肠杆菌spl0224在生产α-熊果苷或含α-熊果苷的产品中的应用,是以蔗糖和氢醌为底物,以大肠杆菌spl0224为生物催化剂。
本发明的第五个目的是提供上述大肠杆菌spl0224在生产1-磷酸葡萄糖或含1-磷酸葡萄糖的产品中的应用。
本发明的第六个目的是提供上述大肠杆菌spl0224在生产d-果糖或含d-果糖的产品中的应用。
本发明的第七个目的是提供上述大肠杆菌spl0224在食品、化妆品或制药领域中的应用。
本发明的有益效果
本发明将seqidno.1所示的核苷酸序列,以pet-28a为载体构建重组质粒pet-28a-spase,转化到大肠杆菌bl21(de3)中,构建得到重组大肠杆菌,发酵产重组蔗糖磷酸化酶,并通过紫外诱变法对构建好的重组菌进行诱变,筛选出高产蔗糖磷酸化酶的大肠杆菌菌株,其发酵胞内破壁上清酶活为819.16u/ml,比酶活为206.91u/mg,其稳定的产酶性可以为进一步的理论研究和实际生产应用打下基础,实践应用意义重大。
生物材料保藏
一株大肠杆菌(escherichiacoli),分类命名为escherichiacolispl022,已于2019年5月24日保藏于中国典型培养物保藏中心,保藏编号为cctccno:m2019389,保藏地址为中国武汉,武汉大学。
附图说明
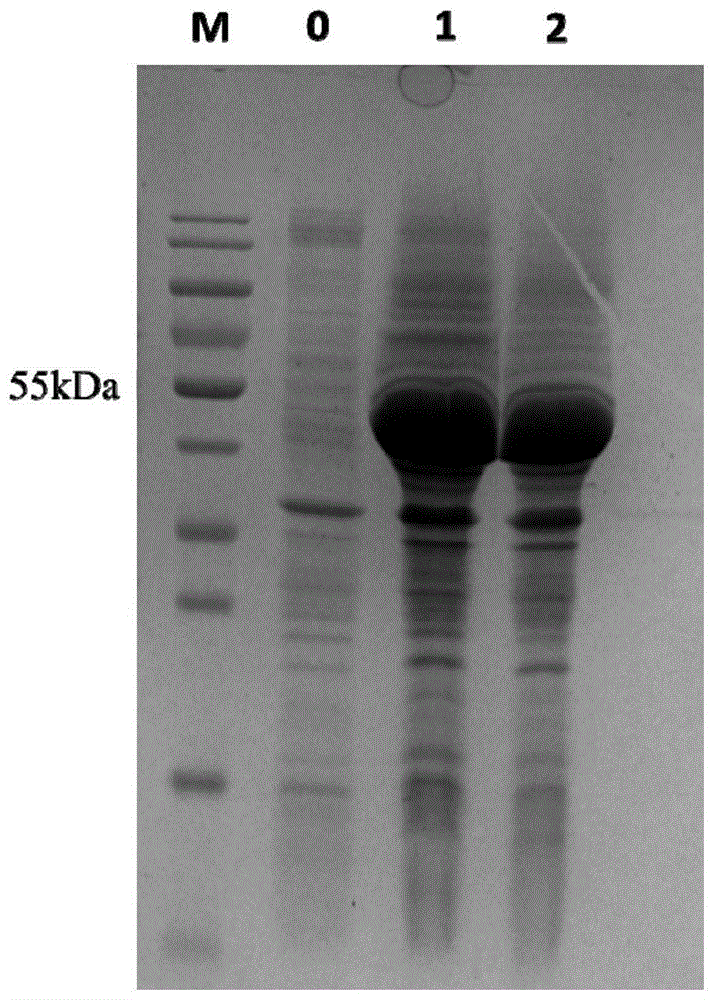
图1为重组菌escherichiacolispl0224摇瓶发酵胞内破壁上清sds-page电泳图,第1泳道为marker,第2泳道为空载菌摇瓶发酵胞内破壁上清,第3、4泳道为重组菌摇瓶发酵胞内破壁上清,可以清楚的看到图中55kda处有明显的条带与蔗糖磷酸化酶一致,表明可以获得蔗糖磷酸化酶。
具体实施方式
实施例1escherichiacolispl02基因工程菌的构建
(1)基因的优化:来源于leuconostocmesenteroidesatcc12291的sucrosephosphorylase(genbankaccessionno.d90314)进行分析优化,获得seqidno.1所示基因序列,并将两个酶切位点ncoi、xhoi加到经过优化后的蔗糖磷酸化酶两端,经过合成得到spase基因。
(2)基因工程菌的构建:将合成的spase基因和pet-28a载体用限制性内切酶ncoi和xhoi双酶切,酶切后产物用solutioni连接,然后将重组载体pet-28a-spase转入大肠杆菌bl21(de3)中表达。
实施例2重组蔗糖磷酸化酶的制备
将重组菌株单菌落接种于含kana的lb液体培养基中,于37℃,200r/min过夜培养后,按1%接种量接入到含kana的tb液体培养基中,于37℃,200r/min培养至菌密度od600达到0.6后,加入iptg诱导剂于25℃,200r/min诱导24h后收集菌液。将菌液于4℃,7000r/min的低温冷冻离心机中离心15min,收集菌体。菌体用50mmol/lk2hpo4/kh2po4缓冲液(ph6.5)洗两次后收集菌体。将收集好的湿菌体加入50mmol/lk2hpo4/kh2po4缓冲液(ph6.5)缓冲液制成菌悬液,放在冰上并固定好,然后用超声波破碎菌体。超声波破碎仪工作时间:2s,间歇时间:4s,总时间:30min。将破碎后的液体于4℃,7000r/min的低温冷冻离心机下离心30min收集上清即为蔗糖磷酸化酶粗酶液。
sds-page检测:吸取10μl粗酶液样品用sds-page检测(12%分离胶,5%浓缩胶),55kda处有明显的条带与蔗糖磷酸化酶一致,表明可以获得蔗糖磷酸化酶。
实施例3重组蔗糖磷酸化酶的酶活测定
在磷酸缓冲液中,蔗糖磷酸化酶能够催化蔗糖和无机磷酸生成葡萄糖-1-磷酸和d-果糖,可以先进行蔗糖水解反应,然后用dns检测生成的d-果糖的含量,从而测定蔗糖磷酸化酶的活力[choih.c.,seod.h.,jungj.h.,etal.developmemtofnewassayforsucrosephosphorylaseanditsapplicationtothecharacterizationofbifidobacteriumlongumsj32sucrosephosphorylase[j].foodscienceandbiotechnology,2011,20(2):513-518.]。
酶活测定方法参照[吴敬,吴丹,朱洁,等.一种表达l.mesenteroides来源的蔗糖磷酸化酶重组枯草芽孢杆菌.中国发明专利申请,申请号:201710637427.6,公开号:cn107236696a]。测定步骤包括:5%蔗糖溶液500μl,蔗糖磷酸化酶粗酶液50μl,50mmol/l磷酸盐缓冲液(ph6.5)450μl,30℃准确反应10min后,加入1.5mldns煮沸15min后迅速置于冷水中冷却,540nm处测定吸光值,以空载为对照。
将每分钟水解蔗糖生成1μmol的果糖所需酶量定义为蔗糖磷酸化酶的一个酶活力单位(u)。
酶活计算方法:
其中,a:吸光值、b:截距、n:稀释倍数、m:果糖分子质量、k:斜率。
蛋白含量测定:brandford法测定所制备酶液中蛋白质的含量。
酶活测定结果显示,酶活为504.19u/ml,比酶活为145.19u/mg。
实施例4将构建好的escherichiacolispl02基因工程菌进行紫外诱变
⑴制作菌悬液:挑取escherichiacolispl02单克隆菌株接种于含50mllb液体培养基(kana浓度100μg/ml)的250ml装量三角瓶中,37℃震荡培养12~18h,将活化的菌体菌液取5ml倒入离心管中,3500r/min离心10min,弃去上清液,吸入5ml无菌生理盐水冲洗两三次,加入15ml生理盐水吹打均匀制成菌悬液。
⑵紫外线处理:打开紫外灯,预热20min。取2ml菌悬液均匀的涂布于无菌培养基中,制作6份,置于紫外灯下,距灯管28.5cm处,先连盖在紫外灯下灭菌lmin,分别在紫外灯下照射15、30、45、60、75、90s和105s,照射后37℃避光培养24h。一般认为紫外致死率在80%时正突变率最高。
⑶初筛:经过紫外诱变后得到大量突变大肠杆菌菌株,挑选菌落大的突变大肠杆菌分别接种斜面培养基及液体培养基中进行培养筛选。37℃、120r/min条件下震荡培养8~10h后测定其600nm处吸光值,选取吸光值大的菌株进行复筛。
⑷复筛:将初筛获得的优良菌株接入含有50mllb培养基(kana浓度100μg/ml)中,37℃、200r/min条件下震荡培养10h后按1%接种量接入到含kana的tb液体培养基中,于37℃,200r/min培养至菌密度od600达到0.6后,加入iptg诱导剂于25℃,200r/min诱导24h后收集菌液制备蔗糖磷酸化酶粗酶液。检测其蔗糖磷酸化酶活性,筛选出蔗糖磷酸化酶活力较高的优良大肠杆菌菌株,并经过3~5代传代培养,最后获得了蔗糖磷酸化酶酶活力有较大提高且遗传稳定性较好的突变株,将其命名为escherichiacolispl0224,该菌株于2019年5月24日保藏于中国典型培养物保藏中心,保藏编号为cctccno:m2019389,保藏地址为中国武汉,武汉大学。
采用实施例2~3相同策略制备重组蔗糖磷酸化酶并测定其酶活,区别在于重组菌为escherichiacolispl0224基因工程菌,粗酶液样品用sds-page检测(12%分离胶,5%浓缩胶),如图1所示,可以清楚的看到图中55kda处有明显的条带与蔗糖磷酸化酶一致,表明可以获得蔗糖磷酸化酶。酶活测定结果显示,酶活为819.16u/ml,比酶活为206.91u/mg。
虽然本发明已以较佳实施例公开如上,但其并非用以限定本发明,任何熟悉此技术的人,在不脱离本发明的精神和范围内,都可做各种的改动与修饰,因此本发明的保护范围应该以权利要求书所界定的为准。
sequencelisting
<110>江南大学
<120>一种产蔗糖磷酸化酶的大肠杆菌
<160>1
<170>patentinversion3.3
<210>1
<211>1473
<212>dna
<213>人工序列
<400>1
atggaaatccagaacaaagctatgctgatcacctacgctgactctctgggtaaaaacctg60
aaagacgttcaccaggttctgaaagaagacatcggtgacgctatcggtggtgttcacctg120
ctgccgttcttcccgtctaccggtgaccgtggtttcgctccggctgactacacccgtgtt180
gacgctgctttcggtgactgggctgacgttgaagctctgggtgaagaatactacctgatg240
ttcgacttcatgatcaaccacatctctcgtgaatctgttatgtaccaggacttcaaaaaa300
aaccacgacgactctaaatacaaagacttcttcatccgttgggaaaaattctgggctaaa360
gctggtgaaaaccgtccgacccaggctgacgttgacctgatctacaaacgtaaagacaaa420
gctccgacccaggaaatcaccttcgacgacggtactaccgaaaacctgtggaacaccttc480
ggtgaagaacagatcgacatcgacgttaactctgctatcgctaaagaatttatcaaaacc540
accctggaagacatggttaaacacggtgctaacctgatccgtctggacgctttcgcttac600
gctgttaaaaaagttgacaccaacgacttcttcgttgaaccggaaatctgggacaccctg660
aacgaagttcgtgaaatcctgaccccgctgaaagctgaaatcctgccggaaatccacgaa720
cactactctatcccgaaaaaaatcaacgaccacggttacttcacctacgacttcgctctg780
ccgatgaccaccctgtacaccctgtactctggtaaaaccaaccagctcgctaaatggctg840
aaaatgtctccgatgaaacagttcaccaccctggacacccacgacggtatcggtgttgtt900
gacgctcgtgacatcctgaccgacgacgaaatcgactacgcttctgaacagctctacaaa960
gttggtgctaacgttaaaaaaacctactcttctgcttcttacaacaacctggacatctac1020
cagatcaactctacctactactctgctctgggtaacgacgacgctgcttacctgctgtct1080
cgtgttttccaggttttcgctccgggtatcccgcagatatactacgttggtctgctggct1140
ggtgaaaacgacatcgctctgctggaatctaccaaagaaggtcgtaacatcaaccgtcac1200
tactacacccgtgaagaagttaaatctgaagttaaacgtccggttgttgctaacctgctg1260
aaactgctgtcttggcgtaacgaatctccggctttcgacctggctggttctatcaccgtt1320
gacaccccgaccgacaccaccatcgttgttacccgtcaggacgaaaacggtcagaacaaa1380
gctgttctgaccgctgacgctgctaacaaaaccttcgaaatcgttgaaaacggtcagacc1440
gttatgtcttctgacaacctgacccagaactaa1473
- 还没有人留言评论。精彩留言会获得点赞!