检测非洲猪瘟病毒MGF360-505R基因的PCR引物组、试剂盒及检测方法与流程
本发明属于生物技术领域,具体地说,涉及一种检测非洲猪瘟病毒mgf360-505r基因的荧光定量pcr引物组、试剂盒及检测方法。
背景技术:
非洲猪瘟(africanswinefever,asf)是由非洲猪瘟病毒(africanswinefevervirus,asfv)感染引起的一种急性、热性、高度接触性传染病。世界动物卫生组织(oie)将其列为法定报告的动物疫病,中国将其列为一类动物疫病。非洲猪瘟对人不致病,不属于人畜共患病,但猪感染后发病率和病死率可高达100%。
目前,asf的实验室检测方法主要包括病毒分离、间接免疫荧光试验、elisa、pcr等。病毒分离和间接免疫荧光试验虽属标准检测方法,但操作繁琐,很难在条件一般的实验室开展。荧光定量pcr技术具有操作简单、敏感性高、特异性好等优点,已在非洲猪瘟病毒检测方面得到应用。然而,荧光定量pcr同时具有易被气溶胶污染的缺点,即使有微量的扩增产物泄露,也会导致假阳性的产生。专利《基因缺失的减毒非洲猪瘟病毒及其作为疫苗的应用》(申请号:201910348878.7,申请日:2019-04-26;公开号:110093324,公开日:2019-08-06)已公布了非洲猪瘟中国流行强毒株mgf360-505r基因缺失或cd2v与mgf360-505r基因联合缺失均能提供100%免疫保护,证明了mgf360-505r基因缺失在非洲猪瘟病毒疫苗研发中的决定性作用。弱毒疫苗一旦投入临床使用,现有的非洲猪瘟病毒荧光定量检测方法将不能用于临床流行毒株与疫苗株的鉴别检测。
因此,研发一种可用于检测非洲猪瘟病毒mgf360-505r基因的防污染荧光定量pcr方法,已经势在必行。
技术实现要素:
本发明的目的首先是提供了一种检测非洲猪瘟病毒mgf360-505r基因的防污染荧光定量pcr引物组,其次是提供该防污染荧光定量pcr快速检测试剂盒,再次是提供该试剂盒的检测方法。
为达到上述目的,本发明采取的具体技术方案为:
一种检测非洲猪瘟病毒mgf360-505r基因的荧光定量pcr引物,其特征在于,该引物包括靶向mgf360-505r基因的上游引物505r-p1、下游引物505r-p2和探针505r-pb;
所述引物505r-p1的核苷酸序列为:5’-catctcaagaagacagcggc-3’;
所述引物505r-p2的核苷酸序列为:5’-gtttacgaggtagttgacgcag-3’;
所述探针505r-pb的核苷酸序列:5’-tctagcacaaagtggaggagccc-3’。
进一步的,所述探针505r-pb在5’端标记rox,3’端标记bhq2。
一种鉴别检测非洲猪瘟病毒mgf360-505r基因的防污染荧光定量pcr试剂盒,包括上述的引物混合液,其中所述引物505r-p1终浓度为0.2mmol/l;所述引物505r-p2终浓度为0.2mmol/l;所述探针505r-pb终浓度为0.1mmol/l。
进一步地,该试剂盒还包括防污染荧光定量pcr预混液,防污染荧光定量pcr预混液含有dutp和ung酶(uracil-n-glycosylase)。若以dutp取代反应体系中的dttp,pcr产物则为含有dutp的dna双链。在pcr反应开始前增加37℃的预处理步骤,ung酶通过降解dutp,即可将反应体系中可能存在的dutp-dna双链污染物消除。变性步骤开始后,ung酶被灭活,不会再影响pcr反应的正常进行。
进一步地,该试剂盒还包括阳性对照,阳性对照为携带mgf360-505r基因的重组质粒。
上述的引物组或试剂盒在检测非洲猪瘟病毒mgf360-505r基因中的应用。
一种检测非洲猪瘟病毒mgf360-505r基因/使用上述试剂盒的检测方法,包括以下步骤:
1)使用所述的引物组配置引物组混合液,其中引物505r-p1终浓度为0.2mmol/l;引物505r-p2终浓度为0.2mmol/l;探针505r-pb终浓度为0.1mmol/l;
2)使用引物组混合液和防污染荧光定量pcr预混液对待测样品进行反应检测;反应体系为20μl,其中引物混合液2μl,荧光定量pcr预混液10μl,待测样品dna2μl,dnasefreewater6μl;
3)结果判读:
a)阴性:若无s型扩增曲线,证明待测样品没有非洲猪瘟病毒感染;
b)阳性:若在rox通道出现一条s型扩增曲线,证明待测样品为非洲猪瘟病毒感染。
进一步地,步骤2)中反应条件包括:37℃孵育2min;95℃预变性5min;95℃,10s;60℃,30s,45个循环。
与现有技术相比,本发明的优点和有益效果:
1)本发明提供的试剂盒可防止气溶胶污染,以dutp取代反应体系中的dttp,将反应体系中可能存在的dutp-dna双链污染物消除。
2)本发明提供的试剂盒特异性好,对血清5型副猪嗜血杆菌、血清2型猪链球菌、猪丹毒杆菌、猪传染性胸膜肺炎放线杆菌、猪伪狂犬病毒、猪圆环病毒2型的基因组dna都呈阴性反应;高灵敏度,最低可以检测到10拷贝的非洲猪瘟病毒mgf360-505r基因。
3)本发明提供的检测试剂盒操作简单、成本低廉,非常适用于出口检疫、食品卫生以及畜牧养殖场的非洲猪瘟病毒鉴别检测。
本发明提供的试剂盒可防止气溶胶污染,特异性强,敏感性高,可满足asfv高通量和精准快速检测的需求,预期可用于缺失株的鉴别诊断。本发明使得非洲猪瘟病毒的检测过程更加方便、快速、准确。
附图说明
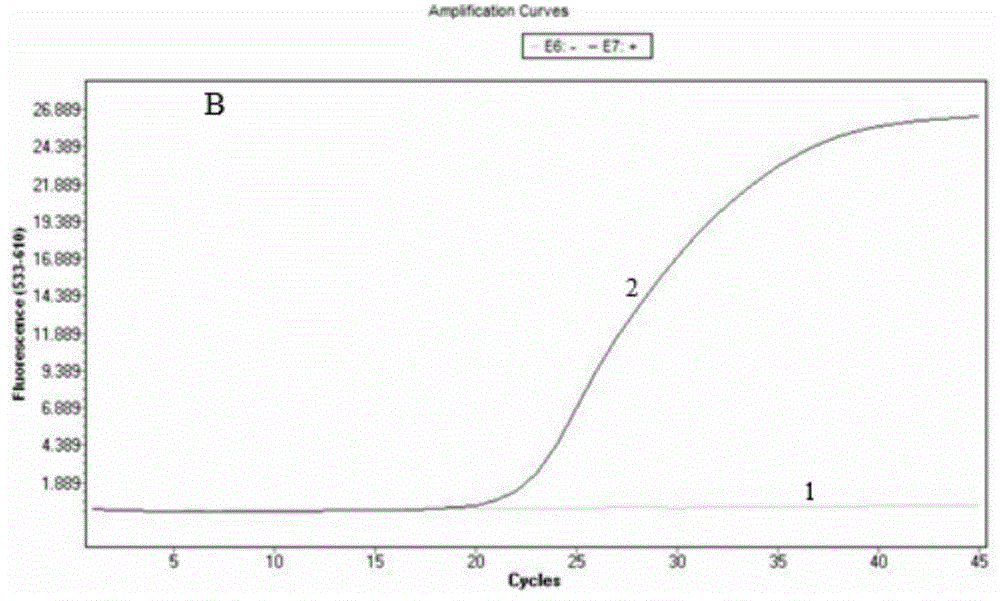
图1是本发明提供的荧光定量pcr试剂盒方法建立的结果图。
图2是本发明提供的荧光定量pcr试剂盒特异性实验中的结果图。
图3是本发明提供的荧光定量pcr试剂盒敏感性试验结果图。
具体实施方式
以下将配合实施例并结合附图来详细说明本发明的实施方式,藉此对本发明如何应用技术手段来解决技术问题并达成技术功效的实现过程能充分理解并据以实施。
实施例中所涉及的材料:
a)非洲猪瘟病毒mgf360-505r基因由上海生工生物工程技术服务有限公司合成;引物和探针由上海生工生物工程技术服务有限公司合成;防污染荧光定量pcr预混液购自南京诺唯赞生物科技有限公司(q113-02);病毒核酸提取试剂盒购自magen(美基)生物(r4410-03);伪狂犬病活疫苗(bartha-k61株)、猪圆环病毒2型灭活疫苗(lg株)购自上海海利生物技术股份有限公司;
b)以下生物材料均已在文献“副猪嗜血杆菌和猪链球菌双重pcr方法的建立与应用.中国兽医学报,2009(9):第1155-1157页.”中公开:血清5型副猪嗜血杆菌、血清2型猪链球菌、猪胸膜肺炎放线杆菌。
实施例1pcr引物的设计和合成
根据引物设计原则,针对非洲猪瘟病毒mgf360-505r基因的保守区域序列,应用primer5软件进行pcr引物和探针的设计,保证引物的gc含量在40%~60%之间。经过多套引物和探针组合的筛选后,最终获得本发明的引物组序列如表1所示,引物由上海生工生物工程技术服务有限公司合成,合成后的引物用灭菌三蒸水稀释成浓度为10μm,-20℃保存。
表1双重荧光定量pcr的引物组
实施例2荧光定量pcr引物在检测待测病毒中的应用
一、核酸标准品的制备
将上海生工生物工程技术服务有限公司合成的非洲猪瘟病毒mgf360-505r基因进行核酸浓度测定后,用超纯水稀释至0.4ng/μl的浓度(1.2×105拷贝),作为核酸标准品。
二、荧光定量pcr检测方法的建立
各取浓度为0.4ng/μl(1.2×105拷贝)的非洲猪瘟病毒mgf360-505r基因dna为模板,应用筛选获得的引物和探针(如表1所示),按照表2配置反应体系,反应条件为37℃孵育2min;95℃预变性5min;95℃,10s;60℃,30s,45个循环。得到的结果如图1所示:1是空白对照,2是非洲猪瘟病毒mgf360-505r基因dna。结果显示:空白对照没有出现s型扩增曲线,以非洲猪瘟病毒mgf360-505r基因dna为模板在rox通道出现一条s型扩增曲线。
表2荧光定量pcr反应体系
三、荧光定量检测方法的特异性
使用猪伪狂犬病毒、猪圆环病毒2型、猪丹毒杆菌、猪传染性胸膜肺炎放线杆菌、血清5型副猪嗜血杆菌、血清2型猪链球菌的基因组dna为模板检测体系的特异性。反应体系如表2所示,反应条件为37℃孵育2min;95℃预变性5min;95℃,10s;60℃,30s,45个循环。得到的结果如图2所示:1是以血清5型副猪嗜血杆菌基因组dna为模板的检测结果;2是以血清2型猪链球菌基因组dna为模板的检测结果;3是以猪丹毒杆菌基因组dna为模板的检测结果;4是以猪胸膜肺炎放线杆菌基因组dna为模板的检测结果;5是以猪伪狂犬病毒基因组dna为模板的检测结果;6是以猪圆环病毒2型基因组dna为模板的检测结果;7是以非洲猪瘟病毒mgf360-505r基因dna(1.2×103拷贝)为模板的检测结果;8是空白对照;以血清5型副猪嗜血杆菌、血清2型猪链球菌、猪丹毒杆菌、猪传染性胸膜肺炎放线杆菌、猪伪狂犬病毒、猪圆环病毒2型的基因组dna分别为模板没有出现s型扩增曲线,以非洲猪瘟病毒mgf360-505r基因dna为模板在rox通道出现一条s型扩增曲线,结果显示检测体系的特异性良好,可特异的检测非洲猪瘟病毒mgf360-505r基因。
四、双重荧光定量pcr检测方法的敏感性
分别取10μl浓度为0.4ng/μl的浓度(1.2×105拷贝)的非洲猪瘟病毒mgf360-505r基因dna,加入80μl的灭菌纯水进行10倍稀释,取此10倍稀释液10μl,依次加入90μl的灭菌纯水进行10倍梯度稀释,各取2μl稀释后样品液进行双重荧光定量pcr检测(反应体系如表2所示;除了模板有变化,反应条件均为37℃孵育2min;95℃预变性5min;95℃,10s;60℃,30s,45个循环)。得到的结果如图3所示:1为1.2×105拷贝的非洲猪瘟病毒mgf360-505r基因;2为1.2×104拷贝的非洲猪瘟病毒mgf360-505r基因;3为1.2×103拷贝的非洲猪瘟病毒mgf360-505r基因;4为120拷贝的非洲猪瘟病毒mgf360-505r基因;5为12拷贝的非洲猪瘟病毒mgf360-505r基因;6为1.2拷贝的非洲猪瘟病毒mgf360-505r基因;7为0.12拷贝的非洲猪瘟病毒mgf360-505r基因;8为空白对照。以1-5号稀释度的非洲猪瘟病毒dnaprimase基因dna为模板在fam通道出现一条s型扩增曲线,以6-8号稀释度的非洲猪瘟病毒mgf360-505r基因dna为模板没有出现s型扩增曲线,结果表明该方法最低可检测12拷贝的非洲猪瘟病毒mgf360-505r基因dna。
上述说明示出并描述了发明的若干优选实施例,但如前所述,应当理解发明并非局限于本文所披露的形式,不应看作是对其他实施例的排除,而可用于各种其他组合、修改和环境,并能够在本文所述发明构想范围内,通过上述教导或相关领域的技术或知识进行改动。而本领域人员所进行的改动和变化不脱离发明的精神和范围,则都应在发明所附权利要求的保护范围内。
序列表
<110>广东省农业科学院动物卫生研究所
<120>检测非洲猪瘟病毒mgf360-505r基因的pcr引物组、试剂盒及检测方法
<160>3
<170>siposequencelisting1.0
<210>1
<211>20
<212>dna
<213>人工序列(artificialsequence)
<400>1
catctcaagaagacagcggc20
<210>2
<211>22
<212>dna
<213>人工序列(artificialsequence)
<400>2
gtttacgaggtagttgacgcag22
<210>3
<211>23
<212>dna
<213>人工序列(artificialsequence)
<400>3
tctagcacaaagtggaggagccc23
- 还没有人留言评论。精彩留言会获得点赞!