用于检测人乳头瘤病毒核酸的组合物和方法与流程
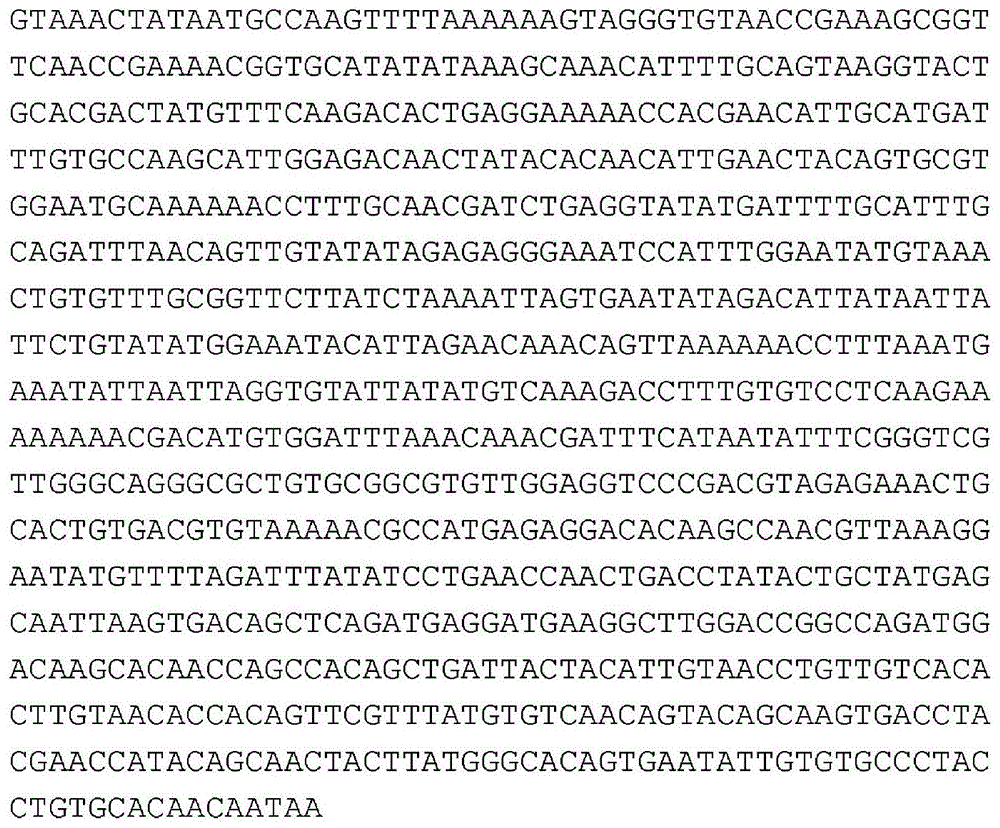
本发明申请是基于申请日为2013年10月11日,申请号为201380064307.1(国际申请号为pct/us2013/064519)、名称为“用于检测人乳头瘤病毒核酸的组合物和方法”的发明专利申请的分案申请。优先权本申请要求以下申请的优先权的权益:2012年10月11日提交的美国临时申请no.61/712,332,该申请的全部内容据此以引用方式并入本文中。
背景技术:
:人乳头瘤病毒(hpv)的感染目标是上皮组织,并且是多种癌症(主要为鳞状细胞癌和腺癌)的病因。与hpv相关的癌症包括头颈(喉、口腔、口咽、扁桃体和食道)、呼吸道组织、乳腺、皮肤、宫颈和肛门的癌症。虽然认为hpv感染是一些癌症发展的必要因素,但其他因素也可能影响癌变过程(braakhuis等,j.natl.cancerinst.96:998-1006,2004(braakhuis等,《美国国立癌症研究所杂志》,第96卷,第998-1006页,2004年);dahlstrand等,anticancerres.24:1829-35,2004(dahlstrand等,《抗癌研究》,第24卷,第1829-1835页,2004年);daling等,cancer101:270-80,2004(daling等,《癌症》,第101卷,第270-280页,2004年);ha等,crit.rev.oralbiol.med.15:188-96,2004(ha等,《口腔生物医学与医学鉴定性评论》,第15卷,第188-196页,2004年);hafkamp等,actaotolaryngol.124:520-6,2004(hafkamp等,《耳鼻喉科学报》,第124卷,第520-526页,2004年);harwood等,br.j.dermatol.150:949-57,2004(harwood等,《英国皮肤病学杂志》,第150卷,第949-957页,2004年);rees等,clin.otolaryngol.29:301-6,2004(rees等,《临床耳鼻喉科学》,第29卷,第301-306页,2004年);widschwendter等,j.clin.virol.31:292-7,2004(widschwendter等,《临床病毒学杂志》,第31卷,第292-297页,2004年))。已鉴定出至少77种不同类型的hpv。在它们中,hpv16和hpv18在很多情况下与多种hpv相关癌症有关联,但是与hpv类型相关的风险等级可随乳头瘤相关癌症的不同形式而变化。已研究了人乳头瘤病毒在上皮细胞中的发病机理以阐明hpv感染与癌症的联系。hpv感染复层上皮细胞的基底层细胞,在此处它们以多拷贝附加体或整合基因组的形式定殖,病毒dna凭借所述多拷贝附加体或整合基因组随同细胞染色体一起复制(由longworth等,microbiol.mol.biol.rev.68:362-72,2004(longworth等,《微生物学与分子生物学评论》,第68卷,第362-372页,2004年)综述)。在细胞分裂时,子细胞迁移离开基底层并经历分化,在分化过程中,hpv营养期病毒复制和晚期基因表达被激活,从而产生子代hpv。虽然被感染个体的免疫系统通常可在1至2年内将hpv感染清除,但被感染的基底细胞可能存留几十年。hpv感染可导致染色体的不稳定性和非整倍性,这些性质可有利于hpv整合(melsheimer等,clin.cancerres.10:3059-63,2004(melsheimer等,《临床癌症研究》,第10卷,第3059-3063页,2004年);reidy等,laryngoscope114:1906-9,2004(reidy等,《喉镜》,第114卷,第1906-1909页,2004年))。在hpv基因组整合期间,hpve2基因可能被破坏,导致编码靶向调节蛋白prb和p53的癌蛋白的hpve6/e7致癌基因的表达失调。因此,对细胞调节进行调控的一连串事件可能导致癌变(braun等,cancerlett.209:37-49,2004(braun等,《癌症快报》,第209卷,第37-49页,2004年);fan等,crit.rev.eukaryot.geneexpr.14:183-202,2004(fan等,《真核状态基因表达评论综述》,第14卷,第183-202页,2004年);fiedler等,fasebj.18:1120-2,2004(fiedler等,《美国实验生物学联合会会刊》,第18卷,第1120-1122页,2004年);psyrri等,cancerres.,64:3079-86,2004(psyrri等,《癌症研究》,第64卷,第3079-3086页,2004年);si等,j.clin.virol.32:19-23,2004(si等,《临床病毒学杂志》,第32卷,第19-23页,2004年))。由于宫颈癌在世界范围内高发(估计每年有450,000例新增病例),故hpv感染与宫颈癌的相关性已成为大量研究工作和流行病学研究的课题。与发展成宫颈癌的高风险相关联的hpv类型(hr-hpv)包括hpv16、18、31、33、35、39、45、51、52、56、58、59、66、68和73型,但各个类型的流行病学意义可随地理区域或临床检验参数不同而变化(munoz等,int.j.cancer111:278-85,2004(munoz等,《国际癌症杂志》,第111卷,第278-285页,2004年);chaturvedi等,j.med.virol.75:105-13,2005(chaturvedi等,《医学病毒学杂志》,第75卷,第105-113页,2005年);smith等,int.j.gynaecol.obstet.87:131-7,2004(smith等,《国际妇产科杂志》,第87卷,第131-137页,2004年))。通常被认为只有较低的发展成宫颈癌的风险的hpv感染(lr-hpv)包括hpv6、11、43、43、44、61、71和72型。在感染hpv的妇女中,宫颈感染可能导致湿疣(生殖器疣)、宫颈上皮内瘤样病变(cin)和宫颈癌(kahn等,adolesc.med.clin.15:301-21,ix,2004(kahn等,《临床青少年医学》,第15卷,第301-321页,第9章,2004年))。在许多国家中,宫颈细胞的细胞学检查已成为用于检测宫颈癌的主要筛查工具,其通常使用cin分级体系(1至3)来监测癌前病变,以便决定治疗和/或进一步监测。除细胞学筛查外,对hpv核酸进行分子筛查也许是有可能延长两次细胞学检验之间的时间间隔的经济有效的预后检验手段(wiley等,curr.oncol.rep.6:497-506,2004(wiley等,《当代肿瘤学报告》,第6卷,第497-506页,2004年);zielinski等,obstet.gynecol.surv.59:543-53,2004(zielinski等,《妇产科调查》,第59卷,第543-553页,2004年);clavel等,br.j.cancer90:1803-8,2004(clavel等,《英国癌症杂志》,第90卷,第1803-1808页,2004年))。已经开发出用于检测人类生物样本中的所选择hpv蛋白和核酸序列的分子测定法,例如巴氏涂片和活组织检查(chen等,gynecol.oncol.99:578-84,2005(chen等,《妇科肿瘤学》,第99卷,第578-584页,2005年);carozzi等,am.j.clin.pathol.124:716-21,2005(carozzi等,《美国临床病理学杂志》,第124卷,第716-721页,2005年);molden等,cancerepidemiol.biomarkersprev.14:367-72,2005(molden等,《癌症流行病学、生物标记与预防》,第14卷,第367-372页,2005年);asato等,j.infect.dis.189:1829-32,2004(asato等,《传染病学杂志》,第189卷,第1829-1832页,2004年);federschneider等,am.j.obstet.gynecol.191:757-61,2004(federschneider等,《美国妇产科杂志》,第191卷,第757-761页,2004年);remmerbach等,j.clin.virol.30:302-8,2004(remmerbach等,《临床病毒学杂志》,第30卷,第302-308页,2004年))。针对常见hpv类型的疫苗对于治疗或预防生殖器疣、或者防止癌症(特别是宫颈癌)发展可能是有用的。各种形式的hpv疫苗是可用的或正在研制中(ault等,vaccine22:3004-7,2004(ault等,《疫苗》,第22卷,第3004-3007页,2004年);coronagutierrez等,hum.genet.ther.15:421-31,2004(coronagutierrez等,《人类基因治疗》,第15卷,第421-431页,2004年);harper等,lancet364:1757-65,2004(harper等,《柳叶刀》,第364卷,第1757-1765页,2004年);roden等,hum.pathol.35:971-82,2004(roden等,《人体病理学》,第35卷,第971-982页,2004年))。需要有效且灵敏地检测生物样本中hpv的存在,以便向治疗感染hpv的患者(特别是宫颈组织已感染hr-hpv类型的妇女)的医生提供诊断和预后信息。还需要有效且灵敏地检测从已接种了抗hpv感染的疫苗的个体获得的生物样本中hpv的存在,以便确定疫苗的短期和长期疗效。技术实现要素:在一个方面,本发明提供了用于检测疑似含有hpv33的样品中的人乳头瘤病毒33型(hpv33)靶标核酸的至少两种低聚物的组合。通常,所述低聚物组合包括用于特异性地扩增与hpv33e6和/或e7基因相对应的hpv33核酸靶标区域的第一扩增低聚物和第二扩增低聚物。在某些实施例中,(a)第一hpv33扩增低聚物包含第一靶标杂交序列,该第一靶标杂交序列为包含在seqidno:66的序列中的约15至约27个连续核苷酸并至少包括seqidno:67、seqidno:68或seqidno:69的序列;并且(b)第二hpv33扩增低聚物包含第二靶标杂交序列,该第二靶标杂交序列为包含在seqidno:70的序列中的约15至约27个连续核苷酸并至少包括seqidno:71、seqidno:72或seqidno:73的序列。特别合适的第一hpv33扩增低聚物和第二hpv33扩增低聚物包括:(a)包含选自seqidno:1、seqidno:2、seqidno:3、seqidno:4、seqidno:5、seqidno:6、seqidno:7和seqidno:8的第一靶标杂交序列的第一hpv33扩增低聚物;以及(b)包含选自seqidno:9、seqidno:10、seqidno:11、seqidno:12、seqidno:13、seqidno:14、seqidno:15和seqidno:16的第二靶标杂交序列的第二hpv33扩增低聚物。在典型的变型形式中,所述低聚物组合用于检测疑似含有hpv33和至少一种其他hpv基因型(例如,hpv16、18、31、45、52和58型中的至少一种)的样品中的hpv33靶标核酸。在一些变型形式中,用于检测hpv33和至少一种其他hpv基因型的低聚物组合包括与表4中的两种或更多种低聚物基本上相同的低聚物的组合。在一些优选的变型形式中,所述低聚物组合还包括用于特异性地扩增与hpv31e6和/或e7基因相对应的hpv31型(hpv31)核酸靶标区域的第一扩增低聚物和第二扩增低聚物。在一些此类实施例中,第一hpv31扩增低聚物包含第一靶标杂交序列,该第一靶标杂交序列为包含在seqidno:74的序列中的约15至约27个连续核苷酸并至少包括seqidno:75、seqidno:76或seqidno:77的序列;并且第二hpv31扩增低聚物包含第二靶标杂交序列,该第二靶标杂交序列为包含在seqidno:78的序列中的约15至约30个连续核苷酸并至少包括seqidno:79、seqidno:80或seqidno:81的序列。特别合适的第一hpv31扩增低聚物和第二hpv31扩增低聚物包括:(a)包含选自seqidno:26、seqidno:27、seqidno:28、seqidno:29、seqidno:30、seqidno:31、seqidno:32和seqidno:33的第一靶标杂交序列的第一hpv31扩增低聚物;以及(b)包含选自seqidno:34、seqidno:35、seqidno:36、seqidno:37、seqidno:38、seqidno:39、seqidno:40和seqidno:41的第二靶标杂交序列的第二hpv33扩增低聚物。在一些变型形式中,第二hpv33扩增低聚物为还包含位于靶标杂交序列5'端的启动子序列的启动子引物或启动子提供者。相似地,在一些还包含hpv31扩增低聚物的实施例中,第二hpv31扩增低聚物为还包含位于靶标杂交序列5'端的启动子序列的启动子引物或启动子提供者。合适的启动子序列包括t7rna聚合酶启动子序列,诸如以seqidno:82示出的序列。在更具体的实施例中,第二hpv33扩增低聚物具有以seqidno:17、seqidno:18、seqidno:19、seqidno:20、seqidno:21、seqidno:22、seqidno:23或seqidno:24示出的序列;并且/或者第二hpv31扩增低聚物具有以seqidno:42、seqidno:43、seqidno:44、seqidno:45、seqidno:46、seqidno:47、seqidno:48或seqidno:49示出的序列。低聚物组合还可包括至少一种捕获探针低聚物。例如,所述低聚物组合还可包括hpv33特异性捕获探针低聚物和/或hpv31特异性捕获探针低聚物。此类hpv33或hpv31特异性捕获探针低聚物通常包含共价连接到结合于固定化探针的序列或部分的靶标杂交序列。合适的hpv33靶标杂交序列和hpv31靶标杂交序列分别以seqidno:50和seqidno:52示出。在特定的变型形式中,hpv33捕获探针低聚物或hpv31捕获探针低聚物分别具有如以seqidno:51或seqidno:53示出的序列。在一些实施例中,低聚物组合还包括至少一种hpv-33特异性检测探针低聚物和/或hpv31特异性检测探针低聚物。合适的hpv33检测探针包括包含靶标杂交序列的低聚物,该靶标杂交序列为约14至约35个核苷酸长并被构造为与包含在seqidno:83内从约核苷酸位置128至约核苷酸位置164的靶标序列(例如,选自seqidno:54、seqidno:55、seqidno:56、seqidno:57和seqidno:58的靶标杂交序列)特异性杂交。合适的hpv31检测探针包括包含靶标杂交序列的低聚物,该靶标杂交序列为约14至约40个核苷酸长并被构造为与包含在seqidno:84内从约核苷酸位置675至约核苷酸位置735的靶标序列(例如,选自seqidno:59、seqidno:60、seqidno:61、seqidno:62、seqidno:63、seqidno:64和seqidno:65的靶标杂交序列)特异性杂交。在其他方面,本发明提供了包含上述低聚物组合的试剂盒或反应混合物。在又一个方面,本发明提供了用于检测样品中的人乳头瘤病毒33型(hpv33)靶标核酸(例如,hpv33e6/e7mrna转录物)的方法。该方法通常包括以下步骤:(a)提供疑似含有hpv33的样品;(b)将该样品与低聚物组合接触,以便特异性地扩增hpv33核酸靶标区域,所述低聚物组合包括:(i)包含第一靶标杂交序列的第一hpv33扩增低聚物,该第一靶标杂交序列为包含在seqidno:66的序列中的约15至约27个连续核苷酸并至少包括seqidno:67、seqidno:68或seqidno:69的序列,以及(ii)包含第二靶标杂交序列的第二hpv33扩增低聚物,该第二靶标杂交序列为包含在seqidno:70的序列中的约15至约27个连续核苷酸并至少包括seqidno:71、seqidno:72或seqidno:73的序列;(c)进行体外核酸扩增反应,其中存在于所述样品中的任何hpv33靶标核酸均被用作产生hpv33扩增产物的模板;以及(d)检测hpv33扩增产物存在与否,从而指示样品中是否存在hpv33。特别合适的第一33型扩增低聚物和第二33型扩增低聚物包括:(a)包含选自seqidno:1、seqidno:2、seqidno:3、seqidno:4、seqidno:5、seqidno:6、seqidno:7和seqidno:8的第一靶标杂交序列的第一hpv33扩增低聚物;以及(b)包含选自seqidno:9、seqidno:10、seqidno:11、seqidno:12、seqidno:13、seqidno:14、seqidno:15和seqidno:16的第二靶标杂交序列的第二hpv33扩增低聚物。在该方法的典型变型形式中,所述低聚物组合用于检测疑似含有hpv33和至少一种其他hpv基因型(例如,hpv16、18、31、45、52和58型中的至少一种)的样品中的hpv33靶标核酸。在该方法的一些变型形式中,还检验了所述样品的hpv33和至少一种其他hpv基因型,其中在该方法中使用的低聚物中的两种或更多种与表4中的那些基本上相同。在一些优选的变型形式中,该方法还用于检测样品中的hpv31型(hpv31)靶标核酸(例如,hpv31e6/e7mrna转录物)。在一些此类变型形式中,该方法还包括以下步骤:(b')将该样品与低聚物组合接触,以便特异性地扩增hpv31核酸靶标区域,所述低聚物组合包括:(i)包含第一靶标杂交序列的第一hpv31扩增低聚物,该第一靶标杂交序列为包含在seqidno:74的序列中的约15至约27个连续核苷酸并至少包括seqidno:75、seqidno:76或seqidno:77的序列,以及(ii)包含第二靶标杂交序列的第二hpv31扩增低聚物,该第二靶标杂交序列为包含在seqidno:78的序列中的约15至约30个连续核苷酸并至少包括seqidno:79、seqidno:80或seqidno:81的序列;(c')进行体外核酸扩增反应,其中存在于所述样品中的任何hpv31靶标核酸均被用作产生hpv31扩增产物的模板;以及(d')检测hpv31扩增产物存在与否,从而指示样品中是否存在hpv31。在方法的一些实施例中,第二hpv33扩增低聚物为还包含位于靶标杂交序列5'端的启动子序列的启动子引物或启动子提供者。相似地,在一些还包括对hpv31靶标核酸进行检测的实施例中,第二hpv31扩增低聚物为还包含位于靶标杂交序列5'端的启动子序列的启动子引物或启动子提供者。合适的启动子序列包括t7rna聚合酶启动子序列,诸如以seqidno:82示出的序列。在更具体的实施例中,第二hpv33扩增低聚物具有以seqidno:17、seqidno:18、seqidno:19、seqidno:20、seqidno:21、seqidno:22、seqidno:23或seqidno:24示出的序列;并且/或者第二hpv31扩增低聚物具有以seqidno:42、seqidno:43、seqidno:44、seqidno:45、seqidno:46、seqidno:47、seqidno:48或seqidno:49示出的序列。在上述的包括对hpv33靶标核酸和hpv31靶标核酸两者进行检测的方法的某些变型形式中,扩增步骤(c)与扩增步骤(c')在同一扩增反应混合物中同时进行。通常,在此类变型形式中,检测步骤(d)与检测步骤(d')在同一检测反应混合物中同时进行。通常,用于检测hpv33靶标核酸的方法还包括在步骤(b)之前从样品中的其他组分纯化hpv33靶标核酸。在特定实施例中,所述纯化步骤包括将样品与至少一种hpv33特异性捕获探针低聚物接触,该hpv33特异性捕获探针低聚物包含共价连接到结合于固定化探针的序列或部分的靶标杂交序列。特别合适的hpv33靶标杂交序列以seqidno:50示出。在更具体的变型形式中,hpv33特异性捕获探针低聚物具有以seqidno:51示出的序列。在包括对hpv31靶标核酸进行检测的方法的变型形式中,该方法通常还包括在步骤(b')之前从样品中的其他组分纯化hpv31靶标核酸。在特定实施例中,所述纯化步骤包括将样品与至少一种hpv31特异性捕获探针低聚物接触,该hpv31特异性捕获探针低聚物包含共价连接到结合于固定化探针的序列或部分的靶标杂交序列。特别合适的hpv31靶标杂交序列以seqidno:52示出。在更具体的变型形式中,hpv31特异性捕获探针低聚物具有以seqidno:53示出的序列。在一些实施例中,检测步骤(d)包括将步骤(c)的扩增反应与hpv33检测探针低聚物接触,该hpv33检测探针低聚物被构造为在这样的条件下与hpv33扩增产物特异性杂交:凭借所述条件可确定hpv33扩增产物存在与否,从而指示样品中是否存在hpv33。在特定实施例中,hpv33检测探针包含靶标杂交序列,该靶标杂交序列为约14至约35个核苷酸长并被构造为与包含在seqidno:83内从约核苷酸位置128至约核苷酸位置164的靶标序列特异性杂交。在具体变型形式中,hpv33检测探针靶标杂交序列选自seqidno:54、seqidno:55、seqidno:56、seqidno:57和seqidno:58。在包括对hpv31靶标核酸进行检测的方法的一些变型形式中,检测步骤(d)'包括将步骤(c)的扩增反应与hpv31检测探针低聚物接触,该hpv31检测探针低聚物被构造为在这样的条件下与hpv31扩增产物特异性杂交:凭借所述条件可确定hpv31扩增产物存在与否,从而指示样品中是否存在hpv31。在特定实施例中,hpv31检测探针包含靶标杂交序列,该靶标杂交序列为约14至约40个核苷酸长并被构造为与包含在seqidno:84内从约核苷酸位置675至约核苷酸位置735的靶标序列特异性杂交。在具体变型形式中,hpv31检测探针靶标杂交序列选自seqidno:59、seqidno:60、seqidno:61、seqidno:62、seqidno:63、seqidno:64和seqidno:65。在利用检测探针低聚物的方法的一些实施例中,所述检测探针包含至少一个标签。在具体变型形式中,一个或多个标签选自化学发光标签、荧光标签、淬光剂、或它们的任何组合。在利用检测探针低聚物的方法的其他实施例中,为了检测hpv33靶标核酸,在扩增步骤(c)期间进行检测步骤(d);并且/或者为了检测hpv31靶标核酸,在扩增步骤(c')期间进行检测(d')。在一些此类实施例中,所述检测探针包含荧光标签、淬光剂,或这两者(例如,taqman检测探针或分子信标)。在利用检测探针低聚物的方法的其他实施例中,所述检测探针还包含非靶标杂交序列。在特定实施例中,包含非靶标杂交序列的检测探针为发夹检测探针,诸如分子信标或分子炬。在该方法的某些实施例中,步骤(c)和/或(c')处的扩增反应为等温扩增反应或pcr反应。在具体变型形式中,等温扩增反应为转录介导的扩增(tma)反应(例如,反向tma反应)。在利用等温或pcr扩增反应的方法的一些实施例中,该反应为实时扩增反应。在该方法的一些优选实施例中,(i)检测步骤(d)包括将步骤(c)的扩增反应与hpv33检测探针低聚物接触,该hpv33检测探针低聚物被构造为在这样的条件下与hpv33扩增产物特异性杂交:凭借所述条件可确定hpv33扩增产物存在与否,从而指示样品中是否存在hpv33;(ii)检测步骤(d')包括将步骤(c')的扩增反应与hpv31检测探针低聚物接触,该hpv31检测探针低聚物被构造为在这样的条件下与hpv31扩增产物特异性杂交:凭借所述条件可确定hpv31扩增产物存在与否,从而指示样品中是否存在hpv31;(iii)步骤(c)与步骤(c')在同一扩增反应混合物中同时进行,并且步骤(d)与步骤(d')在同一检测反应混合物中同时进行;并且(iv)hpv33检测探针低聚物和hpv31检测探针低聚物被差异性标记。在一些此类实施例中,hpv33检测探针低聚物和hpv31检测探针低聚物中的每一者包含独立地选自化学发光标签和荧光标签的标签。在更具体的变型形式中,hpv33检测探针低聚物和hpv31检测探针低聚物中的每一者包含化学发光标签;在一些此类变型形式中,用于hpv33检测探针低聚物和hpv31检测探针低聚物的化学发光标签通过足以区分hpv33特异性化学发光信号和hpv31特异性化学发光信号的不同光发射动力学来表征。用于hpv33检测探针低聚物和hpv31检测探针低聚物的合适化学发光标签包括含有吖啶酯(ae)的标签。在又一方面,本发明提供了用于检测hpv33靶标核酸或hpv31靶标核酸的检测探针低聚物。在一些实施例中,用于检测hpv33的检测探针低聚物包含靶标杂交序列,该靶标杂交序列为约14至约35个核苷酸长并被构造为与包含在seqidno:83内从约核苷酸位置128至约核苷酸位置164的靶标序列(例如,选自seqidno:54、seqidno:55、seqidno:56、seqidno:57和seqidno:58的靶标杂交序列)特异性杂交。在一些实施例中,用于检测hpv31的检测探针低聚物包含靶标杂交序列,该靶标杂交序列为约14至约40个核苷酸长并被构造为与包含在seqidno:84内从约核苷酸位置675至约核苷酸位置735的靶标序列(例如,选自seqidno:59、seqidno:60、seqidno:61、seqidno:62、seqidno:63、seqidno:64和seqidno:65的靶标杂交序列)特异性杂交。在检测探针低聚物的一些实施例中,所述检测探针包含至少一个标签。在具体变型形式中,一个或多个标签选自化学发光标签、荧光标签、淬光剂、或它们的任何组合。在更具体的变型形式中,所述检测探针包含荧光标签和淬光剂(例如,taqman检测探针或分子信标)。在检测探针低聚物的其他实施例中,所述检测探针还包含非靶标杂交序列。在特定变型形式中,包含非靶标杂交序列的检测探针为发夹检测探针,诸如分子信标或分子炬。具体地,本发明涉及如下各项:1.一种用于检测疑似含有hpv33以及hpv31、52和58型中的至少一种的样品中的人乳头瘤病毒33型(hpv33)靶标核酸的低聚物组合,所述低聚物组合包括:用于特异性地扩增hpv33核酸靶标区域的第一扩增低聚物和第二扩增低聚物,其中(a)所述第一hpv33扩增低聚物包含第一靶标杂交序列,所述第一靶标杂交序列为包含在seqidno:66的序列中的约15至约27个连续核苷酸并至少包括seqidno:67、seqidno:68或seqidno:69的序列;并且(b)所述第二hpv33扩增低聚物包含第二靶标杂交序列,所述第二靶标杂交序列为包含在seqidno:70的序列中的约15至约27个连续核苷酸并至少包括seqidno:71、seqidno:72或seqidno:73的序列。2.根据项1所述的低聚物组合,还包括用于特异性地扩增hpv31型(hpv31)核酸靶标区域的第一扩增低聚物和第二扩增低聚物,其中(a)所述第一hpv31扩增低聚物包含第一靶标杂交序列,所述第一靶标杂交序列为包含在seqidno:74的序列中的约15至约27个连续核苷酸并至少包括seqidno:75、seqidno:76或seqidno:77的序列;并且(b)所述第二hpv31扩增低聚物包含第二靶标杂交序列,所述第二靶标杂交序列为包含在seqidno:78的序列中的约15至约30个连续核苷酸并至少包括seqidno:79、seqidno:80或seqidno:81的序列。3.根据项1或2所述的低聚物组合,其中所述第二hpv33扩增低聚物为还包含位于所述靶标杂交序列5'端的启动子序列的启动子引物或启动子提供者。4.根据项3所述的低聚物组合,其中所述第二hpv33低聚物的所述启动子序列为t7启动子序列。5.根据项4所述的低聚物组合,其中所述t7启动子序列具有以seqidno:82示出的序列。6.根据项2所述的低聚物组合,其中所述第二hpv31扩增低聚物为还包含位于所述靶标杂交序列5'端的启动子序列的启动子引物或启动子提供者。7.根据项6所述的低聚物组合,其中所述第二hpv31低聚物的所述启动子序列为t7启动子序列。8.根据项7所述的低聚物组合,其中所述t7启动子序列具有以seqidno:82示出的序列。9.一种用于检测样品中的人乳头瘤病毒33型(hpv33)靶标核酸的低聚物组合,所述低聚物组合包括:用于扩增hpv33核酸靶标区域的第一扩增低聚物和第二扩增低聚物,其中(a)所述第一hpv33扩增低聚物包含选自seqidno:1-seqidno:8的第一靶标杂交序列;并且(b)所述第二hpv33扩增低聚物包含选自seqidno:9-seqidno:16的第二靶标杂交序列。10.根据项9所述的低聚物组合,还包括用于扩增hpv31型(hpv31)核酸靶标区域的第一扩增低聚物和第二扩增低聚物,其中(a)所述第一hpv31扩增低聚物包含选自seqidno:25-seqidno:33的第一靶标杂交序列;并且(b)所述第二hpv31扩增低聚物包含选自seqidno:34-seqidno:41的第二靶标杂交序列。11.根据项9或10所述的低聚物组合,其中所述第二hpv33扩增低聚物为还包含位于所述靶标杂交序列5'端的启动子序列的启动子引物或启动子提供者。12.根据项11所述的低聚物组合,其中所述第二hpv33低聚物的所述启动子序列为t7启动子序列。13.根据项12所述的低聚物组合,其中所述t7启动子序列具有以seqidno:82示出的序列。14.根据项13所述的低聚物组合,其中所述第二hpv33扩增低聚物具有选自seqidno:17-seqidno:24的序列。15.根据项10所述的低聚物组合,其中所述第二hpv31扩增低聚物为还包含位于所述靶标杂交序列5'端的启动子序列的启动子引物或启动子提供者。16.根据项15所述的低聚物组合,其中所述第二hpv31低聚物的所述启动子序列为t7启动子序列。17.根据项16所述的低聚物组合,其中所述t7启动子序列具有以seqidno:82示出的序列。18.根据项17所述的低聚物组合,其中所述第二hpv31扩增低聚物具有选自seqidno:42-seqidno:49的序列。19.根据项1至18中任一项所述的低聚物组合,还包括含有靶标杂交序列的至少一种hpv33检测探针低聚物,所述靶标杂交序列为约14至约35个核苷酸长并被构造为与包含在seqidno:83内从约核苷酸位置128至约核苷酸位置164的靶标序列特异性杂交。20.根据项21所述的低聚物组合,其中所述hpv33检测探针靶标杂交序列选自seqidno:54-seqidno:58。21.根据项2、6至8、10、以及15至18中任一项所述的低聚物组合,还包括含有靶标杂交序列的至少一种hpv31检测探针低聚物,所述靶标杂交序列为约14至约40个核苷酸长并被构造为与包含在seqidno:84内从约核苷酸位置675至约核苷酸位置735的靶标序列特异性杂交。22.根据项21所述的低聚物组合,其中所述hpv31检测探针靶标杂交序列选自seqidno:59-seqidno:65。23.一种包含根据项1至22中任一项所述的低聚物组合的试剂盒。24.一种包含根据项1至22中任一项所述的低聚物组合的反应混合物。25.一种用于检测疑似含有hpv33以及hpv31、52和58型中的至少一种的样品中的人乳头瘤病毒33型(hpv33)靶标核酸的方法,所述方法包括:(a)提供样品,其中所述样品疑似含有hpv33以及hpv31、52和58型中的至少一种;(b)将所述样品与低聚物组合接触,以便特异性地扩增hpv33核酸靶标区域,所述低聚物组合包括:(i)包含第一靶标杂交序列的第一hpv33扩增低聚物,所述第一靶标杂交序列为包含在seqidno:66的序列中的约15至约27个连续核苷酸并至少包括seqidno:67、seqidno:68或seqidno:69的序列;和(ii)包含第二靶标杂交序列的第二hpv33扩增低聚物,所述第二靶标杂交序列为包含在seqidno:70的序列中的约15至约27个连续核苷酸并至少包括seqidno:71、seqidno:72或seqidno:73的序列;(c)进行体外核酸扩增反应,其中存在于所述样品中的任何hpv33靶标核酸均被用作产生hpv33扩增产物的模板;以及(d)检测所述hpv33扩增产物存在与否,从而指示所述样品中是否存在hpv33。26.根据项25所述的方法,其中所述方法用于进一步检测所述样品中的hpv31型(hpv31)靶标核酸,并且其中所述方法还包括:(b')将所述样品与低聚物组合接触,以便特异性地扩增hpv31核酸靶标区域,所述低聚物组合包括:(i)包含第一靶标杂交序列的第一hpv31扩增低聚物,所述第一靶标杂交序列为包含在seqidno:74的序列中的约15至约27个连续核苷酸并至少包括seqidno:75、seqidno:76或seqidno:77的序列;和(ii)包含第二靶标杂交序列的第二hpv31扩增低聚物,所述第二靶标杂交序列为包含在seqidno:78的序列中的约15至约30个连续核苷酸并至少包括seqidno:79、seqidno:80或seqidno:81的序列;(c')进行体外核酸扩增反应,其中存在于所述样品中的任何hpv31靶标核酸均被用作产生hpv31扩增产物的模板;以及(d')检测所述hpv31扩增产物存在与否,从而指示所述样品中是否存在hpv31。27.根据项1或2所述的方法,其中所述第二hpv33扩增低聚物为还包含位于所述靶标杂交序列5'端的启动子序列的启动子引物或启动子提供者。28.根据项27所述的方法,其中所述第二hpv33低聚物的所述启动子序列为t7启动子序列。29.根据项28所述的方法,其中所述t7启动子序列具有以seqidno:82示出的序列。30.根据项26所述的方法,其中所述第二hpv31扩增低聚物为还包含位于所述靶标杂交序列5'端的启动子序列的启动子引物或启动子提供者。31.根据项30所述的方法,其中所述第二hpv31低聚物的所述启动子序列为t7启动子序列。32.根据项31所述的方法,其中所述t7启动子序列具有以seqidno:82示出的序列。33.一种用于检测样品中的人乳头瘤病毒33型(hpv33)靶标核酸的方法,所述方法包括:(a)提供样品,其中所述样品疑似含有hpv33;(b)将所述样品与低聚物组合接触,以便扩增hpv33核酸靶标区域,所述低聚物组合包括:(i)包含选自seqidno:1-seqidno:8的第一靶标杂交序列的第一hpv33扩增低聚物;和(b)包含选自seqidno:9-seqidno:16的第二靶标杂交序列的第二hpv33扩增低聚物;(c)进行体外核酸扩增反应,其中存在于所述样品中的任何hpv33靶标核酸均被用作产生hpv33扩增产物的模板;以及(d)检测所述hpv33扩增产物存在与否,从而指示所述样品中是否存在hpv33。34.根据项25所述的方法,其中所述样品还疑似含有hpv31型(hpv31)并且所述方法用于进一步检测所述样品中的hpv31靶标核酸,并且其中所述方法还包括:(b')将所述样品与低聚物组合接触,以便扩增hpv31核酸靶标区域,所述低聚物组合包括:(i)包含选自seqidno:25-seqidno:33的第一靶标杂交序列的第一hpv31扩增低聚物;和(b)包含选自seqidno:34-seqidno:41的第二靶标杂交序列的第二hpv31扩增低聚物;(c')进行体外核酸扩增反应,其中存在于所述样品中的任何hpv31靶标核酸均被用作产生hpv31扩增产物的模板;以及(d')检测所述hpv31扩增产物存在与否,从而指示所述样品中是否存在hpv31。35.根据项33或34所述的方法,其中所述第二hpv33扩增低聚物为还包含位于所述靶标杂交序列5'端的启动子序列的启动子引物或启动子提供者。36.根据项35所述的方法,其中所述第二hpv33低聚物的所述启动子序列为t7启动子序列。37.根据项36所述的方法,其中所述t7启动子序列具有以seqidno:82示出的序列。38.根据项37所述的方法,其中所述第二hpv33扩增低聚物具有选自seqidno:17-seqidno:24的序列。39.根据项34所述的方法,其中所述第二hpv31扩增低聚物为还包含位于所述靶标杂交序列5'端的启动子序列的启动子引物或启动子提供者。40.根据项39所述的方法,其中所述第二hpv31低聚物的所述启动子序列为t7启动子序列。41.根据项40所述的方法,其中所述t7启动子序列具有以seqidno:82示出的序列。42.根据项41所述的方法,其中所述第二hpv31扩增低聚物具有选自seqidno:42-seqidno:49的序列。43.根据项26或34所述的方法,其中所述步骤(c)与步骤(c')在同一扩增反应混合物中同时进行。44.根据项43所述的方法,其中步骤(d)与步骤(d')在同一检测反应混合物中同时进行。45.根据项25至44中任一项所述的方法,还包括在步骤(b)之前从所述样品中的其他组分纯化所述hpv33靶标核酸。46.根据项45所述的方法,其中所述纯化步骤包括将所述样品与至少一种hpv33特异性捕获探针低聚物接触,所述hpv33特异性捕获探针低聚物包含共价连接到结合于固定化探针的序列或部分的靶标杂交序列。47.根据项46所述的方法,其中所述捕获探针靶标杂交序列具有以seqidno:50示出的序列。48.根据项47所述的方法,其中所述hpv33特异性捕获探针低聚物具有以seqidno:51示出的序列。49.根据项26、30至32、34、以及39至42中任一项所述的方法,还包括在步骤(b')之前从所述样品中的其他组分纯化所述hpv31靶标核酸。50.根据项49所述的方法,其中所述纯化步骤包括将所述样品与至少一种hpv31特异性捕获探针低聚物接触,所述hpv31特异性捕获探针低聚物包含共价连接到结合于固定化探针的序列或部分的靶标杂交序列。51.根据项50所述的方法,其中所述捕获探针靶标杂交序列具有以seqidno:52示出的序列。52.根据项51所述的方法,其中所述hpv31特异性捕获探针低聚物具有以seqidno:53示出的序列。53.根据项25至52中任一项所述的方法,其中所述检测步骤(d)包括将步骤(c)的所述扩增反应与hpv33检测探针低聚物接触,所述hpv33检测探针低聚物被构造为在这样的条件下与所述hpv33扩增产物特异性杂交:凭借所述条件可确定所述hpv33扩增产物存在与否,从而指示所述样品中是否存在hpv33。54.根据项53所述的方法,其中所述hpv33检测探针包含靶标杂交序列,所述靶标杂交序列为约14至约35个核苷酸长并被构造为与包含在seqidno:83内从约核苷酸位置128至约核苷酸位置164的靶标序列特异性杂交。55.根据项54所述的方法,其中所述hpv33检测探针靶标杂交序列选自seqidno:54-seqidno:58。56.根据项53至55中任一项所述的方法,其中所述hpv33检测探针包含选自以下各项的标签:(a)化学发光标签;(b)荧光标签;(c)淬光剂;以及(d)(a)、(b)和(c)中的一者或多者的组合。57.根据项53至56中任一项所述的方法,其中所述检测步骤(d)在所述扩增步骤(c)期间进行。58.根据项57所述的方法,其中所述hpv33检测探针包含荧光标签、淬光剂、或这两者。59.根据项58所述的方法,其中所述hpv33检测探针为taqman检测探针或分子信标。60.根据项53至58中任一项所述的方法,其中所述hpv33检测探针还包含非靶标杂交序列。61.根据项60所述的方法,其中所述hpv33检测探针为发夹检测探针。62.根据项61所述的方法,其中所述发夹检测探针为分子信标或分子炬。63.根据项25至62中任一项所述的方法,其中步骤(c)处的所述扩增反应为等温扩增反应。64.根据项25至62中任一项所述的方法,其中步骤(c)处的所述扩增反应为pcr扩增反应。65.根据项63或64所述的方法,其中所述扩增反应为实时扩增反应。66.根据项26、30至32、34、39至42、以及49至52中任一项所述的方法,其中所述检测步骤(d')包括将步骤(c')的所述扩增反应与hpv31检测探针低聚物接触,所述hpv31检测探针低聚物被构造为在这样的条件下与所述hpv31扩增产物特异性杂交:凭借所述条件可确定所述hpv31扩增产物存在与否,从而指示所述样品中是否存在hpv31。67.根据项66所述的方法,其中所述hpv31检测探针包含靶标杂交序列,所述靶标杂交序列为约14至约40个核苷酸长并被构造为与包含在seqidno:84内从约核苷酸位置675至约核苷酸位置735的靶标序列特异性杂交。68.根据项67所述的方法,其中所述hpv31检测探针靶标杂交序列选自seqidno:59-seqidno:65。69.根据项66至68中任一项所述的方法,其中所述hpv31检测探针包含选自以下各项的标签:(a)化学发光标签;(b)荧光标签;(c)淬光剂;以及(d)(a)、(b)和(c)中的一者或多者的组合。70.根据项66至69中任一项所述的方法,其中所述检测步骤(d')在所述扩增步骤(c')期间进行。71.根据项70所述的方法,其中所述hpv31检测探针包含荧光标签、淬光剂、或这两者。72.根据项71所述的方法,其中所述hpv31检测探针为taqman检测探针或分子信标。73.根据项66至71中任一项所述的方法,其中所述hpv31检测探针还包含非靶标杂交序列。74.根据项73所述的方法,其中所述hpv31检测探针为发夹检测探针。75.根据项74所述的方法,其中所述发夹检测探针为分子信标或分子炬。76.根据项25至75中任一项所述的方法,其中步骤(c')处的所述扩增反应为等温扩增反应。77.根据项25至75中任一项所述的方法,其中步骤(c')处的所述扩增反应为pcr扩增反应。78.根据项76或77所述的方法,其中所述扩增反应为实时扩增反应。79.根据项26所述的方法,其中所述检测步骤(d)包括将步骤(c)的所述扩增反应与hpv33检测探针低聚物接触,所述hpv33检测探针低聚物被构造为在这样的条件下与所述hpv33扩增产物特异性杂交:凭借所述条件可确定所述hpv33扩增产物存在与否,从而指示所述样品中是否存在hpv33;其中所述检测步骤(d')包括将步骤(c')的所述扩增反应与hpv31检测探针低聚物接触,所述hpv31检测探针低聚物被构造为在这样的条件下与所述hpv31扩增产物特异性杂交:凭借所述条件可确定所述hpv31扩增产物存在与否,从而指示所述样品中是否存在hpv31;其中步骤(c)与步骤(c')在同一扩增反应混合物中同时进行,并且步骤(d)与步骤(d')在同一检测反应混合物中同时进行;并且其中所述hpv33检测探针低聚物和所述hpv31检测探针低聚物被差异性标记。80.根据项79所述的方法,其中所述hpv33检测探针低聚物和所述hpv31检测探针低聚物中的每一者包含独立地选自(a)化学发光标签和(b)荧光标签的标签。81.根据项79所述的方法,其中所述hpv33检测探针低聚物和所述hpv31检测探针低聚物中的每一者包含化学发光标签。82.根据项81所述的方法,其中用于所述hpv33检测探针低聚物和所述hpv31检测探针低聚物的所述化学发光标签通过足以区分hpv33特异性化学发光信号和hpv31特异性化学发光信号的不同光发射动力学来表征。83.根据项82所述的方法,其中用于所述hpv33检测探针低聚物和所述hpv31检测探针低聚物的所述化学发光标签中的每一者包含吖啶酯(ae)。84.根据项79至83中任一项所述的方法,其中所述第二hpv33扩增低聚物为还包含位于所述靶标杂交序列5'端的启动子序列的启动子引物或启动子提供者。85.根据项84所述的方法,其中所述第二hpv33低聚物的所述启动子序列为t7启动子序列。86.根据项85所述的方法,其中所述t7启动子序列具有以seqidno:82示出的序列。87.根据项79至86中任一项所述的方法,其中所述第二hpv31扩增低聚物为还包含位于所述靶标杂交序列5'端的启动子序列的启动子引物或启动子提供者。88.根据项87所述的方法,其中所述第二hpv31低聚物的所述启动子序列为t7启动子序列。89.根据项88所述的方法,其中所述t7启动子序列具有以seqidno:82示出的序列。90.根据项79至89中任一项所述的方法,其中所述hpv33检测探针包含靶标杂交序列,所述靶标杂交序列为约14至约35个核苷酸长并被构造为与包含在seqidno:83内从约核苷酸位置128至约核苷酸位置164的靶标序列特异性杂交。91.根据项79至90中任一项所述的方法,其中所述hpv31检测探针包含靶标杂交序列,所述靶标杂交序列为约14至约40个核苷酸长并被构造为与包含在seqidno:84内从约核苷酸位置675至约核苷酸位置735的靶标序列特异性杂交。在参考本发明的以下具体实施方式和附图后,本发明的这些和其他方面将变得显而易见。定义除非另有定义,否则本文所用的所有技术和科学术语具有与跟所描述的方法和组合物有关的领域中的普通技术人员所通常理解相同的含义。如本文所用,以下术语和短语具有归属它们的含义,除非另有规定。除非上下文另有明确说明,否则术语“一个”、“一种”和“该”包括多个指代物。例如,如本文所用的“核酸”应理解为代表一个或多个核酸。同样地,术语“一个”(或“一种”)、“一个或多个”以及“至少一个”在本文中可互换使用。“样品”或“生物样品”是指源自可能含有人乳头瘤病毒(hpv)靶标核酸的活人或死人的任何组织或材料,包括例如喉、口腔、口咽、扁桃体或食道组织、呼吸道组织或渗出液的样品,宫颈或肛门拭子样品,活检组织(包括淋巴结)、胃肠组织、粪便、尿液、精液、痰液、外周血、血浆、血清或其他体液、组织或材料。可对生物样品进行处理以便用物理或机械方式破坏组织或细胞结构,从而使细胞内组分释放到溶液中,所述溶液还可包含酶、缓冲液、盐、洗涤剂等,它们用于使用标准方法制备供分析的生物样品。另外,样品可包括处理过的样品,诸如使样品通过或穿过过滤装置,或在离心后,或通过粘附到培养基、基质或载体而获得的那些。样品还可包括源自人的交联组织或材料,诸如包含在例如bdsurepath保藏液(新泽西州富兰克林湖的百克顿-迪金森公司(becton,dickinsonandcompany,franklinlakes,nj))之类的培养基中的样品,或福尔马林固定的石蜡包埋样品。样品还可包括源自人的组织或材料并且悬浮在诸如thinprep细胞学试剂(马萨诸塞州贝德福德的豪洛捷股份有限公司(hologic,inc.,bedford,ma))之类的细胞学培养基中。“核酸”是指包含两个或更多个共价键合的核苷或核苷类似物的多聚体化合物,这些核苷或核苷类似物具有含氮杂环碱基或碱基类似物,其中所述核苷通过磷酸二酯键或其他键连接在一起形成多核苷酸。核酸包括rna、dna、或嵌合dna-rna聚合物或寡核苷酸,以及它们的类似物。核酸“主链”可由多种键构成,包括糖-磷酸二酯键、肽-核酸键(“肽核酸”或pna中的肽-核酸键,参见例如国际专利申请公布no.wo95/32305)、硫代磷酸酯键、甲基膦酸酯键或它们的组合中的一种或多种。核酸的糖部分可以是核糖或脱氧核糖,或者具有已知取代诸如2’-甲氧基取代和2’-卤化取代(例如,2’-f)的类似化合物。含氮碱基可以是常规碱基(a、g、c、t、u)、其类似物(例如肌苷、5-甲基异胞嘧啶、异鸟嘌呤;参见例如thebiochemistryofthenucleicacids5-36,adams等,ed.,11thed.,1992(《核酸的生物化学》,第5-36页,adams等编辑,第11版,1992年);abraham等,2007,biotechniques43:617-24(abraham等,2007年,《生物技术》,第43卷,第617-624页)),其包括嘌呤或嘧啶碱基的衍生物(例如n4-甲基脱氧鸟苷、去氮或氮杂嘌呤、去氮或氮杂嘧啶、在5或6位具有取代基团的嘧啶碱基,在2、6和/或8位具有改变的或置换取代基的嘌呤碱基,诸如2-氨基-6-甲氨基嘌呤、o6-甲基鸟嘌呤、4-硫代嘧啶、4-氨基嘧啶、4-二甲基肼嘧啶和o4-烷基嘧啶,以及吡唑并化合物,诸如未取代或3-取代的吡唑并[3,4-d]嘧啶;美国专利no.5,378,825、no.6,949,367,以及国际专利申请公布no.wo93/13121,它们各自以引用方式并入本文)。核酸可包含“脱碱基”残基,其中主链的一个或多个残基不包含含氮碱基(参见例如美国专利no.5,585,481,其以引用方式并入本文)。核酸可仅包含如存在于rna和dna中的常规糖、碱基和键,或者可包含常规的组分和取代(例如,由2’-甲氧基主链连接的常规碱基,或包含常规碱基与一种或多种碱基类似物的混合物的核酸)。核酸可包括“锁核酸”(lna),其中一个或多个核苷酸单体具有锁定在rna模拟糖构象中的双环呋喃糖单元,该构象增强了对单链rna(ssrna)、单链dna(ssdna)或双链dna(dsdna)中的互补序列的杂交亲和力(vester等,biochemistry43:13233-41,2004(vester等,《生物化学》,第43卷,第13233-13241页,2004年),其以引用方式并入本文)。核酸可包含用于改变核酸的功能或行为的修饰碱基,例如,添加3’-末端双脱氧核苷酸以阻止另外的核苷酸被添加至核酸。用于体外制备核酸的合成方法在本领域中是众所周知的,但也可使用常规技术从天然来源纯化核酸。如本文所用的术语“多核苷酸”表示核酸链。在本申请通篇中,核酸由5’-端至3’-端指示。标准核酸(例如dna和rna)通常以“3’-至-5’”的方式合成,即通过将核苷酸添加至增长核酸的5’-端而合成。如本文所用的“核苷酸”是由磷酸基团、5-碳糖和含氮碱基组成的核酸亚单元。存在于rna中的5-碳糖为核糖。在dna中,5-碳糖为2’-脱氧核糖。该术语还包括此类亚单元的类似物,诸如在核糖的2’位处的甲氧基(2’-o-me)。如本文所用,含有“t”残基的甲氧基寡核苷酸在核糖部分的2’位处具有甲氧基,并且在核苷酸的碱基位置处具有尿嘧啶。如本文所用的“非核苷酸单元”为未显著地参与聚合物的杂交的单元。此类单元不应(例如)参与与核苷酸的任何显著氢键结合,并且将排除具有五种核苷酸碱基或它们的类似物中的一种作为组分的单元。如本文所用的“靶标核酸”为包含待扩增的靶标序列的核酸。靶标核酸可以是如本文所述的dna或rna,并且可以是单链或双链的。除靶标序列之外,靶标核酸还可包含可能未被扩增的其他序列。所谓“分离的”,意指包含靶标核酸的样品是从其天然环境中提取的,但该术语并不意味着任何程度的纯化。如本文所用的术语“靶标序列”是指靶标核酸的待扩增和/或检测的特定核苷酸序列。“靶标序列”包括在扩增过程(例如,tma)期间寡核苷酸(例如,引发性寡核苷酸和/或启动子寡核苷酸)复合至其上的复合序列。当靶标核酸最初为单链时,术语“靶标序列”还将指与靶标核酸中存在的“靶标序列”互补的序列。当靶标核酸最初为双链时,术语“靶标序列”是指有义(+)链和反义(-)链两者。“靶标杂交序列”在本文中用于指被构造为与靶标核酸序列杂交的低聚物的部分。优选地,靶标杂交序列被构造为与靶标核酸序列特异性杂交。靶标杂交序列可与它们被构造为与其进行杂交的靶标序列的部分100%互补,但未必如此。靶标杂交序列还可包含相对于靶标序列插入、缺失和/或取代的核苷酸残基。可能出现靶标杂交序列与靶标序列的互补性小于100%,例如,当靶标核酸为一个物种内的多个菌株时。应当理解,将靶标杂交序列构造为与靶标核酸的互补性小于100%存在其他原因。除非上下文另有明确规定,否则本文参考特定序列(例如,参考seqidno:83或seqidno:84内的区域)定义的低聚物靶标杂交序列也应理解为包含其功能性互补序列。因此,例如,当第一扩增低聚物和第二扩增低聚物的靶标杂交区域参考分别对应于靶标核酸的有义链和反义链的特定序列定义时,应当理解,所述扩增低聚物组合可包括具有靶标杂交序列的第一扩增低聚物和第二扩增低聚物的功能性组合,所述靶标杂交序列为特定参考序列的相应互补序列。相似地,再举个例子,当用于检测探针低聚物的靶标杂交序列参考特定序列定义时,应当理解,检测探针可包含具有靶标杂交序列的对应检测探针低聚物,所述靶标杂交序列为特定参考序列的互补序列;或者当检测探针低聚物由其与特定序列杂交的构型定义时,应当理解,检测探针可包含具有靶标杂交序列的对应检测探针低聚物,所述靶标杂交序列被构造为与特定参考序列的互补序列杂交。如本文参考hpv核酸的区域所用,术语“靶向序列”是指寡核苷酸以本文所述的允许扩增和检测的方式与靶标序列杂交的过程。在一个优选的实施例中,寡核苷酸与靶标hpv核酸序列互补并且不包含错配。在另一个优选的实施例中,寡核苷酸与靶标hpv核酸序列互补,但包含1、2、3、4或5个错配。优选地,与hpv核酸序列杂交的寡核苷酸包含至少10个至多达50个与靶标序列互补的核苷酸。应当理解,至少10个和多达50个是闭区间,使得10、50以及这两者间的每个整数都包括在内。优选地,低聚物与靶标序列特异性杂交。术语“被构造为”代表参考寡核苷酸靶标杂交序列的多核苷酸序列构型的实际布置方式。例如,被构造为由靶标序列产生指定扩增子的扩增低聚物具有与靶标序列杂交的多核苷酸序列,并且可用于扩增反应以产生扩增子。又如,被构造为与靶标序列特异性杂交的寡核苷酸具有在严格杂交条件下与参考序列特异性杂交的多核苷酸序列。如本文所用的术语“被构造为与……特异性杂交”意指扩增寡核苷酸、检测探针或其他寡核苷酸的靶标杂交区域被设计成具有可靶向参考hpv靶标区域的序列的多核苷酸序列。这种寡核苷酸不仅仅限于靶向该序列,而且可在试剂盒或方法中用作靶向hpv靶标核酸的组合物。所述寡核苷酸被设计成充当用于从样品扩增和检测hpv的测定法的组成部分,因此被设计成在通常存在于测试样品中的其他核酸的存在下靶向hpv。如本领域中所理解的,“与……特异性杂交”并不意味着唯一地与……杂交,因为可能发生一些小程度的与非靶标核酸的杂交。相反,“与……特异性杂交”意指寡核苷酸被构造为在测定法中起到主要与靶标杂交的作用,使得样品中靶标核酸的准确检测结果可被确定。术语“被构造为”代表扩增寡核苷酸靶标杂交序列的多核苷酸序列构型的实际布置方式。如本文参考hpv靶标核酸所用,术语“片段”是指一段连续的核酸,其中该片段中的连续核苷酸的数目小于整个靶标核酸的该数目。如本文所用,术语“区域”是指核酸的一部分,其中所述部分小于整个核酸。例如,当所提到的核酸为寡核苷酸启动子引物时,术语“区域”可用于指整个寡核苷酸的较小启动子部分。相似地,也仅以举例的方式,当核酸为hpv基因组的hpve6和/或e7片段(例如,e6/e7mrna转录物)时,术语“区域”可用于指核酸的较小区域,其中该较小区域被本发明的一种或多种寡核苷酸靶向。作为另一个非限制性例子,当所提到的核酸为扩增子时,术语“区域”可用于指被鉴定以便通过探针的靶标杂交序列进行杂交的较小核苷酸序列。可互换的术语“低聚物”、“寡聚物”和“寡核苷酸”是指通常具有小于1,000个核苷酸(nt)残基的核酸,包括下限为约5个nt残基且上限为约500至900个nt残基的范围内的聚合物。在一些实施例中,寡核苷酸在下限为约12至15个nt且上限为约50至600个nt的尺寸范围内,而其他实施例在下限为约15至20个nt且上限为约22至100个nt的范围内。寡核苷酸可从天然存在的来源纯化,或者可使用多种熟知的酶法或化学方法中的任一种来合成。术语“寡核苷酸”不表示试剂的任何特定功能;相反,其一般用于涵盖本文所述的所有此类试剂。寡核苷酸可发挥各种不同的功能。例如,如果它特异性地针对互补链且能够与互补链杂交,并可在核酸聚合酶的存在下进一步延伸,那么其可充当引物;如果它包含rna聚合酶所识别的序列并且允许转录,那么其可充当引物并提供启动子(例如,t7引物);并且如果它能够与靶标核酸或其扩增子杂交,并进一步提供可检测的部分(例如,吖啶酯化合物),那么其可用于检测靶标核酸。如本文所用,寡核苷酸“基本上对应于”指定参考核酸序列意指寡核苷酸与参考核酸序列足够相似,使得该寡核苷酸具有与参考核酸序列相似的杂交特性,因为其在严格杂交条件下会与相同的靶标核酸序列杂交。本领域的技术人员将理解,“基本上对应的寡核苷酸”可不同于参考序列,且仍与相同的靶标核酸序列杂交。还应当理解,除非上下文另有明确规定,否则与第二核酸相对应的第一核酸包含其rna和dna,并包含其互补序列。来自核酸的该变型可以依据序列内的相同碱基的百分比或者探针或引物与其靶标序列之间的完全互补碱基的百分比来陈述。因此,在某些实施例中,如果碱基同一性或互补性的这些百分比为100%至约80%,那么寡核苷酸“基本上对应于”参考核酸序列。在优选的实施例中,该百分比为100%至约85%。在更优选的实施例中,该百分比为100%至约90%;在其他优选的实施例中,该百分比为100%至约95%。类似地,核酸或扩增核酸的区域在本文中可被称为与参考核酸序列相对应。本领域的技术人员将理解,在各种互补性百分比下可能需要对杂交条件进行各种修改以允许与特定靶标序列杂交,而不会产生不可接受程度的非特异性杂交。如本文所用,“阻断部分”是用于“阻断”寡核苷酸或其他核酸的3'-端以使得其不能被核酸聚合酶有效延伸的物质。不旨在被核酸聚合酶延伸的低聚物可包含取代3'oh以防止低聚物在扩增反应中发生酶介导的延伸的阻断基团。例如,扩增期间存在的被阻断的扩增低聚物和/或检测探针可能不具有功能性3'oh,而是包含位于3'端处或附近的一个或多个阻断基团。在一些实施例中,阻断基团靠近3'端,并且可能在3'端的五个残基内,而且足够大以限制聚合酶结合到低聚物。在其他实施例中,阻断基团共价连接到3'端。可使用许多不同的化学基团来阻断3'端,例如烷基、非核苷酸接头、烷烃-二醇双脱氧核苷酸残基和虫草素。“扩增低聚物”是这样的低聚物,该低聚物的至少3'-端与靶标核酸互补,其与靶标核酸或其互补序列杂交并参与核酸扩增反应。扩增低聚物的例子是与靶标核酸杂交并包含在扩增过程中被聚合酶延伸的3'oh端的“引物”。扩增低聚物的另一个例子是不被聚合酶延伸(例如,因为其具有被阻断的3'端)、但参与或促进扩增的低聚物。例如,扩增寡核苷酸的5'区域可包含不与靶标核酸互补的启动子序列(其可称为“启动子引物”或“启动子提供者”)。本领域的技术人员将理解,充当引物的扩增低聚物可被修饰成包含5'启动子序列,并因此充当启动子引物。结合被阻断的3'端进一步修饰了启动子引物,该启动子引物现在能够与靶标核酸杂交并提供用来引发转录的上游启动子序列,但是不提供使寡聚物延伸的引物。这种经修饰的寡聚物在本文中称为“启动子提供者”低聚物。扩增寡核苷酸的尺寸范围包括长度为约10至约70个nt(不包括任何启动子序列或聚腺苷酸尾),并且包含至少约10个连续碱基、或甚至至少12个与靶标核酸序列(或其互补链)的区域互补的连续碱基的那些范围。所述连续碱基与扩增低聚物结合到其上的靶标序列至少80%互补、或至少90%互补、或完全互补。扩增低聚物可任选地包含经修饰的核苷酸或类似物,或者参与扩增反应但不与靶标核酸或模板序列互补或不包含在靶标核酸或模板序列内的另外核苷酸。应当理解,当提及寡核苷酸、扩增子或其他核酸的长度的范围时,该范围包括所有整数(例如,15-27个连续核苷酸长包括15、16、17、18、19、20、21、22、23、24、25、26和27个连续核苷酸)。如本文所用,“启动子”是被dna依赖性rna聚合酶(“转录酶”)识别为结合至核酸并在特定位点处开始rna转录的信号的特定核酸序列。如本文所用,“启动子提供者”或“提供者”是指包括第一区域和第二区域并且被修饰以便防止引发从其3'-端开始的dna合成的寡核苷酸。启动子提供者寡核苷酸的“第一区域”包含与dna模板杂交的碱基序列,其中所述杂交序列位于3'端,但不一定与启动子区域相邻。启动子寡核苷酸的杂交部分通常为至少10个核苷酸长,并且可延伸最多至50或更多个核苷酸长。“第二区域”包含rna聚合酶的启动子序列。对启动子寡核苷酸进行工程改造,使得其不能被rna依赖性dna聚合酶或dna依赖性dna聚合酶(例如逆转录酶)延伸,优选地如上所述在其3'-端处包含阻断部分。如本文所提及的,“t7提供者”是提供被t7rna聚合酶识别的寡核苷酸序列的被阻断启动子提供者寡核苷酸。“终止寡核苷酸”是包含碱基序列的寡核苷酸,该碱基序列与靶标核酸内位于靶标区域5'端附近的序列基本上互补,以便“终止”包含引发性寡核苷酸的新生核酸的引物延伸,从而提供新生核酸链的限定3'-端。终止寡核苷酸被设计成在足以获得新生核酸链的所需3'-端的位置处与靶标核酸杂交。取决于终止寡核苷酸的设计,其定位具有灵活性。终止寡核苷酸可以是经修饰或未经修饰的。在某些实施例中,使用至少一种或多种2'-o-me核糖核苷酸合成终止寡核苷酸。这些经修饰的核苷酸已表现出互补双链体的更高热稳定性。2'-o-me核糖核苷酸还起到提高寡核苷酸对核酸外切酶的抗性的作用,从而延长经修饰的寡核苷酸的半衰期。(参见例如majlessi等,nucleicacidsres.26:2224-9,1988(majlessi等,《核酸研究》,第26卷,第2224-2229页,1988年),其以引用方式并入本文。)除了2'-o-me核糖核苷酸之外或代替2'-o-me核糖核苷酸,可以使用如本文别处所述的其他修饰。例如,终止寡核苷酸可包含pna或lna。(参见例如petersen等,j.mol.recognit.13:44-53,2000(petersen等,《分子识别杂志》,第13卷,第44-53页,2000年,其以引用方式并入本文。)本发明的终止寡核苷酸通常在其3'-端处包含阻断部分以防止延伸。终止寡核苷酸还可包含接合到寡核苷酸以便终止由聚合酶引起的新生核酸链进一步延伸的蛋白质或肽。本发明的终止寡核苷酸通常为至少10个碱基长,并且可延伸至最多15、20、25、30、35、40、50或更多个核苷酸长。虽然终止寡核苷酸通常或必定包含3'-阻断部分,但“3'-阻断的”寡核苷酸不一定是终止寡核苷酸。“扩增”是指用于获得靶标核酸序列或其互补序列或其片段的多个拷贝的任何已知程序。所述多个拷贝可被称为扩增子或扩增产物。“片段”的扩增是指包含少于完整靶标核酸或其互补序列的经扩增核酸的制备,例如通过使用与靶标核酸的内部位置杂交并且从该内部位置引发聚合反应的扩增寡核苷酸来制备。已知的扩增方法包括例如复制酶介导的扩增、聚合酶链反应(pcr)、连接酶链反应(lcr)、链置换扩增(sda),以及转录介导或转录相关的扩增。复制酶介导的扩增使用自我复制rna分子,以及复制酶诸如qb-复制酶(参见例如美国专利no.4,786,600,其以引用方式并入本文)。pcr扩增使用dna聚合酶、引物对和热循环来合成dsdna的或来自cdna的两条互补链的多个拷贝(参见例如美国专利no.4,683,195、no.4,683,202、和no.4,800,159,它们各自以引用方式并入本文)。lcr扩增使用四个或更多个不同的寡核苷酸,通过使用多个循环的杂交、连接和变性来扩增靶标及其互补链(参见例如美国专利no.5,427,930和no.5,516,663,它们各自以引用方式并入本文)。sda使用含有限制性内切核酸酶(该内切核酸酶将包含靶标序列的半修饰dna双链体的一条链打开缺口)的识别位点的引物,借此扩增以一系列引物延伸和链置换步骤发生(参见例如美国专利no.5,422,252、no.5,547,861、和no.5,648,211,它们各自以引用方式并入本文)。“转录相关的扩增”或“转录介导的扩增”(tma)是指使用rna聚合酶从核酸模板产生多个rna转录物的核酸扩增。这些方法通常采用rna聚合酶、dna聚合酶、脱氧核糖核苷三磷酸、核糖核苷三磷酸,以及包含启动子序列的模板互补寡核苷酸,并且任选地可包含一种或多种其他寡核苷酸。tma方法和单引物转录相关的扩增方法是如本文所述的用于检测hpv靶标序列的扩增方法的实施例。转录相关的扩增的变型形式是本领域熟知的,如此前详细公开的那些(参见例如美国专利no.4,868,105、no.5,124,246、no.5,130,238、no.5,399,491、no.5,437,990、no.5,554,516、和no.7,374,885,以及国际专利申请公布no.wo88/01302、no.wo88/10315,和no.wo95/03430;它们各自以引用方式并入本文)。本领域的普通技术人员将会知道,所公开的组合物可基于用聚合酶延伸低聚物序列而用于扩增方法中。如本文所用,术语“实时tma”是指通过实时检测手段监测的靶标核酸的单引物转录介导的扩增(“tma”)。如本文所用的术语“扩增子”或术语“扩增产物”是指在扩增程序期间产生的与包含在靶标序列内的序列互补或同源的核酸分子。扩增子的互补或同源序列有时在本文中称为“靶标特异性序列”。使用本发明的扩增低聚物产生的扩增子可包含非靶标特异性序列。扩增子可以是双链或单链的,并且可包括dna、rna或这两者。例如,dna依赖性rna聚合酶在转录介导的扩增程序期间从双链dna转录单链扩增子。这些单链扩增子是rna扩增子,并且可以是双链复合物的任一条链,这取决于扩增低聚物的构造方式。因此,扩增子可以是单链rna。rna依赖性dna聚合酶合成与rna模板互补的dna链。因此,扩增子可以是双链dna和rna杂交体。rna依赖性dna聚合酶通常包括rna酶活性,或者与降解rna链的rna酶结合使用。因此,扩增子可以是单链dna。rna依赖性dna聚合酶和dna依赖性dna聚合酶从dna模板合成互补的dna链。因此,扩增子可以是双链dna。rna依赖性rna聚合酶从rna模板合成rna。因此,扩增子可以是双链rna。dna依赖性rna聚合酶从双链dna模板合成rna,也称为转录。因此,扩增子可以是单链rna。扩增子和用于产生扩增子的方法是本领域的技术人员已知的。本文为方便起见,rna的单链或dna的单链可表示由本发明的扩增低聚物组合产生的扩增子。这种陈述并不意味着将扩增子局限为所示的陈述。掌握本公开内容的熟练技术人员将使用扩增低聚物和聚合酶来产生众多类型的扩增子中的任一种,它们全部都在本发明的精神和范围内。如本文所用,“非靶标特异性序列”是指低聚物序列的区域,其中所述区域在标准杂交条件下不与靶标序列稳定地杂交。具有非靶标特异性序列的低聚物包括但不限于启动子引物和分子信标。扩增低聚物可含有不与靶标或模板序列互补的序列;例如,引物的5’区域可包含不与靶标核酸互补的启动子序列(称为“启动子引物”)。本领域的技术人员将理解,充当引物的扩增低聚物可被修饰成包含5’启动子序列,并因此充当启动子引物。类似地,启动子引物可通过移除启动子序列或在没有启动子序列的情况下合成来进行修饰并且仍充当引物。3’阻断的扩增低聚物可提供启动子序列并且充当聚合模板(称为“启动子提供者”)。因此,由扩增低聚物成员诸如启动子引物产生的扩增子将包含靶标特异性序列和非靶标特异性序列。“检测探针”、“检测寡核苷酸”和“检测探针低聚物”可互换使用以指这样的核酸低聚物,该核酸低聚物在促进杂交以允许检测靶标序列或经扩增核酸的条件下与核酸或经扩增核酸中的靶标序列特异性杂交。检测可以是直接检测(例如,探针直接与其靶标序列杂交)或间接检测(例如,探针经由中间分子结构连接至其靶标)。检测探针可以是dna、rna、其类似物或它们的组合,并且它们可被标记或未被标记。检测探针还可包含另选的主链键,诸如2’-o-甲基键。检测探针的“靶标序列”通常是指较大核酸序列内通过标准碱基配对与探针低聚物的至少一部分特异性杂交的较小核酸序列区域。检测探针可包含靶标特异性序列和有助于探针的三维构象的其他序列(参见例如美国专利no.5,118,801、no.5,312,728、no.6,849,412、no.6,835,542、no.6,534,274和no.6,361,945,以及美国专利申请公布no.20060068417;它们各自以引用方式并入本文)。所谓“稳定”或“对于检测稳定”,意指反应混合物的温度比核酸双链体的解链温度低至少2℃。如本文所用,“标签”是指直接或间接地接合到探针的可被检测到或产生可检测信号的部分或化合物。直接标记可通过将标签连接到探针的键或相互作用进行,所述键或相互作用包括共价键或非共价相互作用,例如氢键、疏水和离子相互作用,或形成螯合物或配位复合物。间接标记可通过使用桥联部分或“接头”进行,所述桥联部分或“接头”诸如结合对成员、抗体或另外的低聚物,其要么被直接标记要么被间接标记并且可以放大可检测信号。标签包含任何可检测部分,诸如放射性核素、配体(例如,生物素、亲和素)、酶或酶底物、反应性基团或发色团(例如,赋予可检测颜色的染料、粒子或小珠)、发光化合物(例如生物发光标签、磷光标签或化学发光标签)或者荧光团。标签在均相测定法中可以是可检测的,在均相测定法中,混合物中的结合的被标记探针表现出与未结合的被标记探针不同的可检测变化,例如不稳定性或有差别的降解性质。“均相可检测标签”可以在未将结合形式的标签或被标记探针从未结合形式的标签或被标记探针物理移除的情况下进行检测(参见例如美国专利no.5,283,174、no.5,656,207、和no.5,658,737,它们各自以引用方式并入本文)。标签包含化学发光化合物,例如吖啶酯(“ae”)化合物,其包括标准的ae及衍生物(参见例如美国专利no.5,656,207、no.5,658,737、和no.5,639,604,它们各自以引用方式并入本文)。合成标签、将标签连接到核酸以及检测标签的方法是熟知的。(参见例如sambrook等,molecularcloning,alaboratorymanual,2nded.(coldspringharborlaboratorypress,coldspringhabor,ny,1989),chapter10(sambrook等,《分子克隆:实验室手册》,第2版(冷泉港实验室出版社,纽约冷泉港,1989年,第10章),其以引用方式并入本文。还可参见美国专利no.5,658,737、no.5,656,207、no.5,547,842、no.5,283,174和no.4,581,333,它们各自以引用方式并入本文)。不止一个标签和不止一种类型的标签可存在于特定探针上,或者检测可使用探针的混合物,其中每个探针用产生可检测信号的化合物标记(参见例如美国专利no.6,180,340和no.6,350,579,它们各自以引用方式并入本文)。“捕获探针”、“捕获寡核苷酸”和“捕获探针低聚物”可互换使用以指这样的核酸低聚物,该核酸低聚物通过标准碱基配对与靶标核酸中的靶标序列特异性杂交并且接合到固定化探针上的结合伴侣以将靶标核酸捕获到载体上。捕获低聚物的一个例子包括两个结合区域:通常处于同一低聚物上的序列结合区域(例如,靶标特异性部分)和固定化探针结合区域,但这两个区域可能存在于通过一个或多个接头接合在一起的两个不同的低聚物上。捕获低聚物的另一个实施例使用包含随机或非随机聚gu序列、聚gt序列或聚u序列的靶标序列结合区域来非特异性地结合到靶标核酸并将其连接到载体上的固定化探针。如本文所用,“固定化寡核苷酸”、“固定化探针”或“固定化核酸”是指将捕获低聚物直接或间接地接合到载体的核酸结合伴侣。接合到载体的固定化探针有助于样品中被捕获探针结合的靶标与未结合的材料分离。固定化探针的一个实施例为接合到载体的低聚物,其有助于样品中被结合的靶标序列与未结合的材料分离。载体可包含已知的材料,诸如游离在溶液中的基质和粒子,其可由硝化纤维、尼龙、玻璃、聚丙烯酸酯、混合聚合物、聚苯乙烯、硅烷、聚丙烯、金属或其他组合物制成,其中的一个实施例为可被磁性吸引的粒子。载体可以是单分散磁性球体(例如,均一尺寸±5%),固定化探针直接地(通过共价键、螯合或离子相互作用)或间接地(通过一个或多个接头)接合到其上,其中探针与载体之间的键合或相互作用在杂交条件期间是稳定的。所谓“互补”,意指两种单链核酸的相似区域或同一单链核酸的不同区域的核苷酸序列具有这样的核苷酸碱基组成,该核苷酸碱基组成允许单链区域在严格杂交条件或扩增条件下在稳定的双链氢键合区域中杂交在一起。彼此杂交的序列可通过标准的核酸碱基配对(例g:c、a:t或a:u配对)与预期的靶标序列完全互补或部分互补。所谓“充分互补”,意指能够通过一系列互补碱基之间的氢键结合与另一个序列杂交的连续序列,其可通过标准的碱基配对在序列中的每一位置互补,或可含有一个或多个非互补残基,包括脱碱基残基。充分互补的连续序列通常与低聚物预期特异性杂交的序列至少80%、或至少90%互补。“充分互补”的序列允许核酸低聚物与它的靶标序列在适当的杂交条件下稳定杂交,即使这些序列并不完全互补。当一个单链区域的核苷酸的连续序列能够与另一个单链区域的核苷酸的类似序列形成一系列“规范的”氢键合的碱基对,使得a与u或t配对且c与g配对时,所述核苷酸序列是“完全”互补的(参见例如sambrook等,molecularcloning,alaboratorymanual,2nded.(coldspringharborlaboratorypress,coldspringharbor,ny,1989)(sambrook等,《分子克隆:实验室手册》,第2版,冷泉港实验室出版社,纽约冷泉港,1989年)中的§§1.90-1.91、7.37-7.57、9.47-9.51和11.47-11.57,特别是§§9.50-9.51、11.12-11.13、11.45-11.47和11.55-11.57,该文献以引用方式并入本文)。应当理解,同一性百分比的范围包括所有整数和小数(例如,至少90%包括90%、91%、93.5%、97.687%等)。所谓“优先杂交”或“特异性杂交”意指在严格的杂交测定法条件下,探针与它们的靶标序列或其复制物杂交,以形成稳定的探针:靶标杂交体,而同时稳定的探针:非靶标杂交体的形成最少化。因此,探针与靶标序列或其复制物杂交的程度比其与非靶标序列杂交的程度充分更大,以使本领域的普通技术人员能够准确地定量在扩增期间形成的靶标序列的rna复制物或互补dna(cdna)。适当的杂交条件在本领域中是众所周知的,可根据序列组成进行预测,或可以通过使用常规测试方法来确定(参见例如sambrook等,molecularcloning,alaboratorymanual,2nded.(coldspringharborlaboratorypress,coldspringharbor,ny,1989)(sambrook等,《分子克隆:实验室手册》,第2版,冷泉港实验室出版社,纽约冷泉港,1989年)中的§§1.90-1.91、7.37-7.57、9.47-9.51和11.47-11.57,特别是§§9.50-9.51、11.12-11.13、11.45-11.47和11.55-11.57,该文献以引用方式并入本文)。所谓“核酸杂交体”、“杂交体”或“双链体”意指包含双链氢键合区域的核酸结构,其中每条链与另一条链互补,并且其中所述区域在严格的杂交条件下足够稳定以便通过包括但不限于以下的方法检测:化学发光或荧光检测、放射自显影或凝胶电泳。此类杂交体可包括rna:rna、rna:dna或dna:dna双链体分子。“样品制备”是指为了对存在于样品中的hpv核酸进行后续扩增和/或检测而处理样品的任何步骤或方法。样品可以是多种组分的复杂混合物,在这些组分中,靶标核酸为少数组分。样品制备可包括从较大样品体积浓缩组分(诸如微生物或核酸)的任何已知方法,诸如通过从较大体积样品过滤气载或水载的粒子,或者通过使用标准的微生物学方法从样品分离微生物。样品制备可包括对细胞组分的物理破坏和/或化学裂解以使细胞内组分释放进实质上水性或有机的相中并移除碎片,诸如通过使用过滤、离心或吸附。样品制备可包括使用选择性地或非特异性地捕获靶标核酸并将其与其他样品组分分离的核酸寡核苷酸(例如,如美国专利no.6,110,678和国际专利申请公布no.wo2008/016988中所述,它们各自以引用方式并入本文)。“分离”或“纯化”意指将样品的一种或多种组分从其他样品组分中移除或分离。样品组分包括通常在总体上水性的溶液相中的靶标核酸,其还可包括细胞片段、蛋白质、碳水化合物、脂质和其他核酸。分离或纯化将至少70%、或至少80%、或至少95%的靶标核酸从其他样品组分中移除。如本文所用,“dna依赖性dna聚合酶”是从dna模板合成互补dna拷贝的酶。例子为来自大肠杆菌(e.coli)的dna聚合酶i、噬菌体t7dna聚合酶、或来自噬菌体t4、phi-29、m2或t5的dna聚合酶。dna依赖性dna聚合酶可以是从细菌或噬菌体分离的天然存在的酶或者被重组表达,或者可以是经修饰或“进化”的形式,该形式已被工程改造为具有某些所需特性,例如热稳定性、或者从各种经修饰模板识别或合成dna链的能力。所有已知的dna依赖性dna聚合酶都需要互补引物来引发合成。已知的是在合适的条件下,dna依赖性dna聚合酶可从rna模板合成互补的dna拷贝。rna依赖性dna聚合酶通常还具有dna依赖性dna聚合酶活性。如本文所用,“dna依赖性rna聚合酶”或“转录酶”是从具有通常为双链的启动子序列的双链或部分双链dna分子合成多个rna拷贝的酶。rna分子(“转录物”)沿从正好位于启动子下游的特定位置开始的5'-至-3'方向合成。转录酶的例子为来自大肠杆菌以及噬菌体t7、t3和sp6的dna依赖性rna聚合酶。如本文所用,“rna依赖性dna聚合酶”或“逆转录酶”(“rt”)是从rna模板合成互补的dna拷贝的酶。所有已知的逆转录酶还具有从dna模板制成互补的dna拷贝的能力;因此,它们不仅是rna依赖性dna聚合酶,还是dna依赖性dna聚合酶。rt还可具有rna酶h活性。需要引物来引发利用rna模板和dna模板两者进行的合成。在扩增和/或检测体系的上下文中,术语“特异性”在本文用于指描述体系依赖于序列和测定法条件来区分靶标序列与非靶标序列的能力的体系特性。就核酸扩增而言,特异性一般是指所产生的特异性扩增子的数目与副产物数目的比率(例如,信噪比)。就检测而言,特异性一般是指由靶标核酸产生的信号与由非靶标核酸产生的信号的比率。术语“灵敏度”在本文用于指核酸扩增反应可以被检测或定量的精确度。扩增反应的灵敏度一般为可以在扩增体系中被可靠地检测的靶标核酸的最小拷贝数目的量度,并且将取决于例如所使用的检测测定法以及扩增反应的特异性,例如,特定扩增子与副产物的比率。如本文所用,术语“相对光单位”(“rlu”)是指示样品在给定的波长或波长带下发射的光子的相对数目的任意测量单位。rlu随着测量所用的检测手段的特性而变化。附图说明图1示出hpv33型基因组的e6/e7区域的参考序列(seqidno:83)。图2示出hpv31型基因组的e6/e7区域的参考序列(seqidno:84)。具体实施方式本发明提供了用于从样品扩增和检测人乳头瘤病毒(hpv)核酸,具体地讲是与hpv33型(hpv33)和/或hpv31型(hpv31)基因组的e6/e7区域相对应的序列的组合物、试剂盒和方法。所述组合物、试剂盒和方法提供了识别hpv33或hpv31e6/e7区域内的靶标序列或它们的互补序列的寡核苷酸序列。此类寡核苷酸可用作扩增寡核苷酸,所述扩增寡核苷酸可包括引物、启动子引物、被阻断的寡核苷酸、和启动子提供者寡核苷酸,其功能此前已有描述(参见例如美国专利no.4,683,195、no.4,683,202、no.4,800,159、no.5,399,491、no.5,554,516、no.5,824,518和no.7,374,885,它们各自以引用方式并入本文)。其他寡核苷酸可用作捕获探针低聚物,以用于从各种样品组分捕获和分离靶标核酸。其他寡核苷酸可用作探针,以用于检测hpv33或hpv31的经扩增序列。所述方法提供了对hpv33和/或hpv31核酸(诸如hpv33和/或hpv31e6/e7mrna转录物)的灵敏且特异性的检测。所述方法包括进行hpv33和/或hpv31序列的核酸扩增,以及通过例如如下方式检测所述经扩增产物:使经扩增产物与核酸检测探针特异性杂交,所述核酸检测探针提供用于指示样品中存在hpv33或hpv31的信号。扩增步骤包括将样品与特异性地针对hpv33或hpv31e6/e7区域中的靶标序列的一种或多种扩增低聚物接触,以便在样品中存在hpv33或hpv31核酸的情况下产生扩增产物。扩增通过如下方式合成靶标序列或其互补序列的另外拷贝:使用至少一种核酸聚合酶,利用模板链从扩增低聚物(引物)延伸所述序列。用于检测扩增产物的一个实施例使用杂交步骤,该杂交步骤包括将扩增产物与至少一个探针接触,所述至少一个探针特异性地针对由所选择的扩增低聚物所扩增的序列(例如,包含在侧接有一对所选择的扩增低聚物的靶标序列中的序列)。检测步骤可使用多种已知技术中的任一种来进行,以检测与经扩增的靶标序列特异性地关联的信号,诸如通过使扩增产物与被标记的检测探针杂交并检测由被标记的探针产生的信号。检测步骤还可提供关于经扩增序列诸如其核酸碱基序列的全部或一部分的另外的信息。检测可在扩增反应完成之后进行,或者可与扩增靶标区域同时进行,例如实时地进行。在一个实施例中,检测步骤允许均相检测,例如,在不将未杂交探针从混合物移除的情况下对杂交探针进行检测(参见例如美国专利no.5,639,604和no.5,283,174,它们各自以引用方式并入本文)。在扩增步骤接近结束或结束时检测扩增产物的实施例中,可使用线性检测探针来提供用于指示探针与扩增产物杂交的信号。这种检测的一个例子使用与靶标核酸杂交的发光标记探针。发光标签然后从非杂交探针水解。使用光度计通过化学发光来进行检测。(参见例如国际专利申请公布no.wo89/002476,其以引用方式并入本文)。在使用实时检测的其他实施例中,检测探针可以是用报告子部分标记的发夹探针,诸如分子信标、分子炬或杂交开关探针,所述报告子部分在探针结合到扩增产物时会被检测到。此类探针可包含靶标杂交序列和非靶标杂交序列。此类探针的各种形式此前已有描述(参见例如美国专利no.5,118,801、no.5,312,728、no.5,925,517、no.6,150,097、no.6,849,412、no.6,835,542、no.6,534,274和no.6,361,945,以及美国专利申请公布no.20060068417a1和no.20060194240a1,它们各自以引用方式并入本文)。本发明的优选组合物被构造为与hpv33或hpv31的e6/e7核酸靶标区域特异性杂交且与样品中疑似存在的其他核酸具有最小交叉反应性。在一些方面,本发明的组合物被构造为与hpv33或hpv31的e6/e7核酸靶标区域特异性杂交且与一种或多种其他hpv类型具有最小交叉反应性。例如,在某些实施例中,本发明的组合物被构造为与hpv33的e6/e7区域特异性杂交且与hpv16、18、31、35、39、45、51、52、56、58、59和68型中的一者或多者具有最小交叉反应性;在一些此类变型形式中,所述组合物被构造为与hpv33的e6/e7区域特异性杂交且与至少(i)hpv31和/或(ii)密切相关的hpv52和58型中的一者或两者具有最小交叉反应性(例如,与hpv31、52和58型中的每一者具有最小交叉反应性)。在其他实施例中,本发明的组合物被构造为与hpv31的e6/e7区域特异性杂交且与hpv16、18、33、35、39、45、51、52、56、58、59和68型中的一者或多者具有最小交叉反应性;在一些此类变型形式中,所述组合物被构造为与hpv31的e6/e7区域特异性杂交且与至少(i)hpv33和/或(ii)密切相关的hpv52和58型中的一者或两者具有最小交叉反应性(例如,与hpv33、52和58型中的每一者具有最小交叉反应性)。在一个方面,本发明的组合物是多重体系的一部分,该体系还包括用于检测这些hpv类型中的一者或多者的组分和方法(例如,用于检测hpv33和hpv31中的一者或多者的多重体系)。在本发明的某些方面,提供了至少两种低聚物的组合来对疑似含有hpv33的样品中的hpv33靶标核酸进行检测。通常,所述低聚物组合包括用于特异性地扩增与hpv33e6和/或e7基因相对应的hpv33核酸靶标区域的第一扩增低聚物和第二扩增低聚物。在某些实施例中,(a)第一hpv33扩增低聚物包含第一靶标杂交序列,该第一靶标杂交序列为约15至约27个连续核苷酸长并基本上与这样的序列相对应或相同,所述序列包含在seqidno:66的序列中并至少包括seqidno:67、seqidno:68或seqidno:69的序列;并且(b)第二hpv33扩增低聚物包含第二靶标杂交序列,该第二靶标杂交序列为约15至约27个连续核苷酸长并基本上与这样的序列相对应或相同,所述序列包含在seqidno:70的序列中并至少包括seqidno:71、seqidno:72或seqidno:73的序列。在所述低聚物组合的一些实施例中,(a)第一hpv33扩增低聚物包含基本上与选自seqidno:1、seqidno:2、seqidno:3、seqidno:4、seqidno:5、seqidno:6、seqidno:7和seqidno:8的序列相对应或相同的第一靶标杂交序列;并且/或者(b)第二hpv33扩增低聚物包含基本上与选自seqidno:9、seqidno:10、seqidno:11、seqidno:12、seqidno:13、seqidno:14、seqidno:15和seqidno:16的序列相对应或相同的第二靶标杂交序列。在典型的变型形式中,所述低聚物组合用于检测疑似含有hpv33和至少一种其他hpv基因型(例如,hpv16、18、31、45、52和58型中的至少一种)的样品中的hpv33靶标核酸。在一种变型形式中,所述低聚物组合是包含至少两种基本上与表4中的低聚物相同的低聚物的组合。在一些优选的变型形式中,所述低聚物组合还包括用于特异性地扩增与hpv31e6和/或e7基因相对应的hpv31型(hpv31)核酸靶标区域的第一扩增低聚物和第二扩增低聚物。在某些实施例中,(a)第一hpv31扩增低聚物包含第一靶标杂交序列,该第一靶标杂交序列为约15至约27个连续核苷酸长并基本上与这样的序列相对应或相同,所述序列包含在seqidno:74的序列中并至少包括seqidno:75、seqidno:76或seqidno:77的序列;并且(b)第二hpv31扩增低聚物包含第二靶标杂交序列,该第二靶标杂交序列为约15至约30个连续核苷酸长并基本上与这样的序列相对应或相同,所述序列包含在seqidno:78的序列中并至少包括seqidno:79、seqidno:80或seqidno:81的序列。在所述低聚物组合的一些实施例中,(a)第一hpv31扩增低聚物包含基本上与选自seqidno:26、seqidno:27、seqidno:28、seqidno:29、seqidno:30、seqidno:31、seqidno:32和seqidno:33的序列相对应或相同的第一靶标杂交序列;并且/或者(b)第二hpv31扩增低聚物包含基本上与选自seqidno:34、seqidno:35、seqidno:36、seqidno:37、seqidno:38、seqidno:39、seqidno:40和seqidno:41的序列相对应或相同的第二靶标杂交序列。在某些实施例中,如本文所述的扩增低聚物为还包含位于靶标杂交序列5'端的启动子序列并且不与hpv33或hpv31靶标核酸互补的启动子引物或启动子提供者。例如,在如本文所述用于扩增hpv33或hpv31靶标区域的低聚物组合的一些实施例中,第二扩增低聚物为还包含5'启动子序列的启动子引物或启动子提供者。在特定实施例中,所述启动子序列为t7rna聚合酶启动子序列,诸如具有以seqidno:82示出的序列的t7启动子序列。在具体变型形式中,第二hpv33扩增低聚物为具有以seqidno:17、seqidno:18、seqidno:19、seqidno:20、seqidno:21、seqidno:22、seqidno:23或seqidno:24示出的序列的启动子引物或启动子提供者;并且/或者第二hpv31扩增低聚物为具有以seqidno:42、seqidno:43、seqidno:44、seqidno:45、seqidno:46、seqidno:47、seqidno:48或seqidno:49示出的序列的启动子引物或启动子提供者。在一些实施例中,如本文所述的低聚物组合还包含终止寡核苷酸(本文中也称为“阻断”寡核苷酸),所述终止寡核苷酸包含与包含在靶标区域的5'端附近的靶标核酸内的序列基本上互补(例如,完全互补)的碱基序列。例如,在本文所述的与转录介导的扩增(tma)相关的某些实施例中,终止低聚物通常与例如启动子提供者扩增低聚物结合使用。在一些实施例中,如本文所述的低聚物组合还包含用于捕获hpv33和/或hpv31靶标核酸的至少一种捕获探针低聚物。此类捕获探针可特异性地针对hpv33或hpv31靶标核酸。在一些实施例中,所述捕获探针低聚物包含基本上与包含在seqidno:83(代表性hpv33e6/e7区域)或seqidno:84(代表性hpv31e6/e7区域)的互补序列中的序列相对应的靶标杂交序列,其中所述靶标杂交序列共价连接到结合于固定化探针的序列或部分。在具体变型形式中,hpv33特异性捕获探针低聚物的靶标杂交序列包含基本上与seqidno:50相对应或相同的序列或者由基本上与seqidno:50相对应或相同的序列组成;并且/或者hpv31特异性捕获探针低聚物的靶标杂交序列包含基本上与seqidno:52相对应或相同的序列或者由基本上与seqidno:52相对应或相同的序列组成。根据本发明使用的特别合适的hpv33或hpv31捕获探针低聚物分别包含如以seqidno:51或seqidno:53示出的序列或者分别由如以seqidno:51或seqidno:53示出的序列组成。在某些变型形式中,如本文所述的低聚物组合还包含至少一种检测探针低聚物,该检测探针低聚物被构造为与可使用第一hpv33或hpv31扩增低聚物和第二hpv33或hpv31扩增低聚物扩增的hpv33或hpv31靶标序列(例如,侧接有第一扩增低聚物和第二扩增低聚物的靶标杂交序列的hpv靶标序列)特异性杂交。合适的hpv33检测探针包含具有靶标杂交序列的低聚物,该靶标杂交序列为约14至约35个核苷酸长并被构造为与包含在seqidno:83内从约核苷酸位置128至约核苷酸位置164的靶标序列特异性杂交。例如,在一些变型形式中,hpv33检测探针包含基本上与选自seqidno:54、seqidno:55、seqidno:56、seqidno:57和seqidno:58的序列相对应或相同的靶标杂交序列。合适的hpv31检测探针包含具有靶标杂交序列的低聚物,该靶标杂交序列为约14至约40个核苷酸长并被构造为与包含在seqidno:84内从约核苷酸位置675至约核苷酸位置735的靶标序列特异性杂交。例如,在一些变型形式中,hpv31检测探针包含基本上与选自seqidno:59、seqidno:60、seqidno:61、seqidno:62、seqidno:63、seqidno:64和seqidno:65的序列相对应或相同的靶标杂交序列。通常,根据本发明的检测探针低聚物还包含标签。特别合适的标签包括发出可检测的光信号的化合物,例如,可在均匀混合物中检测到的荧光团或发光(例如,化学发光)化合物。不止一个标签和不止一种类型的标签可存在于特定探针上,或者检测可依赖于使用探针的混合物,其中每个探针用产生可检测信号的化合物标记(参见例如美国专利no.6,180,340和no.6,350,579,它们各自以引用方式并入本文)。标签可通过各种手段连接到探针,包括共价键、螯合和离子相互作用,但优选的是标签被共价连接。例如,在一些实施例中,检测探针具有连接的化学发光标签,诸如吖啶酯(ae)化合物(参见例如美国专利no.5,185,439、no.5,639,604、no.5,585,481和no.5,656,744,它们各自以引用方式并入本文),在典型的变型形式中,其通过非核苷酸接头连接到探针(参见例如美国专利no.5,585,481、no.5,656,744和no.5,639,604,特别是第10栏第6行至第11栏第3行,以及实例8;它们各自以引用方式并入本文)。在其他实施例中,检测探针包含荧光标签和淬光剂两者,这样的组合在荧光共振能量转移(fret)测定法中特别有用。此类检测探针的具体变型形式包括例如taqman检测探针(罗氏分子诊断公司(rochemoleculardiagnostics))和“分子信标”(参见例如tyagi等,naturebiotechnol.16:49-53,1998(tyagi等,《自然生物技术》,第16卷,第49-53页,1998年);美国专利no.5,118,801和no.5,312,728,它们各自以引用方式并入本文)。根据本发明的检测探针低聚物还可包含非靶标杂交序列。此类检测探针的具体实施例包括例如形成由分子内杂交保持的构象的探针,所述构象诸如通常称为发夹的构象。特别合适的发夹探针包括“分子炬”(参见例如美国专利no.6,849,412、no.6,835,542、no.6,534,274和no.6,361,945,它们各自以引用方式并入本文)和“分子信标”(参见例如tyagi等,出处同上;us5,118,801和us5,312,728,出处同上)。使用此类发夹探针的方法是本领域所熟知的。在另有其他实施例中,检测探针为基本上不形成由分子内键保持的构象的线性低聚物。在具体变型形式中,线性检测探针低聚物包含化学发光化合物作为标签,优选地为吖啶酯(ae)化合物。本发明还提供了如本文所述的检测探针低聚物和捕获探针低聚物。在另一个方面,本发明提供了用于使用如本文所述的低聚物组合检测样品中的hpv33靶标核酸和/或hpv31靶标核酸的方法。在某些实施例中,用于检测疑似含有hpv33的样品中的hpv33靶标核酸的方法通常包括以下步骤:(b)将该样品与低聚物组合接触,以便特异性地扩增hpv33核酸靶标区域,其中所述低聚物组合包括如上所述的第一hpv33扩增低聚物和第二hpv33扩增低聚物;(c)进行体外核酸扩增反应,其中存在于所述样品中的任何hpv33靶标核酸均被用作产生hpv33扩增产物的模板;以及(d)检测hpv33扩增产物存在与否,从而指示样品中是否存在hpv33。在一些实施例中,所述样品还疑似含有至少一种其他hpv类型(例如,hpv16、18、31、35、39、45、51、52、56、58、59和68型中的至少一种;通常为hpv31、52和58型中的至少一种),其中所述方法特异性地检测hpv33存在与否,而不管是否存在其他hpv类型(例如,该方法能够区分hpv33与其他hpv类型,诸如hpv16、18、31、35、39、45、51、52、56、58、59和68型中的至少一种;通常为hpv31、52和58型中的至少一种)。在一些变型形式中,检测疑似含有hpv31的样品中的hpv31靶标核酸的方法通常包括以下步骤。(b')将该样品与低聚物组合接触,以便特异性地扩增hpv31核酸靶标区域,其中所述低聚物组合包括如上所述的第一hpv31扩增低聚物和第二hpv31扩增低聚物;(c')进行体外核酸扩增反应,其中存在于所述样品中的任何hpv31靶标核酸均被用作产生hpv31扩增产物的模板;以及(d')检测hpv31扩增产物存在与否,从而指示样品中是否存在hpv31。在一些实施例中,所述样品还疑似含有至少一种其他hpv类型(例如,hpv16、18、33、35、39、45、51、52、56、58、59和68型中的至少一种;通常为hpv33、52和58型中的至少一种),其中所述方法特异性地检测hpv31存在与否,而不管是否存在其他hpv类型(例如,该方法能够区分hpv31与其他hpv类型,诸如hpv16、18、31、35、39、45、51、52、56、58、59和68型中的至少一种;通常为hpv33、52和58型中的至少一种)。在一些优选的实施例中,上述检测方法用于检测疑似含有hpv33和hpv31中的至少一种的样品中的hpv33和hpv31两者。在一些此类实施例中,该方法包括(i)上述用于检测hpv33的步骤(b)-(d),以及(ii)上述用于检测hpv31的步骤(b')-(d')。用于检测hpv33和hpv31的步骤中的任一个或多个可独立进行或一起进行。在一些变型形式中,用于hpv33检测的步骤(b)-(d)中的任一个或多个与用于hpv31检测的一个或多个相应步骤(b')-(d')在同一反应混合物中一起进行(例如,扩增步骤(c)可在扩增步骤(c')期间在同一反应混合物中进行;并且/或者检测步骤(d)可与检测步骤(d')在同一反应混合物中进行)。因此,在一些实施例中,用于检测hpv33和hpv31的方法作为对同一反应混合物内的hpv33和hpv31两者进行同时检测的多重测定法来进行。根据本发明的检测方法通常还包括步骤(a)提供疑似含有hpv33和/或hpv31的样品。在某些实施例中,“提供”将用于步骤(b)-(d)和/或步骤(b')-(d')中的样品包括例如在进行该方法的一个或多个步骤的试验装置或其他位置处接收样品,以及/或者从进行该方法的一个或多个步骤的装置内的位置(例如,从储存装置或其他储存库)取得样品。在某些实施例中,该方法还包括在接触步骤之前从样品中的其他组分纯化hpv33和/或hpv31靶标核酸。这种纯化可包括从其他样品组分分离和/或浓缩包含在样品中的生物体的方法。在特定实施例中,纯化靶标核酸包括捕获靶标核酸以便将靶标核酸从其他样品组分特异性或非特异性地分离。非特异性靶标捕获方法可涉及从基本上水性的混合物选择性沉淀核酸;将核酸粘附于载体,该载体被洗涤以移除其他样品组分;或者将核酸从包含hpv核酸和其他样品组分的混合物物理分离的其他手段。在一些实施例中,通过使hpv靶标核酸与捕获探针低聚物特异性杂交来将hpv33或hpv31核酸从其他样品组分选择性地分离。所述捕获探针低聚物包含靶标杂交序列,该靶标杂交序列被构造为与hpv靶标序列特异性杂交以便形成从样品组分分离的靶标序列:捕获探针复合物。合适的hpv33靶标杂交序列和hpv31靶标杂交序列分别以seqidno:50和seqidno:52示出。在优选的变型形式中,特异性靶标捕获将hpv靶标:捕获探针复合物结合到固定化探针以形成靶标:捕获探针:固定化探针复合物,该复合物从样品分离并任选地被洗涤以移除非靶标样品组分(参见例如美国专利no.6,110,678、no.6,280,952、和no.6,534,273,它们各自以引用方式并入本文)。在此类变型形式中,所述捕获探针低聚物还包含这样的序列或部分,该序列或部分用其结合靶标序列将捕获探针结合于连接到固相载体的固定化探针,从而允许杂交的靶标核酸从其他样品组分分离。在包括扩增和检测hpv33和hpv31两者的实施例中,从单个样品选择性分离hpv33核酸和hpv31核酸可同时进行。在更具体的实施例中,所述捕获探针低聚物包括尾部分(例如,3'尾),该尾部分不与hpv靶标序列互补,但与固定化探针上的序列特异性杂交,从而充当允许靶标核酸从其他样品组分分离的部分,诸如此前在例如美国专利no.6,110,678中所述,该专利以引用方式并入本文。可在尾区域中使用任何序列,其长度通常为约5至50个nt,并且优选的实施例包括约10至40个nt(例如,a10至a40)、更优选地约14至33个nt(例如,a14至a30或t3a14至t3a30)的基本上均聚的尾,所述基本上均聚的尾结合于连接到固相载体(例如,基质或粒子)的互补固定化序列(例如,多聚t)。例如,在包含3'尾的捕获探针的具体实施例中,hpv33捕获探针低聚物或hpv31捕获探针低聚物具有分别以seqidno:51或seqidno:53示出的序列。靶标捕获通常发生在溶液相混合物中,该溶液相混合物包含在杂交条件下,通常在高于尾序列:固定化探针序列双链体的tm的温度下与hpv靶标序列特异性杂交的一种或多种捕获探针低聚物。对于包括捕获探针尾的实施例,hpv靶标:捕获探针复合物通过调整杂交条件以使得捕获探针尾与固定化探针杂交来捕获,然后将固相载体上的整个复合物从其他样品组分分离。可将具有连接的固定化探针:捕获探针:hpv靶标序列的载体洗涤一次或多次,以便进一步移除其他样品组分。优选的实施例使用粒状固相载体(诸如顺磁性小珠),以使得具有连接的hpv靶标:捕获探针:固定化探针复合物的粒子可悬浮在洗涤溶液中,随后优选地通过使用磁吸引将其从洗涤溶液中提取出。为了限制处理步骤的数量,可通过仅将载体上的复合物中的hpv靶标序列与扩增低聚物混合并继续进行扩增步骤来扩增hpv靶标核酸。扩增hpv33或hpv31靶标序列利用体外扩增反应,该反应使用在待扩增的靶标区域旁侧的至少两种扩增低聚物。在特定实施例中,待扩增的hpv33靶标区域基本上与seqidno:83从约核苷酸位置128至约核苷酸位置164相对应。在特定实施例中,待扩增的hpv31靶标区域基本上与seqidno:84从约核苷酸位置675至约核苷酸位置735相对应。用于扩增这些靶标区域的特别合适的扩增低聚物组合在本文中有所描述(参见例如上文的第[82]-[84]段)。合适的扩增方法包括例如复制酶介导的扩增、聚合酶链反应(pcr)、连接酶链反应(lcr)、链置换扩增(sda),以及转录介导或转录相关的扩增(tma)。此类扩增方法是本领域中熟知的(参见例如上文的第[54]和[55]段)并且易于根据本发明的方法使用。例如,使用tma扩增的一些扩增方法包括以下步骤。简而言之,包含待扩增的序列的靶标核酸作为单链核酸(例如,ssrna或ssdna)提供。本领域的技术人员将会知道,可使用双链核酸(例如,dsdna)的常规解链来提供单链靶标核酸。启动子引物在靶标核酸的靶标序列处特异性结合到靶标核酸,并且逆转录酶(rt)使用靶标链作为模板延伸启动子引物的3'端以产生靶标序列链的cdna拷贝,从而获得rna:dna双链体。rna酶消化rna:dna双链体的rna链,随后第二引物特异性地结合到其靶标序列,该靶标序列位于启动子引物端下游的cdna链上。rt通过使用第一cdna模板延伸第二引物的3'端来合成新dna链,从而产生包含功能性启动子序列的dsdna。然后特异性地针对启动子序列的rna聚合酶引发转录以生成rna转录物,该rna转录物为反应中的初始靶标链的约100至1000个扩增拷贝(“扩增子”)。当第二引物在扩增子的每一个中特异性地结合到其靶标序列时,扩增继续,随后rt从扩增子rna模板产生dna拷贝以生成rna:dna双链体。反应混合物中的rna酶消化来自rna:dna双链体的扩增子rna,随后启动子引物在新合成的dna中特异性地结合到其互补序列。rt延伸启动子引物的3'端以产生包含功能性启动子的dsdna,rna聚合酶结合到该功能性启动子以转录与靶标链互补的另外的扩增子。形成更多个扩增子拷贝的自动催化循环在反应的过程中重复,导致存在于样品中的靶标核酸约成十亿倍扩增。可通过使用特异性地结合到包含在扩增产物中的靶标序列的探针在扩增期间实时检测扩增产物,或在扩增反应结束时检测扩增产物。检测得自结合探针的信号指示样品中是否存在靶标核酸。在一些实施例中,该方法利用“反向”tma反应。在此类变型形式中,初始或“正向”扩增低聚物是与靶标区域3'端附近的靶标核酸杂交的引发性寡核苷酸。逆转录酶(rt)通过使用靶标核酸作为模板延伸引物的3'端来合成cdna链。第二或“反向”扩增低聚物是具有被构造为与包含在合成的cdna链中的靶标序列杂交的靶标杂交序列的启动子引物或启动子提供者。当第二扩增低聚物为启动子引物时,rt使用cdna链作为模板延伸启动子引物的3'端以产生靶标序列链的第二cdna拷贝,从而产生包含功能性启动子序列的dsdna。然后扩增基本如上文的第[101]段中所述继续,以便利用rna聚合酶从启动子序列引发转录。作为另外一种选择,当第二扩增低聚物为启动子提供者时,通常利用与靶标区域5'端附近的靶标序列杂交的终止寡核苷酸来终止引发性低聚物在终止寡核苷酸3'端处延伸,从而提供由从引发性低聚物延伸所合成的初始cdna链的限定3'端。然后启动子提供者的靶标杂交序列与初始cdna链的限定3'端杂交,并且cdna链的3'端延伸以添加与启动子提供者的启动子序列互补的序列,从而导致形成双链启动子序列。然后初始cdna链用作模板,以便使用识别双链启动子并从其引发转录的rna聚合酶,来转录与初始cdna链(不包括启动子部分)互补的多个rna转录物。然后这些rna转录物中的每一个可以用来充当模板,以便从第一引发性扩增低聚物进一步扩增。扩增产物的检测可通过多种方法来实现。核酸可与导致物理变化(诸如可检测的电变化)的表面相关联。经扩增的核酸可通过以下方式检测:将它们在基质中或基质上浓缩,并且检测核酸或与它们相关联的染料(例如,嵌入剂,诸如溴化乙锭或核酸绿(cybergreen)),或者检测与溶液相中的核酸相关联的染料的增加。其他检测方法可使用被构造为与扩增产物中的序列特异性杂交并检测是否存在探针:产物复合物的核酸检测探针,或者通过使用可以放大与扩增产物相关联的可检测信号的探针的复合物(例如美国专利no.5,424,413、no.5,451,503和no.5,849,481,它们各自以引用方式并入本文)。与扩增产物特异性相关联的被直接或间接标记的探针提供指示样品中是否存在靶标核酸的可检测信号。例如,如果靶标核酸为hpv33基因组的e6/e7区域或与e6/e7区域相对应的rna,那么扩增产物将在e6/e7区域的序列中包含靶标序列或包含与e6/e7区域中的序列互补的靶标序列,并且探针将直接或间接地结合到包含在扩增产物中的序列以指示测试样品中是否存在靶标核酸。与互补的扩增序列杂交的检测探针的优选实施例可以是dna低聚物或rna低聚物、或包含dna核苷酸和rna核苷酸的组合的低聚物、或具有经修饰的主链的合成的低聚物,例如包含一个或多个2'-甲氧基取代的核糖核苷酸的低聚物。用于检测经扩增的hpv序列的探针可能未被标记且被间接地检测(例如,通过将另一个结合伴侣结合到探针上的部分),或者可以用多种可检测标签来标记。适于根据本发明的方法使用的检测探针的特定实施例在本文有进一步描述(参见例如上文的第[87]-[90]段)。在用于检测hpv序列的方法的一些优选的实施例中,诸如在使用转录介导的扩增(tma)的某些实施例中,检测探针为线性化学发光标记探针,更优选地为线性吖啶酯(ae)标记探针。不旨在被核酸聚合酶延伸的低聚物优选地包含取代3'oh以防止低聚物在扩增反应中发生酶介导的延伸的阻断基团。例如,扩增期间存在的被阻断的扩增低聚物和/或检测探针优选地不具有功能性3'oh,而是包含位于3'端处或附近的一个或多个阻断基团。3'端附近的阻断基团优选地在3'端的五个残基内,而且足够大以限制聚合酶结合到低聚物,并且其他优选的实施例包含共价连接到3'端的阻断基团。可使用许多不同的化学基团来阻断3'端,例如烷基、非核苷酸接头、烷烃-二醇双脱氧核苷酸残基和虫草素。通常在3'端处阻断并且特别适用于使用转录介导的扩增的某些实施例的低聚物的例子是启动子提供者。如前所述,启动子提供者包括位于第一区域的5'端的第一靶标杂交区域,以及包含rna聚合酶的启动子序列的第二区域。启动子提供者寡核苷酸被修饰以防止引发从其3'-端开始的dna合成,诸如通过包含如上所述的阻断基团。在一些实施例中,根据hpv33检测方法使用的启动子提供者包含靶标杂交序列,该靶标杂交序列基本上与这样的序列相对应或相同,所述序列包含在seqidno:70的序列中并至少包括seqidno:71、seqidno:72或seqidno:73的序列(例如,靶标杂交序列具有基本上与选自seqidno:9、seqidno:10、seqidno:11、seqidno:12、seqidno:13、seqidno:14、seqidno:15和seqidno:16的序列相对应或相同的序列;例如,hpv33启动子提供者可具有如以seqidno:17、seqidno:18、seqidno:19、seqidno:20、seqidno:21、seqidno:22、seqidno:23或seqidno:24示出的序列)。在一些实施例中,根据hpv31检测方法使用的启动子提供者包含靶标杂交序列,该靶标杂交序列基本上与这样的序列相对应或相同,所述序列包含在seqidno:78的序列中并至少包括seqidno:79、seqidno:80或seqidno:81的序列(例如,靶标杂交序列具有基本上与选自seqidno:34、seqidno:35、seqidno:36、seqidno:37、seqidno:38、seqidno:39、seqidno:40和seqidno:41的序列相对应或相同的序列;例如,hpv31启动子提供者可具有如以seqidno:42、seqidno:43、seqidno:44、seqidno:45、seqidno:46、seqidno:47、seqidno:48或seqidno:49示出的序列)。通常为3'-阻断的低聚物的另一个例子是上文此前所述的终止(“阻断”)寡核苷酸。例如,在本文所述的与转录介导的扩增(tma)相关的某些实施例中,终止低聚物通常与例如启动子提供者扩增低聚物结合使用。终止低聚物与包含在靶标区域5'端附近的靶标核酸内的序列杂交,以便“终止”包含引发性寡核苷酸的新生核酸的引物延伸,从而提供新生核酸链的限定3'-端。使用转录介导的扩增的其他实施例利用启动子引物,该启动子引物包括位于第一区域5'端的第一靶标杂交区域以及包含rna聚合酶的启动子序列的第二区域,但其不被修饰以防止引发从其3'-端开始的dna合成。在某些变型形式中,根据hpv33检测方法使用的启动子引物包含靶标杂交序列,该靶标杂交序列基本上与这样的序列相对应或相同,所述序列包含在seqidno:70的序列中并至少包括seqidno:71、seqidno:72或seqidno:73的序列(例如,靶标杂交序列具有基本上与选自seqidno:9、seqidno:10、seqidno:11、seqidno:12、seqidno:13、seqidno:14、seqidno:15和seqidno:16的序列相对应或相同的序列;例如,hpv33启动子引物可具有如以seqidno:17、seqidno:18、seqidno:19、seqidno:20、seqidno:21、seqidno:22、seqidno:23或seqidno:24示出的序列)。在某些变型形式中,根据hpv31检测方法使用的启动子引物包含靶标杂交序列,该靶标杂交序列基本上与这样的序列相对应或相同,所述序列包含在seqidno:78的序列中并至少包括seqidno:79、seqidno:80或seqidno:81的序列(例如,靶标杂交序列具有基本上与选自seqidno:34、seqidno:35、seqidno:36、seqidno:37、seqidno:38、seqidno:39、seqidno:40和seqidno:41的序列相对应或相同的序列;例如,hpv31启动子引物可具有如以seqidno:42、seqidno:43、seqidno:44、seqidno:45、seqidno:46、seqidno:47、seqidno:48或seqidno:49示出的序列)。用于检测hpv靶标核酸的测定法可任选地包括非靶标内部对照(ic)核酸,所述核酸在同一测定反应混合物中通过使用特异性地针对ic序列的扩增和检测低聚物来扩增和检测。ic核酸序列可以是加标到样品中的合成核酸序列,或者ic核酸序列可以是细胞组分。作为细胞组分的ic核酸序列可来自外源性细胞源或与样本相关的内源性细胞源。外源性细胞源例如为被添加到样品中,然后连同样本一起流经样品处理程序的细胞。更具体的例子是将hela细胞、jurkat细胞、siha细胞或其他细胞连同被收集以供检验的样本(例如,阴道拭子样本)一起添加到样品培养基。然后处理、扩增和检测样本和外源性细胞,使用扩增低聚物和检测低聚物扩增和检测所述样本以便识别所关注的靶标序列,并且使用扩增低聚物和检测低聚物扩增和检测所述外源性细胞以便识别ic靶标序列。内源性细胞源是在收集样本时将自然获得的细胞源。一个例子:当通过阴道拭子获得样本时将存在上皮细胞。然后类似于上述的示例性外源性细胞处理,对样本和内源性细胞源两者进行处理、扩增和检测。使用扩增低聚物和检测低聚物扩增和检测所述样本以便识别所关注的靶标序列,并且使用扩增低聚物和检测低聚物扩增和检测所述内源性细胞以便识别ic靶标序列;通常,识别存在于内源性细胞源中的管家基因,诸如β-球蛋白基因。(参见例如poljak等,j.clin.virol,25:s89-97,2002(poljak等,《临床病毒学杂志》,第25卷,第s89-s97页,2002年);美国专利no.6,410,321;以及美国专利申请公布no.2004-0023288;它们各自以引用方式并入本文)。使用细胞源ic允许通过检测从样品收集开始进行控制。合成核酸序列提供了对扩增和检测的控制。在某些实施例中,如果没有获得预期靶标hpv核酸的信号(例如,样品的hpv33和/或hpv31靶标核酸检测为阴性),那么对来自经扩增ic序列的信号的放大和检测表明测定法的试剂、条件和测定法步骤的执行在所述测定法中的使用是恰当的。当需要定量结果时,还可将ic用作测定法的内参,即,使用得自ic扩增和检测的信号来设定在基于所获得的经扩增hpv靶标序列信号对样品中的hpv核酸的量进行定量的算法中使用的参数。ic还可用于监测测定法中的一个或多个步骤的完整性。合成ic核酸序列的优选实施例为源自天然存在的来源的随机序列(例如,已按随机方式重新排列的hiv序列)。另一个优选的ic核酸序列可以是从天然存在的来源分离的或者体外合成的rna转录物,所述体外合成诸如通过由克隆的随机序列制备转录物以使得测定法所包括的ic拷贝的数目可被准确地确定。通过使用任何熟知的方法来构造和合成针对ic靶标序列的扩增低聚物和探针,前提条件是所述扩增低聚物和探针的作用是使用与用于扩增和检测hpv靶标序列基本上相同的测定条件来扩增ic靶标序列并且检测经扩增的ic序列。在包括基于靶标捕获的纯化步骤的优选实施例中,优选的是在测定法的靶标捕获步骤中包括特异性地针对ic靶标的靶标捕获探针,使得ic在所述测定法中以与在全部测定法步骤中针对预期hpv分析物所采用的方式类似的方式来处理。在一些优选的实施例中,对hpv33和hpv31的检测作为多重测定法来进行。通常,在此类实施例中,对hpv33靶标核酸的扩增与对hpv31靶标核酸的扩增在同一扩增反应混合物中同时进行,并且对hpv33扩增产物的检测与对hpv31扩增产物的检测在同一检测反应混合物中同时进行。对hpv33和hpv31的检测通常包括将扩增反应与被差异性标记的hpv33检测探针低聚物和hpv31检测探针低聚物接触,所述检测探针低聚物被构造为在这样的条件下与hpv33扩增产物和hpv31扩增产物特异性杂交:凭借所述条件可确定hpv33扩增产物和hpv31扩增产物存在与否。在一些此类变型形式中,hpv33检测探针低聚物和hpv31检测探针低聚物中的每一者包括化学发光标签或荧光标签。例如,hpv33检测探针低聚物和hpv31检测探针低聚物中的每一者可以包括不同的化学发光标签,诸如通过足以区分hpv33特异性化学发光信号和hpv31特异性化学发光信号的不同光发射动力学来表征的化学发光标签。用于hpv33检测探针低聚物和hpv31检测探针低聚物的合适化学发光标签包括具有有差别的光动力学的吖啶酯(ae)标签。在特定的变型形式中,一种检测探针低聚物(例如,特异性地针对hpv33扩增产物的探针)包含2'甲基吖啶酯标签(也称为“发光体”探针),而第二检测探针低聚物(例如,特异性地针对hpv31扩增产物的探针)包含邻位氟代吖啶酯标签(在本文中也称为“闪光体”探针),闪光体探针表现出比发光体探针更迅速的灭光动力学。可使用etf算法将灭光动力学去卷积并计算每个信号。如果使用内部对照(ic),那么ic探针还可以是例如闪光体探针,其可通过例如使用比hpv闪光体探针低得多的探针输入来与hpv测试闪光体信号相区别。(参见例如美国公布no.2012/0003646)。本发明还提供了用于扩增和/或检测hpv33靶标核酸和/或hpv31靶标核酸的反应混合物。根据本发明的反应混合物至少包含以下所述各项中的一者或多者:如本文所述的用于扩增hpv33靶标核酸和/或hpv31靶标核酸的低聚物组合;如本文所述的用于纯化hpv33靶标核酸和/或hpv31靶标核酸的捕获探针低聚物;以及如本文所述的用于确定hpv33扩增产物和/或hpv31扩增产物存在与否的检测探针低聚物。该反应混合物还可包含多种任选的组分,诸如捕获探针核酸的阵列。就扩增反应混合物而言,反应混合物通常将包含适用于进行体外扩增的其他试剂,诸如缓冲液、盐溶液、适当的核苷酸三磷酸(例如,datp、dctp、dgtp、dttp、atp、ctp、gtp和utp)和/或酶(例如,逆转录酶和/或rna聚合酶),并通常将包含试验样品组分,在所述试验样品组分中可能存在或者可能不存在hpv33靶标核酸和/或hpv31靶标核酸。此外,就包含检测探针连同扩增低聚物组合的反应混合物而言,用于反应混合物的扩增低聚物和检测探针低聚物的选择与共用的靶标区域有关(即,所述反应混合物将包含这样的探针,该探针会结合到可通过所述反应混合物的扩增低聚物组合而扩增的序列)。本发明还提供了用于实施如本文所述的方法的试剂盒。根据本发明的试剂盒至少包含以下所述各项中的一者或多者:如本文所述的用于扩增hpv33靶标核酸和/或hpv31靶标核酸的扩增低聚物组合;如本文所述的用于纯化hpv33靶标核酸和/或hpv31靶标核酸的捕获探针低聚物;以及如本文所述的用于确定hpv33扩增产物和/或hpv31扩增产物存在与否的检测探针低聚物。该试剂盒还可包含多种任选的组分,诸如捕获探针核酸的阵列。可存在于试剂盒中的其他试剂包括适于进行体外扩增的试剂,诸如缓冲液、盐溶液、适当的核苷酸三磷酸(例如,datp、dctp、dgtp、dttp、atp、ctp、gtp和utp)和/或酶(例如,逆转录酶和/或rna聚合酶)。如本文所述的低聚物可被包装在多种不同的实施例中,并且本领域的技术人员将会知道,本发明包括多种不同的试剂盒配置。例如,试剂盒可包含针对hpv基因组的仅一个靶标区域的扩增低聚物,或者其可包含针对多个hpv靶标区域的扩增低聚物。此外,就包含检测探针连同扩增低聚物组合的试剂盒而言,用于试剂盒的扩增低聚物和检测探针低聚物的选择与共用的靶标区域有关(即,所述试剂盒将包含这样的探针,该探针会结合到可通过所述试剂盒的扩增低聚物组合而扩增的序列)。在某些实施例中,所述试剂盒还包括用于实施根据本发明的方法的一套说明书,其中该说明书可与包装说明书和/或所述试剂盒或其组件的包装相关联。本发明进一步由以下非限制性例子说明。实例1hpv31/33基因分型测定法该实例描述了根据本发明的示例性hpv31/33基因分型测定法。该实例的测定法在本文中也称为“aptimahpv31/33基因分型测定法”或“aptima31/33gt测定法”。下表1列出了用于该测定法中的所有低聚物各自的浓度。表1:hpv31/33基因分型测定法中所用的低聚物低聚物描述低聚物seqidno浓度hpv31靶标捕获低聚物530.9pmol/rxnhpv33靶标捕获低聚物510.7pmol/rxnhpv31t7扩增低聚物426.6pmol/rxnhpv33t7扩增低聚物205pmol/rxnhpv31非t7扩增低聚物296.7pmol/rxnhpv33非t7扩增低聚物56.6pmol/rxnhpv33检测探针541.3×106rlu/mlhpv31检测探针598.5×106rlu/ml该测定法利用来自hpv测定法(参见例如aptimahpv测定法,目录号303012,美国加利福尼亚州圣地亚哥的基因探针股份有限公司(gen-probeincorporated,sandiego,ca))的方法和试剂。一般来讲,根据aptima测定法包装说明书,使用dts402仪器系统和各种aptima试剂来执行检验。靶标捕获反应混合物被制备成包含靶标捕获低聚物seqidno:53和seqidno:51,它们被构造为分别与hpv31靶标核酸和hpv33靶标核酸特异性杂交。扩增反应混合物被制备成包含seqidno:5、seqidno:20、seqidno:29和seqidno:42作为扩增低聚物。检测反应混合物被制备成包含seqidno:54和seqidno:59作为被ae标记的检测探针低聚物,所述被ae标记的检测探针低聚物被构造为分别与由hpv31和hpv33产生的扩增产物特异性杂交。捕获、扩增和检测反应作为多重反应来执行。hpv阳性样品包括加标有各种浓度的hpv31体外转录物(ivt)、加标有hpv33ivt、或加标有hpv31ivt和hpv33ivt的hpv阴性新柏氏液体子宫颈抹片(thinprepliquicpap)样品,以及hpv阳性样品。阴性对照样品为其中未加标有任何hpvivt的hpv阴性新柏氏液体子宫颈抹片样品。使用hpv测定法(目录号303012,基因探针股份有限公司)来确定是hpv阳性还是hpv阴性。使用样品运输介质(stm)以1:2.9的比率将样品稀释,然后进行靶标捕获反应。将反应混合物在62℃下温育35分钟,然后在室温下温育30分钟。所有温育步骤都使用gen-probesb100系统。使用磁性小珠和gen-probe靶标捕获系统(目录号104555,基因探针股份有限公司)来进行捕获和洗涤步骤。在靶标捕获之后,将扩增反应混合物和油添加到每个反应管中,并且在62℃下温育10分钟以使引物退火。在10分钟的温育之后,将酶试剂添加到每份反应混合物,并且将反应在42℃下温育60分钟,以使靶标核酸能够进行核酸扩增。在扩增后,将检测反应混合物添加到每个扩增反应,并且在62℃下温育20分钟以使探针能够与反应中的扩增产物杂交。将选择试剂添加到反应管并在62℃下温育10分钟,然后在室温下冷却。使用gen-probe光度计,采用autodetect1试剂和autodetect2试剂来执行对靶标的检测。以相对光单位(rlu)来度量扩增产物的检测。一般来讲,为了确定靶标是否存在,针对hpv31使用200,000rlu的rlu截止值,并针对hpv33使用800,000rlu的rlu截止值。分析灵敏度和特异性对于加标到阴性临床样品中的ivt的hpv31和33型两者均观察到非常好的分析灵敏度。对于两种hpv类型均以低至10个拷贝/反应的浓度获得100%阳性。在存在另一个靶标的情况下,还分析了这两个靶标的分析灵敏度。在hpv6、11、16、18、35、39、42、43、44、45、51、52、53、56、58、59、61、66、68、71和81型中的每一者的每次反应中存在1,000,000个拷贝的情况下,以每次反应30个拷贝对hpv31ivt和hpv33ivt进行检测,并且结果显示,在存在不具有交叉反应性的这些其他靶标的情况下,hpv31靶标和hpv33靶标均被有效地扩增。进一步分析了交叉反应性。用1,000,000个拷贝/hpv52、hpv58中的任一者或hpv52和hpv58两者的反应对阴性临床库(clinicalpool)加标。hpv31和hpv33扩增和检测反应大体上如上所述进行。这些样品中的每一个都没有观察到信号。通过用1,000,000个拷贝/若干其他hpv转录物的反应对阴性临床库加标,以1,000,000个拷贝/每次反应来设定相似的实验。hpv31和hpv33扩增和检测反应大体上如上所述进行。这些样品中的每一个都没有观察到信号。这些数据显示,这些其他hpv类型不存在交叉反应性,并且该测定法对hpv31和hpv33具有非常高的特异性。临床灵敏度和特异性在hpv31/33基因分型测定法中对临床样本(n=137)进行检验,以评估临床灵敏度和特异性。用线性阵列hpv基因分型检验(lineararrayhpvgenotypingtest)(洛杉矶罗氏分子诊断公司(la,rochemoleculardiagnostics))来执行hpvdna基因分型。该检验用作确定样品是否包含hpv31和/或hpv33的标准。只有有限数量的样品经检验呈hpv31dna阳性(n=13)或hpv33dna阳性(n=13)。总的说来,利用该有限的数据组,hvp31检测的临床灵敏度为84.6%。在la测定法中经检验呈hpv31dna阳性的两个样本在hpv31/33基因分型测定法中呈阴性。两个样本均包含hpv31dna连同另外的hpv低风险类型。使用aptimahpv筛查测定法,检验得出两个样本均呈阴性,因此这两个样本包含任何hpv31mrna是极不可能的。hpv33检测的临床灵敏度为92.3%。在la测定法中经检验呈hpv33dna阳性的一个样本在hpv31/33基因分型测定法中呈阴性。该样本包含若干其他高风险hpvdna类型和低风险hpvdna类型。使用aptimahpv筛查测定法和hc2检验(美国马里兰州盖瑟斯堡的凯杰公司(qiagen,gaithersburg,md)),检验得出样本呈阴性,表明该样品包含任何hpv33mrna不太可能。hpv31的临床特异性为98.4%。根据la测定法为hpv31阴性的两(2)个样本,在使用hpv31/33基因分型测定法检验时,呈阳性。两个样本均包含另外的hpv高风险类型,并且在使用aptimahpv筛查测定法和hc2检验(凯杰公司(qiagen))检测时呈阳性。hpv33的特异性为100%。临床样本检验结果的总结示于下表2和3中。表2:临床样本的hpv31检验结果根据la测定法的hpv31结果表3:临床样本的hpv33检验结果根据la测定法的hpv33结果序列表4:示例性的低聚物序列、参考序列和区域根据前面所述,应当理解,虽然本文已出于举例说明的目的描述了本发明的具体实施例,但是在不脱离本发明的精神和范围的情况下,可以作出各种修改。因此,本发明仅受所附权利要求书限制。本文引用的所有出版物、专利和专利申请据此全文以引用方式并入以用于所有目的。当前第1页1 2 3
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1