一种利用PCR-ELISA检测具核梭杆菌的方法与流程
本发明涉及分子生物学检测技术领域,更具体的说是涉及一种利用pcr-elisa检测具核梭杆菌的方法。
背景技术:
具核梭杆菌(fusobacteriumnucleatum,f.nucleatum)是一种革兰氏阴性无芽孢厌氧杆菌,由于其形态中间膨大,两端尖细如梭,故名为梭杆菌。f.nucleatum不容易培养,对环境的要求较高,在培养时需要创造严格的厌氧环境,一般在含有5%氢气、5%二氧化碳、90%氮气的厌氧箱中生长较好。除此之外,其对营养要求也比较苛刻,一般采用厌氧血平板培养,48小时以后形成直径约为1-2mm、圆形、表面不平、中间凸起、半透明的菌落,散发恶臭。显微镜之父列文虎克于1893年在牙菌斑中首次发现f.nucleatum,其能够引起口臭及牙周炎,是口腔中的一种常在菌,还能够引起人体肝、肺、血液、关节等部位的感染,与食管癌、口腔癌、胃癌的发生密切相关。f.nucleatum具有许多特征性的因子,最典型的为foma、fap2及fada,其中fada为f.nucleatum的一个黏附素,基因全长390bp,是一个高度保守的基因,与已知的其他类型黏附素没有同源性,其可分为两种形式,一为未分泌形式的fada(pre-fada)以及分泌形式的成熟fada(mfada),pre-fada由129个氨基酸残基构成,含有一个18个氨基酸组成的信号肽,mfada由111个氨基酸残基构成,可存在于酸性环境,两种形式可以结合形成复合物,是具核梭杆菌附着及侵入宿主细胞必需的毒力因子。
目前,f.nucleatum的检测常以pcr为主,包括常规pcr及多重pcr技术,常规pcr技术操作简便,被广泛应用,但是常规pcr需要用溴化乙锭染色,存在一定的危险性,而且,电泳结果单纯靠肉眼观察,敏感性不强;多重pcr技术则需要设计多对引物,不好掌握。此外,环介导等温扩增技术(loop-mediatedisothermalamplification,lamp)是一种新兴的扩增技术,利用lamp检测具核梭杆菌,成本较低,但是对引物要求较高,适用范围小,假阳性问题也比较严重。
因此,提供一种利用pcr-elisa检测具核梭杆菌的方法是本领域技术人员亟需解决的问题。
技术实现要素:
有鉴于此,本发明提供了一种利用pcr-elisa检测具核梭杆菌的方法,具有敏感性高、特异性好、准确度高、安全、快捷等优点,适用于样品的大批量检测。
为了实现上述目的,本发明采用如下技术方案:
一种以非诊断治疗为目的利用pcr-elisa检测具核梭杆菌的特异性引物,所述引物序列如下:
f:5’-cacaagctgacgctgctaga-3’;seqidno.1;
r:5’-ttaccagctcttaaagcttg-3’;seqidno.2;
所述上游引物f的5’端用地高辛标记,所述下游引物r的5’端用生物素标记。
进一步,一种以非诊断治疗为目的利用pcr-elisa检测具核梭杆菌的方法,具体步骤如下:
(1)提取样品基因组dna;
(2)利用权利要求1所述的特异性引物,对步骤(1)获得的模板进行pcr扩增,获得pcr产物;
(3)elisa检测:链霉亲和素按1:800稀释包板,37℃孵育15min,2%的bsa37℃封闭15min,一抗37℃反应30min,二抗按1:2000稀释,37℃反应30min,最终显色7min;
(4)确定pcr-elisa的临界值。
进一步,步骤(2)所述pcr扩增的反应程序为:94℃5min;94℃30s,59℃30s,72℃30s,30个循环;72℃10min;4℃保存。
进一步,步骤(4)所述确定pcr-elisa的临界值:检测样品od450值大于或者等于0.111时判定为阳性样品,小于0.111时则为阴性样品。
经由上述的技术方案可知,与现有技术相比,本发明公开提供了一种以非诊断治疗为目的利用pcr-elisa检测具核梭杆菌的方法,采用链霉亲和素-生物素-地高辛-抗地高辛抗体系统,检测敏感性为常规pcr的100倍,而且不与其他细菌如金黄色葡萄球菌、肉毒梭菌、沙门氏菌等产生交叉反应,特异性较好,批间及批内变异系数均低于10%,本发明建立的具核梭杆菌pcr-elisa检测方法敏感性、特异性、重复性均较好。
附图说明
为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本发明的实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据提供的附图获得其他的附图。
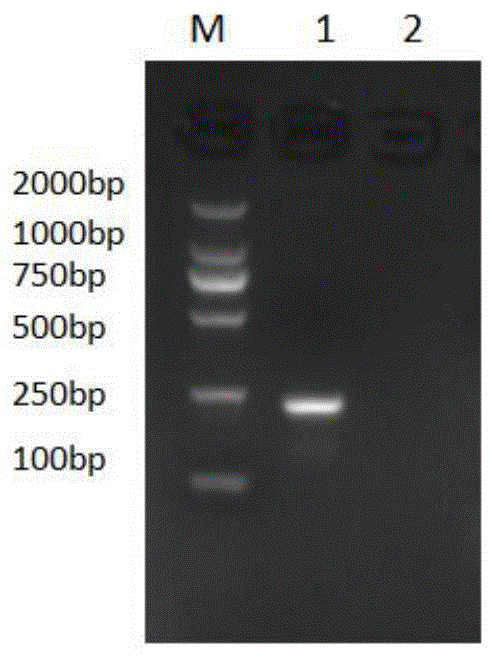
图1附图为本发明fada基因扩增的电泳结果;
其中,m:dl-2000dnamarker;1:目的基因;2:阴性对照;
图2附图为本发明重组质粒测序后的比对结果;
图3附图为本发明pcr敏感性检测电泳结果;
其中,m:dl-2000dnamark;1-11分别是重组质粒稀释浓度:5.86×1011copies/μl、5.86×1010copies/μl、5.86×109copies/μl、5.86×108copies/μl、5.86×107copies/μl、5.86×106copies/μl、5.86×105copies/μl、5.86×104copies/μl、5.86×103copies/μl、5.86×102copies/μl、5.86×101copies/μl。
具体实施方式
下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
具核梭杆菌冻干粉,由美国康奈尔大学提供;阴性对照为经pcr检测为具核梭杆菌fada基因阴性的基因组dna;被检的4份样本为新乡市中心医院提供的结直肠癌患者3份粪便及1份组织。
粪便dna提取试剂盒、质粒提取试剂盒、细菌基因组dna提取试剂盒均购自omega生物技术有限公司;extaqdna聚合酶、pmd-18-tvector、dnamarker均购自大连宝生物有限公司;链霉亲和素、牛血清白蛋白购自上海生物工程技术有限公司;tmb单组份显色液购自sigma公司;辣根过氧化物酶标记的抗地高辛抗体购自鼎国公司。
实施例1fada基因的pcr扩增
根据genebank中f.nucleatum的fada基因设计一对特异性引物,交由上海生物工程有限公司合成。
引物序列如下:
f:5’-cacaagctgacgctgctaga-3’;seqidno.1;
r:5’-ttaccagctcttaaagcttg-3’;seqidno.2。
将f.nucleatum冻干粉活化,用胰酪蛋白胨大豆液体培养基在厌氧箱中操作,收集菌液,提取f.nucleatum基因组dna,以其为模板pcr扩增fada基因。
其中,pcr反应体系为:模板2μl,上游引物0.5μl,下游引物0.5μl,premixtaq25μl,双蒸水22μl。
pcr反应条件为:94℃5min;94℃30s,59℃30s,72℃30s,30个循环;72℃10min;4℃保存。
用1.5%的琼脂糖凝胶对扩增产物进行电泳检测,结果见图1,与预期片段大小232bp一致。
实施例2重组质粒的构建
将扩增的目的基因连接pmd-18-t载体,并转化dh5α细胞,构建重组质粒;将构建的重组质粒送上海生物工程有限公司进行测序,从ncbi上下载具核梭杆菌fada全基因组序列,并用dnaman序列分析软件进行比对,结果显示一致性为100%(图2),与预期结果一致,目的片段大小为232bp。
实施例3pcr-elisa检测
(1)对实施例1的引物进行标记,其中,上游引物f的5’端用地高辛标记,下游引物r的5’端用生物素标记;以实施例2构建的重组质粒为模板,按照实施例1的条件进行pcr扩增,然后进行elisa检测。
(2)将链霉亲和素母液(1mg/ml)用ph为9.5的碳酸盐缓冲液进行稀释,并按每孔100μl加入酶标板包被,每个样品三个重复,4℃过夜;用pbst洗涤3次,每次3min;用2%的bsa进行封闭,每孔200μl,37℃放置2h,同样洗板3次;将以重组质粒为模板的扩增产物用pbst进行稀释,每孔100μl,37℃放置1h,洗板4次,每次3min;将辣根过氧化物酶标记的抗地高辛抗体用pbst进行稀释,每孔100μl,37℃放置1h,洗板5次,每次3min;加入tmb单组份显色液,每孔50μl,室温避光显色10min;加入2mh2so4终止液,每孔50μl,放置于酶标仪测od450的值。
(3)pcr-elisa反应条件
链霉亲和素按1:800稀释包板(浓度为1.25ng/μl),37℃孵育15min,2%的bsa37℃封闭15min,一抗37℃反应30min,二抗按1:2000稀释,37℃反应30min,最终显色7min。
在同样的条件下,分别对各反应条件进行对比试验:
a、将链霉亲和素母液按1:50、1:100、1:200、1:400、1:1600、1:3200稀释,结果见表1。
表1链霉亲和素包被浓度
表1结果表明,采用本发明的包被浓度1:800,浓度1.25ng/μl,od450的值(阳性均值)最接近于1且阴性值较小。
b、链霉亲和素包被条件分别为:4℃过夜、37℃2h、37℃1h、37℃45min、37℃30min、37℃10min,结果见表2。
表2链霉亲和素包被条件
表2结果表明,采用本发明的链霉亲和素包被条件37℃孵育15min,od450的值(阳性均值)最接近于1且阴性值较小。
c、封闭时间分别为:10min、30min、45min、1h、2h,结果见表3。
表3封闭时间
表3结果表明,采用本发明的封闭时间15min,od450的值(阳性均值)最接近于1且阴性值较小。
d、一抗反应时间分别为:5min、10min、15min、45min、1h,结果见表4。
表4一抗反应时间
表4结果表明,采用本发明的一抗反应时间30min,od450的值(阳性均值)最接近于1且阴性值较小。
e、二抗反应浓度按1:500、1:1000、1:4000、1:8000、1:16000、1:32000稀释,结果见表5。
表5二抗反应浓度
表5结果表明,采用本发明的二抗反应浓度1:2000,od450的值(阳性均值)最接近于1且阴性值较小。
f、二抗反应时间分别为10min、15min、45min、1h,结果见表6。
表6二抗反应时间
表6结果表明,采用本发明的二抗反应时间30min,od450的值(阳性均值)最接近于1且阴性值较小。
g、显色时间分别为1min、3min、5min、10min、15min,结果见表7。
表7显色时间
表7结果表明,采用本发明的显色时间7min,od450的值(阳性均值)最接近于1且阴性值较小。
(4)阳性、阴性临界值的确立
取30份普通pcr检测为阴性的样品,应用已建立的pcr-elisa方法进行检测,测定其od450的值。根据公式:临界值=检测样品平均值(x)+3标准偏差(sd),大于或者等于临界值的样品为具核梭杆菌阳性,反之为阴性。
链霉亲和素按1:800稀释包板(浓度为1.25ng/μl),37℃孵育15min,2%的bsa封闭37℃15min,一抗37℃反应30min,二抗按1:2000稀释,37℃反应30min,最终显色7min。在该反应条件下,对30份f.nucleatumpcr检测为阴性的样品进行pcr-elisa检测,30份阴性样品的od450值分别为:0.076、0.065、0.087、0.090、0.067、0.090、0.064、0.086、0.083、0.075、0.058、0.079、0.069、0.089、0.094、0.096、0.068、0.054、0.088、0.068、0.077、0.087、0.089、0.070、0.062、0.082、0.072、0.054、0.060、0.059,30份阴性样品od450的平均值为0.075,标准方差为0.012,根据公式:临界值=x+3sd,求得临界值为0.111,即大于0.111为阳性,反之为阴性。
实施例4敏感性试验
将构建成功的重组质粒母液按倍比稀释,分别以不同浓度作为模板进行pcr和pcr-elisa检测,比较其敏感性。
将构建好的阳性重组质粒(质粒浓度为149ng/μl,换算成拷贝数为5.86×1011copies/μl)依次按10倍进行稀释,即5.86×1011copies/μl-5.86×101copies/μl,分别以不同的浓度为模板进行pcr及pcr-elisa检测。pcr检测结果见图3,结果表明pcr能够检测到5.86×106copies/μl,pcr-elisa检测结果见表8,结果表明pcr-elisa方法最低能够检测到5.86×104copies/μl;上述结果表明pcr-elisa的检测方法比pcr检测方法灵敏度高100倍。
表8pcr-elisa敏感性检测结果
根据大于临界值0.111判定为阳性,pcr-elisa可检测到5.86×104copies/μl。
实施例5特异性试验
为了验证所建立的pcr-elisa检测方法的特异性,利用pcr-elisa方法分别对f.nucleatum、大肠杆菌(escherichiacoli)、金黄色葡萄球菌(staphylococcusaureus)、肉毒梭菌(clostridiumbotulinum)、沙门氏菌(salmonellatype)、三联疫苗(a型产气荚膜梭菌、d型产气荚膜梭菌、魏氏梭菌)进行检测,结果见表9。
表9pcr-elisa特异性检测结果
注:+号表示阳性,-号表示阴性,根据大于临界值0.111判定为阳性。
根据pcr-elisa检测结果可知,只有f.nucleatum结果显示为阳性,其他细菌均显示阴性,且结果不出现交叉反应,说明pcr-elisa检测方法特异性良好。
实施例6重复性评价
以4份阳性样品及1份阴性样品的dna为模板进行pcr-elisa试验,并使用同一时间包被的酶标板进行批内重复试验及不同时间包被的酶标板进行批间重复试验,批间和批内试验使用相同的样品,每个样品设置三个重复,通过对检测结果进行分析进而确定该方法的重复性效果,批间重复性试验结果见表10,批内重复性试验结果见表11。
表10批间重复性试验
注:平均数及标准差均保留三位小数。
表11批内重复性试验
注:平均数及标准差均保留三位小数。
重复性试验结果表明,pcr-elisa检测方法批间变异系数为1.20%-6.99%,批内变异系数为6.07%-8.72%,均低于10%,说明重复性较好。
实施例7样品检测
用所建立的pcr-elisa的方法及pcr方法对临床样本进行检测,比较其结果的可靠性。
由于临床样品较难采集,暂共有三份结直肠癌患者粪便样品及组织样品一份,用所建立的pcr-elisa的检测方法对4份样品进行检测,结果pcr-elisa及pcr方法均在组织样品中检出f.nucleatum,粪便样品中未检出,阳性检出率为25%,此外,粪便样品中菌落经测序鉴定结果为卵形拟杆菌。
对所公开的实施例的上述说明,使本领域专业技术人员能够实现或使用本发明。对这些实施例的多种修改对本领域的专业技术人员来说将是显而易见的,本文中所定义的一般原理可以在不脱离本发明的精神或范围的情况下,在其它实施例中实现。因此,本发明将不会被限制于本文所示的这些实施例,而是要符合与本文所公开的原理和新颖特点相一致的最宽的范围。
序列表
<110>新乡学院
<120>一种利用pcr-elisa检测具核梭杆菌的方法
<160>2
<170>siposequencelisting1.0
<210>1
<211>20
<212>dna
<213>artificialsequence
<400>1
cacaagctgacgctgctaga20
<210>2
<211>20
<212>dna
<213>artificialsequence
<400>2
ttaccagctcttaaagcttg20
- 还没有人留言评论。精彩留言会获得点赞!