一种用于检测新型冠状病毒的单克隆抗体及其制备试剂盒的用途的制作方法
本发明属于生物检测领域,具体涉及一种用于检测新型冠状病毒的单克隆抗体及其制备试剂盒的用途。
背景技术:
人感染了冠状病毒后常见体征有呼吸道症状、发热、咳嗽、气促和呼吸困难等。在较严重病例中,感染可导致肺炎、严重急性呼吸综合征、肾衰竭,甚至死亡。虽然目前对于新型冠状病毒所致疾病没有特异治疗方法,但是轻症、或者无症状患者通过治疗可以大大的提高治愈率,缩短治疗时间。因此,对患者的检测或者鉴定变的尤为重要。
快速准确地诊断传染病是控制疾病暴发的关键因素。随着新型冠状病毒(2019-ncov)感染人数的不断增加,许多体外诊断公司都推出了新型冠状病毒检测试剂盒,而许多生物公司则通过提供检测试剂而加入了竞争。
但是核酸检测在准确性和灵敏度上还有改进的空间。因此,抗体检测试剂盒变得更为重要。新型冠状病毒基因编码多个结构蛋白,例如n蛋白、e蛋白和s蛋白等,这些蛋白包括多个抗原表位,利用抗原与抗体特异性结合的原理,可通过抗体检测抗原的存在,从而直接证明样本中含有新型冠状病毒。新型冠状病毒的上述抗原,可作为免疫原,在病毒感染人体后,刺激浆细胞产生特异性抗体,利用抗原与抗体特异性结合的原理,可通过抗原检测抗体的存在,从而间接证明人体已感染新型冠状病毒。抗体检测试剂的适用样本类型一般为血液,包括血清、血浆和全血。
检测的抗体主要分为igm和igg两类。目前对新型冠状病毒的这两类抗体的产生和持续时间尚缺乏系统性研究。通常情况下,igm抗体产生早,一经感染,快速产生,维持时间短,消失快,血液中检测阳性可作为早期感染的指标。igg抗体产生晚,维持时间长,消失慢,血液中检测阳性可作为感染和既往感染的指标。
因此,开发抗体检测试剂盒变得尤为重要。
技术实现要素:
本发明提供一种具有较好免疫原性的冠状病毒n蛋白,其核苷酸序列如其核苷酸序列如seqidno:1所示:
其氨基酸序列如seqidno:2所示:
本发明另外提供一种表达n蛋白的方法,包括克隆所述的n蛋白基因,在大肠杆菌中表达,并纯化获得相应的n蛋白。
本发明另外提供一种制备n蛋白特异性的单克隆抗体的方法,包括以n蛋白作为免疫原进行免疫小鼠,制备并获得所述的单克隆抗体。
本发明首先用n蛋白免疫小鼠,再用免疫成功小鼠的脾脏淋巴细胞与骨髓瘤细胞融合,通过筛选阳性克隆得到特异性分泌抗n蛋白单克隆抗体杂交瘤细胞株,用于大量生产抗n蛋白单克隆抗体,并通过蛋白纯化的方式制备得到高纯度的抗n蛋白单克隆抗体。
本发明具体的涉及一种单克隆抗体,其中该抗体的重链可变区氨基酸序列为seq.id.no.9:
qiqlqqsgaslvrpgalvklsckasdshyysqslhwvkqrpvqglewigdigsadnstkyappflgkaqitadtssntaylqlssltsedtavyyciryassgwgwgqgttltvss。
轻链可变区序列氨基酸序列为seq.id.no.10:
divitqspalmadspgekvtitcdyseeismsylawyqqssgispkpwiyttaglapgvparfsgsgsgtsysltitsaeaedaatyycssasslpcrfgagtklelk。
本发明还提供所述抗n蛋白单克隆抗体的应用,所述应用为制备elisa试剂盒。
本发明所述抗n蛋白单克隆抗体的应用,具体为用于免疫学检测,具体的为检测n蛋白,从而鉴定是否存在冠状病毒。
本发明的有益效果:
n蛋白是冠状病毒重要的标志蛋白,检测n蛋白能够实现冠状病毒的检测。本发明得到的抗n蛋白单克隆抗体具有特异性高,可大量生产的特点,所得抗体的效价较高。本发明所得到的抗n蛋白单克隆抗体能够特异性的结合n蛋白,可用于细胞的免疫学检测,具有广阔的市场前景,具有重要的临床意义。
附图说明
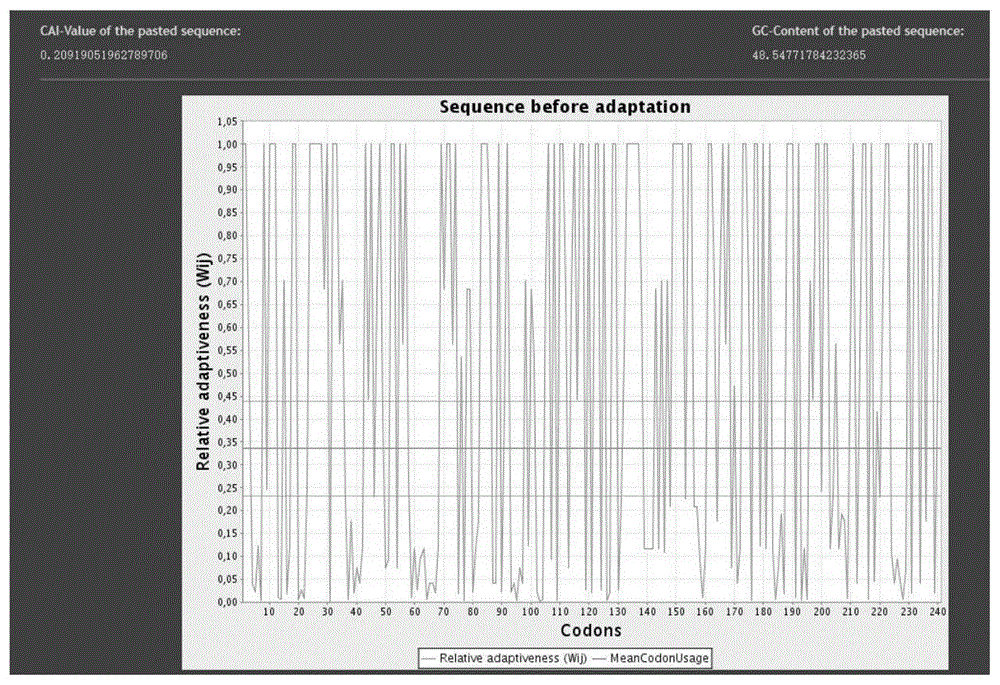
图1为n蛋白基因优化前后对比图,1a为优化前的图,1b为优化后的图。
图2为抗体效价结果图;其中深色柱形为抗体,浅色柱形为对照。
图3mab单克隆抗体对n蛋白进行westernblot实验结果。1为自制marker,2-4分别是空白宿主菌bl21(de3)的裂解物,空白宿主菌bl21(de3)的裂解物,空质粒裂解物,5是n蛋白。
具体实施方式
下面将结合实施例对本申请的实施方案进行详细描述,但是本领域技术人员将会理解,下列实施例仅用于说明本申请,而不应视为限制本申请的范围。实施例中未注明具体条件者,按照常规条件或制造商建议的条件进行。所用试剂或仪器未注明生产厂商者,均为可以通过市购买获得的常规产品。
实施例1n蛋白的表位优化
根据2019-ncov已经公开的全基因组序列,针对其中的n蛋白氨基酸序列肽设计优化的n蛋白表位氨基酸序列。通过clustalw(version1.81)软件多序列比对中国株、意大利株等不同株系的5种氨基酸序列分析序列并根据dnastar分析其免疫原性、亲水性和表面可能性及相关二级结构。通过modeller同源建模,构建蛋白三维结构,进一步分析免疫原多肽的表面可能性,通过moe软件模拟抗体结合表位肽,解析相互作用氨基酸,筛选获得了具有较好免疫原性的n蛋白序列,并且从图1a和图1b的对比来看,图1b优化了的密码子序列使得其中gc含量为50.40,更加适合蛋白表达。
其核苷酸序列如seqidno:1所示:
其氨基酸序列如seqidno:2所示:
实施例2n蛋白的表达
根据优化后的n蛋白核苷酸序列设计特异性引物,分别在引物的5’端加入保护性碱基和限制性内切酶,引物序列如下:
f:5'-cgcggatccatgaaagacctgtctccgcg-3'(seq.id.no.3):
r:5'-ccggaattcgtcgtccagtttgatagcac-3'(seq.id.no.4):
以优化后的通过全基因合成的n蛋白基因为模板(上海生工合成),用上述特异性引物进行pcr扩增。
pcr反应程序为:94℃预变性2min;94℃变性10sec,55℃退火35sec,67℃延伸1min10s,35个循环;68℃延伸7min,4℃保存。
pcr反应体系:2×pcrbuffer12.5μl,2mmdntps5μl,10mmrprimer0.75μl,10mmfprimer0.75μl,ndna1μl,dh2o5μl。
将扩增产物使用限制性内切酶bamhi和ecori和载体pcoldi分别进行双酶切,酶切体系为9.5μlpcr产物或载体,0.5μlbamhi,0.5μlecori,8.5μldh2o。37℃条件下,反应1h。酶切产物进行1%琼脂糖凝胶电泳,采用takara公司的琼脂糖凝胶dna纯化试剂盒回收纯化。
采用takara公司的连接试剂盒dnaligationkit(mightymix〉将酶切产物n基因、pcoldi进行连接,制备重组原核表达载体pcold-n。n、pcoldi的mol数比约为3:1。16℃,连接1小时。将连接产物通过热激转化的方式转化入大肠杆菌感受态细胞dh5α,37℃过夜培养。选取菌落pcr和酶切鉴定均阳性的阳性质粒进行测序鉴定,经鉴定,所述序列与seqidno:1保持一致。
将测序正确的质粒pcold-n通过热激转化的方式转化入表达型的大肠杆菌感受态细胞bl21(de3)。菌落pcr确定阳性菌,即含重组表达质粒pcold-ns3的表达菌。将含重组表达质粒pcold-ns3的表达菌接种至自诱导表达培养基中诱导表达,所述自诱导培养基为overnightexpresstminstantlbmedia,诱导表达的步骤:取少量菌液接种至3ml含amp的lb液体培养基中,37℃过夜培养。取过夜培养的菌液按照1:100的量加入到含amp的自诱导培养基中,17℃条件下,诱导时间22h。表达产物用qiagenhis标签蛋白纯化试剂盒进行重组蛋白的纯化,随后进行sds-page分析,结果显示,本发明的方法使该蛋白占总表达蛋白量的51%以上,表达量极其显著。配置纯化后的蛋白浓度为0.5mg/l备用。
实施例3单克隆抗体的制备
balb-c小鼠15只,雌性,8周,体质量(20±2)g,由扬州大学实验动物中心提供。随机分为3组,每组5只。以实施例2获得n蛋白为免疫原,与等量弗氏完全佐剂充分乳化后,按70μg/只的抗原量在小鼠皮下多点注射,2周后用弗氏不完全佐剂乳化抗原进行第2次免疫,3次免疫后检测elisa效价>1:1万后,用50g抗原腹腔冲击免疫,3~4d后融合。
无菌取小鼠脾脏,制备脾细胞,用体积分数50%peg4000将脾细胞与对数生长期的骨髓瘤sp2/o细胞进行融合;融合后的细胞用hat培养基悬浮,96孔板内置37℃、体积分数5%co2培养箱内培养,5d后用ht换去1/2hat培养基,7~10d后改用ht培养基,定期观察,第2~3次换液后2d采用间接elisa法筛选阳性克隆,采用有限稀释法继续2次亚克隆。采用n蛋白包被elisa板,经elisa结果筛选,3次亚克隆后取形态良好、生长旺盛、反应稳定的阳性单克隆细胞系,命名为n-32。采用饱和硫酸铵盐析法纯化腹水。紫外分光光度计进行蛋白定量。纯化得到mab浓度为2.0g/l。
实施例4mab的鉴定
(1)亚类鉴定:将羊抗鼠igg、igg1、igg2a、igg2b、igg3和igm与浓缩10倍的杂交瘤细胞培养上清进行免疫双扩散,观察沉淀线的形成。免疫双扩散检测该株mab为igg2a亚型。
(2)效价及相对亲和力的测定:
效价测定:
用ph9.6,0.05mol/l的碳酸盐缓冲液将n蛋白稀释为1μg/ml,包被酶标板,100μl/孔,4℃过夜;用样本稀释液(含有0.5%牛血清白蛋白的磷酸盐缓冲液)将以上单克隆抗体按1:103、1:104、1:105、1:106、1:107、1:108、1:109、1:1010稀释,100μl/孔,37℃孵育1h;取出酶标板,经tbs-t洗涤3次,拍干酶标板,每孔加入100μl1:5000稀释的hrp标记的山羊抗小鼠二抗,37℃孵育30min;经tbs-t洗涤5次后,每孔加入100μl加入tmb底物显示液,37℃避光显色10-15min,随后加入50μl终止液终止反应,于酶标仪450nm波长下读取吸光值,结果如图2所示,本发明中纯化后的单克隆抗体的效价均达到8.6×10-9。
亲和力鉴定:以被检mab的不同浓度为横坐标,以其相应的a值为纵坐标绘出测定曲线,曲线上部趋于平坦段的a值为100%,以a值为50%点的mab浓度表示mab的相对亲和力。结果显示,采用间接elisa法测定得到的mab的相对亲和力为1.835×10-10mol/l,显示了较好的亲和力。
(3)特异性鉴定:mab与n蛋白的结合活性采用westernblot法:将纯化的n蛋白进行sds-page,再将凝胶蛋白带电转移至硝酸纤维素膜上,依次与mab及hrp-羊抗鼠igg反应后以dab显色,mab与hbv、hev及hcv抗原的相应n蛋白抗原进行交叉反应性检测,采用间接elisa。
如图3的westernblot鉴定表明,mab可识别mr为大约20-30kd的条带,说明是与目的n蛋白进行的结合;而与宿主菌bl21(de3)的裂解物,空质粒裂解物均无交叉反应。通过间接elisa法测定了mab与hbv、hev及hcv抗原的相应n蛋白抗原均无结合反应。
实施例5mab序列的鉴定
收集实施例3中的筛选后的杂交瘤细胞,利用thermo公司的trizol提取杂交瘤细胞总rna,按南京诺唯赞公司的hiscriptqrtsupermixforqpcr(+gdnawiper)说明书的操作方案将mrna逆转录为cdna,-20℃冻存备用。逆转录反应体系为5μlrna(2500ng),10μl4×gdna,10μl5×supermixⅱ,加ddh2o补足至50μl,总反应体积为50μl。
以cdna为模板,通过ncbi数据库查找鼠源重链fr1区及铰链区基因序列,根据序列设计重链pcr引物,上游序列为(seq.id.no.5):gcgctcgagcagktccagctgaagcagtc,下游序列为(seq.id.no.6):gcgactagtgcatttgcatggaggacag;同样通过ncbi数据库查找鼠源轻链fr1区及恒定区基因序列(nc000072.6),设计轻链pcr引物,上游序列为(seq.id.no.7):gcggagctcgatrttgtgatgacccarac,下游序列为(seq.id.no.8):gcgtctagactcattcctgttgaagctct,分别pcr获得抗体的轻链和重链片段。按南京诺唯赞公司的phantamaxsuper-fidelitydnapolymerase说明书的操作方案进行pcr,pcr反应体系为:25μl2×phanta,1μldntp,4μl10μm引物对,4μl杂交瘤细胞cdna,1μldnapolymerase,15μlddh2o,总反应体积为50μl。扩增条件为:预变性94℃,3min;变性94℃,30s;退火64℃,30s;延伸72℃,5min。按照omega公司omegagelextractionkit说明书对pcr产物进行胶回收,进行测序分析,获得杂交瘤细胞的重链可变区氨基酸序列为seq.id.no.7,轻链可变区序列氨基酸序列为seq.id.no.8。
重链可变区氨基酸序列为seq.id.no.9:
qiqlqqsgaslvrpgalvklsckasdshyysqslhwvkqrpvqglewigdigsadnstkyappflgkaqitadtssntaylqlssltsedtavyyciryassgwgwgqgttltvss
轻链可变区序列氨基酸序列为seq.id.no.10:
divitqspalmadspgekvtitcdyseeismsylawyqqssgispkpwiyttaglapgvparfsgsgsgtsysltitsaeaedaatyycssasslpcrfgagtklelk。
应当理解的是,本发明在其应用上并不一定局限于在以下说明中所描述和/或在附图中所说明的组件的构造和布置的细节。本发明能够具有除所述和以不同方式实践或进行的那些实施方案之外的实施方案。而且,应理解本文所采用的短语和术语以及摘要出于描述目的并且不应视为限制性的。
这样,本领域技术人员将了解在基于本公开时的概念可容易用作设计用于执行本发明的若干目的的其他结构、方法和系统的基础。因此,重要的是权利要求书应被认为是包括此类等效结构至它们不背离本发明的精神和范围的程度。
序列表
<110>北京岳昊科技发展有限公司
<120>一种用于检测新型冠状病毒的单克隆抗体及其制备试剂盒的用途
<160>10
<170>siposequencelisting1.0
<210>1
<211>723
<212>dna
<213>2ambystomalateralexambystomajeffersonianum
<400>1
atgaaagacctgtctccgcgttggtacttctactacctgggtaccggtccggaagctggt60
ctgccgtacggtgctaacaaagacggtatcatctgggttgctaccgaaggtgctctgaac120
accccgaaagaccacatcggtacccgtaacccggctaacaacgctgctatcgttctgcag180
ctgccgcagggtaccaccctgccgaaaggtttctacgctgaaggttctcgtggtggttct240
caggcttcttctcgttcttcttctcgttctcgtaactcttctcgtaactctaccccgggt300
tcttctcgtggtacctctccggctcgtatggctggtaacggtggtgacgctgctctggct360
ctgctgctgctggaccgtctgaaccagctggaatctaaaatgtctggtaaaggtcagcag420
cagcagggtcagaccgttaccaaaaaatctgctgctgaagcttctaaaaaaccgcgtcag480
aaacgtaccgctaccaaagcttacaacgttacccaggctttcggtcgtcgtggtccggaa540
cagacccagggtaacttcggtgaccaggaactgatccgtcagggtaccgactacaaacac600
tggccgcagatcgctcagttcgctccgtctgcttctgctttcttcggtatgtctcgtatc660
ggtatggaagttaccccgtctggtacctggctgacctacaccggtgctatcaaactggac720
gac723
<210>2
<211>241
<212>prt
<213>2ambystomalateralexambystomajeffersonianum
<400>2
metlysaspleuserproargtrptyrphetyrtyrleuglythrgly
151015
proglualaglyleuprotyrglyalaasnlysaspglyileiletrp
202530
valalathrgluglyalaleuasnthrprolysasphisileglythr
354045
argasnproalaasnasnalaalailevalleuglnleuproglngly
505560
thrthrleuprolysglyphetyralagluglyserargglyglyser
65707580
glnalaserserargserserserargserargasnserserargasn
859095
serthrproglyserserargglythrserproalaargmetalagly
100105110
asnglyglyaspalaalaleualaleuleuleuleuaspargleuasn
115120125
glnleugluserlysmetserglylysglyglnglnglnglnglygln
130135140
thrvalthrlyslysseralaalaglualaserlyslysproarggln
145150155160
lysargthralathrlysalatyrasnvalthrglnalapheglyarg
165170175
argglyprogluglnthrglnglyasnpheglyaspglngluleuile
180185190
argglnglythrasptyrlyshistrpproglnilealaglnpheala
195200205
proseralaseralaphepheglymetserargileglymetgluval
210215220
thrproserglythrtrpleuthrtyrthrglyalailelysleuasp
225230235240
asp
<210>3
<211>29
<212>dna
<213>2ambystomalateralexambystomajeffersonianum
<400>3
cgcggatccatgaaagacctgtctccgcg29
<210>4
<211>29
<212>dna
<213>2ambystomalateralexambystomajeffersonianum
<400>4
ccggaattcgtcgtccagtttgatagcac29
<210>5
<211>29
<212>dna
<213>2ambystomalateralexambystomajeffersonianum
<400>5
gcgctcgagcagktccagctgaagcagtc29
<210>6
<211>28
<212>dna
<213>2ambystomalateralexambystomajeffersonianum
<400>6
gcgactagtgcatttgcatggaggacag28
<210>7
<211>29
<212>dna
<213>2ambystomalateralexambystomajeffersonianum
<400>7
gcggagctcgatrttgtgatgacccarac29
<210>8
<211>29
<212>dna
<213>2ambystomalateralexambystomajeffersonianum
<400>8
gcgtctagactcattcctgttgaagctct29
<210>9
<211>116
<212>prt
<213>2ambystomalateralexambystomajeffersonianum
<400>9
glnileglnleuglnglnserglyalaserleuvalargproglyala
151015
leuvallysleusercyslysalaseraspserhistyrtyrsergln
202530
serleuhistrpvallysglnargprovalglnglyleuglutrpile
354045
glyaspileglyseralaaspasnserthrlystyralaproprophe
505560
leuglylysalaglnilethralaaspthrserserasnthralatyr
65707580
leuglnleuserserleuthrsergluaspthralavaltyrtyrcys
859095
ileargtyralaserserglytrpglytrpglyglnglythrthrleu
100105110
thrvalserser
115
<210>10
<211>108
<212>prt
<213>2ambystomalateralexambystomajeffersonianum
<400>10
aspilevalilethrglnserproalaleumetalaaspserprogly
151015
glulysvalthrilethrcysasptyrserglugluilesermetser
202530
tyrleualatrptyrglnglnserserglyileserprolysprotrp
354045
iletyrthrthralaglyleualaproglyvalproalaargpheser
505560
glyserglyserglythrsertyrserleuthrilethrseralaglu
65707580
alagluaspalaalathrtyrtyrcysserseralaserserleupro
859095
cysargpheglyalaglythrlysleugluleulys
100105
- 还没有人留言评论。精彩留言会获得点赞!