一种制备环氧丙烷的方法与流程
1.本发明涉及一种制备环氧丙烷的方法。
背景技术:
2.环氧丙烷(po)是大宗化工原料,位列全球产量最大的50种化学品之中,是丙烯衍生物中产量仅次于聚丙烯的第二大有机化工产品。po化学性质十分活泼,用途广泛,被广泛应用于化工、轻工、医药、食品、纺织等行业,对化学工业及国民经济的发展具有深远的影响。
3.目前工业上生产环氧丙烷主要采用氯醇法和共氧化法,这两种方法的生产能力占世界总生产能力的80%以上。氯醇法较早应用于生产,该方法使用氯气,腐蚀严重并产生大量污染环境的含氯废水,不符合绿色化学和清洁生产的要求,因此随着环境保护要求的日益提高,该工艺将最终被淘汰。共氧化法主要用乙苯过氧化物或叔丁基过氧化氢等作为氧源,将丙烯间接氧化为po。共氧化法克服了氯醇法污染环境和腐蚀设备等缺点,是比氯醇法相对清洁的生产工艺。但联产大量的苯乙烯或叔丁醇等廉价副产品,副产品市场难以消化,加上工艺冗长、建设投资规模大,经济因素是制约其发展的主要原因。
4.以过氧化氢为氧化剂、钛硅分子筛为催化剂的方法可以有较高的丙烯转化率和po选择性。该方法简便,不污染环境,是极具竞争力的po生产过程,符合当代绿色化学和原子经济发展理念的要求,而被认为是生产po的绿色新工艺,是目前第三大的po生产方法。但是,由于h2o2极不稳定,遇热、光,粗糙表面,重金属及其它杂质会分解,且具有腐蚀性,在包装、储存、运输中要采取特别的安全措施。受到成本和安全问题的局限,且制备h2o2需要单独的设备和循环系统,耗资较大,现场生产费用很高,在没有更严格的环保法规出台之前,其经济优势不明显,这也是目前众多采用过氧化氢为氧化剂的生产装置没有投产或者满产的重要原因之一。
5.分子氧廉价易得且无污染,是最理想的氧源。但利用o2直接氧化丙烯,难以有效制备得到环氧丙烷。页岩气革命的成功,丙烷的供给大幅增加,如何利用丙烷也是目前产业界急需思考的问题,以丙烷为原料的直接氧化制备环氧丙烷新工艺二者兼顾,极具研究和产业化应用前景。
技术实现要素:
6.本发明的目的是提供一种制备环氧丙烷的方法,该方法能够直接以丙烷和氧气为原料制备得到环氧丙烷。
7.为了实现上述目的,本发明提供一种制备环氧丙烷的方法,该方法包括:
8.s1、在300~800℃、0~10mpa下,使丙烷与纳米碳基材料接触进行第一反应得到第一反应产物;
9.s2、在双功能催化剂及可选的溶剂存在下,使所述第一反应产物与氧气在0~80℃,0.1~10mpa下接触进行第二反应。
10.可选地,步骤s1中,所述第一反应的条件包括:温度为400~700℃,时间为0~5mpa,丙烷的体积空速为1~100h-1
。
11.可选地,步骤s2中,所述第一反应产物与所述氧气用量的摩尔比为1:(0.1~2),优选为1:(0.2~1);
12.所述第二反应的条件包括:温度为20~60℃,时间为0.5~5mpa。
13.可选地,将碳纳米管在0.1~5体积%的氨气气氛下于200-1000℃焙烧1-24h,得到所述纳米碳基材料。
14.可选地,所述双功能分子筛催化剂中含有pd、pt、au、ag和ru中的一种或几种贵金属元素;以所述双功能分子筛催化剂的干基重量为基准,所述贵金属元素的含量为0.05~10重量%。
15.可选地,所述双功能分子筛催化剂采用包括如下步骤的方法制备:将钛硅分子筛浸渍于含有贵金属元素的溶液中,在20~80℃下浸渍反应1~12小时;所述钛硅分子筛的硅钛比为10~100。
16.可选地,所述第二反应的总气体空速为10~10000h-1
,优选为100~5000h-1
。
17.可选地,步骤s2中,在溶剂存在下进行所述第二反应;
18.所述溶剂选自无机溶剂和/或有机溶剂;所述无机溶剂为去离子水;所述有机溶剂选自甲醇、乙醇、正丙醇、异丙醇、叔丁醇、异丁醇、丙酮、丁酮和乙腈中的一种或几种,优选为甲醇和/或去离子水。
19.可选地,所述溶剂与所述双功能分子筛催化剂用量的重量比为(10~1000):1,优选为(20~500):1。
20.可选地,所述环氧丙烷的选择性为50~100%,所述丙烷的转化率为20~50%。
21.通过上述技术方案,本发明的方法直接以丙烷和氧气为原料,可以以较高的转化率和选择性制备得到环氧丙烷。
22.本发明的其他特征和优点将在随后的具体实施方式部分予以详细说明。
具体实施方式
23.以下对本发明的具体实施方式进行详细说明。应当理解的是,此处所描述的具体实施方式仅用于说明和解释本发明,并不用于限制本发明。
24.本发明提供制备环氧丙烷的方法,该方法包括:
25.s1、在300~800℃、0~10mpa下,使丙烷与纳米碳基材料接触进行第一反应得到第一反应产物;
26.s2、在双功能催化剂及可选的溶剂存在下,使第一反应产物与氧气在0~80℃,0.1~10mpa下接触进行第二反应。
27.本发明的方法直接以丙烷和氧气为原料来制备环氧丙烷,方法简便易行、成本低廉,能够以较高的转化率和选择性制备得到环氧丙烷,特别适用于以丙烷为初始原料的环氧丙烷的工业化生产。
28.在一种优选的具体实施方式中,步骤s1中,第一反应的温度为400~700℃,压力为0~5mpa,丙烷的体积空速为1~100h-1
,优选5~50h-1
。
29.根据本发明,步骤s2中,第一反应产物与氧气用量的摩尔比可以在较大的范围内
变化,例如可以为1:(0.1~2),优选为1:(0.2~1)。在一种优选的具体实施方式中,步骤s2中,第二反应的温度为20~60℃,压力为0.5~5mpa。
30.根据本发明,对第一反应和第二反应采用的装置不做具体限制,第一反应和第二反应采用的装置可以各自独立地为固定床反应器、移动床反应器、微反应器或其他各类反应器。在一种优选的具体实施方式中,第一反应在固定床微型反应器中进行,第二反应在浆态床反应器内进行,采用上述方法可以进一步提高原料的转化率和对环氧丙烷的选择性。
31.根据本发明,纳米碳基材料可以为商购产品,也可以是对商购产品进行改性后得到的改性产品,优选地,纳米碳基材料是经过氨氮活化改性的多壁碳纳米管。在一种实施方式中,改性的多壁碳纳米管采用包括如下步骤的方法制备得到:将碳纳米管在0.1~5体积%优选1~2.5体积%的氨气气氛下于200-1000℃优选400-600℃焙烧1-24h。优选地,碳纳米管为多壁碳纳米管。氨气气氛中还可以含有氮气和/或惰性气体,惰性气体为本领域的技术人员所熟知的,例如可以为氦气、氩气等。
32.根据本发明,双功能催化剂中可以含有pd、pt、au、ag和ru中的一种或几种贵金属元素,优选为pd;以双功能催化剂的干基重量为基准,双功能催化剂含有的贵金属元素的含量可以在较大的范围内变化,例如可以为0.05~10重量%,优选为0.1~5重量%,余量为钛硅分子筛和可选的粘结剂。
33.在一种具体实施方式中,双功能催化剂可以采用包括如下步骤的方法制备:将钛硅分子筛浸渍于含有贵金属元素的溶液中,在20~80℃下浸渍反应1~12小时;含有贵金属元素的溶液中的贵金属可以以硝酸盐、乙酸盐、络合物和盐酸盐等中的一种或几种形式存在。
34.根据本发明,钛硅分子筛为本领域的技术人员所熟知,可以通过自行合成或商购的途经得到。钛硅分子筛的硅钛比可以在较大的范围内变化,例如可以为10~100,优选为20~50。
35.根据本发明,第二反应的总气体空速可以为10~10000h-1
,优选为100~5000h-1
,总气体是指第一反应产物与氧气的总量。
36.根据本发明,步骤s2中,在溶剂存在下进行第二反应;在一种具体实施方式中,溶剂选自无机溶剂和/或有机溶剂;无机溶剂可以为去离子水;有机溶剂可以选自醇、酮和腈中的一种或几种,例如可以为甲醇、乙醇、正丙醇、异丙醇、叔丁醇、异丁醇、丙酮、丁酮和乙腈中的一种或几种,优选为甲醇和/或去离子水。
37.根据本发明,溶剂与双功能催化剂用量的重量比可以为(10~1000):1,优选为(20~500):1。
38.根据本发明,丙烷的转化率可以为5~80%,环氧丙烷的选择性可以为50~100%,优选地,丙烷的转化率为20~50%,环氧丙烷的选择性为80~100%。
39.下面通过实施例来进一步说明本发明,但是本发明并不因此而受到任何限制。
40.实施例中所用到的试剂均为市售的化学纯试剂。
41.纳米碳材料为经过氨氮改性的多壁碳纳米管(cnt经过活化改性)。具体制备如下:利用管式炉将多壁碳纳米管在1体积%的氨气气氛下(余量为氮气)于600℃焙烧4h。
42.钛硅分子筛(ts-1)是按现有技术zeolites,1992,vol.12第943-950页中所描述的方法制备出的(ts-1)分子筛样品。
43.采用气相色谱法来分析得到的反应产物中各成分的含量,在此基础上分别采用以下公式来计算丙烷的转化率和环氧丙烷的选择性:
44.丙烷转化率=[(加入的丙烷的摩尔量-未反应的丙烷的摩尔量)/加入的丙烷的摩尔量]
×
100%;
[0045]
环氧丙烷选择性=[反应生成的环氧丙烷的摩尔量/(加入的丙烷的摩尔量-未反应的丙烷的摩尔量)]
×
100%。
[0046]
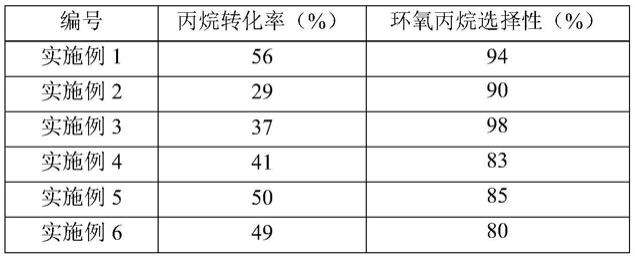
实施例1
[0047]
双功能(0.5重量%pd/ts)催化剂的制备过程如下:
[0048]
取钛硅分子筛(硅钛比为80)10克加入到20ml浓度为0.01g/ml的pdcl2水溶液中,在温度为40℃下搅拌24小时,其间适当密封,然后室温自然干燥48小时,即得到双功能(0.5重量%pd/ts)催化剂,使用前在5体积%的氢气(余量为氮气)混合气氛中、在温度为300℃的条件下还原活化3小时。
[0049]
制备环氧丙烷的过程如下:
[0050]
在常压600℃、丙烷体积空速为100h-1
下,将丙烷先经过以纳米碳基材料为催化剂床层的固定床微型反应器进行第一反应,将得到的第一反应产物与氧气、溶剂甲醇和双功能催化剂在浆态床反应器内按照第一反应产物与氧气的摩尔比为4:1,溶剂甲醇与双功能催化剂的重量比为50,在温度为60℃、压力为0.5mpa下,在总气体体积空速为1000h-1
下进行反应。将反应结束后得到的反应混合物进行气相色谱分析,并计算丙烷转化率、环氧丙烷的选择性。结果在表1中列出。
[0051]
实施例2
[0052]
采用与实施例1相同的方法制备环氧丙烷,不同之处仅在于,在常压400℃下,丙烷体积空速为5h-1
下,将丙烷先经过纳米碳基材料为催化剂床层的固定床微型反应器进行直接第一反应,将得到的第一反应产物与氧气、溶剂甲醇和双功能催化剂按照第一反应产物与氧气的摩尔比为2:1,溶剂甲醇与双功能催化剂的重量比为20,在温度为40℃、压力为2.5mpa下,在总气体体积空速为200h-1
下进行反应。
[0053]
实施例3
[0054]
采用与实施例1相同的方法制备环氧丙烷,不同之处仅在于,在常压500℃下,丙烷体积空速为25h-1
下,将丙烷先经过纳米碳基材料为催化剂床层的固定床微型反应器进行直接第一反应,将得到的第一反应产物与氧气、溶剂甲醇和双功能催化剂按照第一反应产物与氧气的摩尔比为10:1,溶剂甲醇与双功能催化剂的重量比为40,在温度为50℃、压力为1.5mpa下,在总气体体积空速为100h-1
下反应进行反应。
[0055]
实施例4
[0056]
采用与实施例1相同的方法制备环氧丙烷,不同之处仅在于,在6mpa、400℃下,丙烷体积空速为8h-1
下,将丙烷先经过纳米碳基材料为催化剂床层的固定床微型反应器进行第一反应。
[0057]
实施例5
[0058]
采用与实施例1相同的方法制备环氧丙烷,不同之处仅在于,第一反应产物与氧气的摩尔比为6:1。
[0059]
实施例6
[0060]
采用与实施例1相同的方法制备环氧丙烷,不同之处在于,取钛硅分子筛10克加入到10ml浓度为0.008g/ml的pdcl2水溶液中,在温度为40℃下搅拌24小时,其间适当密封,然后室温自然干燥48小时,即得到双功能(0.1重量%pd/ts)催化剂,使用前在5体积%的氢气(余量为氮气)混合气氛中、在温度为300℃的条件下还原活化3小时。
[0061]
实施例7
[0062]
采用与实施例1相同的方法制备环氧丙烷,不同之处在于,总气体体积空速为6000h-1
。
[0063]
对比例1
[0064]
采用与实施例1相同的方法制备环氧丙烷,不同之处在于,不用纳米碳基材料。
[0065]
对比例2
[0066]
采用与实施例1相同的方法制备环氧丙烷,不同之处在于,不用双功能催化剂。
[0067]
对比例3
[0068]
采用与实施例1相同的方法制备环氧丙烷,不同之处在于,不用纳米碳基材料和双功能催化剂。
[0069]
表1
[0070][0071][0072]
从对比例和实施例的结果可知,本发明可以直接以丙烷和氧气制备环氧丙烷,方法简便易行、成本低廉,且具有高的丙烷转化率和环氧丙烷选择性。
[0073]
以上详细描述了本发明的优选实施方式,但是,本发明并不限于上述实施方式中的具体细节,在本发明的技术构思范围内,可以对本发明的技术方案进行多种简单变型,这些简单变型均属于本发明的保护范围。
[0074]
另外需要说明的是,在上述具体实施方式中所描述的各个具体技术特征,在不矛盾的情况下,可以通过任何合适的方式进行组合,为了避免不必要的重复,本发明对各种可能的组合方式不再另行说明。
[0075]
此外,本发明的各种不同的实施方式之间也可以进行任意组合,只要其不违背本发明的思想,其同样应当视为本发明所公开的内容。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1