一种烷基黄原酸盐类重金属螯合剂及其合成方法与流程
[0001]
本发明属于重金属离子螯合剂技术领域,具体涉及一种烷基黄原酸盐类重金属螯合剂及其合成方法。
背景技术:
[0002]
随着工业技术的大力发展,电镀行业、化工行业的发展所带来的水污染问题日益突出,水污染中重金属的污染问题已经成为我们亟待解决的问题。这些废水中的重金属主要包括 cu
2+
、ni
2+
、zn
2+
、cd
3+
等,且这类重金属的存在形式不仅仅是游离态,往往更会和其他具有螯合能力的基团形成稳定的水溶性螯合物以螯合态在废水中长期存在。针对这类在废水中稳定存在的重金属螯合物,重金属螯合剂的研究和开发就显得尤为重要。螯合剂,一般以具有接受配体的孤对电子或π键电子的空轨道的原子或离子为中心,作为螯合物形成体(也称为中心离子或中心原子),在其周围排列有给出孤对电子或π键电子的一定数目的离子或分子作为配体,配合物形成体和配体形成具有一定的空间构型和特性的化学质点,这样形成的带电荷的复杂质点称为配离子,配离子与帯异电荷的离子组成的电中性化合物称为配合物。实际上通常把配离子也称为配合物。金属原子或离子与含有两个或两个以上配位原子的配体作用,生成具有环状结构的配合物,该配合物也称为螯合物,能生成螯合物的这种配位体物质,称为螯合剂,如下式:
[0003][0004]
黄原酸盐类重金属螯合剂,其反应机理是由含有-oh的小分子化合物与二硫化碳、氢氧化钠发生亲电取代反应,首先是由二硫化碳取代-oh上的氢原子,再使氢氧化钠与之成盐,从而使得-oh上得到具有螯合重金属离子作用的黄原酸基团,这类化合物在自然界中也广泛存在,比如淀粉和纤维素等。其反应式如下:
[0005][0006]
工业上使用最广泛的黄药是乙基到辛基的各种黄药,当碳原子数大于四时又称为高级黄药。黄药最常见就是被制备成为钠盐或钾盐的形式。传统小分子黄盐酸类重金属螯
合剂分子量,与重金属离子形成的螯合物体积小,不能自絮凝沉降,需另外添加絮凝剂,沉降析出速度慢,且絮凝剂的加入会对环境造成二次污染。因此,提供一种大分子量的高级黄药,与重金属离子形成大集团的螯合物,以更快速度沉降析出,是非常有必要的。
技术实现要素:
[0007]
本发明的目的在于提供了一种烷基黄原酸盐类重金属离子螯合剂及其合成方法,该螯合剂分子量大,可以与重金属形成大体积的螯合物,有利于快速沉降析出,且合成简单。
[0008]
为了解决上述技术问题,本发明采用以下技术方案:
[0009]
提供一种烷基黄原酸盐类重金属螯合剂,名称为2,4,6-(n-四甲基黄原酸钠)-4,6-(n
-ꢀ
二羟甲基氨基)-1,3,5-三嗪,分子式结构如下:
[0010][0011]
提供上述烷基黄原酸盐类重金属螯合剂的合成方法,化学反应方程式如下:
[0012][0013]
包括以下步骤:
[0014]
步骤1、在60~80℃条件下,将六羟甲基三聚氰胺溶于苛性碱溶液中,六羟甲基三聚氰胺和苛性碱的摩尔比为:1.0~1.5:5.5~6.5;
[0015]
步骤2、将步骤1得到的反应液降温至25~30℃,逐滴加入二硫化碳,滴加完毕后,在 25~30℃条件下继续保温反应1~6h,其中六羟甲基三聚氰胺和二硫化碳摩尔比为1.0~1.5: 5.5~6.5;
[0016]
步骤3、反应结束后,后处理即得烷基黄原酸盐类重金属螯合剂。
[0017]
按上述方案,所述步骤1中,六羟甲基三聚氰胺在苛性碱溶液中溶解时间为0.5~1.0h。
[0018]
按上述方案,所述步骤2中,控制二硫化碳的滴速为1~3ml/min。
[0019]
按上述方案,所述步骤3中,后处理工艺为:反应结束后,将反应液抽滤,滤饼经有机溶剂洗涤2~3次,烘干即得产物。优选地,有机溶剂为丙酮、甲醇、乙醇中的一种或几种。
[0020]
按上述方案,所述步骤1中,苛性碱溶液采用氢氧化钠溶液或氢氧化钾溶液中的任一种,苛性碱溶液的质量分数控制在35%~45%。
[0021]
本发明的有益效果为:
[0022]
1.本发明以六羟甲基三聚氰胺为合成原料,合成了一种新型的黄原酸盐重金属离子螯合剂,通过在六羟甲基三聚氰胺的羟基上引入黄原酸基团,使得其具有与重金属离子螯合的能力,与传统小分子黄盐酸类重金属螯合剂相比,本发明合成的螯合剂其分子量更大,与重金属离子形成的螯合物体积更大,可发生自絮凝沉降,以更快速度沉降析出,且无需添加絮凝剂,避免对环境的二次污染。
[0023]
2.本发明仅以水为溶剂并未使用有机溶剂参与反应,绿色环保,且在常压下即可进行操作,方法简单,操作方便,通过控制二硫化碳的滴加速度、反应温度、反应时间等参数控制反应进度,使反应更加充分,减少了硫代碳酸盐、金属硫化物等副产物的产生,所得产物产率较高,性质稳定,生产成本低。
附图说明
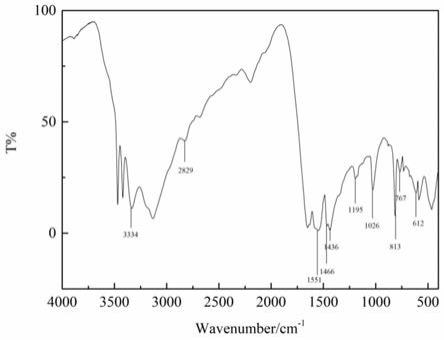
图1为实施例1制备得到的产物的红外谱图。图2为实施例1制备得到的产物的质谱图。
具体实施方式
[0024]
下面结合具体实施方式,对本发明作进一步详细说明,此处所述的优选实施例仅用于说明和解释本发明,并不用于限定本发明。
[0025]
实施例1
[0026]
一种2,4,6-(n-四甲基黄原酸钠)-4,6-(n-二羟甲基氨基)-1,3,5-三嗪的制备方法,包含如下步骤:
[0027]
步骤一、在装有机械搅拌、冷凝管、恒压滴液漏斗的三口烧瓶中,加入38%氢氧化钠溶液和六羟甲基三聚氰胺,60℃下搅拌0.5h,其中六羟甲基三聚氰胺:苛性碱溶液的摩尔比为1.0:5.5。
[0028]
步骤二、将步骤一的反应液温度降至25℃,往恒压滴液漏斗中加入适量二硫化碳,然后向反应液中逐滴滴加二硫化碳,控制滴速在1ml/min,其中六羟甲基三聚氰胺和二硫化碳摩尔比为1.0:6.0。
[0029]
步骤三、步骤二中二硫化碳滴加结束后,在25℃条件下继续保温反应4h,然后将反应液进行抽滤,滤饼经有机溶剂洗涤2~3次,最后于50℃下烘干即得产物。
[0030]
经经验分析,本实施例所制备的固体产物质量百分比含量为88.54%,反应收率为 89.05%。
[0031]
产物2,4,6-(n-四甲基黄原酸钠)-4,6-(n-二羟甲基氨基)-1,3,5-三嗪的红外谱图见图1,红外分析见表1,其质谱图见图2。
[0032]
表1
[0033][0034]
实施例2
[0035]
一种2,4,6-(n-四甲基黄原酸钠)-4,6-(n-二羟甲基氨基)-1,3,5-三嗪的制备方法,包含如下步骤:
[0036]
步骤一、在装有机械搅拌、冷凝管、恒压滴液漏斗的三口烧瓶中,加入39%氢氧化钠溶液和六羟甲基三聚氰胺,70℃下搅拌0.5h,其中六羟甲基三聚氰胺和氢氧化钠的摩尔比为1.0:6.0。
[0037]
步骤二、将步骤一的反应液温度降至26℃,往恒压滴液漏斗中加入适量二硫化碳,逐滴滴加二硫化碳,控制滴速在1.5ml/min,其中六羟甲基三聚氰胺和二硫化碳摩尔比为1.0: 5.5。
[0038]
步骤三、步骤二中二硫化碳滴加结束后,在26℃条件下继续保温反应4.5h,然后将反应液进行抽滤,滤饼经有机溶剂洗涤2~3次,最后于50℃下烘干即得产物。
[0039]
本实施例所制备的固体产物质量百分比含量为87.92%,反应收率为88.78%。
[0040]
实施例3
[0041]
一种2,4,6-(n-四甲基黄原酸钠)-4,6-(n-二羟甲基氨基)-1,3,5-三嗪的制备方法,包含如下步骤:
[0042]
步骤一、在装有机械搅拌、冷凝管、恒压滴液漏斗的三口烧瓶中,加入40%氢氧化钠溶液和六羟甲基三聚氰胺,75℃下搅拌1h,其中六羟甲基三聚氰胺和氢氧化钠的摩尔比为 1.0:6.5。
[0043]
步骤二、将步骤一的反应液温度降至28℃,往恒压滴液漏斗中加入适量二硫化碳,然后向反应液中逐滴滴加二硫化碳,控制滴速在2.5ml/min,其中六羟甲基三聚氰胺和二硫化碳摩尔比为1.0:6.5。
[0044]
步骤三、步骤二中二硫化碳滴加结束后,在28℃条件下继续保温反应5h,然后将反应液进行抽滤,滤饼经有机溶剂洗涤2~3次,最后于50℃下烘干即得产物。
[0045]
本实施例所制备的固体产物质量百分比含量为90.11%,反应收率为89.93%。
[0046]
实施例4
[0047]
一种2,4,6-(n-四甲基黄原酸钠)-4,6-(n-二羟甲基氨基)-1,3,5-三嗪的制备方法,包含如下步骤:
[0048]
步骤一、在装有机械搅拌、冷凝管、恒压滴液漏斗的三口烧瓶中,加入41%氢氧化钾溶液和六羟甲基三聚氰胺,80℃下搅拌1h,其中六羟甲基三聚氰胺和苛性碱的摩尔比为1.5: 6.0。
[0049]
步骤二、将步骤一的反应液温度降至30℃,往恒压滴液漏斗中加入适量二硫化碳,然后向反应液中逐滴滴加二硫化碳,控制滴速在3ml/min,其中六羟甲基三聚氰胺和二硫化碳摩尔比为1.5:6.0。
[0050]
步骤三、步骤二中二硫化碳滴加结束后,在30℃条件下继续保温反应6h,然后将反应液进行抽滤,滤饼经有机溶剂洗涤2~3次,最后于50℃下烘干即得产物。
[0051]
本实施例所制备的固体产物质量百分比含量为90.64%,反应收率为89.72%。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1