反式激活目的基因的同源基因的方法和诊断疾病的体外方法与流程
al.,2008,kefalov 2012,sakurai et al.,2007,shi et al.,2007)。这表明激活视杆细胞中编码视锥视蛋白的基因可以补偿相应小鼠模型中有缺陷的视紫红质。这同样适用于视杆和视锥cng通道亚基,它们已被证明在异源表达系统中在功能上相互补偿(finn et al.,1998,gerstner et al.,2000,sautter et al.,1998)。
5.视紫红质基因(rho)的突变是常染色体显性rp(adrp)的主要原因。相比之下,编码视锥cng通道亚基(cnga3和cngb3)的基因突变是achm最常见的原因。缺乏视紫红质(rho-/-)或cnga3(cnga3-/-)的小鼠模型分别强烈反映了adrp和achm的临床表型(biel et al.,1999,humphries et al.,1997)。
6.在过去的几十年中,许多不同的方法被开发出来对抗ird,如rp或achm(scholl et al.,2016)。从临床角度来看,目前最流行的金标准方法是经典的基因补充疗法,该疗法已成功应用于不同的视网膜变性小鼠模型(boye et al.,2013,koch et al.,2012,michalakis et al.,2010)。在所有这些研究中,重组腺相关病毒(raav)载体用于视网膜中相应基因的有效递送和长期表达。aav是细小病毒衍生的小型病毒,其用作递送目的基因的正确拷贝的媒介物。尽管aav提供了许多优点(即,高转导效率、长期表达而无需基因组整合、无毒性或非常低的毒性、良好的免疫耐受性),但它们也具有一些重要的缺点,这阻碍了它们在经典基因补充疗法中的更广泛应用。raav载体的一个重要缺点是它们有限的基因组包装能力(大约4.7kb,包括启动子和反向末端重复序列(itrs)(wu et al.,2010))。然而,许多ird是由编码序列远远超过aav包装限制的基因引起的,例如ush2a、myo7a、abca4、cacna1f、cdh23、gpr98、eys、rp1或prph8。因此,仍需要开发策略以克服aav的这一重要限制。
7.一种治疗遗传疾病的开创性方法是crispr(成簇的规则间隔的短回文重复序列)/cas9基因组编辑技术。dna靶向核酸内切酶cas9可以通过称为引导rna(grna)的短互补rna分子被募集到基因组内的特定基因座。在以前的工作中,为了进一步拓宽cas9酶的应用范围,已经开发了核酸内切酶缺陷型cas9变体(称为“死”cas9,dcas9)(sander&joung 2014,wang et al.,2016))。其中,这些修饰的cas9变体的应用范围包括在体外和体内对基因的有效激活(sander&joung 2014)。为此,dcas9在c端与转录因子的反式激活结构域融合。在最近的一项研究中,不同crispr/cas9基因激活结构域的效率已经针对多种不同细胞类型中的几种基因进行了比较。在这种情况下,一个特定的基因激活结构域(vpr,杂合vp64-p65-rta三元激活物(chavez et al.,2015))在所有实验和所有测试物种中显示出最高的基因激活效率。此外,这项研究还证明了grna在相应基因的启动子区域中的结合位置影响基因激活的效率。最后,还表明grna数量的增加改善了基因的激活(chavez et al.,2016)。
8.然而,尽管dcas9 vpr方法在体外非常有前景和有效,但其在视网膜和其他组织中的治疗应用受到缺乏有效递送技术的阻碍。由于其大小(5.8kb),dcas9-vpr远远超过了raav载体的dna包装能力。过去,已经开发了多种方法来绕过raav的这种限制(chamberlain et al.,2016,flotte 2000)。这些方法基于在dna、mrna或蛋白质水平上对分裂的raav转基因进行转录前或转录后重组。
9.迄今为止,已经发现了60多种不同的ird基因。尽管基因诊断已经有了实质性的改进,但是仍然有大量(高达40%)的ird患者没有明确的基因诊断(audo et al.,2012,shanks et al.,2013)。缺乏基因诊断的潜在原因可能是技术限制或患者携带未知基因的
致病突变。此外,在没有明确遗传诊断的常染色体隐性ird患者中,有很高比例的患者在单个基因中仅携带一个突变,例如在与leber先天性黑蒙症(lca)、usher综合征(ush)或stargardt病(stgd)相关的关键基因中。这些患者很可能在同一基因的非编码区携带第二个突变,这是标准诊断组没有检测到的。
10.下一代测序技术,如全基因组测序(wgs)或全外显子组测序(wes),促进了遗传疾病的诊断。然而,wgs和wes都有关键的局限性。wes不包括非外显子区域(内含子、启动子或其他调控转录元件),这些区域对mrna的稳定性和/或加工至关重要。wgs在时间和金钱方面仍然是昂贵的,并且在此过程中获得的大数据的解释是具有挑战性的,并且必须由训练有素的生物信息学家来完成。即使使用wgs可以在候选基因的外显子或非外显子区域鉴定出潜在的致病突变,这些突变如何影响mrna水平的实验验证也是不可或缺的。
11.单核苷酸改变可以通过不同的机制影响mrna。其中,最常见的机制是mrna剪接的改变(baralle&buratti 2017,kim et al.,2018)。经典剪接突变是那些影响已知剪接位点的共有序列的突变。这些突变通常通过上述方法(wgs和/或wes)检测,并使用标准剪接预测软件分类为剪接突变。然而,除了那些影响外显子侧翼的前两个内含子核苷酸的突变(gt对ag)外,将突变分类为剪接突变通常需要在受影响细胞中或在基于小基因的测定中进行mrna水平上的实验验证,所述测定在通常可获得的细胞系中表达相应的基因片段。除了假阳性结果,剪接预测软件也可能产生不确定数量的假阴性记录。通常,这些“假阴性”剪接突变位于较深的外显子编码区,在那里剪接预测相当具有挑战性(grodecka et al.,2017,ohno et al.,2018)。通常,预测影响保守和/或功能重要氨基酸的(深)外显子点突变被归类为错义变体。然而,无论其类型如何,致病突变也可能导致异常剪接,这是一个很大程度上未经探索的选择。此外,识别剪接突变对于为受影响的个体开发合适的治疗方案也很重要。因为与ird相关的剪接突变可以例如用反义寡核苷酸治疗(bergsma et al.,2018,godfrey et al.,2017),这种突变的鉴定也将对未来疗法的开发产生强烈的影响。
12.利用wgs,一些出版物鉴定出ird患者的深度内含子(剪接)突变(bax et al.,2015,braun et al.,2013,carss et al.,2017,khan et al.,2017,liquori et al.,2016,mayer et al.,2016,naruto et al.,2015,rio frio et al.,2009,vache et al.,2012,webb et al.,2012)。然而,如上所述,在mrna水平上对这些突变的实验验证相当复杂,因此很难应用于大量患者。
13.在最近的出版物中,在从患者的成纤维细胞诱导的感光细胞前体细胞中,分析了abca4基因中两种深度内含子变体对mrna剪接的潜在影响(albert et al.,2018)。这种方法有两个关键的局限性:i)它复杂且耗时,因此很难用于常规诊断;ii)诱导的前体细胞不表达所有的ird基因,使得它们不适于许多ird患者的基因诊断。
14.总的来说,对于开发能够在转录水平上研究致病基因突变的改进且易于应用的技术存在未满足的需求。分析相应基因转录本的最便捷方法是使用患者的组织。然而,活组织检查(例如视网膜切除术)通常是不可能的,并且许多疾病基因以组织特异性的方式表达(例如大多数ird连锁基因仅在视网膜细胞中表达),而不在容易接近的细胞(例如血细胞、成纤维细胞或在尿中发现的细胞)中表达。
15.本发明提出的技术尤其通过基于dcas9-vpr的反式激活方法来激活患者细胞中的单个(或多个)基因,并通过靶向rna测序和/或通过经典的rt-pcr分析来检查相应的mrna的
致病性变化,从而能够克服这些障碍。
16.在本发明中,发明人使用dcas9-vpr引入了(同源)基因的反式激活,用于治疗(见图1)和诊断(见图2)应用,以克服上述缺点并满足期望的需求。
技术实现要素:
17.本发明涉及反式激活至少一种目的基因的同源基因和任选失活至少一种目的基因的方法,其中由所述至少一种目的基因编码的mrna与对照相比包含突变,并且其中该方法包括以下步骤:-复合物的结合,所述复合物包含天然或遗传修饰的dna结合蛋白、转录激活因子或转录因子的至少一个反式激活结构域和至少一种引导rna,其中所述至少一种引导rna结合到所述至少一种目的基因的同源基因的启动子区域或结合到调节由至少一种目的基因的同源基因编码的mrna的表达的其他元件,任选地其中另一个引导rna结合到编码区域、启动子区域和/或结合到调节由至少一种目的基因编码的mrna的表达的其他元件;并且,其中所述至少一种目的基因选自由如下组成的组:视蛋白基因、环核苷酸门控通道(cng)基因、视黄醛特异性atp结合盒转运蛋白(abc转运蛋白)基因和肌球蛋白基因;-诱导由至少一种目的基因的同源基因编码的mrna的表达;和;任选地使由至少一种目的基因编码的mrna的表达失活;以及-从而反式激活至少一种目的基因。至少一种目的基因的任选失活优选是同源基因已被反式激活的至少一种目的基因的失活,但也包括至少另一种目的基因的失活。其中目的基因和另一目的基因是由于突变而功能受损的基因,或者换句话说,其中由目的基因编码的mrna包含突变。
18.在反式激活方法的一个实施方案中,该方法还包括诱导由至少一种目的基因的同源基因的mrna编码的蛋白质的表达,并分析由该mrna编码的至少一种蛋白质的序列、表达水平、定位或功能。
19.在反式激活方法的一个实施方案中,所述至少一种目的基因的同源基因选自由如下组成的组:abca1(seq id no:1)、abca2(seq id no:3)、abca7(seq id no:7)、abca12(seq id no:9)、abca13(seq id no:11)、cnga1(seq id no:13)、cnga2(seq id no:15)、cnga3(seq id no:17)、cnga4(seq id no:19)、cngb1(seq id no:21)、cngb3(seq id no:23)、myo7b(seq id no:33)、myo5a(seq id no:25)、myo5b(seq id no:27)、myo5c(seq id no:29)、myo10(seq id no:35)、myo15b(seq id no:39)、myo15a(seq id no:37)、opn1lw(seq id no:41)、opn1mw(seq id no:43)和opn1sw(seq id no:45)。
20.在反式激活方法的一个实施方案中,所述天然或遗传修饰的dna结合蛋白选自由如下组成的组:cas酶;优选cas9(seq id no:92)、dcas9-酶(seq id no:96,seq id no:97)、cas12a(seq id no:93)或cas12b(seq id no:94);锌指核酸酶;和转录激活因子样核酸酶;和/或其中转录激活因子或转录因子的至少一个反式激活结构域选自由如下组成的组:vpr(seq id no:89)、sam(seq id no:90)、suntag(seq id no:91)、vp64(seq id no:73)、p65(seq id no:74)、rta(seq id no:75)或其组合;优选地,其中所述天然或遗传修饰的dna结合蛋白和转录激活因子或转录因子的至少一个反式激活结构域的核苷酸序列被分成两个分裂片段。更优选地,天然dna结合蛋白是化脓性链球菌(streptococcus pyogenes)的cas9酶(seq id no:92)。更优选地,遗传修饰的dna结合蛋白选自由如下组成的组:根据seq id no:96具有突变d10a和h840a的dcas9和根据seq id no:97具有突变d10a、d839a、
pyogenes)的cas9酶(seq id no:92)。更优选地,遗传修饰的dna结合蛋白选自由如下组成的组:根据seq id no:96具有突变d10a和h840a的dcas9和根据seq id no:97具有突变d10a、d839a、h840a和n863a的dcas9。然而,原则上任何已知生物的所有cas酶都可以用于本发明的方法中。
28.在诊断疾病的体外方法的一个实施方案中,所述天然或遗传修饰的dna结合蛋白是cas酶;优选cas9(seq id no:92)、dcas9-酶(seq id no:96、seq id no:97)、cas12a(seq id no:93)或cas12b(seq id no:94);并且其中所述复合物进一步包含至少一种引导rna,其能够结合到至少一种目的基因的启动子区域或结合到调节至少一种目的基因表达的其他元件。
29.在诊断疾病的体外方法的一个实施方案中,dna结合蛋白在c-或n-末端与转录激活因子或转录因子的至少一个反式激活结构域融合,优选其中转录激活因子或转录因子的至少一个反式激活结构域选自由如下组成的组:vpr(seq id no:89)、sam(seq id no:90)、suntag(seq id no:91)、vp64(seq id no:73)、p65(seq id no:74)、rta(seq id no:75)或其组合。
30.在诊断疾病的体外方法的一个实施方案中,所述疾病是神经退行性疾病、癫痫、心理疾病;优选抑郁症、躁狂症、双相情感障碍、精神分裂症或自闭症;或视网膜疾病,优选遗传性视网膜营养不良,更优选其中所述遗传性视网膜营养不良选自由如下组成的组:年龄相关性黄斑变性(amd)、遗传性年龄相关性黄斑变性(amd)、常染色体显性、常染色体隐性、x-连锁或双基因视网膜色素变性、色盲、stargardt病、best病、leber氏先天性黑蒙症、视网膜劈裂、先天性静止性夜盲、脉络膜缺失、早发性视网膜营养不良、视锥、视杆-视锥或视锥-视杆营养不良、模式营养不良、usher综合征和其他综合征性纤毛病,更优选bardet-biedl综合征、joubert综合征、senior-综合征或综合征。
附图说明
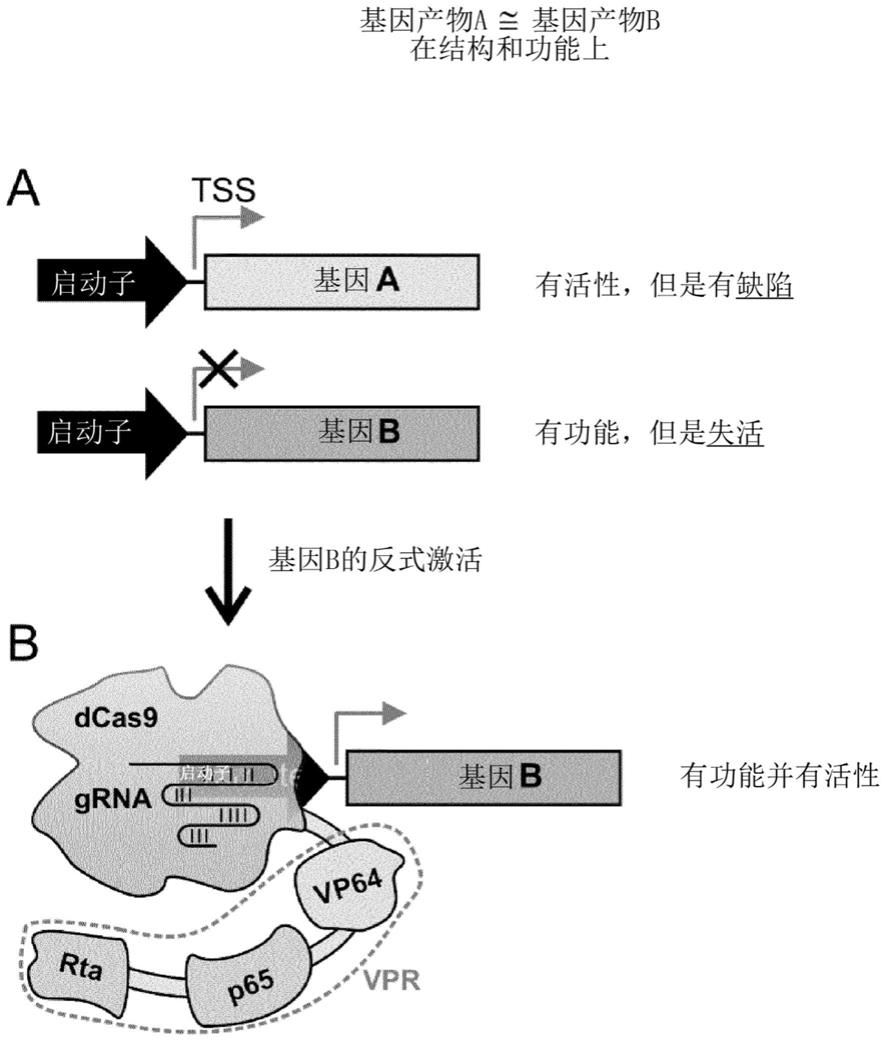
31.图1显示了dcas9-vpr介导的同源基因反式激活作为遗传性疾病的一种新的治疗选择。图1a显示基因a在给定的细胞类型或组织中是有活性的,但是由于致病突变而有缺陷。基因b是基因a的同源物,在结构和功能上与基因a非常相似,但在受影响的细胞类型/组织中不表达(无活性)。图1b显示了反式激活疗法,该疗法旨在使用dcas9-vpr模块结合基因b特异性引导rna(grna)在适当的组织(或细胞类型)中激活基因b。基因b然后补偿缺失的(基因a)功能,并为患者提供治疗益处。tss表示转录起始位点。
32.图2显示了基因反式激活作为用于诊断目的的新工具。
33.图3显示了dcas9-vpr介导的小鼠cnga1在661w细胞中的反式激活。图3a是显示杂合vp64-p65-rta三重激活因子(dcas9-vpr,seq id no:95)的示意图。vp64(seq id no:73)是一种转录激活因子,由与甘氨酸-丝氨酸接头连接的vp16(单纯疱疹病毒蛋白16)的四个串联拷贝组成。dcas9-vpr(seq id no:95)由融合到激活结构域vp64(seq id no:73)、p65(seq id no:74)和rta(seq id no:75)的dcas9组成,其中每个激活结构域被一个短氨基酸接头分开。图3b显示了单个cnga1特异性grna(g1-g3)(cnga1中g1-g3的靶序列(seq id nos:76-78),包括pam序列)相对于小鼠cnga1启动子(黑色箭头)内转录起始位点(tss)的结合位置(以bp表示)。启动子和tss从http://epd.vital-it.ch/mouse/mouse_database.php
网站获得。图3c显示了表达dcas9-vpr(seq id no:95)和cnga1 grna(vpr-a1,上图)(cnga1中g1-g3的靶序列(seq id no:76
–
seq id no:78),包括pam序列)或lacz(vpr-lacz,下图)grnas(lacz中的靶序列(seq id no:125),包括pam序列)的强力霉素诱导型表达盒。每个grna由u6启动子驱动。图3d显示了661w细胞的代表性结果,该细胞表达图3c中所示的一种表达盒,并用cnga1特异性抗体进行了共免疫标记。图3e和图3f显示了在所示的不同强力霉素浓度下,表达vpr-a1表达盒的661w细胞中cnga1(e)或dcas9(f)mrna水平的qrt-pcr定量。图3g-l显示了来自表达vpr-a1(cnga1)或vpr-lacz(lacz)表达盒的661w细胞的切除的内向外膜片钳记录。图3g-j显示了在单独存在cgmp(图3g和图3h)和单独存在ca
2+
/mg
2+
或与cgmp组合存在(图3i和图3j)的情况下,从各个细胞获得的绝对(图3g和图3i)和归一化(图3h和图3j)电流变化。图3k和3l显示了在基础条件下,添加cgmp和/或ca
2+
/mg
2+
后,表达vpr-a1(cnga1,图3k)或vpr-lacz(lacz,图3l)的661w细胞的膜贴片的代表性痕迹。使用不成对的student’s t检验进行统计分析,以比较两组之间的差异。***,p《0.001.
34.图4显示了在hek293细胞中分裂内含肽效率的计算。图4a显示了所用的dcas9分裂内含肽变异体的示意图。通过在aa位置v713(上图)或e573(下图)裂解dcas9产生cas9片段。第一个dcas9片段(dcas9n1或dcas9n2,分别编号为1和3)在c-末端融合到内含肽(intn)的n-末端部分。第二个cas9片段(dcas9c1和dcas9c2,分别编号为2和4)在其n-末端包含c-末端内含肽半(intc)。bp的意思是碱基对。图4b显示了来自hek293细胞的蛋白质印迹,所述hek 293细胞用所示的单一分裂内含肽dcas9组合瞬时共转染。针对dcas9末端部分的特异性抗体用于信号检测。图4c显示了由图4b所示的四个独立转染实验得到的裂解cas9重建效率的半定量计算。通过计算重建的全长dcas9条带和每个泳道相应的dcas9n1或dcas9n2条带的强度比来确定重建效率。平均重建效率值如下:1+2=56.9
±
2.1%;3+4=33.3
±
1.1%。使用不成对的student’s t检验进行统计分析,以比较两组之间的差异。****,p《0.0001.
35.图5显示了在瞬时转染的661w或mef细胞中,dcas9-vpr(seq id no:95)和分裂的v713_dc9介导的cnga1(seq id no:13)、opn1mw(seq id no:43)和opn1sw(seq id no:45)基因的反式激活。图5a显示了与cnga1(a1)、opn1mw(o1mw)或opn1sw(o1sw)grna组合的全长cas9表达盒,用于661w细胞(对于cnga1)或mef细胞(对于opn1mw和opn1sw)的瞬时转染。与lacz grna组合的全长cas9表达盒用作对照(lacz中grna的靶序列,包括pam序列:seq id no:124)。cmv的意思是巨细胞病毒启动子。图5b显示了用于各细胞的瞬时共转染的单一v713_dc9变体。dcas9片段对应于图4所示的dcas9n1和dcas9c1构建体。图5c和图5d显示了单个opn1mw(c)或opn1sw(d)特异性grna(g1-g3)(opn1mw中g1-g3的靶序列(seq id no:79-81)和opn1sw中g1-g3的靶序列(seq id no:83-85),包括pam序列)相对于其启动子(黑色箭头)内转录起始位点(tss)的结合位置(以bp表示)。启动子和tss从http://epd.vital-it.ch/mouse/mouse_database.php网站获得。图5e-图5g显示了使用全长dcas9-vpr(seq id no:95)(图5e,图5g和图5i)或v713_dc9(图5f和图5h)测定所示单个基因的反式激活效率的qrt-pcr。使用不成对的student’s t检验进行统计分析,以比较两组之间的差异。*,p《0.05;**,p《0.01;***,p《0.001;****,p《0.0001.
36.图6显示了使用v713_dc9对opn1mw(seq id no:43)和opn1sw(seq id no:45)的体内反式激活。图6a显示了用于视杆感光细胞共转导的单一v713_dc9 aav载体表达盒。hrho
表示人类视紫红质启动子。使用aav2/8衣壳在p14对野生型小鼠进行视网膜下注射。图6b——图6d显示了注射后三周对注射眼(图6b和图6d)或假注射对照眼(图6c和图6e)的小鼠视网膜的免疫标记。花生凝集素(pna)抗体被用作视锥感光细胞标记。对于opn1mw(seq id no:44)和opn1sw(seq id no:46)的染色,使用在别处描述的特异性抗体(例如,becirovic et al.,2016,nguyen et al.,2016)。图6f和6g,使用从注射了v713_dc9和opn1mw或opn 1sw grna(opn1mw中g1-g3的靶序列(seq id nos:79-81)和opn1sw中g1-g3的靶序列(seq id nos:83-85),包括pam序列)的小鼠中分离的rna进行qrt-pcr,所述病毒在注射后三周表达。假注射的眼睛用作对照(ctrl)。
37.图7显示m-视蛋白激活改善了杂合rho小鼠的视网膜表型。在p14注射杂合(hz)rho小鼠(n=10),并在注射后12个月进行视网膜电图(erg,a)和光学相干断层扫描(oct,b)。一只眼睛注射dcas9-vpr(seq id no:95)(hz治疗),对侧眼睛用nacl进行假注射(hz假)。来自10只未治疗的野生型(wt)小鼠(12个月)的双眼(od,右眼和os,左眼)用作对照。图7a上图显示了三组在不同光强度下的单次erg测量的统计数据。n.s.表示不显著。下图,暗视b波振幅对光强度作图。图7b显示了对用于图7a所示erg的同一组小鼠进行的光学相干断层扫描。onl意味着外核层。所有统计数据均采用方差分析和bonferroni事后检验进行。*,p《0.05;**,p《0.01;***p《0.001.
38.图8显示了人成纤维细胞中dcas9-vpr介导的ush2a(seq id no:49)的反式激活。图8a显示了描述1号染色体q41区域的示意图,其中kcdt3(seq id no:109)和ush2a(seq id no:49)基因位于相对的链上(kcdt3(seq id no:122)的情况下为(+)-链,ush2a的情况下为(-)-链)。注意两个基因3’utr的重叠部分。转录激活位点用箭头表示。图8b显示了由72个外显子组成的ush2a(seq id no:49)转录物的不成比例的示意图(见方框)。5’和3’utr显示在该图的末端。用于扩增单一ush2a(seq id no:49)片段的引物(seq id no:98-seq id no:121)用双箭头表示。相应的pcr产物(a-l)显示为包括碱基对(bp)中片段长度的线。图8c显示了来自人成纤维细胞的rt-pcr,所述成纤维细胞用dcas9-vpr(seq id no:95)与ush2a grna(左图)(ush2a中grna的靶序列(seq id no:86-88),包括pam序列)或对照lacz grna(lacz中的靶序列(seq id no:125),包括pam序列)(右图)联合瞬时转染,使用图8b所示的引物对。使用相同的pcr循环条件扩增所有的pcr产物。kb表示千碱基对。第l行(右图)中的条带对应于kcdt3(seq id no:122)的3’utr。通过sanger测序评估条带的同一性。图8d显示了来自三个独立实验的qrt-pcr,所述实验使用用dcas9-vpr(seq id no:95)与lacz(左)(lacz中的靶序列,包括pam序列:seq id no:125)或ush2a(右)grna(ush2a中grna的靶序列(seq id no:86-88),包括pam序列)组合转染的人成纤维细胞。数据显示为对管家氨基乙酰丙酸合酶(alas)归一化的mrna转录物计数的倍数变化。使用不成对的students t检验进行统计。**,p=0.0033。数据以平均值
±
平均值的标准误差表示(dcas9-vpr_lacz为0.86
±
0.04,dcas9-vpr_ush2a为600.70
±
95.56)。右图描绘了ush2a转录物中qrt-pcr引物的结合位置。如图所示,qu2_for与外显子12结合,qu2_rev与外显子13结合。
39.图9显示杂合rho小鼠中opn1mw的反式激活不引起任何小胶质细胞激活或反应性胶质增生。a、b为注射了v713_dc9和opn1mw(m-视蛋白)特异性grna(a,治疗)或盐水(b,假,对侧眼)的杂合rho小鼠#1的视网膜的代表性免疫染色。使用外周蛋白-2抗体(prph2)作为视杆细胞和视锥细胞的外节标记,使用花生凝集素(pna)作为视锥细胞的标记。c-f为用
iba1或gfap对同一视网膜进行免疫标记,以将接受治疗的(c,e)和注射盐水的对侧眼(d,f)中的小胶质细胞或反应性胶质细胞增生可视化。g,h为用iba1(g)或gfap(h)对p13上pde6b缺陷(rd1)小鼠的视网膜进行免疫标记,作为阳性对照。比例尺30μm。
40.图10显示杂合rho小鼠中opn1mw的反式激活减少了凋亡。a为来自注射了v713_dc9和opn1mw(m-视蛋白)特异性grna的杂合rho小鼠#1的免疫标记视网膜的代表性切片,其显示注射后一年同一视网膜的转导(左图)或未转导(右图)区域。b为用作阳性对照的p13上rd1小鼠视网膜的免疫标记。tunel染色(上图)用于观察凋亡,prph2用作视杆和视锥外节标记(下图)。比例尺30μm。c为在来自注射了v713_dc9和opn1mw特异性sgrna的八只杂合rho小鼠(+/-)的视网膜的转导区域与未转导区域中的tunel+细胞的定量。配对t检验(双尾)用于统计分析。
41.图11显示了使用三个引导rna的多重方法用于同时敲除rho(即失活)和激活opn1mw。a:rho敲除可以通过使用具有原间隔区(ps)》16bp的单个引导rna(sgrna)来实现,其保留了cas9催化活性。相比之下,opn1mw激活可以在具有短原间隔区序列(《16bp)的sgrna存在下实现。在这些条件下,cas9能够结合,但不能切割dna。b,c:raav表达盒用于在蛋白质水平使用断裂内含肽(b)或在rna水平使用mrna反式剪接(revert)方法(c)重建断裂的cas9。itr的意思是反向末端重复。g1-g3表示a中描述的grna。u6表示u6启动子。n-int和c-int是分裂内含肽的n-或c-末端部分。rho表示人视紫红质启动子,sds表示剪接供体位点,sas表示剪接受体位点,pa表示聚腺苷酸化信号,bd表示结合结构域。d-f:在存在两个opn1mw grna和一个rho grna(多重方法)或仅存在一个单一lacz sgrna的情况下,对注射有b(内含肽)或c(revert)所示的表达spcas9-vpr表达盒的双raav的野生型小鼠的视网膜进行qrt-pcr分析。用单因素方差分析进行统计分析,然后用bonferroni事后检验进行多重比较。*;p《0.05;**,p《0.01;***,p《0.001.
具体实施方式
42.本发明涉及反式激活至少一种目的基因的同源基因和任选失活至少一种目的基因的方法,其中由所述至少一种目的基因编码的mrna与对照相比包含突变,并且其中该方法包括以下步骤:-复合物的结合,所述复合物包含天然或遗传修饰的dna结合蛋白、转录激活因子或转录因子的至少一个反式激活结构域和至少一种引导rna,其中所述至少一种引导rna结合到所述至少一种目的基因的同源基因的启动子区域或结合到调节由至少一种目的基因的同源基因编码的mrna的表达的其他元件,任选地其中另一个引导rna结合到编码区域、启动子区域和/或结合到调节由至少一种目的基因编码的mrna的表达的其他元件;并且,其中所述至少一种目的基因选自由如下组成的组:视蛋白基因、环核苷酸门控通道(cng)基因、视黄醛特异性atp结合盒转运蛋白(abc转运蛋白)基因和肌球蛋白基因;-诱导由至少一种目的基因的同源基因编码的mrna的表达;和;任选地使由至少一种目的基因编码的mrna的表达失活;以及-从而反式激活至少一种目的基因。至少一种目的基因的任选失活优选是同源基因已被反式激活的至少一种目的基因的失活,但也包括至少另一种目的基因的失活。其中目的基因和另一目的基因是由于突变而功能受损的基因,或者换句话说,其中由目的基因编码的mrna包含突变。
43.本发明上下文中使用的“反式激活”涉及通过中间反式激活蛋白如本发明复合物
id no:75)。
53.术语“转录的因子”和“转录因子”在本文中同义使用,指通过结合基因启动子和募集rna聚合酶而允许基因转录的蛋白质。转录因子单独或与其他蛋白质(如一种或多种转录激活因子和/或转录抑制因子)复合起作用。
54.本发明上下文中使用的术语“引导rna”可以是将crispr/cas9复合物靶向基因组dna内特定位置的序列,优选特定基因的启动子区域。例如,引导rna可以指包含两种rna的序列,即crispr rna(crrna)和反式激活crrna(tracrrna),或者可以是由crrna和tractrna的基本部分融合产生的单链rna(sgrna)。sgrna由与dna互补的原间隔区、稳定复合物的tractrna和将这两部分连接在一起的接头序列组成。为了被募集到目的基因座(例如启动子),crispr/cas9-引导rna复合物还需要在相应的基因座序列中存在原间隔区相邻基序(pam)。引导rna可以以编码引导rna的rna或dna的形式转移到细胞或生物体中。引导rna可以是分离的rna、整合到病毒载体中的rna或在载体中编码的rna的形式。优选地,载体可以是病毒载体、质粒载体或土壤杆菌载体,但不限于此。编码引导rna的dna可以是包含编码引导rna的序列的载体。例如,可以通过用分离的引导rna或包含编码引导rna的序列和启动子(例如u6启动子)的质粒dna转染细胞或生物体,将引导rna转移到细胞或生物体中。
55.本发明上下文中使用的术语“启动子区”是指导致特定基因转录起始的dna区域。启动子位于基因转录起始位点附近,在dna的上游(朝向有义链的5’区域)。启动子通常由100-1000个碱基对组成。
56.本发明上下文中使用的术语“调节mrna表达的其他元件”可以是关于相应rna或mrna表达的增强子、沉默子和/或边界元件/绝缘子。
57.本发明上下文中使用的术语“视蛋白基因”是指各种无色蛋白质的任何基因,其与视黄醛或相关辅基结合,在光可逆的反应中形成视觉色素(如视紫红质)。这些基因是,例如,m-视蛋白基因(opn1mw)(seq id no:43),l-视蛋白基因(opn1lw)(seq id no:41)或s-视蛋白基因(opn1sw)(seq id no:45)。
58.本发明上下文中使用的术语“环核苷酸门控通道(cng)基因”是指cng通道基因家族的任何成员,其在脊椎动物中由六个成员组成。这些基因根据序列相似性分为两个亚型cnga和cngb。编码cng通道的其他基因已经从秀丽隐杆线虫和黑腹果蝇中克隆。cng通道的一个亚基cnga1(以前被称为视杆α亚基)在视杆感光细胞中表达,并产生由cgmp门控的功能通道,当在非洲爪蟾卵母细胞或人胚胎肾细胞系(hek293)中外部表达时。在人类中,突变的cnga1基因导致色素性视网膜炎的常染色体隐性遗传形式,这是一种失明的退行性形式。cngb1以前称为视杆β亚基,是视杆通道的第二个亚基。与cnga1不同,单独表达的cngb1a亚基不产生功能性cng通道,但cnga1和cngb1a亚基的共表达会产生具有与天然通道相当的调节、渗透、药理学和环核苷酸特异性的异聚通道。cng通道形成四聚体,最近的研究表明天然视杆通道由三个cnga1亚基和一个cngb1a亚基组成。cnga3亚基,以前称为视锥α亚基,在异源表达系统中形成功能通道。另一方面,cngb3以前被称为视锥β亚基,不能独自形成功能性通道。人类cnga3和cngb3的突变与完全色盲有关,这是一种罕见的常染色体隐性遗传和先天性疾病,其特征是完全无法辨别颜色、视力下降和畏光增加。类似于视杆亚基的化学计量,视锥cng通道由三个cnga3和一个cngb3亚基组成。cnga2以前被称为嗅觉α亚基,cnga4以前被称为嗅觉β亚基,和cngb1b参与嗅觉感觉神经元中气味信号的转导。嗅觉cng通道由两
个cnga2、一个cnga4和一个cngb1b亚基组成。
59.本发明上下文中使用的术语“视网膜特异性atp结合盒转运蛋白(abc转运蛋白)基因”是指编码abc转运蛋白家族成员的任何基因。这是一组特定的膜蛋白,利用atp的水解来推动多种底物跨细胞膜转运。abc转运蛋白最少由两个保守区域组成:一个高度保守的核苷酸结合结构域(nbd)和一个不太保守的跨膜结构域(tmd)。真核abc蛋白通常被组织为完全转运蛋白(包含两个nbd和两个tmd)或半转运蛋白(包含一个nbd和一个tmd),它们必须形成同源或异源二聚体才能构成功能蛋白。视网膜特异性atp结合盒转运蛋白abca4(也称为rim蛋白,abcr)是一种真核生物蛋白,属于abc转运蛋白家族的abc-a亚家族。在人类中,abca4与视蛋白光色素一起定位在视杆细胞和视锥细胞的外节视盘膜中。它作为n-视黄醛亚基磷脂酰乙醇胺和磷脂酰乙醇胺的运载体。abca4基因的突变导致stargardt病(stgd1),这是一种隐性疾病,其特征是中心视力丧失,感光细胞和视网膜色素上皮(rpe)细胞进行性双侧萎缩,黄斑中荧光沉积物的积累,以及暗适应的延迟。
60.本发明上下文中使用的术语“肌球蛋白基因”是指编码称为肌球蛋白的相关蛋白质的基因。肌球蛋白通常被称为分子马达,因为它们使用能量来移动。它们可以与肌动蛋白相互作用。肌动蛋白组织成细丝状体,形成网络(细胞骨架),为细胞提供结构,并可以作为肌球蛋白移动的轨道。一些肌球蛋白蛋白质附着(结合)到其他蛋白质上,并沿着肌动蛋白轨道在细胞内和细胞间运输它们。一些肌球蛋白参与肌肉收缩。这些肌球蛋白与其他肌球蛋白相互作用,形成粗丝状体。在肌肉细胞中,由肌球蛋白组成的粗丝状体和由肌动蛋白组成的细丝状体组成了称为肌节的结构,肌节是肌肉收缩的基本单位。重叠的粗丝状体和细丝状体彼此结合并释放,这允许丝状体相对于彼此移动,从而肌肉可以收缩。编码肌肉肌球蛋白的基因突变会导致用于运动的肌肉(骨骼肌)或心脏(心肌)的严重异常。心肌异常会导致心力衰竭和猝死。肌球蛋白参与许多细胞功能。它们运输物质和通过收缩产生力量的能力使它们在细胞分裂过程中非常重要。肌球蛋白也参与细胞运动。一些肌球蛋白存在于内耳中被称为静纤毛的特殊结构中。这些肌球蛋白被认为有助于正确组织静纤毛。这些肌球蛋白的异常会导致耳聋。这个基因组中的基因的例子是:myh3、myh6、myh7、myh9、myh11、myo5a、myo5b和myo7a。myo7a基因突变导致usher综合征,这是全球遗传性耳聋的主要原因。患者患有严重的视网膜色素变性、先天性耳聋和前庭功能障碍(平衡问题)。
61.本发明上下文中使用的术语“对照”涉及目的基因,其不包含导致相应疾病的任何突变,其存在通过根据本发明的任何方法进行研究。不同受试者之间的基因组自然不同,因此不同受试者(同一物种)之间相同基因的“野生型”序列存在一定的偏差。这些差异通常不会改变基因的功能。因此,尽管在序列方面可能存在一些差异,但目的基因的表达产物的功能并未受损。然而,这些差异不包括任何可能导致疾病的突变。这种与疾病相关的突变可能包括单个核苷酸的缺失或改变,也可能包括受影响基因中较长片段的缺失或改变。
62.在根据本发明的反式激活方法的一个实施方案中,该方法还包括诱导由至少一种目的基因的同源基因的mrna编码的蛋白质的表达,并分析由该mrna编码的至少一种蛋白质的序列、表达水平、定位或功能。
63.本发明上下文中使用的术语“表达水平”是指特定序列的任何表达程度。
64.本发明上下文中使用的术语“蛋白质的定位”是指能够检测特定蛋白质的任何方法。这种方法可以包括使用定位信号。然而,对于蛋白质定位的检测,在大多数情况下使用
特异性抗体(自制的、市售的或从别处引入的)。然后抗体识别天然蛋白质的表位。重组蛋白也可以被标记以更好地检测,然后可以被标准商业抗体(例如flag标签、his标签或myc标签)识别。最后,你可以在待检测的蛋白质上安装小的荧光标签,这样就可以用显微镜很容易地检测出来。如在根据本发明的方法中,天然存在的基因或蛋白质被激活,用于检测蛋白质定位的基于抗体的方法是合适的和优选的。
65.本发明上下文中使用的术语“蛋白质的功能”或“蛋白质功能”是指由蛋白质介导的任何功能。存在几种对蛋白质功能进行分类的方案。其中基因本体(go)和功能目录(funcat)是两种常用的方案,它们基于发生在各种生物体和真核生物中的一般生物现象(riley,1998;rison et al.,2000;ouzounis et al.,2003)。
66.同源基因可以具有与目的基因相同或相似的功能,因此在反式激活后可以取代或补充目的基因的功能。这种同源基因的例子可以在下面找到。因此,在反式激活方法的一个实施方案中,至少一种目的基因的同源基因选自由如下组成的组:abca1(seq id no:1)、abca2(seq id no:3)、abca7(seq id no:7)、abca12(seq id no:9)、abca13(seq id no:11)、cnga1(seq id no:13)、cnga2(seq id no:15)、cnga3(seq id no:17)、cnga4(seq id no:19)、cngb1(seq id no:21)、cngb3(seq id no:23)、myo7b(seq id no:33)、myo5a(seq id no:25)、myo5b(seq id no:27)、myo5c(seq id no:29)、myo10(seq id no:35)、myo15b(seq id no:39)、myo15a(seq id no:37)、opn1lw(seq id no:41)、opn1mw(seq id no:43)和opn1sw(seq id no:45)。
67.本发明上下文中的目的基因是由于突变而功能受损的基因,因此是在功能上被同源基因取代的靶。如本文所述,目的基因和同源基因具有相同或相似的功能,但不一定具有相同的序列或结构。在反式激活方法的一个实施方案中,至少一种目的基因选自由如下组成的组:视紫红质基因(rho)(seq id no:47)、m-opsin基因(opn1mw)(seq id no:43)、l-opsin基因(opn1lw)(seq id no:41)或s视蛋白基因(opn1sw)(seq id no:45)、abca4(seq id no:5)、cnga1(seq id no:13)、cnga3(seq id no:17)、cngb1(seq id no:21)、cngb3(seq id no:23)和myo7a(seq id no:31)。
68.在根据本发明的反式激活方法的一个实施方案中,至少一种目的基因选自由如下组成的组:opn1mw(seq id no:43)、l-opsin基因(opn1lw)(seq id no:41)和s视蛋白基因(opn1sw)(seq id no:45)。
69.因此,相关同源基因对的一些说明性例子包括abca4/abca1,cnga1/cnga3,cngb1/cngb3,gucy2e/gucy2f,guca1a/guca1b,myo7a/myo7b。鉴于相应同源基因对的功能和/或结构相似性,在受影响的细胞类型(视锥细胞、视杆细胞或rpe细胞)中通过反式激活开启相应同源基因将在功能上补偿突变基因的缺陷。
70.如本文所述,本发明的基本原理是dna结合蛋白与反式激活结构域的组合。dna结合蛋白可以是天然的或遗传修饰的。dna结合蛋白可选自由如下组成的组:cas酶、锌指核酸酶和转录激活因子样核酸酶(talen)。因为这些天然的dna结合分子可能具有核酸内切酶的功能,它们可能被遗传修饰而失去其核酸内切酶的功能。此外,当grna靶向序列(原间隔区)被缩短时,天然cas-酶可能不具有核酸内切酶的功能。在本发明中,术语“靶向序列”描述了引导rna中直接结合靶dna的部分。当cas9与具有少于16个碱基对的靶向序列的引导rna结合时,cas9不能切割dna,因此不能作为核酸内切酶。
71.不同的反式激活结构域是本领域技术人员已知的。这些反式激活结构域包括但不限于vpr(seq id no:89)、sam(seq id no:90)、suntag(seq id no:91)、vp64(seq id no:73)、p65(seq id no:74)或rta(seq id no:75)。这些反式激活结构域可以与dna结合蛋白融合。因此,dna结合蛋白将反式激活结构域导向同源基因,从而使同源基因能够转录。因此,在反式激活方法的一个实施方案中,天然或遗传修饰的dna结合蛋白选自由如下组成的组:cas酶;优选cas9(seq id no:92)、dcas9-酶(seq id no:96、seq id no:97)、cas12a(seq id no:93)或cas12b(seq id no:94);锌指核酸酶;和转录激活因子样核酸酶;和/或其中转录激活因子或转录因子的至少一个反式激活结构域选自由如下组成的组:vpr(seq id no:89)、sam(seq id no:90)、suntag(seq id no:91)、vp64(seq id no:73)、p65(seq id no:74)、rta(seq id no:75)及其组合;优选地,其中天然或遗传修饰的dna结合蛋白和转录激活因子或转录因子的至少一个反式激活结构域的核苷酸序列被分成两个分裂片段。分裂片段的应用允许将dna结合蛋白-转录激活因子/因子融合蛋白分布在不同的载体上。这些单独的载体中的每一个都较小,因此可以掺入较小的病毒颗粒中,给受试者施用。因此,在根据本发明的反式激活方法的一个实施方案中,转录激活因子或转录因子的至少一个反式激活结构域是反式激活结构域vp64(seq id no:73)、p65(seq id no:74)和rta(seq id no:75),优选地,转录激活因子或转录因子的反式激活结构域包含seq id no:73、74和75中所示的核苷酸序列或由seq id no:73、74和75中所示的核苷酸序列组成。
72.cas9(seq id no:92)可以在e573或v713位置被分裂,用于分裂内含肽介导的蛋白质反式剪接。然而,在本发明的任何方法的背景下,用于分裂的任何其他位置也是可以想到的。因此,在反式激活方法的一个实施方案中,天然或遗传修饰的dna结合蛋白是cas9(seq id no:92),并且由转录激活因子或转录因子的至少一个反式激活结构域的核酸序列和cas9的核酸序列组成的分裂核苷酸序列在dcas9(优选根据seq id no:96或seq id no:97的一种dcas9酶)的e573或v713位置分裂。
73.在根据本发明的反式激活方法的一个实施方案中,所述天然或遗传修饰的dna结合蛋白是cas酶;优选cas9(seq id no:92)、dcas9-酶(seq id no:96、seq id no:97)、cas12a(seq id no:93)或cas12b(seq id no:94);并且该复合物还包含至少一种引导rna,该引导rna能够与至少一种目的基因的同源基因的启动子区域结合,或者与调节至少一种目的基因的同源基因的表达的其它元件结合。更优选地,天然dna结合蛋白是化脓性链球菌(streptococcus pyogenes)的cas9酶(seq id no:92)。更优选地,遗传修饰的dna结合蛋白选自由如下组成的组:根据seq id no:96具有突变d10a和h840a的dcas9和根据seq id no:97具有突变d10a、d839a、h840a和n863a的dcas9。然而,原则上任何已知生物的所有cas酶都可以用于本发明的方法中。
74.在根据本发明的反式激活方法的一个实施方案中,引导rna包含seq id nos:76-88中所示的核苷酸序列或由seq id nos:76-88中所示的核苷酸序列组成。在反式激活方法的另一个实施方案中,至少一种引导rna是2、3、4、5、6、7、8、9、10种或更多的引导rna。
75.在反式激活方法的一个实施方案中,dna结合蛋白在c-或n-末端与转录激活因子或转录因子的至少一个反式激活结构域融合。在反式激活方法的一个实施方案中,dna结合蛋白在n-末端与转录激活因子或转录因子的至少一个反式激活结构域融合。在反式激活方法的一个实施方案中,dna结合蛋白在c-末端与转录激活因子或转录因子的至少一个反式
激活结构域融合。
76.在根据本发明的反式激活方法的一个实施方案中,转录激活因子或转录因子的至少一个反式激活结构域包含vpr(seq id no:89)或由其组成,优选地,其中转录激活因子的至少一个反式激活结构域是反式激活结构域vp64(seq id no:73)、p65(seq id no:74)和rta(seq id no:75),更优选地,其中所述转录激活因子的至少一个反式激活结构域包含如seq id no:73、74和75所示的氨基酸序列或由如seq id no:73、74和75所示的氨基酸序列组成。
77.在根据本发明的反式激活方法的一个实施方案中,天然或遗传修饰的dna结合蛋白和转录激活因子或转录因子的至少一个反式激活结构域的核苷酸序列位于两个独立的质粒和/或载体上。
78.在根据本发明的反式激活方法的一个实施方案中,至少一个目的基因的编码序列的大小至少为0.5kb,优选至少为5kb。
79.在根据本发明的反式激活方法的一个实施方案中,该方法还包括使用天然或工程化来源的重组aav载体,优选具有视网膜细胞类型向性和增强的视网膜转导效率的aav载体变体。与经典的raav介导的基因补充相比,dcas9-vpr介导的基因反式激活方法将提供几个重要的优势。反式激活允许i)激活同源基因,而不管它们的大小,这使得能够开发对由非常大的基因(违反aav基因组大小限制)中的突变引起的疾病的治疗,ii)由于内源基因启动子的激活,基因表达接近生理水平,排除了过强和潜在有害的过表达,所述过表达原则上可能由通常使用的装配有强启动子和无内含子cdna的raav载体引起,iii)用于多个基因的有效和同时激活,这可能与双基因或多基因疾病的治疗相关,和iv)开发更广泛适用的不依赖突变的疗法(与耗时和复杂的依赖突变的基因编辑方法(个体化疗法)相反)。
80.反式激活至少一种目的基因的同源基因和任选失活至少一种目的基因的方法,其中由至少一种目的基因编码的mrna与对照相比包含突变,如本文所述,可以在体内以及体外细胞培养中进行,优选用于体内治疗应用。因此,在某些实施方案中,该方法涉及用于治疗有此需要的患者的方法,该方法包括反式激活至少一种目的基因的同源基因,并任选失活至少一种目的基因(例如,其中由至少一种目的基因编码的mrna包含与对照相比的突变);并且其中所述方法包括以下步骤:-结合复合物,所述复合物包含天然或遗传修饰的dna结合蛋白、转录激活因子或转录因子的至少一个反式激活结构域和至少一个引导rna,其中所述至少一种引导rna与所述至少一种目的基因的同源基因的启动子区或调节由所述至少一种目的基因的同源基因编码的mrna的表达的其他元件结合,任选地,其中另一种引导rna与编码区、启动子区和/或调节由所述至少一种目的基因编码的mrna的表达的其他元件结合;并且,其中所述至少一种目的基因选自由如下组成的组:视蛋白基因、环核苷酸门控通道(cng)基因、视黄醛特异性atp结合表达盒转运蛋白(abc转运蛋白)基因和肌球蛋白基因;-诱导由至少一种目的基因的同源基因编码的mrna的表达(从而反式激活至少一种目的基因);以及任选地使由至少一种目的基因编码的mrna的表达失活。有此需要的患者可以是患有遗传性视网膜营养不良(ird)的患者,优选地,其中ird是由于选自由如下组成的组的至少一种目的基因中的突变所致:视蛋白基因、环核苷酸门控通道(cng)基因、视网膜特异性atp结合盒转运蛋白(abc转运蛋白)基因和肌球蛋白基因。用于所述治疗方法中的复合物可以如本文在本发明方法的上下文中所述来指定。
81.本发明还提供了一种复合物,该复合物包含天然或遗传修饰的dna结合蛋白、转录激活因子或转录因子的至少一个反式激活结构域和至少一个引导rna,该复合物用于治疗遗传性视网膜营养不良(ird)的方法中,该遗传性视网膜营养不良是由于选自由如下组成的组的至少一种目的基因的突变:视蛋白基因、环核苷酸门控通道(cng)基因、视网膜特异性atp结合盒转运蛋白(abc转运蛋白)基因和肌球蛋白基因,该方法包括反式激活至少一种目的基因的同源基因,并任选失活至少一种目的基因(例如,其中由至少一种目的基因编码的mrna与对照相比包含突变);其中所述至少一种引导rna与所述至少一种目的基因的同源基因的启动子区域结合,或者与调节由所述至少一种目的基因的同源基因编码的mrna的表达的其他元件结合;任选地,其中另一种引导rna结合编码区、启动子区和/或调节由至少一种目的基因编码的mrna表达的其它元件;并且其中诱导由至少一种目的基因的同源基因编码的mrna的表达;并且任选地使由至少一种目的基因编码的mrna的表达失活。使用的复合物可以如本文在本发明方法的上下文中所描述的那样指定。
82.具体地,在某些实施方案中,天然或遗传修饰的dna结合蛋白选自由如下组成的组:cas酶;优选cas9(seq id no:92)、dcas9-酶(seq id no:96、seq id no:97)、cas12a(seq id no:93)或cas12b(seq id no:94);锌指核酸酶;和转录激活因子样核酸酶;和/或所述转录激活因子或转录因子的至少一个反式激活结构域选自由如下组成的组:vpr(seq id no:89)、sam(seq id no:90)、suntag(seq id no:91)、vp64(seq id no:73)、p65(seq id no:74)、rta(seq id no:75)及其组合。优选地,天然或遗传修饰的dna结合蛋白和转录激活因子或转录因子的至少一个反式激活结构域以及至少一个引导rna作为核苷酸序列提供,更优选地,天然或遗传修饰的dna结合蛋白和转录激活因子或转录因子的至少一个反式激活结构域被分成两个分裂片段。在某些实施方案中,天然或遗传修饰的dna结合蛋白的核苷酸序列和转录激活因子或转录因子的至少一个反式激活结构域的核苷酸序列位于两个独立的质粒和/或载体上。在某些实施方案中,根据本发明使用的复合物包括重组aav载体的使用。aav载体可以是天然的或工程化的,优选地,aav载体是具有视网膜细胞类型向性和/或增强的视网膜转导效率的aav载体变体。因此,在某些实施方案中,提供了天然或遗传修饰的dna结合蛋白、转录激活因子或转录因子的至少一个反式激活结构域和至少一个引导rna的核苷酸序列,用于治疗遗传性视网膜营养不良(ird)的方法,所述遗传性视网膜营养不良是由于根据本发明的选自由如下组成的组的至少一个目的基因中的突变:视蛋白基因、环核苷酸门控通道(cng)基因、视网膜特异性atp结合表达盒转运蛋白(abc转运蛋白)基因和肌球蛋白基因。优选地,天然或遗传修饰的dna结合蛋白和转录激活因子或转录因子的至少一个反式激活结构域的核苷酸序列位于两个独立的质粒和/或载体上。在某些实施方案中,两种独立的载体是重组aav载体。aav载体可以是天然的或工程化的,优选具有视网膜细胞类型向性和/或增强的视网膜转导效率的aav载体变体。
83.本发明还涉及诊断疾病的体外方法。这里不是同源基因被反式激活,而是可能导致或可能与疾病相关的基因。这种方法的效用在一些情况下变得显而易见,在这些情况下,基因测序在理论上是可能的,但可以被一种更便宜的方法所取代,如pcr或western blot,以寻找mrna或蛋白质水平的突变,而不是基因组水平的突变。当人们必须分析在常规应用中无法获得的细胞中表达的mrna或蛋白质时,例如当需要来自视网膜或脑组织的样品时,这尤其有用。通过应用本文所述的方法,可以分析在细胞或组织中表达的基因的mrna和/或
蛋白质(所述mrna和/或蛋白质很难从患者中获得),而不需要侵入性地去除组织样品,例如视网膜或脑。
84.因此,本发明还涉及一种诊断疾病的体外方法,其中该方法包括以下步骤:a)在从受试者获得的细胞或组织样品中诱导由至少一种目的基因编码的mrna的表达;b)分离步骤a)的mrna;c)分析步骤b)的分离的mrna的序列,以及d)从而检测与对照相比mrna的突变,这表明疾病的存在。本文使用的术语“mrna突变”除了包括mrna序列中的突变(核苷酸缺失、插入和/或取代)之外,还包括mrna的改变,例如改变的剪接模式(也称为剪接突变)、降低的mrna稳定性和/或降低的表达(与对照相比)。通常,mrna的改变是由于目的基因中的突变,其中突变可以在编码区或非编码区,例如在启动子、激活区和/或内含子中(例如产生、修饰或消除剪接供体位点或剪接受体位点)。优选地,突变是编码区中的突变或剪接突变。在某些实施方案中,突变和/或改变由引起疾病的突变导致。
85.在根据本发明的诊断疾病的体外方法的一个实施方案中,该方法还包括诱导由mrna编码的蛋白质的表达,并分析细胞或组织样品中由mrna编码的至少一种蛋白质的序列、表达水平、定位或功能。
86.在根据本发明的诊断疾病的体外方法的一个实施方案中,步骤a)包括将包含天然或遗传修饰的dna结合蛋白和转录激活因子或转录因子的至少一个反式激活结构域的复合物特异性结合到至少一种目的基因的启动子区域或结合到调节所述至少一种目的基因表达的其它元件。
87.在根据本发明的诊断疾病的体外方法的一个实施方案中,所述天然或遗传修饰的dna结合蛋白选自由如下组成的组:cas酶;优选cas9(seq id no:92)、dcas9-酶(seq id no:96、seq id no:97)、cas12a(seq id no:93)或cas12b(seq id no:94);锌指核酸酶(zfn);和转录激活因子样核酸酶(talen)。更优选地,天然dna结合蛋白是化脓性链球菌(streptococcus pyogenes)的cas9酶(seq id no:92)。更优选地,遗传修饰的dna结合蛋白选自由如下组成的组:根据seq id no:96具有突变d10a和h840a的dcas9和根据seq id no:97具有突变d10a、d839a、h840a和n863a的dcas9。然而,原则上任何已知生物的所有cas酶都可以用于本发明的方法中。
88.在根据本发明的诊断疾病的体外方法的一个实施方案中,所述天然或遗传修饰的dna结合蛋白是cas酶;优选cas9(seq id no:92)、dcas9-酶(seq id no:96、seq id no:97)、cas12a(seq id no:93)或cas12b(seq id no:94);并且其中所述复合物进一步包含至少一种引导rna,其能够结合到至少一种目的基因的启动子区域或结合到调节至少一种目的基因表达的其他元件。
89.在根据本发明的诊断疾病的体外方法的一个实施方案中,dna结合蛋白在c-或n-末端与转录激活因子或转录因子的至少一个反式激活结构域融合,优选其中转录激活因子或转录因子的至少一个反式激活结构域选自由如下组成的组:vpr(seq id no:89)、sam(seq id no:90)、suntag(seq id no:91)、vp64(seq id no:73)、p65(seq id no:74)、rta(seq id no:75)及其组合。
90.在根据本发明的诊断疾病的体外方法的一个实施方案中,所述疾病是神经退行性疾病、癫痫、心理疾病;优选抑郁症、躁狂症、双相情感障碍、精神分裂症或自闭症;或视网膜疾病,优选遗传性视网膜营养不良,更优选其中所述遗传性视网膜营养不良选自由如下组
成的组:年龄相关性黄斑变性(amd)、遗传性年龄相关性黄斑变性(amd)、常染色体显性、常染色体隐性、x-连锁或双基因视网膜色素变性、色盲、stargardt病、best病、leber氏先天性黑蒙症、视网膜劈裂、先天性静止性夜盲、脉络膜缺失、早发性视网膜营养不良、视锥、视杆视锥或视锥视杆营养不良、模式营养不良、usher综合征和其他综合征性纤毛病,更优选bardet-biedl综合征、joubert综合征、senior-综合征或综合征。
91.为了实施诊断疾病的体外方法,可以用天然或遗传修饰的dna结合蛋白、转录激活因子或转录因子的至少一个反式激活结构域和至少一种引导rna来转导或转染从受试者获得的细胞或组织样品的细胞。因此,在一个实施方案中,该方法还包括转染或转导从受试者获得的细胞或组织样品。
92.根据本发明的诊断疾病的体外方法也可以用于分析与疾病有关的基因和/或蛋白质的剪接模式。因此,根据本发明的诊断疾病的方法可以进一步包括通过分析至少一个目的基因的剪接模式与对照的剪接模式的差异来检测至少一个目的基因的改变的剪接模式,并且其中改变的剪接模式也指示疾病的存在。在本发明的上下文中使用的术语“剪接模式”是指剪接过程的完整结果。内含子剪接存在于所有真核生物中,但是每种生物采用的剪接方法和剪接频率不同。细菌和古细菌缺乏剪接体途径,很少通过自剪接内含子进行剪接。在单细胞真核生物中,剪接频率有一个很大的范围。在单个基因的单个mrna转录本之间,内含子和识别的剪接位点的数量可能不同,从而引起剪接变异和选择性剪接现象。后者则导致不同的剪接模式。
93.在根据本发明的诊断疾病的体外方法的一个实施方案中,来自受试者的细胞样品是血液样品、唾液样品、尿液样品、皮肤样品或粘膜样品。
94.本发明还涉及用于治疗或预防疾病的核酸序列,其包含根据seq id no:51、seq id no:52、seq id no:53、seq id no:54、seq id no:55、seq id no:56、seq id no:57、seq id no:58、seq id no:59、seq id no:60、seq id no:61、seq id no:62、seq id no:63、seq id no:64、seq id no:65、seq id no:66、seq id no:67、seq id no:68、seq id no:69、seq id no:70、seq id no:71、seq id no:72)和(seq id no:123的任何序列或由其组成。
95.此外,本发明还涉及用于本文所述的任何方法的核酸序列,其包含如下序列或由其组成:seq id no:51、seq id no:52、seq id no:53、seq id no:54、seq id no:55、seq id no:56、seq id no:57、seq id no:58、seq id no:59、seq id no:60、seq id no:61、seq id no:62、seq id no:63、seq id no:64、seq id no:65、seq id no:66、seq id no:67、seq id no:68、seq id no:69、seq id no:70、seq id no:71、seq id no:72和seq id no:123。
96.本发明还包括用于治疗或预防疾病的如上所述的任何核酸序列,其中所述疾病是神经退行性疾病、癫痫、心理疾病;优选抑郁症、躁狂症、双相情感障碍、精神分裂症或自闭症;或视网膜疾病,优选遗传性视网膜营养不良,更优选其中所述遗传性视网膜营养不良选自由如下组成的组:年龄相关性黄斑变性(amd)、遗传性年龄相关性黄斑变性(amd)、常染色体显性、常染色体隐性、x-连锁或双基因视网膜色素变性、色盲、stargardt病、best病、leber氏先天性黑蒙症、视网膜劈裂、先天性静止性夜盲、脉络膜缺失、早发性视网膜营养不良、视锥、视杆视锥或视锥视杆营养不良、模式营养不良、usher综合征和其他综合征性纤毛病,更优选bardet-biedl综合征、joubert综合征、senior-综合征或综合征。
97.因此,本发明的方法提供了几个重要的优点:i)由于其简单性,其适用于常规诊断,ii)其可用于检测已知基因中的新核苷酸变体,iii)其可用于对致病基因中的已知疾病变体进行重新分类,iv)其可用于验证(或质疑)所检测到的突变的拟议致病性,以及v)其可用于任何遗传疾病。
98.所述疾病可以是,例如,神经退行性疾病、癫痫、心理疾病;优选抑郁症、躁狂症、双相情感障碍、精神分裂症或自闭症;或视网膜疾病,优选遗传性视网膜营养不良,更优选其中所述遗传性视网膜营养不良选自由如下组成的组:年龄相关性黄斑变性(amd)、遗传性年龄相关性黄斑变性(amd)、常染色体显性、常染色体隐性、x-连锁或双基因视网膜色素变性、色盲、stargardt病、best病、leber氏先天性黑蒙症、视网膜劈裂、先天性静止性夜盲、脉络膜缺失、早发性视网膜营养不良、视锥、视杆视锥或视锥视杆营养不良、模式营养不良、usher综合征和其他综合征性纤毛病,更优选bardet-biedl综合征、joubert综合征、senior-综合征或综合征。
99.本领域技术人员熟知的多种基于序列的比对方法可用于确定序列间的同一性。这些包括但不限于smith,f.和waterman,m.s.(1981)adv.appl.math.2:482
–
89的局部同一性/同源性算法(the local identity/homology algorithm)、peason,w.r.和lipman,d.j.(1988)proc.natl.acad.sci.usa 85:2444
–
48的同源性比对算法(homology alignment algorithm)、altschul,s.f.et al.(1990)j.mol.biol.215:403
–
10描述的局部序列排比检索基本工具(blast)、或者devereau,j.et al.(1984)nucleic acids.res.12:387
–
95描述的the最佳适应程序(best fit program),以及fasta和tfasta比对程序,优选使用默认设置或通过检查。或者,可以如下对氨基酸序列进行手动/视觉比对:分别如本文所定义的,所讨论的氨基酸序列(查询序列)和本发明的/序列表中公开的氨基酸序列(参考序列)之间的同一性百分比通过使得在两个氨基酸序列之间获得最大的同一性的成对比对来确定。对两个氨基酸序列之间的相同氨基酸残基进行计数,并除以参考序列的残基总数(包括不含氨基酸残基的位置,例如一个或多个缺口),得到同一性百分比。
100.ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
***
101.注意,本文所使用的单数形式“一个(a)”、“一个(an)”和“所述(the)”包括复数引用,除非上下文另有明确说明。因此,例如,对于“一种试剂”包括一种或多种这样的不同试剂,以及对于“所述方法”包括本领域普通技术人员已知的等效步骤和方法,这些步骤和方法可以被修改或替代本文所述的方法。
102.除非另有说明,否则在一系列元素之前的术语“至少”应理解为意指该系列中的每个元素。如果没有特别不同的定义,术语“至少一个”是指一个或多个,例如两个、三个、四个、五个、六个、七个、八个、九个、十个或更多。本领域技术人员将认识到,或者仅使用常规实验就能够确定本文描述的本发明的具体实施方案的许多等同方案。这样的等同方案旨在被本发明所包含。
103.在本文中使用的术语“和/或”包括“和”、“或”和“由所述术语连接的元素的所有或任何其他组合”的含义。
104.术语“小于”或“大于”不包括具体数字。
105.例如,小于20表示小于指定的数值。类似地,“多于”或“大于”是指多于或大于指定的数值,例如多于80%是指多于或大于指定的数值80%。
106.在整个说明书和随后的权利要求中,除非上下文另有要求,否则词语“包括(comprise)”以及诸如“包含(comprises)”和“包含(comprising)”的变体将被理解为意指包括所陈述的整体(integer)、或整体(integers)或步骤(steps)的步骤(step)或分组(group),但不排除任何其他整体(integer)、或整体(integer)或步骤(step)的步骤(step)或分组(group)。当在本文使用时,术语“包含”可以用术语“包括”或“含有”代替,或者当在本文使用时,有时用术语“具有”代替。本文中使用的“由......组成”排除了未具体指明的任何元素、步骤或成分。
107.术语“包括”是指“包括但不限于”。“包括”和“包括但不限于”可互换使用。
108.术语“大约”是指加减10%,优选加减5%,更优选加减2%,最优选加减1%。
109.在本说明书的整个说明书和权利要求书中,除了上下文另外需要之外,单数涵盖复数。特别地,除非上下文另有要求,在使用不定冠词的情况下,说明书应被理解为考虑复数以及单数。
110.应当理解,本发明不限于本文描述的特定的方法、方案、材料、试剂和物质等,并且这些可以变化。本文使用的术语仅仅是为了描述特定的实施方案,而不是为了限制本发明的范围,本发明的范围仅由权利要求来限定。
111.本说明书全文引用的所有出版物(包括所有专利、专利申请、科学出版物、说明书等),无论是上文还是下文,都通过引用整体并入本文。本文中的任何内容均不应解释为承认本发明无权凭借在先发明而早于这种公开。被引入以供参考之数据范围与本说明书抵触或不符时本说明书将取代任何此类资料。
112.本文引用的所有文献和专利文献的内容通过引用整体并入本文。
113.从以下实施例中可以更好地理解本发明及其优点,这些实施例仅用于说明目的。这些实施例无意以任何方式限制本发明的范围。
114.本发明的实施例
115.以下实施例说明了本发明,但不应理解为限制本发明的范围。
116.实施例1:用于眼部基因治疗的dcas9-vpr介导的反式激活
117.cnga1在表达诱导型全长dcas9-vpr表达盒的661w细胞中的反式激活
118.使用dcas9-vpr与结合在小鼠cnga1(seq id no:13)启动子区域的三种不同grna的组合,我们测试了该基因的反式激活效率。对于cnga1(seq id no:13)的激活,我们使用661w细胞,其为表达多种视锥特异性标记物且缺乏cnga1(seq id no:13)表达的永生化鼠视网膜母细胞瘤的衍生物(al-ubaidi et al.,1992)。在稳定表达强力霉素诱导的dcas9-vpr表达盒(seq id no:123)和cnga1grna(cnga1中grna的靶序列(seq id no:76-seq id no:78),包括pam序列)组合的661w细胞中,我们可以在mrna和蛋白质水平上检测cnga1信号,这在稳定表达dcas9-vpr lacz grna表达盒(seq id no:124)的661w对照细胞中完全不存在(图3a-f)。此外,使用膜片钳记录,我们可以证明携带dcas9-vpr cnga1 grna表达盒(seq id no:123)的661w细胞显示cnga1特异性电流的两个关键功能特征:cgmp依赖性激活和ca
2+
/mg
2+
依赖性抑制(图3g-l)。
119.实施例2:cas9断裂内含肽介导的重建效率
120.如上所述,dcas9-vpr表达盒(seq id no:123)超过了aav载体的包装能力。为了扩大dcas9-vpr系统的体内应用范围,我们测试了分裂内含肽技术的效率,以将dcas9-vpr分
裂重组为两个不同的部分,并在两个单独的质粒上提供。已知分裂内含肽介导的重建效率取决于相应蛋白质内的分裂位置。在最近的研究中,两个独立的小组利用分裂内含肽技术研究了cas9在aa位置e573(truong et al.,2015)或v713(chew et al.,2016)分裂的核酸酶活性。这两个小组都表明分裂和重建的cas9的核酸酶活性原则上保持不变。然而,不存在关于在蛋白质水平上这两个位置分裂的cas9的重建效率的绝对或比较数据。在瞬时转染的hek293细胞的初始实验中,我们定量了在这两个位置相交的cas9分裂内含肽片段的重建效率。如图4所示,在v713处分裂的cas9变体的重建效率(56.9%
±
2.1%)显著高于在e573位置分裂的重建效率(33.3%
±
2.1%)。
121.实施例3:在瞬时转染的661w或mef细胞中,dcas9-vpr和分裂内含肽dcas9-vpr介导的cnga1(seq id no:13)、opn1mw(seq id no:43)和opn1sw(seq id no:45)基因的反式激活
122.本发明人还分析了cnga1(seq id no:13)、opn1mw(seq id no:43)和opn1sw(seq id no:13)基因在用全长dcas9-vpr(seq id no:95)或在v713位置分裂的dcas9-vpr(本文称为v713_dc9)与相应grna组合瞬时转染的细胞中的反式激活效率(图5)。对于视锥视蛋白的反式激活,我们使用了小鼠胚胎成纤维细胞(mef),该细胞(与661w细胞相反)不表达大量的这些基因。使用全长dcas9-vpr(seq id no:95),发明人观察到所有三个基因的有效反式激活。类似地,v713_dc9与cnga1(包括pam序列的cnga1中grna的靶序列:seq id nos:76-78)或opn1mw(包括pam序列的grna的靶序列:seq id nos:79-81)grna的组合也可以反式激活两种基因,尽管与全长dcas9变体相比效率较低。到目前为止,本发明人在这种体外设置中没有包括v713_dc9与opn1sw grna(包括pam序列的grna的靶序列:seq id nos:83-85)的组合。在所有情况下,在表达lacz对照grna(包括pam序列的lacz中grna的靶序列:seq id no:125)的细胞中没有检测到相应基因的反式激活。
123.实施例4:视杆感光细胞中v713_dc9介导的opn1mw(seq id no:43)和opn1sw(seq id no:45)的反式激活
124.本发明人还分析了v713_dc9是否可以反式激活野生型小鼠的视杆感光细胞中的opn1mw(seq id no:43)和opn1sw(seq id no:45)基因。为此,本发明人给小鼠注射了aav2/8病毒血清型,该血清型配有人视紫红质启动子(图6a),用于在视杆细胞中特异性表达。注射后三周,将注射动物的视网膜用于免疫标记或rna分离,然后进行qrt-pcr研究。
125.与视锥细胞相比,视杆感光细胞在鼠视网膜的所有部分都以高得多的密度存在。此外,鼠视杆细胞的外节比源自视锥细胞的外节长。这些特性使得能够容易地区分视杆和视锥感光细胞外节。本发明人可以在》50%的用特异性抗体免疫标记的注射视网膜中检测到opn1mw(seq id no:44)和opn1sw(seq id no:46)信号的强烈增加。该信号遍布注射部位周围的感光细胞外节,是视杆感光细胞外节特异性蛋白质的特征。因此,发明人得出结论,增加的opn1mw(seq id no:44)和opn1sw(seq id no:46)信号很可能来源于v713_dc9介导的相应基因的反式激活(图6b-e)。
126.在相应的qrt-pcr实验中,50%(opn1sw,图6g)至100%(opn1mw,图6f)的注射视网膜显示出opn1mw(seq id no:43)和opn1sw(seq id no:45)mrna水平的增加。与图5g所示的mef细胞中的相应实验相比,这种增加较低。然而,这一发现是相当可期待的,因为(与mef细胞相反)两种基因在注射小鼠的视锥细胞中都是内源性高表达的。
127.实施例5:opn1mw反式激活延缓了杂合rho小鼠的视网膜变性并改善了视网膜功能
128.发明人还测试了opn1mw反式激活是否足以改善杂合子视紫红质缺陷型rp小鼠模型中的色素性视网膜炎表型(humphries et al.,1997)。为此目的,向杂合(hz)rho小鼠视网膜下注射滴度匹配的双raav载体,其表达分裂的dcas9-vpr和opn1mw sgrna(hz处理)。对侧对照眼注射nacl(hz假)溶液(图7)。
129.因为杂合rho小鼠表现出缓慢的视网膜变性过程(humphries et al.,1997),注射后一年评估治疗效果,年龄匹配的未治疗wt小鼠作为附加对照。视网膜变性伴随着感光细胞的减少,这种情况可以通过光学相干断层扫描(oct)测量外核层(onl)的厚度来非侵入性地解决。来自表达分裂dcas9-vpr和opn1mw sgrna的眼睛的oct记录显示,与对侧注射nacl的眼睛相比,onl厚度增加,这表明该治疗能够延迟变性(图7b)。
130.为了评估该方法对视杆细胞介导的(暗视)视网膜功能的有益效果,发明人在暗适应杂合rho小鼠中进行了视网膜电图(erg)测量(图7a)。当将经治疗的眼睛与其注射nacl的对照体进行比较时,观察到暗视b波的显著改善。总之,这些数据表明,在杂合rho rp小鼠模型中,opn1mw反式激活可以改善视网膜变性,并导致视网膜功能的改善。
131.实施例6:用于遗传疾病诊断的dcas9-vpr介导的反式激活
132.为了对常见的ird连锁基因提供crispr/cas9介导的反式激活的原理证明,出于以下几个原因,我们聚焦ush2a(seq id no:49)。第一、ush2a(seq id no:49)是最常见的常染色体隐性视网膜色素变性(arrp)和usher综合征(ush)基因(占arrp的10-15%和ush病例的30-40%,(huang et al.,2018))。第二,合作的慕尼黑lmu眼科医院拥有大量ush2a(seq id no:49)患者队列。在其中一些患者中,只能鉴定出一种ush2a(seq id no:49)突变,这表明在常规遗传诊断没有覆盖的区域中存在第二种变体。第三,ush2a(seq id no:49)在可以从患者中常规获得的组织和/或细胞类型中不表达(https://www.proteinatlas.org/ensg00000042781-ush2a/tissue),这阻碍了在未经治疗的患者细胞中ush2a(seq id no:49)mrna的分析。第四,ush2a(seq id no:49)属于人类基因组中最大的基因,阻碍了潜在致病突变的鉴定,尤其是那些位于非编码区的突变。
133.对于解决ush2a(seq id no:49)的反式激活的实验,从一个发明人的皮肤活检中分离出人成纤维细胞。根据先前描述的标准程序培养细胞(chen et al.,2014)并用与三种不同的ush2a grna(包括pam序列的ush2a中grna的靶序列:seq id nos:86-88)组合的dcas9-vpr(seq id no:95)瞬时转染,所述三种不同的ush2a grna靶向人成纤维细胞中的天然ush2a启动子。将与lacz特异性grna(包括pam序列的lacz中grna的靶序列:seq id no:125)组合的dcas9(seq id no:96)用作对照。
134.ush2a(seq id no:49)位于染色体1q41的(-)链上。另一个基因(kctd3)(seq id no:122)紧邻ush2a(seq id no:49)在相反的(+)链上,两个基因在3’非翻译区(utr)的远端部分有重叠(图8a)。使用ush2a特异性引物在rt-pcr和qrt-pcr水平上分析ush2a(seq id no:49)反式激活(参见seq id no:98
–
121;图8b-d)。对于rt-pcr实验,我们设计了一组12个引物对(seq id nos:98
–
121),覆盖了整个ush2a(seq id nos:49)转录本。单个pcr产物的大小范围在1.5-1.8kb之间,使得能够在mrna水平上进行方便的分析,并检测来自患者细胞的潜在剪接突变。在用dcas9-vpr(seq id no:95)与ush2a grna(包括pam序列的ush2a中grna的靶序列:seq id no:86-88)联合转染的细胞中,所有引物对(seq id no:98-121)都
产生预期大小的特异性条带。通过sanger测序确认每个条带的身份。除了覆盖远端3’utr区的最后一对引物外,在用lacz对照grna(包括pam序列的lacz中grna的靶序列:seq id no:125)转染的成纤维细胞中没有检测到条带。正如预期的那样,在lacz对照细胞中3’utr带的sanger测序证实它来源于kcdt3基因(seq id no:122),该基因与ush2a(seq id no:49)在远端3’utr重叠。
135.实施例7:在杂合rho小鼠中,opn1mw反式激活减少了细胞凋亡,而没有诱导神经胶质增生或免疫应答细胞的侵入
136.为了评估这种方法的翻译潜力,我们检测了我们的治疗是否诱导了持续的胶质增生或免疫反应,这将伴随着视网膜中胶质纤维酸性蛋白(gfap)阳性的m
ü
ller胶质细胞或离子化钙结合衔接分子1(iba-1)阳性的小胶质细胞或单核细胞的增殖。重要的是,用这些标记对视网膜进行的免疫标记显示,不同组之间的神经胶质细胞、小神经胶质细胞或单核细胞的数量没有明显增加,而rd1(视网膜变性1)小鼠的视网膜在p13时表现出快速视网膜变性峰值(j.sancho-pelluz et al.,mol neurobiol 38,253-269(2008)))(图9c-h)。为了研究在杂合rho小鼠模型中感光细胞变性是否是由凋亡引起的,我们对来自经处理的杂合rho小鼠的视网膜切片进行了tunel分析(图10a,b)。为了检测凋亡,根据制造商的说明使用原位细胞死亡检测试剂盒,fluorescein(11684795910;roche)。在该试验中,我们可以检测到少量但相当数量的tunel阳性细胞,表明凋亡是该小鼠模型中感光细胞丧失的潜在机制。此外,通过比较经处理的视网膜的转导部分与未转导部分中每单位面积的tunel阳性细胞数,我们表明opn1mw反式激活减少了凋亡(图10c)。这些数据进一步强调了我们的治疗对感光细胞存活的有益作用。
137.实施例8:用于同时rho敲除和opn1mw激活的grna多重方法
138.dcas9-vpr介导的同源基因反式激活能够治疗导致疾病的功能缺失突变,其中缺失由目的基因编码的蛋白是疾病的驱动因素。然而,许多遗传疾病是由功能获得或显性阴性突变引起的,导致目的基因产生有害的蛋白质。成功治疗这种突变不仅需要补偿缺失的功能蛋白,还需要同时去除突变的有害蛋白。为了测试上述方法对此目的的适用性,本发明人使用了催化活性的cas9-vpr与包含》16bp原间隔区(ps)的grna(保留了cas9催化活性)组合来敲除鼠视紫红质基因(rho)(包括pam序列的sgrho的靶序列:seq id no:82)。此外,他们采用了两个或多个具有短原间隔区序列(《16bp)的grna,其抑制cas9蛋白的催化活性,靶向鼠m-视蛋白基因(opn1mw)的启动子(sgopn1mw_1_short:ggggcctttaaggtaagg,seq id no:126(包括pam序列)和sgopn1mw_2_short:gccacccctgtggattgg,seq id no:127(包括pam序列)的靶序列)以激活该视紫红质同源物(图11a)。
139.为了在体内测试该方法,需要将cas9-vpr编码序列分成两部分,通过两个独立的raav载体递送,并在靶细胞即感光细胞中重建。然而,cas9-vpr的有效重建是有效治疗的关键因素。因此,在该实验中比较了两种不同的重建策略:能够在蛋白质水平重建的分裂内含肽方法(图11b)和能够在rna水平重建的mrna反式剪接(revert)方法(图11c)。
140.对于该实验,给2个月大的c57bl/6j野生型小鼠注射含有分裂的cas9-vpr构建体与两个opn1mw靶向grna和一个rho靶向grna(多重方法)组合,或与一个单一lacz靶向对照grna组合的aav(图11b,c)。注射后四周,从视网膜中提取rna,并通过qrt-pcr进行分析。结果显示cas9-vpr通过revert以高水平成功重建(图11d)。无法评估通过分裂内含肽的重建,
the packaging capacity of adeno-associated virus capsids.hum gene ther methods 27:1-12
153.chavez a,scheiman j,vora s,pruitt bw,tuttle m,et al.2015.highly efficient cas9-mediated transcriptional programming.nat methods 12:326-8
154.chavez a,tuttle m,pruitt bw,ewen-campen b,chari r,et al.2016.comparison of cas9 activators in multiple species.nat methods 13:563-7
155.chen cc,keller m,hess m,schiffmann r,urban n,et al.2014.a small molecule restores function to trpml1 mutant isoforms responsible for mucolipidosis type iv.nat commun 5:4681
156.chew wl,tabebordbar m,cheng jk,mali p,wu ey,et al.2016.a multifunctional aav-crispr-cas9 and its host response.nat methods 13:868-74
157.daiger sp,sullivan ls,bowne sj.2013.genes and mutations causing retinitis pigmentosa.clin genet 84:132-41
158.finn jt,krautwurst d,schroeder je,chen ty,reed rr,yau kw.1998.functional co-assembly among subunits of cyclic-nucleotide-activated,nonselective cation channels,and across species from nematode to human.biophys j 74:1333-45
159.flotte tr.2000.size does matter:overcoming the adeno-associated virus packaging limit.respir res 1:16-8
160.fu y,kefalov v,luo dg,xue t,yau kw.2008.quantal noise from human red cone pigment.nat neurosci 11:565-71
161.gerstner a,zong x,hofmann f,biel m.2000.molecular cloning and functional characterization of a new modulatory cyclic nucleotide-gated channel subunit from mouse retina.j neurosci 20:1324-32
162.godfrey c,desviat lr,smedsrod b,pietri-rouxel f,denti ma,et al.2017.delivery is key:lessons learnt from developing splice-switching antisense therapies.embo mol med 9:545-57
163.grodecka l,buratti e,freiberger t.2017.mutations of pre-mrna splicing regulatory elements:are predictions moving forward to clinical diagnostics?int j mol sci 18
164.huang l,mao y,yang j,li y,li y,yang z.2018.mutation screening of the ush2a gene in retinitis pigmentosa and usher patients in a han chinese population.eye(lond)32:1608-14
165.humphries mm,rancourt d,farrar gj,kenna p,hazel m,et al.1997.retinopathy induced in mice by targeted disruption of the rhodopsin gene.nat genet 15:216-9
166.kefalov vj.2012.rod and cone visual pigments and phototransduction through pharmacological,genetic,and physiological approaches.j biol chem 287:
olfactory neurons.proceedings of the national academy of sciences of the united states of america 95:4696-701
180.scholl hp,strauss rw,singh ms,dalkara d,roska b,et al.2016.emerging therapies for inherited retinal degeneration.sci transl med 8:368rv6
181.shanks me,downes sm,copley rr,lise s,broxholme j,et al.2013.next-generation sequencing(ngs)as a diagnostic tool for retinal degeneration reveals a much higher detection rate in early-onset disease.eur j hum genet 21:274-80
182.shi g,yau kw,chen j,kefalov vj.2007.signaling properties of a short-wave cone visual pigment and its role in phototransduction.j neurosci 27:10084-93
183.truong dj,kuhner k,kuhn r,werfel s,engelhardt s,et al.2015.development of an intein-mediated split-cas9 system for gene therapy.nucleic acids res 43:6450-8
184.vache c,besnard t,le berre p,garcia-garcia g,baux d,et al.2012.usher syndrome type 2 caused by activation of an ush2a pseudoexon:implications for diagnosis and therapy.hum mutat 33:104-8
185.wang h,la russa m,qi ls.2016.crispr/cas9 in genome editing and beyond.annu rev biochem 85:227-64
186.webb tr,parfitt da,gardner jc,martinez a,bevilacqua d,et al.2012.deep intronic mutation in ofd1,identified by targeted genomic next-generation sequencing,causes a severe form of x-linked retinitis pigmentosa(rp23).human molecular genetics 21:3647-54
187.wu z,yang h,colosi p.2010.effect of genome size on aav vector packaging.molecular therapy:the journal of the american society of gene therapy 18:80-6
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1