一种酰胺化合物的制备方法与流程
1.本发明属于有机化合物的合成领域,具体涉及一种酰胺化合物的制备方法。
背景技术:
2.酰胺化合物在农药和医药领域中应用广泛,由于这类化合物具有广谱的生物活性,在杀虫、杀菌、除草以及抗病毒等农业方面具有较多的应用。
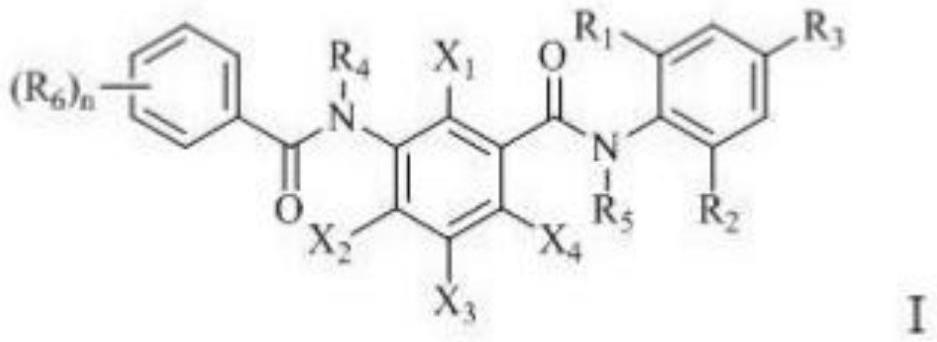
3.公开号cn110194726a的专利文献报道了一种苯甲酰胺类化合物及其应用,具有式i结构的化合物具有优异的杀虫活性,在较低剂量下可有效防治小菜蛾、粘虫、二化螟等害虫。
[0004][0005]
但其合成方法有较大缺陷,尤其是使用溴乙腈与酰胺反应步骤,用到叔丁醇钾和氢化钠等反应条件苛刻,且收率较低,该反应的分离过程需要经过柱层析步骤,限制了其工业化的大规模应用。
[0006]
如公开号为cn108840806a的专利文献公开了一种苯甲酰胺类化合物的制备方法,该方法是经氨基化合物与苯乙腈混合加入溶剂中,在铜催化剂作用下反应,反应结束后,经过柱层析步骤才得到目标产物,而且该方法得到的产物收率较低。
[0007]
一直以来,技术人员致力于不断研究开发新的、更为先进合理、更适合工业化生产的制备方法,以便以更加简单的制备工艺、更高的收率、更低的价格获得酰胺化合物。
[0008]
因此,寻找一种制备工艺简单,可以将氰甲基化步骤提前,产物不需要经过柱层析步骤直接进入下一步反应,且反应的收率高,适合工业化生产的酰胺化合物的制备方法具有十分重要的意义。
技术实现要素:
[0009]
针对目前酰胺化合物制备方法的不足,本发明提供一种制备工艺简单、反应的收率高、适合工业化生产的酰胺化合物制备方法。
[0010]
本发明通过以下技术方案实现:
[0011]
一种酰胺化合物的制备方法,反应式如下:
[0012][0013]
式中:
[0014]
r1、r2各自独立地选自氢、卤素、c1‑
c6的烷基、c1‑
c6的卤代烷基、c1‑
c6的烷氧基或c1‑
c6的卤代烷氧基;
[0015]
r3选自七氟异丙基或九氟
‑2‑
丁基;
[0016]
r4选自氢、c1‑
c6的烷基、c1‑
c6的卤代烷基或氰甲基;
[0017]
r5选自氢、卤素、氰基、硝基、c1‑
c6的烷基、c1‑
c6的卤代烷基、c1‑
c6的烷氧基、c1‑
c6的卤代烷氧基、c1‑
c6的烷硫基或c1‑
c6的卤代烷硫基;
[0018]
x1、x2、x3各自独立地选自氢、卤素、氰基或c1‑
c6的烷氧基;
[0019]
反应步骤如下:
[0020]
①
:式(2)化合物与取代乙腈进行一次取代反应制得式(3)化合物;
[0021]
②
:式(3)化合物和苯甲酰氯进行二次取代反应制得式(4)化合物;
[0022]
③
:式(4)化合物在碱性条件下经水解反应制得式(5)化合物;
[0023]
④
:式(5)化合物经酰氯化后的酰氯化物与式(6)化合物进行酰胺化反应后制得式(1)的酰胺化合物。
[0024]
作为技术方案的优选,所述步骤
①
中取代乙腈为氯乙腈、溴乙腈及羟基乙腈中的一种,所述式(2)化合物与取代乙腈的摩尔比为1:1
‑
2。
[0025]
作为技术方案的优选,所述步骤
②
中式(3)化合物与苯甲酰氯的摩尔比为1:1
‑
3。
[0026]
作为技术方案的优选,所述步骤
③
中反应的碱为碳酸钾、碳酸钠及碳酸氢钠中的一种,所述式(4)化合物与碱的摩尔比为1:0.5
‑
3,所述水解反应的温度为25
‑
80℃。
[0027]
作为技术方案的优选,所述步骤
④
中酰氯化物与式(6)化合物的摩尔比为1:0.5
‑
2。
[0028]
作为技术方案的优选,所述步骤
④
中式(5)化合物酰氯化所用的溶剂为草酰氯或二氯亚砜。
[0029]
作为技术方案的优选,所述步骤
④
中酰氯化物在碘化钾的催化下与式(6)化合物
在乙腈溶剂中反应。
[0030]
作为技术方案的优选,所述式(2)化合物制得式(3)化合物以及式(3)化合物制得式(4)化合物的溶剂各自选择甲苯、丙酮、乙腈、二氯甲烷、二氧六环及二甲基甲酰胺中的一种。
[0031]
作为技术方案的优选,所述步骤
①
中式(2)化合物还可以与甲醛和氢氰酸反应制得式(3)化合物。
[0032]
作为技术方案的优选,所述步骤
①
中式(2)化合物、甲醛和氢氰酸的摩尔比为1:5
‑
6:4
‑
5。
[0033]
与现有技术相比,本发明的优点及有益效果:
[0034]
1.本发明公开的新的制备酰胺化合物的方法避免了现有技术中在溴乙腈与酰胺反应步骤中用到叔丁醇钾和氢化钠等苛刻的反应条件,而且本方法中还将氰甲基化步骤提前,产物不需要经过柱层析步骤,直接进行下一步反应,缩短工艺操作流程,极大地提高了反应的效率。
[0035]
2.本发明的制备酰胺化合物的方法设计合理,该工艺反应条件温和,原料易得,操作方便,产物收率高,适合规模化生产,对于酰胺化合物的工业化生产具有重要的市场价值和经济效益,还为酰胺化合物的进一步研究奠定了基础。
具体实施方式
[0036]
下面将结合具体实施例对本发明进一步详细说明,但不限于本发明的保护范围。
[0037]
实施例1
[0038]
式(1)化合物的合成:
[0039][0040]
步骤a:在圆底烧瓶中依次加入1.5克2
‑
氟
‑3‑
胺基苯甲酸甲酯、1.2克溴乙腈,0.2克碘化钾、10毫升二甲基甲酰胺,将混合物缓慢加热,升温回流反应10h,利用薄层色谱法跟踪,反应完成后冷却至室温,将反应得到的混合物进行蒸馏,产物依次用石油醚、水洗涤,乙酸乙酯萃取真空干燥后得1.5克式(3)化合物,收率81%;
[0041][0042]
步骤b:在圆底烧瓶中依次加入1克步骤a的产物式(3)化合物、15克乙腈、0.8克苯甲酰氯,将混合物缓慢加热,升温回流反应15h,利用薄层色谱法跟踪,反应完成后冷却至室温,将反应得到的混合物进行蒸馏,收集固体,依次用异辛烷、碳酸钠水溶液、水洗涤,40℃下真空干燥得1.2克式(4)化合物,收率80%;
[0043][0044]
步骤c:在圆底烧瓶中依次加入1克式(4)化合物后、2克二氧六环、4克水、0.6克碳酸钾,30℃下水解2h后,加入10%盐酸调节ph至6,用乙酸乙酯萃取,有机相用饱和食盐水洗,无水硫酸钠干燥,减压下蒸干溶剂,得1.3克式(5)化合物,收率85%;
[0045][0046]
步骤d:烧瓶中依次加入1克步骤3产物式(5)化合物、10克二氯甲烷,冰浴下滴加20克草酰氯,常温下搅拌5h,产生的氯化氢气体用水吸收得到副产物盐酸,减压蒸馏,干燥后得到式(5)化合物的酰氯化物,待用;
[0047]
步骤e:烧瓶中依次加入10克乙腈、0.7克式2,6
‑
二溴
‑4‑
七氟异丙基苯胺、0.5克碘化钾,搅拌加入0.6克式(5)化合物的酰氯化物,缓慢加热,升温回流反应8小时,降温后加入剩余的酰氯化物,再次加热升温回流,点板跟踪至胺反应完全,将反应液倾入饱和碳酸氢钠溶液中,过滤析出的的固体,真空干燥后得1.1克式(1)化合物,收率71%。
[0048][0049]
实施例2
[0050]
式(1)化合物的合成:
[0051][0052]
步骤a:在圆底烧瓶中依次加入1.8克2
‑
氟
‑3‑
胺基苯甲酸甲酯、1.5克溴乙腈,0.3克碘化钾、15毫升丙酮,将混合物缓慢加热,升温回流反应10h,利用薄层色谱法跟踪,反应完成后冷却至室温,将反应得到的混合物进行蒸馏,收集产物,依次用石油醚、水洗涤,40℃真空干燥后得1.7克式(3)化合物,收率83%;
[0053][0054]
步骤b:在圆底烧瓶中依次加入1.2克步骤a的产物式(3)化合物、15克二氯乙烷、1.0克苯甲酰氯,将混合物缓慢加热,升温回流反应8h,利用薄层色谱法跟踪,反应完成后冷却至室温,将反应得到的混合物进行蒸馏,收集固体,依次用异辛烷、水、碳酸钠、水洗涤,40℃真空干燥得1.2克式(4)化合物,收率80%;
[0055][0056]
步骤c:在圆底烧瓶中依次加入1.2克式(4)化合物后、3克二氧六环、6克水、0.8克碳酸钠,40℃下水解2h后,加入盐酸中和,用乙酸乙酯萃取,有机相用饱和食盐水洗,无水硫酸镁干燥,减压下蒸干溶剂,得1.3克式(5)化合物,收率84%;
[0057][0058]
步骤d:烧瓶中依次加入1.2克步骤3产物式(5)化合物、15克二氯甲烷,冰浴下滴加10克氯化亚砜,常温下搅拌5h,产生的氯化氢气体用水吸收得到副产物盐酸,减压蒸馏,干燥后得到式(5)化合物的酰氯化物,待用;
[0059]
步骤e:烧瓶中依次加入15克乙腈、0.8克2,6
‑
二溴
‑4‑
七氟异丙基苯胺、0.7克碘化钾,搅拌加入0.7克式(5)化合物的酰氯化物,将混合物缓慢加热,升温回流反应10h,降温后加入剩余的酰氯化物,再次加热升温回流,点板跟踪至胺反应完全,将反应液倾入饱和碳酸氢钠溶液中,过滤析出的的固体,真空干燥后得1.3克式(1)化合物,收率76%。
[0060][0061]
实施例3
[0062]
式(1)化合物的合成:
[0063][0064]
步骤a:在圆底烧瓶中依次加入2.0克2
‑
氟
‑3‑
胺基苯甲酸甲酯、1.8克溴乙腈,0.5克碘化钾、18毫升乙腈,将混合物缓慢加热,升温回流反应8h,利用薄层色谱法跟踪,反应完成后冷却至室温将反应得到的混合物进行蒸馏,收集固体,依次用石油醚、水洗涤,40℃真空干燥后得2.1克式(3)化合物,收率85%;
[0065][0066]
步骤b:在圆底烧瓶中依次加入1.5克步骤a的产物式(3)化合物、20克甲苯、1.2克苯甲酰氯,将混合物缓慢加热,升温回流反应8h,利用薄层色谱法跟踪,反应完成后冷却至室温,将反应得到的混合物进行蒸馏,收集固体,依次用异辛烷、水、碳酸钠、水洗涤,40℃真空干燥得1.6克式(4)化合物,收率82%;
[0067][0068]
步骤c:在圆底烧瓶中依次加入1.5克式(4)化合物后、4克二甲基亚酰胺、8克水、1.2克碳酸氢钠,50℃下水解2h后,加入盐酸中和,用乙酸乙酯萃取,有机相用饱和食盐水洗,无水硫酸镁干燥,减压下蒸干溶剂,得1.3克式(5)化合物,收率65%;
[0069][0070]
步骤d:烧瓶中依次加入1.2克步骤3产物式(5)化合物、10克二氯甲烷,冰浴下滴加20克草酰氯,常温下搅拌5h,产生的氯化氢气体用水吸收得到副产物盐酸,减压蒸馏,干燥后得到式(5)化合物的酰氯化物,待用;
[0071]
步骤e:烧瓶中依次加入10克乙腈、1.0克2,6
‑
二溴
‑4‑
七氟异丙基苯胺、0.5克碘化钾,搅拌加入0.8克式(5)化合物的酰氯化物,将混合物缓慢加热,升温回流反应8h,降温后加入剩余的酰氯化物,再次加热升温回流,点板跟踪至胺反应完全,将反应液倾入饱和碳酸氢钠溶液中,过滤析出的的固体,真空干燥后得1.4克式(1)化合物,收率73%。
[0072][0073]
实施例4
[0074]
如实施例3中的方法,所不同的是,步骤a中的1.8克溴乙腈替换为1.6克氯乙腈,最后得到式(3)化合物的收率为70%。
[0075]
实施例5
[0076]
如实施例3中的方法,所不同的是,步骤a中的1.4克溴乙腈替换为1.1克羟基乙腈,最后得到式(3)化合物的收率为69%。
[0077]
实施例6
[0078]
如实施例3中的方法,所不同的是,步骤a中的溴乙腈替换为甲醛和氢氰酸。具体方式:在圆底烧瓶中依次加入1.5克2
‑
氟
‑3‑
胺基苯甲酸甲酯、将1.5克甲醛,1克氢氰酸盛于恒压漏斗中,控制温度于75℃左右,2小时同时滴加完毕,保温3小时。静置10分钟,分去水相,用水萃取油相两次,再用有机溶剂萃取一次,结晶,得产品,收率71%。
[0079]
实施例7
[0080]
如实施例3中的方法,所不同的是,步骤a中的1.8克溴乙腈替换为1.6克氯乙腈,碘化钾替换为溴化钠,最后式(3)产物的收率为75%。
[0081]
结果如下表所示:
[0082]
表1.实施例4
‑
7式步骤a中式(3)的收率
[0083][0084]
上述实施例4
‑
7的结果表明,2
‑
氟
‑3‑
胺基苯甲酸甲酯与分别与氯乙腈、羟基乙腈、甲醛和氢氰酸、氯乙腈和溴化钠反应时,获得的式(3)化合物的收率都较高,这说明这几种物质均可以与2
‑
氟
‑3‑
胺基苯甲酸甲酯反应,使得反应过程中的氰甲基化步骤提前,而且反应达到了很好的效果。
[0085]
实施例8
[0086]
式(1)化合物的合成:
[0087][0088]
步骤a:在圆底烧瓶中依次加入1.5克2
‑
氟
‑3‑
胺基苯甲酸甲酯、1.2克溴乙腈,0.2克碘化钾、10毫升二氧六烷将混合物缓慢加热,升温至70℃回流反应10h,利用薄层色谱法跟踪,反应完成后冷却至室温,将反应得到的混合物进行蒸馏,依次用石油醚、水洗涤,真空干燥得1.5克式(3)化合物,收率83%;
[0089][0090]
步骤b:在圆底烧瓶中依次加入1克步骤a的产物式(3)化合物、15克二甲基甲酰胺、0.8克苯甲酰氯,将混合物缓慢加热,升温回流反应10h,反应完成后冷却至室温,利用薄层色谱法跟踪,将反应得到的混合物进行蒸馏,依次用异辛烷、水、碳酸钠、水洗涤,40℃真空干燥得1.2克式(4)化合物,收率80%;
[0091][0092]
步骤c:在圆底烧瓶中依次加入1克式(4)化合物后、2克二氧六环、4克水、0.6克碳酸钾,40℃下水解2h后,加入盐酸中和,用乙酸乙酯萃取,有机相用饱和食盐水洗,无水硫酸镁干燥,减压下蒸干溶剂,得1.3克式(5)化合物,收率85%;
[0093][0094]
步骤d:烧瓶中依次加入1克步骤3产物式(5)化合物、10克二氯甲烷,冰浴下滴加20
克草酰氯,常温下搅拌5h,产生的氯化氢气体用水吸收得到副产物盐酸,减压蒸馏,干燥后得到式(5)化合物的酰氯化物,待用;
[0095]
步骤e:烧瓶中依次加入10克乙腈、0.73克2
‑
碘
‑6‑
溴
‑4‑
七氟异丙基苯胺、0.3克碘化钾,搅拌加入0.6克式(5)化合物的酰氯化物,将混合物缓慢加热,升温回流反应8h,降温后加入剩余的酰氯化物,再次加热升温回流,点板跟踪至胺反应完全,将反应液倾入饱和碳酸氢钠溶液中,过滤析出的的固体,真空干燥后得1.3克式(1)化合物,收率78%。
[0096][0097]
实施例9
[0098]
式(1)化合物的合成:
[0099][0100]
步骤a:在圆底烧瓶中依次加入1.5克2
‑
氟
‑3‑
胺基苯甲酸甲酯、1.2克溴乙腈,0.2克碘化钾、10毫升丙酮,将混合物缓慢加热,升温至60℃回流反应10h,利用薄层色谱法跟踪,反应完成后冷却至室温,将反应得到的混合物进行蒸馏,依次用石油醚、水洗涤,真空干燥得1.5克式(3)化合物,收率82%;
[0101][0102]
步骤b:在圆底烧瓶中依次加入1克步骤a的产物式(3)化合物、15克二甲基甲酰胺、0.8克苯甲酰氯,将混合物缓慢加热,升温至70℃回流反应10h,利用薄层色谱法跟踪,反应完成后冷却至室温,将反应得到的混合物进行蒸馏,依次用异辛烷、水、碳酸钠、水洗涤,40℃真空干燥得1.2克式(4)化合物,收率80%;
[0103][0104]
步骤c:在圆底烧瓶中依次加入1克式(4)化合物后、2克二氧六环、4克水、0.6克碳酸钠,30℃下水解2h后,加入盐酸中和,用乙酸乙酯萃取,有机相用饱和食盐水洗,无水硫酸镁干燥,减压下蒸干溶剂,得1.3克式(5)化合物,收率83%;
[0105][0106]
步骤d:烧瓶中依次加入1克步骤3产物式(5)化合物、10克二氯甲烷,冰浴下滴加20克草酰氯,常温下搅拌5h,产生的氯化氢气体用水吸收得到副产物盐酸,减压蒸馏,干燥后
得到式(5)化合物的酰氯化物,待用;
[0107]
步骤e:烧瓶中依次加入10克乙腈、0.78克2
‑
碘
‑6‑
溴
‑4‑
七氟异丙基苯胺、0.3克碘化钾,搅拌加入0.7克式(5)化合物的酰氯化物,将混合物缓慢加热,升温回流反应9h,降温后加入剩余的酰氯化物,再次加热升温回流,点板跟踪至胺反应完全,将反应液倾入饱和碳酸氢钠溶液中,过滤析出的的固体,真空干燥后得1.3克式(1)化合物,收率75%。
[0108][0109]
实施例10
[0110]
式(1)化合物的合成:
[0111][0112]
步骤a:在圆底烧瓶中依次加入1.8克2
‑
氟
‑3‑
胺基苯甲酸甲酯、1.4克溴乙腈,0.4克碘化钾、15毫升二甲基甲酰胺,将混合物缓慢加热,升温回流反应10h,利用薄层色谱法跟踪,反应完成后冷却至室温,将反应混合物进行蒸馏,依次用石油醚、水洗涤,真空干燥得1.7克式(3)化合物,收率81%;
[0113][0114]
步骤b:在圆底烧瓶中依次加入1.3克步骤a的产物式(3)化合物、18克甲苯、1.0克邻氟苯甲酰氯将混合物缓慢加热,升温回流反应10h,利用薄层色谱法跟踪,将反应混合物进行蒸馏,依次用异辛烷、水、碳酸钠、水洗涤,真空干燥得1.5克式(4)化合物,收率82%;
[0115][0116]
步骤c:在圆底烧瓶中依次加入1.3克式(4)化合物后、2.2克二氧六环、6克水、0.8克碳酸钾,50℃下水解2h后,加入盐酸中和,用乙酸乙酯萃取,有机相用饱和食盐水洗,无水硫酸镁干燥,减压下蒸干溶剂,得1.4克式(5)化合物,收率81%;
[0117][0118]
步骤d:烧瓶中依次加入1.2克步骤c的产物式(5)化合物、15克二氯甲烷,冰浴下滴加23克草酰氯,常温下搅拌5h,产生的氯化氢气体用水吸收得到副产物盐酸,减压蒸馏,干燥后得到式(5)化合物的酰氯化物,待用;
[0119]
步骤e:烧瓶中依次加入15克乙腈、0.8克2,6
‑
二溴
‑4‑
七氟异丙基苯胺、0.6克碘化
钾,搅拌加入0.6克式(5)化合物的酰氯化物,将混合物缓慢加热,升温回流反应10h,降温后加入剩余的酰氯化物,再次加热升温回流,点板跟踪至胺反应完全,将反应液倾入饱和碳酸氢钠溶液中,过滤析出的的固体,真空干燥后得1.2克式(1)化合物,收率73%。
[0120][0121]
实施例11
[0122]
式(1)化合物的合成:
[0123][0124]
步骤a:在圆底烧瓶中依次加入1.8克2
‑
氟
‑3‑
胺基苯甲酸甲酯、1.4克溴乙腈,0.5克碘化钾、15毫升乙腈,将混合物缓慢加热,升温回流反应9h,利用薄层色谱法跟踪,反应完成后冷却至室温,将反应混合物进行蒸馏,依次用石油醚、水洗涤,40℃真空干燥得1.7克式(3)化合物,收率81%;
[0125][0126]
步骤b:在圆底烧瓶中依次加入1.5克步骤a的产物式(3)化合物、20克二氧六烷、1.2克邻氟苯甲酰氯,将混合物缓慢加热,升温回流反应8h,利用薄层色谱法跟踪,将反应混合物进行蒸馏,依次用异辛烷、水、碳酸钠、水洗涤,真空干燥得1.4克式(4)化合物,收率80%;
[0127][0128]
步骤c:在圆底烧瓶中依次加入1.5克式(4)化合物后、4克二氧六环、6克水、1.8克碳酸钠,50℃下水解2h后,加入盐酸中和,用乙酸乙酯萃取,有机相用饱和食盐水洗,无水硫酸镁干燥,减压下蒸干溶剂,得1.8克式(5)化合物,收率85%;
[0129][0130]
步骤d:烧瓶中依次加入1.5克步骤c的产物式(5)化合物、20克二氯甲烷,冰浴下滴加23克草酰氯,常温下搅拌5h,产生的氯化氢气体用水吸收得到副产物盐酸,减压蒸馏,干燥后得到式(5)化合物的酰氯化物,待用;
[0131]
步骤e:烧瓶中依次加入15克乙腈、1.0克2,6
‑
二溴
‑4‑
七氟异丙基苯胺、0.8克碘化
钾,搅拌加入0.8克式(5)化合物的酰氯化物,将混合物缓慢加热,升温回流反应8h,降温后加入剩余的酰氯化物,再次加热升温回流,点板跟踪至胺反应完全,将反应液倾入饱和碳酸氢钠溶液中,过滤析出的的固体,真空干燥后得1.4克式(1)化合物,收率76%。
[0132][0133]
实施例12
[0134]
式(1)化合物的合成:
[0135][0136]
步骤a:在圆底烧瓶中依次加入2.2克2
‑
氟
‑3‑
胺基苯甲酸甲酯、2.0克溴乙腈,0.8克碘化钾、20毫升二氧六烷,将混合物缓慢加热,升温回流反应8h,利用薄层色谱法跟踪,反应完成后冷却至室温,将反应混合物进行蒸馏,依次用石油醚、水洗涤,40℃真空干燥得2.3克式(3)化合物,收率83%;
[0137][0138]
步骤b:在圆底烧瓶中依次加入1.8克步骤a的产物式(3)化合物、25克二氯甲烷、1.5克邻氟苯甲酰氯,将混合物缓慢加热,升温回流反应10h,利用薄层色谱法跟踪,反应完成后冷却至室温,将反应得到的混合物进行蒸馏,收集固体,依次用异辛烷、水、碳酸钠、水洗涤,真空干燥得2.0克式(4)化合物,收率82%;
[0139][0140]
步骤c:在圆底烧瓶中依次加入1.8克式(4)化合物后、2克二氧六环、4克水、0.6克碳酸钠,45℃下水解2h后,加入盐酸中和,用乙酸乙酯萃取,有机相用饱和食盐水洗,无水硫酸镁干燥,减压下蒸干溶剂,得1.3克式(5)化合物,收率84%;
[0141][0142]
步骤d:烧瓶中依次加入1.8克步骤c的产物式(5)化合物、20克二氯甲烷,冰浴下滴加28克草酰氯,常温下搅拌5h,产生的氯化氢气体用水吸收得到副产物盐酸,减压蒸馏,干燥后得到式(5)化合物的酰氯化物,待用;
[0143]
步骤e:烧瓶中依次加入20克乙腈、1.2克2,6
‑
二溴
‑4‑
七氟异丙基苯胺、0.8克碘化
钾,搅拌加入0.8克式(5)化合物的酰氯化物,将混合物缓慢加热,升温回流反应10h,降温后加入剩余的酰氯化物,再次加热升温回流,点板跟踪至胺反应完全,将反应液倾入饱和碳酸氢钠溶液中,过滤析出的的固体,真空干燥后得1.5克式(1)化合物,收率78%。
[0144][0145]
实施例13
[0146]
式(1)化合物的合成:
[0147][0148]
步骤a:在圆底烧瓶中依次加入2.5克2
‑
氟
‑3‑
胺基苯甲酸甲酯、2克溴乙腈,0.4克碘化钾、25毫升二氯甲烷,将混合物缓慢加热,升温回流反应10h,利用薄层色谱法跟踪,反应完成后冷却至室温,将反应得到的混合物进行蒸馏,依次用石油醚、水洗涤,真空干燥得2.6克式(3)化合物,收率83%;
[0149][0150]
步骤b:在圆底烧瓶中依次加入2克步骤a的产物式(3)化合物、30克丙酮、1.6克苯甲酰氯,将混合物缓慢加热,升温回流反应8h,利用薄层色谱法跟踪,反应完成后冷却至室温,将反应得到的混合物进行蒸馏,依次用异辛烷、水、碳酸钠、水洗涤,40℃真空干燥得2.3克式(4)化合物,收率82%;
[0151][0152]
步骤c:在圆底烧瓶中依次加入2克式(4)化合物后、4克二氧六环、8克水、1.2克碳酸钠,35℃下水解2h后,加入盐酸中和,用乙酸乙酯萃取,有机相用饱和食盐水洗,无水硫酸镁干燥,减压下蒸干溶剂,得1.8克式(5)化合物,收率85%;
[0153][0154]
步骤d:烧瓶中依次加入1.5克步骤3产物式(5)化合物、10克二氯甲烷,冰浴下滴加30克草酰氯,常温下搅拌5h,产生的氯化氢气体用水吸收得到副产物盐酸,减压蒸馏,干燥后得到式(5)化合物的酰氯化物,待用;
[0155]
步骤e:烧瓶中依次加入20克乙腈、1.46克2
‑
碘
‑6‑
溴
‑4‑
七氟异丙基苯胺、0.6克碘
化钾,搅拌加入1.2克式(5)化合物的酰氯化物,将混合物缓慢加热,升温回流反应8h,降温后加入剩余的酰氯化物,再次加热升温回流,点板跟踪至胺反应完全,将反应液倾入饱和碳酸氢钠溶液中,过滤析出的的固体,真空干燥后得1.6克式(1)化合物,收率74%。
[0156][0157]
上述实施例仅用于解释说明本发明的发明构思,而非对本发明权利保护的限定,凡是根据本发明的技术和方法实质对以上实施例所做的任何简单修改、等同变化与修饰,均仍属于本发明的技术和方法方案的范围内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1