一种α-珠蛋白过表达载体及其应用的制作方法
一种
α-珠蛋白过表达载体及其应用
技术领域
1.本发明属于生物医药领域,具体涉及一种α-珠蛋白过表达载体及其应用。
背景技术:
2.正常血红蛋白是由两条α-珠蛋白链和两条β-珠蛋白链组成的四聚体。有两个功能性α-血红蛋白基因,分别命名为hba1和hba2。α地中海贫血病(α地贫)是由于α珠蛋白基因缺失或功能障碍使α-珠蛋白链的合成减少或不能合成,造成α链和非α链合成不均衡所引起的一种常染色体隐性遗传病。α-珠蛋白基因簇上常见的缺失有αα/
‑‑
sea
和-α
4.2
/-α
4.2
等,其发生机理是由于α珠蛋白基因一条或两条染色体发生同源性和非同源性重组而缺失,该基因缺失可使α珠蛋白基因表达水平下调而降低α珠蛋白链产生。
3.据报道,α地中海贫血是世界上最常见的单基因遗传病之一,在地中海、东南亚、非洲、中东和印度次大陆尤其常见,在我国长江以南地区发病率较高。根据世界卫生组织(who)估计,全球20%的人口可能有一个或多个α-珠蛋白基因缺失。中国南方省份及东南亚地区,最常见的缺失类型为
‑‑
sea(东南亚缺失型)、-α
4.2
(左缺失)和-α
3.7
(右缺失)三种。在过去几十年中,由于人口结构的变化,北欧和北美的α地中海贫血发病率有所上升。目前,国内外对地中海贫血有效的治疗手段包括异源性造血细胞移植、规范性长期输血和去铁治疗,但是有排斥风险,并发症和其它毒性效应,因此基因治疗方案正在被评估作为一种新的方案。
4.近年来,由于基因工程技术的突飞猛进,crispr/cas技术俨然已经成为科学界的热点之一。研究表明,crispr/cas系统相较于其他基因编辑工具,在干细胞中有更高的切割效率,可用于构建疾病模型、筛选药物,制备治疗性干细胞等,为疾病治疗带来了新希望,但可能存在的脱靶风险不容忽视。病毒载体具有高感染率、低细胞毒性的特点,目前仍然是很多科学研究和临床试验的较优方案。慢病毒载体衍生自hiv-1慢病毒,包含多个用于增加转导效率的辅助元件、病毒包装和/或增加治疗基因表达的元件,以及经过修饰的5'ltr和/或3'ltr,这样的载体整合入目的细胞后,即使存在所有病毒蛋白也不能转录出rna,使病毒变成复制缺陷型来增加慢病毒系统的安全性。慢病毒载体具有能感染非分裂期细胞、容纳外源性目的基因片段大、稳定性强、感染效率高等特点。
5.第三代慢病毒系统,将gag、pol基因与rev或env基因分别构建在不同的质粒上,并且在病毒基因组的3'ltr引入缺失以产生自失活(sin)慢病毒载体,破坏ltr的启动子/增强子活性,进一步提高了安全性,并降低致癌风险。目前有2/3的基因治疗临床试验是运用病毒载体来引入基因到靶细胞目前使用较多的是来源于hiv的慢病毒载体。通过慢病毒载体进行基因治疗为血红蛋白病带来了新的选择,其临床研究已经开展,结果令人鼓舞,但远期疗效和安全性仍待证明。体外基因治疗,通过载体转移和染色体整合的基因添加一个正常的珠蛋白基因连同合适的顺式连接的调节元件到造血干细胞(hscs)仍然是选择的方法。慢病毒载体基因治疗需要非常高效的造血干细胞感染效率和长期稳定的α-珠蛋白表达才具有临床意义。
6.但目前现有技术中对珠蛋白过表达载体的研究几乎针对β-珠蛋白基因,因此急需一种表达率适于临床应用的α-珠蛋白过表达载体。
技术实现要素:
7.本发明要解决的技术问题是为克服现有技术中缺乏表达α-珠蛋白基因的过表达载体的缺陷,提供一种表达率适中的α-珠蛋白过表达载体及其应用。
8.在人体中,α-类珠蛋白基因的调控序列包含多种顺式和反式作用因子的结合位点,它们间的协同作用保证了α类珠蛋白基因表达的组织和时序特异性。而对于异源的α-珠蛋白基因的表达调控,完全复制天然的过程需大量合成多种功能区序列,过程十分复杂且从成本上讲也难以实现;而对于目前已经取得一定研究进展的异源hbb基因的表达,均是基于天然hbb基因本身的调控元件进行表达调控,而对于异源α-珠蛋白基因的表达调控元件的选择,现有技术却没有这方面的研究,因此,异源α-珠蛋白基因的表达目前仍为一个技术难题。
9.为解决上述技术问题,本发明提供的技术方案之一为:一种α-珠蛋白过表达载体,其依次包含:(1)基因座控制区、α-珠蛋白启动子、hba2基因和hba2基因3’sequence片段,所述基因座控制区为hs40;
10.或(2)基因座控制区hs4、hs3和hs2、β-珠蛋白启动子、hba2基因和hbb基因3’sequence片段。
11.所述依次包含指的是从5’端到3’端的依次包含。
12.较佳地,所述的α-珠蛋白过表达载体依次包含顺式作用元件、hba2基因和hba2基因3’sequence片段,所述顺式作用元件由基因座控制区hs40和α-珠蛋白启动子构成。
13.本发明所述α-珠蛋白启动子较佳地为hba2启动子;更佳地,其序列包含如seq id no:2所示的序列,或包含与如seq id no:2所示序列具有80%以上序列同一性的序列,例如,其序列如seq id no:2所示。
14.本发明所述基因座控制区hs40可为本领域常规,其序列优选包含如seq id no:1所示的序列,或包含与如seq id no:1所示序列具有80%以上序列同一性的序列,例如,其序列如seq id no:1所示。
15.本发明所述hba2基因3’sequence片段可为本领域常规,其序列优选包含如seq id no:4所示的序列,或包含与如seq id no:4所示序列具有80%以上序列同一性的序列,例如,其序列如seq id no:4所示。
16.本发明中所述β-珠蛋白启动子较佳地为hbb启动子;更佳地,其序列包含如seq id no:8所示的序列,或包含与如seq id no:8所示序列具有80%以上序列同一性的序列,例如,其序列如seq id no:8所示。
17.在本发明所述基因座控制区hs4可为本领域常规,其序列优选包含如seq id no:5所示的序列,或包含与如seq id no:5所示序列具有80%以上序列同一性的序列,例如,其序列如seq id no:5所示。
18.本发明所述基因座控制区hs3可为本领域常规,其序列优选包含如seq id no:6所示的序列,或包含与如seq id no:6所示序列具有80%以上序列同一性的序列,例如,其序列如seq id no:6所示。
19.本发明所述基因座控制区hs2可为本领域常规,其序列优选包含如seq id no:7所示的序列,或包含与如seq id no:7所示序列具有80%以上序列同一性的序列,例如,其序列如seq id no:7所示。
20.本发明所述hbb基因3’sequence片段可为本领域常规,其序列优选包含如seq id no:9所示的序列,或包含与如seq id no:9所示序列具有80%以上序列同一性的序列,例如,其序列如seq id no:9所示。
21.本发明所述hba2基因的序列可为本领域常规;其序列优选包含如seq id no:3所示的序列,或包含与如seq id no:3所示序列具有80%以上序列同一性的序列,例如,其序列如seq id no:3所示。
22.本发明所述的α-珠蛋白过表达载体的质粒载体较佳地为lenti载体,所述lenti载体的序列优选包含如seq id no:10所示的序列,或包含与如seq id no:10所示序列具有80%以上序列同一性的序列,例如,其序列如seq id no:10所示。
23.以上所述80%以上序列同一性包含81%、82%、83%、84%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%以上序列同一性。
24.本发明提供的技术方案之二为:一种包含上述α-珠蛋白过表达载体的转化体。
25.所述转化体的宿主细胞较佳地为红系细胞。
26.所述红系细胞优选为hudep2或cd34
+
造血干细胞。
27.本发明提供的技术方案之三为:一种包含上述过表达载体的慢病毒载体系统。
28.所述慢病毒载体系统较佳地还包含pspax2和pcag-vsvg质粒。
29.本发明提供的技术方案之四为:一种上述过表达载体在制备治疗地中海贫血的制剂中的应用。
30.所述地中海贫血较佳地为α-地中海贫血。
31.本发明提供的技术方案之五为:一种如上技术方案所定义的hs40、α-珠蛋白启动子、hba2基因3’sequence片段、hs4、hs3、hs2、β-珠蛋白启动子或hbb基因3’sequence片段在构建hba2过表达载体中的应用。
32.所述载体较佳地为慢病毒载体。
33.在符合本领域常识的基础上,上述各优选条件,可任意组合,即得本发明各较佳实例。
34.本发明所用试剂和原料均市售可得。
35.本发明的积极进步效果在于:
36.本发明所构建的α-珠蛋白过表达载体能够高效转导目的基因,并且能够使目的基因长期稳定的表达,具有高感染效率及表达稳定性;本发明用慢病毒载体介导的基因治疗能够显著提升缺失型α-地中海贫血患者中α-珠蛋白基因的表达,使α-珠蛋白基因的表达量达到适中状态,既不过高也不过低,为成功治疗所有的α地贫患者提供了希望,具有重要的临床意义。经该载体慢病毒感染过的红系细胞系和造血干细胞诱导红系分化后,都能过表达α珠蛋白,因此该载体结合造血干细胞移植有望治疗各种突变类型的α地中海贫血患者。
附图说明
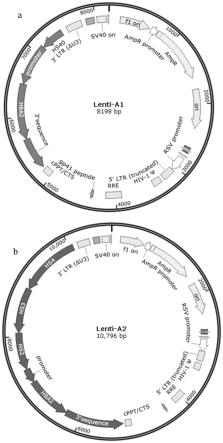
37.图1为lenti-a1(a)和lenti-a2(b)慢病毒载体示意图。
r,suda n,sudo k,miharada k,hiroyama t,et al.(2013)establishment of immortalized human erythroid progenitor cell lines able to produce enucleated red blood cells.plos one 8(3):e59890.doi:10.1371/journal.pone.0059890)和cd34
+
细胞(来源于正常人骨髓)中红系分化18天后,可以提升α-珠蛋白的表达水平(图2和图3)。
51.实施例3.构建缺失型α-地贫cd34
+
细胞模型及α-珠蛋白慢病毒载体在该模型中的应用
52.正常人有4个α珠蛋白基因(αα/αα,2个α2和2个α1);缺失突变型α地贫分为以下几种类型:缺失1个α珠蛋白基因(-α/αα)为静止型;缺失2个α珠蛋白基因(
‑‑
/αα或-α/-α)为标准型;缺失3个α珠蛋白基因(
‑‑
/-α)称为血红蛋白h病(hbh);4个α珠蛋白基因均缺失(
‑‑
/
‑‑
)的即为hb bart's胎儿水肿综合征。引起α珠蛋白基因缺失的原因主要是dna大片段缺失,缺失范围从2.7kb到整个基因簇不等。实验通过构建-α
4.2
缺失α-地中海贫血疾病模型,针对hba2基因外显子区域设计了sgrna,通过同时诱发此区域的两端发生双链断裂,达到删除dna片段的目的。我们将该sgrna与cas9蛋白形成的rnp通过电转导入人cd34+造血干细胞中,构建纯合型和杂合型细胞株,进而检验α-珠蛋白与β-珠蛋白的表达水平及它们之间的比例。体外红系分化18天后rt-qpcr检测α-珠蛋白表达水平,结果表明,α-珠蛋白表达水平显著下降,证明疾病模型构建成功(图4)。疾病模型构建成功后,感染lenti-a1和lenti-a2慢病毒载体,体外红系分化18天后检测α-珠蛋白表达水平。结果表明,两种慢病毒载体均可以显著升高α-珠蛋白表达水平(图4),这说明这两种载体都有望成为α地贫疾病的基因治疗载体。
53.sgrna序列:gatggagagcgtatgttaac。(seq id no:11)
54.实施例4.α-珠蛋白过表达慢病毒载体在hbh病地贫患者cd34
+
中的应用
55.将两种α-珠蛋白过表达载体包装成慢病毒后分别感染了hbh病(输血依赖性α地贫,基因型为
‑‑
sea
/αα
cs
)地贫患者的cd34
+
造血干细胞进行验证。所述hbh病患者cd34
+
造血干细胞通过以下方法获得:取hbh病地贫患者的外周血10ml,经过ficoll分离单个核细胞后,以cd34磁珠获取cd34
+
细胞,重悬在培养基中。结果显示(图5),感染病毒的细胞内表达的α-珠蛋白水平比未感染病毒的显著升高。从上述已经获得的研究结果表明,我们构建的α-珠蛋白过表达载体,包装成慢病毒后感染红系细胞系或cd34
+
造血干细胞后,在其诱导分化来的红系细胞中可高效的表达α-珠蛋白。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1