一种耐盐蛋白、编码其的基因及应用的制作方法
本发明涉及一种耐盐蛋白。
背景技术:
西伯利亚白刺(nitrariasibirica)隶属蒺藜科白刺属落叶具刺灌木,是典型的稀盐型盐生植物,可在重盐碱地正常生长,对恶劣环境有非常强的适应能力,是防风固沙、保持水土及重盐碱地改良的先锋型植物,不但具有极高的生态应用价值,同时也是研究植物耐盐分子机制和挖掘耐盐抗逆基因资源的重要材料。
技术实现要素:
本发明之一提供了一种蛋白,其氨基酸序列如seqidno.4所示。
本发明之二提供了编码如本发明之一所述的蛋白的基因。
在一个具体实施方式中,所述基因的核苷酸序列如seqidno.3所示。
本发明之三提供了根据本发明之一所述的蛋白或本发明之二所述的基因在耐盐中的应用。
本发明的有益效果:
本发明首次发现了西伯利亚白刺中一种耐盐基因,可以将其用于植物的耐盐改良。
附图说明
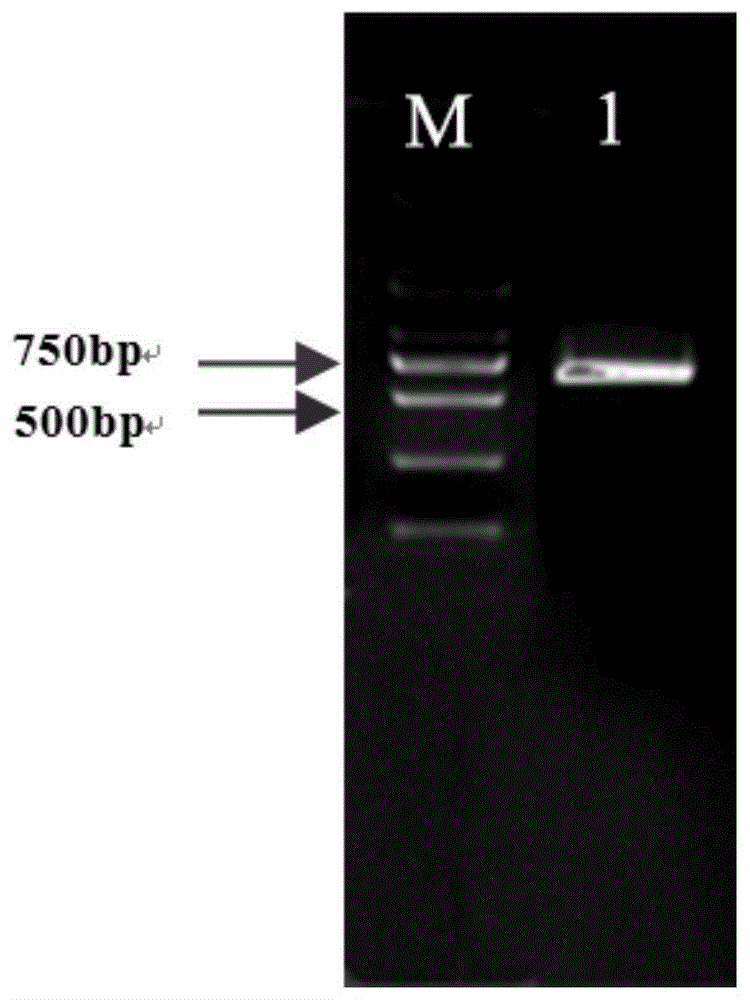
图1显示了rt-pcr技术克隆得到的核苷酸序列如seqidno.3所示的耐盐基因全长电泳图,图中m为dl2000dnamarker,1为耐盐基因。
图2显示了200mmnacl处理后根中耐盐基因的rt-qpcr检测结果。
图3显示了200mmnacl处理后茎中耐盐基因的rt-qpcr检测结果。
图4显示了200mmnacl处理后叶中耐盐基因的rt-qpcr检测结果。
图5显示了400mmnacl处理后根中耐盐基因的rt-qpcr检测结果。
图6显示了400mmnacl处理后茎中耐盐基因的rt-qpcr检测结果。
图7显示了400mmnacl处理后叶中耐盐基因的rt-qpcr检测结果。
图8为转基因烟草的pcr鉴定图。
图9显示了五株转基因烟草中耐盐基因的rt-qpcr检测结果。
图10显示了超氧化物歧化酶活性在nacl处理1d、5d、10d的变化。
图11显示了过氧化氢含量在nacl处理1d、5d、10d的变化。
图12显示了脯氨酸含量在nacl处理1d、5d、10d的变化。
图13显示了丙二醛含量在nacl处理1d、5d、10d的变化。
具体实施方式
以下通过优选的实施案例的形式对本发明的上述内容作进一步的详细说明,但其不构成对本发明的限制。
如无特别说明,本发明的实施例中的试剂均可通过商业途径购买。
peasy-blunt质粒载体和大肠trans1-1感受态细胞购自全式金公司。
实施例1
西伯利亚白刺耐盐基因cdna序列的克隆。
采用擎科生物技术有限公司rna提取试剂盒从nacl处理后的西伯利亚白刺全株中提取总rna。
利用takara公司反转录试剂盒对所提取的总rna进行反转录合成得到cdna,然后以合成的cdna为模板,以引物ns-f(seqidno.1)和ns-r(seqidno.2)为引物进行pcr,得到pcr产物。其中,pcr程序为:(1)94℃,预变性5分钟。(2)pcr扩增,33个循环:94℃,变性45秒;60℃退火45秒;72℃,延伸45秒;(2)72℃,延伸10分钟。利用琼脂糖凝胶电泳对pcr产物进行分离,结果见图1,用omegbio-tek试剂盒对pcr产物中的目的片断进行回收;回收产物连接到peasy-blunt载体上并转化至大肠杆菌trans1-1感受态细胞中,挑选转化菌落进行pcr鉴定,然后将扩增出符合预先大小的pcr片段(大小与图1相同)的转化子送至擎科生物技术有限公司测序,得到的测序结果与转录组中的测序片段完全相同,说明克隆所得的基因即为目的基因,将测序正确的质粒命名为peasy-blunt-ns5,测序正确的大肠杆菌菌株命名为peasy-blunt-ns5/trans1-1。其中,所克隆基因的核苷酸序列如seqidno.3所示,其编码的氨基酸序列如seqidno.4所示。
实施例2
西伯利亚白刺耐盐基因在逆境中的表达特性
对于西伯利亚白刺一年生组培苗进行200mm及400mm浓度的nacl胁迫,并对每个浓度下培养的组培苗在0h、6h、12h、24h、48h及72h后对根、茎及叶片进行取样,之后迅速放入液氮中速冻,在液氮中研磨后采用与实施例1相同的操作分别提取rna以及反转录合成cdna。以nsrt-f(seqidno.5)和nsrt-r(seqidno.6)为引物,以每个样品的反转录合成的cdna分别为模板进行rt-qpcr(方法参考transstarttopgreenqpcrsupermix说明书,货号:aq131-04,购自全式金生物技术有限公司),并以西伯利亚白刺的肌动蛋白(actin)为内参,内参引物为actin-f(seqidno.7)和actin-r(seqidno.8)。rt-qpcr结果如图2至7所示,相较于200mmnacl浓度,耐盐基因的表达水平对400mmnacl浓度更加敏感,并在处理6h后该基因的表达量达到最高。
实施例3
1.西伯利亚白刺耐盐基因表达载体的构建
以引物nsxbai-f(seqidno.9,添加xbai酶切位点)和nssepi-r(seqidno.10,添加sepi酶切位点)为引物,以peasy-blunt-ns5质粒为模板进行pcr,获得添加了酶切位点的目的片段,对pbi121载体进行xbai和sepi双酶切后,利用sosoo同源重组酶(sosoo同源重组酶试剂盒,购自擎科生物技术有限公司,货号:tsv-s2)将回收后的酶切载体与加了酶切位点目的片段进行无缝融合连接。将连接产物转入大肠杆菌trans1-1,挑选转化菌落进行pcr鉴定,然后将扩增出符合预先大小的pcr片段的转化子送至擎科生物技术有限公司测序,将测序正确的质粒命名为pbi121-ns5,测序正确的大肠菌菌株命名为pbi121-ns5/trans1-1。
2.根癌农杆菌感受态制备
(1)将根癌农杆菌gv3101培养液加入到含50mg/l利福平的固态lb培养基上面并进行划线,28℃连续培养2d;
(2)从固体lb细菌培养基挑选提取一个单克隆菌落接种于液体lb(50mg/l利福平)中进行扩繁,摇床28℃,200rpm持续培养18-24h,直至od600=0.4;
(3)然后将5μlod600=0.4的菌液涂布到含有50mg/l卡那霉素、25mg/l利福平和50mg/l庆大霉素三种抗性的lb液体培养基中,在28℃、200rpm摇床室中培养8小时;
(4)在超净化工作台里面移取步骤(3)培养的菌液,均匀分装至已经消毒灭菌的1.5ml离心管中,冰水浸泡30min后,4℃、5000rpm离心5min,倒掉菌液上清;
(5)用0.15mnacl重悬;
(6)5000rpm离心5min,于20ml无菌水重悬,制得根癌农杆菌gv3101的感受态。
3.利用冻融法将pbi121-ns5质粒转化根癌农杆菌
(1)将10μlpbi121-ns5质粒加入至100μl的根癌农杆菌gv3101的感受态中,随后进行35min的冰浴;
(2)液氮冷冻1min;
(3)37℃水浴3min;
(4)加入500μl液体lb培养基,28℃,200rpm摇床培养2h,得到转化菌液;
(5)取200μl的转化菌液均匀地涂布在含有50mg/l卡那霉素、25mg/l利福平和50mg/l庆大霉素的培养基上,然后放到28℃恒温箱中,倒置培养2d,然后以nsxbai-f(seqidno.9)和nssepi-r(seqidno.10)为引物进行菌落pcr鉴定,并进行测序验证,将得到的阳性重组菌株命名为pbi121-ns5/gv3101。
实施例4
根癌农杆菌介导耐盐基因转化烟草方法
(1)农杆菌液活化制备:取pbi121-ns5/gv3101根癌农杆菌,在含有50mg/l卡那霉素、25mg/l利福平和50mg/l庆大霉素的固体lb的培养基中进行划线倒置在28℃下活化培养2d;挑取单菌落于含50mg/l卡那霉素、25mg/l利福平和50mg/l庆大霉素的lb液体培养基在28℃、200rpm下培养8小时;取2ml的根癌农杆菌培养液,加入至50ml相同的液体培养基中,继续培养直至根癌农杆菌od600达到0.4,3500g低温离心10min后,弃上清,将沉淀用等体积的无菌水重悬,得到侵染菌液。
(2)侵染:在无菌条件下,从一月龄烟草组培苗中选取第二片和第三片叶,剪成大约1×1cm的小方块放至侵染菌液中进行10min的侵染,轻轻摇晃使其充分侵染。完成后取出叶片,在共培培养基上共培养48h,得到共培养烟草叶片。
(3)筛选分化:将共培养烟草叶片放入含250mg/l头孢的去离子水中轻晃5min,捞入无菌水水中清洗4至5次,直至水清澈透明。用灭菌滤纸吸干大部分水分,放在含有100mg/l卡那霉素、100mg/l利福平和100mg/l庆大霉素的无菌分化培养基(蔗糖:20g/l、琼脂:5.5g/l、6-ba:0.03mg/l,ph:6.0)上进行无菌培养。每9-10天更换一次培养基,直至共培养烟草叶片分化出绿芽。(4)分化生根培养:在绿芽生长到2cm左右时,将其从培养基中切下并转移至含有50mg/l卡那霉素、50mg/l利福平和50mg/l庆大霉素无菌生根培养基(蔗糖:20g/l、琼脂:5.5g/l、iba:0.25mg/l,ph:6.0)上进行培养,直至生根。
(5)转基因烟草阳性株的筛选:将经转基因操作生长的t0代烟草和野生生长的烟草在组培瓶中种植生长一个月时分别提取基因组总dna,其中以野生烟草的基因组总dna为模板进行pcr以作为阴性对照,以pbi121-ns5质粒为模板进行pcr以作为阳性对照,以nt-f(seqidno.11)和nt-r(seqidno.12)为引物进行pcr检测(由于使用的通用引物设计在pbi121多克隆位点两侧的载体序列,且pbi121-ns5两端添加了酶切位点及保护碱基,因而进行阳性鉴定的片段长于基因全长及pbi121-ns5)。pcr结果如图8所示,wt为野生型烟草(阴性对照),1为pbi121-ns5质粒(阳性对照),2-6为转基因烟草。结果显示,从五株t0代转基因烟草株中均可以扩增出目的条带,而阴性对照无目的片段,测序结果证明五株转基因烟草株均已成功地转入耐盐基因,将五株t0代转基因烟草株编号为oe-1至5。
以nsrt-f(seqidno.5)和nsrt-r(seqidno.6)为引物,肌动蛋白(actin)为内参,对五株转基因烟草株生长一个月的样本进行rt-qpcr分析,获得耐盐基因在t0代转基因植株中的表达情况,结果如图9所示,选取表达最高的oe-3与oe-4结籽后播种,获得t1子代,在对t1子代进行阳性筛选,并将两株植株的子代分别命名为n-oe-3和n-oe-4以用于后续实验。
实施例5
转基因烟草株系在盐胁迫下的生长情况
以野生型为阴性对照,选取培养的株系oe-3和oe-4中长势一致的转基因t1代植株,放置于室温为23±1℃的培养室培养,土壤成分为蛭石:珍珠岩:东北黑土=1:3:5,培养光周期:16h光照/8h黑暗;在组培苗长至高10-15cm时,用175mm的氯化钠处理,在处理之后观察植株的长势,观察结果显示,在经过175mm的氯化钠处理的10天时,野生型对照植株的叶片出现明显卷曲,生长受到阻碍;而转基因烟草植株的叶片肥大,几乎不受影响。
同时,在用175mm的氯化钠处理之后的第1天、第5天和第10天剪去叶片以用于超氧化物歧化酶(sod)活性、脯氨酸(pro)含量、过氧化氢(h2o2)含量及丙二醛(mda)含量的测定(参见试剂盒,南京建成生物工程研究所)。吸光值利用可见分光光度计(shimadzucorporation型号:uv-1800)测定,并根据试剂盒提供的公式计算获得超氧化物歧化酶的酶活,脯氨酸、过氧化氢及丙二醛的含量,每个指标进行三次生物学重复,显著性利用spss进行单因素方差分析获得,所有分析均为p<0.05水平上差异显著。结果见图10至13。
从超氧化物歧化酶活性、脯氨酸、过氧化氢及丙二醛四个指标的结果可以看出,相比于野生型烟草,转基因烟草在盐胁迫下能够保持较高的sod活性及脯氨酸含量且在处理初期显著高于野生型(阴性对照),而过氧化氢及丙二醛含量显著低于野生型。具体地,转基因烟草在盐胁迫下持续保持较高sod活性,故认为有较高的耐盐性,但由于sod作业时会产生的过氧化氢并可穿透大部分细胞膜,造成氧化胁迫,因此对盐处理后第1天、第5天和第10天的各植株中h2o2的含量进行了测定,结果表明盐处理后过氧化氢的含量随时间变化呈现先增加后减少的趋势,且处理10d后转基因植株过氧化氢含量显著低于野生型,可见转入耐盐基因的烟草对过氧化氢的调节能力要高于野生型;在盐胁迫下,转基因植株中的脯氨酸累积在第1天和第5天显著高于野生型植株,在第10天,耐盐基因表达量高的转基因植株n-oe-3中的脯氨酸累积仍然显著高于野生型植株,不过耐盐基因表达量低的转基因植株n-oe-4中的脯氨酸累积与野生型植株相当;在盐胁迫下,转基因烟草中丙二醛的含量持续下降,而野生型植株中丙二醛含量先降低后保持不变。
综合以上分析,说明在转入了本发明的耐盐基于后的转基因植株耐盐性显著增强。
序列表
<110>中国林业科学研究院
中国林业科学研究院黄河三角洲综合试验中心
<120>一种耐盐蛋白、编码其的基因及应用
<130>lha2160329
<160>12
<170>siposequencelisting1.0
<210>1
<211>24
<212>dna
<213>人工序列(artificialsequence)
<400>1
atgaacattcagctaacacgttgt24
<210>2
<211>22
<212>dna
<213>人工序列(artificialsequence)
<400>2
ctagactcgagcttgggaatca22
<210>3
<211>681
<212>dna
<213>西伯利亚白刺(nitrariasibirica)
<400>3
atgaacattcagctaacacgttgttgtactgaagtcatggatgctcttacgggctgcttg60
tgcatgaagaattacagacaaagacgtggctatgagaagccttcgcgccttgcttctgag120
acgccatttactgttaatgaggtagaagcattgtatgatttgttcaagaagatcagtggc180
tctatatgtgatgatggtcttattaacaaggaagaattccagcttgcactatttaggaac240
agcaagaagaagaatctttttgcggacagggtatttgacctgtttgacgtcaagcacaat300
ggggtaattgaattcggagaatttgttcgggcactaagtgtcttccatcctaatactccc360
gtggaagacaaaattgccttcgcatttagattgtacgatcttcggcagactggcttcatt420
gagcataatgaggtgaaggagatggtggtggctctattgtgtgaatcagaactagaactt480
tctgatgatgtcatcgaatcaattgtagacaagaccatgtcggaggcagatttaactgga540
gatagaaaaattgatatggaagaatggaagcagtatgtggcacagaatccaactatcatt600
aaaaacatgacacttccatatctaaaggaaataaccatggcatttccaagcttcttactt660
gattcccaagctcgagtctag681
<210>4
<211>226
<212>prt
<213>西伯利亚白刺(nitrariasibirica)
<400>4
metasnileglnleuthrargcyscysthrgluvalmetaspalaleu
151015
thrglycysleucysmetlysasntyrargglnargargglytyrglu
202530
lysproserargleualasergluthrprophethrvalasngluval
354045
glualaleutyraspleuphelyslysileserglyserilecysasp
505560
aspglyleuileasnlysgluglupheglnleualaleupheargasn
65707580
serlyslyslysasnleuphealaaspargvalpheaspleupheasp
859095
vallyshisasnglyvalileglupheglygluphevalargalaleu
100105110
servalphehisproasnthrprovalgluasplysilealapheala
115120125
pheargleutyraspleuargglnthrglypheilegluhisasnglu
130135140
vallysglumetvalvalalaleuleucysglusergluleugluleu
145150155160
seraspaspvalilegluserilevalasplysthrmetsergluala
165170175
aspleuthrglyasparglysileaspmetgluglutrplysglntyr
180185190
valalaglnasnprothrileilelysasnmetthrleuprotyrleu
195200205
lysgluilethrmetalapheproserpheleuleuaspserglnala
210215220
argval
225
<210>5
<211>22
<212>dna
<213>人工序列(artificialsequence)
<400>5
atcctaccgttcttgctgctgt22
<210>6
<211>21
<212>dna
<213>人工序列(artificialsequence)
<400>6
ttcttccttgtgaatgagccc21
<210>7
<211>22
<212>dna
<213>人工序列(artificialsequence)
<400>7
ggaatccacgagaccacctaca22
<210>8
<211>22
<212>dna
<213>人工序列(artificialsequence)
<400>8
gattgatcctccgatccagaca22
<210>9
<211>49
<212>dna
<213>人工序列(artificialsequence)
<400>9
tggagagaacacgggggactctagaatgaacattcagctaacacgttgt49
<210>10
<211>44
<212>dna
<213>人工序列(artificialsequence)
<400>10
cctcgcccttgctcaccatactagtgactcgagcttgggaatca44
<210>11
<211>23
<212>dna
<213>人工序列(artificialsequence)
<400>11
ggccatcgttgaagatgcctctg23
<210>12
<211>20
<212>dna
<213>人工序列(artificialsequence)
<400>12
gaacttcagggtcagcttgc20
- 还没有人留言评论。精彩留言会获得点赞!