基于表型与SSR分子标记联合构建普通菜豆的指纹图谱
基于表型与ssr分子标记联合构建普通菜豆的指纹图谱
技术领域
1.本发明涉及植物品种鉴别领域,特别是涉及一种基于表型与ssr分子标记联合构建普通菜豆的指纹图谱。
背景技术:
2.普通菜豆属豆科普通菜豆属作物,普通菜豆适宜在温带和热带高海拔地区种植,比较耐冷喜光。普通菜豆属短日照植物,但多数品种对日照长短的要求不严格,栽培季节主要受温度的制约。中国的西北和东北地区在春夏栽培;直播或育苗移栽均可。同时,普通菜豆营养丰富,含有丰富的蛋白质、脂肪、碳水化合物、膳食纤维、维生素a、萝卜素、硫胺素、核黄素、尼克酸、维生素c、维生素e、钙、磷、钠等成分。多年来,品种鉴定是以形态学标记为依据的。这种方法虽然简单经济,但周期长,花费大,受季节限制,而且很多性状的表现受栽培措施及环境因子影响,从而制约了鉴定的准确性。dna分子标记技术则具有高效、准确、不受环境条件影响、实验操作简单等优点,已广泛应用于植物品种真实性鉴定及纯度检测研究。ssr标记是近年来发展起来的建立在pcr基础上的第二代分子标记。由于ssr分子标记具有数量丰富、多态性高、遗传共显性、谱带扩增稳定、精度高、检测时间短、技术成熟等特点,已应用于作物遗传学研究。目前,菜豆中也有利用分子标记技术进行研究的,但是没有具体只针对普通菜豆品种开发的ssr分子标记以及利用ssr分子标记构建的技术体系。
技术实现要素:
3.本发明的目的是提供一种基于表型与ssr分子标记联合构建普通菜豆的指纹图谱,以解决上述现有技术存在的问题,能够准确鉴别不同品种的普通菜豆。
4.为实现上述目的,本发明提供了如下方案:
5.本发明提供一种用于鉴别菜豆的分子标记组合,所述分子标记包括pvssr
‑
01
‑
1、pvssr
‑
01
‑
2、pvssr
‑
02
‑
1、pvssr
‑
02
‑
2、pvssr
‑
03
‑
1、pvssr
‑
03
‑
2、pvssr
‑
04
‑
1、pvssr
‑
04
‑
2、pvssr
‑
05
‑
1、pvssr
‑
05
‑
2、pvssr
‑
06
‑
1、pvssr
‑
06
‑
2、pvssr
‑
07
‑
1、pvssr
‑
07
‑
2、pvssr
‑
08
‑
1、pvssr
‑
08
‑
2、pvssr
‑
09
‑
1、pvssr
‑
09
‑
2、pvssr
‑
10
‑
1、pvssr
‑
10
‑
2、pvssr
‑
11
‑
1、pvssr
‑
11
‑
2,所述分子标记分别通过如下引物对扩增得到:seq id no:1
‑
2、seq id no:3
‑
4、seq id no:5
‑
6、seq id no:7
‑
8、seq id no:9
‑
10、seq id no:11
‑
12、seq id no:13
‑
14、seq id no:15
‑
16、seq id no:17
‑
18、seq id no:19
‑
20、seq id no:21
‑
22、seq id no:23
‑
24、seq id no:25
‑
26、seq id no:27
‑
28、seq id no:29
‑
30、seq id no:31
‑
32、seq id no:33
‑
34、seq id no:35
‑
36、seq id no:37
‑
38、seq id no:39
‑
40、seq id no:41
‑
42、seq id no:43
‑
44所示引物。
6.本发明还提供一种引物组合,包括22对特异性引物对,其核苷酸序列分别如seq id no:1
‑
seq id no:44所示。
7.本发明还提供一种试剂盒,包含所述的分子标记组合或者所示的引物组合。
8.本发明还提供一种普通菜豆指纹图谱的构建方法,包括构建表型指纹图谱和dna
指纹图谱:
9.不同普通菜豆的花色,生长习性,结荚习性,荚色,荚面,种皮斑纹,种皮斑纹色,粒形性状被采集并进行编号,构建表型指纹图谱;
10.利用所述的引物组合对不同品种普通菜豆的dna进行pcr扩增,再对扩增产物进行电泳检测,根据电泳检测结果构建dna指纹图谱;
11.所述表型指纹图谱和dna指纹图谱组合构建成普通菜豆的指纹图谱。
12.优选的是,普通菜豆品种包括资源库号为yd001的红腰饭豆、资源库号为yd002的33、资源库号为yd003的绿黑豆y124、资源库号为yd005的普通菜豆y137、资源库号为yd006的日本白普通菜豆、资源库号为yd007的黑普通菜豆y92、资源库号为yd008的黑普通菜豆y120、资源库号为yd009的红普通菜豆f3389、资源库号为yd010的奶圆粒、资源库号为yd011的英国红、资源库号为yd012的有机斑豆、资源库号为yd013的点滴褐、资源库号为yd016的黑普通菜豆、资源库号为yd017的蒙古圆、资源库号为yd018的英国红普通菜豆y84、资源库号为yd019的77、资源库号为yd020的y10y14、资源库号为yd022的英国红普通菜豆y84、资源库号为yd023的普通菜豆y80、资源库号为yd024的黑豆y135、资源库号为yd025的紫花普通菜豆、资源库号为yd026的黑普通菜豆、资源库号为yd027的y09、资源库号为yd028的叙利亚奶花、资源库号为yd029的英国红普通菜豆、资源库号为yd031的点滴褐、资源库号为yd032的英国红普通菜豆y84、资源库号为yd033的有机红小豆、资源库号为yd034的普通菜豆y137、资源库号为yd035的普通菜豆。
13.上述资源库号由国家杂粮技术工程研究中心提供。
14.优选的是,扩增反应体系包括如下组分:dna模板0.8μl,l0pmo1/l上游引物0.2μl,10pmo1/l下游引物0.2μl,10
×
pcr buffer 2μl,25mmol/l mg2+1.2μl,10mmol/l dntp 0.5μl,5u/μl taq酶0.2μl,ddh2o 14.4μl;所述pcr buffer不含mg
2+
。
15.优选的是,扩增反应程序包括:94℃预变性3min;94℃变性30s,56℃退火30s,72℃延伸30s,共30个循环;72℃延伸5min,4℃保存。
16.优选的是,根据标准dna分子量和引物的迁移率记录电泳结果,每对引物迁移率最大的条带记为1,迁移率次之的记为2,依次类推,无条带记为0,不同引物之间用
‘‑’
隔开,建立ssr基因型信息数据,按照引物顺序进行编码,得到的指纹代码即为该品种的特征指纹图谱。
17.本发明还提供根据所述的分子标记组合或者所述的引物组合或者所述的试剂盒在获取普通菜豆指纹图谱中的应用。
18.本发明还提供根据所述的分子标记组合或者所述的引物组合或者所述的试剂盒或者所述的构建方法在鉴别普通菜豆品种中的应用。
19.本发明公开了以下技术效果:
20.本发明公开了用于鉴别普通菜豆的分子标记组合,仅利用22对普通菜豆引物对即能扩增出上述的分子标记组合,进而能够将普通菜豆品种有效鉴别开,鉴别准确率高达100%。因此,本发明公开的分子标记组合和引物组合在进一步鉴别大量普通菜豆品种方面具有很大潜力,与现有常规形态鉴定相比,具有效果更佳,且节约时间、成本等优点,本发明可为普通菜豆品种dna指纹鉴定提供技术支持。
附图说明
21.为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
22.图1为pvssr
‑
01
‑
1的电泳带型示意图,图中自左向右,第1个泳道为marker,第2
‑
25个泳道为前24种普通菜豆的电泳带型图。
具体实施方式
23.现详细说明本发明的多种示例性实施方式,该详细说明不应认为是对本发明的限制,而应理解为是对本发明的某些方面、特性和实施方案的更详细的描述。
24.应理解本发明中所述的术语仅仅是为描述特别的实施方式,并非用于限制本发明。另外,对于本发明中的数值范围,应理解为还具体公开了该范围的上限和下限之间的每个中间值。在任何陈述值或陈述范围内的中间值以及任何其他陈述值或在所述范围内的中间值之间的每个较小的范围也包括在本发明内。这些较小范围的上限和下限可独立地包括或排除在范围内。
25.除非另有说明,否则本文使用的所有技术和科学术语具有本发明所述领域的常规技术人员通常理解的相同含义。虽然本发明仅描述了优选的方法和材料,但是在本发明的实施或测试中也可以使用与本文所述相似或等同的任何方法和材料。本说明书中提到的所有文献通过引用并入,用以公开和描述与所述文献相关的方法和/或材料。在与任何并入的文献冲突时,以本说明书的内容为准。
26.在不背离本发明的范围或精神的情况下,可对本发明说明书的具体实施方式做多种改进和变化,这对本领域技术人员而言是显而易见的。由本发明的说明书得到的其他实施方式对技术人员而言是显而易见的。本技术说明书和实施例仅是示例性的。
27.关于本文中所使用的“包含”、“包括”、“具有”、“含有”等等,均为开放性的用语,即意指包含但不限于。
28.实施例1普通菜豆指纹图谱的构建方法
29.1、实验材料
30.以30份普通菜豆品种作为样本材料,根据其表型的稳定特征以及开发的ssr分子标记构建普通菜豆品种的指纹数据,以达到品种鉴定的目的。
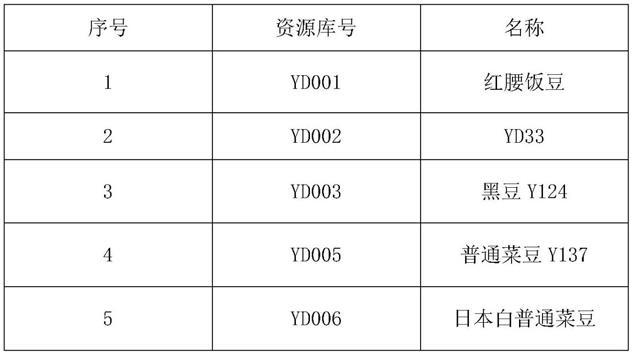
31.30种普通菜豆品种信息如表1所示。以下实施例中普通菜豆品种名称及资源库号均来自于国家杂粮工程技术研究中心种质资源库。
32.表1 30种普通菜豆品种信息
33.34.[0035][0036]
2、表型指纹图谱构建
[0037]
上述30品种分别于2017以及2018年种植于大庆市和平牧场以及黑龙江九三地区建边农场,花色,生长习性,结荚习性,荚色,荚面,种皮斑纹,种皮斑纹色,粒形等性状被采集以及编号。表型指纹排序依照主要性状、次要性状、易变性状、特殊性状进行排序,其先后顺序为:花色、生长习性、结荚习性、荚色、荚面、种皮斑纹、种皮斑纹色、粒形(如表2所示),表型指纹图谱见表3。
[0038]
表2表型指纹图谱编号
[0039] 12345花色白粉红黄白浅紫 生长习性直立蔓生半蔓生
ꢀꢀ
结荚习性无限有限
ꢀꢀꢀ
荚色斑纹褐黄白
ꢀꢀ
荚面平微凸凸
ꢀꢀ
种皮斑纹点条网无 种皮斑纹色粉红褐浅黄无紫粒形圆方卵肾 [0040]
表3 30份菜豆材料的表型指纹代码
[0041]
[0042]
[0043][0044]
3、不同品种普通菜豆标准dna指纹图谱库的构建
[0045]
3.1普通菜豆各品种总dna提取
[0046]
将普通菜豆种植于土壤中,室温培养,长出10
‑
15d天后取普通菜豆幼叶在液氮冷冻后于
‑
80℃保存备用。取各品种普通菜豆幼嫩的叶片0.2g于1.5m离心管中,加入液氮研磨成粉末。采用试剂盒法提取dna,操作实验步骤按照试剂盒说明书进行。用琼脂糖凝胶电泳和分光光度计检测总dna的质量,然后将总dna稀释成100ng/μl,储存于
‑
20℃备用。
[0047]
3.2引物的筛选
[0048]
a.ssr标记合成:由生物公司合成ssr分子标记的扩增引物,引物合成的纯度要求为page纯化,并分装成10d/管,把上、下游引物的浓度均稀释成10pmol/l。
[0049]
b.ssr分子标记引物组合的筛选方法
[0050]
步骤一,筛选引物:筛选出在不同普通菜豆品种间具有多态性、带型清晰且能够稳定重复的ssr初筛引物。
[0051]
通过筛选获得以下引物,其标记、引物名称、位置如表4所示。
[0052]
表4引物标记名称
[0053]
[0054]
[0055]
[0056][0057]
c.ssr标记扩增引物组合的筛选
[0058]
以所述普通菜豆品种为材料,利用所述合成的ssr分子标记的扩增引物(如表3)分别对各普通菜豆品种的dna进行pcr扩增,pcr反应试验中采用的pcr反应体系为20μl体系:dna模板0.8μl,f
‑
primer(10pmol/l)0.2μl,r
‑
primer(10pmol/l)0.2μl,10
×
pcr buffer(不含mg
2+
)2μl,mg
2+
(25mmo1/l)1.2μl,dntp(10mmol/l)0.5μl,taq酶(5u/μl)0.2μl,ddh2o 14.4μl,总计20.0μl。
[0059]
pcr反应程序为:94℃预变性3min;94℃变性30s,56℃退火30s,72℃延伸30s,共30个循环;72℃延伸5min,4℃保存。
[0060]
d.凝胶电泳及gel
‑
red显色
[0061]
扩增产物采用10%非变性聚丙烯酰胺凝胶电泳检测,电泳在sequi
‑
gen gt核酸电泳系统(bio
‑
rad,usa)中进行。
[0062]
显色:利用gelred固定30min,放入凝胶成像(bio
‑
red)中照相记录,根据标准dna分子量和引物的迁移率记录电泳结果,每对引物迁移率最大的条带记为1,迁移率次之的记为2,依次类推,无条带记为0,建立ssr基因型信息数据,按照引物顺序进行编码,得到的指纹代码即为该品种的特征指纹图谱;记录方式如图1所示。
[0063]
3.3普通菜豆dna特征指纹图谱的构建
[0064]
表5 30份菜豆材料分子标记指纹代码
[0065]
[0066][0067]
4普通菜豆表型与分子联合标记的指纹图谱表6 30份菜豆的表型及ssr分子联合标记的指纹代码
[0068]
30份菜豆的表型及ssr分子联合标记的指纹代码见表6,
“‑”
前面是代表表型图谱,
“‑”
后面是代表dna指纹图谱,
[0069]
[0070][0071]
由表6可得出结论,任意两个品种的联合标记指纹图谱都不相同,可判断出30份供试普通菜豆品种是不同的品种,且所对应的指纹代码是该品种所特有的指纹。
[0072]
结果表明,8种表型标记及22对引物组合可用于植物基因型的鉴定之中,能应用于鉴定普通菜豆品种的遗传特征,保护这些品种权免受侵犯。
[0073]
实施例2引物组合多态性验证
[0074]
本发明利用上述技术体系和筛选出的22对普通菜豆ssr多态性引物,构建了30个普通菜豆dna指纹图谱,可把30个普通菜豆品种区分开,将为普通菜豆的鉴定和品种权保护提供技术支撑。
[0075]
以上所述的实施例仅是对本发明的优选方式进行描述,并非对本发明的范围进行限定,在不脱离本发明设计精神的前提下,本领域普通技术人员对本发明的技术方案做出的各种变形和改进,均应落入本发明权利要求书确定的保护范围内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1