一种用于COVID-19的口服性疫苗及抗体加强剂的制作方法
一种用于covid
‑
19的口服性疫苗及抗体加强剂
技术领域
1.本发明涉及药物领域,具体地,本发明涉及一种用于covid
‑
19的口服性疫苗及抗体加强剂。
背景技术:
2.由sars
‑
cov
‑
2病毒引起的covid
‑
19(corona virus disease 2019,新型冠状病毒肺炎)大流行对人类健康造成重大威胁。针对sars
‑
cov
‑
2的疫苗是控制疾病传播的有效手段,目前虽然有多种疫苗处于开发阶段,但疫苗的疗效、安全性和患者顺从性方面还存在许多问题,例如疫苗施用后血清抗体水平低、注射给药疫苗对药物的安全性带来问题,且患者对注射给药的顺从性低等等。
3.因此,本领域需要开发一种有效、安全性高和患者顺从性好的用于sars
‑
cov
‑
2病毒的疫苗。
技术实现要素:
4.本发明的目的在于提供一种有效、安全性高和患者顺从性好的用于sars
‑
cov
‑
2病毒的疫苗。
5.本发明的第一方面提供了一种枯草芽孢杆菌,所述的枯草芽孢杆菌表达sars
‑
cov
‑
2的核衣壳蛋白和/或sars
‑
cov
‑
2的刺突蛋白的受体结合区域。
6.优选地,所述的枯草芽孢杆菌为基因工程化的枯草芽孢杆菌。
7.优选地,枯草芽孢杆菌的菌株包括枯草芽孢杆菌wb800n菌株。
8.优选地,所述的sars
‑
cov
‑
2的核衣壳蛋白的核苷酸序列如seq id no:1所示。
9.优选地,所述的sars
‑
cov
‑
2的刺突蛋白的受体结合区域的核苷酸序列如seq id no:2所示。
10.优选地,所述的枯草芽孢杆菌通过以下方法制备:
11.将表达sars
‑
cov
‑
2的核衣壳蛋白和/或sars
‑
cov
‑
2的刺突蛋白的受体结合区域掺入或导入到所述的枯草芽孢杆菌中,表达sars
‑
cov
‑
2的核衣壳蛋白和/或sars
‑
cov
‑
2的刺突蛋白的受体结合区域,得到枯草芽孢杆菌。
12.本发明第二方面,提供一种转化子,所述的转化子包括含有表达sars
‑
cov
‑
2的核衣壳蛋白和/或sars
‑
cov
‑
2的刺突蛋白的受体结合区域的基因的枯草芽孢杆菌。
13.优选地,所述的基因包括dna和/或rna。
14.优选地,所述的基因掺入或导入到所述的枯草芽孢杆菌中。
15.优选地,枯草芽孢杆菌的菌株包括枯草芽孢杆菌wb800n菌株。
16.优选地,所述的表达sars
‑
cov
‑
2的核衣壳蛋白的基因的核苷酸序列如seq id no:1所示。
17.优选地,所述的表达sars
‑
cov
‑
2的刺突蛋白的受体结合区域的核苷酸序列如seq id no:2所示。
18.优选地,所述的基因负载在质粒上。
19.优选地,所述的质粒包括穿梭载体pht01。
20.优选地,所述的表达sars
‑
cov
‑
2的核衣壳蛋白的基因的核苷酸序列如seq id no:3所示。
21.优选地,所述的表达sars
‑
cov
‑
2的刺突蛋白的受体结合区域的核苷酸序列如seq id no:4所示。
22.优选地,所述的转化子通过以下方法制备:
23.将表达sars
‑
cov
‑
2的核衣壳蛋白和/或sars
‑
cov
‑
2的刺突蛋白的受体结合区域掺入或导入到所述的枯草芽孢杆菌中,得到转化子。
24.本发明第三方面,提供一种组合物,所述的组合物包括如本发明第一方面所述的枯草芽孢杆菌和/或如本发明第二方面所述的转化子。
25.优选地,所述的组合物为药物组合物或疫苗组合物。
26.优选地,所述的组合物还包括药学上、疫苗上可接受的载体。
27.优选地,所述的组合物的剂型为注射用制剂、外用制剂或口服制剂。
28.优选地,所述的组合物的剂型为口服制剂。
29.优选地,所述的组合物的剂型为肠道口服制剂。
30.优选地,所述的组合物的剂型为小肠口服制剂。
31.优选地,所述的组合物的剂型为固体制剂、液体制剂或半固体制剂。
32.优选地,所述的组合物的剂型为片剂、胶囊剂、散剂、注射剂、粉针剂、乳剂、输液剂、口服液、气雾剂、膏剂、凝胶剂、微球、霜剂。
33.本发明第四方面,提供一种如本发明第一方面所述的枯草芽孢杆菌和/或如本发明第二方面所述的转化子的用途,用于制备组合物,所述的组合物用于预防和/或治疗sars
‑
cov
‑
2病毒感染或covid
‑
19;和/或用作sars
‑
cov
‑
2抗体的加强剂。
34.优选地,所述的sars
‑
cov
‑
2抗体包括接种sinovac
‑
corona疫苗产生的抗体。
35.优选地,所述的组合物的剂型为注射用制剂、外用制剂或口服制剂。
36.优选地,所述的组合物为药物组合物或疫苗组合物。
37.优选地,所述的组合物还包括药学上、疫苗上可接受的载体。
38.优选地,所述的组合物的剂型为口服制剂。
39.优选地,所述的组合物的剂型为肠道口服制剂。
40.优选地,所述的组合物的剂型为小肠口服制剂。
41.本发明第五方面,提供一种制备抗sars
‑
cov
‑
2的核衣壳蛋白和/或抗sars
‑
cov
‑
2病毒的刺突蛋白的受体结合区域的抗体的方法,所述的方法包括步骤:
42.将如本发明第一方面所述的枯草芽孢杆菌和/或如本发明第二方面所述的转化子口服给药对象,从血液中分离得到抗sars
‑
cov
‑
2的核衣壳蛋白的抗体和/或抗sars
‑
cov
‑
2病毒的刺突蛋白的受体结合区域的抗体。
43.优选地,所述的方法为非诊断性和非治疗性方法。
44.优选地,所述对象为人和非人哺乳动物。
45.优选地,所述的非人哺乳动物为鼠、狗、猫、牛、羊、马、猪。
46.本发明第六方面,提供一种预防和/或治疗sars
‑
cov
‑
2病毒感染或covid
‑
19的方
法,所述的方法包括步骤:口服给予所述的对象如如本发明第一方面所述的枯草芽孢杆菌和/或如本发明第二方面所述的转化子,从而预防和/或治疗sars
‑
cov
‑
2病毒感染或covid
‑
19。
47.优选地,所述对象为人和非人哺乳动物。
48.优选地,所述的非人哺乳动物为鼠、狗、猫、牛、羊、马、猪。
49.在本发明范围内中,本发明的上述各技术特征和在下文中具体描述的各技术特征之间都可以互相组合,从而构成新的或优选的技术方案。
附图说明
50.图1为sars
‑
cov
‑
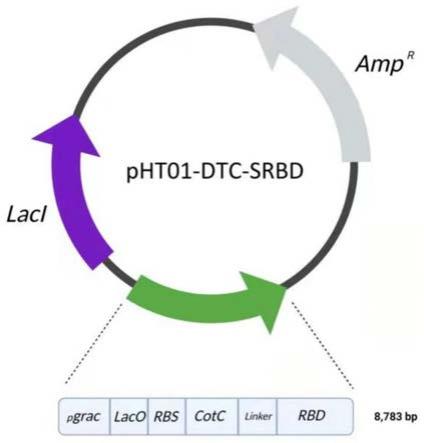
2的s蛋白的构建质粒的参考示意图。
51.图2为表达sars
‑
cov
‑
2的n蛋白和s蛋白表达的基因工程化枯草芽孢杆菌的蛋白质印迹。
52.图3为用anti
‑
srbd
‑
af488染色的野生芽孢杆菌的孢子和表达s蛋白的基因工程化的芽孢杆菌孢子。
53.图4为基因工程化枯草芽孢杆菌孢子的s蛋白印迹。
54.图5为野生型枯草芽孢杆菌和含有s蛋白的基因工程化枯草芽孢杆菌孢子的免疫染色。
55.图6为野生型枯草芽孢杆菌和基因工程化枯草芽孢杆菌孢子的流式细胞术分析。
56.图7为表达n和s蛋白的基因工程化的枯草芽孢杆菌孢子灌胃小鼠后的血清抗s蛋白的抗体。
具体实施方式
57.本发明开发了一种枯草芽孢杆菌,所述的枯草芽孢杆菌表达sars
‑
cov
‑
2的核衣壳蛋白和/或sars
‑
cov
‑
2的刺突蛋白的受体结合区域。本发明所述的基因工程化的枯草芽孢杆菌口服能够用于预防和/或治疗sars
‑
cov
‑
2病毒感染或covid
‑
19。此外,本发明所述的基因工程化的枯草芽孢杆菌还能够用作sars
‑
cov
‑
2抗体的加强剂,从而提高sars
‑
cov
‑
2的治疗效果。
58.术语
59.如本文所用,术语“包括”、“包含”与“含有”可互换使用,不仅包括开放式定义,还包括半封闭式、和封闭式定义。换言之,所述术语包括了“由
……
构成”、“基本上由
……
构成”。
60.如本文所用,术语“刺突蛋白”与“spike蛋白”可互换使用。
61.如本文所用,术语“受体结合区域”与“rbd”可互换使用。
62.如本文所用,术语“枯草芽孢杆菌wb800n”与“bacillus subtilis wb800n”可互换使用。
63.在本发明中,术语“预防”表示预防疾病和/或它的附随症状的发作或者保护对象免于获得疾病的方法。
64.本发明所述的“治疗”包括延缓和终止疾病的进展,或消除疾病,并不需要100%抑制、消灭和逆转。
65.枯草芽孢杆菌
66.本发明提供一种枯草芽孢杆菌,所述的枯草芽孢杆菌表达sars
‑
cov
‑
2的核衣壳蛋白和/或sars
‑
cov
‑
2的刺突蛋白的受体结合区域。
67.优选地,枯草芽孢杆菌的菌株包括枯草芽孢杆菌wb800n菌株。
68.在本发明的一个优选例中,所述的sars
‑
cov
‑
2的核衣壳蛋白的核苷酸序列如seq id no:1所示:
69.seq id no:1:
70.atgtcagacaatggccctcaaaaccagagaaacgctccccgtataacttttggaggaccgtcggattcaacaggtagcaatcagaatggcgagagatctggcgcaaggagtaaacagcggagaccccagggattacccaataatacagcctcatggtttactgccctaactcagcatggcaaagaagatcttaagtttcctcggggtcaaggcgtacccataaatacaaattcttccccggatgatcaaatcggatactatcgcagggcgactagacgcatcagaggcggcgatggcaagatgaaggatctgagtcccagatggtatttttattatttgggaacaggacccgaggcaggattaccgtatggagcaaacaaggatgggattatttgggtggctacggaaggagcattaaatactccgaaggatcacattggtactcggaacccggcaaacaatgctgctattgtccttcaattaccacaaggcacgaccttaccgaaaggcttttacgcggaaggttcccgcggcggctctcaggcaagctcacgttcatcatccagatctcgtaatagcagccggaactcaacacccggaagttcgagagggacaagccctgcgcgaatggcaggaaacggtggcgacgccgcgctcgccttgttgcttttggatcggttgaatcagcttgagtcaaaaatgtctggaaaggggcaacaacaacaaggtcaaacagtgacgaaaaaatcagctgcggaagcgtcaaaaaaaccccgtcaaaaacgcacggctacaaaggcgtataacgtaacacaagcatttggaagaagggggccggaacaaacgcaaggtaattttggagatcaagaactgattaggcagggcacagactataaacactggccgcagatcgcacagtttgcgcccagcgcgtcggcatttttcggcatgtcgcgtattggaatggaggtcacacccagcggcacatggcttacgtataccggcgcgatcaagctcgacgataaagatcctaactttaaagatcaggtaatactgttgaacaagcatatagacgcttacaaaacgtttccccctacagaacctaaaaaagataaaaaaaaaaaagcggatgagacccaagcgttaccccagagacagaagaaacaacaaacagtgacactgttaccagccgcagatctggatgattttagcaaacagttacaacagtctatgtcttccgctgattcaacacaagcgtaa(seq id no:1)。
71.优选地,所述的sars
‑
cov
‑
2的刺突蛋白的受体结合区域的核苷酸序列如seq id no:2所示:
72.seq id no:2:
73.aatatcacgaatttgtgcccatttggcgaagtattcaacgcaacgagatttgcctccgtttatgcgtggaaccggaagagaatctcaaattgtgtcgcggattatagcgtcctgtataattcagcgtcattctccacctttaagtgctacggcgtgtcaccaacgaaattgaatgatctgtgtttcactaatgtatatgcagatagctttgtgatccgcggcgacgaagtcagacaaattgcgccaggccaaacgggaaaaatcgcagattataattataaacttcctgatgacttcacgggatgtgtaattgcatggaactctaataaccttgattcgaaagtcggaggaaattataactatctgtatagactgttccgcaagagcaatctcaagcctttcgaacgcgatatctcgacggagatttatcaagccggcagcaccccgtgtaacggtgttgaaggcttcaattgctatttcccgctgcagagctatggctttcaaccgacgaacggggttggctaccagccctaccgcgtcgtggttctgtccttcgaattactccatgccccggctacggtttaatgaaa(seq id no:2)。
74.转化子
75.转化子(transformant)是掺入或导入外源dna后获得了新的遗传标志的细菌细胞或其他受体细胞。转化后的受体菌,称转化子transformant。
76.本发明提供一种转化子,所述的转化子包括含有表达sars
‑
cov
‑
2的核衣壳蛋白和/或sars
‑
cov
‑
2的刺突蛋白的受体结合区域的基因的枯草芽孢杆菌。
77.优选地,所述的基因包括dna和/或rna。
78.优选地,所述的基因掺入或导入到所述的枯草芽孢杆菌中。
79.优选地,枯草芽孢杆菌的菌株包括枯草芽孢杆菌wb800n菌株。
80.优选地,所述的表达sars
‑
cov
‑
2的核衣壳蛋白的基因的核苷酸序列如上文seq id no:1所示。
81.优选地,所述的表达sars
‑
cov
‑
2的刺突蛋白的受体结合区域的核苷酸序列如上文seq id no:2所示。
82.优选地,所述的基因负载在质粒上。
83.优选地,所述的质粒包括穿梭载体pht01。
84.优选地,所述的表达sars
‑
cov
‑
2的核衣壳蛋白的基因的核苷酸序列如seq id no:3所示。
85.优选地,所述的表达sars
‑
cov
‑
2的刺突蛋白的受体结合区域的核苷酸序列如seq id no:4所示。
86.组合物
87.本发明提供了一种组合物,所述的组合物能够用于预防和/或治疗sars
‑
cov
‑
2病毒感染或covid
‑
19。
88.代表性地,所述的组合物为药物组合物或疫苗组合物。
89.本发明所述的组合物还可以包括药学上、疫苗上可接受的载体。
90.在本发明中,组合物的剂型包括(但不限于)口服制剂、注射剂、外用制剂。
91.代表性地,组合物的剂型包括(但不限于):片剂、胶囊剂、散剂、注射剂、粉针剂、乳剂、输液剂、口服液、气雾剂、膏剂、凝胶剂、微球、霜剂。
92.术语“药学上、疫苗上可接受的载体”指的是:一种或多种相容性固体、半固体、液体或凝胶填料,它们适合于人体或动物使用,而且必须有足够的纯度和足够低的毒性。“相容性”是指药物组合物中的各组分和药物的活性成分以及它们之间相互掺和,而不明显降低药效。
93.应理解,在本发明中,所述的载体没有特别的限制,可选用本领域常用材料,或用常规方法制得,或从市场购买得到。药学可接受的载体部分例子有纤维素及其衍生物(如甲基纤维素、乙基纤维素、羟丙甲基纤维素、羧甲基纤维素钠等)、明胶、滑石粉、固体润滑剂(如硬脂酸、硬脂酸镁)、硫酸钙、植物油(如豆油、芝麻油、花生油、橄榄油、等)、多元醇(如丙二醇、甘油、甘露醇、山梨醇等)、乳化剂(如吐温)、润湿剂(如十二烷基硫酸钠)、缓冲剂、螯合剂、增稠剂、ph调节剂、透皮促进剂、着色剂、调味剂、稳定剂、抗氧化剂、防腐剂、抑菌剂、无热原水等。
94.代表性的,液体剂型除了活性药物成分外,液体剂型可包含本领域中常规采用的惰性稀释剂,如水或其它溶剂,增溶剂和乳化剂,例如,乙醇、异丙醇、碳酸乙酯、乙酸乙酯、丙二醇、1,3
‑
丁二醇、二甲基甲酰胺以及油,特别是棉籽油、花生油、玉米胚油、橄榄油、蓖麻油和芝麻油或这些物质的混合物等。除了这些惰性稀释剂外,组合物也可包含助剂,如润湿剂、乳化剂和悬浮剂等
95.药物制剂应与给药方式相匹配。本发明药剂还可与其他协同治疗剂一起使用(包括之前、之中或之后使用)。使用药物组合物时,是将安全有效量的药物施用于所需对象(如人或非人哺乳动物),所述安全有效量通常至少约10微克/千克体重,而且在大多数情况下不超过约8毫克/千克体重,较佳地该剂量是约10微克/千克体重
‑
约1毫克/千克体重。当然,具体剂量还应考虑给药途径、病人健康状况等因素,这些都是熟练医师技能范围之内的。
96.用途
97.本发明还提供一种如本发明所述的枯草芽孢杆菌和/或如本发明所述的转化子的用途,用于制备组合物,所述的组合物用于预防和/或治疗sars
‑
cov
‑
2病毒感染或covid
‑
19;和/或用作sars
‑
cov
‑
2抗体的加强剂。
98.本发明还提供一种制备抗sars
‑
cov
‑
2的核衣壳蛋白和/或抗sars
‑
cov
‑
2病毒的刺突蛋白的受体结合区域的抗体的方法,所述的方法包括步骤:
99.将如本发明所述的枯草芽孢杆菌和/或如本发明所述的转化子口服给药对象,从血液中分离得到抗sars
‑
cov
‑
2病毒的刺突蛋白的受体结合区域的抗体。
100.优选地,所述的方法为非诊断性和非治疗性方法。
101.优选地,所述对象为人和非人哺乳动物。
102.优选地,所述的非人哺乳动物为鼠、狗、猫、牛、羊、马、猪。
103.本发明还提供一种预防和/或治疗sars
‑
cov
‑
2病毒感染或covid
‑
19的方法,所述的方法包括步骤:口服给予所述的对象如本发明所述的枯草芽孢杆菌和/或如本发明所述的转化子,从而预防和/或治疗sars
‑
cov
‑
2病毒感染或covid
‑
19。
104.本发明的主要技术效果包括:
105.本发明开发了一种基因工程化枯草芽孢杆菌,所述的枯草芽孢杆菌表达sars
‑
cov
‑
2的核衣壳蛋白和sars
‑
cov
‑
2的刺突蛋白的受体结合区域,本发明所述的基因工程化的枯草芽孢杆菌通过口服能够用于预防治疗sars
‑
cov
‑
2病毒感染或covid
‑
19,口服给药成本低、安全性高、服用方便、患者顺应性高。此外,本发明所述的基因工程化的枯草芽孢杆菌还能够用作sars
‑
cov
‑
2抗体的加强剂,从而提高sars
‑
cov
‑
2的治疗效果。
106.下面结合具体实施例,进一步阐述本发明。应理解,以下具体实施例以本技术方案为前提,给出了详细的实施方式和具体操作过程,但本发明的保护范围并不限于本实施例。
107.实施例
108.sars
‑
cov
‑
2的n蛋白为sars
‑
cov
‑
2的核衣壳蛋白。
109.sars
‑
cov
‑
2的s蛋白为sars
‑
cov
‑
2的刺突蛋白(spike)的rbd(受体结合区域)。
110.表达sars
‑
cov
‑
2的n和s蛋白的基因工程化枯草芽孢杆菌简称基因工程化枯草芽孢杆菌。
111.实施例1
112.1.1表达sars
‑
cov
‑
2的n和s蛋白的基因工程化枯草芽孢杆菌的制备
113.枯草芽孢杆菌wb800n(bacillus subtilis wb800n)菌株用于研究。该细菌用编码sars
‑
cov
‑
2病毒s/n蛋白的质粒进行转化。枯草芽孢杆菌的孢子形成是用difcosporulationmedium从营养细胞诱导的,并进一步用溶酶体处理以去除营养细胞。
114.包含来自枯草芽孢杆菌的全长cotc级联、肽连接区域和来自sars
‑
cov
‑
2的核衣壳蛋白或刺突蛋白(spike)的rbd(受体结合区域)的表达构建体是针对枯草芽孢杆菌进行密
码子优化的,通过invitrogengeneart基因合成,进一步克隆到大肠杆菌(e.coli)和枯草芽孢杆菌的穿梭载体pht01中。大肠杆菌菌株dh5α(neb)用于克隆,表达sars
115.sars
‑
cov
‑
2的n和s蛋白的构建质粒转化到枯草芽孢杆菌菌株wb800n(mobitec)中进行n和s蛋白表达。质粒的dna序列通过sanger测序确认。
116.转化到枯草芽孢杆菌菌株wb800n的pht01
‑
sars
‑
cov
‑
2的核衣壳蛋白构建质粒和pht01
‑
sars
‑
cov
‑
2的spike蛋白的rbd的构建质粒的测序结果如下所示:
117.pht01
‑
核衣壳蛋白的核苷酸序列如下seq id no:3所示:
118.seq id no:3:
119.[0120][0121]
其中:cotc:无加黑下划线
[0122]
肽连接区域:加黑斜体
[0123]
sars
‑
cov
‑
2的核衣壳蛋白核苷酸:加黑有下划线
[0124]
pht01
‑
spike蛋白的rbd的核苷酸序列如下seq id no:4所示:
[0125]
seq id no:4:
[0126]
[0127][0128]
其中:cotc:无加黑下划线
[0129]
肽连接区域:加黑斜体
[0130]
sars
‑
cov
‑
2的刺突蛋白的rbd核苷酸序列:加黑有下划线。
[0131]
sars
‑
cov
‑
2的s蛋白的构建质粒的参考示意图如图1所示。
[0132]
1.2从基因工程化枯草芽孢杆菌中诱导sars
‑
cov
‑
2的n和s蛋白
[0133]
枯草芽孢杆菌转化子将在37℃、200rpm下生长,直到od600值在补充有氯霉素(5μg/ml)的2xlb中达到1.0。培养物用终浓度为1mm iptg进行诱导,并在37℃、200rpm下再诱导12h。收集培养物并以4,200rpm离心15min。细胞沉淀将用1x磷酸盐缓冲盐水(pbs,ph7.4)洗涤并重悬于1/2体积的difcosporulationmedium(dsm)(8g营养肉汤、0.1%kcl、1mm mgso4和10μm mncl2溶于1l蒸馏水中,添加0.5mm cacl2和1μm feso4)。细胞在37℃、200rpm下生长24小时。细胞在37℃下通过溶菌酶(0.1mg/ml)裂解1h,10,000rpm离心15分钟,然后用1xpbs洗涤三次。来自转化的枯草芽孢杆菌孢子用pbs洗涤,用裂解缓冲液(pbs+1%triton和完全蛋白酶抑制剂)裂解,然后在100℃下变性10min,然后在14,800g下离心15min。进行bca测定以确定蛋白质浓度。100ng刺突蛋白(spike protein)标准品的rbd和10μg孢子裂解物将在sds
‑
page中进行分析,然后用针对刺突蛋白的rbd和核衣壳蛋白单克隆抗体进行蛋白印迹考察。
[0134]
1.3.人单核细胞与肠道ht
‑
29细胞共培养
[0135]
为了模拟肠道粘膜区域,将采用人单核细胞和肠道ht
‑
29细胞的体外共培养系统。人单核细胞从健康志愿者的新鲜人血沉棕黄层中制备,用于纯化原代人类巨噬细胞。外周血单核细胞(pbmc)将通过ficoll密度(1.082g/ml)以1800rpm离心25min进行分离。红细胞裂解后,cd14特异性macs珠(miltenyibiotec)将用于富集cd14+单核细胞。为了诱导巨噬细胞分化,cd14+单核细胞将在含有l
‑
谷氨酰胺、10%fcs、1%青霉素
‑
链霉素、1%丙酮酸钠和1%glutamax(gibco)和gm
‑
csf(25ng/ml)的rpmi1640培养基中培养6
‑
7天和,细胞培养密度
为1.5x105/cm2。
[0136]
将人小肠上皮ht
‑
29细胞在24孔培养板中培养至融合,然后在37℃下用pbs冲洗以防止细胞脱离。然后将单核细胞悬液(5x105/ml)添加到培养板中的ht
‑
29细胞上。上皮细胞
‑
单核细胞共培养物在有或没有野生枯草芽孢杆菌/基因工程化枯草芽孢杆菌中孵育。通过bio
‑
plex200system(bio
‑
rad)的bio
‑
plex人细胞因子/趋化因子多重分析对培养上清液或小鼠血清中促炎因子(il
‑
1、il
‑
6、il
‑
8、il
‑
12、干扰素
‑
γ(ifnγ)和tnf
‑
α)的浓度进行定量分析。
[0137]
1.4.体外细胞分离和dcs的产生
[0138]
单核细胞将在24孔板中以2
×
106/ml密度铺在24孔板中,并在37℃和5%co2条件下粘附45分钟。通过用温和的培养基流冲洗孔2到3次,可以去除未贴壁的细胞。然后在存在两种细胞因子的条件下培养单核细胞:粒细胞巨噬细胞集落刺激因子(50ng/ml)和il
‑
4(40ng/ml),在37℃和5%co2条件下培养。在第3天,50%的培养基将替换为新鲜培养基和细胞因子。然后在第6天收集dcs并洗涤。细胞成熟通过野生枯草芽孢杆菌/基因工程化枯草芽孢杆菌诱导48小时。脂多糖(lps)(0.1g/ml)将用作阳性对照。收获细胞后收集dcs培养物的上清液,并储存在
‑
80℃检测细胞因子。
[0139]
通过bio
‑
plex200system(bio
‑
rad)的bio
‑
plex人细胞因子/趋化因子多重分析测定(il
‑
1、il
‑
12、il
‑
10、ifn
‑
γ和tnf
‑
α)的浓度。
[0140]
1.5.dcs的流式细胞分析
[0141]
第8天,收集dcs(树突状细胞),洗涤并用荧光色素偶联抗体标记。标记后,清洗细胞悬浮液并重新悬浮以进行流式细胞术分析。fitc、pe和pe
‑
cyanin5.1(pc5)
‑
偶联同型对照和cd11c
‑
apc、cd14
‑
fitc、cd40
‑
percp、cd80
‑
fitc、cd83
‑
pe、cd86
‑
pe和hla
‑
dr
‑
apc抗体。dcs通过标准前向散射和侧向散射曲线测定大细胞,将不同cd标记物的平均荧光强度与rpmi处理的阴性对照的平均荧光强度归一化为相对荧光强度。
[0142]
1.6.免疫方案
[0143]
1.6.1首先使用上述体外实验研究和比较野生枯草芽孢杆菌/基因工程化枯草芽孢杆菌的不同组合的免疫调节活性。后续动物研究中使用的是野生枯草芽孢杆菌/基因工程化枯草芽孢杆菌基于体外实验的结果。
[0144]
使用balb/小鼠,8周大的小鼠将通过灌胃(p.o.)途径接种野生枯草芽孢杆菌或基因工程化枯草芽孢杆菌的孢子。
[0145]
第1组:野生未免疫组
[0146]
第2组:1.0
×
10
10
个孢子的基因工程化枯草芽孢杆菌
[0147]
通过不锈钢圆头饲插管灌胃给予小鼠含有1
×
10
10
个孢子的悬浮液(0.5毫升等分试样)。在施用孢子前30min,小鼠灌胃给予0.5ml 0.1m碳酸氢钠溶液。将在免疫方案前三天和第给药后收集血液,测试每个小鼠组的个体血液样品的抗体反应。
[0148]
1.6.2抗体的血清学
[0149]
小鼠在全身麻醉下放血,用于elisa分析,并将血清冷冻以备将来检测。靶向抗原是sars
‑
cov
‑
2n和s蛋白。为了确定小鼠血清中抗体的滴度,elisa平板上涂有抗原,通常为0.1ng/孔。将在含有1%hsa的pbs中连续稀释的血清上清液加入包被板的孔中,并在室温下孵育1h。山羊抗小鼠igm或igg与碱性磷酸酶偶联(southernbiotechnology,birmingham,
al,usa)作为二抗。抗体效价定义为最高血清稀释度,其吸光度比正常血清样品的吸光度高0.1或更高。如果反应性滴度从无法检测到的预处理增加到疫苗接种后的至少1:40,或者如果可检测到预处理的8倍,则反应效价通过elisa测定为阳性的。
[0150]
1.6.3脾细胞的分离和活化
[0151]
最后一次免疫后,将处死小鼠,无菌收集脾脏用于脾细胞分离。脾脏将灌注rpmi
‑
1640(添加有10%热灭活胎牛血清、25mm hepes、2mm l
‑
谷氨酰胺、1mm丙酮酸钠、100iu/ml青霉素和100mg/ml链霉素)和配备26g针头的5ml注射器将用于获得脾细胞的单细胞悬液。脾细胞悬液将在300
×
g离心5分钟。rbcs使用3ml 0.84%的无菌nh4cl裂解2分钟。细胞用rpmi
‑
1640洗涤以去除裂解的红细胞和nh4cl。脾细胞(2
×
105/ml)将在不存在或存在纯化的重组sars
‑
cov
‑
2s和n蛋白的情况下培养48小时。然后将收集含有释放的细胞因子的上清液样品并储存在
‑
80℃。sars
‑
cov
‑
2s和n蛋白刺激的细胞分泌的il
‑
1、il
‑
6、il
‑
10、il
‑
17、ifn
‑
γ和tnf
‑
α的水平将通过bio
‑
plex200system(bio
‑
rad)的bio
‑
plexhuman进行细胞因子/趋化因子多重分析。
[0152]
1.7临床试验
[0153]
志愿者被随机分成未接种疫苗组和接种疫苗组。
[0154]
对于未接种其它疫苗组的志愿者,志愿者分别在第0天、14天和28天口服1粒含有1x10
10
cfu基因工程化枯草芽孢杆菌孢子的胶囊,分别在第0天、27天和42天进行血液检测。
[0155]
对于接种其它疫苗组的志愿者,在接种sinovac
‑
corona疫苗4个月后,进行血液检测(计为第0天),然后口服1粒含有1x10
10
cfu基因工程化枯草芽孢杆菌孢子的胶囊后第14天进行血液检测。
[0156]
对血液样本进行maglumi sars
‑
cov
‑
2中和抗体测试,以定量测定志愿者中抗sars
‑
cov
‑
2的中和抗体滴度,测定的检测限为0.003μg/ml。
[0157]
1.8.统计分析
[0158]
将使用graphpadprism软件5.0版(graphpadsoftware,sandiego,ca,usa)进行统计分析和显着性分析,如通过配对样本的学生t检验或单向方差分析(anova)进行测量。在所有比较中,p<0.05将被视为具有统计学意义。
[0159]
2.实验结果
[0160]
2.1从基因工程化的枯草芽孢杆菌中诱导sars
‑
cov
‑
2的n蛋白和s蛋白
[0161]
通过枯草芽孢杆菌裂解物的蛋白质印迹和用抗s蛋白的rbd
‑
af488染色孢子,证实工程化枯草芽孢杆菌的sars
‑
cov
‑
2的n和s蛋白表达,如图2和图3所示。
[0162]
2.2孢子的表征
[0163]
通过蛋白质印迹和免疫染色也证实了的孢子特征,如图4和图5所示。染色后的孢子还通过流式细胞仪进一步确认其特征,流式细胞仪分析结果如图6所示。
[0164]
2.3动物实验
[0165]
小鼠在第0天开始进行3个疗程给予表达n蛋白和s蛋白的枯草芽孢杆菌孢子的灌胃(first log),第98天后另外连续3天、每天一次的灌胃(second log)则给予表达s蛋白的枯草芽孢杆菌孢子,小鼠血清中的抗s蛋白的抗体igm和igg的含量如图7所示。
[0166]
可以看出,口服给予表达n蛋白和s蛋白的枯草芽孢杆菌孢子后,血清中能够高含量的产生抗体sars
‑
cov
‑
2的s蛋白抗体igm和igg,表明表达n蛋白和s蛋白的枯草芽孢杆菌
能够口服用作sars
‑
cov
‑
2感染的疫苗。
[0167]
2.4人细胞因子/趋化因子多重分析测定结果
[0168]
人细胞因子/趋化因子多重分析测定il
‑
1、il
‑
12、il
‑
10、ifn
‑
γ和tnf
‑
α的浓度在人单核细胞与肠道ht
‑
29上皮细胞共培养物和dcs通过野生枯草芽孢杆菌/基因工程化枯草芽孢杆菌诱导下,以及小鼠免疫后分离的脾细胞在存在纯化的重组sars
‑
cov
‑
2s和n蛋白活化下,均有显著的上升。
[0169]
2.5临床试验结果
[0170]
对于未接种其它疫苗组的志愿者,在口服基因工程化枯草芽孢杆菌孢子的胶囊后的第0天、27天和42天,血液中的抗体sars
‑
cov
‑
2的含量如下表1所示:
[0171]
表1未接种其它疫苗组的志愿者口服基因工程化枯草芽孢杆菌孢子的胶囊后的第0天、27天和42天血液中的抗体sars
‑
cov
‑
2中和抗体的含量
[0172]
志愿者第0天第27天第42天男性(65岁)<0.003μg/ml0.016μg/ml0.037μg/ml女性(58岁)<0.003μg/ml0.003μg/ml0.034μg/ml女性(48岁)<0.003μg/ml<0.003μg/ml0.022μg/ml男性(54岁)<0.003μg/ml0.003μg/ml0.050μg/ml男性(71岁)<0.003μg/ml<0.003μg/ml0.042μg/ml
[0173]
对于接种其它疫苗组的志愿者,在接种sinovac
‑
corona疫苗4个月后(计为第0天)和口服基因工程化枯草芽孢杆菌孢子的胶囊后第14天血液中的抗体sars
‑
cov
‑
2中和抗体的含量如下表2所示:
[0174]
表2接种其它疫苗组的志愿者在接种sinovac
‑
corona疫苗4个月后(计为第0天)和口服基因工程化枯草芽孢杆菌孢子的胶囊后第14天血液中的抗体
[0175]
sars
‑
cov
‑
2中和抗体的含量
[0176]
志愿者第0天第14天男性(58岁)0.08μg/ml0.082μg/ml男性(58岁)0.108μg/ml0.194μg/ml男性(55岁)0.073μg/ml0.090μg/ml
[0177]
从表1和表2中可以看出,口服表达sars
‑
cov
‑
2的n和s蛋白的基因工程化枯草芽孢杆菌能够产生抗体sars
‑
cov
‑
2中和抗体,从而对sars
‑
cov
‑
2进行治疗,表明表达n蛋白和s蛋白的枯草芽孢杆菌能够口服用作sars
‑
cov
‑
2感染的疫苗。
[0178]
以上所述是本发明针对一种案例设计的实施方案,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下还可以作出若干改进,这些改进也应视为本发明的保护范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1