一种温度响应性透明质酸、水凝胶及其制备方法与应用
1.本发明属于组织工程与再生医学技术领域,特别涉及一种温度响应性透明质酸、水凝胶及其制备方法与应用。
背景技术:
2.角膜上皮位于角膜的最上层,与外界环境直接接触,眼外伤、细菌或病毒感染都可引起角膜上皮缺损,从而导致视力下降。正常情况下角膜上皮缺损经过潜伏期、迟滞期、迁移期、增殖期和再上皮化期可在7
‑
14天愈合,但是复发性角膜糜烂可发生在外伤或者某些营养不良,易导致基底膜的破坏,会出现难以愈合和反复性上皮缺损现象,甚至会引起角膜瘢痕形成,影响正常视力。这主要是周围上皮细胞分泌炎症因子和活化因子致使基质细胞纤维化。目前对于角膜上皮缺损治疗的方法有口服四环素、使用局部类固醇或自体血清滴眼液以及羊膜修补或移植。虽然这些药物治疗表现出了一定的效果,但是具有耐受性和副作用,治疗成功率低等问题。有大量的文献曾研究过角膜上皮损伤愈合,通过许多不同种类的实验动物以及不同的损伤方法获得了巨大的进展,提高了患者的生活质量,但仍然会发生许多由于角膜瘢痕的形成而导致失明和生活质量下降的病例。促进角膜上皮细胞的快速、完全愈合和屏障功能重建是维持良好视力的关键,然而目前尚未见有能够有效和快速促进角膜上皮愈合的药物或者其他治疗方法来挽救悲剧的发生。
3.间充质干细胞(mesenchyma stem cells,mscs)作为一种成体干细胞,广泛存在于结缔组织和器官间质,因其全能性与多向分化潜能广泛应用于自身免疫性疾病,实体器官移植物存活,肝硬化,肾病疾病,神经和肌肉退化疾病,心肌梗塞或脊髓引起的病变和损伤等。脂肪间充质干细胞(adipose
‑
derived stem cell)因来源丰富、易于获取、低免疫原性等优点而受到广泛的关注,但是其治疗的具体机制仍然不明确,而且具有致瘤风险。另外,mscs会因为免疫排斥反应而被机体排斥,因此研究者将目光投向了细胞的旁分泌作用,其是细胞经过“内吞
‑
融合
‑
外排”等一系列主动调控过程而形成的细胞外纳米级小囊泡。有研究已表明细胞旁分泌与其具有和来源细胞相似的治疗功能,例如减少心肌梗死的面积,促进肾脏损伤修复等。
4.在20世纪80年代早期,研究人员首次描述了有网织红细胞分泌的小内皮细胞囊泡,并应用外泌体(exosome)进行命名。exosome是一种由脂质,蛋白质,细胞骨架元素,分子伴侣和信号分子动态组成的脂质分子膜包裹的小囊泡,电镜下观察呈茶托状,直径约为30
‑
150nm,具有来源细胞的胞质包膜成分。其中含有丰富的mrna,microrna和dna成分,无免疫原性,是运输载体。有研究已表明外泌体在皮肤、软骨和肾脏等修复方面取到了明显的治疗效果,但在角膜修复方面报道甚少。
5.可注射超分子水凝胶即能够从注射器针头轻松地挤出后能快速的恢复或成为稳定凝胶网络的水凝胶,由于其在损伤部位能够实现原位成胶,且操作简单,不需要二次手术,是构建组织工程用细胞支架或载生物活性药物的有效方法之一。透明质酸作为一种天然大分子化合物,具有卓越保水性能和可降解性等物理参数,同时也具有生物相容性和提
供生物相关微环境的生物学特征,在医学领域具有广泛的应用前景。天然水凝胶具有疏松多孔的网络结构,可以模拟天然的细胞外基质并为细胞粘附、迁移和增殖提供支持;另外,天然水凝胶可以被溶酶体降解,在生物体内具有良好的生物可降解性,可以被机体降解并吸收,以便在组织修复损伤区与活性物质进行协调作用。
6.鉴于眼部的清洁作用,眼部给药一直以来存在一个问题:药物在角膜表面停留时间短。目前眼部给药的方法就是多次给药,但反复的药物刺激可能产生炎症反应,且药物使用量增加,患者依从性差。因此,如何选择合适的生物材料使外泌体与生物材料结合,从而有效避免临床药物在眼部的快速流失和频繁的给药,促使外泌体在眼部驻留,提高治疗效果是实现角膜组织损伤修复的关键。
技术实现要素:
7.本发明的首要目的在于克服现有技术的缺点与不足,提供一种温度响应性透明质酸控缓释水凝胶的制备方法。
8.本发明的另一目的在于提供由上述制备方法制备得到的温度响应性透明质酸控缓释水凝胶。
9.本发明的再一目的在于提供上述温度响应性透明质酸控缓释水凝胶的应用。
10.为实现上述目的,本发明通过下述技术方案实现:
11.一种温度响应性透明质酸的制备方法,包括如下步骤:
12.(1)称取透明质酸(ha)加入水中,4~6℃搅拌至其完全溶解,得溶解液;
13.(2)将步骤(1)的溶解液降低温度至0~2℃,逐滴滴入甲基丙烯酸酐(ma),得溶液1;其中,甲基丙烯酸酐:ha中二糖的重复单元的摩尔比=20:1;
14.(3)向步骤(2)的溶液1中逐滴滴入naoh溶液,维持ph在8~12之间,加入naoh溶液后反应体系由透明变为乳白色;升温至4℃继续反应,得到溶液2;
15.(4)将步骤(3)的溶液2用无水乙醇沉淀,得到白色絮状物,加入水搅拌溶解完全后,置于截留分子量为8000~12000的透析袋透析;
16.(5)透析结束后,冷冻干燥得到白色海绵状产物,命名为hama;
17.(6)向步骤(5)得到的hama中加入水,搅拌溶解,得到反应体系1;
18.(7)向0.45mol/l 2
‑
甲基
‑2‑
丙烯酸
‑2‑
(2
‑
甲氧基
‑
乙氧基)乙酯(pdegma)溶液中加入步骤(6)的反应体系1中,得到反应体系2;
19.(8)将30mol/l过硫酸钾(k2s2o8,kps)溶液加入步骤(7)的反应体系2中;
20.(9)将步骤(8)的反应体系2进行除氧处理,得到除氧后的反应体系2;
21.(10)取四甲基乙二胺(temed)加入水,除氧后加入步骤(9)的除氧后的反应体系2中;
22.(11)保持氮气正压,20℃反应12~24h,透析,得到的反应体系3;
23.(12)将步骤(11)得到的反应体系3干燥,即得温度响应性透明质酸。
24.步骤(1)中所述的水优选为超纯水或去离子水;更优选为去离子水。
25.步骤(1)中所述的透明质酸与水按质量体积比(g:ml)1~10:100计算;更优选按质量体积比(g:ml)1:100计算。
26.步骤(1)中所述的搅拌优选在低温反应器中进行。
27.步骤(3)中所述的naoh溶液的浓度优选为3~7m;更优选为5m。
28.步骤(3)中所述的继续反应的时间优选为8~24h;更优选为12h。
29.步骤(4)中所述的水优选为去离子水。
30.步骤(4)中所述的透析的试剂为水;更优选为去离子水。
31.步骤(6)中所述的水优选为去离子水。
32.步骤(6)中所述的搅拌溶解优选为磁力搅拌溶解。
33.步骤(6)中所述的hama与水按质量体积比(g:ml)0.1~0.3:180计算;更优选质量与体积比(g:ml)0.2:180计算。
34.步骤(7)中所述的2
‑
甲基
‑2‑
丙烯酸
‑2‑
(2
‑
甲氧基
‑
乙氧基)乙酯溶液优选通过注射器加入步骤(6)的反应体系1中。
35.步骤(7)中所述的2
‑
甲基
‑2‑
丙烯酸
‑2‑
(2
‑
甲氧基
‑
乙氧基)乙酯溶液的溶剂优选为水;更优选为去离子水。
36.步骤(7)中所述的0.45mol/l2
‑
甲基
‑2‑
丙烯酸
‑2‑
(2
‑
甲氧基
‑
乙氧基)乙酯溶液的配置方法优选为:500μl 0.5g纯度为95%的2
‑
甲基
‑2‑
丙烯酸
‑2‑
(2
‑
甲氧基
‑
乙氧基)乙酯加入5ml的去离子水中,冰水浴溶解完全即得0.45mol/l 2
‑
甲基
‑2‑
丙烯酸
‑2‑
(2
‑
甲氧基
‑
乙氧基)乙酯溶液。
37.步骤(8)中所述的30mol/l过硫酸钾(k2s2o8,kps)溶液优选通过如下方法制备得到:称40mg的过硫酸钾(k2s2o8,kps)加入5ml的去离子水,低温搅拌溶解完全,即得30mol/l过硫酸钾(k2s2o8,kps)溶液。
38.步骤(9)中所述的除氧处理是指通氮除氧。
39.步骤(10)中所述的水优选为去离子水。
40.步骤(10)中所述的四甲基乙二胺与水优选按体积比0.2:3~7计算;更优选为按体积比0.2:5计算。
41.步骤(11)中所述的透析优选为用截留分子量为8000~12000的透析袋进行透析。
42.步骤(11)中所述的透析的试剂为水;所述的透析的时间优选为2~4天;更优选为3天。
43.步骤(12)中所述的干燥优选为冷冻干燥。
44.一种温度响应性透明质酸,通过上述制备方法制备得到。所述的温度响应性透明质酸即接枝有温敏侧链的功能化透明质酸。所述接枝有温敏侧链的功能化透明质酸的温敏侧链为2
‑
甲基
‑2‑
丙烯酸
‑2‑
(2
‑
甲氧基
‑
乙氧基)乙酯(pdegma)。
45.所述的温度响应性透明质酸在制备温度响应性复合水凝胶中的应用。
46.一种温度响应性复合水凝胶,是以上述温度响应性透明质酸与pbs缓冲液形成的温度响应性透明质酸溶胶作为载体,加入脂肪间充质干细胞来源的外泌体得到。
47.所述的温度响应性复合水凝胶的制备方法,包括以下步骤:
48.(a)在4℃条件下,将上述温度响应性透明质酸溶解在pbs缓冲液中,磁力搅拌,得温度响应性透明质酸溶胶;
49.(b)将脂肪间充质干细胞来源的外泌体缓慢加入步骤(a)的温度响应性透明质酸溶胶中,充分混合得到包含外泌体的温度响应性透明质酸复合溶胶,即温度响应性复合水凝胶。
50.步骤(a)中所述的pbs缓冲液的ph为7.4,浓度为0.1m。
51.步骤(a)中所述的磁力搅拌的转速为100~400rpm;更优选为200rpm。
52.步骤(a)中所述的磁力搅拌是指磁力搅拌过夜;所述的过夜的时间是8~12h。
53.步骤(a)中所述的温度响应性透明质酸与pbs缓冲液按质量比1~5:100计算;更优选按质量比5:100计算。
54.步骤(b)中所述的脂肪间充质干细胞来源的外泌体在温度响应性透明质酸溶胶和脂肪间充质干细胞来源的外泌体形成的体系中的浓度优选为5~100μg/ml;更优选为20μg/ml。
55.所述的温度响应性复合水凝胶或温度响应性透明质酸在滴眼液中的应用。
56.所述的滴眼液优选为能够促进眼角膜上皮创伤愈合,和/或治疗眼部炎症的滴眼液。
57.本发明的温度响应性复合水凝胶可作为滴眼液的组分应用于眼角膜上皮组织创伤的修复和/或眼部炎症治疗中。
58.本发明相对于现有技术具有如下的优点及效果:
59.(1)本发明提供的温度响应性复合水凝胶对角膜上皮创伤愈合具有良好的促使效果,是一种较好的促进角膜上皮损伤愈合的药物。本发明通过将脂肪间充质干细胞来源的外泌体缓慢加入温度响应性透明质酸溶胶中,利用温度响应性透明质酸对脂肪间充质干细胞来源的外泌体的控缓释作用,将脂肪间充质干细胞来源的外泌体释放至损伤处,调控其释放速度和释放方式。
60.(2)本发明的温度响应性复合水凝胶,其包裹脂肪间充质干细胞来源的外泌体。相比干细胞本身,温度响应性复合水凝胶具有精准高效的靶向作用机制、易于收集保存、结构稳定不易降解老化、避免不良分化导致肿瘤形成等优势,使得温度响应性复合水凝胶在角膜上皮创伤愈合中具有极高的商品化潜能和转化应用前景。
61.(3)本发明的温度响应性复合水凝胶能在4℃环境下保持流动状态,但在生理温度(37℃)下转变为凝胶状态,即非流动状态,可以避免临床药物在眼部的快速流失,避免频繁给药的麻烦,可以让脂肪间充质干细胞来源的外泌体在眼部驻留,提高治疗效果,从而为角膜组织损伤修复提供新的视角。
附图说明
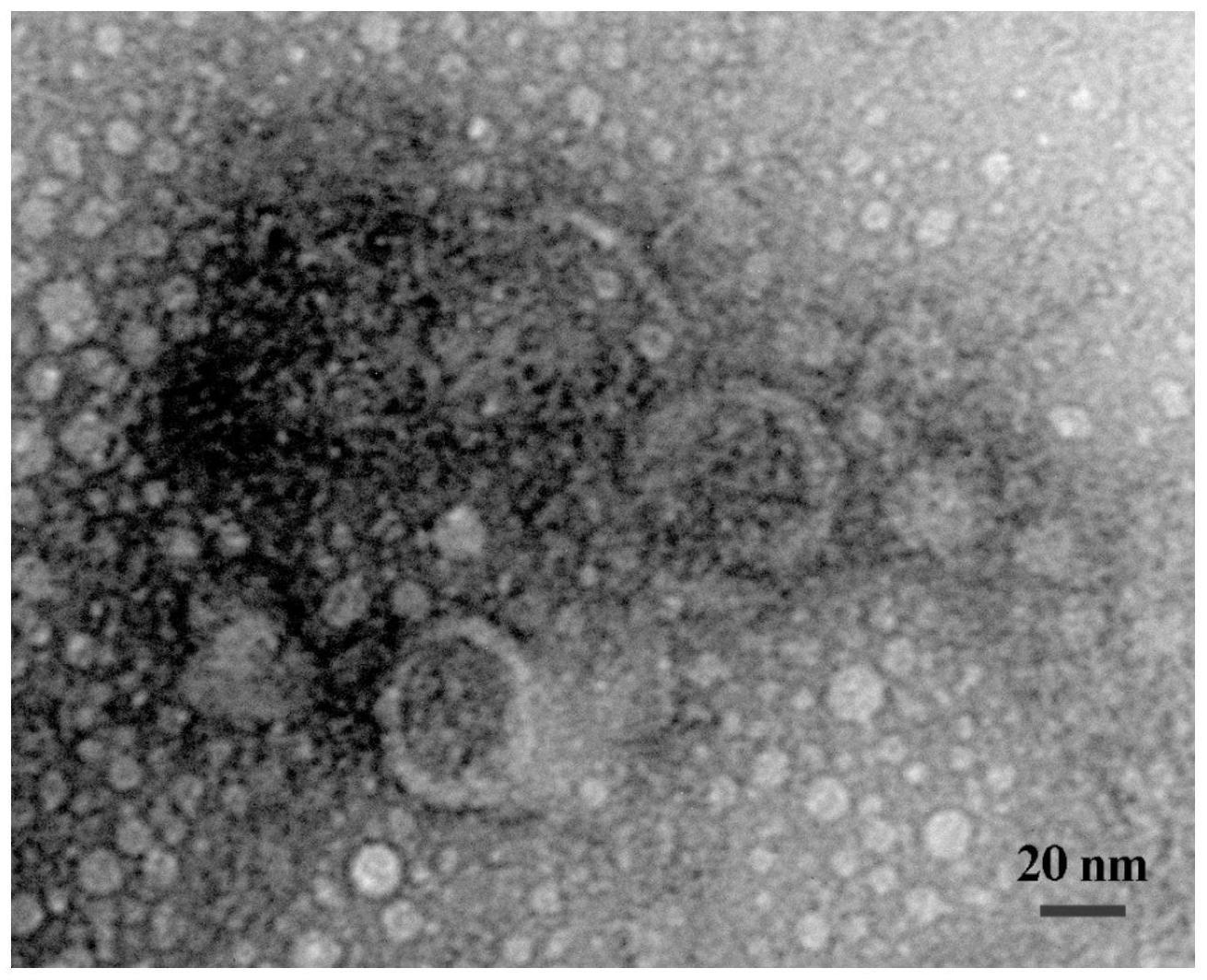
62.图1为实施例1的脂肪间充质干细胞来源的外泌体的透射电镜结果图。
63.图2为实施例1温度响应性复合水凝胶在不同温度下的状态结果图。
64.图3为实施例1温度响应性复合水凝胶在pbs缓冲液中的稳定性检测结果图。
65.图4为实施例2不同物质的核磁共振成像结果图。
66.图5为实施例3不同组分对角膜上皮缺损的荧光素钠染色结果图。
具体实施方式
67.下面结合实施例及附图对本发明作进一步详细的描述,但本发明的实施方式不限于此。
68.透明质酸购自上海源叶生物科技有限公司。
69.实施例1
70.一种温度响应性透明质酸的制备方法,包括如下步骤:
71.(1)称取2g透明质酸(ha,mw 100~150万,usp级)加入200ml去离子水,6℃低温反应器搅拌12h使其完全溶解,得溶解液;
72.(2)将步骤(1)的溶解液降低温度至0℃,用恒压漏斗逐滴滴入甲基丙烯酸酐(ma),得溶液1;其中,甲基丙烯酸酐:ha二糖单元的摩尔比=20:1;
73.(3)向步骤(2)的溶液1中逐滴滴入5m naoh溶液,维持ph在8~12之间,加入naoh溶液后反应体系由透明变为乳白色;升温至4℃继续反应12小时,得到溶液2;
74.(4)将步骤(3)的溶液2用1l无水乙醇沉淀,得到白色絮状物,加入去离子水搅拌溶解完全后,置于截留分子量为8000~12000的透析袋透析一周,每天换三次水;
75.(5)透析结束后,冷冻干燥得到白色海绵状产物,命名为hama,产物保存于
‑
20℃冰箱备用;
76.(6)称0.2g的hama加入250ml(24#)单口圆底烧瓶,加入180ml的去离子水,磁力搅拌溶解(放冰盒,控制温度不要太高),一般搅拌24小时,确保溶解充分,得到反应体系1;
77.(7)取500μl 0.5g 2
‑
甲基
‑2‑
丙烯酸
‑2‑
(2
‑
甲氧基
‑
乙氧基)乙酯(pdegma,纯度95%(w/w))加入5ml的去离子水,冰水浴溶解完全用注射器加入步骤(6)的反应体系1中,得到反应体系2;
78.(8)称40mg的过硫酸钾(k2s2o8,kps)加入5ml的去离子水,低温搅拌溶解完全,用注射器打入步骤(7)的反应体系2中;
79.(9)向步骤(8)的反应体系2中通氮气除氧1小时,得到除氧后的反应体系2;
80.(10)取200μl的四甲基乙二胺(temed)加入5ml的去离子水,除氧后加入步骤(9)的除氧后的反应体系2中;
81.(11)保持少量氮气正压,20℃反应12小时,用截留分子量为8000~12000的透析袋透析三天,第一天换3次水,第二天换2次水,第三天换一次水,得反应体系3;
82.(12)将步骤(11)得到的反应体系3冷冻干燥,即得温度响应性透明质酸,保存在4℃冰箱备用。
83.步骤(5)中,hama产率的计算方法:hama产率(%)=最终产物质量/投入总物料质量
×
100%,其中,最终产物质量是指白色海绵状产物质量;投入总物料质量是指透明质酸、甲基丙烯酸酐和naoh溶液的总质量。
84.经计算可知,hama的产率为85%。
85.脂肪间充质干细胞来源的外泌体的制备方法,包括如下步骤:
86.a)新西兰大白兔(购于广东省医学实验动物中心)使用安乐死法处死,无菌状态下取兔腹股沟皮下脂肪组织,用4℃预冷的含有双抗(100μg/ml链霉素、100μg/ml青霉素)的pbs缓冲液(ph 7.4,0.1m下同;)反复冲洗3次;
87.b)使用眼科剪和眼科镊清除筋膜和血管,4℃条件下预冷的pbs缓冲液冲洗3洗,取其中的脂肪球轻柔地转入至无菌平皿中,再向其中加入2倍体积溶解在pbs缓冲液中的1%ⅱ型胶原酶溶液(购于sigma公司),并放置在37℃培养箱中,每隔10min取出平皿轻轻摇晃,总消化时间为120min,得消化内容物;
88.c)将平皿中的消化内容物转移至50ml离心管内,紧接着等体积加入含10%fbs的
dmem/f12培养基(购于gibco公司),转速为1000r/min离心5min,弃上层脂肪,使用100目的细胞过滤筛收集下层悬液,并再次使用转速为1500r/min离心10min,收集下层沉淀物;
89.d)将所述的沉淀物加入新鲜的含10%fbs的dmem/f12培养基重悬,接种于25cm2的培养瓶中,置于37℃及5%co2恒温培养箱中培养;
90.e)待细胞长满细胞培养瓶50%面积时,换含10%无外泌体fbs的dmem/f12培养基培养,每隔2天收集细胞上清液;
91.f)将所述上清液于4℃,300
×
g,10min离心去除细胞;4℃,3000
×
g,10min离心去除死细胞;4℃,10000
×
g,30min离心去除细胞碎片;4℃,100000
×
g,70min超速离心得到外泌体沉淀;加入6ml pbs缓冲液再次4℃,100000
×
g,70min超速离心,弃上清,加入100μlpbs缓冲液重悬后,即可得到纯化后的脂肪间充质干细胞来源的外泌体,最终外泌体的浓度为100~1000μg/ml。
92.上述脂肪间充质干细胞来源的外泌体的透射电镜结果如图1所示;由图1可以看出:脂肪间充质干细胞来源外泌体形貌为茶托状,直径在30
‑
150nm之间,符合经典外泌体的特征。
93.一种温度响应性复合水凝胶的制备方法,包括以下步骤:
94.(a)在4℃条件下,将温度响应性透明质酸溶解在pbs缓冲液(ph 7.4,0.1m)中,其中,温度响应性透明质酸与pbs缓冲液的质量比为5:100,200rpm磁力搅拌过夜,得温度响应性透明质酸溶胶;
95.(b)将提前制备好的脂肪间充质干细胞来源的外泌体缓慢加入步骤(a)中的温度响应性透明质酸溶胶中,使脂肪间充质干细胞来源的外泌体在温度响应性透明质酸溶胶和脂肪间充质干细胞来源的外泌体形成的体系中的浓度维持在20μg/ml,充分混合得到包含外泌体的温度响应性透明质酸复合溶胶,即温度响应性复合水凝胶。
96.性能测试:
97.(1)温度响应性复合水凝胶由4℃至37℃的温度转变过程实验:将复合溶胶放置在4℃冰箱中维持4℃环境,倾斜拍照为溶胶,即为流动状态;在恒温37℃条件下,倾斜拍照为凝胶,即为非流动状态。
98.温度响应性复合水凝胶由4℃至37℃的温度转变过程如图2所示;从图2可知:在4℃条件下,复合溶胶为溶胶状态,而在37℃条件下为凝胶状态,表明本发明制得的温度响应性复合水凝胶具有温度响应性。
99.(2)温度响应性复合水凝胶在pbs缓冲液中的稳定性检测实验:将温度响应性复合水凝胶使用1ml注射器缓慢注射入在室温环境下的pbs缓冲液(ph 7.4,0.1m)中,可观察到溶胶完整性较好,没有与pbs缓冲液进行互溶,即说明温度响应性复合水凝胶的稳定性较好。
100.所得温度响应性复合水凝胶在pbs缓冲液中的稳定性结果如图3所示。由由图3可知:溶胶在pbs缓冲液中仍然可以保持注射器积压出的形状,证明本发明的温度响应性复合水凝胶可在生理环境中维持一个稳定的状态。
101.实施例2
102.通过核磁共振成像分别对实施例1制备得到的hama和温度响应性透明质酸溶胶进行分析。
103.hama和温度响应性透明质酸溶胶的1h nmr谱如图4所示,从图4可以看出,对比hama在5.5
‑
6.5ppm位置的双键特征峰,温度响应性透明质酸溶胶在此位置的双键特征峰消失,证明反应单体的双键反应完全。4.2ppm位置出现pdegma的特征峰(
‑
coo
‑
ch2‑
)[250],3.22ppm位置归属于pdegma末端甲基特征峰,侧链上其他亚甲基的特征峰位于3.5
‑
4.0ppm之间,证明温度响应性侧链pdegma接枝成功,温度响应性透明质酸溶胶合成成功。3
‑
4ppm之间的峰与ha二糖单元糖苷键上的10个氢的位置重叠。1ppm左右为pdegma骨架链上的氢。1.9ppm(
‑
ch3)归属于透明质酸链上的甲基和侧链骨架链上的亚甲基(
‑
ch2)。由以上结果可知,hama和温度响应性透明质酸溶胶是完全不同的材料,二者性能完全不同。
[0104]
实施例3
[0105]
使用环钻钻取直径为5.5mm的滤纸,在1m的naoh溶液中浸泡1分钟,取出放入滤纸表面,滤干表面的碱液,然后将滤纸放在新西兰大白兔(购于南方医科大学实验动物中心)眼部中心位置放置30秒,立刻弃掉滤纸并使用生理盐水对眼部进行冲洗3分钟,然后使用pbs缓冲液(ph 7.4,0.1m)、实施例1的温度响应性透明质酸(hd),脂肪间充质干细胞来源的外泌体(exo)和温度响应性复合水凝胶(hd
‑
exo)进行干预并拍照。
[0106]
荧光素钠染色结果(图5)表明:在第一天,单独使用hd,exo或hd
‑
exo表现出较好的效果,而且exo和hd
‑
exo比使用hd效果更好,在所有的组分中hd
‑
exo的愈合效果最好,证明温度响应性透明质酸和脂肪间充质干细胞来源的外泌体都对角膜上皮愈合有一定的效果,而且温度响应性复合水凝胶表现出了最佳的治疗效果。
[0107]
上述实施例为本发明较佳的实施方式,但本发明的实施方式并不受上述实施例的限制,其他的任何未背离本发明的精神实质与原理下所作的改变、修饰、替代、组合、简化,均应为等效的置换方式,都包含在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1