铁死亡相关基因在弥漫大B细胞淋巴瘤预后评估中的应用
铁死亡相关基因在弥漫大b细胞淋巴瘤预后评估中的应用
技术领域
1.本发明属于疾病预后和分子生物学技术领域,具体涉及铁死亡相关基因在弥漫大b细胞淋巴瘤预后评估中的应用。
背景技术:
2.公开该背景技术部分的信息仅仅旨在增加对本发明的总体背景的理解,而不必然被视为承认或以任何形式暗示该信息构成已经成为本领域一般技术人员所公知的现有技术。
3.弥漫大b细胞淋巴瘤(dlbcl)是源于b系淋巴细胞的一种恶性侵袭性肿瘤,占非霍奇金淋巴瘤的30
–
40%。dlbcl是一种高度异质性的淋巴肿瘤,具有基因表达谱的变异和遗传信息的改变。目前,r-chop(利妥昔单抗、环磷酰胺、阿霉素、长春新碱和泼尼松)是治疗弥漫大b细胞淋巴瘤最常见的化学免疫疗法。然而,由于dlbcl患者具有高度的异质性,60%的患者可以通过联合治疗治愈,部分患者仍然无法获得痊愈。而且,前期治疗无效或缓解后复发的患者往往预后不良。所以,为了提高dlbcl患者的预后水平,需要更多的研究来探讨dlbcl发生发展的潜在分子机制。
4.铁死亡是一种新型的细胞死亡形式,具有独特的性质和特性,且参与包括肿瘤在内的多种疾病的发生发展。2012年,研究者们首次将铁死亡区别于凋亡、坏死和自噬而作为一种新的细胞死亡形式。与自噬和凋亡不同,铁死亡是一种铁依赖、脂质过氧化介导的细胞死亡形式。研究表明,在从各种肿瘤组织中获得的肿瘤细胞中,dlbcl细胞是对铁死亡诱导剂最敏感的一种。因此,铁死亡可能是一个值得关注的参与dlbcl发生发展的重要机制。然而,迄今为止,鲜有基于铁死亡相关基因在dlbcl预后预测中的报道。
技术实现要素:
5.针对现有技术存在的不足,本发明提供铁死亡相关基因在弥漫大b细胞淋巴瘤预后评估中的应用。本发明通过筛选铁死亡相关基因,构建相关预后模型,证明其对弥漫大b细胞淋巴瘤患者的生存具有良好的预测作用,从而可用于弥漫大b细胞淋巴瘤的预后预测且用于辅助临床决策。
6.具体的,本发明涉及以下技术方案:
7.本发明的第一个方面,提供一种用于弥漫大b细胞淋巴瘤预后评估的生物标志物,所述生物标志物选自下列基因中的任意一种或多种:gclc、slc38a1、gabarapl2、epas1、capg和znf419。
8.进一步的,所述生物标志物具体为上述gclc、slc38a1、gabarapl2、epas1、capg和znf419组成的组。
9.所述预后评估具体包括对弥漫大b细胞淋巴瘤患者总生存期(os)的评估。
10.本发明的第二个方面,提供检测上述生物标志物表达水平的物质在制备产品中的应用,所述产品用于弥漫大b细胞淋巴瘤患者生存期预后评估。
11.本发明的第三个方面,提供一种产品,所述产品包含检测上述用于弥漫大b细胞淋巴瘤患者生存期预后评估的生物标志物的物质,所述产品用于弥漫大b细胞淋巴瘤患者生存期预后评估。
12.所述产品可以为试剂盒。
13.本发明的第四个方面,提供一种用于弥漫大b细胞淋巴瘤患者生存期预后评估的系统,所述系统包括:
14.i)分析单元,所述分析单元包含:用于确定受试者的待测样品中选自上述铁死亡相关基因表达水平的检测物质,以及;
15.ii)评估单元,所述分析单元包含:根据i)中确定的所述铁死亡相关基因表达水平对所述受试者进行生存预后评估;
16.其中,所述步骤i)分析单元中,所述铁死亡相关基因包括选自下列基因中的任意一种或多种:
17.gclc、slc38a1、gabarapl2、epas1、capg和znf419。
18.进一步的,所述标志物为上述gclc、slc38a1、gabarapl2、epas1、capg和znf419组成的组。
19.所述步骤ii)分析单元具体评估流程包括:根据i)中确定的所述铁死亡相关基因表达水平,基于预后模型进行生存预后评估;
20.其中,所述预后模型,其计算公式=e
(0.397*gclc表达水平+-0.204*epas1表达水平+-0.441*gabarapl2表达水平+0.329*slc38a1表达水平+-0.138*capg表达水平+0.035*znf 419表达水平)
。
21.更进一步的,
22.受试者预后模型指数高于阈值时为高表达,则指示受试者预后较差(总生存期较短);
23.受试者预后模型指数低于阈值时为低表达,则指示受试者预后较好(总生存期较长);
24.所述阈值为预后模型的评分中位数临界值。
25.本发明的第五个方面,提供一种弥漫大b细胞淋巴瘤患者预后风险评估的方法,所述方法包括使用上述生物标志物和/或上述系统进行评估;
26.所述预后风险评估包括对受试者的总生存期(os)进行预测评估。
27.以上一个或多个技术方案的有益技术效果:
28.上述技术方案基于铁死亡相关基因构建弥漫大b细胞淋巴瘤预后模型,从而对弥漫大b细胞淋巴瘤的预后进行预测评估,经试验证明,预后模型与dlbcl患者的os显著相关,高风险值的dlbcl患者的os明显短于低风险值的患者,死亡的可能性也更大,因此具有良好的预测作用,从而可用于弥漫大b细胞淋巴瘤的预后预测且用于辅助临床决策,具有良好的实际应用之价值。
附图说明
29.构成本发明的一部分的说明书附图用来提供对本发明的进一步理解,本发明的示意性实施例及其说明用于解释本发明,并不构成对本发明的不当限定。
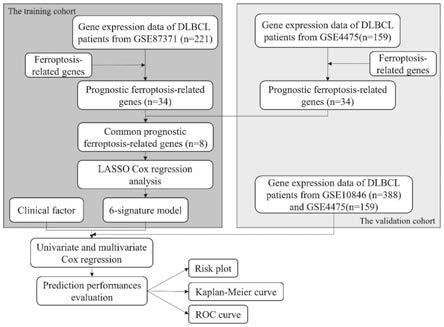
30.图1为本发明实施例中数据收集和分析的流程图。
31.图2为本发明实施例中gse87371中具有预后价值的铁死亡相关基因的筛选。a.热图显示了34个预后基因在不同coo亚型中的表达。b.从string数据库下载的ppi网络表明了候选基因之间的相互作用。c.gse87371和gse4475预后基因的venn图。d.森林图显示基因表达和os之间的单因素cox回归分析结果。
32.图3为本发明实施例中基于6个铁死亡相关基因构建lasso cox回归模型。最佳对数λ值由图中的垂直黑线表示。
33.图4为本发明实施例gse87371队列中6基因预后模型的预后分析。a.gse87371队列中风险得分的分布和中值。b.在gse87371队列中os状态、os和风险评分的分布。c.gse87371队列的主成分分析图。d.对gse87371队列的t-sne分析。e.gse87371队列中os状态、os和风险评分的分布。gse87371队列中高风险组和低风险组患者的os的生存曲线。f.时间相关roc曲线的auc验证了gse87371队列中风险评分的预后预测能力。
34.图5为本发明实施例在gse4475队列中验证6基因预后模型。a.gse4475队列中风险评分的分布和中值。b.os状态、os和风险评分在gse4475队列中的分布。c.gse4475队列的主成分分析图。d.对gse4475队列的t-sne分析。e.gse4475队列中os状态、os和风险评分的分布。gse4475队列中高风险组和低风险组患者的os的生存曲线。f.时间相关roc曲线的auc验证了gse4475队列中风险评分的预后表现。
35.图6为本发明实施例在gse10846队列中验证6基因预后模型。a.gse10846队列中风险评分的分布和中值。b.在gse10846队列中os状态、os和风险评分的分布。c.gse10846队列的主成分分析图。d.对gse10846队列的t-sne分析。e.gse10846队列中os状态、os和风险评分的分布。gse10846队列中高风险组和低风险组患者的os的生存曲线。f.时间相关roc曲线的auc验证了gse10846队列中风险评分的预后表现。
36.图7为本发明实施例中风险评分是dlbcl患者的一个独立的预后预测因子;gse87371衍生队列中关于os的a.单因素和b.多因素cox回归分析的结果。
37.图8为本发明实施例风险评分分层组中的铁死亡相关性;铁死亡相关基因在a.gse87371、b.gse4475和c.gse10846队列中高风险和低风险亚组之间表达水平的比较。*p《0.05;**p《0.01;***p《0.001;****p《0.0001。
具体实施方式
38.应该指出,以下详细说明都是例示性的,旨在对本技术提供进一步的说明。除非另有指明,本文使用的所有技术和科学术语具有与本技术所属技术领域的普通技术人员通常理解的相同含义。
39.需要注意的是,这里所使用的术语仅是为了描述具体实施方式,而非意图限制根据本技术的示例性实施方式。如在这里所使用的,除非上下文另外明确指出,否则单数形式也意图包括复数形式,此外,还应当理解的是,当在本说明书中使用术语“包含”和/或“包括”时,其指明存在特征、步骤、操作、器件、组件和/或它们的组合。下列具体实施方式中如果未注明具体条件的实验方法,通常按照本领域技术内的分子生物学的常规方法和条件,这种技术和条件在文献中有完整解释。参见例如sambrook等人,《分子克隆:实验手册》中所述的技术和条件,或按照制造厂商所建议的条件。
40.如前所述,研究发现许多基因参与调节这种新形式的细胞死亡,有些是铁死亡的
抑制因子,有些是铁死亡的驱动因子,有些是铁死亡的标志分子。研究报道称谷胱甘肽过氧化物酶4(gpx4)可以抑制铁死亡的发生,从而抑制ros诱导的dlbcl细胞的死亡。另一方面,gclc、mt1g和其他铁死亡相关基因可能参与调节肿瘤患者的预后。
41.由于弥漫大b细胞淋巴瘤的发生发展机制仍不清楚,本发明旨在阐明铁死亡相关的基因在预测dlbcl患者的总生存期中的作用。在本发明中,使用来自公共数据库的dlbcl患者的mrna表达谱和相应的临床数据,发现了与dlbcl预后密切相关的铁死亡相关基因,在geo数据库中构建和验证了用于dlbcl患者诊断和预后的分子模型。基于以上研究结果,进一步探讨了铁死亡在dlbcl发生发展中的潜在作用及机制。
42.本发明的一个典型具体实施方式中,一种用于弥漫大b细胞淋巴瘤预后评估的生物标志物,所述生物标志物选自下列基因中的任意一种或多种:gclc、slc38a1、gabarapl2、epas1、capg和znf419。
43.本发明的又一具体实施方式中,所述生物标志物具体为上述gclc、slc38a1、gabarapl2、epas1、capg和znf419组成的组。
44.本发明的又一具体实施方式中,所述预后评估具体包括对弥漫大b细胞淋巴瘤患者总生存期(os)的评估。
45.本发明的又一具体实施方式中,提供检测上述生物标志物表达水平的物质在制备产品中的应用,所述产品用于弥漫大b细胞淋巴瘤患者生存期预后评估。
46.本发明的又一具体实施方式中,提供一种产品,所述产品包含检测上述用于弥漫大b细胞淋巴瘤患者生存期预后评估的生物标志物的物质,所述产品用于弥漫大b细胞淋巴瘤患者生存期预后评估。
47.本发明的又一具体实施方式中,所述产品可以为试剂盒。
48.本发明的又一具体实施方式中,提供一种用于弥漫大b细胞淋巴瘤患者生存期预后评估的系统,所述系统包括:
49.i)分析单元,所述分析单元包含:用于确定受试者的待测样品中选自上述铁死亡相关基因表达水平的检测物质,以及;
50.ii)评估单元,所述分析单元包含:根据i)中确定的所述铁死亡相关基因表达水平对所述受试者进行生存预后评估;
51.本发明的又一具体实施方式中,所述步骤i)分析单元中,所述铁死亡相关基因包括选自下列基因中的任意一种或多种:
52.gclc、slc38a1、gabarapl2、epas1、capg和znf419。
53.进一步的,所述标志物为上述gclc、slc38a1、gabarapl2、epas1、capg和znf419组成的组。
54.所述步骤ii)分析单元具体评估流程包括:根据i)中确定的所述铁死亡相关基因表达水平,基于预后模型进行生存预后评估;
55.本发明的又一具体实施方式中,所述预后模型,其计算公式=e
(0.397*gclc表达水平+-0.204*epas1表达水平+-0.441*gabarapl2表达水平+0.329*slc38a1表达水平+-0.138*capg表达水平+0.035*znf 419表达水平)
。
56.本发明的又一具体实施方式中,受试者预后模型指数高于阈值时为高表达,则指示受试者预后较差(总生存期较短);
57.受试者预后模型指数低于阈值时为低表达,则指示受试者预后较好(总生存期较
长);
58.本发明的又一具体实施方式中,所述阈值为预后模型的评分中位数临界值。
59.本发明的又一具体实施方式中,提供一种弥漫大b细胞淋巴瘤患者预后风险评估的方法,所述方法包括使用上述生物标志物和/或上述系统进行评估;
60.所述预后风险评估包括对受试者的总生存期(os)进行预测评估。
61.以下通过实施例对本发明做进一步解释说明,但不构成对本发明的限制。应理解这些实施例仅用于说明本发明而不用于限制本发明的范围。
62.实施例
63.材料和方法
64.本研究的流程图如图1所示。
65.研究人群和数据采集
66.公开的关于dlbcl的数据可从geo数据库下载(http://www.ncbi.nlm.nih.gov/geo),(gse87371/gpl570、gse10846/gpl570和gse4475/gpl96)。患者的入组标准包括:(a)组织学诊断为dlbcl(b)完备的基因表达数据;(c)完备的生存信息。表1总结了这三个队列中患者的基线特征。来自gse87371数据集的221名患者被用作训练队列,分别来自gse10846和gse4475数据集的388名和159名患者被用作验证队列。
67.表1 本研究中dlbcl患者的临床特征
[0068][0069][0070]
frg的生成
[0071]
frg是从ferdb网站(http://www.zhou nan.org/ferdb/)下载的。用以下标准补充了frg列表(补充表1):(a)基因的抑制剂或激活剂可以调节铁死亡;(b)基因的过度表达或下调可调控铁死亡;(c)铁死亡的标志分子。本研究涉及301个基因。
[0072]
在dlbcl组织中鉴定铁死亡相关基因
[0073]
将来自frgs队列的mrna测序数据进行匹配,并使用fc》1及调整后p值《0.05的limma(r包)进行铁死亡相关基因的预后评估。将预后基因上传到string数据库(https://string-db.org/)中,构建成蛋白质-蛋白质相互作用(ppi)网络。这些基因在不同来源细胞
(coo)中的表达通过r语言中的中的“pheatmap”包以达到可视化。
[0074]
构建和验证预后相关铁死亡相关基因的模型
[0075]
通过单因素cox分析,阐明铁死亡相关基因的表达水平与dlbcl患者总生存期(os)之间的关系。在gse87371中,筛选同时具有差异表达和预后价值的铁死亡相关基因用于构建预后模型。使用基于lasso方法的“glmnet”r语言包评估生成的关键基因。应用多因素cox回归模型计算这些关键基因的回归系数。基于这些基因的多因素cox回归,我们建立了一个预后模型。根据每个基因的标准化表达水平及其相应的回归系数计算患者的风险评分。公式建立如下:得分=e
总和(每个基因的表达量
×
对应系数)
。根据风险值的中位数临界值将患者分为高风险组和低风险组。基于该模型,作为验证队列的gse4475和gse10846以相同的方式进行计算。
[0076]
统计分析
[0077]
基于模型中基因的表达,使用“统计”r包的“prcomp”功能进行主成分分析。此外,还进行了t-sne检验,用“tsne”r包探讨了不同组的分布。使用r中的“timeroc”包进行时间相关roc分析和随后的曲线下面积(auc)计算。进行单因素和多因素cox回归分析以验证独立预测因子。计算每个变量的危险比和95%置信区间。r(4.0.2版)中的“ggplot2”、“ggforest”和“venndiagram”包用于可视化。p值小于0.05被认为具有统计学意义。(*p《0.05;**p《0.01;***p《0.001;****p《0.0001)。
[0078]
结果
[0079]
来自gse87371数据集的221名患者、来自gse10846数据集的388名患者和来自gse4475数据集的159名患者被纳入本研究。这些患者的详细临床特征总结在表1中。
[0080]
在gse87371队列中筛选预后相关性铁死亡相关基因
[0081]
在不同亚型的dlbcl中,收集了301个铁死亡基因,其中34个是gse87371中的预后相关性铁死亡相关基因(均为fdr《0.05,图2a)。这些基因之间的相互作用网络表明,gabarapl2、gclc、epas1 myc是中心基因(图2b)。同样,在gse4475中有34个基因被认为与铁死亡相关。结果显示,gse87371和gse4475队列中的8个基因具有显著的预后相关性(图2c-d)。
[0082]
建立dlbcl中的预后模型
[0083]
应用lasso cox回归分析,利用上述8个基因的表达谱,构建了一个预测dlbcl患者os的预后模型。该模型基于最优值λ确定了6个基因(图3)。其中,gclc是铁死亡的抑制因子,slc38a1、gabarapl2、epas1是铁死亡的驱动因子,capg、znf419是铁死亡的标记物。风险评分计算如下:e
(0.397*gclc表达水平+-0.204*epas 1表达水平+-0.441*gabarap l2表达水平+0.329*slc38a 1表达水平+-0.138*capg表达水平+0.035*znf 419表达水平)
。根据中位数临界值,患者被分为高风险组(n=111)和低风险组(n=110)(图4a)。如图4b所示,高风险组患者的死亡概率明显高于低风险组患者。主成分分析和t-sne分析显示,不同组的患者有明显的聚集性(图4c-d)。生存曲线表明,高风险亚组患者的总生存期明显短于低风险亚组患者(图4e,p《0.001)。通过依赖于时间的roc曲线计算不同时间点的os风险评分预测性能,roc曲线由r软件绘制。如图4f所示,1年的auc达到0.736,2年的auc达到0.711,3年的auc达到0.752。
[0084]
在gse4475和gse10846队列中验证6基因预后模型
[0085]
为了在大的dlbcl患者队列中验证6基因模型的预后预测能力,通过使用来自gse87371队列的相同风险公式计算的中值来计算gse4475和gse10846数据集中的值(图5a,
6a)。与gse87371队列中的结果相似,主成分分析和t-sne表明,两个亚组的患者都聚集在gse4475和gse87371队列中(图5c-d,6c-d)。与低风险亚组相比,高风险组的患者更容易死亡,存活时间更短(图5b、5e、6b、6e,p《0.001)。同样,在gse4475队列中,auc在1年时达到0.654,2年时达到0.673,3年时达到0.661(图5f)。在gse10846队列中,1年auc为0.641,2年auc为0.651,3年auc为0.641(图6f)。
[0086]
6基因预后模型的独立预后价值
[0087]
上述分析表明,不同亚组中的dlbcl患者与6基因预后模型有密切联系。为了验证这些患者的风险评分和临床病理特征之间的关联是否可信,进行了单因素和多因素cox回归分析。在单因素回归分析中,在gse87371队列中,风险评分与os显著相关(hr=4.655,95%ci=3.435-6.309,p《0.001)(图7a)。如图7b所示,在校正其他因素后,风险评分仍为多变量cox回归中os的独立预测因子(hr=4.137,95%ci=3.007-5.693,p《0.001)。此外,这个结果在gse4475和gse10846队列中都是可变的。
[0088]
6基因预后模型的铁死亡相关性
[0089]
gse87371数据集的相关性分析揭示了风险评分和frgs之间的相关性(图8a)。gclc、slc38a1和znf419在低风险组中显著下调(p《0.001),表明它们可能是新的癌基因。同样,我们发现epas1、capg和gabarapl2在低风险组上调(p《0.001),这意味着它们可能是新的抗癌基因。在gse4475和gse10846队列中发现了相同的结果(图8b-c)。
[0090]
讨论
[0091]
一些基因可能调节药物诱导的dlbcl的铁死亡,但它们与os的相关性仍然是未知的。本发明研究结果显示,在单因素cox回归分析中,铁死亡预后模型与dlbcl患者的os显著相关。高风险值的dlbcl患者的os明显短于低风险值的患者,死亡的可能性也更大。
[0092]
本发明提出的预后模型由6个铁死亡相关基因(gclc、epas1、gabarapl2、slc38a1、capg、znf419)组成,这些基因可以大致分为三类,包括dof、sof和mof。高危亚组中的患者表现出铁死亡抑制状态,因为该亚组中的sof显著上调,而dofs下调。gclc,一种抗氧化酶和铁代谢蛋白,由nrf2转录调节,可通过在胱氨酸饥饿下维持谷氨酸稳态来抑制铁死亡。epas1在铁死亡中起重要作用,它选择性地富集铁死亡所必需的多不饱和脂质。gabarapl2可正向调节噬体载体和自噬体的形成,多项研究表明gabarapl2是铁死亡的一个新的调节分子。slc38a1曾被认为是铁死亡的驱动因素,但多项研究表明,slc38a1的高表达预示着新发急性髓系白血病患者预后不良。在本发明的研究中,slc38a1在高危dlbcl患者中有较高的表达,详细的作用机制仍需要进一步研究和探讨。至于刚刚在相关研究中提到的capg和znf419,还需要进一步研究其在铁死亡中的作用及机制。总之,铁死亡抑制因子在预后不良患者中有高表达,但在低风险患者中则相反。而且铁死亡促进因子在dlbcl患者中有相反的表达。
[0093]
总之,本发明的研究发现,高危组中的dlbcl患者具备铁死亡抑制表型,并构建了6个铁死亡相关基因的新预后模型。推导和验证队列中的研究表明该模型与os有显著相关,为dlbcl患者的预后预测提供了新的见解。
[0094]
最后应说明的是:以上所述仅为本发明的优选实施例而已,并不用于限制本发明,尽管参照前述实施例对本发明进行了详细的说明,对于本领域的技术人员来说,其依然可以对前述各实施例所记载的技术方案进行修改,或者对其中部分技术特征进行等同替换。
凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1