一种快速识别重症肺炎的检测产品
1.本发明涉及重症肺炎分子检测技术领域,具体地,一种快速识别重症肺炎的检测产品。
背景技术:
2.重症肺炎是指终末气道、肺泡和肺间质的炎症,可由病原微生物、理化因素、免疫损伤、过敏及药物所致(刘凤英,齐洁,李自喜,郁兴彩,曹秀芬主编;马青凤,王三菊,朱丽,李晓康等副主编.肺康复临床实践与护理[m].2019)。重症肺炎至今仍无普遍认同的定义,需入住icu患者可认为是重症肺炎。根据肺炎获得途径的不同,可将重症肺炎分为社区获得性重症肺炎和医院获得性重症肺炎。社区获得性重症肺炎是指在医院外罹患的感染性肺实质(含肺泡壁,即广义上的肺间质)炎症反应,包括具有明确潜伏期的病原体感染而在入院后潜伏期内发病的肺炎。医院获得性重症肺炎是指患者入院时不存在、也不处于潜伏期,而于入院48小时在医院(包括老年护理院、康复院)内发生的肺炎(梁名吉著.呼吸内科急危重症[m].2018)。
[0003]
我国制定的重症肺炎判定标准:符合下列1项主要标准或≥3项次要标准者可诊断为重症肺炎,需密切观察积极救治,并建议收住监护病房治疗。主要标准:(1)气管插管需要机械通气;(2)感染性休克积极液体复苏后仍需要血管活性药物。次要标准:(1)呼吸频率≥30次/分;(2)pao2/fio2≤250mmhg;(3)多肺叶浸润;(4)意识障碍和(或)定向障碍;(5)血尿素氮大于等于7mmol/l;(6)低血压需要积极的液体复苏。c反应蛋白(crp)为常见炎症因子,在炎症反应中异常变化;降钙素原(pct)在细菌感染的诊断中具有较高的特异性和敏感性;d-二聚体(dd)能反应机体纤溶亢进和高凝状态。但这些生物标志物仍然缺乏足够的特异性。
[0004]
1987年,john等在研究网织红细胞时,从培养的上清液中分离出一种囊泡状物质,它由多泡体限制性膜与细胞质膜融合而成脂质双层膜囊泡,在电镜下呈独特的杯状结构,命名其为外泌体。外泌体广泛存在于血液、尿液、脑脊液、关节液、腹水和羊水等体液中,其内含有大量的蛋白质及核酸类物质,可以沟通细胞交流,通过调节临近或远处的靶细胞而发挥生物学作用(崔家康.清热活血方调控外泌体mirna干预类风湿关节炎骨破坏的机制及方药优化研究[d].中国中医科学院,2020.)。外泌体mirna的功能通常可分为两种类型:一种是常规功能,即通过与靶基因的规范结合来调节接收细胞中的基因表达;另一种是配体功能,即mirna作为特定受体家族的激动剂直接与蛋白质相互作用。虽然很难完全排除外泌体其它内容物对受体细胞的影响,但mirna被认为是外泌体内关键的功能元件,细胞释放的外泌体mirna可以与相关载体一起循环到达相邻细胞和远处细胞发挥作用(武庆娟,陈恒文,高健,吴晓博,赵薇,李军.外泌体mirna在心血管疾病中的研究进展[j].中国病理生理杂志,2020,36(02):371-377.)。
[0005]
现有技术公开了肺结核的外泌体生物标志物诊断,该mirna可以很好地区分受试者是否被mtb感染。但目前还未有针对于重症肺炎的外泌体mirna检测方法。
技术实现要素:
[0006]
本发明的目的是为了克服现有技术的上述不足,提供一种快速识别重症肺炎的检测产品。本发明基于检测支气管肺泡灌洗液中外泌体mir-193a-5p的表达水平,实现快速特异性识别重症肺炎患者的检测。
[0007]
本发明的第一个目的是提供一种快速识别重症肺炎的检测产品。
[0008]
本发明的第二个目的是提供一种检测试剂盒。
[0009]
本发明的第三个目的是提供一种检测试剂。
[0010]
本发明的第四个目的是提供检测试剂盒在重症肺炎检测中的应用。
[0011]
为了实现上述目的,本发明是通过以下方案予以实现的:
[0012]
本发明采用超速离心法提取受检者支气管肺泡灌洗液中的外泌体的总rna,逆转录并合成cdna时,按照takara公司的mirna firststrand synthesis操作说明书进行。设计hsa-mir-193a-5p的特异性引物,配制rt-qpcr反应体系并进行扩增,按照2-δδct
计算各样本对应mir-193a-5p表达水平,并根据外泌体表达水平判断受检者是否为重症肺炎患者。
[0013]
因此,本发明要求保护以下内容:
[0014]
一种快速识别重症肺炎的检测产品,所述检测产品含有外泌体mir-193a-5p的表达水平检测试剂。
[0015]
优选地,所述外泌体mir-193a-5p的核苷酸序列如seq id no:1所示。
[0016]
优选地,所述外泌体mir-193a-5p为支气管肺泡灌洗液中的外泌体。
[0017]
优选地,所述检测试剂为核苷酸序列如seq id no:2所示的检测引物。
[0018]
外泌体mir-193a-5p的表达水平检测试剂在重症肺炎检测中的应用。
[0019]
一种检测试剂盒,含有权利要求1中所述的检测试剂。
[0020]
优选地,所述检测试剂盒还包括rt-qpcr的试剂。
[0021]
优选地,所述rt-qpcr的试剂为takara公司的mirna firststrand synthesis试剂盒和premix ex taq
tm
。
[0022]
所述检测试剂盒在重症肺炎检测中的应用。
[0023]
与现有技术相比,本发明具有以下有益效果:
[0024]
由于支气管肺泡灌洗液与肺组织病理生理联系最为紧密,本发明外泌体采集自支气管肺泡灌洗液;利用rt-qpcr方法高效检测重症肺炎,结合现代分子生物学技术快速准确地检测mir-193a-5p的表达水平,通过引物与靶序列特异性结合,提高了检测重症肺炎患者的准确性。基于上述方法,开发了一种快速识别重症肺炎的检测产品,该产品能够通过外泌体中mir-193a-5p的表达水平表征受试者是否患有重症肺炎,为重症肺炎的检测提供了新的思路和方法。
附图说明
[0025]
图1为rt-qpcr方法检测支气管肺泡灌洗液中外泌体mir-193a-5p表达水平的方法流程图;
[0026]
图2支气管肺泡灌洗液中外泌体中mir-193a-5p表达诊断重症肺炎的受试者工作特征曲线;
[0027]
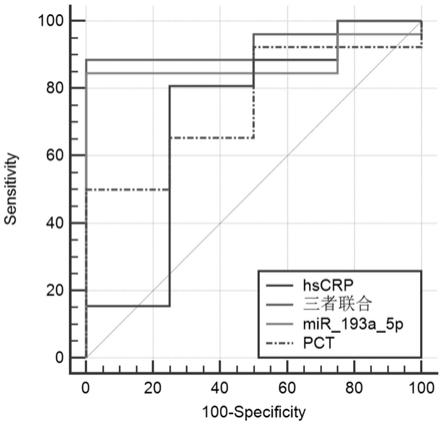
图3balf中外泌体mir-193a-5p与临床常用血清生物标志物hscrp、pct水平诊断效
果的比较。
具体实施方式
[0028]
下面结合说明书附图及具体实施例对本发明做出进一步地详细阐述,所述实施例只用于解释本发明,并非用于限定本发明的范围。下述实施例中所使用的试验方法如无特殊说明,均为常规方法;所使用的材料、试剂等,如无特殊说明,为可从商业途径得到的试剂和材料。
[0029]
实施例1引物设计
[0030]
1、实验方法
[0031]
登录网址为http://www.mirbase.org/index.shtml的mirbase数据库,得到hsa-mir-193a-5p的成熟体序列的核苷酸序列如seq id no:1所示,mirbase:》hsa-mir-193a-5p mimat0004614。
[0032]
mature sequence hsa-mir-193a-5p(seq id no:1):
[0033]5’‑
ugggucuuugcgggcgagauga-3’;
[0034]
2、实验结果
[0035]
确定了一组特异性强、灵敏度高和扩增效率高的检测外泌体中mir-193a-5p的rt-qpcr的特异引物组合,其信息如下表所示:
[0036]
表1检测外泌体中mir-193a-5p的rt-qpcr的特异引物组合信息
[0037][0038]
实施例2检测重症肺炎的试剂盒
[0039]
一、试剂盒的成分
[0040]
含有如实施例1中的表1所示的引物组合(核苷酸序列如seq id no:2所示的外泌体mir-654-5p的特异引物、来自takara公司的mirna firststrand synthesis试剂盒中的mrq3’prime、u6 forward primer和u6 reverse primer),另外还含有ddh2o、premix ex taq
tm
和takara公司的mirna firststrand synthesis试剂盒。
[0041]
二、试剂盒的使用流程
[0042]
如图1所示,为利用本试剂盒检测支气管肺泡灌洗液中外泌体mir-193a-5p表达水平的使用方法流程图,具体使用方法为:
[0043]
1.支气管肺泡灌洗液预处理
[0044]
2.超速离心法提取外泌体
[0045]
(1)将收集的支气管肺泡灌洗液置于离心管中,采用300
×
g的离心力,进行10min离心,离心结束后,弃去下层细胞,收集上清液。
[0046]
(2)将上一步收集得到的上清液转移到新的离心管中,采用14000
×
g的离心力,进行30min离心,离心结束后,弃去残留的细胞、细菌及凋亡小体等,收集上清液。
[0047]
(3)将上一步收集得到的上清液转移至超速离心管中,采用100000
×
g的离心力,
进行90min超速离心,弃去上清液,加入无菌磷酸盐缓冲盐溶液重悬沉淀,得到外泌体,置于-80℃保存备用或立即使用。
[0048]
3.提取外泌体总rna并逆转录合成cdna。
[0049]
(1)向超速离心法提取到的外泌体中加入trizol试剂,补足1ml,在15~30℃的温度下,静置5min;
[0050]
(2)取出上一步的样品,加入氯仿200μl,通过15s的涡旋振荡混匀,在室温下静置5min;在4℃的温度下,采用12000
×
g的离心力,离心15min;离心后,收取无色透明上层,即rna层备用;
[0051]
(3)收集上一步的rna层,转移到新的体积为1.5ml的离心管中,加入与上一步rna层等体积的二甲基甲醇,用来使rna分子沉淀;在15~30℃的温度下,静置5min;在4℃的温度下,采用12000
×
g的离心力,离心10min,可以清除地观察到离心管有胶状沉淀;
[0052]
(4)弃去上一步的上清液,保留胶状沉淀,加入1ml 75%乙醇,涡旋震荡混匀,在4℃温度下,采用12000
×
g的离心力,离心5min,洗涤两次后,将1.5ml的离心管打开口倒置在滤纸,从而使乙醇挥发干净;
[0053]
(5)在上一步的离心管中加入15μl焦碳酸二乙酯处理过并经高温高压消毒的milli-q纯水,以使rna沉淀溶解,用移液器吹打沉淀,在55~60℃的温度下,放置10min,以促进rna沉淀溶解;
[0054]
(6)采用nanodprop2000超微量分光光度计测定rna质量和浓度。
[0055]
(7)按照takara公司的mirna firststrand synthesis操作说明书,对提取到的外泌体rna进行逆转录合成cdna。
[0056]
4.rt-qpcr反应所用试剂及扩增程序分别如表2和3所示:
[0057]
表2 rt-qpcr实验所用试剂
[0058][0059]
表3 rt-qpcr实验扩增程序参数
[0060][0061]
5.按照2-δδct
计算各样本对应mir-193a-5p表达水平
[0062]
每个样设置三个复孔,读取各个样本的ct值,再进行2-δδct
计算。
[0063]
6.统计学分析,选定诊断界值
[0064]
使用专业统计分析软件medcalc 19.6.0处理和分析上一步计算所得的mir-193a-5p相对表达量,得到最佳诊断标准为1.49,即mir-193a-5p相对表达量大于1.49则初步判断为重症肺炎患者,需密切监测或进行影像学检查。
[0065]
实施例3诊断效果分析
[0066]
一、实验方法
[0067]
使用实施例2的检测试剂盒对7名icu内气管插管的无呼吸道感染者和28名重症肺炎患者的支气管肺泡灌洗液(balf)样品进行检测。
[0068]
二、实验结果
[0069]
结果显示,支气管肺泡灌洗液(balf)中外泌体mir-193a-5p的表达水平诊断重症肺炎的受试者工作特征(roc)曲线下面积(auc)为0.875,95%置信区间(95%ci)为0.703~0.967,标准误为0.066,p=0.001;当临界值取1.49时,灵敏度为84.62%,特异度为100%。结果如图2所示,采用受试者工作特征(roc)曲线评价外泌体mir-193a-5p对重症肺炎的诊断效果。
[0070]
实施例4诊断效果比较
[0071]
一、实验方法
[0072]
采集icu患者常用感染生物标志物:降钙素原(pct)和超敏c反应蛋白(hscrp);采集方法为:外周静脉穿刺采血方法获取患者外周血标本。检测方法和设备为:日立(日本)600型全自动生化分析仪进行检测。
[0073]
使用实施例2的检测试剂盒对患者支气管肺泡灌洗液中外泌体mir-193a-5p表达量进行rt-qpcr检测。采用受试者工作特征(roc)曲线比较所述三种生物标志物的诊断效果。
[0074]
二、实验结果
[0075]
结果显示,支气管肺泡灌洗液(balf)中的外泌体mir-193a-5p具有较高的诊断效果,其曲线下面积(auc)值为0.875,比临床常用的降钙素原(pct)和超敏c反应蛋白(hscrp)高。多指标联合诊断的曲线下面积(auc)为0.933,大于其他单项指标检测。结果见表4和图3。
[0076]
其中三者联合的具体操作如下所示:
[0077]
采用medcalc软件实现多个指标联合诊断的受试者工作特征(roc)曲线分析。
[0078]
步骤1:定义变量、建立表格:如第一列(testa)为降钙素原(pct)的值;第二列(testb)为超敏c反应蛋白(hscrp)的值;第三列(testc)为外泌体mir-193a-5p的值,为数值变量;disease为疾病状态,0为无病,1为患有重症肺炎。
[0079]
步骤2:将数据导入medcalc
[0080]
步骤3:logistic回归
[0081]
点击statistics——regression——logistic regression在logistic regression对话框中,在dependent variable框选择disease,在independent variable框中第一、二、三行分别选择testa、testb和testc。在logistic regression结果对话框中,save predicted probabilities,就把概率保存到数据集中了
[0082]
步骤4:此时数据框中多了一logregr_pred1,即testa、testb和testc通过logistic产生的预测概率值,综合反应testa、testb和testc的诊断能力,用logregr_pred1
绘制的受试者工作特征(roc)曲线即为三者的联合诊断结果。
[0083]
表4血清降钙素原(pct)、超敏c反应蛋白(hscrp)和外泌体mir-193a-5p的诊断效果
[0084][0085]
最后所应当说明的是,以上实施例仅用以说明本发明的技术方案而非对本发明保护范围的限制,对于本领域的普通技术人员来说,在上述说明及思路的基础上还可以做出其它不同形式的变化或变动,这里无需也无法对所有的实施方式予以穷举。凡在本发明的精神和原则之内所作的任何修改、等同替换和改进等,均应包含在本发明权利要求的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1