靶向Nectin-4的双环肽核素配体与探针
靶向nectin-4的双环肽核素配体与探针
技术领域
1.本发明属于核医学领域,具体地,涉及一种靶向nectin-4的双环肽核素配体,以及由该配体形成的靶向nectin-4的双环肽核素探针。
背景技术:
2.细胞粘附因子(cell adhesion molecular,cam)是一类介导细胞-细胞及细胞-细胞外基质相互作用的细胞膜表面糖蛋白分子,在介导细胞极化、分化、粘附、增殖、迁移等生理过程中有重要作用,同时也参与细胞信号转导过程。因此,cam的表达异常在一定程度上可以反映机体的病理改变。cam可大致分为选择素(selectin)家族、整合素家族(integrin)、钙黏蛋白家族(cadherin)及免疫球蛋白超家族(immunoglobulin superfamily,igsf)。大部分cam在机体中的表达不具有特异性,各组织细胞表达没有显著差异。而igsf家族的nectin-4蛋白在正常人体中仅于胚胎、胎盘、成熟上皮组织中表达,而在乳腺癌、膀胱癌等多种癌细胞表面特异性过量,已有研究证实nectin-4蛋白参与介导癌细胞凋亡抵抗、新生血管、淋巴管等多种癌症进展、转移过程,且在恶性肿瘤中的表达水平与病情的恶性程度及患者的生存密切相关。因此,nectin-4蛋白是一种高灵敏度、高特异性的癌症病灶定位显像和靶向治疗的理想生物标志物。
3.在癌症治疗药物研发领域,靶向nectin-4的人源化单克隆抗体ags-22m6与微管抑制剂(microtubule-disrupting agent monomethyl auristatin e,mmae)的抗体偶联药物enfortumab vedotin在2019年12月被fda批准为治疗晚期转移性膀胱癌的药物。但是目前在癌症早期诊断及复发患者转移灶精准定位等领域,靶向nectin-4的影像试剂开发尚在探索阶段。相比于传统影像模态,具有极高灵敏度的核医学显像手段通过配合高特异性的分子探针,能够特异、准确、无创伤地反映组织器官的功能和代谢,故开发靶向nectin-4的核医学探针对膀胱癌的诊断和精准定位具有重要的临床意义。
4.目前报道的nectin-4靶向核医学诊疗试剂的是放射性核素
89
zr及
18
f标记的nectin-4单克隆抗体(ags-22m6),但受限于单克隆抗体分子量大、在生物体内代谢时间长、血本底高、细胞膜穿透性差等缺陷,直接将单克隆抗体应用于临床常规分子影像试剂具有一定的局限性,而小分子药物在体内循环半衰期较短、组织渗透性好,在临床转化方面具有天然的优势。
技术实现要素:
5.本发明的目的是提供靶向nectin-4的双环肽核素配体与探针,本发明的发明人依托噬菌体展示技术得到的靶向nectin-4双环肽序列,进行结构优化、功能化标记、显像等一系列评估,得到可以用于nectin-4靶向的核医学小分子诊疗试剂。
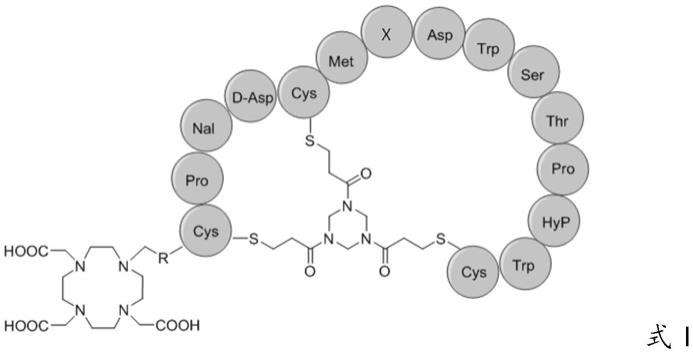
6.为了实现上述目的,本发明的第一方面提供一种靶向nectin-4的双环肽核素配体,具有式i所示结构:
[0007][0008]
其中,
[0009]
x为lys或arg;
[0010]
r为式ii、式iii、式iv或式v所示基团,
[0011][0012]
其中,a为1-5的整数,优选为1-3的整数,b为3-8的整数,优选为4-6的整数,c为1-5的整数,优选为1-3的整数。
[0013]
进一步优选地,r为式ii、式vi、式vii或式viii所示基团,
[0014][0015]
更优选地,所述双环肽核素配体为式(1)、式(2)、式(3)、式(4)或式(5)所示化合物,即本技术编号dxj187、dxj188、dxj194、dxj196、dxj204的化合物:
[0016]
[0017]
[0018][0019]
本发明的所述靶向nectin-4的双环肽核素配体可通过图2或图4所示的合成路线合成得到。
[0020]
具体地,图2合成路线的各步反应条件如下:(a)20%哌啶,1,4,7,10-四氮杂环十二烷-1,4,7,10-四乙酸三叔丁酯的dmf溶液;(b)三氟乙酸,水和三异丙基硅烷;(c)ph=8的含20%乙腈缓冲液(20mm nh4hco3,5mm edta),30℃,1h后加入10倍tata当量的半胱氨酸。
[0021]
图4合成路线的各步反应条件如下:反应条件:(a)20%哌啶的dmf溶液,fmoc-氨基酸、hbtu、hobt和eipea的dmf溶液;(b)20%哌啶,1,4,7,10-四氮杂环十二烷-1,4,7,10-四乙酸三叔丁酯(dota)的dmf溶液;(c)三氟乙酸,水和三异丙基硅烷;(d)ph=8的含20%乙腈缓冲液(20mm nh4hco3,5mm edta),30℃,2h后加入10倍tata当量的cys。
[0022]
各步骤所用原料均可商购获得或通过常规有机合成方法制得。
[0023]
本发明的第二方面提供一种靶向nectin-4的双环肽核素探针,该探针为放射性核素标记的上述靶向nectin-4的双环肽核素配体。
[0024]
本发明的所述双环肽核素探针可由所述双环肽核素配体经放射性核素标记制得,具体地,将配体溶于放射性标记缓冲液中,随后加入不同的放射性核素进行反应,得到相应的分子探针。
[0025]
根据本发明,所述放射性核素可以为诊断用放射性核素,也可以为治疗用放射性核素。
[0026]
根据本发明一些优选实施方式,所述诊断用放射性核素为
68
ga、
64
cu、
18
f、
86
y、
90
y、
89
zr、
111
in、
99m
tc、
11
c、
123
i、
125
i和
124
i中的至少一种。
[0027]
根据本发明一些优选实施方式,所述治疗用放射性核素为
177
lu、
125
i、
131
i、
211
at、
111
in、
153
sm、
186
re、
188
re、
67
cu、
212
pb、
225
ac、
213
bi、
212
bi和
212
pb中的至少一种。
[0028]
本发明的探针具有较高的肿瘤摄取以及较高的肿瘤与肌肉摄取比,良好的体内代谢性能,具有良好的临床应用前景。
[0029]
本发明的其它特征和优点将在随后具体实施方式部分予以详细说明。
附图说明
[0030]
通过结合附图对本发明示例性实施方式进行更详细的描述,本发明的上述以及其它目的、特征和优势将变得更加明显。
[0031]
图1示出了dxj187的结构式。
[0032]
图2示出了dxj187的制备总路线。
[0033]
图3示出了dxj188、dxj194、dxj196、dxj204的总结构式(a)和具体结构式(b)。
[0034]
图4示出了dxj188、dxj194、dxj196、dxj204的制备总路线。
[0035]
图5-1至5-5分别示出了dxj187、dxj188、dxj194、dxj196、dxj204的质谱图。
[0036]
图6示出了
68
ga标记的dxj187、dxj188、dxj194、dxj196、dxj204在注射后1h及2h的荷瘤小鼠pet图。
[0037]
图7示出了
177
lu-dxj188在荷瘤裸鼠体内的spect成像和生物分布。左图为实验组荷瘤鼠注射
177
lu-dxj188 2小时后的spect/ct图像,右图为抑制组荷瘤鼠共注射冷配体及
177
lu-dxj188 2小时后的spect/ct图像。
具体实施方式
[0038]
下面将更详细地描述本发明的优选实施方式。虽然以下描述了本发明的优选实施方式,然而应该理解,可以以各种形式实现本发明而不应被这里阐述的实施方式所限制。
[0039]
nectin-4靶向配体合成
[0040]
配体dxj187的制备
[0041]
dxj187的具体结构如图1所示。化合物dxj187的合成步骤如图2所示,前体多肽树脂187resin购于上海楚肽生物科技公司,其他试剂购买于试剂公司,未经纯化。购得的树脂与1,4,7,10-四氮杂环十二烷-1,4,7,10-四乙酸三叔丁酯偶联后脱除保护基,随后与环化连接子tata反应得到化合物187。上述dota-nectin 4配体(dxj187)合成路线如图2所示。反应条件:(a)20%哌啶,1,4,7,10-四氮杂环十二烷-1,4,7,10-四乙酸三叔丁酯的dmf溶液;(b)三氟乙酸,水和三异丙基硅烷;(c)ph=8的含20%乙腈缓冲液(20mm nh4hco3,5mm edta),30℃,1h后加入10倍tata当量的半胱氨酸。
[0042]
取一定质量的树脂(70mg)于10ml固相合成管,加入2ml二氯甲烷(dcm)溶胀,重复三次,每次5分钟,随后用n,n-二甲基甲酰胺(dmf)洗涤三次,每次5分钟。使用含20%哌啶的dmf溶液(v/v)脱去氨基保护基fmoc,具体操作为2ml 20%哌啶的dmf溶液反应2分钟、10分钟、10分钟,随后使用2ml dmf洗涤3-5次,每次2分钟。相对于树脂(70mg)6倍化学量的1,4,7,10-四氮杂环十二烷-1,4,7,10-四乙酸三叔丁酯经7.2倍化学量的hbtu活化后加入到合成管中,电磁搅拌下反应1小时。配体从树脂上解离和叔丁酯、三苯甲基的脱去使用5ml三氟乙酸/三异丙基硅烷/水(95:2.5:2.5,v/v/v),搅拌2小时后收集滤液,并用2ml三氟乙酸清洗树脂,收集所有滤液,经减压除去三氟乙酸后,经hplc反向制备得到化合物2。取4.5mg化合物2溶于5ml的ph=8的含20%乙腈缓冲液(20mm nh4hco3,5mm edta),加入1.3mg tata(1,3,5-三丙烯酰基六-1,3,5-三嗪),在30℃反应1小时后,加入10倍于tata当量的半胱氨酸,在30℃反应10分钟以终止环化反应。经hplc反向制备,冻干后得到目标配体dxj187。配体结构经质谱鉴定,如图3-1所示。
[0043]
配体dxj188、dxj194、dxj196、dxj204的制备
[0044]
dxj188,194,196,204的具体结构如图3所示,合成步骤如图4所示。前体多肽树脂188resin购于上海楚肽生物科技公司,其他试剂购买于试剂公司,未经进一步纯化。购得的树脂脱去笏甲氧羰基(fmoc)后直接与1,4,7,10-四氮杂环十二烷-1,4,7,10-四乙酸三叔丁
酯(dota)偶联(dxj188);或与笏甲氧羰基(fmoc)保护的8-氨基辛酸(dxj194)、肌氨酸(dxj196)、4-氨甲基苯甲酸(dxj204)偶联,随后与1,4,7,10-四氮杂环十二烷-1,4,7,10-四乙酸三叔丁酯(dota)偶联;最后脱除保护基,与环化连接子tata反应得到化合物dxj188、dxj194、dxj196、dxj204。
[0045]
图4示出了dxj188、dxj194、dxj196、dxj204的制备总路线。反应条件:(a)20%哌啶的dmf溶液,fmoc-氨基酸、hbtu、hobt和eipea的dmf溶液;(b)20%哌啶,1,4,7,10-四氮杂环十二烷-1,4,7,10-四乙酸三叔丁酯(dota)的dmf溶液;(c)三氟乙酸,水和三异丙基硅烷;(d)ph=8的含20%乙腈缓冲液(20mm nh4hco3,5mm edta),30℃,2h后加入10倍tata当量的cys。
[0046]
dxj188/194/196/204的合成:
[0047]
取一定质量的树脂(70mg)于10ml固相合成管,加入2ml二氯甲烷(dcm)溶胀,重复三次,每次5分钟,随后用n,n-二甲基甲酰胺(dmf)洗涤三次,每次5分钟。使用含20%哌啶的dmf溶液(v/v)脱去氨基保护基fmoc,随后氨基酸linker的偶连依照标准的fmoc固相合成法进行,hbtu活化的dota三叔丁酯偶连,并继续使用含20%哌啶的dmf溶液(v/v)脱去氨基保护基fmoc。具体操作为2ml 20%哌啶的dmf溶液反应2分钟、10分钟、10分钟,随后使用2ml dmf洗涤3-5次,每次2分钟。相对于树脂(70mg)6倍化学量的1,4,7,10-四氮杂环十二烷-1,4,7,10-四乙酸三叔丁酯(dota)经7.2倍化学量的hbtu活化后加入到合成管中,电磁搅拌下反应1小时。配体从树脂上解离和叔丁酯、三苯甲基和2,2,4,6,7-五甲基二氢苯并呋喃-5-磺酰基的脱去使用5ml三氟乙酸/三异丙基硅烷/水(95:2.5:2.5,v/v/v)搅拌2小时完成后收集滤液,并用2ml三氟乙酸清洗树脂,收集所有滤液,经减压除去三氟乙酸后,得到化合物11/12/13/14。取4.5mg化合物11/12/13/14溶于5ml的ph=8的含20%乙腈缓冲液(20mm nh4hco3,5mm edta),加入1.3mg tata,在30℃反应1小时后,加入10倍tata当量的半胱氨酸,在30℃反应10分钟以终止环化反应。经hplc反向制备,冻干后得到目标配体dxj188/194/196/204。配体结构经质谱鉴定。
[0048]
质谱鉴定结果汇总于表1,dxj188、dxj194、dxj196、dxj204的质谱图分别如图5-2至5-5所示。
[0049]
表1化合物dxj188、dxj194、dxj196、dxj204的质谱结果汇总
[0050][0051]
标记与质控
[0052]
标记:
[0053]
68
ga:精确称取一定质量配体,加入一定体积的dmso(二甲基亚砜)溶解至浓度为20μg/μl的溶液。吸取4μl配体溶液和130μl naoac溶液(1mol/l)于西林瓶中,加入2ml新淋洗得到的
68
ga
3+
离子溶液(溶剂为0.05mol/l的盐酸溶液,放射活度为7-10mci),摇匀后密封,在95℃下反应10分钟。反应液冷却至室温后经radio-tlc分析质控。
[0054]
177
lu:精确称取一定质量配体,加入一定体积的dmso(二甲基亚砜)溶解至浓度为20μg/μl的溶液。取5μl dxj188溶液溶于20μl 1mol/l的醋酸钠溶液中;以0.05m的盐酸溶液将
177
lucl3溶液稀释至300μl于反应瓶中;将两种溶液混合后在95℃下反应10分钟。反应液冷却至室温后经radio-tlc分析质控。
[0055]
质控:
[0056]
68
ga及
177
lu标记的配合物的放射化学纯度使用radio-tlc(放射性薄层色谱仪)测定。先将10μl饱和edta(乙二胺四乙酸)溶液与5μl反应液混合,取混合液点至itlc-sg层析版,展开剂为生理盐水(0.9%nacl),所有配合物的放射化学纯度均大于95%,未经纯化即进行下一步研究。
[0057]
68
ga/
177
lu标记产物的显像
[0058]
取0.1ml新制备的
68
ga标记配合物(5.6mbq-7.4mbq)经尾静脉注射到雌性荷sw780肿瘤的balb/c裸鼠体内(肿瘤直径为1.0cm左右),分别在1h和2h后用异氟烷麻醉,进行小动物pet/ct(super-nova,平生科技,中国)显像,对感兴趣区域进行标准摄取值suv的勾画。
[0059]
实验组取0.1ml新制备的
177
lu-dxj188(18.5mbq)经尾静脉注射到雌性荷sw780肿瘤的balb/c裸鼠体内;在
177
lu-dxj188的抑制实验中,将100μg冷的dxj188配体与活度为18.5mbq的
177
lu-dxj188经小鼠尾静脉共注射注射放射性配合物与实验组一起经异氟烷麻醉在注射后2h进行spect/ct静态显像。
[0060]
如图6和表2所示,
68
ga配合物
68
ga-dxj187、
68
ga-dxj188、
68
ga-dxj194、
68
ga-dxj196和
68
ga-dxj204均能在肿瘤区域明显浓集,主要经肾脏排泄出体外,非靶器官清除迅速。随时间延长,配合物在肿瘤与肌肉的摄取比值增加。其中
68
ga-dxj204在肿瘤中拥有最高的suvmax值,在注射1h和2h时,分别为1.00
±
0.25和1.01
±
0.26。
68
ga-dxj188在肿瘤中有着较高的摄取,在肌肉中的摄取最低,其在肿瘤与肌肉的摄取比值达到最高,在注射1h和2h时,肿瘤与肌肉的比值分别为10.21
±
1.15和10.64
±
1.35。这两种配体具有更好的临床应用前景。
[0061]
图7是
177
lu-dxj188在实验组和抑制组荷瘤鼠体内的spect/ct显像结果,通过对肿瘤及正常肌肉区域的圈画定量分析可知,
177
lu-dxj188在肿瘤中有着较高的摄取,在肌肉中的摄取最低,其在肿瘤与肌肉的摄取比值在注射2h时达到6.92。
[0062][0063]
以上已经描述了本发明的各实施例,上述说明是示例性的,并非穷尽性的,并且也不限于所披露的各实施例。在不偏离所说明的各实施例的范围和精神的情况下,对于本技
术领域的普通技术人员来说许多修改和变更都是显而易见的。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1