用于阻遏TAU表达的锌指蛋白转录因子的制作方法
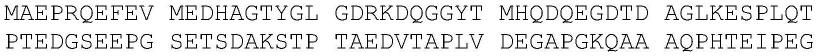
用于阻遏tau表达的锌指蛋白转录因子
1.对相关申请的交叉引用
2.本技术要求2020年1月22日提交的美国临时申请62/964,501的优先权。上述临时申请的内容通过引用其整体并入本文。
3.序列表
4.本技术含有序列表,该序列表已经以ascii格式电子提交,并通过引用整体并入本文。所述ascii副本创建于2021年1月19日,命名为025297_wo016_sl.txt,并且大小为304,337字节。
5.发明背景
6.微管相关蛋白tau(mapt),也称为tau,在某些脑病理学中起重要作用。错误折叠的tau聚集成神经原纤维缠结(nft)和其他病理性tau包涵物牵涉许多神经退行性疾病,统称为tau蛋白病。这些包括阿尔茨海默病(ad)、额颞叶痴呆(ftd)、进行性核上性麻痹(psp)、难治性遗传性癫痫(例如dravet综合征)、创伤性脑损伤(tbi)、皮质基底节变性(cbd)和慢性创伤性脑病(cte)。参见,例如,benussi et al.,front aging neurosci.(2015)7:171;gheyara et al.,ann neurol.(2014)76:443-56;scholz and bras,int j mol sci.(2015)16(10):24629-55;和mckee et al.,brain pathol.(2015)25(3):350-64。
7.已经表明tau具有朊病毒样特性。几项研究显示,tau的过度磷酸化可以导致tau错误折叠。错误折叠的tau聚集体可以扩散遍及脑(takeda et al.,nat comm.(2015)6:8490;hyman,neuron(2014)82:1189;de calignon et al.,neuron(2012)73:685-97)。这些聚集体可能是在tau蛋白病中发现的nft形成的初始步骤。尽管nft在ad早期仅限于内嗅皮层和内侧颞叶,但等到出现严重的临床症状,nft在整个脑中广泛遍布。在患有ad的患者中发现nft和β淀粉样蛋白斑块,并且已显示淀粉样蛋白沉积增加tau病理学和远端脑区中的沉积(bennett et al.,am j pathol.(2017)187(7):1601-12)。区域tau累积和扩散与啮齿动物模型和人疾病中的神经元损失密切相关(pooler et al.,acta neuropathol commun.(2015)3:14;la joie et al.,sci transl med.(2020)。除了聚集的tau的累积产生的神经毒性外,tau的可溶性寡聚形式似乎也具有毒性(guerrero-munoz et al.,front cell neurosci.(2015)9:464)。可溶性错误折叠的内源性tau似乎在各种神经元应激条件下作为神经毒性的介质发挥作用。
8.已显示内源性tau的减少对不同遗传小鼠模型中的ad样病理学有益(roberson et al.,science(2007)316:750-4;devos et al.,sci translmed.(2017)9(374):eaag0481;wegmann et al.,embo j.(2015)1-14)。降低脑中的tau水平似乎也可以保护免受应力诱导和癫痫发作诱导的神经元损伤,以及免受因创伤性脑损伤导致的学习和记忆缺陷(lopes et al.,pnas(2016)113:e3755-63;gheyara,,同上;devos et al.,jneurosci.(2013)33(31):12887-97;cheng et al.,plos one(2014)9(12):e115765)。然而,目前还没有对tau蛋白病的有效治疗。已通过施用结合tau mrna并阻止其翻译的反义寡核苷酸(aso)(devos(2017)同前;devos et al.,neurotherapeutics(2013)10(3):486-97)或通过静脉注射抗tau抗体(asuni et al.,jneurosci.(2007)27:9115-29;ittner et al.,jneurochem.
(2015)132:135-45;herrmann et al.,j neurochem.(2015)132:1-4;yanamandra et al.,neuron(2013)80(2):402-14)来实现体内tau敲低。尽管这两种方法均可以促进脑中tau蛋白的减少,但它们需要在患者的一生中长期施用。抗体具有差的血脑屏障和细胞膜通透性,这可能限制它们在中枢神经系统内的扩散以及它们接合神经元内tau的能力。此外,抗tau抗体治疗剂的开发一直很困难,因为致病性tau种类的身份和数量目前是未知的,并且在tau蛋白病中可能变化。
9.鉴于tau在脑病理学中的显著作用和有效治疗的缺乏,迫切需要开发靶向这种蛋白质的治疗剂用于预防和治疗tau蛋白病,包括ad。
技术实现要素:
10.本公开提供了靶向人mapt基因中或附近的位点的锌指蛋白(zfp)。本公开的zfp可以与转录因子融合以在dna水平上特异性抑制微管相关蛋白tau(mapt)基因的表达。这些融合蛋白含有(i)与mapt基因中的靶区特异性结合的zfp结构域和(ii)至少一个减少基因转录的转录阻遏物结构域。
11.在一个方面,本公开提供了融合蛋白,其包含锌指蛋白(zfp)结构域和转录阻遏物结构域,其中zfp结构域结合至人mapt基因的靶区。在一些实施方案中,靶区在mapt基因中的转录起始位点(tss)的1.5kb内,例如,在mapt基因的tss上游的1000bp内,和/或tss下游的500bp内。
12.在一些实施方案中,zfp结构域包含一个或多个(例如,一个、两个、三个、四个、五个、六个或更多个)锌指,并且融合蛋白任选地阻遏mapt基因的表达至少约40%、75%、90%、95%或99%,任选地没有或具有最小的通过众所周知的方法可检测的脱靶结合或活性(例如,与不是mapt基因的基因结合)。本zfp的dna结合识别螺旋氨基酸序列的非限制性实例显示于图14或图16中。在一些实施方案中,融合蛋白包含图14或图16中所示的一个或多个识别螺旋序列。在进一步的实施方案中,融合蛋白包含图14或图16中单行中所示的一些或全部识别螺旋序列,具有或不具有图16中所示的指定主链突变。在某些实施方案中,融合蛋白包含图15或图17中所示的氨基酸序列。
13.在一些实施方案中,本融合蛋白的转录阻遏物结构域包含krab结构域,其中krab结构域任选地来自人kox1蛋白。在一些实施方案中,zfp结构域通过肽接头与转录阻遏物连接。在一些实施方案中,融合蛋白包含核定位信号。
14.在一些实施方案中,融合蛋白的zfp结构域包含图14或图16的单行中所示的四个、五个或六个锌指识别螺旋序列;结合至图14或图16中所示的靶序列;包含图15或图17中所示zfp转录因子的锌指识别螺旋序列(例如,zfp-tf 71377、71385、73034、73122、73131或73133);和/或包含如图14、图15、图16或图17中所示连接的锌指识别螺旋序列(例如,zfp-tf 71377、71385、73034、73122、73131或73133)。
15.在特定的实施方案中,本融合蛋白包含选自seq id no:89-196、197-248和267-307的氨基酸序列。
16.另一方面,本公开提供了核酸构建体,其包含本融合蛋白的编码序列,其中编码序列与转录调节元件可操作地连接。在一些实施方案中,转录调节元件是在脑细胞中具有组成型活性或可诱导的哺乳动物启动子。在某些实施方案中,构建体是重组病毒构建体,诸如
重组腺相关病毒(aav)构建体。
17.在另一个方面,本公开提供了包含本核酸构建体的宿主细胞。宿主细胞可以是人细胞,诸如人脑细胞或多能干细胞(例如,胚胎干细胞或诱导型多能干细胞(ipsc))。
18.在又一方面,本公开提供抑制人脑细胞(例如,神经元、胶质细胞、室管膜细胞、神经上皮细胞、内皮细胞或少突胶质细胞)中tau表达的方法,其包括任选地通过引入本文的核酸构建体,将本文的融合蛋白引入至细胞中,从而抑制细胞中tau的表达。在一些实施方案中,细胞在患有或有风险发展阿尔茨海默病、额颞叶痴呆、进行性核上性麻痹、创伤性脑损伤(tbi)、癫痫发作病症、皮质基底节变性(cbd)、慢性创伤性脑病(cte)或另一种tau蛋白病的患者的脑中。在特定实施方案中,该方法包括将表达融合蛋白的重组病毒(例如,神经营养血清型或假型诸如aav9等的重组aav)引入至细胞中。
19.在一个相关方面,本公开提供了治疗患者的tau蛋白病(例如,减缓其进展)的方法,其包括向患者施用编码本文的融合蛋白的重组aav。在一些实施方案中,aav经由静脉内、鞘内、大脑内、脑室内、小脑延髓池内、海马内、丘脑内或实质内途径引入患者。在一些实施方案中,tau蛋白病是阿尔茨海默病或额颞叶痴呆、进行性核上性麻痹、创伤性脑损伤(tbi)、癫痫发作病症、皮质基底节变性(cbd)或慢性创伤性脑病(cte)。
20.本文还提供了用于本文所述的治疗方法中的融合蛋白,以及本文的融合蛋白用于制备治疗方法中的药物的用途。
21.本发明的其他特征、目的和优点在下面的详细描述中是显而易见的。然而,应该理解的是,详细描述虽然指示了本发明的实施方案和方面,但仅以说明的方式给出而不是限制。根据详细描述,本领域技术人员将清楚本发明范围内的各种变化和修改。
22.附图简述
23.图1是例示工程化的6指锌指蛋白转录因子(zfp-tf)特异性靶向mapt基因的示图,其识别基因中的18个碱基对。zfp-tf与基因的结合导致mapt转录减少,其进而导致mapt mrna和tau蛋白水平降低。该图公开了seq id no:308。
24.图2是例示抗tau zfp-tf靶向mapt基因的示图。初级mapt mrna显示在顶部条中,外显子1由粗箭头表示。基因和mrna下方簇中的小五边形(370;橙色和蓝色)描绘了由本文举例的代表性zfp-tf靶向的mapt基因中区域。蓝色五边形描绘了特异性靶向人mapt基因的zfp-tf,而橙色五边形靶向人和非人灵长类动物(nhp)mapt基因。指向右侧的五边形指示zfp-tf结合基因的有义链。指向左侧的五边形指示zfp-tf结合基因的反义链。
25.图3是显示选自370个zfp-tf的文库(图14)的48个zfp-tf的tau阻遏活性的一组曲线图。每个曲线图中的y轴是归一化至两个管家基因(atp5b和eif4a2)的几何均值的tau mrna表达,并在用编码sk-n-mc细胞中的不同zfp-tf的mrna转染20小时后进行评估。mrna剂量从左到右增加(3、10、30、100、300和1,000ng)。条代表四个技术重复的均值,并且误差条代表标准偏差。曲线图下方的数字是zfp-tf的内部参考编号。放大型式的滴定标尺显示在图的右下方。
26.图4是例示用于改善亲本zfp-tf的靶标特异性的优化策略的示图。它涉及在亲本zfp-tf的多达三个锌指模块中的位置(-4)、(-5)、(-9)和/或(-14)处将精氨酸(r)残基突变为谷氨酰胺(q)。该突变影响锌指和靶dna的磷酸主链之间保守的非特异性接触。
27.图5a和5b是例示mapt基因中的突变抗tau zfp-tf的靶区的示图。mapt mrna显示
为红色条。在图5a中,基因下方第一簇中的小五边形(红色和白色)描绘了mapt基因中由亲本zfp-tf靶向的区域。基因下方第二簇中的小五边形(红色)描绘了mapt基因中由亲本zfp-tf的r
→
q变体靶向的区域。图5b显示了mapt基因中代表性亲本和突变zfp-tf的靶区的放大图。橙色五边形代表亲本zfp-tf,并且红色五边形代表其r
→
q变体。指向右侧的五边形指示zfp-tf结合基因的有义链。指向左侧的五边形指示zfp-tf结合基因的反义链。亲本zfp-tf用71###编号,而突变zfp-tf用73###编号。图5b按出现顺序分别公开了seq id no:309-311。
28.图6是显示来自约340个变体文库的代表性r
→
q变体zfp-tf(图16)的tau阻遏活性的一组曲线图。每个曲线图中的y轴是归一化至两个管家基因(atp5b和eif4a2)的几何均值的tau mrna表达,并在用编码sk-n-mc细胞中的不同zfp-tf的mrna转染20小时后进行评估。mrna剂量从左到右增加(3、10、30、100、300和1,000ng)。对于每个亲本zfp-tf,显示多达七个r
→
q变体。条代表四个技术重复的均值,并且误差条代表标准偏差。曲线图下方的数字是zfp-tf的内部参考编号。放大型式的滴定标尺显示在图的右下方。
29.图7a是显示代表性zfp-tf在人ipsc衍生神经元中的tau阻遏活性的一组曲线图。y轴是归一化至三个管家基因(atp5b、eif4a2和gapdh)的几何均值的tau mrna表达,并对于人ipsc衍生神经元中的不同zfp-tf,在用aav6转导32天后进行评估。使用的aav6的量在右下角的图例中指示,aav6剂量从左到右增加(1e3、3e3、1e4、3e4、1e5和3e5的moi)。用配制剂缓冲液(模拟品)处理的神经元用作阴性对照。条代表四个技术重复的均值,并且误差条代表标准偏差。
30.图7b是比较代表性r
→
q变体zfp-tf在人ipsc衍生神经元、人sk-n-mc细胞和原代小鼠神经元中的人tau阻遏活性的一组曲线图。y轴是归一化至管家基因atp5b、eif4a2和任选地gapdh的几何均值的tau mrna表达,并且对于人ipsc衍生神经元和原代小鼠神经元中的不同zfp-tf,分别在用aav6转导后32天和7天进行评估;或在用编码sk-n-mc细胞中的不同zfp-tf的mrna转染20小时后进行评估。使用的aav6或mrna的量在x轴下方指示,aav6(1e3、3e3、1e4、3e4、1e5和3e5的moi)和mrna(3、10、30、100、300和1,000ng)剂量从左到右增加。条代表四个技术重复的均值,并且误差条代表标准偏差。放大型式的滴定标尺显示于图下方。对于在原代小鼠神经元中测试的每个zfp,人mapt中的靶序列与小鼠mapt中的直系同源靶位点之间的错配数显示在条形上方。
31.图8是affymetrix/微阵列数据的一组火山/散点图,其显示在用代表性r
→
q变体zfp-tf处理后,人ipsc衍生神经元和原代小鼠神经元的转录组分别在19天或7天后的变化。蓝色矩形指示在神经元中测试的最高剂量下,用每个代表性zfp-tf实现的人tau阻遏的水平。以红色和绿色显示的数字分别指示下调和上调的脱靶基因的计数。黄色圆圈代表tau基因座内的不同转录物;红色圆圈代表下调的脱靶基因;绿色圆圈代表上调的脱靶基因。人和小鼠微阵列数据衍生自至少两个独立实验和每个实验5-8个生物学重复。显示了cpne6是参考zfp的人工产物,并因此从脱靶计数中排除。
32.图9是显示代表性r
→
q变体zfp-tf对tau基因座(人tau和sth)和脱靶基因(cpne6和igf2)内转录物表达水平的影响的一组曲线图。模拟品处理和不与tau基因座结合的zfp-tf用作阴性对照。y轴是归一化至三个管家基因(atp5b、eif4a2和gapdh)的几何均值的mrna表达,并在编码人ipsc衍生神经元中的不同zfp-tf的mrna转染32天后进行评估。使用的
aav6的量在右下角的图例中指示,aav6剂量从左到右增加(1e3、3e3、1e4、3e4、1e5和3e5的moi)。蓝色矩形指示在神经元中测试的最大剂量下,每个代表性zfp-tf实现的人tau阻遏的水平。条代表四个技术重复的均值,并且误差条代表标准偏差。
33.图10是显示在c57bl/6小鼠中实质内(ipa)递送编码代表性r
→
q变体zfp-tf的aav9后zfp-tf、小鼠mapt、neun和神经炎性标志物mrna表达水平的一组曲线图。每个曲线图中的y轴是用在人突触蛋白1启动子下编码zfp-tf的aav9(剂量-每半球3e10vg)处理后四周,从成年小鼠的脑的右半球获得的海马组织中zfp-tf、mapt、gfap、iba1和neun的绝对或归一化mrna表达水平。媒介物处理(veh)和用编码gfp的zfp-tf处理用作阴性对照。使用的zfp-tf在x轴中指示。彩色条代表来自四只小鼠的值的均值,并且误差条代表标准偏差。每个图中的箭头指示其他组的值所归一化至的组。
34.图11是显示在htau小鼠中实质内(ipa)递送编码代表性r
→
q变体zfp-tf或阳性对照zfp-tf构建体(57890-t2a-65918)的aav9后,zfp-tf、人mapt、小鼠mapt、人sth、gfp、neun和神经炎性标志物mrna表达水平的一组曲线图。每个曲线图中的y轴是用在人突触蛋白1启动子下编码zfp-tf的aav9(剂量-每半球3e9、1e10或3e10vg)处理后3或6个月,从成年小鼠的脑的右半球获得的海马组织中zfp-tf、人mapt、小鼠mapt、人sth、gfp、gfap、iba1和neun的绝对或归一化mrna表达水平。媒介物处理(veh)用作阴性对照。评估的zfp-tf、剂量和时间点在x轴上指示。彩色条代表来自每组5-8只小鼠的值的均值,并且误差条代表标准偏差。
35.图12是显示在htau小鼠中实质内(ipa)递送编码代表性r
→
q变体zfp-tf或阳性对照zfp-tf构建体(57890-t2a-65918)的aav9后,人tau蛋白水平的曲线图。每个曲线图中的y轴是用在人突触蛋白1启动子下编码zfp-tf的aav9(剂量-每半球3e9、1e10或3e10vg)处理后3或6个月,从成年小鼠的脑的右半球获得的海马组织中的绝对或归一化总tau蛋白水平。媒介物处理(veh)用作阴性对照。评估的zfp-tf、剂量和时间点在x轴上指示。彩色条代表来自每组5-8只小鼠的值的均值,并且误差条代表标准偏差。
36.图13是来自多路复用原位杂交/免疫荧光染色的一组图像,其显示了在htau小鼠中实质内(ipa)递送编码代表性r
→
q变体zfp-tf的aav9后的人mapt转录物、neun蛋白和dapi。用在人突触蛋白1启动子下编码zfp-tf的aav9(剂量-每半球3e9vg)处理后3个月,显示了来自成年小鼠的脑的左半球的海马区的代表性图像。媒介物处理(veh)用作阴性对照。
37.图14是显示本公开的示例性zfp的表。以大写字母显示的是dna结合识别螺旋序列的基因组靶序列(即结合序列),其对于所示的每四个、五个或六个指zfp(即f1-f4、f1-f5或f1-f6)在单个行中显示。对于所示每个zfp,该图还指示了如表1中所示的锌指之间以及zfp结构域与阻遏物结构域之间的示例性肽接头序列(即l1、l2、l3、l4、l5或l6)。每个序列的seq id no显示在括号中。
38.图15是显示包含图14中所示zfp的zfp-tf的例示性全蛋白质序列的表。dna结合识别螺旋序列以粗体显示。锌指接头带有下划线,而域间接头带有双下划线。每个序列的seq id no显示在括号中。
39.图16是显示本公开的示例性r
→
q zfp的表。以大写字母显示的是dna结合识别螺旋序列的基因组靶序列(即结合序列),其对于所示的每四个、五个或六个指zfp(即f1-f4、f1-f5或f1-f6)在单个行中显示。对于所示每个zfp,该图还显示了如表1中所示的锌指之间以及zfp结构域与阻遏物结构域之间的示例性肽接头序列(即l1、l2、l3、l4、l5或l6)。符号“^”指示在指定指中第1氨基酸上游第4位的精氨酸(r)残基变为谷氨酰胺(q)。每个序列的seq id no显示在括号中。
40.图17是显示包含图16中所示zfp的r
→
q zfp-tf的例示性全蛋白质序列的表。dna结合识别螺旋序列以粗体显示。锌指接头带有下划线,而域间接头带有双下划线。每个序列的seq id no显示在括号中。
41.发明详述
42.本公开提供了靶向人mapt基因中或附近的位点(即,结合dna序列)的zfp结构域。如本文所述的zfp结构域可以附接或融合至另一个功能分子或结构域。本公开的zfp结构域可以与转录因子融合以阻遏人mapt基因转录成mrna。这些融合蛋白被称为锌指蛋白转录因子(zfp-tf),其特异性靶向人mapt基因并阻遏其转录为rna。这些zfp-tf包含与mapt基因中或附近的靶区特异性结合的锌指蛋白(zfp)结构域,以及减少基因转录的转录阻遏物结构域。预期通过将zfp-tf引入至患者的脑来降低神经元中的tau水平以抑制(例如,减少或停止)tau组装成聚集体和nft。将减少或阻止tau聚集体的细胞间传播。本发明的zfp-tf可以用于预防和/或治疗tau蛋白病。
43.本发明的用以tau抑制的zfp-tf方法与通过其他测试的当前方法相比具有几个优点,其包括施用(i)结合tau mrna并阻止其翻译的反义寡核苷酸(aso)和(ii)免疫治疗性抗tau抗体。zfp-tf可能只需要施用一次(通过向患者引入zfp-tf表达构建体),而aso需要重复给药。此外,zfp-tf方法只需要在每个细胞的基因组中接合mapt基因的两个等位基因。相比之下,aso需要在每个细胞中接合mapt mrna的大量拷贝。此外,aso的分布和向性是固定的,而zfp-tf方法可以通过改变启动子、血清型和施用途径来靶向不同的细胞类型和脑区。
44.本发明的zfp-tf方法优于抗体方法,因为抗体只能结合tau蛋白种类或构象的子集。为了稳健的治疗作用,这可能不足够。相比之下,zfp-tf在dna水平上阻遏tau表达,并导致所有形式的tau,包括在tau蛋白病中发现的不同tau构象异构体和翻译后修饰形式的水平降低。因此,与抗体不同,zfp-tf对毒性种类的形式是不可知的。此外,抗体被认为主要作用于细胞外tau,而zfp-tf可以直接降低细胞内的总tau水平,从而间接降低细胞外tau水平。因此,预期本zfp-tf方法更有效,因为tau在细胞内施加其病理作用并且致病种类未知。此外,抗体需要重复施用,通常施用至外周,这导致无法有效地穿过血脑屏障,而zfp-tf仅需要一次性递送其表达构建体,并且可以经由多种途径施用,包括直接施用至脑实质,施用至脑脊液中,或经静脉施用。
45.i.zfp结构域的靶标
46.本融合蛋白的zfp结构域特异性结合至人mapt基因中或附近的靶区。图1例示了zfp结构域与mapt基因中的dna序列的结合。图中的zfp结构域具有六个锌指;然而,如下文进一步描述的,也可以使用具有更少或更多锌指的zfp结构域。
47.人mapt基因跨越约134kb,并已定位至chr17q21.31:45,894,382-46,028,334(grch38.p13)。其核苷酸序列可在genbank登录号ensg00000186868获得。mapt基因包含13-16个外显子。外显子1、4、5、7、9、11和12组成型表达,而外显子2、3和10可以存在于衍生自可变剪接变体(alternatively spliced variant)的tau蛋白种类中,导致成人脑中六种不同tau蛋白同等型的存在。全长人tau蛋白具有以下序列:
[0048][0049][0050]
zfp-tf的dna结合zfp结构域将融合蛋白引导至mapt基因的靶区并将融合蛋白的转录阻遏物结构域带至靶区。阻遏物结构域招募转录共阻遏物复合物,以将染色质修饰为不允许rna聚合酶ii转录的状态。zfp-tf的靶区可以是mapt基因中或附近的任何合适的位点,其允许基因表达的阻遏。例如,靶区包括或邻近(其下游或上游)mapt转录起始位点(tss)或mapt转录调节元件(例如,启动子、增强子、rna聚合酶暂停位点以及等等)。
[0051]
在一些实施方案中,基因组靶区的长度为至少8bp。例如,靶区的长度可以为8bp至40bp,诸如长度为12、15、16、17、18、19、20、21、24、27、30、33或36bp。靶向序列可以在基因的有义链上,也可以在基因的反义链上。为了确保靶向准确性并减少zfp-tf的脱靶结合或活性,所选mapt靶区的序列优选与其他基因中的序列具有小于75%的同源性(例如,小于70%、小于65%、小于60%,或小于50%)。在某些实施方案中,本zfp-tf的靶区的长度为12-20(例如,12-18、15-19、15、18或19)bp,并且位于tss的上游1500bp至下游1000bp(例如、-1000bp到+1000bp、+750或+500bp)内。
[0052]
在一些实施方案中,本工程化zfp与如图14或图16的单行中所示的靶位点(即,靶序列)结合,优选没有或几乎没有可检测的脱靶结合或活性。
[0053]
用于进一步评估靶区段的其他标准包括与此类区段或相关区段结合的zfp的先前可用性、设计新zfp以结合给定靶区段的容易性以及脱靶结合风险。
[0054]
ii.锌指蛋白结构域
[0055]“锌指蛋白”或“zfp”是指具有由锌稳定的dna结合结构域的蛋白质。zfp以序列特异性方式与dna结合。zfp的个体dna结合单元称为“锌指”。每个指含有dna结合“识别螺旋”,其通常由七个氨基酸残基组成,并决定dna结合特异性。zfp结构域具有至少一个指,并且每个指结合核苷酸的2到4个碱基对,通常是dna的3或4个碱基对(连续或非连续)。每个锌指通常包含约30个氨基酸并螯合锌。与天然存在的zfp相比,工程化的zfp可以具有新的结合特异性。工程化方法包括但不限于合理设计和各种类型的选择。合理设计包括,例如,使用包含三联体(或四联体)核苷酸序列和个体锌指氨基酸序列的数据库,其中每个三联体或四联体核苷酸序列与结合特定三联体或四联体序列的锌指的一个或多个氨基酸序列相关。参见,例如,美国专利中5,789,538;5,925,523;6,007,988;6,013,453;6,140,081;6,200,
759;6,453,242;6,534,261;6,979,539;和8,586,526;和国际专利出版物wo 95/19431;wo 96/06166;wo 98/53057;wo 98/53058;wo 98/53059;wo 98/53060;wo 98/54311;wo 00/27878;wo 01/60970;wo 01/88197;wo 02/016536;wo 02/099084;和wo 03/016496详细描述的zfp设计方法。如本文所述的zfp结构域可以附接或融合至另一个分子(例如结构域),例如蛋白质。此类zfp融合物可以包含能够基因激活(例如,激活结构域)、基因阻遏(例如,阻遏物结构域)、配体结合(例如,配体结合结构域)、高通量筛选(例如,配体结合结构域)、局部超突变(例如,活化诱导的胞苷脱氨酶结构域)、染色质修饰(例如,组蛋白脱乙酰酶结构域)、重组(例如,重组酶结构域)、靶向整合(例如,整合酶结构域)、dna修饰(例如,dna甲基转移酶结构域)、碱基编辑(例如碱基编辑器结构域)或靶向dna切割(例如核酸酶结构域)的结构域。工程化zfp结构域的实例显示于图14和图16中。
[0056]
本工程化zfp融合物的zfp结构域可以包括至少一个(例如,一个、两个、三个、四个、五个、六个、七个、八个、九个、十一个、十一个、十二个、十三个或更多个)锌指。具有一个指的zfp结构域通常识别包括3或4个核苷酸的靶位点。具有两个指的zfp结构域通常识别包含6或8个核苷酸的靶位点。具有三个指的zfp结构域通常识别包含9或12个核苷酸的靶位点。具有四个指的zfp结构域通常识别包含12至15个核苷酸的靶位点。具有五个指的zfp结构域通常识别包含15至18个核苷酸的靶位点。具有六个指的zfp结构域可以识别包含18到21个核苷酸的靶位点。
[0057]
在一些实施方案中,本工程化zfp包含dna结合识别螺旋序列,其具有如图14或图16中所示的任何识别螺旋的至少4个氨基酸。在其他实施方案中,本工程化zfp包含图14或图16中所示的dna结合识别螺旋序列。例如,工程化zfp可以包含如图14或图16中所示的f1、f2、f3、f4、f5或f6的序列。
[0058]
在一些实施方案中,本工程化zfp包含图14或图16的单行中所示的两个相邻的dna结合识别螺旋序列。例如,工程化zfp可以包含如图14或图16的单行中所示的f1-f2、f2-f3、f3-f4、f4-f5或f5-f6的序列。
[0059]
在一些实施方案中,本工程化zfp包含图14或图16的单行中所示的dna结合识别螺旋序列。例如,工程化zfp可以包含如图14或图16的单行中所示的f1、f2、f3、f4、f5和f6(例如,f1-f4、f1-f5或f1-f6)的序列。
[0060]
在一些实施方案中,本文所述的工程化zfp包含图15的单行中所示序列的识别螺旋和主链部分。在一些实施方案中,本文所述的工程化zfp包含图15的单行中所示序列的识别螺旋和主链部分,因为该序列将在翻译后修饰后出现。例如,翻译后修饰可以从图15中所示的序列中除去起始甲硫氨酸残基。
[0061]
zfp结构域的靶特异性可以通过zfp主链序列的突变来改善,如例如美国专利号2018/0087072中所述。突变包括对zfp主链中的残基进行的突变,这些突变可以与dna主链上的磷酸盐非特异性相互作用,但不涉及核苷酸靶标特异性。在一些实施方案中,这些突变包括将阳离子氨基酸残基突变为中性或阴离子氨基酸残基。在一些实施方案中,这些突变包括将极性氨基酸残基突变为中性或非极性氨基酸残基。在进一步的实施方案中,突变在相对于dna结合螺旋的位置(-4)、(-5)、(-9)和/或(-14)进行。在一些实施方案中,锌指可以包含位置(-4)、(-5)、(-9)和/或(-14)处的一个或多个突变。在进一步的实施方案中,多指zfp结构域中的一个或多个锌指可以包含位置(-4)、(-5)、(-9)和/或(-14)处的突变。在一
些实施方案中,位置(-4)、(-5)、(-9)和/或(-14)处的氨基酸(例如,精氨酸(r)或赖氨酸(k))突变为丙氨酸(a)、亮氨酸(l)、丝氨酸(s)、天冬氨酸(d)、谷氨酸(e)、酪氨酸(y)和/或谷氨酰胺(q)。在一些实施方案中,位置(-5)处的r残基突变为q。图16中的符号“^”指示在指定识别螺旋中第1氨基酸上游第4位的精氨酸(r)残基变为谷氨酰胺(q)。在每个识别螺旋序列中,七个dna结合氨基酸的位置编号为-1、+1、+2、+3、+4、+5和+6。因此,r至q替代的位置编号为(-5)。
[0062]
在一些实施方案中,本工程化zfp包含dna结合如图16中所示的识别螺旋序列和相关的主链突变。在一些实施方案中,本工程化zfp包含如图16的单行中所示的dna结合识别螺旋序列和相关的主链突变。
[0063]
在一些实施方案中,本文所述的工程化zfp包含图17的单行中所示序列的识别螺旋和主链部分。在一些实施方案中,本文所述的工程化zfp包含图17的单行中所示序列的识别螺旋和主链部分,因为该序列将在翻译后修饰后出现。例如,翻译后修饰可以从图17中所示的序列中除去起始甲硫氨酸残基。
[0064]
iii.锌指蛋白转录因子
[0065]
本文所述的zfp结构域可以与转录因子融合。在一些实施方案中,本融合蛋白含有dna结合锌指蛋白(zfp)结构域和转录因子结构域(即zfp-tf)。在一些实施方案中,转录因子可以是转录阻遏物结构域,其中zfp和阻遏物结构域可以通过直接肽基键联或肽接头或通过二聚化(例如,通过亮氨酸拉链、stat蛋白n端结构域,或fk506结合蛋白)彼此缔合。如本文所用,“融合蛋白”是指具有共价连接结构域的多肽以及通过非共价键彼此缔合的多肽的复合物。转录阻遏物结构域可以在任何合适的位置(包括zfp结构域的c或n端)与zfp结构域缔合。
[0066]
在一些实施方案中,本zfp-tf以小于约25nm的kd与其靶标结合,并将人mapt基因的转录阻遏20%或更多(例如,30%、40%、50%、60%、70%、80%、90%、95%、99%或更多)。在一些实施方案中,两种或更多种本zfp-tf在细胞中表达以协同调节细胞中的mapt表达(参见,例如,美国专利申请公布号2020/0101133和2020/0109406)。此类协同zfp可以通过2a接头肽,例如t2a gsgegrgslltcgdveenpgp(seq id no:19)连接。因此,本zfp-tf中的两种或多种可以同时用于患者,其中zfp-tf与mapt基因中的不同靶区结合,从而实现对mapt表达的最佳阻遏。
[0067]
在一些实施方案中,本zfp-tf包含一个或多个锌指结构域。这些结构域可以经由可延伸的柔性接头连接在一起,使得例如,一个结构域包含一个或多个(例如,4、5或6个)锌指,并且另一个结构域包含另外的一个或多个(例如,4、5、或6)锌指。在一些实施方案中,接头是标准的指间接头,使得指阵列包含一个dna结合结构域,该dna结合结构域包含8、9、10、11或12个或更多个指。在其他实施方案中,接头是非典型接头,诸如柔性接头。例如,两个zfp结构域可以以构型zfp-zfp-tf、tf-zfp-zfp、zfp-tf-zfp或zfp-tf-zfp-tf与转录阻遏物tf连接(两个zfp-tf融合蛋白经由接头融合在一起)。
[0068]
在一些实施方案中,zfp-tf是“双手的”,即它们含有由插入的氨基酸分开的两个锌指簇(两个zfp结构域),使得两个zfp结构域与两个不连续的靶位点结合。双手型锌指结合蛋白的实例是sip1,其中四个锌指的簇位于蛋白质的氨基端,并且三个指的簇位于羧基端(参见remacle et al.,embo j.(1999)18(18):5073-84)。这些蛋白质中的锌指的每个簇
能够与独特的靶序列结合,并且两个靶序列之间的间隔可以包含许多核苷酸。
[0069]
在一些实施方案中,本文所述的工程化zfp-tf与如图14或图16的单行中所示的靶位点结合,优选地没有或几乎没有可检测的脱靶结合或活性。脱靶结合可以例如通过测量zfp-tf在脱靶基因处的活性来确定。在一些实施方案中,本文所述的工程化zfp-tf包含图14或图16中所示的dna结合识别螺旋序列。在一些实施方案中,本文所述的工程化zfp-tf包含图14或图16的单行中所示的两个相邻的dna结合识别螺旋序列。在一些实施方案中,本文所述的工程化zfp-tf包含图14或图16的单行中所示的dna结合识别螺旋序列。
[0070]
a.转录阻遏物结构域
[0071]
本zfp-tf包含如本文所述的工程化zfp结构域和减弱mapt基因转录活性的一个或多个转录阻遏物结构域。一个或多个工程化zfp结构域和一个或多个转录阻遏物结构域可以通过柔性接头连接。转录阻遏物结构域的非限制性实例是kox1或zim3的krab结构域(或任何其他含有krab结构域的蛋白质。参见,例如alerasool et al.,nature methods(2020)17:1093-6)、kap-1,mad、fkhr、egr-1、erd、sid、tgf-β诱导早期基因(tieg)、v-erb-a、mbd2、mbd3、tra、组蛋白甲基转移酶、组蛋白脱乙酰酶(hdac)、核激素受体(例如,雌激素受体或甲状腺激素受体)、dnmt家族的成员(例如dnmt1、dnmt3a、dnmt3b)、rb和mecp2。参见,例如,bird et al.,cell(1999)99:451-4;tyler et al.,cell(1999)99:443-6;knoepfler et al.,cell(1999)99:447-50;和robertson et al.,nature genet.(2000)25:338-42。另外的示例性阻遏物结构域包括但不限于rom2和athd2a。参见,例如,chem et al.,plant cell(1996)8:305-21;和wu et al.,plant j.(2000)22:19-27。
[0072]
在一些实施方案中,转录阻遏物结构域包含来自人锌指蛋白10/kox1(znf10/kox1)的kruppel相关盒(krab)结构域的序列(例如,genbank号nm_015394.4)。示例性krab结构域序列是:
[0073][0074]
也可以使用该krab序列的变体,只要它们具有相同或相似的转录阻遏物功能。
[0075]
b.肽接头
[0076]
本zfp-tf的zfp结构域和转录阻遏物结构域和/或zfp结构域内的锌指可以通过肽接头,例如约5至200个氨基酸的不可切割肽接头(例如、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20个或更多个氨基酸)连接。优选的接头通常是合成为重组融合蛋白的柔性氨基酸子序列。在一些实施方案中,连接锌指以致在靶核酸分子中连接的模块靶亚位点之间没有间隙。在其他实施方案中,锌指通过接头连接,该接头经设计以允许连接的模块与靶位点结合,在靶核酸分子中连接的模块靶亚位点之间具有1、2或3个碱基对间隙。参见,例如美国专利号8,772,453。
[0077]
在一些实施方案中,肽接头的长度为3至20个氨基酸残基并且富含g和/或s。此类接头的非限制性实例是g4s型接头(seq id no:18),即含有一个或多个(例如,2、3或4个)ggggs(seq id no:15)基序的接头,或该基序的变异(诸如相比该基序具有一个、两个或三个氨基酸插入、缺失和替代的基序)。
[0078]
可以用于连接本zfp-tf的zfp结构域和转录阻遏物结构域和/或zfp结构域内的锌
指的接头设计方法和例示性接头描述于美国专利号6,479,626;7,851,216;8,772,453;9,394,531;9,567,609;和10,724,020;和pct公布号wo 1999/045132;wo 2001/053480;wo 2009/154686;wo 2011/139349;wo 2015/031619;和wo 2017/136049。本文所述的蛋白质可以包括合适接头的任何组合。
[0079]
接头的非限制性实例是dgggs(seq id no:3)、tgekp(seq id no:4)、lrqkdgerp(seq id no:5)、ggrr(seq id no:6)、ggrrgggs(seq id no:7)、lrqrdgerp(seq id no:8)、lrqkdgggserp(seq id no:9)、lrqkd(g3s)2erp(seq id no:10)、tgsqkp(seq id no:11)、lrqkdaargs(seq id no:13)、lrqkdaargsgg(seq id no:14)。用于连接锌指和/或用于连接结构域的其他例示性接头列于表1中。表1中列出的指-指接头包括主链序列的部分,例如fq或fa。
[0080]
表1显示了可以用于连接如图14或图16中所示的锌指氨基酸序列和/或zfp和功能结构域序列的例示性替代肽接头。
[0081]
表1
[0082][0083]
在一些实施方案中,本文所述的本工程化zfp包含如图14或图16的单行所示连接的两个相邻的dna结合识别螺旋序列。例如,工程化zfp可以包含如图14或图16的单行中所示的f1-f2、f2-f3、f3-f4、f4-f5或f5-f6的序列。在其他实施方案中,可以使用来自相同接头类别的不同接头。在一些实施方案中,本文所述的本工程化zfp包含如图14或图16的单行中所示连接的dna结合识别螺旋序列。例如,工程化zfp可以包含如图14或图16的单行中所示的f1-f4、f1-f5或f1-f6的连接的序列。在其他实施方案中,可以使用来自相同接头类别的一个或多个不同接头。
[0084]
在一些实施方案中,本文所述的工程化zfp-tf包含如图14或图16的单行中所示序
列的识别螺旋和接头部分。在其他实施方案中,可以使用来自相同接头类别的一个或多个不同接头。在一些实施方案中,本文所述的工程化zfp-tf包含如图15或图17的单行中所示序列的识别螺旋、主链和接头部分。在其他实施方案中,可以使用来自相同接头类别的一个或多个不同接头。在一些实施方案中,本文所述的工程化zfp-tf包含如图15或图17的单行中所示的氨基酸序列。在一些实施方案中,本文所述的工程化zfp-tf包含图15或图17的单行中所示序列的识别螺旋、主链和接头部分,因为该序列将在翻译后修饰后出现。在一些实施方案中,本文所述的工程化zfp-tf包含如图15或图17的单行中所示的氨基酸序列,因为该序列将在翻译后修饰后出现。例如,翻译后修饰可以从图15或图17中所示的序列中除去起始甲硫氨酸残基。
[0085]
iv.zfp-tf的表达
[0086]
本公开的zfp-tf可以通过编码其的核酸分子引入患者。核酸分子可以是rna或cdna分子。可以通过注射包含脂质:核酸复合物(例如,脂质体)的组合物将核酸引入患者的脑中。替代地,可以通过包含编码zfp-tf的序列的核酸表达载体将zfp-tf引入患者。表达载体可以包括表达控制序列,诸如启动子、增强子、转录信号序列和转录终止序列,其允许zfp-tf的编码序列在神经系统的细胞中表达。在一些实施方案中,表达载体作为稳定的附加体保持存在于细胞中。在其他实施方案中,将表达载体整合至细胞的基因组中。
[0087]
在一些实施方案中,载体上用于在脑中指导zfp-tf表达的启动子是组成型活性启动子或诱导型启动子。合适的启动子包括但不限于劳斯肉瘤病毒(rsv)长末端重复(ltr)启动子(任选地具有rsv增强子)、巨细胞病毒(cmv)启动子(任选地具有cmv增强子)、cmv立即早期启动子、猿猴病毒40(sv40)启动子、二氢叶酸还原酶(dhfr)启动子、β-肌动蛋白启动子、磷酸甘油酸激酶(pgk)启动子、eflα启动子、莫洛尼鼠白血病病毒(momlv)ltr、基于肌酸激酶的(ck6)启动子、甲状腺素转运蛋白启动子(ttr)、胸苷激酶(tk)启动子、四环素反应启动子(tre)、乙型肝炎病毒(hbv)启动子、人α1-抗胰蛋白酶(haat)启动子、嵌合肝特异性启动子启动子(lsp)、e2因子(e2f)启动子、人端粒酶逆转录酶(htert)启动子、cmv增强子/鸡β-肌动蛋白/兔β-珠蛋白启动子(cag启动子;niwa et al.,gene(1991)108(2):193-9)和ru-486响应启动子。也可以使用神经元特异性启动子,诸如突触蛋白i启动子、钙/钙调蛋白依赖性蛋白激酶ii(camkii)启动子、甲基cpg结合蛋白2(mecp2)启动子、胆碱乙酰转移酶(chat)启动子、钙结合蛋白(calb)、camkii启动子、prp启动子、gfap启动子或将表达限制在神经元和胶质细胞的工程化或天然启动子。也可以使用星形胶质细胞特异性启动子,诸如胶质原纤维酸性蛋白(gfap)启动子或醛脱氢酶1家族成员l1(aldh1l1)启动子。也可以使用少突胶质细胞特异性启动子,诸如olig2启动子。此外,启动子可以包括一种或多种自我调节元件,zfp-tf可以凭此结合并阻遏其自身的表达水平至预设阈值。参见美国专利9,624,498。
[0088]
可以采用将核苷酸序列引入细胞的任何方法,包括但不限于电穿孔、磷酸钙沉淀、显微注射、阳离子或阴离子脂质体、脂质体联合核定位信号、天然存在的脂质体(例如,外泌体)或病毒转导。
[0089]
对于表达载体的体内递送,可以使用病毒转导。本领域技术人员可以调整本领域已知的多种病毒载体以用于本公开,例如,牛痘载体、腺病毒载体、慢病毒载体、痘病毒载体、腺相关病毒(aav)载体、逆转录病毒载体和杂合病毒载体。在一些实施方案中,本文使用
的病毒载体是重组aav(raav)载体。aav载体特别适用于cns基因递送,因为它们感染分裂细胞和非分裂细胞两者,以稳定的附加型结构存在用于长期表达,并且具有非常低的免疫原性(hadaczek et al.,mol ther.(2010)18:1458-61;zaiss,et al.,gene ther.(2008)15:808-16)。可以使用任何合适的aav血清型。例如,aav可以是aav1、aav2、aav3、aav3b、aav4、aav5、aav6、aav7、aav8、aav8.2、aav9、aav.php.b、aav.php.eb或aavrh10,或新的血清型或假型,诸如aav2/8、aav2/5、aav2/6、aav2/9或aav2/6/9,或作为本文所列aav血清型之一的变体或衍生物的血清型(即衍生自多种血清型的aav;例如,raav在其基因组中包含aav2反向末端重复(itr)和aav8、5、6或9衣壳)。在一些实施方案中,表达载体是aav病毒载体并且通过重组aav病毒体引入靶人细胞,该重组体aav病毒体的基因组包含构建体,包括在两末端具有itr序列以允许在生产系统,诸如昆虫细胞/杆状病毒生产系统或哺乳动物细胞生产系统中产生aav病毒体。aav可以经工程化改造,使得其衣壳蛋白在人或非人灵长类动物中具有降低的免疫原性或增强的转导能力。在一些实施方案中,使用aav9。本文所述的病毒载体可以使用本领域已知的方法产生。可以采用任何合适的允许细胞或包装细胞类型来产生病毒颗粒。例如,哺乳动物(例如,293)或昆虫(例如,sf9)细胞可以用作包装细胞系。
[0090]
v.制药应用
[0091]
本zfp-tf可以用于治疗需要下调tau表达的患者。患者患有或有风险发展神经退行性疾病,诸如阿尔茨海默病、额颞叶痴呆、进行性核上性麻痹、创伤性脑损伤、癫痫发作病症、皮质基底节变性、帕金森病、路易体痴呆(dlb)和/或任何其他tau蛋白病。处于风险下的患者包括有遗传倾向的患者、反复遭受脑损伤(诸如脑震荡)的患者以及暴露于环境神经毒素的患者。本公开提供了治疗受试者(诸如有此需要的人患者)的神经疾病(例如,tau蛋白病诸如神经退行性疾病)的方法,其包括向受试者的神经系统引入治疗有效量(例如,允许充分阻遏mapt表达的量)的zfp-tf(例如,表达其的raav载体)的。术语“治疗”包括缓和症状、预防症状发作、减缓疾病进展、改善生活质量和增加生存。
[0092]
本公开提供了药物组合物,其包含病毒载体诸如raav,其重组基因组包含zfp-tf的表达盒。药物组合物(例如人工脑脊液或acsf)可以进一步包含药学上可接受的载体,诸如水、盐水(例如磷酸盐缓冲盐水)、右旋糖、甘油、蔗糖、乳糖、明胶、葡聚糖、白蛋白或果胶。此外,该组合物可以含有辅助物质,诸如润湿剂或乳化剂、ph缓冲剂、稳定剂或其他增强药物组合物有效性的试剂。药物组合物可以含有递送媒介物,诸如脂质体、纳米胶囊、微粒、微球、脂质颗粒和囊泡。
[0093]
本公开的治疗剂靶向的细胞是脑中的细胞,包括但不限于神经元细胞(例如,运动神经元、感觉神经元、多巴胺能神经元、胆碱能神经元、谷氨酸能神经元、gaba能神经元或血清素能神经元);胶质细胞(例如,少突胶质细胞、星形胶质细胞、周细胞、施万细胞或小胶质细胞);室管膜细胞;或神经上皮细胞。
[0094]
治疗剂靶向的脑区可能是在tau蛋白病中受影响最显著的那些脑区,诸如某些皮质区、内嗅皮质、海马、小脑、苍白球、丘脑、中脑、尾状核、壳核、黑质、脑桥和髓质。这些区域可以通过海马内注射、大脑内注射、小脑延髓池内(icm)注射直接到达,或更通常地通过实质内注射、丘脑内注射、脑室内(icv)注射、鞘内注射或静脉内注射到达。其他施用途径包括但不限于大脑内、心室内、鼻内或眼内施用。在一些实施方案中,病毒载体在直接施用到脑脊液(csf)中后,例如经由鞘内和/或大脑内注射,或小脑延髓池内注射或脑室内注射而扩
散遍及cns组织。在其他实施方案中,在静脉内施用后病毒载体穿过血脑屏障并在整个受试者的cns组织中实现广泛分布。在其他实施方案中,病毒载体经由实质内注射直接递送至靶区。在一些情况下,在实质内递送后病毒载体可能经历逆行或顺行转运至其他脑区。在某些方面,病毒载体具有不同的cns组织靶向能力(例如,cns组织趋向性),其以高效率实现稳定且无毒的基因转移。
[0095]
例如,药物组合物可以通过脑室内施用,例如,至患者前脑的脑室区,诸如右侧脑室、左侧脑室、第三脑室或第四脑室而提供给患者。药物组合物可以通过大脑内施用提供给患者,例如,将组合物注射到大脑、髓质、脑桥、小脑、丘脑、纹状体、尾状核、壳核、黑质、中脑、尾状核、壳核、嗅球、蓝斑、脑干、苍白球、海马、大脑皮层、颅内腔、脑膜、硬脑膜、蛛网膜或脑软膜中或其附近。在一些情况下,大脑内施用可以包括将药剂施用到脑周围的蛛网膜下空隙的脑脊液(csf)中。
[0096]
在一些情况下,大脑内施用包括使用立体定向规程进行注射。立体定向规程在本领域中是众所周知的并且通常涉及使用计算机和3维扫描装置,它们一起使用以将注射引导至特定的大脑内区,例如脑室区。也可以使用微型注射泵(例如,来自world precision instruments)。在一些情况下,使用显微注射泵来递送包含病毒载体的组合物。在一些情况下,组合物的输注速率在0.1μl/min至100μl/min的范围内。如本领域技术人员将理解的,输注速率将取决于多种因素,包括例如受试者的物种、受试者的年龄、受试者的体重/大小、aav的血清型、所需的剂量和靶向的大脑内区。因此,本领域技术人员可以认为其他输注速率在某些情况下是合适的。
[0097]
raav向受试者的递送可以例如通过静脉内施用来完成。在某些情况下,可能期望将raav(例如,10
10-10
15
vg)局部递送至脑组织、脊髓、脑脊液(csf)、神经元细胞、胶质细胞、脑膜、星形胶质细胞、少突胶质细胞、小胶质细胞、间质空隙以及等等。在一些情况下,重组aav可以通过注射到脑室区中或其附近,以及至海马、大脑皮层、小脑小叶、小脑、大脑、髓质、脑桥、丘脑、纹状体、尾状核、壳核、黑质、中脑、尾状核、壳核、嗅球、蓝斑、脑干、苍白球、颅内腔、脑膜、硬脑膜、蛛网膜或脑软膜或其他脑区而直接递送至cns。可以使用本领域已知的神经外科技术,诸如通过立体定向注射,用针、导管或相关装置递送aav(参见,例如,stein et al.,j vir.(1999)73:3424-9;davidson et al.,pnas(2000)97:3428-32;davidson et al.,nat genet.(1993)3:219-223;和alisky and davidson,hum gene ther.(2000)11:2315-29)。
[0098]
除非本文另有定义,否则与本公开结合使用的科学和技术术语应具有本领域普通技术人员通常理解的含义。下文描述了示例性方法和材料,尽管与本文所述的那些相似或等同的方法和材料也可以用于本公开的实践或测试。在冲突的情况下,以本说明书(包括定义)为准。通常,本文所述的与神经病学、医学、医药化学以及细胞生物学结合使用的命名法以及其技术是本领域熟知和常用的那些。酶促反应和纯化技术根据制造商的说明书进行,如本领域通常完成的或如本文所述。此外,除非上下文另有要求,否则单数术语应包括复数,复数术语应包括单数。在整篇说明书和实施方案中,词语“具有(have)”和“包含(comprise)”或变异诸如“具有(has、having)”或“包括(comprises、comprising)”将理解为暗示包含所述整体或整体的组,但不排除任何其他整体或整体的组。本文提及的所有出版物和其他参考文献通过引用其整体并入。尽管本文引用了许多文件,但该引用并不构成承
id的dna结合锌指识别螺旋序列,其中zfp id是71345。
[0118]
17.zfp-tf融合蛋白,其与靶序列结合并包含对应于如图14的单行中所示的zfp id的dna结合锌指识别螺旋序列,其中zfp id是71347。
[0119]
18.zfp-tf融合蛋白,其与靶序列结合并包含对应于如图14的单行中所示的zfp id的dna结合锌指识别螺旋序列,其中zfp id是71351。
[0120]
19.zfp-tf融合蛋白,其与靶序列结合并包含对应于如图14的单行中所示的zfp id的dna结合锌指识别螺旋序列,其中zfp id是71352。
[0121]
20.zfp-tf融合蛋白,其与靶序列结合并包含对应于如图14的单行中所示的zfp id的dna结合锌指识别螺旋序列,其中zfp id是71357。
[0122]
21.zfp-tf融合蛋白,其与靶序列结合并包含对应于如图14的单行中所示的zfp id的dna结合锌指识别螺旋序列,其中zfp id是71364。
[0123]
22.zfp-tf融合蛋白,其与靶序列结合并包含对应于如图14的单行中所示的zfp id的dna结合锌指识别螺旋序列,其中zfp id是71366。
[0124]
23.zfp-tf融合蛋白,其与靶序列结合并包含对应于如图14的单行中所示的zfp id的dna结合锌指识别螺旋序列,其中zfp id是71370。
[0125]
24.zfp-tf融合蛋白,其与靶序列结合并包含对应于如图14的单行中所示的zfp id的dna结合锌指识别螺旋序列,其中zfp id是71373。
[0126]
25.zfp-tf融合蛋白,其与靶序列结合并包含对应于如图14的单行中所示的zfp id的dna结合锌指识别螺旋序列,其中zfp id是71374。
[0127]
26.zfp-tf融合蛋白,其与靶序列结合并包含对应于如图14的单行中所示的zfp id的dna结合锌指识别螺旋序列,其中zfp id是71377。
[0128]
27.zfp-tf融合蛋白,其与靶序列结合并包含对应于如图14的单行中所示的zfp id的dna结合锌指识别螺旋序列,其中zfp id是71378。
[0129]
28.zfp-tf融合蛋白,其与靶序列结合并包含对应于如图14的单行中所示的zfp id的dna结合锌指识别螺旋序列,其中zfp id是71385。
[0130]
29.zfp-tf融合蛋白,其与靶序列结合并包含对应于如图14的单行中所示的zfp id的dna结合锌指识别螺旋序列,其中zfp id是71389。
[0131]
30.zfp-tf融合蛋白,其与靶序列结合并包含对应于如图14的单行中所示的zfp id的dna结合锌指识别螺旋序列,其中zfp id是71391。
[0132]
31.zfp-tf融合蛋白,其与靶序列结合并包含对应于如图14的单行中所示的zfp id的dna结合锌指识别螺旋序列,其中zfp id是71393。
[0133]
32.zfp-tf融合蛋白,其与靶序列结合并包含对应于如图14的单行中所示的zfp id的dna结合锌指识别螺旋序列,其中zfp id是71395。
[0134]
33.zfp-tf融合蛋白,其与靶序列结合并包含对应于如图14的单行中所示的zfp id的dna结合锌指识别螺旋序列,其中zfp id是71397。
[0135]
34.zfp-tf融合蛋白,其与靶序列结合并包含对应于如图14的单行中所示的zfp id的dna结合锌指识别螺旋序列,其中zfp id是71398。
[0136]
35.zfp-tf融合蛋白,其与靶序列结合并包含对应于如图14的单行中所示的zfp id的dna结合锌指识别螺旋序列,其中zfp id是71399。
id的dna结合锌指识别螺旋序列和主链突变,其中zfp id是73016。
[0157]
56.zfp-tf融合蛋白,其与靶序列结合并包含对应于如图16的单行中所示的zfp id的dna结合锌指识别螺旋序列和主链突变,其中zfp id是73017。
[0158]
57.zfp-tf融合蛋白,其与靶序列结合并包含对应于如图16的单行中所示的zfp id的dna结合锌指识别螺旋序列和主链突变,其中zfp id是73018。
[0159]
58.zfp-tf融合蛋白,其与靶序列结合并包含对应于如图16的单行中所示的zfp id的dna结合锌指识别螺旋序列和主链突变,其中zfp id是73019。
[0160]
59.zfp-tf融合蛋白,其与靶序列结合并包含对应于如图16的单行中所示的zfp id的dna结合锌指识别螺旋序列和主链突变,其中zfp id是73020。
[0161]
60.zfp-tf融合蛋白,其与靶序列结合并包含对应于如图16的单行中所示的zfp id的dna结合锌指识别螺旋序列和主链突变,其中zfp id是73021。
[0162]
61.zfp-tf融合蛋白,其与靶序列结合并包含对应于如图16的单行中所示的zfp id的dna结合锌指识别螺旋序列和主链突变,其中zfp id是73029。
[0163]
62.zfp-tf融合蛋白,其与靶序列结合并包含对应于如图16的单行中所示的zfp id的dna结合锌指识别螺旋序列和主链突变,其中zfp id是73030。
[0164]
63.zfp-tf融合蛋白,其与靶序列结合并包含对应于如图16的单行中所示的zfp id的dna结合锌指识别螺旋序列和主链突变,其中zfp id是73031。
[0165]
64.zfp-tf融合蛋白,其与靶序列结合并包含对应于如图16的单行中所示的zfp id的dna结合锌指识别螺旋序列和主链突变,其中zfp id是73032。
[0166]
65.zfp-tf融合蛋白,其与靶序列结合并包含对应于如图16的单行中所示的zfp id的dna结合锌指识别螺旋序列和主链突变,其中zfp id是73034。
[0167]
66.zfp-tf融合蛋白,其与靶序列结合并包含对应于如图16的单行中所示的zfp id的dna结合锌指识别螺旋序列和主链突变,其中zfp id是73035。
[0168]
67.zfp-tf融合蛋白,其与靶序列结合并包含对应于如图16的单行中所示的zfp id的dna结合锌指识别螺旋序列和主链突变,其中zfp id是73120。
[0169]
68.zfp-tf融合蛋白,其与靶序列结合并包含对应于如图16的单行中所示的zfp id的dna结合锌指识别螺旋序列和主链突变,其中zfp id是73121。
[0170]
69.zfp-tf融合蛋白,其与靶序列结合并包含对应于如图16的单行中所示的zfp id的dna结合锌指识别螺旋序列和主链突变,其中zfp id是73122。
[0171]
70.zfp-tf融合蛋白,其与靶序列结合并包含对应于如图16的单行中所示的zfp id的dna结合锌指识别螺旋序列和主链突变,其中zfp id是73123。
[0172]
71.zfp-tf融合蛋白,其与靶序列结合并包含对应于如图16的单行中所示的zfp id的dna结合锌指识别螺旋序列和主链突变,其中zfp id是73124。
[0173]
72.zfp-tf融合蛋白,其与靶序列结合并包含对应于如图16的单行中所示的zfp id的dna结合锌指识别螺旋序列和主链突变,其中zfp id是73125。
[0174]
73.zfp-tf融合蛋白,其与靶序列结合并包含对应于如图16的单行中所示的zfp id的dna结合锌指识别螺旋序列和主链突变,其中zfp id是73126。
[0175]
74.zfp-tf融合蛋白,其与靶序列结合并包含对应于如图16的单行中所示的zfp id的dna结合锌指识别螺旋序列和主链突变,其中zfp id是73127。
[0176]
75.zfp-tf融合蛋白,其与靶序列结合并包含对应于如图16的单行中所示的zfp id的dna结合锌指识别螺旋序列和主链突变,其中zfp id是73128。
[0177]
76.zfp-tf融合蛋白,其与靶序列结合并包含对应于如图16的单行中所示的zfp id的dna结合锌指识别螺旋序列和主链突变,其中zfp id是73129。
[0178]
77.zfp-tf融合蛋白,其与靶序列结合并包含对应于如图16的单行中所示的zfp id的dna结合锌指识别螺旋序列和主链突变,其中zfp id是73130。
[0179]
78.zfp-tf融合蛋白,其与靶序列结合并包含对应于如图16的单行中所示的zfp id的dna结合锌指识别螺旋序列和主链突变,其中zfp id是73131。
[0180]
79.zfp-tf融合蛋白,其与靶序列结合并包含对应于如图16的单行中所示的zfp id的dna结合锌指识别螺旋序列和主链突变,其中zfp id是73133。
[0181]
80.zfp-tf融合蛋白,其与靶序列结合并包含对应于如图16的单行中所示的zfp id的dna结合锌指识别螺旋序列和主链突变,其中zfp id是73190。
[0182]
81.zfp-tf融合蛋白,其与靶序列结合并包含对应于如图16的单行中所示的zfp id的dna结合锌指识别螺旋序列和主链突变,其中zfp id是73191。
[0183]
82.zfp-tf融合蛋白,其与靶序列结合并包含对应于如图16的单行中所示的zfp id的dna结合锌指识别螺旋序列和主链突变,其中zfp id是73192。
[0184]
83.zfp-tf融合蛋白,其与靶序列结合并包含对应于如图16的单行中所示的zfp id的dna结合锌指识别螺旋序列和主链突变,其中zfp id是73193。
[0185]
84.zfp-tf融合蛋白,其与靶序列结合并包含对应于如图16的单行中所示的zfp id的dna结合锌指识别螺旋序列和主链突变,其中zfp id是73194。
[0186]
85.zfp-tf融合蛋白,其与靶序列结合并包含对应于如图16的单行中所示的zfp id的dna结合锌指识别螺旋序列和主链突变,其中zfp id是73195。
[0187]
86.zfp-tf融合蛋白,其与靶序列结合并包含对应于如图16的单行中所示的zfp id的dna结合锌指识别螺旋序列和主链突变,其中zfp id是73196。
[0188]
87.zfp-tf融合蛋白,其与靶序列结合并包含对应于如图16的单行中所示的zfp id的dna结合锌指识别螺旋序列和主链突变,其中zfp id是73197。
[0189]
88.zfp-tf融合蛋白,其与靶序列结合并包含对应于如图16的单行中所示的zfp id的dna结合锌指识别螺旋序列和主链突变,其中zfp id是73198。
[0190]
89.zfp-tf融合蛋白,其与靶序列结合并包含对应于如图16的单行中所示的zfp id的dna结合锌指识别螺旋序列和主链突变,其中zfp id是73199。
[0191]
90.zfp-tf融合蛋白,其与靶序列结合并包含对应于如图16的单行中所示的zfp id的dna结合锌指识别螺旋序列和主链突变,其中zfp id是73200。
[0192]
91.zfp-tf融合蛋白,其与靶序列结合并包含对应于如图16的单行中所示的zfp id的dna结合锌指识别螺旋序列和主链突变,其中zfp id是73201。
[0193]
92.zfp-tf融合蛋白,其与靶序列结合并包含对应于如图16的单行中所示的zfp id的dna结合锌指识别螺旋序列和主链突变,其中zfp id是73202。
[0194]
93.zfp-tf融合蛋白,其与靶序列结合并包含对应于如图16的单行中所示的zfp id的dna结合锌指识别螺旋序列和主链突变,其中zfp id是73203。
[0195]
94.实施方案1-93中任一项的zfp-tf融合蛋白,其中zfp-tf融合蛋白包含转录阻
遏物结构域。
[0196]
95.实施方案94的zfp-tf融合蛋白,其中转录阻遏物结构域包含krab结构域。
[0197]
96.实施方案94的zfp-tf融合蛋白,其中转录阻遏物结构域包含seq id no:2。
[0198]
97.抑制人脑细胞中tau表达的方法,其包括将实施方案1-96中任一项的融合蛋白引入至细胞中。
[0199]
98.抑制人脑细胞中tau表达的方法,其包括将根据实施方案1-96中任一项的两种或更多种不同融合蛋白引入至细胞中。
[0200]
99.抑制人脑细胞中tau表达的方法,其包括将根据实施方案4(zfp id57890)和实施方案53(zfp id 65918)的融合蛋白引入至细胞中。
[0201]
100.实施方案98或99的方法,其中融合蛋白的每一种包含转录阻遏物结构域,任选地其中转录阻遏物结构域是krab结构域。
[0202]
101.实施方案98-100中任一项的方法,其中融合蛋白经共同递送。
[0203]
102.实施方案98-100中任一项的方法,其中融合蛋白通过2a自切割肽连接。
实施例
[0204]
实施例1:抗tau zfp-tf的筛选
[0205]
为了鉴定阻遏tau表达的zfp-tf,设计了预期在跨越tss上游1000bp到下游500bp的人mapt基因区中结合15、18或19bp序列的370个zfp-tf文库并筛选了tau阻遏活性。zfp-tf的靶区在图2中由五边形表示,五边形的方向指示zfp-tf结合的dna链(5’至3’)。在该研究中,krab结构域序列(seq id no:2)用作转录阻遏物并融合到zfp结构域的c端。52个代表性zfp-tf的序列显示于以下图14中。使用pcr(正向引物gcagagctctctggctaactagag(seq id no:16);反向引物t(180)ctggcaactagaaggcacag(seq id no:17))从pvax-zfp或pvax-gfp质粒生成用于体外转录的模板。按照制造商的说明使用mmessage mmachine t7ultra转录试剂盒(thermo fisher scientific)合成信使rna并使用rneasy96柱(qiagen)进行纯化。然后将编码每个zfp-tf的mrna以6个剂量稀释物等分到96孔板中。
[0206]
在sk-n-mc人神经上皮细胞系中进行筛选。sk-n-mc细胞以高水平表达人tau,因此适于测试降低tau表达的zfp-tf。将sk-n-mc细胞在组织培养瓶中培养直至汇合。将细胞以每孔150,000个细胞铺板在96孔板上,并重悬浮于sf溶液中。然后将细胞与zfp-tf mrna(6个剂量:3、10、30、100、300和1000ng)混合并转移到梭板孔中。使用梭板孔中。使用装置(lonza;程序cm-137)转染细胞。将eagle氏mem细胞培养基添加到板的每个孔中。将细胞转移到96孔组织培养板中,并在37℃下温育20小时。
[0207]
然后裂解细胞并按照制造商的说明使用c2ct试剂盒进行逆转录。使用taqman定量聚合酶链反应(qpcr)以测量mapt的表达水平,将其归一化至管家基因atp5b和eif4a2表达水平的几何均值。模拟品转染和用已知不靶向mapt的zfp-tf的转染用作阴性对照。
[0208]
我们发现了所测试的约29%的zfp-tf对tau的≥50%剂量依赖性阻遏。所达到的最大阻遏为100%,但我们还鉴定了对tau阻遏程度较低(例如,在最高剂量下为约90%、约75%或约50%)的zfp-tf。图3a-d显示了筛选数据。我们还在人ipsc衍生神经元中测试了52个具有代表性的zfp-tf(数据未显示)。
[0209]
实施例2:抗tau zfp-tf的靶标特异性的优化
[0210]
为了优化zfp-tf的靶标特异性,将多达三个锌指中的精氨酸(r)残基突变为谷氨酰胺(q)。该精氨酸残基位于dna结合螺旋中第1个氨基酸上游的第4个氨基酸处,并且在每个锌指的β-片层中(图4、5a和5b)。该残基参与了与靶dna的磷酸主链的保守非特异性接触。每个亲本zfp-tf在指示螺旋中第1个氨基酸上游的第4位处突变,以生成多达7个不同的r
→
q变体。41个代表性r
→
q变体zfp-tf的序列显示于以下图16中。也参见miller et al.,nat biotechnol.(2019)37:945-52。
[0211]
实施例3:亲本抗tau zfp-tf的r
→
q变体的筛选
[0212]
为了鉴定最佳阻遏人tau表达的亲本zfp-tf的r
→
q变体,如实施例1中所述筛选约340个变体zfp-tf的文库。代表性r
→
q变体zfp-tf的tau阻遏活性还在用编码各自zfp-tf的aav转导的人ipsc衍生神经元和原代小鼠皮层神经元中进行了测试。
[0213]
aav生产
[0214]
通过三重转染方法生成重组腺相关病毒载体(raav)。简而言之,将hek293细胞铺板在十层cellstack室(corning,acton,ma)中并生长三天至密度为80%。使用磷酸钙将三种质粒-(i)含有rep和cap基因的aav辅助质粒,(ii)含有腺病毒辅助基因的腺病毒辅助质粒,和(iii)含有侧翼为aav2反向末端重复的待包装序列的转基因质粒转染至细胞中。三天后,收获细胞。然后通过三轮冷冻/解冻裂解细胞并通过离心除去细胞碎片。使用聚乙二醇沉淀raav。重悬浮后,通过在氯化铯梯度上超速离心过夜来纯化病毒。病毒通过透析配制,然后过滤灭菌。在通过用pbs+0.001%pluronic f-68稀释调整所有aav批次的滴度(病毒基因组/ml)后,将aav等分至单一使用剂量并贮存在-80℃下直至使用。解冻后,不进行再冷冻。
[0215]
人ipsc衍生神经元培养和zfp-tf aav感染
[0216]
人ipsc衍生的gaba能神经元购自cellular dynamics international,并以每孔40,000个细胞的密度铺板到聚-l-鸟氨酸和层粘连蛋白包被的96孔板上,并根据制造商的说明维持。在铺板后48小时,以指示的moi用表达期望zfp-tf的aav感染细胞,并维持长达32天(每3-5天进行50-75%的培养基更换)。在实验期结束时收获细胞,分离rna,并进行rt-qpcr用于基因表达分析。对于微阵列分析,在铺板后48小时用1e5vg/细胞转染细胞,并在病毒转染后19天收获。
[0217]
原代小鼠神经元培养和zfp-tf aav感染
[0218]
原代小鼠皮层神经元(mcn)购自gibco。将细胞分别以50,000或200,000个细胞/孔铺板到聚d-赖氨酸包被的96孔或24孔板上,并根据制造商的说明使用含有glutamaxtmi补充剂、b27补充剂和青霉素/链霉素的gibco neurobasal培养基维持。在铺板后48小时(在div2),以指示的moi用aav-zfp感染96孔板中的50,000个细胞/孔,并在7天后收获(在div9;每3-4天进行50%的培养基更换),接着是rna分离和通过rt-qpcr进行的基因表达分析。替代地,用1e5vg/细胞处理24孔板中的200,000个神经元/孔,以确保100%的转导率,并以类似的方式处理用于在div9的微阵列分析。
[0219]
图6显示了代表性r
→
q变体zfp-tf的筛选数据。图7a和7b显示了用编码各自zfp-tf的aav转导的人ipsc衍生神经元和小鼠原代神经元中代表性zfp-tf及其r
→
q变体的剂量依赖性活性。
[0220]
这些图中的数据显示,r
→
q变体zfp-tf展示出大范围的tau阻遏活性谱,在测试的最高剂量下,人ipsc衍生神经元中的人tau mrna阻遏在约45%至100%的范围。同样显而易见的是,测试的zfp-tf特异性靶向人mapt,因为在原代皮质小鼠神经元中代表性r
→
q变体zfp-tf的表达在7天后不导致总小鼠mapt的剂量依赖性阻遏。
[0221]
实施例4:抗tau zfp-tf的脱靶活性
[0222]
为了评估亲本zfp-tf的r
→
q变体对全局基因表达的脱靶影响,我们对从用编码代表性r
→
q变体zfp-tf的aav处理的人ipsc衍生神经元和原代小鼠皮层神经元分离的总rna进行了微阵列(clariom s阵列和clariom d阵列)实验。我们还进行了定量rt-qpcr分析,以比较这些zfp-tf对tau基因座(人tau和sth)和微阵列研究中鉴定的明显脱靶基因(cpne6和igf2)内转录物表达水平的影响。
[0223]
微阵列分析
[0224]
按照制造商的方案(thermo fisher scientific)进行微阵列分析,并使用tac4软件分析测定结果。使用rt-qpcr分析进一步研究了具有fdr校正的p值≤0.05的明显脱靶。
[0225]
使用rt-qpcr进行的基因表达分析
[0226]
使用c2ct试剂盒按照制造商的说明进行逆转录。使用taqman定量聚合酶链反应(qpcr)以测量mapt、sth、cpne6和igf2的转录物水平。将基因表达水平归一化至管家基因atp5b、eif4a2和gapdh的表达水平的几何均值。模拟品转染和用已知不靶向mapt、sth、cpne6和igf2的zfp-tf转染用作阴性对照。
[0227]
图8显示了人ipsc衍生神经元和原代小鼠皮层神经元中6种代表性r
→
q变体zfp-tf的微阵列结果。图9显示了用代表性r
→
q变体zfp-tf转导的人ipsc衍生神经元中mapt、sth、cpne6和igf2基因表达的rt-qpcr结果。
[0228]
我们发现r
→
q变体zfp-tf展示出低至不可检测的脱靶活性。
[0229]
实施例5:抗tau zfp-tf的代表性r
→
q变体的体内耐受
[0230]
为了评估海马内立体定向aav9施用后zfp-tf介导的tau阻遏的潜在不良作用,我们通过对海马组织中的zfp-tf、tau、gfap、iba1和neun表达的定量rt-qpcr分析评估了转基因表达和神经炎性标志物的表达水平,该海马组织分离自用编码具有一系列人tau阻遏活性的亲本zfp-tf的r
→
q变体的aav处理4周后的成年c57bl/6小鼠的脑。
[0231]
为了收获海马组织用于随后的分析,用pbs灌注小鼠,并且提取脑并在冰上解剖。用保险刀片或手术刀将海马切碎,并将切碎的组织分成指定用于rna和dna分析的两部分。然后将切碎的组织在液氮中速冻并维持在-80℃下直到分析。
[0232]
使用high capacity rt kit(thermo fisher scientific)试剂盒按照制造商的说明进行逆转录。使用taqman定量聚合酶链反应(qpcr)以测量zfp-tf、mapt、gfap、iba1和neun的表达水平。将基因表达水平归一化至管家基因atp5b、eif4a2和gapdh表达水平的几何均值。媒介物处理和用aav表达绿色荧光蛋白(gfp)处理用作阴性对照。
[0233]
我们发现大多数测试的r
→
q变体zfp-tf在最大施用剂量下在体内耐受良好。几个候选物导致神经炎性标志物的表达水平没有显著变化。此外,一些候选物对小鼠tau显示无交叉反应性,表明具有高度的特异性。用具有代表性的r
→
q变体zfp-tf处理的成年小鼠展示出稳定的小鼠mapt表达,从而显示这些zfp-tf特异性靶向人mapt基因。然而,一种融合蛋白表现出zfp-tf的表达降低,另一种融合蛋白导致神经炎性标志物gfap和iba1的表达水平
升高。所测试的zfp-tf均未导致神经元标志物neun的表达水平降低。这些发现表明,在该研究中测试的tau zfp-tf候选物在小鼠中体内具有期望的概况,其在小鼠脑中表达后没有神经炎性标志物升高的证据至具有最少神经炎性标志物升高的证据并且没有神经元损失(图10)。
[0234]
实施例6:通过抗tau zfp-tf的代表性r
→
q变体的人tau mrna和蛋白质的体内减少
[0235]
为了评估体内人tau mrna和蛋白质的减少,如本文所述,将抗tau zfp-tf施用于htau小鼠(b6.cg-mapt
tm1(egfp)klt
tg(mapt)8cpdav/j,jackson labs)。htau小鼠在通过将表达gfp的构建体插入至小鼠mapt的第一编码外显子中来功能性敲除内源性(小鼠)mapt的背景上表达野生型人mapt基因。小鼠接受aav9载体至背侧和腹侧海马中的立体定向双重双侧注射,该aav9载体编码媒介物73133、73034、73122或65918.t2a.57890(共表达经设计以靶向小鼠mapt基因中的位点的两个zfp的构建体)。zfp-tf 73133、73034和73122以每半球3e9、1e0和3e10vg的剂量进行测试,而zfp-tf65918.t2a.57890以仅每半球3e9vg的剂量进行测试。在注射后3个月或6个月处死小鼠的单独组,以获得分子、生化和免疫组织学终点。
[0236]
在分离自htau小鼠脑的海马组织中通过定量rt-qpcr评估了zfp转基因、人mapt、内源性小鼠mapt和破坏内源性mapt翻译的gfp盒的表达水平。还评估了神经炎性和神经元标志物,包括gfap、iba1和neun。此外,还评估了命名为saitohin(sth)的人mapt内未知功能的内含子转录物的水平。
[0237]
为了收获海马组织用于随后的分析,用pbs灌注小鼠,并且提取脑并在冰上解剖。对于右半球,用保险刀片或手术刀将海马切碎,并将切碎的组织分成指定用于rna和蛋白质分析的两部分。然后将切碎的组织在液氮中速冻并维持在-80℃下直到分析。对于左半球,将海马在10%nbf中滴固定24小时,转移到70%乙醇中,然后包埋在石蜡块中于随后的原位杂交(ish)分析。
[0238]
对于mrna分析,使用用于微阵列rna提取试剂盒(thermo fisher scientific)的magmax提取总rna,并按照制造商的说明使用high capacity rt kit(thermo fisher scientific)试剂盒进行逆转录。使用taqman
tm
定量聚合酶链反应(qpcr)以测量靶基因表达水平。zfp-转基因表达归一化至用作rt-qpcr反应的输入的总rna的量。所有其他靶基因表达水平均归一化至管家基因atp5b、eif4a2和gapdh表达水平的几何均值。所有处理组均按媒介物组观察到的归一化水平的均值进行缩放。
[0239]
对于蛋白质分析,按照制造商的方案,使用总人tau elisa(thermo fisher scientific)试剂盒来定量人tau蛋白的水平。将总tau水平归一化至如通过bca蛋白质测定法确定的总蛋白质。所有处理组均按针对媒介物组观察到的归一化水平的均值进行缩放。
[0240]
对于ish分析,将石蜡包埋的块切片并根据制造商的方案(advanced cell diagnostics)处理用于多路复用rnascope/免疫荧光染色。切片用dapi染色细胞核,通过rnascope染色人mapt转录物,通过免疫荧光染色neun蛋白。
[0241]
zfp-tf中的每一个以持续的、剂量依赖性的方式表达,并且在3个月和6个月时间点针对每个相应剂量测试的所有构建体中以相似的水平表达。在两个时间点测试的最高剂量下,人靶向抗tau zfp-tf能够特异性降低人tau mrna高达93%(73133)或54-61%(73034和73122)。zfp-tf 73133和73034导致tau mrna的剂量依赖性降低,而73122导致在测试剂
量范围内的平台效应(约46-68%降低)。对于所有测试的zfp-tf和时间点,对于内含子mapt转录物sth观察到了相似的结果。对于73133、73034和73034,内源性小鼠mapt或gfp表达没有显著降低。靶向65918.t2a.57890的交叉物种在所测试的单一剂量(每半球3e9vg)下在两个时间点处确实使人和小鼠tau降低了》50%。在zfp处理组中未观察到神经炎性和神经元标志物gfap、iba1或neun的表达水平的显著变化或观察到最小显著变化(图11)。
[0242]
在两个时间点测试的最高剂量下,人靶向的抗tau zfp-tf类似地使人tau蛋白水平降低了高达97%(73133)至》64-80%(73034和73122)。zfp-tf 73133和73034导致tau蛋白的剂量依赖性降低,而73122导致在测试剂量范围内的平台效应(约54-80%降低;图12)。
[0243]
rnascope分析显示了在经处理的htau小鼠的海马中,人mapt转录物减少的zfp依赖性程度。与媒介物处理的小鼠相比,用zfp-tf 73133处理的海马中的neun阳性神经元在3e9测试剂量下在三个月时具有最小的可检测mapt转录物残留。相反,73122具有中等水平的可检测mapt转录物残留,这与整体mapt mrna和tau蛋白分析一致,显示该zfp-tf的总阻遏较少(图13)。这些单细胞数据支持在sk-n-mc细胞、培养的人ipsc衍生神经元和来自htau小鼠的大块脑组织中表达的mapt靶向zfp-tf获得的阻遏结果。
[0244]
这些发现表明,在该研究中测试的tau zfp-tf候选物在小鼠中体内具有期望的tau降低概况,其在htau小鼠脑中表达后具有最少的神经炎性标志物升高证据并且没有神经元损失。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1