新的大环化合物、它们的制备方法和含有它们的药物组合物与流程
新的大环化合物、它们的制备方法和含有它们的药物组合物
1.本发明涉及新的大环化合物、它们的制备方法和含有它们的药物组合物。
2.本发明的化合物是新的并且具有非常有价值的药理学特征。
3.发明背景
4.核因子红细胞2相关因子2(nrf2),也称为红细胞衍生核因子2样蛋白2,是一种在人类中由nfe2l2基因编码转录因子(moi p,chan k,asunis i,cao a,kan yw 1994..proceedings of the national academy of sciences of the united states of america.91(21):9926
–
30)。nrf2是一种碱性亮氨酸拉链(bzip)蛋白,可调节和协调大量细胞保护基因的基础激活和应激诱导激活。在这方面特别重要的是谷胱甘肽和硫氧还蛋白抗氧化系统成分以及参与外源性和内源性产物的i期和ii期解毒、nadph再生和血红素代谢的酶的转录。因此,nrf2代表了针对外源性物质和氧化应激的细胞防御机制的关键调节因子(vomund s,a,parnham mj,br
ü
ne b,和von knethen a int j mol sci.2017dec;18(12):2772;bischof ljm,isoude a.kuijper1 schimming jp,wolters l,ter braak b,langenberg jp,noort d,beltman jb和van de water b archives of toxicology(2019)93:435
–
451)。同样重要的是,nrf2参与并调节关键的细胞过程,例如炎症、自噬、葡萄糖和脂质代谢、干细胞静止和未折叠蛋白质反应(综述于yamamoto m,kensler tw,motohashi h(2018).physiol rev 98:1169
–
1203;ahmed smu,luo l,namani a,wang xj,tang x biochimica et biophysica acta 1863(2017)585
–
597;hayes jd和dinkova-kostova at,trends in biochemical sciences,vol.39,no.4,pp.199
–
218,2014)。
5.由于这些基本生理过程的改变与许多疾病密切相关,nrf2活性的调节系统被证明是许多重要医学适应症(如代谢、心血管、神经退行性和自身免疫性疾病)的有吸引力的药物靶标(综述于cuadrado a,rojo ai,wells g,hayes jd,cousin sp,rumsey wl,ttucks oc,franklin s,levonen a-l,kensler tw and dinkova-kostova at nature reviews drug discovery 2019第18卷,295
–
317页;robledinos-ant
ó
n n,fern
á
ndez-gin
é
s r,manda g,cuadrado a.oxid med cell longev.2019:9372182;satta s,mahmoud am,wilkinson fl,alexander my和white sj.oxidative medicine and cellular longevity 2017卷;gao b.,doan a.,hybertson b.m.clin.pharmacol.2014;6:19
–
34)。
6.nrf2是哺乳动物进化保守的防御机制的重要组成部分,斑马鱼、果蝇和秀丽隐杆线虫已被证明具有相似的抗应激系统(fuse y和kobayashi m的综述molecules.2017mar;22(3):436)。nrf2在细胞中普遍存在且组成型表达,从而确保它们对氧化、炎症和代谢应激的迅速保护性反应。nrf2的表达受到严格调控,在健康/非应激条件下,低nrf2水平提供其靶基因的基础表达。在这些条件下,由于nrf2被泛素蛋白酶体系统不断降解,因此其更新速度很快(mcmahon m,thomas n,itoh k,yamamoto m和hayes jd,journal of biological chemistry 2004 vol.279,no.30,pp.31556
–
31567;katoh y,iida k,kang mi,kobayashi a,mizukami m,tong ki,mcmahon m,hayes jd,itoh k,yamamoto m.archives of biochemistry and biophysics,vol.433,no.2,pp.342
–
350,2005)。
7.nrf2的降解通过与e3泛素连接酶的衔接蛋白keap1(kelch样ech相关蛋白1)结合
来调节。在存在氧化和外源性物质应激的情况下,nrf2的降解通过keap1的释放而被阻断,从而使nrf2积累并转移到细胞核中,在那里它通过含有cnc-bzip结构域的neh1与小肌肉腱膜纤维瘤病(maf)k、g和f等bzip蛋白形成异二聚体(ma q.annual review of pharmacology and toxicology,vol.53,no.1,pp.401
–
426,2013;hayes jd和dinkova-kostova at,trends in biochemical sciences,vol.39,no.4,pp.199
–
218,2014)。在人类中,这些异二聚体直接调节约250个基因的表达,这些基因呈现出称为抗氧化反应元件(are)的调节增强子序列。这些基因参与并调节多种稳态功能,包括氧化还原稳态、解毒、炎症、蛋白质稳态和新陈代谢(pajares m,jim
é
nez-moreno n,garc
í
a-yag
ü
e aj等人,autophagy 2016,vol.12,no.10,pp.1902
–
1916;pajares m,cuadrado a和rojo ai,redox biology,2017vol.11,pp.543
–
553;pajares m,jim
é
nez-moreno n,dias ihk等人,redox biology 2015,vol.6,pp.409
–
420;de la vega mr,dodson m,gross c等人,current pharmacology reports,vol.2,no.2,pp.91
–
101,2016)。
8.keap1包含两个离散的结构域,即n端区域的btb(broad complex、tramtrack和bric-a-brac)结构域和c端区域的双甘氨酸重复序列(dgr;也称为kelch结构域)(itoh k,wakabayashi n,katoh y,ishii t,igarashi k,engel jd和yamamoto m genes dev.1999 jan 1;13(1):76
–
86)。虽然btb结构域有助于keap1的同二聚化及其与cul3的相互作用,但kelch结构域通过与neh2结构域的相互作用介导keap1与nrf2的结合。在这种keap1-nrf2相互作用中,nrf2的neh2结构域中的两个特定基序,即dlg和etge,分别与keap1同源二聚体的kelch结构域结合。keap1同源二聚体与nrf2的双位点结合的识别导致提出了亲电应力传感的分子机制,tong等人对此进行了详细描述(tong ki,katoh y,kusunoki h,itoh k,tanaka t,yamamoto m(2006)mol cell biol 26:2887
–
2900;tong ki,padmanabhan b,kobayashi a,shang c,hirotsu y,yokoyama s,yamamoto m(2007).mol cell biol27:7511
–
7521.https://doi.org/10.1128/mcb.00753-072006)并在yamamoto等人(yamamoto m,kensler tw,motohashi h(2018).physiol rev 98:1169
–
1203)中进行了综述。
9.keap1的干预区(ivr)位于btb和dgr/kelch结构域之间,富含可作为应激传感器的反应性半胱氨酸(cys)残基。分别在人和小鼠keap1蛋白中鉴定出27个和25个cys残基。其中,btb结构域中的cys151和ivr中的cys273/288是主要的传感器半胱氨酸残基(dinkova-kostova,a.t.,holtzclaw,w.d.,cole,r.n.,itoh,k.,wakabayashi,n.,katoh,y.,yamamoto,m.和talalay,p.(2002).proc.natl.acad.sci.usa 99,11908
–
11913;zhang,d.d.和hannink,m.(2003)mol.cell.biol.23,8137
–
8151;saito,r.,suzuki,t.,hiramoto,k.,asami,s.,naganuma,e.,suda,h.,iso,t.,yamamoto,h.,morita,m.,baird,l.等人,(2016).mol.cell.biol.36,271
–
284;suzuki t,muramatsu a,saito r,iso t,shibata t,kuwata k,kawaguchi si,iwawaki t,adachi s,suda h,morita m,uchida k,baird l,yamamoto m(2019)cell rep 28:746-758)。通过使用三种主要半胱氨酸残基的突变体,即cys151、cys273和cys288,研究了keap1半胱氨酸残基对nrf2的各种化学诱导剂的特异性。这些实验将nrf2诱导剂分为了四类,即i类(cys151偏好)、ii类(cys288偏好)、iii类(cys151/cys273/cys288协作偏好)和iv类(cys151/cys273/cys288独立)(saito,r.,suzuki,t.,hiramoto,k.,asami,s.,naganuma,e.,suda,h.,iso,t.,yamamoto,h.,morita,m.,baird,l.等人,(2016).mol.cell.biol.36,271
–
284)。最近总结了各种亲电体的keap1
修饰位点的半胱氨酸密码(unoki t,akiyama m,kumagai y.int j mol sci.2020jan 15;21(2))。然而,如15-脱氧-前列腺素j2(15d-pgj2)和前列腺素a2(pga2)的示例所示,定义每个类别的化学性质似乎具有挑战性。尽管具有相似的结构特征,但15d-pgj2和pga2分别属于ii类和iv类。因此,亲电体的结构和反应性等复杂特性可能决定了与特定keap1反应性半胱氨酸残基的相互作用(unoki t,akiyama m,kumagai y.int j mol sci.2020jan 15;21(2))。
10.由于其分子靶标是keap1(magesh s.,chen y.和hu l.medicinal research reviews,2012vol.32,no.4,pp.687
–
726),nrf2激活剂或keap1抑制剂可归类为亲电体、蛋白质-蛋白质相互作用(ppi)抑制剂和多靶点药物。
11.大多数药理学nrf2激活剂是亲电性分子,它们通过氧化或烷基化共价修饰富含硫醇的keap1蛋白中的一个或多个半胱氨酸残基(hur w.,gray n.s.current opinion in chemical biology.2011;15(1):162
–
173;satoh t.,mckercher s.r.,lipton s.a.free radical biology&medicine.2013;65:645
–
657;wilson a.j.,kerns j.k.,callahan j.f.,moody c.j.journal of medicinal chemistry.2013;56(19):7463
–
7476)。迄今为止,唯一上市的nrf2激活剂是来自biogen的富马酸二甲酯(bg-12或tecfidera)和富马地罗昔美(drf)。富马酸二甲酯于2013年、drf于2019年获批用于复发缓解型多发性硬化症(ms)(schimrigk s.,brune n.,hellwig k.等人,european journal of neurology.2006;13(6):604
–
610;gold r.,kappos l.,arnold d.l.等人,the new england journal of medicine.2012;367(12):1098
–
1107;fox r.j.,miller d.h.,phillips j.t.等人,the new england journal of medicine.2012;367(12):1087
–
1097;xu z.,zhang f.,sun f.,gu k.f.,dong s.,he d.cochrane database of systematic reviews.2015;4;mills e.a.,ogrodnik m.a.,plave a.,mao-draayer y.frontiers in neurology.2018;9(5))。此前,富马酸二甲酯被批准用于治疗银屑病(hoxtermann s.,nuchel c.,altmeyer p.dermatology.1998;196(2):223
–
230)。在实验性过敏性脑脊髓炎的ms小鼠模型中描述了富马酸二甲酯诱导的中枢神经系统nrf2的激活(linker r.a.,lee d.h.,ryan s.等人,brain.2011;134(3):678
–
692)。
12.在该模型中,依赖富马酸二甲酯的nrf2激活与ms临床病程的改善、轴突保存和星形胶质细胞活化增加相关。富马酸二甲酯的这些有益作用在nrf2-null小鼠中没有发生,因此表明富马酸二甲酯主要通过靶向nrf2途径起作用。富马酸二甲酯主要通过肠道酯酶转化为富马酸单甲酯(mmf),在血液中仅发现一小部分与谷胱甘肽结合的富马酸二甲酯(dibbert s.,clement b.,skak-nielsen t.,mrowietz u.,rostami-yazdi m.archives of dermatological research.2013;305(5):447
–
451)。由于mmf被认为是富马酸二甲酯的活性代谢物,因此正在进行多项临床试验以评估mmf的功效和安全性。
13.nrf2激活剂凭借其固有的亲电性质与keap1的半胱氨酸残基相互作用,并且也与蛋白质中的谷胱甘肽或硫醇发生反应。由于这种硫醇反应性化学物质有可能在细胞中引起亲电性损伤,因此直接抑制keap1和nrf2的蛋白质-蛋白质相互作用(ppi)的化学物质正在成为有吸引力的新型nrf2诱导剂(bertrand,h.c.,schaap,m.,baird,l.,georgakopoulos,n.d.,fowkes,a.,thiollier,c.,kachi,h.,dinkova-kostova,a.t.和wells,g.(2015).j.med.chem.58,7186
–
7194;davies,t.g.,wixted,w.e.,coyle,j.e.,griffiths-jones,
c.,hearn,k.,mcmenamin,r.,norton,d.,rich,s.j.,richardson,c.,saxty,g.,willems,h.m.,woolford,a.j.,cottom,j.e.,kou,j.p.,yonchuk,j.g.等人,(2016).j.med.chem.59,3991
–
4006;jiang,zy,lu,m c.和you,q.d.(2016).j.med.chem.59,10837
–
10858;lu,m.c.,ji,j.a.,jiang,y.l.,chen,z.y.,yuan,z.w.,you,q.d.和jiang,z.y.(2016).sci.rep.6,26585;yasuda,d.,nakajima,m.,yuasa,a.,obata,r.,takahashi,k.,ohe,t.,ichimura,y.,komatsu,m.,yamamoto,m.,imamura,r.,kojima,h.,okabe,t.,nagano,t.和mashino,t.(2016)bioorg.med.chem.lett.26,5956
–
5959)。
14.ppi抑制剂会干扰nrf2与keap1的kelch螺旋桨的对接,并且很可能提供比亲电化合物更高的选择性(richardson b.g.,jain a.d.,speltz t.e.,moore t.w.bioorganic&medicinal chemistry letters.2015;25(11):2261
–
2268)。基于keap1的x射线晶体结构,设计了小的ppi抑制剂来阻止dlg和etge基序与keap1的结合。etge基序采取β-发夹结构,其通过特定的疏水和静电相互作用与keap1的kelch螺旋桨对接(padmanabhan b.,tong k.i.,ohta t.等人,molecular cell.2006;21(5):689
–
700;lo s.c.,li x.,henzl m.t.,beamer l.j.,hannink m.the embo journal.2006;25(15):3605
–
3617)。迄今为止,还没有ppi抑制剂进入临床开发阶段,但是,已经描述了keap1kelch
–
nrf2相互作用的强效和选择性ppi抑制剂,并且它们的活性分别在体外和体内研究中得到证实(davies,t.g.,wixted,w.e.,coyle,j.e.,griffiths-jones,c.,hearn,k.,mcmenamin,r.,norton,d.,rich,s.j.,richardson,c.,saxty,g.,willems,h.m.,woolford,a.j.,cottom,j.e.,kou,j.p.,yonchuk,j.g.等人,(2016).j.med.chem.59,3991
–
4006;jiang,zy,lu,m c.和you,q.d.(2016).j.med.chem.59,10837
–
10858;robledinos-ant
ó
n n,fern
á
ndez-gin
é
s r,manda g,cuadrado a.oxid med cell longev.2019:9372182)。
15.keap1抑制的另一种机制涉及与cul3/rbx1复合物的相互作用,这是nrf2泛素化和降解所必需的。位于btb结构域的cys-151影响keap1与cul3的相互作用。与五环三萜类化合物2-氰基-3,12-二氧代-齐墩果-1,9(11)-二烯-28-酸(bardoxolone,cddo-me或rta 402)结合的btb结构域的晶体结构表明与cys-151的加合物的形成破坏了keap1和cul3之间的相互作用(cleasby a.,yon j.,day p.j.等人,structure of the btb domain of keap1 and its interaction with the triterpenoid antagonist cddo.plos one.2014;9(6,article e98896);iso t.,suzuki t.,baird l.,yamamoto m.molecular and cellular biology.2016;36(24):3100
–
3112;dayalan naidu s.,muramatsu a.,saito r.等人,scientific reports.2018;8(1):p.8037)。结果,keap1被锁定在nrf2结合构象中,新表达的nrf2从而逃脱了keap1-cul3介导的泛素化。
16.bardoxolone进入了治疗晚期慢性肾病(ckd)和2型糖尿病的临床试验(pergola p.e.,raskin p.,toto r.d.等人,the new england journal of medicine.2011;365(4):327
–
336)。尽管ii期临床试验表明肾小球滤过长期增加,但由于心血管安全问题,该化合物在iii期停止(zhang d.d.antioxidants&redox signaling.2013;19(5):517
–
518.doi:10.1089/ars.2012.5118)。kyowa kirin最近开始了一项新的bardoxolone在糖尿病肾病患者中的iii期临床试验(ayame研究),以更好地确定cddo-me的安全性和有效性。目前,bardoxolone也在进行alport综合征(2/3期cardinal试验)和肺动脉高压(3期catalyst试验)的临床研究。此外,reata正在开发bardoxolone用于罕见的ckd形式,包括常染色体显性
遗传多囊肾病(adpkd)、iga肾病(igan)、1型糖尿病ckd(t1d ckd)和局灶节段性肾小球硬化症(fsgs)。bardoxolone的第二代衍生物,称为omaveloxone(rta-408),正在对friedreich共济失调的关键性注册moxie试验进行临床研究(lynch d.r.,farmer j.,hauser l.等人,annals of clinical translational neurology.2019;6(1):15
–
26;https://www.reatapharma.com/our-science/pipeline/)。
17.已经提出了几种额外的机制来解释nrf2在应激条件下与keap1的解离。除了keap1的半胱氨酸残基的氧化和靶向dlg和etge结合位点外,p62与keap1的结合以及gsk3对nrf2的磷酸化也受到了特别的关注。
18.p62,也称为sequestosome 1(sqstm1),是一种泛素结合蛋白,可通过自噬途径靶向降解蛋白质聚集体。p62与nrf2竞争结合keap1,p62与keap1的结合导致keap1的降解和随之而来的nrf2稳定化(komatsu m,kurokawa h,waguri s,taguchi k,kobayashi a,ichimura y等人,nat cell biol 2010;12(3):213
–
23;lau a,wang xj,zhao f,villeneuve nf,wu t,jiang t等人,.mol cell biol 2010;30(13):3275
–
85)。p62基因启动子包含一个are,并通过诱导are驱动的p62基因转录创建一个nrf2驱动的正反馈环(jain a,lamark t,sjottem e,larsen kb,awuh ja,overvatn a等人,j biol chem 2010;285(29):22576
–
91)。由于p62是选择性自噬的货物受体,keap1-nrf2与自噬具有有趣的功能相互作用(towers cg,fitzwalter be,regan d,goodspeed a,morgan mj,liu cw等人,dev cell 2019.23;50(6):690-703.doi:10.1016/j.devcel.2019.07.010)。
19.nrf2的稳定性也受到糖原合酶激酶(gsk)-3介导的磷酸化的调节。gsk-3磷酸化位于nrf2的neh6结构域的dsgis基序,从而为含有e3泛素蛋白连接酶(β-trcp)的β-转导素重复序列创建一个识别位点。这种相互作用将nrf2靶向于泛素依赖性蛋白酶体降解(rada p1,rojo ai,chowdhry s,mcmahon m,hayes jd,cuadrado a.mol cell biol.(2011)mar;31(6):1121-33)。这些数据可能表明gsk-3抑制剂可用作nrf2激活剂。
20.除了富马酸二甲酯分别用于治疗复发-缓解型多发性硬化症和银屑病外,许多研究都支持nrf2激活剂的广泛治疗潜力。
21.nrf2在防护反应性亲电子试剂方面的重要性首先用对乙酰氨基酚进行了证实。在对乙酰氨基酚暴露后,nrf2敲除小鼠与wt小鼠相比表现出更大的肝毒性,表现为血清alt值增加和肝脏组织学改变(chan k,han x,kan y.proc natl acad sci u s a 2001;98:4611
–
4616;enomoto a,itoh k,nagayoshi e,haruta j,kimura t,o'connor t,harada t,yamamoto m.toxicol sci 2001;59:169
–
177)。
22.对乙酰氨基酚还显示在无毒剂量下激活nrf2的核转位,从而说明nrf2在协调导致对乙酰氨基酚毒性减弱的适应性反应中的作用(goldring c,kitteringham n,elsby r,randle l,clement y,williams d,mcmahon m,hayes j,itoh k,yamamoto m,park b.hepatology 2004;39:1267
–
1276)。这种适应性反应导致谷胱甘肽从头合成和反应性对乙酰氨基酚代谢物的结合和排泄增加。通过使用肝细胞特异性条件性keap1敲除小鼠进一步证实了这一观察结果,该模型中nrf2信号通路的抑制成分不存在,导致nrf2升高和持续的核积累。由于nrf2调节的细胞保护酶水平较高,这些条件性敲除小鼠对对乙酰氨基酚毒性的抵抗力明显高于wt小鼠(okawa h,motohashi h,kobayashi a,aburatani h,kensler t,yamamoto m.biochem biophys res commun 2006;339:79
–
88)。
x.front pharmacol.2018;9:1428)。已发现nrf2是防止nash发展的关键调节剂(gupte a.a.,lyon c.j.,hsueh w.a.(2013)..curr.diabetes rep.13 362
–
371.10.1007/s11892-013-0372-1),反之,已发现nrf2的缺乏或缺失会导致良性脂肪变性,其进而发展为nash并导致疾病状态恶化(chowdhry s.,nazmy m.h.,meakin p.j.,dinkova-kostova a.t.,walsh s.v.,tsujita t.等人,(2010).free radic.biol.med.48 357
–
371;wang c.,cui y.,li c.,zhang y.,xu s.,li x.等人,(2013).lipids health dis.12:165.10.1186/1476-511x-12-165;ramadori p.,drescher h.,erschfeld s.,fragoulis a.,kensler t.w.,wruck c.j.等人,(2017).oxid.med.cell.longev.2017:3420286)。在p62:nrf2双敲除(dko)小鼠中也研究了nash的发展。dko小鼠表现出严重的肝肿大和脂肪性肝炎、摄食过多引起的肥胖伴胰岛素抵抗和脂肪因子失衡(akiyama k,warabi e,okada k,yanagawa t,ishii t,kose k,tokushige k,ishige k,mizokami y,yamagata k,onizawa k,ariizumi si,yamamoto m,shoda j.exp anim.2018 may 10;67(2):201-218)。
28.sharma及其同事通过使用nrf2激活小分子tbe-31证明了nrf2在nash中的保护作用。tbe31治疗逆转了高脂肪高果糖喂养的野生型小鼠的胰岛素抵抗,但在nrf2缺失小鼠中没有。此外,tbe-31治疗小鼠显著降低了肝脏脂肪变性和脂质合成基因的表达,同时增加了脂肪酸氧化和脂蛋白组装基因的肝脏表达。此外,tbe-31治疗降低了喂食高脂肪高果糖的野生型小鼠肝脏中的er应激、炎症基因的表达以及细胞凋亡、纤维化和氧化应激的标志物。相比之下,tbe-31并未减少hffr喂养的nrf2缺失小鼠肝脏中的脂肪变性、er应激、脂肪生成、炎症、纤维化或氧化应激。作者得出结论,在已经变得肥胖和胰岛素抵抗的小鼠中,nrf2的药理学激活可逆转胰岛素抵抗,抑制肝脂肪变性,并减轻nash和肝纤维化。这些作用主要归因于对er、炎症和氧化应激的抑制(sharma rs,harrison dj,kisielewski d,cassidy dm,mcneilly ad,gallagher jr,walsh sv,honda t,mccrimmon rj,dinkova-kostova at,ashford mlj,dillon jf,hayes jd cell mol gastroenterol hepatol.2017 dec 13;5(3):367-398)。
29.还使用nrf2-ko小鼠证明了在急性高剂量酒精暴露后nrf2的肝脏保护作用。酒精处理导致这些动物的肝脏和胰腺损伤以及胰腺β细胞损伤显著恶化(sun j,fu j,zhong y,li l,chen c,wang x,wang l,hou y,wang h,zhao r,zhang x,yamamoto m,xu y,pi j.food chem toxicol.2018 nov;121:495-503)。
30.nrf2激活剂对与氧化应激和炎症增加、氧化还原电位受损、解毒受损和代谢失调有关的疾病/适应症具有潜在用途。
31.分别基于nrf2敲除、keap1敲除、基因多态性和化合物介导的nrf2激活研究,为包括以下在内的疾病提供了证据:i型糖尿病和ii型糖尿病以及相关并发症如糖尿病心肌病、糖尿病视网膜病变、糖尿病神经病变、糖尿病肾病和糖尿病伤口愈合;孕妇糖尿病;肝病,例如非酒精性脂肪性肝炎(nash)、非酒精性脂肪肝病、毒素引起的肝病(例如,对乙酰氨基酚引起的肝病)、酒精性肝病(ald)、胆汁淤积、原发性硬化性胆管炎(psc)、病毒性肝炎、肝硬化、原发性胆汁性肝硬化(pbc)、终末期肝病、纤维化;肾脏疾病,如慢性肾病(ckd)、急性肾损伤、造影剂肾病、常染色体显性多囊肾病(adpkd)、和alport综合征、败血症引起的急性肾损伤;肾移植期间出现的肾脏疾病或功能障碍、局灶节段性肾小球硬化、iga肾小球肾炎/肾病、纤维化;肺部疾病,例如肺纤维化、特发性肺纤维化(ipf)、囊性纤维化、急性
肺损伤、肺部感染、慢性阻塞性肺病(copd)、肺气肿、肺动脉高压、环境暴露继发性肺病、慢性和急性哮喘、急性呼吸窘迫综合征;心脏病,例如动脉粥样硬化、高血压、心力衰竭、中风、心肌病、冠心病、心肌缺血;神经元损伤、创伤性脑损伤、抑郁症、癫痫、肝性脑病、亨廷顿病、帕金森病、阿尔茨海默病、自闭症、弗里德赖希共济失调、肌萎缩侧索硬化症(als)、多发性硬化症(ms)、中风、脑梗塞、脑病、神经元受损/损伤,脊髓损伤;炎症性疾病,例如炎症性肠病、溃疡性结肠炎、克罗恩病、胰腺炎、关节炎、狼疮性肾炎;眼部疾病,例如年龄相关性黄斑变性(amd)、眼部神经退行性疾病、年龄相关性黄斑变性、白内障、青光眼、眼部损伤、fuchs内皮性角膜营养不良(fecd)、葡萄膜炎、视神经病变/眼部神经退行性疾病;结肠癌;自身免疫性疾病;牛皮癣、皮炎/辐射的局部影响、辐射暴露引起的免疫抑制、先兆子痫、高原反应;伤口愈合;代谢综合征;线粒体肌病;疟疾;铁死亡/铁过载;过敏性接触性皮炎;酒精依赖;淀粉样变性;贫血;焦虑症;阿斯伯格综合症;湿疹;脑水肿;脑缺血;脑血管疾病;慢性疲劳综合症;认知能力下降;皮炎/辐射引起的皮炎;杜氏肌营养不良症;浮肿;脑炎;男性/女性生育能力;骨折愈合;胃食管反流病;听力损失;流感感染;肠屏障功能障碍;骨关节炎;骨质疏松症;辐射引起的损伤;反流性食管炎;再灌注损伤(脑、心、肾、肝、视网膜);精神分裂症;癫痫发作;干燥综合征;镰状细胞性贫血症;皮肤溃疡;血管内皮功能障碍;血脑屏障功能障碍;唐氏综合症。
32.wo 2015/092713公开了作为nrf2调节剂的二芳基化合物。
33.本发明尤其涉及式(i)的化合物:
[0034][0035]
其中
[0036]
z是-o-(ch2)n
1-、-o-(ch2)n
1-o-(ch2)n2、-o-(ch2)n
1-s-(ch2)n2、o-(ch2)n
1-s(o)-(ch2)n2、o-(ch2)n
1-s(o2)-(ch2)n2、-o-(ch2)n
1-nr-(ch2)n2、-o-(ch2)n
1-chr
’‑
(ch2)n2、-nr-(ch2)n
1-、-nr-(co)-(ch2)n
1-、-o-(ch2)n
1-ar-(ch2)n2、-o-(ch2)n
1-ar-o-(ch2)n2、-o-(ch2)n
1-ar-s-(ch2)n2、-o-(ch2)n
1-ar-s(o)-(ch2)n2、-o-(ch2)n
1-ar-s(o2)-(ch2)n2、-o-(ch2)n
1-ar-chr
’‑
(ch2)n2、-o-(ch2)n
1-ar-ch=ch-、o-ar-nr-(ch2)n1、-(ch2)n
1-nr-(co)-(ch2)n
2-[0037]
或者z是
[0038]
y1是c或n,
[0039]
y2是o或nr’,
[0040][0041]
ar是任选取代的芳基或杂芳基,
[0042]
r是氢原子、直链或支链的c
1-c3烷基或任选取代的芳基,
[0043]
r’是氢原子或选自下列的基团:羟基、任选取代的芳基和任选地被烷氧基或被1至3个卤原子取代的直链或支链的c
1-c3烷基,
[0044]
n1、n2是1至6的整数,
[0045]
r1、r2、r4、r8、r9、r
10
相同或不同,并且各自是氢原子或选自下列的基团:卤素、氰基、任选地被1至3个卤原子取代的直链或支链的c
1-c3烷基、直链或支链的c
1-c3烷氧基或任选取代的芳基,
[0046]
r3是氢或任选地被1至3个卤原子取代的直链或支链的c
1-c3烷基,
[0047]
r1、r2、r4、r8、r9、r
10
相同或不同,并且各自是氢原子或选自下列的基团:卤素、氰基、任选地被1至3个卤原子取代的直链或支链的c
1-c3烷基、直链或支链的c
1-c3烷氧基或任选取代的芳基,
[0048]
r3是氢或任选地被1至3个卤原子取代的直链或支链的c
1-c3烷基,
[0049]
或者r2和r3与携带它们的原子一起形成一个环,
[0050]
r5、r6相同或不同,并且各自是氢、氘或卤原子或直链或支链的c
1-c3烷基,
[0051]
r7是选自羟基和nhr
’7的基团,
[0052]
其中r
’7是直链或支链的c
1-c6烷基或任选取代的芳基或杂芳基,
[0053]
其光学异构体及其与药学上可接受的碱的加成盐。
[0054]“芳基”是指任选被一个或多个相同或不同的基团取代的苯基、萘基或联苯基,所述基团选自卤素、羟基、氨基、任选被1-3个卤原子取代的直链或支链(c
1-c6)-烷基、羧基、氰基、任选被1-3个卤原子取代的直链或支链(c
1-c6)-烷氧基、任选被一个或两个直链或支链(c
1-c6)-烷基n-取代的直链或支链(c
1-c6)-氨基烷基、任选被1-3个卤原子取代的直链或支
chr
’‑
(ch2)n2、-(ch2)n
1-ar
1-(ch2)n2、-ch2)n
1-ar
1-o-(ch2)n2、-(ch2)n
1-ar
1-s-(ch2)n2、-(ch2)n
1-ar
1-chr
’‑
(ch2)n2、-ar
1-nr-(ch2)n1,
[0066]
或者z1是
[0067]
其光学异构体及其与药学上可接受的碱的加成盐。
[0068]
本发明的另一方面涉及式(ib)的化合物,式(i)化合物的一种具体情况:
[0069][0070]
其中z、y1、y2、r1至r7如上所定义,
[0071]
其光学异构体及其与药学上可接受的碱的加成盐。
[0072]
本发明的另一方面涉及式(ic)的化合物,式(i)化合物的一种具体情况:
[0073][0074]
z、y1、y2、r1至r8和r
10
如上所定义,
[0075]
其光学异构体及其与药学上可接受的碱的加成盐。
[0076]
本发明的另一方面涉及式(i)的化合物,其中z是-o-(ch2)n
1-、-o-(ch2)n
1-o-(ch2)n2或-o-(ch2)n
1-s-(ch2)n2。
[0077]
本发明的另一方面涉及式(i)的化合物,其中y1是c。
[0078]
本发明的另一方面涉及式(i)的化合物,其中y2是o或nch3。
[0079]
本发明的另一方面涉及式(i)的化合物,其中是
[0080]
本发明的另一方面涉及式(i)的化合物,其中r7是羟基。
[0081]
本发明的另一方面涉及从式(ii)的化合物开始制备式(ia1)的化合物(式(i)化合物的一种具体情况)的方法:
[0082][0083]
其中p1是酸官能团的保护基例如烷基,p2是醇官能团的保护基,
[0084]
所述式(ii)的化合物与式(iii)的化合物反应:
[0085][0086]
其中r
1-r3和y1如关于式(i)所定义,
[0087]
生成式(iv)的化合物:
[0088][0089]
其中r
1-r3、r
8-r9、y1、z1和p
1-p2如上所定义,
[0090]
将式(iv)的化合物与式(v)的化合物反应:
[0091][0092]
其中r4和y2如关于式(i)所定义,p3是醇官能团的保护基,
[0093]
生成式(vi)的化合物:
[0094][0095]
其中r
1-r4、r
8-r9、y1、y2、z1和p
1-p3如上所定义,
[0096]
将式(vi)的化合物脱保护得到式(vii)的化合物:
[0097][0098]
其中r
1-r4、r
8-r9、y1、y2、z1和p1如上所定义,
[0099]
将式(vii)的化合物卤化得到式(viii)的化合物:
[0100][0101]
其中r
1-r4、r
8-r9、y1、y2、z1和p1如上所定义,并且x是卤原子例如br或cl,
[0102]
将式(viii)的化合物与碱(例如cs2co3)反应得到式(ix)的化合物:
[0103][0104]
将式(ix)的化合物通过碱例如lioh的反应脱保护得到式(ia1)的化合物,如果需要,将其立体异构体用手性分离技术进行分离。
[0105]
本发明的化合物是nrf2活化剂。
[0106]
因此,它们可用于治疗与氧化应激和炎症增加、氧化还原电位受损、解毒受损和代谢失调有关的疾病,包括:i型糖尿病和ii型糖尿病以及相关并发症如糖尿病心肌病、糖尿病视网膜病变、糖尿病神经病变、糖尿病肾病和糖尿病伤口愈合;孕妇糖尿病;肝病,例如非酒精性脂肪性肝炎(nash)、非酒精性脂肪肝病、毒素引起的肝病(例如,对乙酰氨基酚引起的肝病)、酒精性肝病(ald)、胆汁淤积、原发性硬化性胆管炎(psc)、病毒性肝炎、肝硬化、原发性胆汁性肝硬化(pbc)、终末期肝病、纤维化;肾脏疾病,如慢性肾病(ckd)、急性肾损伤、造影剂肾病、常染色体显性多囊肾病(adpkd)、和alport综合征、败血症引起的急性肾损伤;肾移植期间出现的肾脏疾病或功能障碍、局灶节段性肾小球硬化、iga肾小球肾炎/肾病、纤维化;肺部疾病,例如肺纤维化、特发性肺纤维化(ipf)、囊性纤维化、急性肺损伤、肺部感染、慢性阻塞性肺病(copd)、肺气肿、肺动脉高压、环境暴露继发性肺病、慢性和急性哮喘、急性呼吸窘迫综合征;心脏病,例如动脉粥样硬化、高血压、心力衰竭、中风、心肌病、冠心病、心肌缺血;神经元损伤、创伤性脑损伤、抑郁症、癫痫、肝性脑病、亨廷顿病、帕金森病、阿尔茨海默病、自闭症、弗里德赖希共济失调、肌萎缩侧索硬化症(als)、多发性硬化症(ms)、中风、脑梗塞、脑病、神经元受损/损伤,脊髓损伤;炎症性疾病,例如炎症性肠病、溃疡性结肠炎、克罗恩病、胰腺炎、关节炎、狼疮性肾炎;眼部疾病,例如年龄相关性黄斑变性(amd)、眼部神经退行性疾病、年龄相关性黄斑变性、白内障、青光眼、眼部损伤、fuchs内皮性角膜营养不良(fecd)、葡萄膜炎、视神经病变/眼部神经退行性疾病;结肠癌;自身免疫性疾病;牛皮癣、皮炎/辐射的局部影响、辐射暴露引起的免疫抑制、先兆子痫、高原反应;伤口愈合;代谢综合征;线粒体肌病;疟疾;铁死亡/铁过载;过敏性接触性皮炎;酒精依赖;淀粉样变性;贫血;焦虑症;阿斯伯格综合症;湿疹;脑水肿;脑缺血;脑血管疾病;慢性疲劳综合症;认知能力下降;皮炎/辐射引起的皮炎;杜氏肌营养不良症;浮肿;脑炎;男性/女性生育能力;骨折愈合;胃食管反流病;听力损失;流感感染;肠屏障功能障碍;骨关节炎;骨质疏松症;辐射引起的损伤;反流性食管炎;再灌注损伤(脑、心、肾、肝、视网膜);精神分裂症;癫痫发作;干燥综合征;镰状细胞性贫血症;皮肤溃疡;血管内皮功能障碍;血脑屏障功能障碍;唐氏综合症。
[0107]
本发明的化合物特别适用于治疗ii型糖尿病和nash。
[0108]
本发明还涉及包含式(i)化合物与一种或多种惰性、无毒、药学上可接受的赋形剂或载体的药物组合物。
[0109]
有用的剂量根据患者的年龄和体重、给药途径、疾病的性质和严重程度以及任何相关治疗而变化,并且在每天0.5mg至1000mg的范围内,分一次或多次给药。
[0110]
在根据本发明的药物组合物中,可以更特别地提及适用于口服、肠胃外(静脉内、肌肉内或皮下)、经皮或透皮、经鼻、直肠、经舌、眼部或呼吸给药的那些,尤其是片剂或糖衣丸、舌下片剂、明胶胶囊、胶囊、栓剂、乳膏、软膏、皮肤凝胶、注射或饮用制剂、气雾剂和滴眼剂或滴鼻剂。
[0111]
根据本发明的一个方面,药物组合物是用于口服给药的片剂。
[0112]
除了式(i)化合物之外,本发明的片剂还包含一种或多种赋形剂或载体,例如稀释剂、润滑剂、粘合剂、崩解剂、吸收剂、着色剂和甜味剂。
[0113]
作为赋形剂或载体的例子可以提及:
[0114]
◆
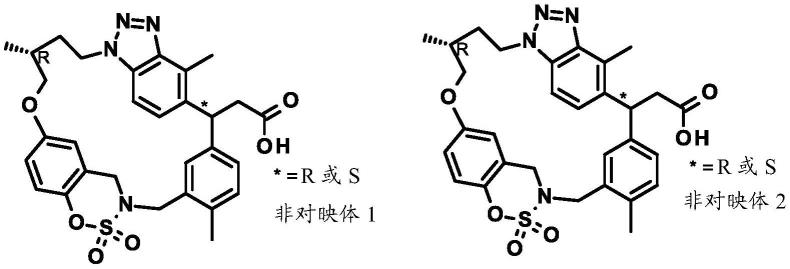
作为稀释剂:乳糖、右旋糖、蔗糖、甘露醇、山梨糖醇、纤维素、甘油,
[0115]
◆
作为润滑剂:二氧化硅、滑石、硬脂酸及其镁盐和钙盐、聚乙二醇,
[0116]
◆
作为粘合剂:硅酸铝和镁、淀粉、明胶、黄蓍胶、甲基纤维素、羧甲基纤维素钠和聚乙烯吡咯烷酮,
[0117]
◆
作为崩解剂:琼脂、海藻酸及其钠盐、泡腾混合物。
[0118]
片剂中式(i)的活性成分的百分比优选为5重量%至50重量%。
[0119]
根据本发明的一个方面,本发明的式(i)化合物与一种或多种附加活性成分联合给药。
[0120]
联合给药可以是将两种或多种各自含有一种活性成分的单独的药物组合物同时或连续共同给药的形式(自由联合),或者是两种或多种活性成分在同一药物组合物中的固定联合给药的形式。
[0121]
更具体地,式(i)化合物及其药学上可接受的盐可以与一种或多种可用于预防或治疗糖尿病或nash的其他活性成分组合使用,包括双胍类、磺酰脲类、dpp 4抑制剂、sglt2抑制剂、glp1激动剂、双重glp1-gcg或glp1-gip激动剂、fxr激动剂、ppar调节剂、甲状腺激素受体激动剂、fgf21激动剂、fgf19激动剂、dgat2抑制剂、acc抑制剂或fas抑制剂。
[0122]
缩写
[0123]
abs.:绝对
[0124]
acoh:乙酸
[0125]
aq.:含水的
[0126]ata
phos.pdcl2:双(二-叔丁基(4-二甲基氨基苯基)膦)二氯化钯(ii)
[0127]
cs2co3:碳酸铯
[0128]
℃:摄氏度
[0129]
dcm:二氯甲烷
[0130]
ddq:2,3-二氯-5,6-二氰基-1,4-苯醌
[0131]
dia:非对映异构体
[0132]
diad:偶氮二甲酸二异丙酯
[0133]
二氧杂环己烷:1,4-二氧杂环己烷
[0134]
dipea:二异丙基乙基胺,n-乙基-n-(丙-2-基)丙-2-胺
[0135]
dmem:达尔伯克(氏)改良伊格尔(氏)培养基
[0136]
dmf:n,n-二甲基甲酰胺
[0137]
dmso:二甲亚砜
[0138]
e1:第一洗脱的对映体
[0139]
e2:第二洗脱的对映体
[0140]
et2o:乙醚
[0141]
etoac:乙酸乙酯
[0142]
etoh:乙醇
[0143]
fbs:胎牛血清
[0144]
g:克
[0145]
h:小时
[0146]
hcl:盐酸
[0147]
hcooh:甲酸
[0148]
hec:羟乙基纤维素
[0149]
h2so4:硫酸
[0150]
hplc:高效液相色谱
[0151]
hrms:高分辨质谱
[0152]
ipa:丙-2-醇
[0153]
k2co3:碳酸钾
[0154]
lc:液相色谱
[0155]
lc-ms:液相色谱-质谱
[0156]
lioh:氢氧化锂
[0157]
m:摩尔
[0158]
meoh:甲醇
[0159]
mecn:乙腈
[0160]
mg:毫克
[0161]
mgso4:硫酸镁
[0162]
mhz:兆赫
[0163]
min:分钟
[0164]
ml:毫升
[0165]
mmol:毫摩尔
[0166]
ms:质谱
[0167]
mtbe:甲基-叔丁基醚
[0168]
n2:氮气
[0169]
nacl:氯化钠
[0170]
nah:氢化钠
[0171]
naoh:氢氧化钠
[0172]
nahco3:碳酸氢钠
[0173]
na2so4:硫酸钠
[0174]
nbs:n-溴代琥珀酰亚胺
[0175]
nh4hco3:碳酸氢铵
[0176]
nh4cl:氯化铵
[0177]
nmr:核磁共振
[0178]
nmp:n-甲基吡咯烷酮
[0179]
pd/c:钯/活性碳
[0180]
pd2(dba)
3:
三(二亚苄基丙酮)二钯(0)
[0181]
pph3:三苯基膦
[0182]
quant.:定量收率
[0183]
rac:外消旋
[0184]
rt:室温
[0185]
sat.:饱和的
[0186]
tbuxphos:2-二-叔丁基膦-2',4',6'-三异丙基联苯
[0187]
tea:三乙胺
[0188]
tfa:三氟乙酸
[0189]
thf:四氢呋喃
[0190]
wt%:重量百分比
[0191]
通用信息
[0192]
iupac化学名称是使用acd/labs 2018 2.2(文件版本c60h41,build 106041,2018年12月7日)生成的。
[0193]
所有得自商品来源的试剂都不经进一步纯化直接使用。无水溶剂得自商品来源并且不经进一步干燥直接使用。
[0194]
正相硅胶(快速)色谱在isco combiflash rf 200i上进行,预装硅胶柱( gold high performance)。
[0195]
在anton parr monowave或cem 仪器中进行微波加热。
[0196]
反相(制备型)hplc纯化在hanbon np7000液相色谱系统上进行,配备 5μm c18,250mm
×
50mm内径色谱柱,以99.9ml min-1
的流速运行,uv二极管阵列检测(210
–
400nm),使用纯水或5mm nh4hco3水溶液,或5mm hcooh水溶液,或5mm tfa水溶液和mecn作为洗脱剂,除非另有说明。
[0197]
分析lc-ms:本发明的化合物通过agilent hp1200上的高效液相色谱-质谱(hplc-ms)和agilent 6140四极杆lc/ms进行表征,以正离子或负离子电喷雾电离模式操作。分子量扫描范围为100至1350。平行紫外检测在210nm和254nm进行。样品以1mm的acn溶液或thf-水(1:1)溶液的形式提供,并带有5μl定量环进样。lc-ms分析在两台仪器上进行,其中一台使用碱性洗脱剂,另一台使用酸性洗脱剂。
[0198]
碱性lc-ms:gemini-nx,3μm,c18,50mm
×
3.00mm内径色谱柱,在23℃下进行,流速为1ml min-1
,使用5mm nh4hco3(溶剂a)和乙腈(溶剂b)梯度洗脱,在不同/一定的时间内,从100%溶剂a开始,以100%溶剂b结束。
[0199]
酸性lcms:zorbax eclipse xdb-c18,1.8μm,50mm
×
4.6mm内径色谱柱,在40℃下
进行,流速为1ml min-1
,使用0.02%v/v hcooh水溶液(溶剂a)和0.02%v/v hcooh的mecn溶液(溶剂b)梯度洗脱,在不同/一定的时间内,从100%溶剂a开始,以100%溶剂b结束。
[0200]1h-nmr测定用bruker avance iii 500mhz光谱仪和bruker avance iii 400mhz光谱仪进行,用dmso-d6(六氘代二甲基亚砜)或cdcl3(氘代氯仿)作为溶剂。1h nmr数据为δ值的形式,以百万分率(ppm)给出,采用溶剂残留峰(dmso-d6为2.50ppm,cdcl3为7.26ppm)作为内标。分裂模式被指定为:s(单峰),2s(2x单峰),d(二重峰),2d(2x二重峰),t(三重峰),2t(2x三重峰),q(四重峰),2q(2x四重峰),quint(五重峰),sept(七重峰),m(多重峰),2m(2x多重峰),brs(宽单峰),brd(宽二重峰),brt(宽三重峰),brq(宽四重峰),brm(宽多重峰),vbrs(极宽单峰),dd(双二重峰),td(三二重峰),dt(双三重峰),dq(双四重峰),ddd(双双二重峰),dm(双多重峰),tm(三多重峰),qm(四多重峰)。
[0201]
hrms在shimadzu it-tof上测定,离子源温度200℃,esi+/-,电离电压:(+-)4.5kv。质量分辨率最小10000。
[0202]
使用sfc-piclab-prep 200设备(pic solution)通过以下方法,使用手性超临界流体色谱(sfc)以毫克级将最终产物或最终中间体分离为纯对映异构体/非对映异构体:
[0203]
●
流动相是二氧化碳作为超临界流体或混合流体(通过添加质子溶剂,例如:等度35-45%ipa或etoh/超临界co2)
[0204]
●
根据色谱图选择色谱柱,例如:
[0205]
whelk 01 rr 30x250mm x 5μm(粒度)或
[0206]
lux(phenomenex)30mm x 150mm x 5μm(粒度)或
[0207]
chiralpak ig 30x250mm x 5μm(粒度)
[0208]
●
温度:40℃
[0209]
●
检测:230nm
[0210]
●
流速:120-150ml/min。
[0211]
下面的实施例说明了本发明。
[0212]
通用方法1
[0213]
通用方法1步骤1
[0214]
向1-氟-3-甲基-2-硝基-苯(1eq.,64.5mmol)的mecn(2ml/mmol,101.3g,128.92ml)溶液中在室温下加入氨基醇(3eq.,193.5mmol)。将反应混合物加热至70℃并搅拌过夜。反应完成后,将溶剂减压蒸发。将残余物在250ml水和200ml etoac之间进行分配。将分离出的有机层进一步用150ml盐水洗涤。将合并的水层用100ml etoac洗涤。将合并的有机层用无水硫酸钠干燥,过滤,浓缩至干得到粗产物,将其通过正相硅胶色谱纯化,用庚烷-etoac(例如100:0至75:25)作为洗脱剂得到标题化合物。
[0215]
通用方法1步骤2
[0216]
向通用方法1步骤1的产物(1eq.,834mmol)的acoh(1.2ml/mmol,42g,40ml)溶液中在室温下加入nbs(1eq.,6g,34mmol)。将反应混合物加热至110℃并搅拌2小时。反应完成后,将混合物冷却至室温并用200ml冰水淬灭。将ph用naoh溶液调节至14。将混合物在室温下搅拌10分钟。将混合物用3x150ml dcm萃取。将合并的有机层用盐水洗涤。将有机相用无水硫酸钠干燥,过滤,浓缩至干得到标题化合物,其不经进一步纯化直接用于下一步骤,或用反相色谱纯化,用水-mecn作为洗脱剂。
[0217]
通用方法1步骤3
[0218]
向通用方法1步骤2的产物(1eq.,35.1mmol)或适当的芳基硝基化合物的etoh(25ml/mmol,692g,877ml)和水(3ml/mmol,105g,105ml)溶液中在室温下加入铁粉(15eq.,29.4g,526mmol)和nh4cl(5eq.,9.38g,175mmol)。将反应混合物加热至50℃并搅拌2小时。反应完成后,将混合物通过硅藻土垫过滤,然后用2x100ml etoh洗涤。将溶剂减压蒸发,将蒸发的残余物溶于100ml dcm。将溶液用无水硫酸钠干燥,过滤,浓缩至干得到标题化合物,其不经进一步纯化直接用于下一步骤。
[0219]
通用方法1步骤4
[0220]
向通用方法1步骤3的产物(1eq.,32mmol)的acoh(0.3ml/mmol,10g,9.6ml)和水(3ml/mmol,96g,96ml)溶液中在0℃下加入h2so4(0.3ml/mmol,18g,9.6ml)。分批加入亚硝酸钠(1.5eq.,3.3g,48mmol)并将反应混合物在0℃下搅拌10分钟。将形成的黑色异相混合物升温至室温并继续搅拌30分钟。反应完成后,将混合物用300ml水淬灭并将ph用浓naoh溶液调节至~12。将混合物用3x70ml dcm萃取。将有机层用150ml盐水洗涤。将有机层用无水硫酸钠干燥,过滤,浓缩至干得到黑色油,将其通过正相硅胶色谱纯化,用dcm-etoac(100:0至70:30)作为洗脱剂得到标题化合物。
[0221]
通用方法1步骤5
[0222]
向通用方法1步骤4的产物(1eq.,22mmol)的thf(10ml/mmol,200g,220ml)、水(5ml/mmol,110g,110ml)和meoh(2.5ml/mmol,44g,55ml)溶液中在室温下加入lioh(3eq.,1.6g,66mmol)并将混合物继续搅拌30分钟。反应完成后,将混合物用400ml水和50ml 2m hcl水溶液淬灭。将混合物用3x20ml etoac萃取。将有机层用盐水洗涤并用无水硫酸钠干燥,过滤,浓缩至干得到油状物,将其通过正相硅胶色谱纯化,用dcm-etoh(100:0至80:20)作为洗脱剂得到标题化合物。
[0223]
通用方法1步骤6
[0224]
向通用方法1步骤5的产物(1eq.,10mmol)的thf(7ml/mmol,63g,70ml)溶液中在0℃下加入nah(1.2eq.,480mg,12mmol,60wt%的矿物油溶液)。将混合物升温至室温并在该温度下搅拌30分钟。将反应混合物冷却至0℃,加入4-甲氧基-苄基氯(1.2eq.,1.9g,12mmol)并将混合物在室温下搅拌过夜。反应完成后,将混合物用100ml水淬灭并用3x100ml etoac萃取。将合并的有机层用盐水洗涤。将有机层用无水硫酸钠干燥,过滤,浓缩至干得到橙色油,将其通过正相硅胶色谱纯化,用庚烷-etoac(100:0至75:25)作为洗脱剂得到标题化合物。
[0225]
通用方法1步骤7
[0226]
向通用方法1步骤6的产物(1eq.,7.1mmol)的dmf(7ml/mmol,47.4g,50ml)溶液中在室温下加入丙-2-烯酸乙酯(2eq.,1.44g,1.56ml,14.2mmol)、dipea(3eq.,2.78g,3.75ml,21.5mmol)、三-邻-甲苯基膦(0.2eq.,0.44g,1.4mmol)和二乙酸钯(0.1eq.0.161g,0.71mmol)。将混合物用氩气冲洗两次并在封闭的schlenk试管中于100℃加热过夜。反应完成后,将溶剂减压蒸发至干得到黑色油,将其通过正相硅胶色谱纯化,用庚烷-etoac(100:0至75:25)作为洗脱剂得到标题化合物。
[0227]
通用方法2
[0228]
通用方法2步骤1
[0229]
向1-氟-3-甲基-2-硝基-苯(1eq.,1.93mmol)的mecn(2ml/mmol,101.3g,128.92ml)溶液中在室温下加入邻-苄基-氨基醇(1.2eq.,2.32mmol),然后加入cs2co3(2eq.,1.26g,3.87mmol)或tea(2eq.,3.87mmol)。将反应混合物加热至70℃并在该温度下搅拌过夜。反应完成后,将混合物过滤,将母液减压蒸发。将粗产物通过反相色谱纯化,用水-mecn梯度洗脱(95:5至0:100)得到标题化合物。
[0230]
通用方法2步骤2
[0231]
向通用方法2步骤1的产物(1eq.,22mmol)的acoh(26ml)溶液中在室温下加入nbs(1.2eq.,4.6g,26mmol)。将反应混合物加热至110℃并搅拌1.5h。反应完成后,将混合物冷却至室温,用200ml冰水淬灭反应。将ph用naoh溶液调节至14。将混合物在室温下搅拌10分钟。将混合物用3x150ml dcm萃取。将合并的有机层用盐水洗涤。将有机相用无水硫酸钠干燥,过滤,浓缩至干得到标题化合物,将其通过反相色谱纯化,用水-mecn梯度洗脱(95:5至0:100)得到标题化合物。
[0232]
通用方法2步骤3
[0233]
向通用方法2步骤2的产物(1eq.,17mmol)的etoh(430ml)(或ipa)和水(50ml)溶液中在室温下加入铁粉(15eq.,14g,260mmol)和nh4cl(5.5eq.,5g,93.5mmol)。将反应混合物加热至50℃并在该温度下搅拌过夜。反应完成后,将混合物通过硅藻土垫过滤,并用2x100ml etoh洗涤。将母液减压浓缩。将粗产物通过反相色谱纯化,用水-mecn梯度洗脱(95:5至0:100)得到标题化合物。
[0234]
通用方法2步骤4
[0235]
向通用方法2步骤3的产物(1eq.,13mmol)的acoh(30ml)和水(30ml)溶液中在0℃下加入h2so4(8.9g,4.6ml,90mmol)。分小批加入亚硝酸钠(1.5eq.,3.3g,48mmol)并将反应混合物在0℃下搅拌10分钟。将形成的黑色异相混合物升温至室温并在该温度下继续搅拌30分钟。反应完成后,将混合物用300ml水淬灭并将ph用2m naoh水溶液调节至~12。将混合物用3x70ml dcm萃取。将合并的有机层用150ml盐水洗涤。将有机层用无水硫酸钠干燥,过滤,浓缩至干得到粗产物,将其通过正相硅胶色谱纯化,用dcm-etoac(100:0至95:5)作为洗脱剂得到标题化合物。
[0236]
通用方法2步骤5
[0237]
向通用方法2步骤4的产物(1eq.,2.91mmol)的dmf(20ml)溶液中在室温下加入丙-2-烯酸乙酯(2.2eq.,642g,0.699ml,6.41mmol)、dipea(3eq.,1.13g,1.52ml,8.74mmol)、三-邻-甲苯基膦(0.2eq.,0.177g,0.583mmol)和乙酸钯(0.1eq.0.65g,0.291mmol)。将混合物用氩气冲洗两次并在封闭的schlenk试管中于100℃加热过夜。反应完成后将溶剂减压蒸发至干。将粗产物通过正相硅胶色谱纯化,用dcm-etoh(100:0至95:5)作为洗脱剂得到标题化合物。
[0238]
通用方法3
[0239]
将芳基溴衍生物(1eq.,10mmol)引入到圆底烧瓶中并溶于二氧杂环己烷(5ml/mmol,50ml)。在室温下加入4,4,5,5-四甲基-2-(4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷-2-基)-1,3,2-二氧杂环戊硼烷(1.1eq.,2.79g,11mmol)和干燥乙酸钾(3.5eq.,3.43g,35mmol)。将混合物用氩气或氮气冲洗。最后加入[1,1'-二(二苯基膦)二茂铁]二氯化钯(ii)催化剂(0.02eq.,146mg,0.2mmol)并将混合物再次用氩气或氮气冲洗,然后在75℃下
在惰性气氛下加热过夜。反应完成后,将混合物通过硅藻土垫过滤并将母液减压蒸发至干。将粗产物通过正相硅胶色谱纯化,用dcm-etoac(100:0至90:10)作为洗脱剂,或通过反相色谱纯化,用水-mecn(95:5至0:100)作为洗脱剂得到标题化合物。
[0240]
通用方法4
[0241]
通用方法4步骤1
[0242]
将多聚甲醛(3eq.,12.8mmol)、二氯化镁(2eq.,0.812mg,8.5mmol)和tea(2eq.,1.18ml,8.5mmol)引入到圆底烧瓶中。将混合物溶于thf(20ml)并在室温下搅拌30分钟。加入取代的苯酚(1eq.,4.3mmol)并将混合物在回流温度下搅拌过夜。反应完成后将溶剂减压蒸发至干。将残余物用50ml etoac稀释,用50ml 1m hcl溶液洗涤,然后用50ml盐水洗涤。将有机层用无水mgso4干燥,过滤,浓缩以得到粗产物,将其通过正相硅胶色谱纯化,用庚烷-etoac作为洗脱剂得到标题化合物。
[0243]
通用方法4步骤2
[0244]
于0℃将氯磺酰异氰酸酯(4eq.,13g,8.1ml,93mmol)引入到圆底烧瓶中。于0℃在40分钟内滴加hcooh(4eq.,3.5ml,93mmol)。将混合物在30分钟内升温至室温并在室温下继续搅拌1小时。将混合物冷却至0℃并在10分钟内滴加溶于nmp(3.5ml/mmol,81ml)的通用方法4步骤1的产物(1eq.,23mmol)。将混合物升温至室温并在该温度下搅拌过夜。反应完成后,将混合物用500ml饱和nh4cl水溶液淬灭。将混合物用2x200ml etoac萃取,将合并的有机层用无水硫酸钠干燥,过滤,浓缩至干得到粗产物,将其通过正相硅胶色谱纯化,用庚烷-etoac(100:0至50:50)作为洗脱剂得到标题化合物。
[0245]
通用方法4步骤3
[0246]
向冷却的通用方法4步骤2的产物(1eq.,22.4mmol)的meoh(8ml/mmol,179ml)溶液中于-5℃在20分钟内缓慢加入硼氢化钠(1.2eq.,1.02g,26.9mmol)。将混合物于-5℃搅拌1小时。反应完成后,将混合物升温至室温并浓缩至干得到粗产物,将其通过正相硅胶色谱纯化,用dcm-etoh(100:0至99:1)作为洗脱剂,或通过反相色谱纯化,用水-mecn梯度洗脱(95:5至0:100)得到标题化合物。
[0247]
通用方法5
[0248]
通用方法5步骤1
[0249]
在室温下向搅拌中的6-溴-3,4-二氢-1,2λ6,3-噁噻嗪2,2-二氧化物衍生物(1eq.,17mmol)的dcm(92ml)溶液中加入tea(1.1eq.,2.5ml,18mmol)、n,n-二甲基吡啶-4-胺(0.1eq.,0.2g,1.7mmol)和二碳酸二叔丁酯(1.1eq.,4g,18mmol)。将混合物在室温下搅拌过夜。反应完成后将混合物用3x50ml 10wt%柠檬酸水溶液萃取,然后用50ml水萃取。将有机层用无水硫酸钠干燥,过滤,浓缩至干得到标题化合物,其不经进一步纯化直接用于下一步骤。
[0250]
通用方法5步骤2
[0251]
将通用方法5步骤1的产物(1eq.,16mmol)引入到圆底烧瓶中并溶于二氧杂环己烷(7.5ml/mmol,120ml)。在室温下将4,4,5,5-四甲基-2-(4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷-2-基)-1,3,2-二氧杂环戊硼烷(1.1eq.,4.6g,18mmol)和干燥乙酸钾(3.5eq.,5.6g,57mmol)加入到混合物中。将混合物用氩气或氮气冲洗。最后加入[1,1'-二(二苯基膦)二茂铁]二氯化钯(ii)催化剂(0.02eq.,160mg,0.33mmol)并将混合物再次用氩气或氮
气冲洗。在75℃下在惰性气氛下加热过夜。然后将混合物用硅藻土垫过滤并将母液减压浓缩至干。将粗产物通过正相硅胶色谱纯化,用庚烷-etoac(100:0至80:20)作为洗脱剂得到标题化合物。
[0252]
通用方法5步骤3
[0253]
在室温下向搅拌中的通用方法5步骤2的产物(1eq.,11.5mmol)的etoh(15ml/mmol,73ml)和水(7.5ml/mmol,37ml)溶液中分批加入间-氯-过苯甲酸(1eq.,2.84g,11.5mmol)。将混合物在室温下搅拌过夜。反应完成后将混合物用100ml饱和nahco3水溶液淬灭。将混合物用3x50ml etoac萃取。将合并的有机层用50ml饱和nahco3水溶液洗涤,然后用50ml水洗涤。将有机层用无水硫酸钠干燥,过滤,浓缩至干得到粗产物,将其通过正相硅胶色谱纯化,用庚烷-etoac(100:0至50:50)作为洗脱剂得到标题化合物。
[0254]
通用方法5步骤4
[0255]
向通用方法5步骤3的产物(1eq.,9.2mmol)的mecn(58ml)溶液中加入cs2co3(2.4eq.,7.2g,22mmol)和苄基溴(2.2eq.,3.4g,2.4ml,20mmol)并将混合物在室温下搅拌过夜。反应完成后将溶剂减压蒸发,然后用40ml etoac稀释。将混合物用40ml盐水洗涤,然后用40ml水洗涤。将有机层用无水硫酸钠干燥,过滤,浓缩至干得到粗产物,其不经进一步纯化直接用于下一步骤。
[0256]
通用方法5步骤5
[0257]
向通用方法5步骤4的产物(1eq.,9.2mmol)的dcm(75ml)溶液中滴加tfa(8eq.,8.4g,5.66ml,74mmol)并将混合物在室温下搅拌过夜。将混合物的ph用饱和nahco3水溶液调节至9。分层,将有机层用30ml盐水萃取,然后用30ml水萃取。将有机层用无水硫酸钠干燥,过滤,浓缩至干得到粗产物,将其通过正相硅胶色谱纯化,用庚烷-etoac(100:0至70:30)作为洗脱剂得到标题化合物。
[0258]
通用方法6
[0259]
向搅拌中的芳基(丙-2-烯酸乙酯)衍生物或杂芳基(丙-2-烯酸乙酯)衍生物(1eq.,4.6mmol)的二氧杂环己烷(5-8ml/mmol,23ml)和水(1-2.7ml/mmol,4.6ml)溶液中加入[3-(4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷-2-基)芳基衍生物(1.5-2eq.,6.9mmol)和tea(1.5eq.,0.96ml,6.9mmol)。将悬浮液用氩气或氮气冲洗并脱气。最后加入氯(1,5-环辛二烯)铑(i)二聚体催化剂(0.05eq.,56mg,0.23mmol)并将混合物于80℃在惰性气氛下加热4-16小时。反应完成后将混合物用100ml水稀释,分层,将水层用2x50ml etoac萃取。将合并的有机层用50ml盐水洗涤,然后用无水na2so4干燥,过滤并浓缩至干得到粗产物,将其通过正相硅胶色谱纯化,用庚烷-etoac(100:0至50:50)作为洗脱剂,或通过反相色谱纯化,用水-mecn梯度洗脱(95:5至0:100)得到标题化合物。
[0260]
通用方法7
[0261]
向搅拌中的羟基甲基苯基衍生物(1eq.,1.6mmol)的thf(22ml/mmol,35ml)溶液中加入取代的噁噻嗪2,2-二氧化物或1,3-苯并噻二嗪2,2-二氧化物衍生物(1-2.5eq.,2.4mmol)和pph3(2.2eq.,0.93g,3.5mmol)。将反应混合物冷却至15℃并在5分钟内滴加diad(2eq.,0.63ml,3.2mmol)。将混合物升温至室温并在该温度下搅拌过夜。反应完成后将混合物浓缩至干并通过正相硅胶色谱纯化,用dcm-etoac(100:0至80:20)作为洗脱剂,或通过反相色谱纯化,用水-mecn梯度洗脱(95:5至0:100)得到标题化合物。
[0262]
通用方法8
[0263]
向不锈钢加氢高压釜中加入3-[3-[(6-苄氧基-2,2-二氧代-4h-1,2λ6,3-噁噻嗪-3-基)甲基]苯基]-3-(4-甲基-1h-苯并三唑-5-基)丙酸乙酯或3-[3-[(6-苄氧基-2,2-二氧代-1,4-二氢-2,1,3-苯并噻二嗪-3-基)甲基]苯基]-3-(4-甲基-1h-苯并三唑-5-基)丙酸乙酯(1eq.,0.883mmol)、pd/c催化剂(0.1eq.,0.0883mmol)、二氧杂环己烷(3ml)、meoh或etoh(10ml)和dcm(4ml)并将该高压釜密封、惰性化并用氢气充填(1-8bar)。在室温下搅拌10-40小时后,将反应混合物用硅藻土垫过滤并将滤液中的挥发物蒸发得到标题化合物。将粗产物通过正相硅胶色谱或反相色谱纯化,用水-mecn梯度洗脱(95:5至0:100)得到标题化合物。
[0264]
通用方法9
[0265]
向搅拌中的n-羟基烷基3-[3-[(6-羟基-2,2-二氧代-4h-1,2λ6,3-噁噻嗪-3-基)甲基]苯基]-3-(4-甲基-1h-苯并三唑-5-基)丙酸乙酯或n-羟基烷基3-[3-[(6-羟基-2,2-二氧代-1,4-二氢-2,1,3-苯并噻二嗪-3-基)甲基]苯基]-3-(4-甲基-1h-苯并三唑-5-基)丙酸乙酯(1eq.,0.122mmol)的dcm(1ml)溶液中加入四溴化碳(7eq.,69mg,0.2074mmol)和pph3(1.7eq.,54.4mg,0.2074mmol)。室温搅拌5-20小时后,将反应混合物减压浓缩并将粗产物通过正相硅胶色谱纯化,用己烷-etoac梯度洗脱得到标题化合物。
[0266]
通用方法10
[0267]
在n2气氛下将n-羟基烷基3-[3-[(6-羟基-2,2-二氧代-4h-1,2λ6,3-噁噻嗪-3-基)甲基]苯基]-3-(4-甲基-1h-苯并三唑-5-基)丙酸乙酯或者n-羟基烷基3-[3-[(6-羟基-2,2-二氧代-1,4-二氢-2,1,3-苯并噻二嗪-3-基)甲基]苯基]-3-(4-甲基-1h-苯并三唑-5-基)丙酸乙酯(1eq.,88.7mmol)溶于dcm(355ml)。在n2气氛下将该溶液冷却至0℃并滴加亚硫酰氯(1.2-4eq.,12.7g,7.77ml,106.5mmol)。于40℃搅拌4小时后,将反应混合物冷却至0℃。缓慢加入水(155ml)和饱和nahco3水溶液(155ml)并分层。将有机层用水洗涤,用硫酸镁干燥并减压除去溶剂。粗产物不经进一步纯化即可使用,或者如果需要的话通过正相硅胶色谱纯化,用dcm-meoh或己烷-etoac梯度洗脱得到标题化合物。
[0268]
通用方法11
[0269]
向搅拌中的氯或溴烷基3-[3-[(6-羟基-2,2-二氧代-4h-1,2λ6,3-噁噻嗪-3-基)甲基]苯基]-3-(4-甲基-1h-苯并三唑-5-基)丙酸乙酯或者氯或溴烷基3-[3-[(6-羟基-2,2-二氧代-1,4-二氢-2,1,3-苯并噻二嗪-3-基)甲基]苯基]-3-(4-甲基-1h-苯并三唑-5-基)丙酸乙酯(1eq.,0.055mmol)的mecn(16ml)溶液中加入cs2co3(1-3eq.,11mg,0.055mmol)并将混合物于室温至80℃搅拌4-36小时。反应完成后将水(10ml)加入到混合物中并减压蒸发mecn。将残余物用dcm萃取(3x10ml)并将合并的有机层用水洗涤。将有机层用硫酸钠干燥,过滤,将滤液浓缩至干得到标题化合物,将其通过正相硅胶色谱纯化,或通过反相色谱纯化,用水-mecn梯度洗脱(95:5至0:100)得到标题化合物。
[0270]
通用方法12
[0271]
向大环酯(1eq.,0.067mmol)的thf(0.67ml)、meoh或etoh(0.17ml)和水(0.34ml)的混合物溶液中加入氢氧化锂(3eq.-4eq.,4.8mg,0.20mmol)。将反应混合物在室温至80℃下搅拌2-30小时。反应完成后,将柠檬酸溶液(10%)或1m hcl水溶液加入到反应混合物中并将中和的混合物用dcm萃取三次。将有机层用硫酸钠干燥,过滤,并将滤液浓缩。将残余物
通过制备型反相色谱纯化,用水-mecn梯度洗脱(95:5至0:100)得到标题化合物。
[0272]
实施例1:[4,32-二甲基-28,28-二氧代-22,27-二氧杂-28λ
6-硫杂-1,14,15,16-四氮杂六环[21.5.3.1
3,7
.1
9,13
.0
12,16
.0
26,30
]三十三碳-3(33),4,6,9(32),10,12,14,23,25,30-十烯-8-基]乙酸
[0273][0274]
步骤a1:5-(3-甲基-2-硝基苯氨基)戊-1-醇的制备
[0275]
采用通用方法1步骤1,用1-氟-3-甲基-2-硝基-苯(1eq.,10.0g,7.85ml,64.5mmol)和5-氨基戊-1-醇(3eq.,19.950g,21ml,193.5mmol)作为起始试剂,得到标题化合物(12.6g,82%收率)。
[0276]1h-nmr(400mhz,dmso-d6)δppm:7.26(t,1h),6.76(d,1h),6.54(d,1h),6.39(t,2h),4.34(t,1h),3.39(q,2h),3.16(q,2h),2.3(s,2h),1.55(s,2h),1.44(m,2h),1.34(m,2h)。
[0277]
步骤a2:5-(4-溴-3-甲基-2-硝基苯氨基)戊基乙酸酯的制备
[0278]
采用通用方法1步骤2,用5-(3-甲基-2-硝基苯氨基)戊-1-醇(8g,34mmol)作为起始试剂,得到标题化合物(12.6g橙色油,定量)。
[0279]1h-nmr(400mhz,dmso-d6)δppm:7.5(d,1h),6.72(d,1h),6.12(tl,1h),4(t,2h),3.15(q,2h),2.25(s,3h),2(s,3h),1.6-1.3(m,6h)。
[0280]
步骤a3:5-(2-氨基-4-溴-3-甲基苯氨基)戊基乙酸酯的制备
[0281]
采用通用方法1步骤3,用5-(4-溴-3-甲基-2-硝基苯氨基)戊基乙酸酯(12.6g,35.1mmol)作为起始试剂,得到标题化合物(11.7g橙色固体,91%收率)。
[0282]1h-nmr(400mhz,dmso-d6)δppm:6.7(d,1h),6.25(d,1h),5.8(m,3h),4(t,2h),3(t,2h),2.2(s,3h),2.01(s,3h),1.65-1.4(m,6h)。
[0283]
步骤a4:5-(5-溴-4-甲基-1h-苯并三唑-1-基)戊基乙酸酯的制备
[0284]
采用通用方法1步骤4,用5-(2-氨基-4-溴-3-甲基苯氨基)戊基乙酸酯(12g,32mmol)作为起始试剂,得到标题化合物(7.5g橙色油,69%收率)。
[0285]1h-nmr(400mhz,dmso-d6)δppm:7.7(2d,2h),4.7(t,2h),3.97(t,2h),2.71(s,3h),1.99(s,3h),1.95(m,2h),1.6(m,2h),1.29(m,2h)。
[0286]
步骤a5:5-(5-溴-4-甲基-1h-苯并三唑-1-基)戊-1-醇的制备
[0287]
采用通用方法1步骤5,用5-(5-溴-4-甲基-1h-苯并三唑-1-基)戊基乙酸酯(7.5g,22mmol)作为起始试剂,得到标题化合物(6.7g橙色油,定量)。
[0288]1h-nmr(400mhz,dmso-d6)δppm:7.7(2d,2h),4.7(t,2h),4.35(m,1h),3.35(t,2h),2.71(s,3h),1.9(m,2h),1.45(m,2h),1.28(m,2h)。
[0289]
步骤a6:5-溴-1-{5-[(4-甲氧基苯基)甲氧基]戊基}-4-甲基-1h-苯并三唑的制备
[0290]
采用通用方法1步骤6,用5-(5-溴-4-甲基-1h-苯并三唑-1-基)戊-1-醇(3.0g,10mmol)作为起始试剂,得到标题化合物(3g黄色油,72%收率)。
[0291]1h-nmr(400mhz,dmso-d6)δppm:7.7(2d,2h),7.15(d,2h),6.85(d,2h),4.7(t,2h),4.3(s,2h),3.75(s,3h),3.32(t,2h),2.71(s,3h),1.9(m,2h),1.52(m,2h),1.28(m,2h)。
[0292]
步骤a7:(2e)-3-(1-{5-[(4-甲氧基苯基)甲氧基]戊基}-4-甲基-1h-苯并三唑-5-基)丙-2-烯酸乙酯的制备
[0293]
采用通用方法1步骤7,用5-溴-1-{5-[(4-甲氧基苯基)甲氧基]戊基}-4-甲基-1h-苯并三唑(3g,7.1mmol)作为起始试剂,得到标题化合物(3g黄色固体,91%收率)。
[0294]1h-nmr(500mhz,dmso-d6)δppm:8.03(d,1h),7.96(d,1h),7.73(d,1h),7.16(d,2h),6.86(d,2h),6.64(d,1h),4.7(t,2h),4.3(s,2h),4.22(q,2h),3.73(s,3h),3.33(t,2h),2.81(s,3h),1.9(m,2h),1.53(m,2h),1.28(t,3h),1.26(m,2h)。
[0295]
步骤c1:6-(苄氧基)-2h-1,2λ6,3-噁噻嗪-2,2-二酮的制备
[0296]
采用通用方法4步骤2,用5-(苄氧基)-2-羟基苯甲醛(1eq.,5.3g,23mmol)作为起始试剂,得到标题化合物(6.48g黄色固体,96%收率)。
[0297]1h-nmr(400mhz,cdcl3)δppm:8.6(s,1h),7.4(m,5h),7.35(dd,1h),7.3(d,1h),7.15(d,1h),5.1(s,2h)。
[0298]
步骤c2:6-(苄氧基)-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮的制备
[0299]
采用通用方法4步骤3,用6-(苄氧基)-2h-1,2λ6,3-噁噻嗪-2,2-二酮(1eq.,6.48g,22.4mmol)作为起始试剂,得到标题化合物(5.9g,黄色固体,90%收率)。
[0300]1h-nmr(400mhz,dmso-d6)δppm:8.4(sl,1h),7.45(d,2h),7.4(t,2h),7.3(t,1h),7(m,m h),5.1(s,2h),4.5(s,2h)。
[0301]
步骤1:3-[3-(羟基甲基)-4-甲基苯基]-3-(1-{5-[(4-甲氧基苯基)甲氧基]戊基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯的制备
[0302]
采用通用方法6,用((2e)-3-(1-{5-[(4-甲氧基苯基)甲氧基]戊基}-4-甲基-1h-苯并三唑-5-基)丙-2-烯酸乙酯(1eq.,4g,4.6mmol)和[2-甲基-5-(4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷-2-基)苯基]甲醇(1.5eq.,1.7g,6.9mmol)作为起始试剂,得到标题化合物(0.96g,38%收率)。
[0303]1h-nmr(400mhz,dmso-d6)δppm:7.6(d,1h),7.48(d,1h),7.25(d,1h),7.18(d,2h),7.08(dd,1h),7(d,1h),6.88(d,2h),4.98(t,1h),4.82(t,1h),4.61(t,2h),4.4(d,2h),4.3(s,2h),3.92(q,2h),3.71(s,3h),3.3(t,2h),3.11(2dd,2h),2.75(s,3h),2.15(s,3h),1.88(m,2h),1.52(m,2h),1.28(m,2h),1(t,3h)。
[0304]
步骤2:3-(3-{[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-甲基苯基)-3-(1-{5-[(4-甲氧基苯基)甲氧基]戊基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯的制备
[0305]
采用通用方法7,用3-[3-(羟基甲基)-4-甲基苯基]-3-(1-{5-[(4-甲氧基苯基)甲氧基]戊基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯(1eq.,0.96g,1.6mmol)和6-(苄氧基)-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮(1.5eq.,0.7g,2.4mmol)作为起始试剂,得到标题化合物(90%收率)。
[0306]1h-nmr(400mhz,dmso-d6)δppm:1.16(m.,3h)1.21-1.29(m,1h)1.44-1.56(m,1h)1.78-1.89(m,1h)2.21(s,1h)2.76(s,1h)3.16(dd,j=7.95,4.77hz,1h)3.26-3.29(m,1h)3.92(q,j=7.09hz,2h)4.21(s,2h)4.28(s,2h)4.42(s,2h)4.59(t,j=6.91hz,2h)4.85(t,j=7.95hz,1h)5.10(s,2h)6.82-6.88(m,2h)6.94(d,j=2.81hz,1h)7.03-7.10(m,1h)7.10-7.17(m,4h)7.17-7.21(m,1h)7.22(s,1h)7.31-7.37(m,1h)7.37-7.43(m,2h)7.45(s,2h)7.48(d,j=8.44hz,2h)7.56-7.61(m,1h)。
[0307]
步骤3:3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}-3-[1-(5-羟基戊基)-4-甲基-1h-苯并三唑-5-基]丙酸乙酯的制备
[0308]
采用通用方法8,用3-(3-{[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-甲基苯基)-3-(1-{5-[(4-甲氧基苯基)甲氧基]戊基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯(1eq.,2g,1.4mmol)作为起始试剂,得到标题化合物(830mg黄色油,90%收率)。
[0309]1h-nmr(400mhz,dmso-d6)δppm:9.7/4.38(2m,2h),7.61(d,1h),7.5(d,1h),7.21(d,1h),7.2(dd,1h),7.12(d,1h),6.99(d,1h),6.8(dd,1h),6.6(d,1h),4.82(t,1h),4.61(t,2h),4.39(s,2h),4.29(m,2h),3.95(q,2h),3.31(t,2h),3.18(m,2h),2.75(s,3h),2.2(s,3h),1.88(m,2h),1.4(m,2h),1.25(m,2h),1(t,3h)。
[0310]
步骤4:3-[1-(5-溴戊基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}丙酸乙酯的制备
[0311]
采用通用方法9,用3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}-3-[1-(5-羟基戊基)-4-甲基-1h-苯并三唑-5-基]丙酸乙酯(1eq.,0.8g,1.3mmol)作为起始试剂,得到标题化合物(710mg白色固体,80%收率)。
[0312]1h-nmr(400mhz,dmso-d6)δppm:9.7(m,1h),7.61(d,1h),7.5(d,1h),7.21(d,1h),7.2(dd,1h),7.12(d,1h),6.99(d,1h),6.8(dd,1h),6.6(d,1h),4.82(t,1h),4.65(t,2h),4.39(s,2h),4.29(m,2h),3.92(q,2h),3.45(t,2h),3.18(m,2h),2.75(s,3h),2.21(s,3h),1.9(m,2h),1.8(m,2h),1.35(m,2h),1(t,3h)。
[0313]
步骤5:[4,32-二甲基-28,28-二氧代-22,27-二氧杂-28λ
6-硫杂-1,14,15,16-四氮杂六环[21.5.3.1
3,7
.1
9,13
.0
12,16
.0
26,30
]三十三碳-3(33),4,6,9(32),10,12,14,23,25,30-十烯-8-基]乙酸乙酯的制备
[0314]
采用通用方法11,用3-[1-(5-溴戊基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}丙酸乙酯(1eq.,0.7g,0.99mmol)作为起始试剂,得到标题化合物(620mg黄色油,93%收率)。
[0315]1h-nmr(400mhz,dmso-d6)δppm:7.65(d,1h),7.52(d,1h),7.5(dd,1h),7.3(d,1h),7.05(d,1h),6.9(dd,1h),6.78(d,1h),6.12(d,1h),4.8(t,1h),4.7(t,2h),4.2/3.9(m,2h),4.15/4(m,2h),3.9(m,2h),3.85(m,2h),3.07(m,2h),2.68(s,3h),2.35(s,3h),2(m,2h),1.75(m,2h),1.5/1.4(m,2h),1(t,3h)。
[0316]
步骤6:实施例1的制备
[0317]
采用通用方法12,用[4,32-二甲基-28,28-二氧代-22,27-二氧杂-28λ
6-硫杂-1,14,15,16-四氮杂六环[21.5.3.1
3,7
.1
9,13
.0
12,16
.0
26,30
]三十三碳-3(33),4,6,9(32),10,12,14,23,25,30-十烯-8-基]乙酸乙酯(1eq.,0.62g,0.92mmol)作为起始试剂,得到标题化合
物(291mg白色固体,55%收率)。
[0318]
通过手性柱色谱分离得到对映体纯产物。
[0319]
实施例1a(e1)
[0320]c30h32
n4o6s的hrms计算值:576.2042;[m+h]
+
,实测值:577.2115(δ=-0.1ppm)。
[0321]
实施例1b(e2)
[0322]c30h32
n4o6s的hrms计算值:576.2042;[m+h]
+
,实测值:577.2113(δ=-0.4ppm)。
[0323]1h-nmr(400mhz,dmso-d6)δppm:11.55(m,1h),7.62(d,1h),7.5(d,2h),7.29(d,1h),7.02(d,1h),6.9(dd,1h),6.72(d,1h),6.11(d,1h),4.8(t,1h),4.7(t,2h),4.2/3.9(2d,2h),4.11/4(2d,2h),3.9/3.8(2m,2h),2.92(2dd,2h),2.65(s,3h),2.31(s,3h),1.99(m,2h),1.72(m,2h),1.48/1.38(2m,2h)。
[0324]
实施例2:[4,30-二甲基-26,26-二氧代-20,25-二氧杂-26λ
6-硫杂-1,14,15,16-四氮杂六环[19.5.3.1
3,7
.1
9,13
.0
12,16
.0
24,28
]三十一碳-3(31),4,6,9(30),10,12,14,21,23,28-十烯-8-基]乙酸
[0325][0326]
步骤a1:n-[3-(苄氧基)丙基]-3-甲基-2-硝基苯胺的制备
[0327]
采用通用方法2步骤1,用1-氟-3-甲基-2-硝基-苯(1eq.,1.93mmol)和3-苄氧基丙-1-胺(1.2eq.,383mg,2.32mmol)作为起始试剂,得到标题化合物(375mg,64%收率)。
[0328]1h-nmr(400mhz,dmso-d6)δppm:7.37-7.26(m,5h),7.26(t,1h),6.77(d,1h),6.55(d,1h),6.47(t,1h),4.47(s,2h),3.51(t,2h),2.29(s,2h),2.26(q,2h),1.83(m,2h)
[0329]
步骤a2:n-[3-(苄氧基)丙基]-4-溴-3-甲基-2-硝基苯胺的制备
[0330]
采用通用方法2步骤2,用n-[3-(苄氧基)丙基]-3-甲基-2-硝基苯胺(6.5g,22mmol)作为起始试剂,得到标题化合物(6.54g,80%收率)。
[0331]1h-nmr(400mhz,dmso-d6)δppm:7.5(d,1h),7.3(m,5h),6.72(d,1h),6.18(t),4.45(s,2h),3.48(t,2h),3.22(q,2h),2.25(s,3h),1.8(m,2h)。
[0332]
步骤a3:n
1-[3-(苄氧基)丙基]-4-溴-3-甲基苯-1,2-二胺的制备
[0333]
采用通用方法2步骤3,用n-[3-(苄氧基)丙基]-4-溴-3-甲基-2-硝基苯胺(6.5g,17mmol)作为起始试剂,得到标题化合物(5.4g,75%收率)。
[0334]1h-nmr(400mhz,dmso-d6)δppm:7.39-7.24(s,5h),6.71(d,1h),6.26(d,1h),4.62-4.54(m,3h),4.48(s,2h),3.55(t,2h),3.08(q,2h),2.16(s,3h),1.86(m,2h)。
[0335]
步骤a4:1-[3-(苄氧基)丙基]-5-溴-4-甲基-1h-苯并三唑的制备
[0336]
采用通用方法2步骤4,用n
1-[3-(苄氧基)丙基]-4-溴-3-甲基苯-1,2-二胺(5.4g,13mmol)作为起始试剂,得到标题化合物(1.09g,23%收率)。
[0337]1h-nmr(400mhz,dmso-d6)δppm:7.68/7.65(d,2h),7.34-7.2(m,5h),4.78(t,2h),
4.38(s,2h),3.41(t,2h),2.71(s,3h),2.18(m,2h)。
[0338]
步骤a5:(2e)-3-{1-[3-(苄氧基)丙基]-4-甲基-1h-苯并三唑-5-基}丙-2-烯酸乙酯的制备
[0339]
采用通用方法2步骤5,用1-[3-(苄氧基)丙基]-5-溴-4-甲基-1h-苯并三唑(1.05g,2.91mmol)作为起始试剂,得到标题化合物(1.18g,70%收率)。
[0340]1h-nmr(400mhz,dmso-d6)δppm:1.28(t,j=7.09hz,2h)2.14-2.23(m,3h)3.41(td,j=5.96,3.00hz,3h)4.22(q,j=7.17hz,2h)4.36-4.41(m,3h)4.78(t,j=6.79hz,3h)6.65(d,j=15.77hz,1h)7.28(s,7h)7.69(d,j=8.80hz,1h)7.95-7.97(m,1h)8.03(d,j=15.89hz,1h)。
[0341]
步骤1:3-{1-[3-(苄氧基)丙基]-4-甲基-1h-苯并三唑-5-基}-3-[3-(羟基甲基)-4-甲基苯基]丙酸乙酯的制备
[0342]
采用通用方法6,用(2e)-3-{1-[3-(苄氧基)丙基]-4-甲基-1h-苯并三唑-5-基}丙-2-烯酸乙酯(1当量)和[2-甲基-5-(4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷-2-基)苯基]甲醇(1.5当量)作为起始试剂,得到标题化合物(黄色油,44%收率)。
[0343]1h-nmr(400mhz,dmso-d6)δppm:7.55(d,1h),7.45(d,1h),7.25(m,6h),7.1(dd,1h),7.01(d,1h),4.81(t,1h),4.81(t,1h),4.7(t,2h),4.4(d+s,4h),3.92(q,2h),3.4(t,2h),3.12(2dd,2h),2.75(s,3h),2.15(m+s,5h),1(t,3h)。
[0344]
步骤2:3-(3-{[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-甲基苯基)-3-{1-[3-(苄氧基)丙基]-4-甲基-1h-苯并三唑-5-基}丙酸乙酯的制备
[0345]
采用通用方法7,用3-{1-[3-(苄氧基)丙基]-4-甲基-1h-苯并三唑-5-基}-3-[3-(羟基甲基)-4-甲基苯基]丙酸乙酯(1当量)和6-(苄氧基)-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮(1.5当量)作为起始试剂,得到标题化合物(94%收率)。
[0346]1h-nmr(400mhz,dmso-d6)δppm:0.98(t,j=7.09hz,3h)2.13(quint,j=6.36hz,2h)2.22(s,3h)2.76(s,3h)3.17(dd,j=8.01,3.36hz,2h)3.36(t,j=6.05hz,2h)3.92(q,j=7.13hz,2h)4.21(s,2h)4.37(s,2h)4.41(s,2h)4.68(t,j=6.79hz,2h)4.85(t,j=8.01hz,1h)5.10(s,2h)6.94(d,j=2.81hz,1h)7.03-7.09(m,1h)7.10-7.16(m,2h)7.16-7.31(m,7h)7.32-7.37(m,1h)7.37-7.43(m,1h)7.44-7.47(m,1h)7.48(d,j=8.80hz,1h)7.53-7.59(m,1h)。
[0347]
步骤3:3-[1-(3-溴丙基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}丙酸乙酯的制备
[0348]
采用通用方法8,用3-(3-{[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-甲基苯基)-3-{1-[3-(苄氧基)丙基]-4-甲基-1h-苯并三唑-5-基}丙酸乙酯(1当量)作为反应试剂,得到3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}-3-[1-(3-羟基丙基)-4-甲基-1h-苯并三唑-5-基]丙酸乙酯(65%收率)。将粗产物用通用方法9进行反应得到标题化合物(69%收率)。
[0349]1h-nmr(400mhz,dmso-d6)δppm:9.65(s,1h),7.62(d,1h),7.51(d,1h),7.2(d,1h),7.18(dd,1h),7.1(d,1h),7(d,1h),6.8(dd,1h),6.6(d,1h),4.85(t,1h),4.75(t,2h),4.38(s,2h),4.2(m,2h),3.92(q,2h),3.48(t,2h),3.18(d,2h),2.75(s,3h),2.42(m,2h),2.21(s,3h),1(t,3h)。
[0350]
步骤4:[4,30-二甲基-26,26-二氧代-20,25-二氧杂-26λ
6-硫杂-1,14,15,16-四氮杂六环[19.5.3.1
3,7
.1
9,13
.0
12,16
.0
24,28
]三十一碳-3(31),4,6,9(30),10,12,14,21,23,28-十烯-8-基]乙酸乙酯的制备
[0351]
采用通用方法11,用3-[1-(3-溴丙基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}丙酸乙酯(1当量)作为起始试剂,得到标题化合物(96%收率)。
[0352]1h-nmr(400mhz,dmso-d6)δppm:7.54(d,1h),7.48(dd,1h),7.44(d,1h),7.28(d,1h),7.01(d,1h),6.85(dd,1h),6.47(d,1h),5.2(d,1h),4.87(m,2h),4.76(t,1h),4.36/3.64(d,2h),4.13/3.44(d,2h),4.01/3.7(tt,2h),3.91(q,2h),3.03(d,2h),2.63(s,3h),2.47/2.38(m,2h),2.32(s,3h),1(t,3h)。
[0353]
步骤5:实施例2的制备
[0354]
采用通用方法12,用[4,30-二甲基-26,26-二氧代-20,25-二氧杂-26λ
6-硫杂-1,14,15,16-四氮杂六环[19.5.3.1
3,7
.1
9,13
.0
12,16
.0
24,28
]三十一碳-3(31),4,6,9(30),10,12,14,21,23,28-十烯-8-基]乙酸乙酯(1当量)作为起始试剂,得到外消旋化合物形式的标题化合物(白色固体,70%收率)。c
28h28
n4o6s的hrms计算值:548.1730;[m+h]
+
,实测值:549.1805(δ=0.5ppm)。
[0355]1h-nmr(400mhz,dmso-d6)δppm:12.2(m,1h),7.55(d,1h),7.45(dd,1h),7.4(d,1h),7.25(d,1h),7(d,1h),6.85(dd,1h),6.43(d,1h),5.22(d,1h),4.85(m,2h),4.75(t,1h),4.35/3.65(m,2h),4.15/3.45(m,2h),4/3.7(m,2h),2.95(d,2h),2.65(s,3h),2.4(m,2h),2.3(s,3h)。
[0356]
实施例3:[(2r,8r)-2,4,31-三甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸和
[0357]
[(2r,8s)-2,4,31-三甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸
[0358][0359]
步骤a1:4-(3-甲基-2-硝基苯氨基)丁-1-醇的制备
[0360]
采用通用方法1步骤1,用1-氟-3-甲基-2-硝基-苯(1当量)和4-氨基丁-1-醇(3当量)作为起始试剂,得到标题化合物(44%收率)。
[0361]1h-nmr(400mhz,dmso-d6)δppm:7.28(t,1h),6.78(d,1h),6.52(d,1h),6.4(t,1h),4.4(t,1h),3.41(q,2h),3.2(q,2h),2.3(s,3h),1.58(m,2h),1.48(m,2h)。
[0362]
步骤a2:4-(4-溴-3-甲基-2-硝基苯氨基)丁基乙酸酯的制备
[0363]
采用通用方法1步骤2,用4-(3-甲基-2-硝基苯氨基)丁-1-醇(1当量)作为起始试剂,得到标题化合物(橙色油,93%收率)。
[0364]1h-nmr(400mhz,dmso-d6)δppm:7.52(d,1h),6.72(d,1h),6.15(t,1h),4(t,2h),3.15(q,2h),2.25(s,3h),2(s,3h),1.55(m,4h)。
[0365]
步骤a3:4-(2-氨基-4-溴-3-甲基苯氨基)丁基乙酸酯的制备
[0366]
采用通用方法1步骤3,用4-(4-溴-3-甲基-2-硝基苯氨基)丁基乙酸酯(1当量)作为起始试剂,得到标题化合物(72%收率)。
[0367]1h-nmr(400mhz,dmso-d6)δppm:6.7(d,1h),6.25(d,1h),5.2-4.5(ml,3h),4.01(t,2h),3(t,2h),2.19(s,3h),2(s,3h),1.7-1.5(m,4h)。
[0368]
步骤a4:4-(5-溴-4-甲基-1h-苯并三唑-1-基)丁基乙酸酯的制备
[0369]
采用通用方法1步骤4,用4-(2-氨基-4-溴-3-甲基苯氨基)丁基乙酸酯(1当量)作为起始试剂,得到标题化合物(橙色油,49%收率)。
[0370]c13h16
brn3o2的hrms计算值:325.0426;[m+h]
+
,实测值:326.0502(δ=1.0ppm)。
[0371]
步骤a5:4-(5-溴-4-甲基-1h-苯并三唑-1-基)丁-1-醇的制备
[0372]
采用通用方法1步骤5,用4-(5-溴-4-甲基-1h-苯并三唑-1-基)丁基乙酸酯(1当量)作为起始试剂,得到标题化合物(橙色油,85%收率)。
[0373]1h-nmr(400mhz,dmso-d6)δppm:7.7(m,2h),4.75(t,2h),4.45(t,1h),3.45(q,2h),2.75(s,3h),1.95(m,2h),1.4(m,2h)。
[0374]
步骤a6:5-溴-1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑的制备
[0375]
采用通用方法1步骤6,用4-(5-溴-4-甲基-1h-苯并三唑-1-基)丁-1-醇(1当量)作为起始试剂,得到标题化合物(黄色油,74%收率)。
[0376]1h-nmr(400mhz,dmso-d6)δppm:7.68(s,2h),7.19(d,2h),6.88(d,2h),4.71(t,2h),4.32(s,2h),3.73(s,3h),3.39(t,2h),2.72(s,3h),1.95(quint,2h),1.48(quint,2h)。
[0377]
步骤a7:(2e)-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙-2-烯酸乙酯的制备
[0378]
采用通用方法1步骤7,用5-溴-1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑(1当量)作为起始试剂,得到标题化合物(黄色固体,74%收率)。
[0379]1h-nmr(400mhz,dmso-d6)δppm:8.02(d,1h),7.95(d,1h),7.7(d,1h),7.19(d,2h),6.88(d,2h),6.65(d,1h),4.71(t,2h),4.32(s,2h),4.22(q,2h),3.73(s,3h),3.39(t,2h),2.81(s,3h),1.95(m,2h),1.49(m,2h),1.28(t,3h)。
[0380]
步骤1:3-{3-[(1s)-1-羟基乙基]-4-甲基苯基}-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯的制备
[0381]
采用通用方法6,用(2e)-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙-2-烯酸乙酯(1当量)和(1s)-1-[2-甲基-5-(4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷-2-基)苯基]乙-1-醇(2当量)作为起始试剂,得到标题化合物(黄色油,82%收率)。
[0382]1h-nmr(400mhz,dmso-d6)δppm:0.99(t,j=7.09hz,3h)1.22(dd,j=8.74,6.42hz,3h)1.42-1.53(m,2h)1.92(quin,j=7.21hz,2h)1.99(s,2h)2.19(s,3h)2.76(d,j
1-(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)乙基]-4-甲基苯基}丙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体,91%收率)。
[0394]1h-nmr(400mhz,dmso-d6)δppm:1.03(td,j=7.09,3.30hz,9h)1.23-1.30(m,7h)1.33-1.94(m,12h)2.25-2.35(m,11h)2.67(s,6h)2.96-3.15(m,5h)3.34-3.53(m,9h)3.62-3.75(m,4h)3.88-3.98(m,5h)3.99-4.11(m,4h)4.70-4.85(m,10h)4.92(t,j=7.95hz,2h)5.18-5.31(m,2h)5.72(d,j=2.81hz,1h)5.89(br.s.,1h)6.74-6.78(m,1h)6.88-6.98(m,2h)7.17(s,1h)7.31(d,j=8.07hz,1h)7.44(d,j=7.58hz,2h)7.75(d,j=8.68hz,1h)7.89(d,j=8.68hz,1h)。
[0395]
通过手性柱色谱分离得到非对映纯的最终中间体。
[0396]
步骤6:实施例3的制备
[0397]
采用通用方法12,用[(2r,8r)-2,4,31-三甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯(1当量)或[(2r,8s)-2,4,31-三甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯(1当量)作为起始试剂,得到标题化合物(收率分别为34%-78%)。
[0398]
实施例3a(2r,8r)
[0399]c30h32
n4o6s的hrms计算值:576.2042;[m+h]
+
,实测值:577.2119(δ=0.6ppm)。
[0400]1h-nmr(400mhz,dmso-d6)δppm:12.21(m,1h),7.7(d,1h),7.43(d,1h),7.3(d,1h),7.1(d,1h),6.9(d,1h),6.7(m,2h),5.89(m,1h),5.21(q,1h),4.9(t,1h),4.73(m,2h),4.05/3.48(m,2h),3.7(m,2h),3.25/2.89(2dd,2h),2.8(s,3h),2.3(s,3h),2.2/2(2m,2h),1.61/1.29(2m,2h),1.1(d,3h)。
[0401]
实施例3b(2r,8s)
[0402]c30h32
n4o6s的hrms计算值:576.2042;[m+h]
+
,实测值:577.2118(δ=0.5ppm)。
[0403]1h-nmr(400mhz,dmso-d6)δppm:12.5-11.8(m,1h),7.88(d,1h),7.73(d,1h),7.43(d,1h),7.2(d,1h),7.11(d,1h),6.93(d,1h),6.78(dd,1h),5.69(d,1h),5.25(q,1h),4.82-4.67(m,2h),4.78(t,1h),4.01/3.4(m,2h),3.68/3.47(m,2h),3.19/2.99(2dd,2h),2.62(s,3h),2.29(s,3h),2.23-2(2m,2h),1.92-1.68(2m,2h),1.23(d,3h)。
[0404]
实施例4:[5-氟-31-甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸
[0405]
[0406]
步骤1:3-[3-氟-5-(羟基甲基)苯基]-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯的制备
[0407]
采用通用方法6,用(2e)-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙-2-烯酸乙酯(1当量)和[3-氟-5-(4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷-2-基)苯基]甲醇(1.5当量)作为起始试剂,得到标题化合物(黄色油,30%收率)。
[0408]1h-nmr(400mhz,dmso-d6)δppm:7.6(d,1h),7.5(d,1h),7.2(d,2h),7.1-6.9(m,3h),6.88(d,2h),5.22(t,1h),4.85(t,1h),4.62(t,2h),4.41(d,2h),4.3(s,2h),3.95(q,2h),3.71(s,3h),3.39(t,2h),3.18(m,2h),2.78(s,3h),1.9(m,2h),1.5(m,2h),1(t,3h)。
[0409]
步骤2:3-(3-{[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-5-氟苯基)-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯的制备
[0410]
采用通用方法7,用3-[3-氟-5-(羟基甲基)苯基]-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯(1当量)和6-(苄氧基)-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮(1.1当量)作为起始试剂,得到标题化合物(64%收率)。
[0411]1h-nmr(400mhz,dmso-d6)δppm:7.6(d,1h),7.48(d,1h),7.4-7.3(m,5h),7.2-7(m,3h),7.18(d,2h),7-6.9(m,3h),6.85(d,2h),5.05(s,2h),4.87(t,1h),4.62(s+t,4h),4.3(s,4h),3.92(q,2h),3.71(s,3h),3.38(t,2h),3.18(d,2h),2.78(s,3h),1.92(m,2h),1.5(m,2h),1(t,3h)。
[0412]
步骤3:3-{3-氟-5-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]苯基}-3-[1-(4-羟基丁基)-4-甲基-1h-苯并三唑-5-基]丙酸乙酯的制备
[0413]
采用通用方法8,用3-(3-{[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-5-氟苯基)-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯(1当量)作为起始试剂,得到标题化合物(96%收率)。
[0414]1h-nmr(400mhz,dmso-d6)δppm:9.6/4.4(s+t,2h),7.62(d,1h),7.5(d,1h),7.21(d,1h),7.1(dd,1h),7.02(dd,1h),6.81(d,1h),6.7(dd,1h),6.6(d,1h),4.85(t,1h),4.65(t,2h),4.52(s,2h),4.29(s,2h),3.95(q,2h),3.4(q,2h),3.2(d,2h),2.79(s,3h),1.9(m,2h),1.38(m,2h),1(t,3h)。
[0415]
步骤4:3-[1-(4-溴丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-氟-5-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]苯基}丙酸乙酯的制备
[0416]
采用通用方法9,用3-{3-氟-5-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]苯基}-3-[1-(4-羟基丁基)-4-甲基-1h-苯并三唑-5-基]丙酸乙酯(1当量)作为起始试剂,得到标题化合物(66%收率)。
[0417]1h-nmr(400mhz,dmso-d6)δppm:9.6(s,1h),7.64(d,1h),7.51(d,1h),7.2(t,1h),7.13/7(2dt,2h),6.88(d,1h),6.7(dd,1h),6.59(d,1h),4.87(t,1h),4.69(t,2h),4.57(s,2h),4.29(s,2h),3.92(q,2h),3.52(t,2h),3.19(d,2h),2.78(s,3h),1.99(m,2h),1.78(m,2h),1(t,3h)。
[0418]
步骤5:[5-氟-31-甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯的制备
[0419]
采用通用方法11,用3-[1-(4-溴丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-氟-5-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]苯基}丙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体,72%收率)。
[0420]1h-nmr(400mhz,dmso-d6)δppm:7.59(d,1h),7.4/7.06(2m,2h),7.32(d,1h),6.91(d,1h),6.74(m,1h),6.69(dd,1h),6(d,1h),4.87-4.67(m,3h),4.15/4.05(2dd,4h),3.93(m,2h),3.67/3.37(2m,2h),3.27/3.11(2m,2h),2.75(s,3h),2.18/1.96(2m,2h),1.68/1.45(2m,2h),1.01(t,3h)
[0421]
步骤6:实施例4的制备
[0422]
采用通用方法12,用[5-氟-31-甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体,98%收率)。
[0423]c28h27
fn4o6s的hrms计算值:566.1635;[m+h]
+
实测值:567.1710(δ=0.3ppm)。
[0424]1h-nmr(400mhz,dmso-d6)δppm:12.19(m,1h),7.59(d,1h),7.4/7.06(2m,2h),7.3(d,1h),6.91(d,1h),6.71(m,1h),6.69(dd,1h),6(d,1h),4.87-4.67(m,3h),4.14/4.04(2dd,4h),3.68/3.38(2m,2h),3.17/2.91(2m,2h),2.75(s,3h),2.19/1.97(2m,2h),1.69/1.46(2m,2h)。
[0425]
实施例5:[5,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸
[0426][0427]
步骤b1:[3-甲基-5-(4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷-2-基)苯基]甲醇的制备
[0428]
采用通用方法3,用(3-溴-5-甲基苯基)甲醇(1eq.,2.01g,10mmol)作为起始试剂,得到标题化合物(1.13g,45%收率)。
[0429]1h-nmr(400mhz,dmso-d6)δppm:7.44/7.35/7.23(3tf,3h),5.12(t,1h),4.46(d,2h),2.29(s,3h),1.28(s,12h)。
[0430]
步骤1:3-[3-(羟基甲基)-5-甲基苯基]-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯的制备
[0431]
采用通用方法6,用(2e)-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙-2-烯酸乙酯(1当量)和[3-甲基-5-(4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷-2-基)苯基]甲醇(2当量)作为起始试剂,得到标题化合物(68%收率)。
[0432]1h-nmr(400mhz,dmso-d6)δppm:7.58(d,1h),7.47(d,1h),7.2(d,2h),7.04/7/6.93(3sl,3h),6.87(d,2h),5.05(t,1h),4.82(t,1h),4.64(t,2h),4.39(d,2h),4.32(s,2h),3.92(qd,2h),3.73(s,3h),3.38(t,2h),3.13(m,2h),2.76(s,3h),2.23(s,3h),1.92(m,2h),1.48(m,2h),0.99(t,3h)。
[0433]
步骤2:3-(3-{[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-5-甲基苯基)-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯的制备
[0434]
采用通用方法7,用3-[3-(羟基甲基)-5-甲基苯基]-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯(1当量)和6-(苄氧基)-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮(1.5当量)作为反应试剂得到标题化合物(86%收率)。
[0435]1h-nmr(400mhz,dmso-d6)δppm:7.57(d,1h),7.45-7.3(m,5h),7.45(d,1h),7.18(d,2h),7.14/7.07/6.98(3tf,3h),7.03/7/6.94(dd+d+d,3h),6.86(d,2h),5.05(s,2h),4.82(t,1h),4.63(t,2h),4.55(s,2h),4.31(s,2h),4.23(s,2h),3.92(q,2h),3.73(s,3h),3.36(t,2h),3.12(d,2h),2.76(s,3h),2.22(s,3h),1.91(m,2h),1.47(m,2h),0.98(t,3h)。
[0436]
步骤3:3-[1-(4-羟基丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-5-甲基苯基}丙酸乙酯的制备
[0437]
采用通用方法8,用3-(3-{[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-5-甲基苯基)-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯(1当量)作为起始试剂,得到标题化合物(99%收率)。
[0438]1h-nmr(400mhz,dmso-d6)δppm:9.63(m,1h),7.62(d,1h),7.47(d,1h),7.15/7.08/6.99(3tf,3h),6.91(d,1h),6.73(dd,1h),6.6(d,1h),4.83(t,1h),4.65(t,2h),4.5/4.22(2s,4h),3.94(q,2h),3.39(t,2h),3.14(d,2h),2.77(s,3h),2.24(s,3h),1.91(m,2h),1.37(m,2h),1(t,3h)。
[0439]
步骤4:3-[1-(4-溴丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-5-甲基苯基}丙酸乙酯的制备
[0440]
采用通用方法9,用3-[1-(4-羟基丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-5-甲基苯基}丙酸乙酯(1当量)作为起始试剂,得到标题化合物(78%收率)。
[0441]1h-nmr(400mhz,dmso-d6)δppm:9.61(m,1h),7.63(d,1h),7.49(d,1h),7.14/7.07/6.98(3tf,3h),6.9(d,1h),6.73(dd,1h),6.59(d,1h),4.82(t,1h),4.69(t,2h),4.49/4.2(2s,4h),3.93(q,2h),3.54(t,2h),3.14(d,2h),2.76(s,3h),2.22(s,3h),1.99(m,2h),1.77(m,2h),0.99(t,3h)。
[0442]
步骤5:[5,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯的制备
[0443]
采用通用方法11,用3-[1-(4-溴丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-5-甲基苯基}丙酸乙酯(1当量)作为起始试剂,得到标题化合物(98%收率)。
[0444]1h-nmr(400mhz,dmso-d6)δppm:7.6(d,1h),7.35(d,1h),7.34/7.09/6.58(3m,
3h),6.93(d,1h),6.73(dd,1h),5.98(d,1h),4.84-4.66(2m,3h),4.03/3.98(2s,4h),3.93(m,2h),3.68/3.45(2m,2h),3.21/3.09(2m,2h),2.71(s,3h),2.36(s,3h),2.19/1.99(2m,2h),1.68/1.48(2m,2h),1.01(t,3h)。
[0445]
步骤6:实施例5的制备
[0446]
采用通用方法12,用[5,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体,50%收率)。
[0447]c29h30
n4o6s的hrms计算值:562.1886;[m+h]
+
,实测值:563.1963(δ=0.7ppm)。
[0448]1h-nmr(400mhz,dmso-d6)δppm:12.15(m,1h),7.6(d,1h),7.34/7.09/6.57(3sl,3h),7.33(d,1h),6.94(d,1h),6.73(dd,1h),5.98(d,1h),4.85-4.67(2m,3h),4.03/3.98(2s,4h),3.68/3.45(2m,2h),3.11/2.97(2m,2h),2.71(s,3h),2.36(s,3h),2.19/1.99(2m,2h),1.71/1.47(2m,2h)。
[0449]
实施例6:[31-甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸
[0450][0451]
步骤1:3-[3-(羟基甲基)苯基]-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯的制备
[0452]
采用通用方法6,用(2e)-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙-2-烯酸乙酯(1当量)和[3-(4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷-2-基)苯基]甲醇(2当量)作为反应试剂得到标题化合物(75%收率)。
[0453]1h-nmr(400mhz,dmso-d6)δppm:7.58(d,1h),7.48(d,1h),7.26-7.1(m,4h),7.2(d,2h),6.88(d,2h),5.09(t,1h),4.86(t,1h),4.64(t,2h),4.42(d,2h),4.32(s,2h),3.92(q,2h),3.73(s,3h),3.38(t,2h),3.18/3.13(2dd,2h),2.77(s,3h),1.92(m,2h),1.48(m,2h),0.99(t,3h)。
[0454]
步骤2:3-[1-(4-羟基丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]苯基}丙酸乙酯的制备
[0455]
采用通用方法7,用3-[3-(羟基甲基)苯基]-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯(1当量)和6-(苄氧基)-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮(1.5当量)作为反应试剂,得到3-(3-{[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}苯基)-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯。采用通用方法8,将粗产物不经纯化直接使用。得到标题化合
4-甲基苯基]丙酸乙酯的制备
[0483]
采用通用方法6,用(2e)-3-{1-[4-(苄氧基)丁基]-4-甲基-1h-苯并三唑-5-基}丙-2-烯酸乙酯(1当量)和[2-甲基-5-(4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷-2-基)苯基]甲醇(1.5当量)作为反应试剂得到标题化合物(49%收率)。
[0484]1h-nmr(400mhz,dmso-d6)δppm:7.6(d,1h),7.45(d,1h),7.35-7.2(m,6h),7.1(dd,1h),7.01(d,1h),4.99(t,1h),4.82(t,1h),4.65(t,2h),4.4(d+s,4h),3.91(q,2h),3.45(t,2h),3.15(d,2h),2.75(s,3h),2.15(s,3h),1.95(m,2h),1.5(m,2h),1(t,3h)。
[0485]
步骤2:3-{1-[4-(苄氧基)丁基]-4-甲基-1h-苯并三唑-5-基}-3-(3-{[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-甲基苯基)丙酸乙酯的制备
[0486]
采用通用方法7,用3-{1-[4-(苄氧基)丁基]-4-甲基-1h-苯并三唑-5-基}-3-[3-(羟基甲基)-4-甲基苯基]丙酸乙酯(1当量)和6-(苄氧基)-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮(2.2当量)作为反应试剂得到标题化合物(60%收率)。
[0487]1h-nmr(400mhz,dmso-d6)δppm:7.58(d,1h),7.48(d,1h),7.45-7.2(m,13h),7.15(d,1h),7.05(dd,1h),6.95(d,1h),5.1(s,2h),4.85(t,1h),4.65(t,2h),4.45/4.4(2s,4h),4.22(s,2h),3.92(q,2h),3.42(t,2h),3.15(m,2h),2.75(s,3h),2.2(s,3h),1.92(m,2h),1.48(m,2h),1.2(t,3h)。
[0488]
步骤3:3-[1-(4-羟基丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}丙酸乙酯的制备
[0489]
采用通用方法8,用3-{1-[4-(苄氧基)丁基]-4-甲基-1h-苯并三唑-5-基}-3-(3-{[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-甲基苯基)丙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体,定量)。
[0490]1h-nmr(400mhz,dmso-d6)δppm:7.62(d,1h),7.5(d,1h),7.22(s,1h),7.2(d,1h),7.15(d,1h),7(s,1h),6.8(dd,1h),6.6(d,1h),4.85(t,1h),4.65(t,2h),4.4(m,1h),4.4(s,2h),4.2(m,2h),3.95(q,2h),3.38(tl,2h),3.15(m,2h),2.75(s,3h),2.32(s,3h),1.9(m,2h),1.35(m,2h),1(t,3h)。
[0491]
步骤4:3-[1-(4-溴丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}丙酸乙酯的制备
[0492]
采用通用方法9,用3-[1-(4-羟基丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}丙酸乙酯(1当量)作为起始试剂,得到标题化合物(73%收率)。
[0493]1h-nmr(400mhz,dmso-d6)δppm:9.68(s,1h),7.63(d,1h),7.52(d,1h),7.22(d,1h),7.2(dd,1h),7.13(d,1h),6.99(d,1h),6.79(dd,1h),6.6(d,1h),4.84(t,1h),4.69(t,2h),4.38(s,2h),4.2(m,2h),3.94(q,2h),3.54(t,2h),3.19(m,2h),2.76(s,3h),2.22(s,3h),1.99(quint,2h),1.77(quint,2h),1(t,3h)。
[0494]
步骤5:[4,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯的制备
[0495]
采用通用方法11,用3-[1-(4-溴丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}丙酸乙酯(1当量)作为
起始试剂,得到标题化合物(白色固体,79%收率)。
[0496]1h-nmr(400mhz,dmso-d6)δppm:7.7(d,1h),7.5(dd,1h),7.45(d,1h),7.3(d,1h),7(d,1h),6.8(dd,1h),6.55(d,1h),5.85(d,1h),4.8(m,3h),4.1/3.95(m,2h),4/3.8(m,2h),3.9(m,2h),3.7/3.45(m,2h),3.15/3.08(m,2h),2.63(s,3h),2.31(s,3h),2.2/2(m,2h),1.8/1.6(m,2h),1.02(t,3h)。
[0497]
步骤6:实施例7的制备
[0498]
采用通用方法12,用[4,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体,93%收率)。
[0499]
通过手性柱色谱分离得到对映体纯的最终产物或最终中间体。
[0500]
实施例7a(8s)
[0501]c29h30
n4o6s的hrms计算值:562.1886;[m+h]
+
,实测值:563.1962(δ=0.6ppm)。
[0502]
实施例7b(8r)
[0503]c29h30
n4o6s的hrms计算值:562.1886;[m+h]
+
,实测值:563.1962(δ=0.6ppm)。
[0504]1h-nmr(400mhz,dmso-d6)δppm:12.12(m,1h),7.69(d,1h),7.49(dd,1h),7.41(d,1h),7.3(d,1h),7(d,1h),6.8(dd,1h),6.55(d,1h),5.85(d,1h),4.75(m,3h),4.11-3.92(d,2h),4-3.85(d,2h),3.62/3.4(m,2h),3.05/2.95(dd,2h),2.65/2.31(s,6h),2.2/2.08(m,2h),1.8/1.65(m,2h)。
[0505]
实施例8:[5-甲氧基-31-甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸
[0506][0507]
步骤1:3-[3-(羟基甲基)-5-甲氧基苯基]-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯的制备
[0508]
采用通用方法6,用(2e)-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙-2-烯酸乙酯(1当量)和[3-甲氧基-5-(4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷-2-基)苯基]甲醇(1当量)作为起始试剂,得到标题化合物(黄色油,30%收率)。
[0509]1h-nmr(400mhz,dmso-d6)δppm:7.59(d,1h),7.5(d,1h),7.2(d,2h),6.88(d,2h),6.3-6.15(3sl,3h),5.1(t,1h),4.81(t,1h),4.62(t,2h),4.4(d,2h),4.3(s,2h),3.95(q,2h),3.71(s,6h),3.39(t,2h),3.12(m,2h),2.75(s,3h),1.92(m,2h),1.5(m,2h),1(t,3h)。
[0510]
步骤2:3-(3-{[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-5-甲氧基苯基)-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙
酸乙酯的制备
[0511]
采用通用方法7,用3-[3-(羟基甲基)-5-甲氧基苯基]-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯(1当量)和6-(苄氧基)-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮(1.1当量)作为起始试剂,得到标题化合物(88%收率)。
[0512]1h-nmr(400mhz,dmso-d6)δppm:7.72-7.3(m,5h),7.58(d,1h),7.48(d,1h),7.2(d,2h),7-6.9(m,3h),6.91/6.8/6.72(3d,3h),6.87(d,2h),5.05(s,2h),4.81(t,1h),4.62(t,2h),4.55(s,2h),4.3/4.23(2s,4h),3.91(q,2h),3.7(2s,6h),3.35(t,2h),3.12(d,2h),2.78(s,3h),1.9(m,2h),1.48(m,2h),1(t,3h)。
[0513]
步骤3:3-[1-(4-羟基丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-5-甲氧基苯基}丙酸乙酯的制备
[0514]
采用通用方法8,用3-(3-{[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-5-甲氧基苯基)-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体,96%收率)。
[0515]1h-nmr(400mhz,dmso-d6)δppm:9.6/4.4(s+t,2h),7.6(d,1h),7.5(d,1h),6.91(d,1h),6.9(d,1h),6.8/6.72/6.6(3sl,3h),6.71(dd,1h),4.81(t,1h),4.62(t,2h),4.52(s,2h),4.21(s,2h),3.92(q,2h),3.7(s,3h),3.4(q,2h),3.17(d,2h),2.78(s,3h),1.9(m,2h),1.38(m,2h),1(t,3h)。
[0516]
步骤4:3-[1-(4-溴丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-5-甲氧基苯基}丙酸乙酯的制备
[0517]
采用通用方法9,用3-[1-(4-羟基丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-5-甲氧基苯基}丙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体,82%收率)。
[0518]1h-nmr(400mhz,dmso-d6)δppm:9.61(m,1h),7.64(d,1h),7.51(d,1h),6.91/6.81(2sl,2h),6.88(d,1h),6.73(sl,1h),6.71(dd,1h),6.58(d,1h),4.82(t,1h),4.69(t,2h),4.51/4.21(2s,4h),3.93(q,2h),3.69(s,3h),3.54(t,2h),3.15(d,2h),2.76(s,3h),1.99(m,2h),1.78(m,2h),1(t,3h)。
[0519]
步骤5:[5-甲氧基-31-甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯的制备
[0520]
采用通用方法11,用3-[1-(4-溴丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-5-甲氧基苯基}丙酸乙酯(1当量)作为起始试剂,得到标题化合物(95%收率)。
[0521]1h-nmr(400mhz,dmso-d6)δppm:7.6(d,1h),7.33(d,1h),7.09/6.78/6.37(3sl,3h),6.93(d,1h),6.71(dd,1h),5.98(d,1h),4.85-4.67(m,3h),4.12-3.9(2dd,4h),3.94(m,2h),3.81(s,3h),3.52/3.42(2m,2h),3.2/3.08(2dd,2h),2.72(s,3h),2.19/1.98(2m,2h),1.68/1.48(2m,2h),1.02(t,3h)。
[0522]
步骤6:实施例8的制备
[0523]
采用通用方法12,用[5-甲氧基-31-甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),
10,12,14,22,24,29-十烯-8-基]乙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体,28%收率)。
[0524]
通过手性柱色谱分离得到对映体纯产物。
[0525]
实施例8a(e1)
[0526]c29h30
n4o7s的hrms计算值:578.1835;[m+h]
+
,实测值:579.1911(δ=0.5ppm)。
[0527]
实施例8b(e2)
[0528]c29h30
n4o7s的hrms计算值:578.1835;[m+h]
+
,实测值:579.1912(δ=0.7ppm)。
[0529]1h-nmr(400mhz,dmso-d6)δppm:12.15(m,1h),7.6(d,1h),7.31(d,1h),7.31(2dd,4h),7.1/6.8/6.38(3sl,3h),6.95(d,1h),6.71(dd,1h),5.98(d,1h),4.85-4.67(m,3h),3.81(s,3h),3.68/3.41(2m,2h),3.1/2.98(2dd,2h),2.71(s,3h),2.19/1.98(2m,2h),1.68/1.48(2m,2h)。
[0530]
实施例9:[4-氯-31-甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸
[0531][0532]
步骤1:3-[4-氯-3-(羟基甲基)苯基]-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯的制备
[0533]
采用通用方法6,用(2e)-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙-2-烯酸乙酯(1当量)和[2-氯-5-(4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷-2-基)苯基]甲醇(2当量)作为起始试剂,得到标题化合物(黄色油,83%收率)。
[0534]1h-nmr(400mhz,dmso-d6)δppm:7.6(d,1h),7.48(d,1h),7.47(d,1h),7.3(d,1h),7.22(dd,1h),7.19(d,2h),6.88(d,2h),5.3(t,1h),4.89(t,1h),4.63(t,2h),4.49(d,2h),4.3(s,2h),3.92(q,2h),3.71(s,3h),3.39(t,2h),3.17(m,2h),2.75(s,3h),1.91(m,2h),1.49(m,2h),1(t,3h)。
[0535]
步骤2:3-(3-{[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-氯苯基)-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯的制备
[0536]
采用通用方法7,用3-[4-氯-3-(羟基甲基)苯基]-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯(1当量)和6-(苄氧基)-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮(1.5当量)作为起始试剂,得到标题化合物(92%收率)。
[0537]1h-nmr(400mhz,dmso-d6)δppm:7.6(d,1h),7.5-7.3(m,8h),7.49(d,1h),7.18(d,2h),7.09(d,1h),7.04(dd,1h),6.96(d,1h),6.86(d,2h),5.09(s,2h),4.89(t,1h),4.63
(t,2h),4.56/4.34(2s,4h),4.3(s,2h),3.94(q,2h),3.72(s,3h),3.36(t,2h),3.2(2ddd,2h),2.77(s,3h),1.9(m,2h),1.46(m,2h),1(t,3h)。
[0538]
步骤3:3-{4-氯-3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]苯基}-3-[1-(4-羟基丁基)-4-甲基-1h-苯并三唑-5-基]丙酸乙酯的制备
[0539]
采用通用方法8,用3-(3-{[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-氯苯基)-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯(1当量)作为起始试剂,得到标题化合物(77%收率)。
[0540]1h-nmr(400mhz,dmso-d6)δppm:9.68(m,1h),7.64(d,1h),7.51(d,1h),7.49(d,1h),7.39(dd,1h),7.31(d,1h),6.95(d,1h),6.77(dd,1h),6.63(d,1h),4.89(t,1h),4.66(t,2h),4.51/4.33(2s,4h),4.41(t,2h),3.95(q,2h),3.38(q,2h),3.23/3.17(2dd,2h),2.76(s,3h),1.91(m,2h),1.37(m,2h),1.01(t,3h)。
[0541]
步骤4:3-[1-(4-溴丁基)-4-甲基-1h-苯并三唑-5-基]-3-{4-氯-3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]苯基}丙酸乙酯的制备
[0542]
采用通用方法9,用3-{4-氯-3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]苯基}-3-[1-(4-羟基丁基)-4-甲基-1h-苯并三唑-5-基]丙酸乙酯(1当量)作为起始试剂,得到标题化合物(79%收率)。
[0543]1h-nmr(400mhz,dmso-d6)δppm:9.67(s),7.66(d,1h),7.53(d,1h),7.49(d,1h),7.39(d,1h),7.32(dd,1h),6.95(d,1h),6.77(dd,1h),6.62(d,1h),4.89(t,1h),4.7(t,2h),4.52(s,2h),4.33(s,2h),3.95(q,d h),3.55(t,2h),3.2(m,2h),2.77(s,3h),2(m,2h),1.78(m,2h),1.01(t,3h)。
[0544]
步骤5:[4-氯-31-甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯的制备
[0545]
采用通用方法11,用3-[1-(4-溴丁基)-4-甲基-1h-苯并三唑-5-基]-3-{4-氯-3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]苯基}丙酸乙酯(1当量)作为起始试剂,得到标题化合物(97%收率)。
[0546]1h-nmr(400mhz,dmso-d6)δppm:7.69(d,1h),7.64(dd,1h),7.57(d,1h),7.45(d,1h),6.99(d,1h),6.8(dd,1h),6.8(d,1h),5.86(d,1h),4.82(m,2h),4.79(m,1h),4.24/4.05(dd,2h),4.01/3.84(dd,2h),3.93(q,2h),3.67/3.47(2m,2h),3.21/3.08(2dd,2h),2.63(s,3h),2.2/2.05(2m,2h),1.8/1.64(2m,2h),1(t,3h)。
[0547]
步骤6:实施例9的制备
[0548]
采用通用方法12,用[4-氯-31-甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体,56%收率)。
[0549]
通过手性柱色谱分离得到对映体纯产物。
[0550]
实施例9a(e1)
[0551]c28h27
cln4o6s的hrms计算值:582.1340;[m+h]
+
,实测值:583.1418(δ=0.9ppm)。
[0552]
实施例9b(e2)
[0553]c28h27
cln4o6s的hrms计算值:582.1340;[m+h]
+
,实测值:583.1417(δ=0.8ppm)。
[0554]1h-nmr(400mhz,dmso-d6)δppm:12.28(m,1h),7.69(d,1h),7.64(dd,1h),7.57(d,1h),7.44(d,1h),6.99(d,1h),6.79(dd,1h),6.78(d,1h),5.85(d,1h),4.84-4.7(m,1h),4.8(t,2h),4.23/4.05(dd,2h),4/3.83(dd,2h),3.67/3.45(2m,2h),3.09/2.96(2dd,2h),2.63(s,3h),2.2/2.08(2m,2h),1.82/1.63(2m,2h)。
[0555]
实施例10:[4-甲氧基-31-甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸
[0556][0557]
步骤1:3-[3-(羟基甲基)-4-甲氧基苯基]-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯的制备
[0558]
采用通用方法6,用(2e)-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙-2-烯酸乙酯(1当量)和[2-甲氧基-5-(4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷-2-基)苯基]甲醇(1.4当量)作为起始试剂,得到标题化合物(黄色油,68%收率)。
[0559]1h-nmr(400mhz,dmso-d6)δppm:7.6(d,1h),7.45(d,1h),7.28(d,1h),7.2(d,2h),7.19(dd,1h),6.9(d,2h),6.82(d,1h),4.9(t,1h),4.82(t,1h),4.65(t,2h),4.41(d,2h),4.31(s,2h),3.92(q,2h),3.71(2s,6h),3.4(t,2h),3.12(dd,2h),2.78(s,3h),1.91(m,2h),1.5(m,2h),1(t,3h)。
[0560]
步骤2:3-(3-{[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-甲氧基苯基)-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯的制备
[0561]
采用通用方法7,用3-[3-(羟基甲基)-4-甲氧基苯基]-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙酸酯(1当量)和6-(苄氧基)-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮(1.1eq.)作为起始试剂,得到标题化合物(79%收率)。
[0562]1h-nmr(400mhz,dmso-d6)δppm:7.6(d,1h),7.49(d,1h),7.45-7.3(m,5h),7.28(d,1h),7.21(dd,1h),7.18(d,2h),7-6.9(m,3h),6.85(d,3h),5.08(s,2h),4.8(t,1h),4.65(t,2h),4.52(s,2h),4.31(s,2h),4.2(s,2h),3.92(q,2h),3.72/3.65(2s,6h),3.38(t,2h),3.12(d,2h),2.79(s,3h),1.9(m,2h),1.45(m,2h),1(t,3h)。
[0563]
步骤3:3-[1-(4-羟基丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲氧基苯基}丙酸乙酯的制备
[0564]
采用通用方法8,用3-(3-{[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-甲氧基苯基)-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三
4-甲基苯基]丙酸乙酯的制备
[0598]
采用通用方法6,用(2e)-3-{1-[6-(苄氧基)己基]-4-甲基-1h-苯并三唑-5-基}丙-2-烯酸乙酯(1当量)和[2-甲基-5-(4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷-2-基)苯基]甲醇(1.5当量)作为起始试剂,得到标题化合物(14%收率)。
[0599]1h-nmr(400mhz,dmso-d6)δppm:7.6(d,1h),7.45(d,1h),7.3(s,1h),7.3(m,5h),7.1(d,1h),7(d,1h),5(t,1h),4.85(t,1h),4.65(t,2h),4.4(2s,4h),3.95(q,2h),3.35(t,2h),3.15(m,2h),2.75(s,3h),2.15(s,3h),1.85(m,2h),1.5(m,2h),1.35-1.2(m,4h),1(t,3h)。
[0600]
步骤2:3-(3-{[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-甲基苯基)-3-{1-[6-(苄氧基)己基]-4-甲基-1h-苯并三唑-5-基}丙酸乙酯的制备
[0601]
采用通用方法7,用3-{1-[6-(苄氧基)己基]-4-甲基-1h-苯并三唑-5-基}-3-[3-(羟基甲基)-4-甲基苯基]丙酸乙酯(1当量)和6-(苄氧基)-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮(1.2当量)作为起始试剂,得到标题化合物(84%收率)。
[0602]1h-nmr(400mhz,dmso-d6)δppm:7.61-6.93(m,18h),5.1(s,2h),4.84(t,1h),4.58(t,2h),4.42/4.21(s,2h),4.42/4.21(s,2h),4.38(s,2h),3.92(q,2h),3.32(m,2h),3.16(m,2h),2.76(s,3h),2.21(s,3h),1.83(m,2h),1.45(m,2h),1.3(m,2h),1.19(m,2h),0.97(t,3h)。
[0603]
步骤3:3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}-3-[1-(6-羟基己基)-4-甲基-1h-苯并三唑-5-基]丙酸乙酯的制备
[0604]
采用通用方法8,用3-(3-{[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-甲基苯基)-3-{1-[6-(苄氧基)己基]-4-甲基-1h-苯并三唑-5-基}丙酸乙酯(1当量)作为起始试剂,得到标题化合物(95%收率)。
[0605]1h-nmr(400mhz,dmso-d6)δppm:9.68(m,1h),7.61(d,1h),7.5(d,1h),7.21(d,1h),7.19(dd,1h),7.13(d,1h),6.99(d,1h),6.79(dd,1h),6.6(d,1h),4.84(t,1h),4.63(t,2h),4.38(s,2h),4.29(t,1h),4.2(dd,2h),3.94(q,2h),3.32(m,2h),3.17(m,2h),2.75(s,3h),2.22(s,3h),1.87(m,2h),1.38-1.15(m,6h),0.99(t,3h)。
[0606]
步骤4:3-[1-(6-溴己基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}丙酸乙酯的制备
[0607]
采用通用方法9,用3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}-3-[1-(6-羟基己基)-4-甲基-1h-苯并三唑-5-基]丙酸乙酯(1当量)作为起始试剂,得到标题化合物(87%收率)。
[0608]1h-nmr(400mhz,dmso-d6)δppm:9.68(m,1h),7.61(d,1h),7.5(d,1h),7.21(d,1h),7.2(dd,1h),7.13(d,1h),6.99(d,1h),6.78(dd,1h),6.6(d,1h),4.84(t,1h),4.63(t,2h),4.38(s,2h),4.19(dd,2h),3.94(q,2h),3.46(t,2h),3.16(dd,2h),2.75(s,3h),2.22(s,3h),1.88(m,2h),1.74(m,2h),1.39(m,2h),1.24(m,2h),1(t,3h)。
[0609]
步骤5:[4,33-二甲基-29,29-二氧代-23,28-二氧杂-29λ
6-硫杂-1,14,15,16-四氮杂六环[22.5.3.1
3,7
.1
9,13
.0
12,16
.0
27,31
]三十四碳-3(34),4,6,9(33),10,12,14,24,26,31-十烯-8-基]乙酸乙酯的制备
[0610]
采用通用方法11,用3-[1-(6-溴己基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(6-羟
基)丙酸乙酯的制备
[0626]
采用通用方法6,用(2e)-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙-2-烯酸乙酯(1当量)和[3-(4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷-2-基)-5-(三氟甲基)苯基]甲醇(1当量)作为起始试剂,得到3-[3-(羟基甲基)-5-(三氟甲基)苯基]-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯(无色油,16%收率)。将粗产物用通用方法7与6-(苄氧基)-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮(1.1当量)进行反应得到标题化合物(85%收率)。
[0627]1h-nmr(400mhz,dmso-d6)δppm:7.68(s,1h),7.61(d,1h),7.6(s,1h),7.52(s,1h),7.5(d,1h),7.42-7.3(m,5h),7.19(d,2h),7-6.9(m,3h),6.88(d,2h),5.05(s,2h),4.95(t,1h),4.7(t,2h),4.62(s,2h),4.42/4.3(2s,4h),3.92(q,2h),3.71(s,3h),3.38(t,2h),3.21(d,2h),2.79(s,3h),1.9(m,2h),1.48(m,2h),1(t,3h)。
[0628]
步骤2:3-[1-(4-羟基丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-5-(三氟甲基)苯基}丙酸乙酯的制备
[0629]
采用通用方法8,用3-[3-{[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-5-(三氟甲基)苯基]-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体,89%收率)。
[0630]1h-nmr(400mhz,dmso-d6)δppm:9.59(s),7.67(sl,1h),7.65(d,1h),7.61(sl,1h),7.53(sl,1h),7.52(d,1h),6.8(d,1h),6.68(dd,1h),6.58(d,1h),4.95(t,1h),4.65(t,2h),4.63(s,2h),4.41(t),4.4(s,2h),3.95(q,2h),3.38(q,2h),3.23(d,2h),2.78(s,3h),1.91(m,2h),1.37(m,2h),1.01(t,3h)。
[0631]
步骤3:3-[1-(4-溴丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-5-(三氟甲基)苯基}丙酸乙酯的制备
[0632]
采用通用方法9,用3-[1-(4-羟基丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-5-(三氟甲基)苯基}丙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体,50%收率)。
[0633]1h-nmr(400mhz,dmso-d6)δppm:9.6(s,1h),7.69/7.6/7.52(3sl,3h),7.69(d,1h),7.55(d,1h),6.8(d,1h),6.7(dd,1h),6.58(d,1h),4.98(t,1h),4.7(t,2h),4.6(s,2h),4.4(s,2h),3.92(q,2h),3.55(t,2h),3.22(d,2h),2.79(s,3h),2(m,2h),1.78(m,2h),1.02(t,3h)。
[0634]
步骤4:[31-甲基-27,27-二氧代-5-(三氟甲基)-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯的制备
[0635]
采用通用方法11,用3-[1-(4-溴丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-5-(三氟甲基)苯基}丙酸乙酯(1当量)作为起始试剂,得到标题化合物(93%收率)。
[0636]1h-nmr(400mhz,dmso-d6)δppm:7.81/7.6/7.25(3s,3h),7.71/4.81(2m,2h),7.6(d,1h),7.35(d,1h),6.9(d,1h),6.69(dd,1h),6.02(d,1h),4.81(t,1h),4.28(s,2h),4.05(m,2h),3.95(m,2h),3.88/3.68(2m,2h),3.32/3.18(2dd,2h),2.78(s,3h),2.2/1.98(2m,2h),1.68/1.45(2m,2h),1(t,3h)。
[0637]
步骤5:实施例12的制备
[0638]
采用通用方法12,用[31-甲基-27,27-二氧代-5-(三氟甲基)-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体,定量)。
[0639]
通过手性柱色谱分离得到对映体纯产物。
[0640]
实施例12a(e1)
[0641]c29h27
f3n4o6s的hrms计算值:616.1603;[m+h]
+
,实测值:617.1677(δ=0.1ppm)。
[0642]
实施例12b(e2)
[0643]c29h27
f3n4o6s的hrms计算值:616.1603;[m+h]
+
,实测值:617.1678(δ=0.3ppm)。
[0644]1h-nmr(400mhz,dmso-d6)δppm:12.3(m,1h),7.84/7.58/7.23(3s,3h),7.6(d,1h),7.33(d,1h),6.89(d,1h),6.68(dd,1h),6.02(d,1h),4.89(t,1h),4.81/4.72(2m,2h),4.27(s,2h),4.06(m,2h),3.68/3.34(2m,2h),3.32/3.18(2dd,2h),2.78(s,3h),2.2/1.98(2m,2h),1.69/1.45(2m,2h)。
[0645]
实施例13:[(2r,8r)-2,4,32-三甲基-28,28-二氧代-19,22,27-三氧杂-28λ
6-硫杂-1,14,15,16-四氮杂六环[21.5.3.1
3,7
.1
9,13
.0
12,16
.0
26,30
]三十三碳-3(33),4,6,9(32),10,12,14,23,25,30-十烯-8-基]乙酸和
[0646]
[(2r,8s)-2,4,32-三甲基-28,28-二氧代-19,22,27-三氧杂-28λ
6-硫杂-1,14,15,16-四氮杂六环[21.5.3.1
3,7
.1
9,13
.0
12,16
.0
26,30
]三十三碳-3(33),4,6,9(32),10,12,14,23,25,30-十烯-8-基]乙酸
[0647][0648]
步骤a1:2-[2-(3-甲基-2-硝基苯氨基)乙氧基]乙-1-醇的制备
[0649]
采用通用方法1步骤1,用1-氟-3-甲基-2-硝基苯(1当量)和2-(2-氨基乙氧基)乙-1-醇(3当量)作为起始试剂,得到标题化合物(24%收率)。
[0650]1h-nmr(400mhz,dmso-d6)δppm:7.28(t,1h),6.83(d,1h),6.58(d,1h),6.43(t,1h),4.59(t,1h),3.6(t,2h),3.5(m,2h),3.45(m,2h),3.34(q,2h),2.31(s,3h)。
[0651]
步骤a2:2-[2-(4-溴-3-甲基-2-硝基苯氨基)乙氧基]乙-1-醇的制备
[0652]
采用通用方法1步骤2,用2-[2-(3-甲基-2-硝基苯氨基)乙氧基]乙-1-醇(1当量)作为起始试剂,得到标题化合物(67%收率)。
[0653]1h-nmr(400mhz,dmso-d6)δppm:7.53(d,1h),6.8(d,1h),6.1(t),4.56(t),3.56(t,2h),3.5(q,2h),3.44(t,2h),3.3(q,2h),2.28(s,3h)。
[0654]
步骤a3:2-[2-(2-氨基-4-溴-3-甲基苯氨基)乙氧基]乙-1-醇的制备
基)-3-{3-[(1s)-1-羟基乙基]-4-甲基苯基}丙酸乙酯(1当量)和6-(苄氧基)-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮(1.5当量)作为起始试剂,得到标题化合物(79%收率)。
[0671]1h-nmr(400mhz,dmso-d6)δppm:7.62(d,1h),7.5(d,1h),7.48-7(m,13h),7.1-6.96(m,2h),6.89/6.83(2d,1h),5.26(m,1h),5.08(m,2h),4.86(m,1h),4.78(m,2h),4.41(s,2h),4.28(s,2h),3.91(q,2h),3.88(m,2h),3.49/3.39(2m,4h),3.18(m,2h),2.76(s,3h),2.27(s,3h),1.4(d,3h),0.98(t,3h)。
[0672]
步骤3:3-{3-[(1r)-1-(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)乙基]-4-甲基苯基}-3-{1-[2-(2-羟基乙氧基)乙基]-4-甲基-1h-苯并三唑-5-基}丙酸乙酯的制备
[0673]
采用通用方法8,用3-(3-{(1r)-1-[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]乙基}-4-甲基苯基)-3-(1-{2-[2-(苄氧基)乙氧基]乙基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体,94%收率)。
[0674]1h-nmr(400mhz,dmso-d6)δppm:9.63(m,1h),7.65-7.53(2dd,2h),7.47(m,1h),7.14-7.08(m,2h),6.91(2,1h),6.76-6.7(m,1h),6.6/6.56(2d,1h),5.26(q,1h),4.88(q,1h),4.8(t,2h),4.37/4.31(s+dd,2h),3.95(2q,2h),3.89(m,2h),3.48-3.27(m,4h),3.22(2d,2h),2.77(s,3h),2.28(s,3h),1.43/1.41(2d,3h),1.02/1(2t,3h)。
[0675]
步骤4:3-{1-[2-(2-溴乙氧基)乙基]-4-甲基-1h-苯并三唑-5-基}-3-{3-[(1r)-1-(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)乙基]-4-甲基苯基}丙酸乙酯的制备
[0676]
采用通用方法9,用3-{3-[(1r)-1-(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)乙基]-4-甲基苯基}-3-{1-[2-(2-羟基乙氧基)乙基]-4-甲基-1h-苯并三唑-5-基}丙酸乙酯(1当量)作为起始试剂,得到标题化合物(71%收率)。
[0677]1h-nmr(400mhz,dmso-d6)δppm:9.64(m,1h),7.67-7.55(2dd,2h),7.47(m,1h),7.14-7.08(m,2h),6.91(m,1h),6.76-6.7(m,1h),6.6/6.56(2d,1h),5.26(q,1h),4.88(q,1h),4.83(t,2h),4.36/4.31(s+dd,2h),3.95(2q,2h),3.93(m,2h),3.66(m,2h),3.44(t,2h),3.3/3.22(2d,2h),2.77(s,3h),2.28(s,3h),1.43/1.41(2d,3h),1.02/1(2t,3h)。
[0678]
步骤5:[(2r)-2,4,32-三甲基-28,28-二氧代-19,22,27-三氧杂-28λ
6-硫杂-1,14,15,16-四氮杂六环[21.5.3.1
3,7
.1
9,13
.0
12,16
.0
26,30
]三十三碳-3(33),4,6,9(32),10,12,14,23,25,30-十烯-8-基]乙酸乙酯的制备
[0679]
采用通用方法11,用3-{1-[2-(2-溴乙氧基)乙基]-4-甲基-1h-苯并三唑-5-基}-3-{3-[(1r)-1-(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)乙基]-4-甲基苯基}丙酸乙酯(1当量)作为起始试剂,得到标题化合物(99%收率)。
[0680]1h-nmr(400mhz,dmso-d6)δppm:7.72/7.65(2d,1h),7.52/6.91(2s,1h),7.52/7.16(2d,1h),7.45/7.09(2d,1h),7.28/6.98(2d,1h),6.93/6.88(2d,1h),6.8/6.75(2d,1h),6.36/5.99(2sl,1h),5.4/5.26(2m,1h),4.93/4.85(2m,1h),4.83(m,2h),4.71/4.17/3.81(2m,2h),4.14-3.58(m,6h),4.03/3.93(2q,2h),3.23/2.96(m+dd,2h),2.81/2.8(2s,3h),2.33/2.29(2s,3h),1.53/1.42(s+sl,3h),1.17/1.02(2m,3h)。
[0681]
步骤6:实施例13的制备
[0682]
采用通用方法12,用[(2r)-2,4,32-三甲基-28,28-二氧代-19,22,27-三氧杂-28
λ
6-硫杂-1,14,15,16-四氮杂六环[21.5.3.1
3,7
.1
9,13
.0
12,16
.0
26,30
]三十三碳-3(33),4,6,9(32),10,12,14,23,25,30-十烯-8-基]乙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体,59%收率)。
[0683]
通过手性柱色谱分离得到非对映体纯的最终产物或最终中间体。
[0684]
实施例13a(2r,8r)
[0685]c30h32
n4o7s的hrms计算值:592.1992;[m+h]
+
,实测值:593.2072(δ=1.3ppm)
[0686]1h-nmr(400mhz,dmso-d6)δppm:13.6-11(m,1h),7.64(d,1h),7.48(dd,1h),7.27(d,1h),7.11(d,1h),6.94(d,1h),6.88(sl,1h),6.8(dd,1h),6.01(d,1h),5.24(q,1h),4.92(t,1h),4.81(t,2h),4.14/3.78(dd,2h),4.1/4.04(2m,2h),3.99-3.63(m,4h),3.06/2.75(2dd,2h),2.79(s,3h),2.33(s,3h),1.15(d,3h)。
[0687]
实施例13b(2r,8s)
[0688]c30h32
n4o7s的hrms计算值:592.1992;[m+h]
+
,实测值:593.2071(δ=1.1ppm)。
[0689]1h-nmr(400mhz,dmso-d6)δppm:13.6-11(m,1h),7.71(d,1h),7.51(d,1h),7.49(d,1h),7.1(dd,1h),6.99(d,1h),6.89(d,1h),6.76(dd,1h),6.33(d,1h),5.37(q,1h),4.88-4.77(m,3h),4.64/4.13(dd,2h),3.96(m,2h),3.96-3.58(m,4h),3.08(d,2h),2.79(s,3h),2.28(s,3h),1.49(d,3h)。
[0690]
钠盐的制备:
[0691]
于25℃将实施例13b的化合物(2.03g)和氢氧化钠(0.14g)悬浮于水(235ml)中。将叔丁醇(100ml)加入到悬浮液中并将反应混合物于60℃加热至少1小时(至完全溶解)。然后将溶液冷却至-20℃以快速固化,然后进行冷冻干燥96小时。从冷冻器中分离得到2.10g无定形的[(2r,8s)-2,4,32-三甲基-28,28-二氧代-19,22,27-三氧杂-28λ
6-硫杂-1,14,15,16-四氮杂六环[21.5.3.1
3,7
.1
9,13
.0
12,16
.0
26,30
]三十三碳-3(33),4,6,9(32),10,12,14,23,25,30-十烯-8-基]乙酸的钠盐(水含量:3.0%)。
[0692]
ir:2980至2860cm-1
(ch2,ch3),1574cm-1
(coo-asym),1492cm-1
(c=c),1391cm-1
(coo-sym和so
2 asym),1200至1130cm-1
(so
2 sym,=c-o-c asym和c-o-c asym)。
[0693]
实施例14:[4-氟-31-甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸
[0694][0695]
步骤1:3-(3-{[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-氟苯基)-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯的制备
[0696]
采用通用方法6,用(e)-3-[1-[4-[(4-甲氧基苯基)甲氧基]丁基]-4-甲基-苯并三唑-5-基]丙-2-烯酸乙酯(1当量)和[2-氟-5-(4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷-2-基)苯基]甲醇(1当量)作为起始试剂,得到3-[4-氟-3-(羟基甲基)苯基]-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯(17%收率)。将粗产物用通用方法7与6-(苄氧基)-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮(1.1当量)进行反应得到标题化合物(85%收率)。
[0697]1h-nmr(400mhz,dmso-d6)δppm:7.6(d,1h),7.5-7.35(m,5h),7.49(d,1h),7.35/7.3(m,2h),7.2(d,2h),7.08(t,1h),7-6.95(m,3h),6.88(d,2h),5.08(s,2h),4.88(t,1h),4.65(t,2h),4.58(s,2h),4.31(2s,4h),3.92(q,2h),3.71(s,3h),3.38(t,2h),3.18(d,2h),2.79(s,3h),1.91(m,2h),1.48(m,2h),1(t,3h)。
[0698]
步骤2:3-{4-氟-3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]苯基}-3-[1-(4-羟基丁基)-4-甲基-1h-苯并三唑-5-基]丙酸乙酯的制备
[0699]
采用通用方法8,用3-(3-{[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-氟苯基)-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体,77%收率)。
[0700]1h-nmr(400mhz,dmso-d6)δppm:9.4/4.4(s+t,2h),7.63(d,1h),7.5(d,1h),7.45(dd,1h),7.3(m,1h),7.1(t,1h),6.88(d,1h),6.71(dd,1h),6.61(d,1h),4.88(t,1h),4.67(t,2h),4.53(s,2h),4.3(s,2h),3.95(q,2h),3.4(q,2h),3.2(d,2h),2.78(s,3h),1.9(m,2h),1.38(m,2h),1.02(t,3h)。
[0701]
步骤3:3-[1-(4-溴丁基)-4-甲基-1h-苯并三唑-5-基]-3-{4-氟-3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]苯基}丙酸乙酯的制备
[0702]
采用通用方法9,用3-{4-氟-3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]苯基}-3-[1-(4-羟基丁基)-4-甲基-1h-苯并三唑-5-基]丙酸乙酯(1当量)作为起始试剂,得到标题化合物(31%收率)。
[0703]1h-nmr(400mhz,dmso-d6)δppm:9.6(s,1h),7.65(d,1h),7.51(d,1h),7.45(dd,1h),7.3(m,1h),7.1(t,1h),6.88(d,1h),6.71(dd,1h),6.6(d,1h),4.88(t,1h),4.7(t,2h),4.52(s,2h),4.31(s,2h),3.93(q,2h),3.55(t,2h),3.2(d,2h),2.79(s,3h),2(m,2h),1.8(m,2h),1(t,3h)。
[0704]
步骤4:[4-氟-31-甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯的制备
[0705]
采用通用方法11,用3-[1-(4-溴丁基)-4-甲基-1h-苯并三唑-5-基]-3-{4-氟-3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]苯基}丙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体,75%收率)。
[0706]1h-nmr(400mhz,dmso-d6)δppm:7.7(d,1h),7.61(dd,1h),7.45(d,1h),7.29(t,1h),6.98(d,1h),6.81(dd,1h),6.78(dd,1h),6.4(d,1h),4.85-4.7(m,3h),4.21/4.05(2d,2h),4.02/3.92(2d,2h),3.95(q,2h),3.68/3.42(2m,2h),3.2/3.1(2dd,2h),2.65(s,3h),2.2/2.02(2m,2h),1.8/1.65(2m,2h),1.01(t,3h)。
[0707]
步骤5:实施例14的制备
甲酸叔丁酯(1eq.,6.2g,16.39mmol)作为起始试剂,得到标题化合物(4.9g,70%收率)。
[0724]1h-nmr(400mhz,dmso-d6)δppm:7.69/7.65(2sl,2h),5.06(s,2h),2.29(s,3h),1.48(s,9h),1.3(s,12h)。
[0725]
步骤c5:6-羟基-8-甲基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-甲酸叔丁酯的制备
[0726]
采用通用方法5步骤3,用8-甲基-2,2-二氧代-6-(4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷-2-基)-2h-1,2λ6,3-噁噻嗪-3(4h)-甲酸叔丁酯(1eq.,4.9g,11.52mmol)作为起始试剂,得到标题化合物(3.9g,97%收率)。
[0727]1h-nmr(400mhz,dmso-d6)δppm:9.81(m,1h),6.74/6.7(2d,2h),4.9(s,2h),2.19(s,3h),1.48(s,9h)。
[0728]
步骤c6:6-(苄氧基)-8-甲基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-甲酸叔丁酯的制备
[0729]
采用通用方法5步骤4,用6-羟基-8-甲基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-甲酸叔丁酯(1eq.,2.9g,9.19mmol)作为起始试剂,得到标题化合物(5g,定量)。
[0730]1h-nmr(400mhz,dmso-d6)δppm:7.46-7.29(m,5h),7.12/7.03(2d,2h),5.1(s,2h),4.97(s,2h),2.26(s,3h),1.48(s,9h)。
[0731]
步骤c7:6-(苄氧基)-8-甲基-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮的制备
[0732]
采用通用方法5步骤5,用6-(苄氧基)-8-甲基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-甲酸叔丁酯(1eq.,5.0g,12.33mmol)作为起始试剂,得到标题化合物(1.85g,65%收率)。
[0733]1h-nmr(400mhz,dmso-d6)δppm:8.37(m,1h),7.46-7.3(m,5h),6.92/6.79(2d,2h),5.06(s,2h),4.47(s,2h),2.16(s,3h)。
[0734]
步骤1:3-[3-(羟基甲基)-4-甲基苯基]-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯的制备
[0735]
采用通用方法6,用(e)-3-[1-[4-[(4-甲氧基苯基)甲氧基]丁基]-4-甲基-苯并三唑-5-基]丙-2-烯酸乙酯(1当量)和[2-甲基-5-(4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷-2-基)苯基]甲醇(2当量)作为起始试剂,得到标题化合物(43%收率)。
[0736]1h-nmr(400mhz,dmso-d6)δppm:7.58(d,1h),7.45(d,1h),7.28(d,1h),7.2(d,2h),7.1(dd,1h),7.01(d,1h),6.88(d,2h),4.98(t,1h),4.82(t,1h),4.65(t,2h),4.4(d,2h),4.3(s,2h),3.91(q,2h),3.71(s,3h),3.4(t,2h),3.11(dd,2h),2.75(s,3h),2.15(s,3h),1.91(m,2h),1.48(m,2h),1(t,3h)。
[0737]
步骤2:3-(3-{[6-(苄氧基)-8-甲基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-甲基苯基)-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯的制备
[0738]
采用通用方法7,用3-[3-(羟基甲基)-4-甲基苯基]-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯(1当量)和6-(苄氧基)-8-甲基-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮(1.5当量)作为起始试剂,得到标题化合物(88%收率)。
[0739]1h-nmr(400mhz,dmso-d6)δppm:7.56(d,1h),7.47(d,1h),7.46-7.31(m,5h),7.46-7.12(m,3h),7.19(d,2h),7/6.75(2d,2h),6.86(d,2h),5.08(s,2h),4.85(t,1h),4.6
(t,2h),4.38(s,2h),4.23(s,2h),4.21(s,2h),3.92(q,2h),3.72(s,3h),3.35(t,2h),3.16(m,2h),2.76(s,3h),2.22/2.21(2s,6h),1.89(m,2h),1.44(m,2h),0.97(t,3h)。
[0740]
步骤3:3-[1-(4-羟基丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(6-羟基-8-甲基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}丙酸乙酯的制备
[0741]
采用通用方法8,用3-(3-{[6-(苄氧基)-8-甲基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-甲基苯基)-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体,97%收率)。
[0742]1h-nmr(400mhz,dmso-d6)δppm:9.55(m,1h),7.61(d,1h),7.49(d,1h),7.22-7.11(3m,3h),6.68/6.42(2d,2h),4.84(t,1h),4.65(t,2h),4.34(s,2h),4.19(dd,2h),3.94(q,2h),3.38(t,2h),3.18/3.13(2dd,2h),2.75(s,3h),2.22/2.17(2s,6h),1.9(m,2h),1.36(m,2h),1(t,3h)。
[0743]
步骤4:3-[1-(4-溴丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(6-羟基-8-甲基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}丙酸乙酯的制备
[0744]
采用通用方法9,用3-[1-(4-羟基丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(6-羟基-8-甲基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}丙酸乙酯(1当量)作为起始试剂,得到标题化合物(78%收率)。
[0745]1h-nmr(400mhz,dmso-d6)δppm:9.55(s,1h),7.65(d,1h),7.5(d,1h),7.2(m,2h),7.11(d,1h),6.7/6.41(2d,2h),4.85(t,1h),4.7(t,2h),4.38(s,2h),4.2(m,2h),3.95(q,2h),3.55(t,2h),3.18(m,2h),2.78(s,3h),2.22/2.18(2s,6h),1.98(m,2h),1.78(m,2h),1(t,3h)。
[0746]
步骤5:[4,24,31-三甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯的制备
[0747]
采用通用方法11,用3-[1-(4-溴丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(6-羟基-8-甲基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}丙酸乙酯(1当量)作为起始试剂,得到标题化合物(定量)。
[0748]1h-nmr(400mhz,dmso-d6)δppm:7.67(d,1h),7.47(dd,1h),7.43(d,1h),7.43(d,1h),6.71(d,1h),6.55(d,1h),5.67(d,1h),4.84-4.7(m,3h),4.13-3.79(2dd,4h),3.92(q,2h),3.63-3.43(2m,2h),3.17/3.04(2dd,2h),2.63(s,3h),2.33(s,3h),2.25-2(m,2h),2.11(s,3h),1.79/1.6(2m,2h),1(t,3h)。
[0749]
步骤6:实施例15的制备
[0750]
采用通用方法12,用[4,24,31-三甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体,66%收率)。
[0751]
通过手性柱色谱分离得到对映体纯产物。
[0752]
实施例15a(e1)
[0753]c30h32
n4o6s的hrms计算值:576.2042;[m+h]
+
,实测值:577.2119(δ=0.6ppm)。
[0754]
实施例15b(e2)
[0755]c30h32
n4o6s的hrms计算值:576.2042;[m+h]
+
,实测值:577.2117(δ=0.3ppm)。
[0756]1h-nmr(400mhz,dmso-d6)δppm:12.14(m,1h),7.67(d,1h),7.49(dd,1h),7.42(d,1h),7.29(d,1h),6.71(d,1h),6.53(d,1h),5.66(d,1h),4.84-4.7(m,3h),4.13-3.79(2dd,4h),3.63-3.43(2m,2h),3.07/2.94(2dd,2h),2.63(s,3h),2.33(s,3h),2.19/2.08(2m,2h),2.11(s,3h),1.8/1.6(2m,2h)。
[0757]
实施例16:[24-甲氧基-4,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸
[0758][0759]
步骤c1:6-溴-8-甲氧基-2h-1,2λ6,3-噁噻嗪-2,2-二酮的制备
[0760]
采用通用方法4步骤2,用5-溴-2-羟基-3-甲氧基-苯甲醛(1当量)作为起始试剂,得到标题化合物(32%收率)。
[0761]1h-nmr(400mhz,dmso-d6)δppm:9.14(s,1h),7.83/7.79(2d,2h),3.98(s,3h)。
[0762]
步骤c2:6-溴-8-甲氧基-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮的制备
[0763]
采用通用方法4步骤3,用6-溴-8-甲氧基-2h-1,2λ6,3-噁噻嗪-2,2-二酮(1当量)作为起始试剂,得到标题化合物(95%收率)。
[0764]1h-nmr(400mhz,dmso-d6)δppm:8.6(sl,1h),7.26(d,1h),7.1(d,1h),4.55(s,2h),3.85(s,3h)。
[0765]
步骤c3:6-溴-8-甲氧基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-甲酸叔丁酯的制备
[0766]
采用通用方法5步骤1,用6-溴-8-甲氧基-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮(1当量)作为起始试剂,得到标题化合物(88%收率)。
[0767]1h-nmr(400mhz,dmso-d6)δppm:7.48(s,1h),7.4(s,1h),5.05(s,2h),3.9(s,3h),1.5(s,9h)。
[0768]
步骤c4:8-甲氧基-2,2-二氧代-6-(4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷-2-基)-2h-1,2λ6,3-噁噻嗪-3(4h)-甲酸叔丁酯的制备
[0769]
采用通用方法5步骤2,用6-溴-8-甲氧基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-甲酸叔丁酯(1当量)作为起始试剂,得到标题化合物(80%收率)。
[0770]1h-nmr(400mhz,dmso-d6)δppm:7.41(d,1h),7.31(d,1h),5.09(s,2h),3.9(s,3h),1.49(s,9h),1.3(s,12h)。
[0771]
步骤c5:6-羟基-8-甲氧基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-甲酸叔丁酯的制备
[0772]
采用通用方法5步骤3,用8-甲氧基-2,2-二氧代-6-(4,4,5,5-四甲基-1,3,2-二氧
羟基-8-甲氧基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}丙酸乙酯(1当量)作为起始试剂,得到标题化合物(黄色固体,86%收率)。
[0788]1h-nmr(400mhz,dmso-d6)δppm:9.69(s,1h),7.62(d,1h),7.5(d,1h),7.2(d,1h),7.19(dd,1h),7.11(d,1h),6.5(d,1h),6.11(d,1h),4.82(t,1h),4.68(t,2h),4.32(s,2h),4.19(m,2h),3.91(q,2h),3.79(s,3h),3.51(t,2h),3.18(m,2h),2.73(s,3h),2.2(s,3h),1.99(m,2h),1.78(m,2h),1(t,3h)。
[0789]
步骤4:[24-甲氧基-4,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯的制备
[0790]
采用通用方法11,用3-[1-(4-溴丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(6-羟基-8-甲氧基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}丙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体,73%收率)。
[0791]
通过手性柱色谱分离得到对映体纯的最终中间体。
[0792]1h-nmr(400mhz,dmso-d6)δppm:7.69(d,1h),7.48(dd,1h),7.42(d,1h),7.29(d,1h),6.57/6.51(2d,2h),5.32(d,1h),4.79(m,3h),4.12/3.8(2d,2h),3.91/3.8(2d,2h),3.91(q,2h),3.74(s,3h),3.6/3.39(m,2h),3.14/3.03(m,2h),2.61(s,3h),2.3(s,3h),2.2/2.05(m,2h),1.8/1.6(m,2h),1(t,3h)。
[0793]
步骤5:实施例16的制备
[0794]
采用通用方法12,用[24-甲氧基-4,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯e1(1当量)或e2(1当量)作为起始试剂,得到标题化合物(收率分别为85%-67%)。
[0795]
实施例16a(e1)
[0796]c30h32
n4o7s的hrms计算值:592.1992;[m+h]
+
,实测值:593.2070(δ=0.9ppm)。
[0797]
实施例16b(e2)
[0798]c30h32
n4o7s的hrms计算值:592.1992;[m+h]
+
,实测值:[m+h]+=593.2073(δ=1.4ppm)。
[0799]1h-nmr(400mhz,dmso-d6)δppm:12.2(m,1h),7.68(d,1h),7.49(dd,1h),7.41(d,1h),7.29(d,1h),5.31(d,1h),4.75(m,3h),4.11/3.92(2d,2h),3.98/3.8(2d,2h),3.73(s,3h),3.59/3.33(2m,2h),3.52/3.51(2d,2h),3.05/2.92(2dd,2h),2.6(s,3h),2.3(s,3h),2.19/2.07(2m,2h),1.8/1.6(2m,2h)。
[0800]
实施例17:[24-氟-4,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸
[0801][0802]
步骤c1:6-溴-8-氟-2h-1,2λ6,3-噁噻嗪-2,2-二酮的制备
[0803]
采用通用方法4步骤2,用5-溴-3-氟-2-羟基苯甲醛(1当量)作为起始试剂,得到标题化合物(25%收率)。
[0804]1h-nmr(400mhz,dmso-d6)δppm:9.2(s,1h),8.3(dd,1h),8.1(s,1h)。
[0805]
步骤c2:6-溴-8-氟-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮的制备
[0806]
采用通用方法4步骤3,用6-溴-8-氟-2h-1,2λ6,3-噁噻嗪-2,2-二酮(1当量)作为起始试剂,得到标题化合物(87%收率)。
[0807]1h-nmr(400mhz,dmso-d6)δppm:8.91(sl,1h),7.72(dd,1h),7.41(tf,1h),4.68(s,2h)。
[0808]
步骤c3:6-溴-8-氟-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-甲酸叔丁酯的制备
[0809]
采用通用方法5步骤1,用6-溴-8-氟-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮(1当量)作为起始试剂,得到标题化合物(85%收率)。
[0810]1h-nmr(400mhz,dmso-d6)δppm:7.88(d,1h),7.74(s,1h),5.18(s,2h),1.5(s,9h)。
[0811]
步骤c4:8-氟-2,2-二氧代-6-(4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷-2-基)-2h-1,2λ6,3-噁噻嗪-3(4h)-甲酸叔丁酯的制备
[0812]
采用通用方法5步骤2,用6-溴-8-氟-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-甲酸叔丁酯(1当量)作为起始试剂,得到标题化合物(71%收率)。
[0813]1h-nmr(400mhz,dmso-d6)δppm:7.69(s,1h),7.57(d,1h),5.21(s,2h),1.49(s,9h),1.31(s,12h)。
[0814]
步骤c5:8-氟-6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-甲酸叔丁酯的制备
[0815]
采用通用方法5步骤3,用8-氟-2,2-二氧代-6-(4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷-2-基)-2h-1,2λ6,3-噁噻嗪-3(4h)-甲酸叔丁酯(1当量)作为起始试剂,得到标题化合物(81%收率)。1h-nmr(400mhz,dmso-d6)δppm:10.4(m,1h),6.79(dd,1h),6.78(d,1h),5.02(s,2h),1.49(s,9h)。
[0816]
步骤c6:6-(苄氧基)-8-氟-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮的制备
[0817]
采用通用方法5步骤4,用8-氟-6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-甲酸叔丁酯(1当量)作为反应试剂,得到6-(苄氧基)-8-氟-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-甲酸叔丁酯(36%收率)。将粗产物用通用方法5步骤5进行反应得到标题化合物(91%收率)。
[0818]1h-nmr(400mhz,dmso-d6)δppm:8.7(m,1h),7.48-7.3(m,5h),7.1(dd,1h),6.8(d,1h),5.09(s,2h),4.58(s,2h)。
[0819]
步骤1:3-(3-{[6-(苄氧基)-8-氟-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-甲基苯基)-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯的制备
[0820]
采用通用方法7,用3-[3-(羟基甲基)-4-甲基苯基]-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯(1当量)和6-(苄氧基)-8-氟-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮(1当量)作为起始试剂,得到标题化合物(85%收率)。
[0821]1h-nmr(400mhz,dmso-d6)δppm:0.97(t,j=7.09hz,3h)1.39-1.51(m,2h)1.89(quint,j=7.27hz,2h)1.99(s,2h)2.22(s,3h)2.76(s,3h)3.16(dd,j=8.07,2.69hz,2h)3.35(t,j=6.30hz,2h)3.72(s,3h)3.92(q,j=7.05hz,2h)4.24-4.32(m,4h)4.49(s,2h)4.60(t,j=6.97hz,2h)4.84(t,j=8.07hz,1h)5.11(s,2h)6.79(s,1h)6.82-6.89(m,2h)7.10-7.22(m,5h)7.24(s,1h)7.32-7.50(m,6h)7.53-7.59(m,1h)。
[0822]
步骤2:3-{3-[(8-氟-6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}-3-[1-(4-羟基丁基)-4-甲基-1h-苯并三唑-5-基]丙酸乙酯的制备
[0823]
采用通用方法8,用3-(3-{[6-(苄氧基)-8-氟-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-甲基苯基)-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体,97%收率)。
[0824]1h-nmr(400mhz,dmso-d6)δppm:10.1/4.4(s+t,2h),7.62(d,1h),7.5(d,1h),7.28(d,1h),7.2(dd,1h),7.15(d,1h),6.78(dd,1h),6.48(d,1h),4.85(t,1h),4.65(t,2h),4.49(s,2h),4.28(m,2h),3.95(q,2h),3.4(q,2h),3.18(d,2h),2.78(s,3h),2.22(s,3h),1.9(m,2h),1.38(m,2h),1(t,3h)。
[0825]
步骤3:3-[1-(4-溴丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(8-氟-6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}丙酸乙酯的制备
[0826]
采用通用方法9,用3-{3-[(8-氟-6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}-3-[1-(4-羟基丁基)-4-甲基-1h-苯并三唑-5-基]丙酸乙酯(1当量)作为起始试剂,得到标题化合物(灰白色固体,65%收率)。
[0827]1h-nmr(400mhz,dmso-d6)δppm:10.1(s,1h),7.62(d,1h),7.5(d,1h),7.22(d,1h),7.19(dd,1h),7.12(d,1h),6.78(d,1h),6.45(d,1h),4.83(t,1h),4.69(t,2h),4.48(s,2h),4.26(m,2h),3.91(q,2h),3.51(t,2h),3.15(m,2h),2.73(s,3h),2.21(s,3h),2(m,2h),1.78(m,2h),1(t,3h)。
[0828]
步骤4:[24-氟-4,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯的制备
[0829]
采用通用方法11,用3-[1-(4-溴丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(8-氟-6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}丙酸乙酯(1当量)作为起始试剂,得到标题化合物(灰白色固体,74%收率)。
[0830]
通过手性柱色谱分离得到对映体纯的最终中间体。
[0831]1h-nmr(400mhz,dmso-d6)δppm:7.68(d,1h),7.49(dd,1h),7.41(d,1h),7.3(d,
1h),6.9(dd,1h),6.6(d,1h),5.75(d,1h),4.79(m,3h),4.2/4.02(2d,2h),4.02/3.95(2d,2h),3.95(q,2h),3.7/3.5(2m,2h),3.18/3.05(2dd,2h),2.63(s,3h),2.32(s,3h),2.2/2.05(2m,2h),1.8/1.62(2m,2h),1(t,3h)。
[0832]
步骤5:实施例17的制备
[0833]
采用通用方法12,用[24-氟-4,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯e1(1当量)或e2(1当量)作为起始试剂,得到标题化合物(收率分别为65%-99%)。
[0834]
实施例17a(e1)
[0835]c29h29
fn4o6s的hrms计算值:580.1792;[m+h]
+
,实测值:581.1871(δ=1.1ppm)。
[0836]
实施例17b(e2)
[0837]c29h29
fn4o6s的hrms计算值:580.1792;[m+h]
+
,实测值:581.1867(δ=0.4ppm)。
[0838]1h-nmr(400mhz,dmso-d6)δppm:12.3(m,1h),7.55(d,1h),7.5(dd,1h),7.4(d,1h),7.3(d,1h),6.9(dd,1h),6.55(d,1h),5.7(sl,1h),4.8(m,3h),4.15/4(2d,2h),4/3.9(2d,2h),3.7/3.5(2m,2h),3/2.9(2m,2h),2.6(s,3h),2.3(s,3h),2.2/2.1(2m,2h),1.8/1.6(2m,2h)。
[0839]
19
f-nmr(376mhz,dmso-d6)δppm:133。
[0840]
实施例18:[5-氟-4,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸
[0841][0842]
步骤b1:(5-溴-3-氟-2-甲基苯基)甲醇的制备
[0843]
将氢化铝锂(4eq.,3.07g,80.9mmol)置于圆底烧瓶中。加入无水thf(5ml/mmol,101ml),将混合物冷却至0℃。于0℃滴加5-溴-3-氟-2-甲基苯甲酸甲酯(5g,20.2mmol)的无水thf溶液(5ml/mmol,101ml),同时继续搅拌。将反应混合物升温至室温并在该温度下搅拌过夜。反应完成后将混合物小心地用150ml水淬灭并加入100ml 2m naoh水溶液。将混合物浓缩至干,然后通过正相硅胶色谱纯化,用dcm-etoh(90:10)作为洗脱剂得到标题化合物(1.8g,41%收率)。
[0844]1h-nmr(400mhz,dmso-d6)δppm:7.41(d,1h),7.35(dd,1h),5.35(t,1h),4.5(d,2h),2.1(s,3h)
[0845]
步骤b2:[3-氟-2-甲基-5-(4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷-2-基)苯基]甲醇的制备
[0846]
采用通用方法3,用(5-溴-3-氟-2-甲基苯基)甲醇(1eq.,1.8g,8.2mmol)作为起始试剂,得到标题化合物(2.5g,73%收率)。
[0847]1h-nmr(400mhz,dmso-d6)δppm:7.55(s,1h),7.2(d,1h),5.2(t,1h),4.52(d,2h),2.18(s,3h),1.31(s,12h)。
[0848]
步骤1:3-[3-氟-5-(羟基甲基)-4-甲基苯基]-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯的制备
[0849]
采用通用方法6,用(2e)-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙-2-烯酸乙酯(1当量)和[3-氟-2-甲基-5-(4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷-2-基)苯基]甲醇(1.4当量)作为起始试剂,得到标题化合物(32%收率)。
[0850]1h-nmr(400mhz,dmso-d6)δppm:7.6(d,1h),7.5(d,1h),7.2(d,2h),7.12(sl,1h),7.05(d,1h),6.9(d,2h),5.1(t,1h),4.82(t,1h),4.65(t,2h),4.45(d,2h),4.32(s,2h),3.95(q,2h),3.72(s,3h),3.4(t,2h),3.15(t,2h),2.78(s,3h),2.08(s,3h),1.92(m,2h),1.5(m,2h),1(t,3h)。
[0851]
步骤2:3-(3-{[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-5-氟-4-甲基苯基)-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯的制备
[0852]
采用通用方法7,用3-[3-氟-5-(羟基甲基)-4-甲基苯基]-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯(1当量)和6-(苄氧基)-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮(1.1当量)作为起始试剂,得到标题化合物(91%收率)。
[0853]1h-nmr(400mhz,dmso-d6)δppm:7.6/7.5(2d,2h),7.45(dl,2h),7.4(t,2h),7.35(tl,1h),7.2(d,2h),7.1(m,3h),7.05(dd,1h),6.95(d,1h),6.85(d,2h),5.1(s,2h),4.85(t,1h),4.6(t,2h),4.45-4.25(3s,6h),3.95(q,2h),3.7(s,3h),3.35(t,2h),3.2(m,2h),2.8(sl,3h),2.1(sl,3h),1.9(quint,2h),1.45(quint,2h),1(t,3h)。
[0854]
步骤3:3-{3-氟-5-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}-3-[1-(4-羟基丁基)-4-甲基-1h-苯并三唑-5-基]丙酸乙酯的制备
[0855]
采用通用方法8,用3-(3-{[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-5-氟-4-甲基苯基)-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体,定量)。
[0856]1h-nmr(400mhz,dmso-d6)δppm:9.7(s,1h),7.6(d,1h),7.5(d,1h),7.15(m,2h),7(d,1h),6.8(dd,1h),6.6(d,1h),4.85(t,1h),4.65(t,2h),4.4(m,3h),4.25(2d,2h),3.9(q,2h),3.4(q,2h),3.2(m,2h),2.8(s,3h),2.1(d,3h),1.9(quint,2h),1.4(quint,2h),1(t,3h)。
[0857]
步骤4:3-[1-(4-溴丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-氟-5-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}丙酸乙酯的制备
[0858]
采用通用方法9,用3-{3-氟-5-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}-3-[1-(4-羟基丁基)-4-甲基-1h-苯并三唑-5-基]丙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体,73%收率)。
[0859]1h-nmr(400mhz,dmso-d6)δppm:9.7(s,1h),7.65/7.5(2d,2h),7.15(m,2h),7(d,1h),6.8(dd,1h),6.6(d,1h),4.85(t,1h),4.7(t,2h),4.4(2d,2h),4.25(2d,2h),3.9(q,
2h),3.5(t,2h),3.2(m,2h),2.75(sl,3h),2.1(d,3h),2(m,2h),1.8(quint,2h),1(t,3h)。
[0860]
步骤5:[5-氟-4,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯的制备
[0861]
采用通用方法11,用3-[1-(4-溴丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-氟-5-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}丙酸乙酯(1当量)作为起始试剂,得到标题化合物(96%收率)。
[0862]
通过手性柱色谱分离得到对映体纯的最终中间体。
[0863]1h-nmr(400mhz,dmso-d6)δppm:1.17(t,j=7.15hz,3h)1.58(dt,j=13.63,6.76hz,1h)1.70-1.86(m,1h)2.20-2.27(m,3h)2.65(s,3h)3.05(dd,j=15.83,8.74hz,1h)3.16-3.26(m,1h)3.43-3.57(m,1h)3.62-3.73(m,1h)3.83-4.00(m,7h)4.03-4.17(m,4h)4.63-4.89(m,4h)5.89(d,j=2.81hz,1h)6.45(s,1h)6.79(dd,j=9.05,2.93hz,1h)6.97-7.01(m,1h)7.39-7.47(m,2h)7.68(d,j=8.68hz,1h)。
[0864]
步骤6:实施例18的制备
[0865]
采用通用方法12,用[5-氟-4,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯e1(1当量)或e2(1当量)作为反应试剂得到标题化合物(收率分别为80%-72%)。
[0866]
实施例18a(e1)
[0867]c29h29
fn4o6s的hrms计算值:580.1792;[m+h]
+
,实测值:581.1867(δ=0.4ppm)。
[0868]
实施例18b(e2)
[0869]c29h29
fn4o6s的hrms计算值:580.1792;[m+h]
+
,实测值:581.1866(δ=0.2ppm)。
[0870]1h-nmr(400mhz,dmso-d6)δppm:12.2(m,1h),7.7(d,1h),7.41(2d,2h),7(d,1h),6.8(dd,1h),6.45(d,1h),5.9(d,1h),4.79(m,3h),4.09(m,2h),3.91(m,2h),3.68/3.45(2m,2h),3.1/2.95(2dd,2h),2.65(s,3h),2.22(s,3h),2.2/2.05(2m,2h),1.8/1.6(2m,2h)。
[0871]
实施例19:[(2r,8r)-2,4,33-三甲基-29,29-二氧代-23,28-二氧杂-29λ
6-硫杂-1,14,15,16-四氮杂六环[22.5.3.1
3,7
.1
9,13
.0
12,16
.0
27,31
]三十四碳-3(34),4,6,9(33),10,12,14,24,26,31-十烯-8-基]乙酸和
[0872]
[(2r,8s)-2,4,33-三甲基-29,29-二氧代-23,28-二氧杂-29λ
6-硫杂-1,14,15,16-四氮杂六环[22.5.3.1
3,7
.1
9,13
.0
12,16
.0
27,31
]三十四碳-3(34),4,6,9(33),10,12,14,24,26,31-十烯-8-基]乙酸
[0873][0874]
步骤1:3-{1-[6-(苄氧基)己基]-4-甲基-1h-苯并三唑-5-基}-3-{3-[(1s)-1-羟基乙基]-4-甲基苯基}丙酸乙酯的制备
[0875]
采用通用方法6,用(2e)-3-{1-[6-(苄氧基)己基]-4-甲基-1h-苯并三唑-5-基}丙-2-烯酸乙酯(1当量)(1s)-1-[2-甲基-5-(4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷-2-基)苯基]乙-1-醇(2当量)作为起始试剂,得到标题化合物(70%收率)。
[0876]1h-nmr(400mhz,dmso-d6)δppm:7.59(d,1h),7.46(d,1h),7.4(d,1h),7.34-7.22(br,5h),6.99(d,1h),4.97(d,1h),4.82(m,1h),4.82(m,1h),4.62(dd,2h),4.4(s,2h),4.05(dd,1h),3.92(q,2h),3.36(t,2h),3.11(m,2h),2.75(s,3h),2.19(s,3h),1.87(quint,2h),1.48(quint,2h),1.32(quint,2h),1.22(m,3h),1.22(m,2h),0.99(t,3h)。
[0877]
步骤2:3-(3-{(1r)-1-[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]乙基}-4-甲基苯基)-3-{1-[6-(苄氧基)己基]-4-甲基-1h-苯并三唑-5-基}丙酸乙酯的制备
[0878]
采用通用方法7,用3-{1-[6-(苄氧基)己基]-4-甲基-1h-苯并三唑-5-基}-3-{3-[(1s)-1-羟基乙基]-4-甲基苯基}丙酸乙酯(1当量)和6-(苄氧基)-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮(1.5当量)作为起始试剂,得到标题化合物(米黄色固体,71%收率)。
[0879]1h-nmr(400mhz,dmso-d6)δppm:0.95-1.00(m,3h)1.23-1.36(m,3h)1.37-1.49(m,5h)1.83(sxt,j=6.85hz,2h)1.99(s,1h)2.28(s,3h)2.76(d,j=3.67hz,3h)3.14-3.26(m,2h)3.33-3.36(m,1h)3.86-3.97(m,2h)4.27-4.49(m,4h)4.59(q,j=6.64hz,2h)4.87(td,j=7.98,4.10hz,1h)5.02-5.14(m,2h)5.27(q,j=6.93hz,1h)6.96-7.16(m,4h)7.24-7.48(m,11h)7.49-7.55(m,1h)7.57-7.63(m,1h)。
[0880]
步骤3:3-{3-[(1r)-1-(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)乙基]-4-甲基苯基}-3-[1-(6-羟基己基)-4-甲基-1h-苯并三唑-5-基]丙酸乙酯的制备
[0881]
采用通用方法8,用3-(3-{(1r)-1-[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]乙基}-4-甲基苯基)-3-{1-[6-(苄氧基)己基]-4-甲基-1h-苯并三唑-5-基}丙酸乙酯(1当量)作为起始试剂,得到标题化合物(灰色固体,78%收率)。
[0882]1h-nmr(400mhz,dmso-d6)δppm:9.66(m,1h),7.63/7.56(2dd,2h),7.47/7.44(2d,1h),7.15-7.08(m,2h),6.92/6.9(2d,1h),6.72(2dd,1h),6.58(2dd,1h),5.26(m,1h),4.87(m,1h),4.63(t,2h),4.31(m,2h),3.94(2d,2h),3.32(m,2h),3.22(d,2h),2.76(s,3h),2.28(s,3h),1.87(m,2h),1.43/1.41(2d,3h),1.38-1.1(m,4h),1.33(m,2h),1/0.99(2t,3h)。
[0883]
步骤4:3-[1-(6-溴己基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(1r)-1-(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)乙基]-4-甲基苯基}丙酸乙酯的制备
[0884]
采用通用方法9,用3-{3-[(1r)-1-(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)乙基]-4-甲基苯基}-3-[1-(6-羟基己基)-4-甲基-1h-苯并三唑-5-基]丙酸乙酯(1当量)作为起始试剂,得到标题化合物(84%收率)。
[0885]1h-nmr(400mhz,dmso-d6)δppm:9.61/9.6(2s,1h),7.62(dd,1h),7.58(d,1h),7.48/7.42(2d,1h),7.1(m,2h),6.91(d,1h),6.71(m,1h),6.6/6.53(2d,1h),5.26(m,1h),4.89(m,1h),4.62(t,2h),4.4-4.2(m,2h),3.92(2d,2h),3.46(m,2h),3.21(d,2h),2.77(s,3h),2.28(s,3h),1.88(m,2h),1.71(m,2h),1.4(2d,3h),1.38(m,2h),1.21(m,3h),1(2t,1h)。
[0886]
步骤5:[(2r)-2,4,33-三甲基-29,29-二氧代-23,28-二氧杂-29λ
6-硫杂-1,14,15,16-四氮杂六环[22.5.3.1
3,7
.1
9,13
.0
12,16
.0
27,31
]三十四碳-3(34),4,6,9(33),10,12,14,24,26,31-十烯-8-基]乙酸乙酯的制备
[0887]
采用通用方法11,用3-[1-(6-溴己基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(1r)-1-(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)乙基]-4-甲基苯基}丙酸乙酯(1当量)作为起始试剂,得到标题化合物(81%收率)。
[0888]1h-nmr(400mhz,dmso-d6)δppm:1.00(dt,j=11.62,7.09hz,12h)1.20-1.29(m,9h)1.29-1.76(m,25h)1.86-1.98(m,5h)2.30(d,j=9.05hz,10h)2.63-2.79(m,1h)2.97(dd,j=15.77,7.46hz,1h)3.09-3.27(m,2h)3.64-3.76(m,1h)3.77-3.99(m,6h)4.00-4.10(m,1h)4.18(d,j=17.48hz,1h)4.59-4.72(m,3h)4.86(t,j=8.01hz,1h)4.94(t,j=7.95hz,1h)5.24-5.42(m,3h)5.99(d,j=2.81hz,1h)6.40(d,j=2.81hz,1h)6.75-6.86(m,2h)6.93-7.04(m,3h)7.09-7.20(m,2h)7.29(dd,j=12.41,7.76hz,2h)7.47(d,j=7.58hz,1h)7.55(s,1h)7.61(d,j=8.80hz,1h)7.66(d,j=8.68hz,1h)7.77(d,j=8.93hz,1h)。
[0889]
步骤6:实施例19的制备
[0890]
采用通用方法12,用[(2r)-2,4,33-三甲基-29,29-二氧代-23,28-二氧杂-29λ
6-硫杂-1,14,15,16-四氮杂六环[22.5.3.1
3,7
.1
9,13
.0
12,16
.0
27,31
]三十四碳-3(34),4,6,9(33),10,12,14,24,26,31-十烯-8-基]乙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体,91%收率)。
[0891]
通过手性柱色谱分离得到非对映体纯产物。
[0892]
实施例19a(2r,8r)
[0893]c32h36
n4o6s的hrms计算值:604.2356;[m+h]
+
,实测值:605.2430(δ=0.3ppm)。
[0894]1h-nmr(400mhz,dmso-d6)δppm:12.2(sl),7.6(d,1h),7.48(dd,1h),7.3(d,1h),7.14(d,1h),7(d,1h),6.96(d,1h),6.78(dd,1h),6(d,1h),5.3(q,1h),4.92(t,1h),4.64(m,2h),4.04/3.83(2d,2h),3.7(m,2h),3.11/2.85(2dd,2h),2.82(s,3h),2.32(s,3h),2(m,2h),1.6(m,2h),1.4(m,2h),1.25(m,2h),1.25(d,3h)。
[0895]
13
c-nmr(100mhz,dmso-d6)δppm:131.6,128.4,128,126.5,119.5,115.7,111.4,107.8,68.4,55.3,47.8,45,41.6,39.9,29.5,27.5,25.7,25.5,18.7,15.1,13.6。
[0896]
实施例19b(2r,8s)
[0897]c32h36
n4o6s的hrms计算值:604.2356;[m+h]
+
,实测值:605.2431(δ=0.4ppm)。
[0898]1h-nmr(400mhz,dmso-d6)δppm:12.1(sl),7.75(d,1h),7.65(d,1h),7.52(d,1h),7.3(dd,1h),7.12(d,1h),7(d,1h),6.82(dd,1h),6.4(d,1h),5.34(q,1h),4.84(t,1h),4.67(m,2h),4.18/3.92(2d,2h),3.82(t,2h),3.15/3.05(2dd,2h),2.82(s,3h),2.3(s,3h),1.85(m,2h),1.7(m,2h),1.6-1.4(m,2h),1.5(d,3h),1.35(m,2h)。
[0899]
13
c-nmr(100mhz,dmso-d6)δppm:131.4,129.9,126.9,125.2,119.5,116.1,111.1,107.9,68.4,55.4,47.6,45.4,42.1,40.9,30,28.2,25.7,24.8,18.7,15.7,13.5。
[0900]
实施例20:[(2r,8s)-2,4,32-三甲基-28,28-二氧代-22,27-二氧杂-28λ
6-硫杂-1,14,15,16-四氮杂六环[21.5.3.1
3,7
.1
9,13
.0
12,16
.0
26,30
]三十三碳-3(33),4,6,9(32),10,12,14,23,25,30-十烯-8-基]乙酸和
[0901]
[(2r,8r)-2,4,32-三甲基-28,28-二氧代-22,27-二氧杂-28λ
6-硫杂-1,14,15,16-四氮杂六环[21.5.3.1
3,7
.1
9,13
.0
12,16
.0
26,30
]三十三碳-3(33),4,6,9(32),10,12,14,23,25,30-十烯-8-基]乙酸
[0902][0903]
步骤1:3-{3-[(1s)-1-羟基乙基]-4-甲基苯基}-3-(1-{5-[(4-甲氧基苯基)甲氧基]戊基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯的制备
[0904]
采用通用方法6,用(2e)-3-(1-{5-[(4-甲氧基苯基)甲氧基]戊基}-4-甲基-1h-苯并三唑-5-基)丙-2-烯酸乙酯(1当量)和(1s)-1-[2-甲基-5-(4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷-2-基)苯基]乙-1-醇(2当量)作为起始试剂,得到标题化合物(77%收率)。
[0905]1h-nmr(400mhz,dmso-d6)δppm:7.59(d,1h),7.45(d,1h),7.41(d,1h),7.18(d,2h),7.04(dd,1h),6.98(d,1h),6.87(d,2h),4.96(d,1h),4.82(m,1h),4.82(m,1h),4.62(dd,2h),4.31(s,2h),3.92(q,2h),3.73(s,3h),3.31(m,2h),3.15-3.09(m,2h),2.77(s,3h),2.19(s,3h),1.87(m,2h),1.51(m,2h),1.27(m,2h),1.23/1.21(d,3h),0.99(t,3h)。
[0906]
步骤2:3-(3-{(1r)-1-[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]乙基}-4-甲基苯基)-3-(1-{5-[(4-甲氧基苯基)甲氧基]戊基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯的制备
[0907]
采用通用方法7,用3-{3-[(1s)-1-羟基乙基]-4-甲基苯基}-3-(1-{5-[(4-甲氧基苯基)甲氧基]戊基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯(1当量)和6-(苄氧基)-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮(1.5当量)作为起始试剂,得到标题化合物(64%收率)。
[0908]1h-nmr(400mhz,dmso-d6)δppm:7.6(d,1h),7.51(2d,1h),7.5-6.8(m,15h),5.27(q,1h),5.09(m,2h),4.88(m,1h),4.59(m,2h),4.41(m,2h),4.29(s,2h),3.9(q,2h),3.71(s,3h),3.29(m,2h),3.2(m,2h),2.76(2s,3h),2.28(s,3h),1.82(m,2h),1.49(m,2h),1.4(m,3h),1.22(m,2h),0.96(m,3h)。
[0909]
步骤3:3-{3-[(1r)-1-(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)乙基]-4-甲基苯基}-3-[1-(5-羟基戊基)-4-甲基-1h-苯并三唑-5-基]丙酸乙酯的制备
[0910]
采用通用方法8,用3-(3-{(1r)-1-[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]乙基}-4-甲基苯基)-3-(1-{5-[(4-甲氧基苯基)甲氧基]戊基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯(1当量)作为起始试剂,得到标题化合物(灰色固体,98%收率)。
[0911]1h-nmr(400mhz,dmso-d6)δppm:9.63/9.62(2m,3h),7.62/7.56(2dd,2h),7.47/7.45(2sl,1h),7.1(m,2h),6.92/6.9(2d,1h),6.73(m,1h),6.58(2d,1h),5.25(m,1h),4.88(m,1h),4.63(t,2h),4.32(m,2h),3.94(m,2h),3.32(m,2h),3.22(m,2h),2.77(s,3h),2.28(s,3h),1.88(m,2h),1.46-1.37(m+d,5h),1.24(m,2h),1/0.99(2t,3h)。
[0912]
步骤4:3-[1-(5-溴戊基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(1r)-1-(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)乙基]-4-甲基苯基}丙酸乙酯的制备
[0913]
采用通用方法9,用3-{3-[(1r)-1-(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)乙基]-4-甲基苯基}-3-[1-(5-羟基戊基)-4-甲基-1h-苯并三唑-5-基]丙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体,78%收率)。
[0914]1h-nmr(400mhz,dmso-d6)δppm:9.6/9.59(2s,1h),7.62(2d,1h),7.58(d,1h),7.48/7.42(2d,1h),7.1(m,2h),6.9(d,1h),6.71(m,1h),6.59/6.55(2d,1h),5.26(m,1h),4.88(m,1h),4.65(t,2h),4.4-4.25(m,2h),3.93(q,2h),3.48(t,2h),3.21(m,2h),2.77(s,3h),2.28(s,3h),1.9(m,2h),1.8(m,2h),1.41(2d,3h),1.32(m,2h),1/0.99(2t,3h)。
[0915]
步骤5:[(2r)-2,4,32-三甲基-28,28-二氧代-22,27-二氧杂-28λ
6-硫杂-1,14,15,16-四氮杂六环[21.5.3.1
3,7
.1
9,13
.0
12,16
.0
26,30
]三十三碳-3(33),4,6,9(32),10,12,14,23,25,30-十烯-8-基]乙酸乙酯的制备
[0916]
采用通用方法11,用3-[1-(5-溴戊基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(1r)-1-(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)乙基]-4-甲基苯基}丙酸乙酯(1当量)作为起始试剂,得到标题化合物(78%收率)。
[0917]1h-nmr(400mhz,dmso-d6)δppm:0.92-1.07(m,7h)1.27-1.53(m,9h)1.55-1.81(m,5h)1.85-1.98(m,3h)1.99-2.09(m,2h)2.23-2.36(m,7h)2.75(s,4h)2.80(s,3h)2.94(dd,j=15.71,7.52hz,1h)3.10(dd,j=16.08,7.03hz,2h)3.21-3.29(m,2h)3.57-3.78(m,3h)3.80-3.98(m,8h)4.04-4.21(m,2h)4.56-4.76(m,4h)4.81-4.89(m,1h)4.95(t,j=7.82hz,1h)5.21-5.36(m,2h)5.99(s,2h)6.76-6.88(m,3h)6.91-6.99(m,2h)7.13(dd,j=10.51,8.19hz,2h)7.24-7.38(m,3h)7.48(d,j=7.95hz,1h)7.60-7.71(m,2h)7.84(d,j=8.68hz,1h)。
[0918]
步骤6:实施例20的制备
[0919]
采用通用方法12,用[(2r)-2,4,32-三甲基-28,28-二氧代-22,27-二氧杂-28λ
6-硫杂-1,14,15,16-四氮杂六环[21.5.3.1
3,7
.1
9,13
.0
12,16
.0
26,30
]三十三碳-3(33),4,6,9(32),10,12,14,23,25,30-十烯-8-基]乙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体,32%收率)。
[0920]
通过手性柱色谱分离得到非对映体纯产物。
[0921]
实施例20a(2r,8s)
[0922]c31h34
n4o6s的hrms计算值:590.2199;[m+h]
+
,实测值:591.2273(δ=0.2ppm)。
[0923]1h-nmr(400mhz,dmso-d6)δppm:12.4-11.9(m,1h),7.62(d,1h),7.49(dd,1h),7.31(d,1h),7.09(d,1h),6.94(d,1h),6.84(d,1h),6.81(dd,1h),5.99(d,1h),5.28(q,1h),4.91(m,1h),4.75-4.6(t,2h),4.08/3.7(m,2h),3.89/3.7(m,2h),3.16/2.8(2m,2h),2.8(s,3h),2.32(s,3h),2.1-1.85(m,2h),1.69(m,2h),1.55-1.23(m,2h),1.12(d,3h)。
[0924]
实施例20b(2r,8r)
[0925]c31h34
n4o6s的hrms计算值:590.2199;[m+h]
+
,实测值:591.2274(δ=0.4ppm)。
[0926]1h-nmr(400mhz,dmso-d6)δppm:12.4-11.9(m,1h),7.81(d,1h),7.68(d,1h),7.37(dd,1h),7.29(d,1h),7.13(d,1h),6.98(d,1h),6.83(dd,1h),5.97(d,1h),5.3(q,1h),4.81(m,1h),4.7(t,2h),4.15/3.6(m,2h),3.85(m,2h),3.18/2.99(2m,2h),2.71(s,3h),2.29(s,3h),2.1-1.85(m,2h),1.8-1.55(m,2h),1.5-1.2(m,5h)。
[0927]
实施例21:[(2r,8s)-2,4,19,33-四甲基-29,29-二氧代-23,28-二氧杂-29λ
6-硫杂-1,14,15,16,19-五氮杂六环[22.5.3.1
3,7
.1
9,13
.0
12,16
.0
27,31
]三十四碳-3(34),4,6,9(33),10,12,14,24,26,31-十烯-8-基]乙酸和
[0928]
[(2r,8r)-2,4,19,33-四甲基-29,29-二氧代-23,28-二氧杂-29λ
6-硫杂-1,14,15,16,19-五氮杂六环[22.5.3.1
3,7
.1
9,13
.0
12,16
.0
27,31
]三十四碳-3(34),4,6,9(33),10,12,14,24,26,31-十烯-8-基]乙酸
[0929][0930]
步骤a1:(2-{[3-(苄氧基)丙基](甲基)氨基}乙基)氨基甲酸叔丁酯的制备
[0931]
在室温下向[(3-溴丙氧基)甲基]苯(10g,43.6mmol,7.7ml)的mecn(3ml/mmol,131ml)溶液中加入[2-(甲基氨基)乙基]氨基甲酸叔丁酯(1eq.,7.61g,43.6mmol)和k2co3(2eq.,8.65g,87.3mmol)。将反应混合物加热至50℃并搅拌2小时。反应完成后将混合物用500ml etoac稀释,用500ml水萃取,然后用500ml盐水萃取。将有机层用无水硫酸钠干燥,过滤,浓缩至干得到无色油状粗产物,其不经进一步纯化直接用于下一步骤(14g,99%收率)。
[0932]1h-nmr(400mhz,dmso-d6)δppm:7.38-7.28(m,5h),6.58(t,1h),4.43(s,2h),3.45(t,2h),2.99(q,2h),2.38(t,2h),2.32(t,2h),2.13(s,3h),1.65(quint,2h),1.37(s,9h)。
[0933]
步骤a2:n
1-[3-(苄氧基)丙基]-n
1-甲基乙烷-1,2-二胺的制备
[0934]
在室温下向(2-{[3-(苄氧基)丙基](甲基)氨基}乙基)氨基甲酸叔丁酯(14g,43mmol)的二氧杂环己烷(5ml/mmol,220ml)溶液中加入hcl(4n的二氧杂环己烷溶液)(4eq.,43ml)并将反应混合物搅拌过夜。反应完成后将挥发物减压蒸发至干。将粗产物在200ml dcm和300ml饱和nahco3水溶液之间进行分配。分层,将水层减压蒸发至干。加入50ml mecn,然后将固体滤出并用2x20ml mecn洗涤。将母液浓缩至干得到黄色油状粗产物。粗产
物不经纯化即可使用(6.2g,62%收率)。
[0935]1h-nmr(400mhz,dmso-d6)δppm:7.38-7.23(m,5h),4.44(s,2h),3.45(t,2h),2.56(t,2h),2.36(t,2h),2.33(t,2h),2.1(s,3h),1.67(quint,2h)。
[0936]
步骤a3:n
1-[3-(苄氧基)丙基]-n
1-甲基-n
2-(3-甲基-2-硝基苯基)乙烷-1,2-二胺的制备
[0937]
采用通用方法2步骤1,用1-氟-3-甲基-2-硝基-苯(1当量)和n
1-[3-(苄氧基)丙基]-n
1-甲基乙烷-1,2-二胺粗产物(1.2当量)作为起始试剂,得到标题化合物(58%收率)。
[0938]1h-nmr(400mhz,dmso-d6)δppm:7.35-7.22(m,1h),7.35-7.22(m,5h),6.78(d,1h),6.61(t,1h),6.58(d,1h),4.41(s,2h),3.49(t,2h),3.2(q,2h),2.55(t,2h),2.41(t,2h),2.32(s,3h),2.19(s,3h),1.69(quint,2h)。
[0939]
步骤a4:n
1-(2-{[3-(苄氧基)丙基](甲基)氨基}乙基)-4-溴-3-甲基苯-1,2-二胺的制备
[0940]
采用通用方法2步骤2,用n
1-[3-(苄氧基)丙基]-n
1-甲基-n
2-(3-甲基-2-硝基苯基)乙烷-1,2-二胺(1当量)作为反应试剂,得到n
1-[3-(苄氧基)丙基]-n
2-(4-溴-3-甲基-2-硝基苯基)-n
1-甲基乙烷-1,2-二胺(71%收率)。将粗产物用通用方法2步骤3进行反应得到标题化合物(76%收率)。c
20h28
brn3o的lc-ms计算值:405;[m+h]
+
,实测值:406/408。
[0941]
步骤a5:3-(苄氧基)-n-[2-(5-溴-4-甲基-1h-苯并三唑-1-基)乙基]-n-甲基丙-1-胺的制备
[0942]
采用通用方法2步骤4,用n
1-(2-{[3-(苄氧基)丙基](甲基)氨基}乙基)-4-溴-3-甲基苯-1,2-二胺(1当量)作为起始试剂,得到标题化合物(85%收率)。
[0943]1h-nmr(400mhz,dmso-d6)δppm:8.19(s,1h),7.4(2d,2h),7.3(t,2h),7.25(t,1h),7.2(d,2h),4.3(t,2h),4.22(s,2h),3.18(t,2h),2.68(t,2h),2.55(s,3h),2.35(t,2h),2.2(s,3h),1.5(m,2h)。
[0944]
步骤a6:(2e)-3-[1-(2-{[3-(苄氧基)丙基](甲基)氨基}乙基)-4-甲基-1h-苯并三唑-5-基]丙-2-烯酸乙酯的制备
[0945]
采用通用方法2步骤5,用3-(苄氧基)-n-[2-(5-溴-4-甲基-1h-苯并三唑-1-基)乙基]-n-甲基丙-1-胺(1当量)作为起始试剂,得到标题化合物(93%收率)。
[0946]1h-nmr(400mhz,dmso-d6)δppm:8(d,1h),7.91(d,1h),7.7(d,1h),7.3(t,2h),7.22(t,1h),7.19(d,2h),6.61(d,1h),4.77(t,2h),4.2(q,2h),4.18(s,2h),3.08(t,2h),2.82(t,2h),2.79(s,3h),2.31(t,2h),2.19(s,3h),1.42(q,2h),1.28(t,3h)。
[0947]
步骤1:3-[1-(2-{[3-(苄氧基)丙基](甲基)氨基}乙基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(1s)-1-羟基乙基]-4-甲基苯基}丙酸乙酯的制备
[0948]
采用通用方法6,用(2e)-3-[1-(2-{[3-(苄氧基)丙基](甲基)氨基}乙基)-4-甲基-1h-苯并三唑-5-基]丙-2-烯酸乙酯(1当量)和(1s)-1-[2-甲基-5-(4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷-2-基)苯基]乙醇(1当量)作为起始试剂,得到标题化合物(33%收率)。
[0949]1h-nmr(400mhz,dmso-d6)δppm:7.59(d,1h),7.45(d,1h),7.41(m,1h),7.35(d,1h),7.31(dd,1h),7.22(m,2h),7.02(m,1h),6.97(m,2h),4.93(d,1h),4.82(m,1h),4.82(m,1h),4.7(t,2h),4.22(s,2h),3.91(q,2h),3.15(m,2h),3.15-3.05(m,2h),2.82(t,2h),
2.75(s,3h),2.35(t,2h),2.19(s,3h),2.19(s,3h),1.47(quint,2h),1.21(d,3h),0.99(t,3h)。
[0950]
步骤2:3-(3-{(1r)-1-[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]乙基}-4-甲基苯基)-3-[1-(2-{[3-(苄氧基)丙基](甲基)氨基}乙基)-4-甲基-1h-苯并三唑-5-基]丙酸乙酯的制备
[0951]
采用通用方法7,用3-[1-[2-[3-苄氧基丙基(甲基)氨基]乙基]-4-甲基-苯并三唑-5-基]-3-[3-[(1s)-1-羟基乙基]-4-甲基-苯基]丙酸乙酯(1当量)和6-(苄氧基)-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮(1.1当量)作为起始试剂,得到标题化合物(58%收率)。
[0952]c48h55
n5o7s的lc-ms计算值:845;[m+h]
+
,实测值:846。
[0953]
步骤3:3-{3-[(1r)-1-(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)乙基]-4-甲基苯基}-3-(1-{2-[(3-羟基丙基)(甲基)氨基]乙基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯的制备
[0954]
采用通用方法8,用3-(3-{(1r)-1-[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]乙基}-4-甲基苯基)-3-[1-(2-{[3-(苄氧基)丙基](甲基)氨基}乙基)-4-甲基-1h-苯并三唑-5-基]丙酸乙酯(1当量)作为起始试剂,得到标题化合物(黄色油,97%收率)。
[0955]c34h43
n5o7s的lc-ms计算值:665;[m+h]
+
,实测值:666。
[0956]
步骤4:3-(1-{2-[(3-溴丙基)(甲基)氨基]乙基}-4-甲基-1h-苯并三唑-5-基)-3-{3-[(1r)-1-(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)乙基]-4-甲基苯基}丙酸乙酯的制备
[0957]
采用通用方法9,用3-{3-[(1r)-1-(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)乙基]-4-甲基苯基}-3-(1-{2-[(3-羟基丙基)(甲基)氨基]乙基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体,20%收率)。
[0958]c34h42
brn5o6s的lc-ms计算值:727;[m+h]
+
,实测值:728/730。
[0959]
步骤5:[(2r)-2,4,19,33-四甲基-29,29-二氧代-23,28-二氧杂-29λ
6-硫杂-1,14,15,16,19-五氮杂六环[22.5.3.1
3,7
.1
9,13
.0
12,16
.0
27,31
]三十四碳-3(34),4,6,9(33),10,12,14,24,26,31-十烯-8-基]乙酸乙酯的制备
[0960]
采用通用方法11,用3-(1-{2-[(3-溴丙基)(甲基)氨基]乙基}-4-甲基-1h-苯并三唑-5-基)-3-{3-[(1r)-1-(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)乙基]-4-甲基苯基}丙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体,99%收率)。
[0961]1h-nmr(400mhz,dmso-d6)δppm:7.74/7.63(2d,1h),7.73/7.48(2d,1h),7.58(s,1h),7.27/7.04(2d,1h),7.25/7.12(d,1h),7.01/6.93(2d,1h),6.84/6.73(2d,1h),6.37/5.81(2sl,1h),5.35/5.29(2q,1h),4.93/4.87(2t,1h),4.8/4.71/4.61/4.58(4m,2h),4.24/4.02/3.98/3.87(4d,2h),3.91(q,2h),3.83(m,2h),3.34-3.13/3.02(4dd,2h),3.11/3.06/2.86/2.72(4m,2h),2.84(2s,3h),2.59-2.46/2.4(2m,2h),2.29(s,3h),2.19/2.13(2sl,3h),1.85(m,2h),1.52/1.27(2d,3h),1.01(2d,3h)。
[0962]
步骤6:实施例21的制备
[0963]
采用通用方法12,用[(2r)-2,4,19,33-四甲基-29,29-二氧代-23,28-二氧杂-29
λ
6-硫杂-1,14,15,16,19-五氮杂六环[22.5.3.1
3,7
.1
9,13
.0
12,16
.0
27,31
]三十四碳-3(34),4,6,9(33),10,12,14,24,26,31-十烯-8-基]乙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体,83%收率)。
[0964]
通过手性柱色谱分离得到非对映体纯产物。
[0965]
实施例21a(2r,8s)
[0966]c32h37
n5o6s的hrms计算值:619.2464;[m+h]
+
,实测值:620.2538(δ=0.1ppm)。
[0967]1h-nmr(400mhz,dmso-d6)δppm:12.05(m,1h),7.71(m,2h),7.55(d,1h),7.29(dd,1h),7.12(d,1h),7(d,1h),6.81(dd,1h),6.38(d,1h),5.35(q,1h),4.85(t,1h),4.78/4.58(2m,2h),4.21/3.95(2d,2h),3.82(m,2h),3.1/3(2dd,2h),3.05/2.7(2m,2h),2.81(s,3h),2.55(m,2h),2.3(s,3h),2.15(s,3h),1.82(m,2h),1.5(d,3h)。
[0968]
实施例21b(2r,8r)
[0969]c32h37
n5o6s的hrms计算值:619.2464;[m+h]
+
,实测值:620.2576(δ=6.2ppm)。
[0970]1h-nmr(400mhz,dmso-d6)δppm:12.3(m,1h),7.65/7.22(2d,2h),7.5(dd,1h),7.22(d,1h),7(d,1h),6.95(d,1h),6.72(dd,1h),5.82(d,1h),5.3(q,1h),4.91(t,1h),4.7/4.6(2m,2h),4.02/3.85(2d,2h),3.48/3.32(2m,2h),3.1(m,2h),2.88(m,2h),2.81(s,3h),2.4(t,2h),2.3(s,3h),2.2(s,3h),1.68(m,2h),1.25(d,3h)。
[0971]
实施例22:[23-氯-4,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸
[0972][0973]
步骤c1:5-(苄氧基)-4-氯-2-羟基苯甲醛的制备
[0974]
采用通用方法4步骤1,用4-(苄氧基)-3-氯苯酚(1当量)作为起始试剂,得到标题化合物(45%收率)。
[0975]1h-nmr(500mhz,dmso-d6)δppm:10.66(s,1h),10.22(s,1h),7.49-7.3(m,5h),7.38(s,1h),7.12(s,1h),5.16(s,2h)。
[0976]
步骤c2:6-(苄氧基)-7-氯-2h-1,2λ6,3-噁噻嗪-2,2-二酮的制备
[0977]
采用通用方法4步骤2,用5-(苄氧基)-4-氯-2-羟基苯甲醛(1当量)作为起始试剂,得到标题化合物(91%收率)。
[0978]1h-nmr(500mhz,dmso-d6)δppm:9.16(s,1h),7.93(s,1h),7.92(s,1h),7.53-7.34(m,5h),5.28(s,2h)。
[0979]
步骤c3:6-(苄氧基)-7-氯-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮的制备
[0980]
采用通用方法4步骤3,用6-(苄氧基)-7-氯-2h-1,2λ6,3-噁噻嗪-2,2-二酮(1当
量)作为起始试剂,得到标题化合物(定量)。
[0981]1h-nmr(500mhz,dmso-d6)δppm:8.5(br.,1h),7.47(dm,2h),7.41(tm,2h),7.35(tm,1h),7.34(s,1h),7.25(s,1h),5.17(s,2h),4.52(s,2h)。
[0982]
步骤1:3-(3-{[6-(苄氧基)-7-氯-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-甲基苯基)-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯的制备
[0983]
采用通用方法7,用3-[3-(羟基甲基)-4-甲基苯基]-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯(1当量)和6-(苄氧基)-7-氯-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮(1.4当量)作为起始试剂,得到标题化合物(黄色油,50%收率)。
[0984]1h-nmr(500mhz,dmso-d6)δppm:7.57(d,1h),7.51-7.33(m,5h),7.48(d,1h),7.45(s,1h),7.26(s,1h),7.26(d,1h),7.19(dd,1h),7.18(dm,2h),7.13(d,1h),6.86(dm,2h),5.16(s,2h),4.85(t,1h),4.62(t,2h),4.49/4.44(d+d,2h),4.29(s,2h),4.27/4.21(d+d,2h),3.91(q,2h),3.72(s,3h),3.35(t,2h),3.2/3.16(dd+dd,2h),2.77(s,3h),2.2(s,3h),1.89(m,2h),1.45(m,2h),0.96(t,3h)。
[0985]
步骤2:3-{3-[(7-氯-6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}-3-[1-(4-羟基丁基)-4-甲基-1h-苯并三唑-5-基]丙酸乙酯的制备
[0986]
采用通用方法8,用3-[3-[(6-苄氧基-7-氯-2,2-二氧代-4h-1,2λ6,3-噁噻嗪-3-基)甲基]-4-甲基-苯基]-3-[1-[4-[(4-甲氧基苯基)甲氧基]丁基]-4-甲基-苯并三唑-5-基]丙酸乙酯(1当量)作为起始试剂,得到标题化合物(黄色油,74%收率)。
[0987]1h-nmr(500mhz,dmso-d6)δppm:10.48(brs,1h),7.61(d,1h),7.51(d,1h),7.31(s,1h),7.27(d,1h),7.19(dd,1h),7.13(d,1h),6.85(s,1h),4.83(t,1h),4.64(t,2h),4.45/4.42(d+d,2h),4.43(brs,1h),4.25/4.2(d+d,2h),3.93(q,2h),3.37(t,2h),3.17(d,2h),2.76(s,3h),2.22(s,3h),1.9(m,2h),1.35(m,2h),0.99(t,3h)。
[0988]
步骤3:[23-氯-4,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯的制备
[0989]
采用通用方法10,用3-{3-[(7-氯-6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}-3-[1-(4-羟基丁基)-4-甲基-1h-苯并三唑-5-基]丙酸乙酯(1当量)作为反应试剂,得到3-[1-(4-氯丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(7-氯-6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}丙酸乙酯(黄色固体泡沫,定量),其不经进一步纯化即可用通用方法11进行下一步的反应。得到标题化合物(白色固体)(64%收率)。
[0990]1h-nmr(500mhz,dmso-d6)δppm:7.68(d,1h),7.47(dd,1h),7.47(d,1h),7.35(s,1h),7.27(d,1h),6.67(d,1h),6.1(s,1h),4.85/4.74(dm+dm,2h),4.77(t,1h),4.27/3.9(d+d,2h),4/3.76(d+d,2h),3.92(q,2h),3.7/3.44(m+m,2h),3.13/3.06(dd+dd,2h),2.64(s,3h),2.31(s,3h),2.22/1.99(m+m,2h),1.82/1.62(m+m,2h),1.01(t,3h)。
[0991]
步骤4:[23-氯-4,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,
24,29-十烯-8-基]乙酸的制备
[0992]
采用通用方法12,用[23-氯-4,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体,94%收率)。
[0993]
通过手性柱色谱分离得到对映体纯产物。
[0994]
实施例22a(e1)
[0995]c29h29
cln4o6s的hrms计算值:596.1497;[m+h]
+
,实测值:597.1564(δ=-0.9ppm)。实施例22b(e2)
[0996]c29h29
cln4o6s的hrms计算值:596.1497;[m+h]
+
,实测值:597.1549(δ=-3.4ppm)1h-nmr(500mhz,dmso-d6)δppm:12.23(brs,1h),7.68(d,1h),7.48(dd,1h),7.46(d,1h),7.35(s,1h),7.27(d,1h),6.65(d,1h),6.09(s,1h),4.85/4.74(m+m,2h),4.75(m,1h),4.26/3.91(d+d,2h),4.01/3.77(d+d,2h),3.69/3.42(m+m,2h),3.02/2.96(dd+dd,2h),2.64(s,3h),2.31(s,3h),2.22/2.01(m+m,2h),1.83/1.63(m+m,2h)。
[0997]
13
c-nmr(125mhz,dmso-d6)δppm:131.3,131.2,128.7,127.2,120.1,111.5,107.9,68.7,52.1,48.7,48.1,41.8,40.9,26.7,25.5,18.5,13.4。
[0998]
实施例23:[(2r,8r)-24-甲氧基-2,4,31-三甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸和
[0999]
[(2r,8s)-24-甲氧基-2,4,31-三甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸
[1000][1001]
步骤1:3-(3-{(1r)-1-[6-(苄氧基)-8-甲氧基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]乙基}-4-甲基苯基)-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯的制备
[1002]
采用通用方法7,用3-{3-[(1r)-1-羟基乙基]-4-甲基苯基}-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯(1当量)和6-(苄氧基)-8-甲氧基-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮(1.05当量)作为起始试剂,得到标题化合物(79%收率)。
[1003]1h-nmr(400mhz,dmso-d6)δppm:0.88-1.05(m,14h)1.13-1.30(m,10h)1.36-1.49(m,20h)1.82-1.94(m,9h)2.27(s,11h)2.74-2.81(m,11h)3.12-3.26(m,8h)3.34(q,j=
6.15hz,8h)3.72(s,13h)3.81(s,11h)3.92(q,j=7.09hz,8h)4.23-4.36(m,11h)4.39(s,4h)4.55-4.65(m,8h)4.87(t,j=7.76hz,4h)5.01-5.14(m,7h)5.21-5.30(m,3h)6.35(d,j=2.57hz,1h)6.42(d,j=2.57hz,1h)6.72-6.78(m,1h)6.86(d,j=8.56hz,2h)7.07-7.14(m,2h)7.17(d,j=8.56hz,2h)7.28-7.38(m,1h)7.38-7.44(m,3h)7.44-7.49(m,2h)7.49-7.55(m,1h)7.56-7.62(m,1h)。
[1004]
步骤2:3-[1-(4-羟基丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(1r)-1-(6-羟基-8-甲氧基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)乙基]-4-甲基苯基}丙酸乙酯的制备
[1005]
采用通用方法8,用3-(3-{(1r)-1-[6-(苄氧基)-8-甲氧基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]乙基}-4-甲基苯基)-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯(1当量)作为起始试剂,得到标题化合物(黄色固体,98%收率)。
[1006]1h-nmr(400mhz,dmso-d6)δppm:0.92-1.06(m,6h)1.10-1.48(m,13h)1.90(quin,j=7.18hz,4h)2.27(s,5h)2.70-2.79(m,5h)3.22(d,j=7.70hz,3h)3.34-3.42(m,4h)3.77(s,5h)3.88-3.99(m,3h)4.27(d,j=5.26hz,1h)4.33(d,j=2.32hz,1h)4.37-4.46(m,1h)4.65(t,j=6.97hz,2h)4.80-4.94(m,1h)5.24(q,j=6.77hz,1h)6.10(d,j=2.45hz,1h)6.15(d,j=2.57hz,1h)6.40-6.49(m,1h)6.76-6.84(m,1h)7.04-7.16(m,3h)7.45(d,j=10.15hz,1h)7.53-7.59(m,1h)7.59-7.66(m,1h)9.60-9.65(m,1h)。
[1007]
步骤3:3-[1-(4-溴丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(1r)-1-(6-羟基-8-甲氧基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)乙基]-4-甲基苯基}丙酸乙酯的制备
[1008]
采用通用方法9,用3-[1-(4-羟基丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(1r)-1-(6-羟基-8-甲氧基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)乙基]-4-甲基苯基}丙酸乙酯(1当量)作为起始试剂,得到标题化合物(65%收率)。
[1009]1h-nmr(400mhz,dmso-d6)δppm:1.00(q,j=6.89hz,5h)1.35-1.46(m,3h)1.77(quin,j=7.03hz,3h)1.94-2.05(m,5h)2.27(s,4h)2.76(s,4h)3.22(d,j=7.70hz,3h)3.53(t,j=6.66hz,3h)3.76(s,4h)3.94(qd,j=7.09,2.32hz,3h)4.23-4.37(m,2h)4.69(t,j=6.79hz,3h)4.81-4.94(m,2h)5.24(d,j=6.72hz,1h)6.03-6.18(m,2h)6.34-6.51(m,2h)6.96-7.22(m,3h)7.44(d,j=11.37hz,1h)7.52-7.68(m,3h)9.63(d,j=5.14hz,1h)。
[1010]
步骤4:[(2r)-24-甲氧基-2,4,31-三甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯的制备
[1011]
采用通用方法11,用3-[1-(4-溴丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(1r)-1-(6-羟基-8-甲氧基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)乙基]-4-甲基苯基}丙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体,69%收率)。
[1012]1h-nmr(400mhz,dmso-d6)δppm:0.92-1.06(m,11h)1.11(d,j=6.85hz,4h)1.27(d,j=6.85hz,8h)1.54-1.92(m,8h)2.00-2.22(m,7h)2.23-2.36(m,13h)2.66(s,7h)2.81(s,4h)2.92-3.15(m,5h)3.33-3.50(m,7h)3.59-3.79(m,14h)3.83-4.00(m,10h)4.64-4.99
(m,11h)5.15-5.31(m,5h)5.37(br.s.,1h)6.46(dd,j=19.93,2.45hz,3h)6.73(s,1h)7.08-7.25(m,4h)7.30(d,j=8.07hz,1h)7.44(d,j=7.70hz,3h)7.68(d,j=8.68hz,1h)7.75(d,j=8.80hz,1h)7.89(d,j=8.80hz,1h)。
[1013]
步骤5:实施例23的制备
[1014]
采用通用方法12,用[(2r)-24-甲氧基-2,4,31-三甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯(1当量)作为起始试剂,得到标题化合物(72%收率)。
[1015]
通过手性柱色谱分离得到对映体纯产物。
[1016]
实施例23a(2r,8r)
[1017]c31h34
n4o7s的hrms计算值:606.2148;[m+h]
+
,实测值:607.2223(δ=0.3ppm)。
[1018]1h-nmr(400mhz,dmso-d6)δppm:12(sl,1h),7.69(d,1h),7.44(dd,1h),7.39(d,1h),7.09(d,1h),6.72(d,1h),6.42(d,1h),5.38(dl,1h),5.21(q,1h),4.89(t,1h),4.76(m,2h),4.02/3.4(2*d,2h),3.7(m,2h),3.7(s,3h),3.28/2.87(dd,2h),2.81(s,3h),2.31(s,3h),2.2/2(m,2h),1.61/1.28(m,2h),1.11(d,3h)。
[1019]
实施例23b(2r,8s)
[1020]c31h34
n4o7s的hrms计算值:606.2148;[m+h]
+
,实测值:607.2224(δ=0.5ppm)。
[1021]1h-nmr(400mhz,dmso-d6)δppm:12.2(sl,1h),7.88/7.74(d,2h),7.44(dd,1h),7.2(d,1h),7.11(d,1h),6.49(d,1h),5.23(q,1h),5.19(d,1h),4.8-4.67(m,1h),4.8-4.67(m,2h),3.99/3.36(d,2h),3.73(s,3h),3.63/3.41(m,2h),3.28/2.96(dd,2h),2.64(s,3h),2.29(s,3h),2.18/2.09(m,2h),1.87/1.74(m,2h),1.27(d,3h)。
[1022]
实施例24:[(2r,8s)-18-(2-甲氧基乙基)-2,4,31-三甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸和
[1023]
[(2r,8r)-18-(2-甲氧基乙基)-2,4,31-三甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸
[1024][1025]
步骤a1:2-[2-(苄氧基)乙基]-4-甲氧基丁腈的制备
[1026]
于-78℃下,向4-甲氧基丁腈(6.88g,69.4mmol)的无水thf(1ml/mmol,70ml)溶液中滴加双(三甲基硅烷基)氨基锂(1.2eq.,1m的thf溶液,83.3ml,83.3mmol),同时继续搅拌。于-78℃滴加溶于35ml thf的[(2-碘乙氧基)甲基]苯(1.2eq.,21.8g,83.3mmol)。将反应混合物升温至室温并搅拌过夜。反应完成后将混合物用水淬灭。加入200ml etoac并分层。将有机层用150ml盐水洗涤并用无水硫酸钠干燥。过滤并浓缩至干得到粗产物,将其通过正相硅胶色谱纯化,用庚烷-etoac(100:0至70:30)作为洗脱剂得到标题化合物(8.1g,50%收率)。1h-nmr(400mhz,dmso-d6)δppm:7.4-7.25(m,5h),4.5(s,2h),3.55(m,2h),3.45(m,2h),3.25(s,3h),2.95(m,1h),1.9-1.7(m,4h)。
[1027]
步骤a2:2-[2-(苄氧基)乙基]-4-甲氧基丁-1-胺的制备
[1028]
将氢化铝锂(1eq.,1.3g,35mmol)置于圆底烧瓶中。加入无水thf(70ml)后将混合物冷却至10℃。于10℃滴加2-[2-(苄氧基)乙基]-4-甲氧基丁腈(8.1g,35mmol)的无水thf(70ml)溶液,同时继续搅拌15分钟。将反应混合物升温至室温并在该温度下继续搅拌3小时。反应完成后将混合物冷却至10℃并用na2so4水溶液淬灭。将混合物在室温下搅拌过夜并过滤。将滤饼用thf洗涤。将母液浓缩至干得到标题化合物(8.3g,96%收率)。
[1029]1h-nmr(400mhz,dmso-d6)δppm:7.39-7.22(m,5h),4.44(s,2h),3.45(t,2h),3.32(t,2h),3.19(s,3h),2.46(d,2h),1.68-1.37(m,5h),1.44-1.14(m,2h)。
[1030]
步骤a3:n-{2-[2-(苄氧基)乙基]-4-甲氧基丁基}-3-甲基-2-硝基苯胺的制备
[1031]
采用通用方法2步骤1,用1-氟-3-甲基-2-硝基-苯(1当量)和2-[2-(苄氧基)乙基]-4-甲氧基丁-1-胺(1.2eq)作为起始试剂,得到标题化合物(50%收率)。
[1032]1h-nmr(400mhz,dmso-d6)δppm:7.3(m,5h),7.2(t,1h),6.75(d,1h),6.5(d+t,2h),4.45(s,2h),3.5(m,2h),3.4(m,2h),3.2(s,3h),3.15(m,2h),2.3(s,3h),1.9(sept.,1h),1.55(m,4h)。
[1033]
步骤a4:n-{2-[2-(苄氧基)乙基]-4-甲氧基丁基}-4-溴-3-甲基-2-硝基苯胺的制
5-基)丙酸乙酯的制备
[1049]
采用通用方法7,用3-(1-{2-[2-(苄氧基)乙基]-4-甲氧基丁基}-4-甲基-1h-苯并三唑-5-基)-3-{3-[(1s)-1-羟基乙基]-4-甲基苯基}丙酸乙酯(1当量)和6-(苄氧基)-8-甲氧基-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮(1.1当量)作为起始试剂,得到标题化合物(59%收率)。
[1050]1h-nmr(400mhz,dmso-d6)δppm:7.6-7.2(m,15h),7.12-6.95(m,2h),6.9/6.85(2d,1h),5.28(m,1h),5.1(2s,2h),4.9(m,1h),4.6(d,2h),4.45-4.3(m,4h),3.9(q,2h),3.45(m,2h),3.3/3.2(2m,5h),3.1(m,2h),2.8/2.3(s,6h),2.28(m,1h),1.5(m,4h),1.4(d,3h),1.22(t,3h)。
[1051]
步骤3:3-[3-[(1r)-1-(6-羟基-2,2-二氧代-4h-1,2λ6,3-噁噻嗪-3-基)乙基]-4-甲基-苯基]-3-[1-[2-(2-羟基乙基)-4-甲氧基-丁基]-4-甲基-苯并三唑-5-基]丙酸乙酯的制备
[1052]
采用通用方法8,用3-(3-{(1r)-1-[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]乙基}-4-甲基苯基)-3-(1-{2-[2-(苄氧基)乙基]-4-甲氧基丁基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯(1当量)作为起始试剂,得到标题化合物(81%收率)。
[1053]1h-nmr(400mhz,dmso-d6)δppm:9.6/4.35(s+t,2h),7.6(m,2h),7.5(d,1h),7.12(m,2h),6.91(d,1h),6.75(dd,1h),6.6/6.55(2d,1h),5.25(q,1h),4.9(m,1h),4.6(d,2h),4.35(m,2h),3.92(q,2h),3.45(m,4h),3.21(d,2h),3.12(s,3h),2.8(s,3h),2.3(s,3h),2.25(m,1h),1.5-1.3(m,4h),1.45(d,3h),1.2(t,3h)。
[1054]
步骤4:3-{1-[2-(2-溴乙基)-4-甲氧基丁基]-4-甲基-1h-苯并三唑-5-基}-3-{3-[(1r)-1-(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)乙基]-4-甲基苯基}丙酸乙酯的制备
[1055]
采用通用方法9,用3-[3-[(1r)-1-(6-羟基-2,2-二氧代-4h-1,2λ6,3-噁噻嗪-3-基)乙基]-4-甲基-苯基]-3-[1-[2-(2-羟基乙基)-4-甲氧基-丁基]-4-甲基-苯并三唑-5-基]丙酸乙酯(1当量)作为起始试剂,得到标题化合物(39%收率)。
[1056]1h-nmr(400mhz,dmso-d6)δppm:9.6(s,1h),7.6(d,1h),7.55(d,1h),7.45(2d,1h),7.11(m,2h),6.9(d,1h),6.71(dd,1h),6.59(2d,1h),5.28(q,1h),4.9(m,1h),4.61(d,2h),4.4-4.3(m,2h),3.92(q,2h),3.58(m,2h),3.3(m,2h),3.21(d,2h),3.15(s,3h),2.78(s,3h),2.3(m,1h),2.28(s,3h),1.9-1.7(2m,2h),1.5(m,2h),1.4(d,3h),1(2t,3h)。
[1057]
步骤5:实施例24的制备
[1058]
采用通用方法11,用3-{1-[2-(2-溴乙基)-4-甲氧基丁基]-4-甲基-1h-苯并三唑-5-基}-3-{3-[(1r)-1-(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)乙基]-4-甲基苯基}丙酸乙酯(1当量)作为反应试剂,得到[(2r)-18-(2-甲氧基乙基)-2,4,31-三甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯(白色固体,57%收率)。将粗产物用通用方法12进行反应得到标题化合物(定量)。
[1059]
通过手性柱色谱分离得到非对映体纯产物。
[1060]
实施例24a(2r,8sdia1)
[1061]c33h38
n4o7s的hrms计算值:634.246;[m+h]
+
,实测值:635.2534。
[1062]1h-nmr(400mhz,dmso-d6)δppm:12.2(ml,1h),7.79(d,1h),7.61(d,1h),7.45(dd,1h),7.22(d,1h),7.02(d,1h),6.9(d,1h),6.7(dd,1h),5.4(d,1h),5.22(q,1h),4.79(dd,1h),4.75/4.6(2dd,2h),4.12/3.4(2d,2h),3.58(m,3h),3.3(s,3h),3.2-3(m,2h),2.9(dd,1h),2.6(s,3h),2.3(s,3h),1.9-1.7(m,5h),1.2(d,3h)。
[1063]
实施例24b(2r,8sdia2)
[1064]c33h38
n4o7s的hrms计算值:634.246;[m+h]
+
,实测值:635.2534。
[1065]1h-nmr(400mhz,dmso-d6)δppm:12.2(ml,1h),7.89(d,1h),7.78(d,1h),7.45(dd,1h),7.21(d,1h),7.04(d,1h),6.95(d,1h),6.75(dd,1h),5.4(d,1h),5.25(q,1h),4.79(dd,1h),4.61/4.55(2dd,2h),4.05/3.35(2d,2h),3.55(t,2h),3.45(m,1h),3.3(m,4h),3.1/2.9(2m,2h),2.6(s,3h),2.3(s,3h),1.9-1.7(m,5h),1.2(d,3h)。
[1066]
实施例24c(2r,8rdia1)
[1067]c33h38
n4o7s的hrms计算值:634.246;[m+h]
+
,实测值:635.2536(δ=0.3ppm)。
[1068]1h-nmr(400mhz,dmso-d6)δppm:7.6(d,1h),7.49(dd,1h),7.28(d,1h),7.2(d,1h),6.9(d,1h),6.89(d,1h),6.7(dd,1h),5.6(d,1h),5.26(q,1h),4.9(dd,1h),4.7/4.6(2dd,2h),4.1/3.55(2d,2h),3.6-3.35(m,4h),3.3(s,3h),3.2/2.88(2m,2h),2.8(s,3h),2.3(s,3h),1.8(m,3h),1.68/1.5(2m,2h),1.2(d,3h)。
[1069]
实施例24d(2r,8rdia2)
[1070]c33h38
n4o7s的hrms计算值:634.246;[m+h]
+
,实测值:635.2535(δ=0.2ppm)。
[1071]1h-nmr(400mhz,dmso-d6)δppm:7.7(d,1h),7.49(dd,1h),7.31(d,1h),7.09(d,1h),6.91(d,1h),6.82(d,1h),6.7(dd,1h),5.65(d,1h),5.26(q,1h),4.95(t,1h),4.6(m,2h),4.05/3.6(2d,2h),3.6-3.35(m,4h),3.23(s,3h),3.15/2.82(2m,2h),2.8(s,3h),2.32(s,3h),1.88/1.78(2m,2h),1.7(m,3h),1.1(d,3h)。
[1072]
实施例25:[23-甲氧基-4,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸
[1073][1074]
步骤c1:5-(苄氧基)-2-羟基-4-甲氧基苯甲醛的制备
[1075]
采用通用方法4步骤1,用4-(苄氧基)-3-甲氧基苯酚(1当量)作为起始试剂,得到标题化合物(55%收率)。
[1076]1h-nmr(500mhz,dmso-d6)δppm:10.71(s,1h),10.02(s,1h),7.46-7.29(m,5h),7.24(s,1h),6.58(s,1h),5.03(s,2h),3.84(s,3h)。
[1077]
步骤c2:6-(苄氧基)-7-甲氧基-2h-1,2λ6,3-噁噻嗪-2,2-二酮的制备
[1078]
采用通用方法4步骤2,用5-(苄氧基)-2-羟基-4-甲氧基-苯甲醛(1当量)作为起始
试剂,得到标题化合物(67%收率)。
[1079]1h-nmr(500mhz,dmso-d6)δppm:8.96(s,1h),7.64(s,1h),7.5-7.33(m,5h),7.26(s,1h),5.14(s,2h),3.95(s,3h)。
[1080]
步骤c3:6-(苄氧基)-7-甲氧基-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮的制备
[1081]
采用通用方法4步骤3,用6-(苄氧基)-7-甲氧基-2h-1,2λ6,3-噁噻嗪-2,2-二酮(1当量)作为起始试剂,得到标题化合物(白色固体,98%收率)。
[1082]1h-nmr(500mhz,dmso-d6)δppm:8.4(t,1h),7.52-7.29(m,5h),6.98(s,1h),6.76(s,1h),5.04(s,2h),4.42(d,2h),3.76(s,3h)。
[1083]
步骤1:3-(3-{[6-(苄氧基)-7-甲氧基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-甲基苯基)-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯的制备
[1084]
采用通用方法7,用3-[3-(羟基甲基)-4-甲基苯基]-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯(1当量)和6-(苄氧基)-7-甲氧基-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮(1.2当量)作为起始试剂,得到标题化合物(白色固体,74%收率)。
[1085]1h-nmr(500mhz,dmso-d6)δppm:7.57(d,1h),7.48(d,1h),7.48-7.31(m,5h),7.22(d,1h),7.19(dd,1h),7.18(m,2h),7.13(d,1h),6.99(s,1h),6.88(s,1h),6.86(m,2h),5.03(s,2h),4.85(t,1h),4.62(t,2h),4.38/4.34(d+d,2h),4.29(s,2h),4.22/4.18(d+d,2h),3.91(q,2h),3.8(s,3h),3.72(s,3h),3.35(t,2h),3.19/3.16(dd+dd,2h),2.76(s,3h),2.2(s,3h),1.89(m,2h),1.44(m,2h),0.97(t,3h)。
[1086]
步骤2:3-[1-(4-羟基丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(6-羟基-7-甲氧基-2,2-二氧代
[1087]-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}丙酸乙酯的制备
[1088]
采用通用方法8,用3-(3-{[6-(苄氧基)-7-甲氧基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-甲基苯基)-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯(1当量)作为起始试剂,得到标题化合物(定量)。
[1089]1h-nmr(500mhz,dmso-d6)δppm:9.26(s,1h),7.61(d,1h),7.5(d,1h),7.2(s,1h),7.19(dd,1h),7.13(d,1h),6.8(s,1h),6.6(s,1h),4.83(t,1h),4.65(t,2h),4.63(t,1h),4.3(s,2h),4.19/4.16(d+d,2h),3.93(q,2h),3.79(s,3h),3.37(m,2h),3.18/3.14(dd+dd,2h),2.75(s,3h),2.21(s,3h),1.9(m,2h),1.35(m,2h),1(t,3h)。
[1090]
步骤3:3-[1-(4-氯丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(6-羟基-7-甲氧基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}丙酸乙酯盐酸盐的制备
[1091]
采用通用方法10,用3-[1-(4-羟基丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(6-羟基-7-甲氧基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}丙酸乙酯(1当量)作为起始试剂,得到标题化合物(定量)。
[1092]1h-nmr(500mhz,dmso-d6)δppm:9.26(s,1h),7.63(d,1h),7.52(d,1h),7.2(m,1h),7.2(m,1h),7.13(d,1h),6.8(s,1h),6.59(s,1h),4.83(t,1h),4.69(t,2h),4.3(s,2h),4.19/4.15(d+d,2h),3.93(q,2h),3.79(s,3h),3.64(t,2h),3.19/3.15(dd+dd,2h),
2.75(s,3h),2.21(s,3h),1.99(m,2h),1.68(m,2h),0.99(t,3h)。
[1093]
步骤4:[23-甲氧基-4,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯的制备
[1094]
采用通用方法11,用3-[1-(4-氯丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(6-羟基-7-甲氧基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}丙酸乙酯盐酸盐(1当量)作为起始试剂,得到标题化合物(白色固体,34%收率)。
[1095]1h-nmr(500mhz,dmso-d6)δppm:7.69(d,1h),7.47(dd,1h),7.46(d,1h),7.28(d,1h),6.75(s,1h),6.56(d,1h),5.77(s,1h),4.82/4.75(m+m,2h),4.78(dd,1h),4.18/3.87(d+d,2h),3.93(q,2h),3.93/3.69(d+d,2h),3.72(s,3h),3.56/3.3(m+m,2h),3.14/3.06(dd+dd,2h),2.61(s,3h),2.32(s,3h),2.2/2.02(m+m,2h),1.78/1.61(m+m,2h),1.01(t,3h)。
[1096]
步骤5:实施例25的制备
[1097]
采用通用方法12,用[23-甲氧基-4,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体,86%收率)。
[1098]
通过手性柱色谱分离得到对映体纯产物。
[1099]
实施例25a(e1,光学纯度:99.9%)
[1100]c30h32
n4o7s的hrms计算值:592.1992;[m+h]
+
,实测值:593.2048(δ=-2.8ppm)。
[1101]
实施例25b(e2,光学纯度~99.4%)
[1102]c30h32
n4o7s的hrms计算值:592.1992;[m+h]
+
,实测值:593.2047(δ=-2.9ppm)。
[1103]1h-nmr(500mhz,dmso-d6)δppm:12.54(br.,1h),7.68(d,1h),7.48(brd.,1h),7.45(d,1h),7.27(d,1h),6.74(s,1h),6.53(brs.,1h),5.75(s,1h),4.81/4.74(m+m,2h),4.75(m,1h),4.16/3.87(d+d,2h),3.93/3.69(d+d,2h),3.72(s,3h),3.55/3.28(m+m,2h),2.99/2.92(dd+dd,2h),2.6(s,3h),2.32(s,3h),2.2/2.03(m+m,2h),1.78/1.61(m+m,2h)。
[1104]
13
c-nmr(125mhz,dmso-d6)δppm:173.3,131.3,131.3,128.8,127.3,110.8,107.9,102.9,68.3,56.3,51.9,48.4,48.2,42,41.3,27,25.6,18.5,13.4。
[1105]
实施例26:[(2r,8s)-2,4,33-三甲基-29,29-二氧代-20,23,28-三氧杂-29λ
6-硫杂-1,14,15,16-四氮杂六环[22.5.3.1
3,7
.1
9,13
.0
12,16
.0
27,31
]三十四碳-3(34),4,6,9(33),10,12,14,24,26,31-十烯-8-基]乙酸和
[1106]
[(2r,8r)-2,4,33-三甲基-29,29-二氧代-20,23,28-三氧杂-29λ
6-硫杂-1,14,15,16-四氮杂六环[22.5.3.1
3,7
.1
9,13
.0
12,16
.0
27,31
]三十四碳-3(34),4,6,9(33),10,12,14,24,26,31-十烯-8-基]乙酸
[(1s)-1-羟基乙基]-4-甲基苯基}丙酸乙酯的制备
[1124]
采用通用方法6,用(2e)-3-(1-{3-[2-(苄氧基)乙氧基]丙基}-4-甲基-1h-苯并三唑-5-基)丙-2-烯酸乙酯(1当量)和(1s)-1-[2-甲基-5-(4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷-2-基)苯基]乙-1-醇(1当量)作为起始试剂,得到标题化合物(59%收率)。
[1125]1h-nmr(400mhz,dmso-d6)δppm:7.56(d,1h),7.41(d,1h),7.39(m,1h),7.35-7.22(m,5h),7.02(dd,1h),6.99(d,1h),4.97(m,1h),4.82(m,1h),4.82(m,1h),4.68(t,2h),4.46(s,2h),3.92(q,2h),3.52/3.49(m,4h),3.35(t,2h),3.14-3.07(m,2h),2.75(s,3h),2.19(s,3h),2.1(quint,2h),1.21(d,3h),1(t,3h)。
[1126]
步骤2:3-{3-[(1r)-1-(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)乙基]-4-甲基苯基}-3-{1-[3-(2-羟基乙氧基)丙基]-4-甲基-1h-苯并三唑-5-基}丙酸乙酯的制备
[1127]
采用通用方法7,用3-(1-{3-[2-(苄氧基)乙氧基]丙基}-4-甲基-1h-苯并三唑-5-基)-3-{3-[(1s)-1-羟基乙基]-4-甲基苯基}丙酸乙酯(1当量)和6-(苄氧基)-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮(1.1当量)作为起始试剂,得到3-(3-{(1r)-1-[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]乙基}-4-甲基苯基)-3-(1-{3-[2-(苄氧基)乙氧基]丙基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯(橙色油,84%收率)。将粗产物用通用方法8进行反应得到标题化合物(白色固体,87%收率)。
[1128]1h-nmr(400mhz,dmso-d6)δppm:9.62(m,1h),7.64-7.54(m,2h),7.47/7.47(2sl,1h),7.14-7.08(m,2h),6.92/6.9(2d,1h),6.76-6.7(m,1h),6.57(2d,1h),5.25(m,1h),4.88(q,1h),4.7(t,2h),4.57(m,1h),4.36/4.31(s+dd,2h),3.95(2d,2h),3.47(m,2h),3.39-3.28(m,4h),3.22(m,2h),2.77(s,3h),2.28(s,3h),2.1(m,2h),1.43/1.41(2d,3h),1.01/1(2t,3h)。
[1129]
步骤3:3-{1-[3-(2-溴乙氧基)丙基]-4-甲基-1h-苯并三唑-5-基}-3-{3-[(1r)-1-(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)乙基]-4-甲基苯基}丙酸乙酯的制备
[1130]
采用通用方法9,用3-{3-[(1r)-1-(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)乙基]-4-甲基苯基}-3-{1-[3-(2-羟基乙氧基)丙基]-4-甲基-1h-苯并三唑-5-基}丙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体,60%收率)。
[1131]1h-nmr(400mhz,dmso-d6)δppm:9.55(s,1h),7.7-7.5(2d,2h),7.49(2d,1h),7.11(m,2h),6.91(d,1h),6.71(2dd,1h),6.48(2d,1h),5.28(m,1h),4.9(m,1h),4.7(t,2h),4.4-4.3(m,2h),3.95(q,2h),3.68(t,2h),3.55(t,2h),3.41(t,2h),3.21(d,2h),2.79(s,3h),2.3(s,3h),2.12(m,2h),1.45(2d,3h),1.02(2t,3h)。
[1132]
步骤4:[(2r)-2,4,33-三甲基-29,29-二氧代-20,23,28-三氧杂-29λ
6-硫杂-1,14,15,16-四氮杂六环[22.5.3.1
3,7
.1
9,13
.0
12,16
.0
27,31
]三十四碳-3(34),4,6,9(33),10,12,14,24,26,31-十烯-8-基]乙酸乙酯的制备
[1133]
采用通用方法11,用3-{1-[3-(2-溴乙氧基)丙基]-4-甲基-1h-苯并三唑-5-基}-3-{3-[(1r)-1-(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)乙基]-4-甲基苯基}丙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体,定量)。
[1134]1h-nmr(400mhz,dmso-d6)δppm:1.01(td,j=7.09,4.16hz,6h)1.18(d,j=
6.85hz,2h)1.55(d,j=6.85hz,3h)2.18(d,j=5.38hz,3h)2.26-2.36(m,6h)2.79(s,2h)2.85(s,3h)2.95(dd,j=15.77,8.31hz,1h)3.14-3.26(m,3h)3.39-3.54(m,3h)3.55-3.61(m,1h)3.61-3.73(m,2h)3.74-3.85(m,2h)3.87-3.98(m,5h)4.01(d,j=6.60hz,1h)4.08(t,j=4.71hz,2h)4.19(d,j=17.73hz,1h)4.35(d,j=17.61hz,1h)4.53-4.82(m,4h)4.83-4.96(m,2h)5.23-5.31(m,1h)5.33-5.42(m,1h)6.25(d,j=2.81hz,1h)6.50(d,j=2.81hz,1h)6.78-6.94(m,2h)6.96-7.04(m,2h)7.10(dd,j=19.38,8.25hz,2h)7.17-7.25(m,2h)7.42(d,j=6.48hz,1h)7.54-7.65(m,4h)
[1135]
步骤5:实施例26的制备
[1136]
采用通用方法12,用[(2r)-2,4,33-三甲基-29,29-二氧代-20,23,28-三氧杂-29λ
6-硫杂-1,14,15,16-四氮杂六环[22.5.3.1
3,7
.1
9,13
.0
12,16
.0
27,31
]三十四碳-3(34),4,6,9(33),10,12,14,24,26,31-十烯-8-基]乙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体,85%收率)。
[1137]
通过手性柱色谱分离得到非对映体纯产物。
[1138]
实施例26a(2r,8s)
[1139]c31h34
n4o7s的hrms计算值:606.2148;[m+h]
+
,实测值:607.2223(δ=0.3ppm)。
[1140]1h-nmr(400mhz,dmso-d6)δppm:12.1(sl,1h),7.62/7.59(d,2h),7.59(d,1h),7.19(dd,1h),7.08(d,1h),7.01(d,1h),6.91(dd,1h),6.49(d,1h),5.37(q,1h),4.87(t,1h),4.77/4.67(m,2h),4.33/3.95(d,2h),4.08(t,2h),3.79/3.66(m,2h),3.49(m,2h),3.11(m,2h),2.83(s,3h),2.29(s,3h),2.19(m,2h),1.54(d,3h)。
[1141]
实施例26b(2r,8r)
[1142]c31h34
n4o7s的hrms计算值:606.2148;[m+h]
+
,实测值:607.2223(δ=0.3ppm)。
[1143]1h-nmr(400mhz,dmso-d6)δppm:12.11(sl,1h),7.61(d,1h),7.43(dd,1h),7.23(d,1h),7.11(d,1h),6.99(d,1h),6.88(d,1h),6.85(dd,1h),6.24(d,1h),5.28(q,1h),4.9(t,1h),4.75/4.61(m,2h),4.16/3.96(d,2h),3.91/3.83(m,2h),3.71/3.59(m,2h),3.59/3.5(m,2h),3.11/2.84(dd,2h),2.8(s,3h),2.3(s,3h),2.29/2.18(m,2h),1.19(d,3h)。
[1144]
实施例27:[(2r,8r)-2,4,33-三甲基-29,29-二氧代-19,23,28-三氧杂-29λ
6-硫杂-1,14,15,16-四氮杂六环[22.5.3.1
3,7
.1
9,13
.0
12,16
.0
27,31
]三十四碳-3(34),4,6,9(33),10,12,14,24,26,31-十烯-8-基]乙酸和
[1145]
[(2r,8s)-2,4,33-三甲基-29,29-二氧代-19,23,28-三氧杂-29λ
6-硫杂-1,14,15,16-四氮杂六环[22.5.3.1
3,7
.1
9,13
.0
12,16
.0
27,31
]三十四碳-3(34),4,6,9(33),10,12,14,24,26,31-十烯-8-基]乙酸
[1146]
[1147]
步骤a1:{2-[3-(苄氧基)丙氧基]乙基}氨基甲酸叔丁酯的制备
[1148]
向3-(苄氧基)丙基4-甲基苯-1-磺酸酯(41g,130mmol)的甲苯(2ml/mmol,260ml)溶液中加入四丁基硫酸氢铵(0.1eq.,4.3g,13mmol)、(2-羟基乙基)氨基甲酸叔丁酯(1eq.,21g,130mmol)和50wt%naoh水溶液(9eq.,92g,1.2mol)。将混合物于85℃加热16小时。反应完成后将混合物用1l etoac稀释。将混合物用2l饱和nh4cl水溶液洗涤,分层,将有机层用无水硫酸钠干燥,过滤,浓缩至干得到粗产物,将其通过反相色谱纯化,用水-mecn洗脱得到标题化合物(19.6g,黄色油,47%收率)。
[1149]1h-nmr(400mhz,dmso-d6)δppm:7.38-7.24(m,5h),6.73(t,1h),4.44(s,2h),3.49(t,2h),3.44(t,2h),3.33(t,2h),3.04(q,2h),1.76(quint,2h),1.38(s,9h)。
[1150]
步骤a2:2-[3-(苄氧基)丙氧基]乙-1-胺盐酸盐的制备
[1151]
在室温下,向{2-[3-(苄氧基)丙氧基]乙基}氨基甲酸叔丁酯(19.6g,59.5mmol)的二氧杂环己烷(5ml/mmol,298ml)溶液中加入hcl(4n的二氧杂环己烷溶液)(4eq.,59.5ml)。将反应混合物在室温下搅拌过夜。反应完成后将溶剂减压蒸发至干。粗产物不经纯化直接以hcl盐的形式使用(15.6g,定量)。
[1152]1h-nmr(400mhz,dmso-d6)δppm:7.98(s,3h),7.4-7.36(m,5h),4.46(s,2h),3.56(t,2h),3.5(t,2h),3.5(t,2h),2.93(t,2h),1.81(quint,2h)。
[1153]
步骤a3:n-{2-[3-(苄氧基)丙氧基]乙基}-3-甲基-2-硝基苯胺的制备
[1154]
采用通用方法2步骤1,用1-氟-3-甲基-2-硝基苯(1当量)和2-[3-(苄氧基)丙氧基]乙-1-胺盐酸盐(1.2当量)作为起始试剂,得到标题化合物(93%收率)。
[1155]1h-nmr(400mhz,dmso-d6)δppm:7.38-7.24(m,5h),7.27(m,1h),6.82(d,1h),6.59(d,1h),6.46(t,1h),4.42(s,2h),3.57(t,2h),3.52-3.47(m,4h),3.33(dt,2h),2.31(s,3h),1.79(quint,2h)。
[1156]
步骤a4:n-{2-[3-(苄氧基)丙氧基]乙基}-4-溴-3-甲基-2-硝基苯胺的制备
[1157]
采用通用方法2步骤2,用n-{2-[3-(苄氧基)丙氧基]乙基}-3-甲基-2-硝基苯胺(1当量)作为起始试剂,得到标题化合物(58%收率)。
[1158]1h-nmr(400mhz,dmso-d6)δppm:7.54(d,1h),7.38-7.23(m,5h),6.8(d,1h),6.09(t,1h),4.42(s,2h),3.51(t,2h),3.47(m,4h),3.3(q,2h),2.38(s,3h),1.77(quint,2h)。
[1159]
步骤a5:n
1-{2-[3-(苄氧基)丙氧基]乙基}-4-溴-3-甲基苯-1,2-二胺的制备
[1160]
采用通用方法2步骤3,用n-{2-[3-(苄氧基)丙氧基]乙基}-4-溴-3-甲基-2-硝基苯胺(1当量)作为起始试剂,得到标题化合物(定量)。
[1161]1h-nmr(400mhz,dmso-d6)δppm:7.38-7.23(m,5h),6.71(d,1h),6.29(d,1h),4.6(sl,3h),4.42(s,2h),3.56/3.5(m,2h),3.56/3.5(m,4h),3.16(t,2h),2.17(s,3h),1.79(quint,2h)。
[1162]
步骤a6:(2e)-3-(1-{2-[3-(苄氧基)丙氧基]乙基}-4-甲基-1h-苯并三唑-5-基)丙-2-烯酸乙酯的制备
[1163]
采用通用方法2步骤4,用n
1-{2-[3-(苄氧基)丙氧基]乙基}-4-溴-3-甲基苯-1,2-二胺(1当量)作为反应试剂,得到1-{2-[3-(苄氧基)丙氧基]乙基}-5-溴-4-甲基-1h-苯并三唑(29%收率)。将粗产物用通用方法2步骤5进行反应得到标题化合物(91%收率)。
[1164]1h-nmr(400mhz,dmso-d6)δppm:8.01(d,1h),7.92(d,1h),7.69(d,1h),7.3(t,
3-{3-[(1r)-1-(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)乙基]-4-甲基苯基}丙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体,83%收率)。
[1176]1h-nmr(400mhz,dmso-d6)δppm:1.00(td,j=7.09,5.50hz,5h)1.24(d,j=6.85hz,2h)1.52(d,j=6.85hz,3h)1.77-1.86(m,1h)1.92(dt,j=12.90,6.39hz,2h)2.30(d,j=1.59hz,5h)2.79(s,2h)2.85(s,3h)2.92-3.27(m,4h)3.44-3.66(m,5h)3.81-3.88(m,3h)3.92-4.01(m,3h)4.01-4.16(m,2h)4.34(d,j=17.85hz,1h)4.70-4.82(m,2h)4.82-4.96(m,3h)5.28(d,j=7.09hz,1h)5.35(q,j=6.64hz,1h)6.00(d,j=2.81hz,1h)6.44(d,j=2.81hz,1h)6.71-6.85(m,2h)6.91-7.02(m,2h)7.11(d,j=7.82hz,1h)7.19-7.31(m,2h)7.48(d,j=6.85hz,1h)7.57(s,1h)7.58-7.69(m,3h)。
[1177]
步骤5:实施例27的制备
[1178]
采用通用方法12,用[(2r)-2,4,33-三甲基-29,29-二氧代-19,23,28-三氧杂-29λ
6-硫杂-1,14,15,16-四氮杂六环[22.5.3.1
3,7
.1
9,13
.0
12,16
.0
27,31
]三十四碳-3(34),4,6,9(33),10,12,14,24,26,31-十烯-8-基]乙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体,97%收率)。
[1179]
通过手性柱色谱分离得到非对映体纯产物。
[1180]
实施例27a(2r,8r)
[1181]c31h34
n4o7s的hrms计算值:606.2148;[m+h]
+
,实测值:607.2224(δ=0.5ppm)。
[1182]1h-nmr(400mhz,dmso-d6)δppm:12.2(sl,1h),7.6(d,1h),7.49(dd,1h),7.26(d,1h),7.19(d,1h),7(d,1h),6.95(d,1h),6.76(dd,1h),6.01(d,1h),5.28(q,1h),4.9(t,1h),4.78(m,2h),4.11/3.9(d,2h),4(m,2h),3.6(m,2h),3.55(m,2h),3.08/2.85(dd,2h),2.79(s,3h),2.3(s,3h),1.83(m,2h),1.23(d,3h)。
[1183]
实施例27b(2r,8s)
[1184]c31h34
n4o7s的hrms计算值:606.2148;[m+h]
+
,实测值:607.2222(δ=0.2ppm)。
[1185]1h-nmr(400mhz,dmso-d6)δppm:12.1(sl,1h),7.64(d,1h),7.59(d,1h),7.55(d,1h),7.23(dd,1h),7.11(d,1h),6.99(d,1h),6.81(dd,1h),6.43(d,1h),5.33(q,1h),4.85/4.76(m,2h),4.85(t,1h),4.32/4.01(d,2h),4-3.97(m,2h),3.86(m,2h),3.61/3.52(m,2h),3.07(m,2h),2.83(s,3h),2.3(s,3h),1.91(m,2h),1.5(d,3h)。
[1186]
实施例28a和28b:[(2r,8r)-4-甲氧基-2,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸和
[1187]
[(2r,8s)-4-甲氧基-2,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸
[1188][1189]
步骤1:3-{3-[(1s)-1-羟基乙基]-4-甲氧基苯基}-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯的制备
[1190]
采用通用方法6,用(2e)-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙-2-烯酸乙酯(1当量)和(1s)-1-[2-甲氧基-5-(4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷-2-基)苯基]乙-1-醇(1.5当量)作为起始试剂,得到标题化合物(65%收率)。
[1191]1h-nmr(400mhz,dmso-d6)δppm:7.58(2d,1h),7.45(2d,1h),7.37(d,1h),7.2(d,2h),7.13(2dd,1h),6.87(d,2h),6.82(d,1h),4.91(m,1h),4.89(d,1h),4.82(m,1h),4.64(m,2h),4.32(s,2h),3.92(q,2h),3.73/3.72(2s,6h),3.38(t,2h),3.11(m,2h),2.76/2.75(2s,3h),1.92(m,2h),1.48(m,2h),1.22-1.15(2d,3h),0.99(t,3h)。
[1192]
步骤2:3-(3-{(1r)-1-[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]乙基}-4-甲氧基苯基)-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯的制备
[1193]
采用通用方法7,用3-{3-[(1s)-1-羟基乙基]-4-甲氧基苯基}-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯(1当量)和6-(苄氧基)-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮(1.1eq.)作为起始试剂,得到标题化合物(66%收率)。
[1194]1h-nmr(400mhz,dmso-d6)δppm:7.6(d,1h),7.5(2d,1h),7.45-7.3(m,6h),7.2(d,2h),7.1(dd,1h),6.9(m,4h),6.75(m,2h),5.39(m,1h),5(m,2h),4.8(m,1h),4.6(2t,2h),4.55(m,2h),4.3(s,2h),3.91(q,2h),3.71/3.65(2s,6h),3.48(m,2h),3.18(d,2h),2.79(s,3h),1.91(m,2h),1.5(m,2h),1.45(2d,3h),1(t,3h)。
[1195]
步骤3:3-[1-(4-羟基丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(1r)-1-(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)乙基]-4-甲氧基苯基}丙酸乙酯的制备
[1196]
采用通用方法8,用3-(3-{(1r)-1-[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]乙基}-4-甲氧基苯基)-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯(1当量)作为起始试剂,得到标题化合物(灰白色固体,83%收率)。
[1197]1h-nmr(400mhz,dmso-d6)δppm:1.01(td,j=7.09,3.79hz,3h)1.21(dd,j=13.69,5.99hz,1h)1.31-1.39(m,2h)1.42(t,j=6.42hz,3h)1.91(quint,j=7.31hz,2h)2.76(d,j=3.67hz,3h)3.09-3.21(m,2h)3.38(t,j=5.93hz,2h)3.67(s,3h)3.70(s,1h)3.94(q,j=7.09hz,2h)4.34-4.57(m,3h)4.65(t,j=6.97hz,2h)4.83(q,j=7.62hz,1h)5.37(quint,j=6.79hz,1h)6.51(dd,j=13.14,2.75hz,1h)6.64(dd,j=8.99,2.75hz,1h)6.73-6.85(m,3h)7.08(d,j=8.19hz,1h)7.13(dd,j=8.56,2.08hz,1h)7.42(dd,j=9.35,
2.02hz,1h)7.53(t,j=9.11hz,1h)7.59-7.67(m,1h)9.54(br.s.,1h)。
[1198]
步骤4:3-[1-(4-溴丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(1r)-1-(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)乙基]-4-甲氧基苯基}丙酸乙酯的制备
[1199]
采用通用方法9,用3-[1-(4-羟基丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(1r)-1-(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)乙基]-4-甲氧基苯基}丙酸乙酯(1当量)作为起始试剂,得到标题化合物(73%收率)。
[1200]1h-nmr(400mhz,dmso-d6)δppm:1.00(td,j=7.09,3.79hz,3h)1.42(t,j=6.66hz,3h)1.71-1.83(m,2h)1.94-2.05(m,2h)2.70-2.79(m,3h)3.08-3.25(m,2h)3.53(t,j=6.66hz,2h)3.62-3.70(m,3h)3.94(q,j=7.13hz,2h)4.34-4.57(m,2h)4.69(t,j=6.85hz,2h)4.83(q,j=7.83hz,1h)5.31-5.42(m,1h)6.51(dd,j=11.37,2.81hz,1h)6.64(dd,j=8.93,2.81hz,1h)6.62-6.68(m,1h)6.74-6.84(m,2h)7.13(dd,j=8.50,2.02hz,1h)7.42(dd,j=10.03,2.08hz,1h)7.55(t,j=8.74hz,1h)7.61-7.68(m,1h)9.52(d,j=5.01hz,1h)。
[1201]
步骤5:[(2r)-4-甲氧基-2,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯的制备
[1202]
采用通用方法11,用3-[1-(4-溴丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(1r)-1-(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)乙基]-4-甲氧基苯基}丙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体,73%收率)。
[1203]1h-nmr(400mhz,dmso-d6)δppm:1.02(td,j=7.09,2.81hz,6h)1.12-1.22(m,5h)1.22-1.29(m,4h)1.31(d,j=7.21hz,3h)1.40(d,j=7.46hz,1h)1.48-1.61(m,1h)1.62-1.88(m,2h)2.00-2.28(m,4h)2.63-2.90(m,6h)3.09(td,j=15.62,7.89hz,2h)3.24-3.37(m,10h)3.46(td,j=9.54,6.11hz,1h)3.53-3.69(m,3h)3.70-3.80(m,7h)3.88-3.98(m,5h)4.05-4.15(m,1h)4.68-4.97(m,6h)5.43(dq,j=17.93,7.19hz,2h)5.62(d,j=2.57hz,1h)5.75(d,j=2.81hz,1h)6.62-6.72(m,2h)6.80-6.94(m,4h)6.99(d,j=8.56hz,1h)7.20-7.29(m,2h)7.42(dd,j=8.44,1.96hz,1h)7.50(dd,j=8.56,1.83hz,1h)7.67(d,j=8.68hz,1h)7.74-7.81(m,1h)7.83-7.89(m,1h)。
[1204]
步骤6:实施例28a和28b的制备
[1205]
采用通用方法12,用[(2r)-4-甲氧基-2,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体,77%收率)。
[1206]
通过手性柱色谱分离得到非对映体纯产物。
[1207]
实施例28a(2r,8r)
[1208]c30h32
n4o7s的hrms计算值:592.1992;[m+h]
+
,实测值:593.2067(δ=0.4ppm)。
[1209]1h-nmr(400mhz,dmso-d6)δppm:12.5-11.8(m,1h),7.67(d,1h),7.5(dd,1h),7.19(d,1h),7(d,1h),6.83(d,1h),6.8(d,1h),6.65(dd,1h),5.63(d,1h),5.4(q,1h),4.87(dd,1h),4.72(m,2h),4/3.71(am,2h),3.76(s,3h),3.6/3.32(2m,2h),3.2/2.9(2dd,2h),2.81(s,3h),2.2/2.01(2m,2h),1.7/1.4(2m,2h),1.17(d,3h)。
[1210]
实施例28b(2r,8s)
[1211]c30h32
n4o7s的hrms计算值:592.1992;[m+h]
+
,实测值:593.2066(δ=0.3ppm)。
[1212]1h-nmr(400mhz,dmso-d6)δppm:12.3-11.6(m,1h),7.92(dd,1h),7.82(d,1h),7.77(d,1h),7.18(d,1h),6.9(d,1h),6.88(d,1h),6.69(dd,1h),5.7(d,1h),5.42(q,1h),4.75(m,3h),4.08/3.69(am,2h),3.72(s,3h),3.62/3.45(2m,2h),3.2/2.99(2dd,2h),2.68(s,3h),2.2/2.1(2m,2h),1.8/1.59(2m,2h),1.29(d,3h)。
[1213]
实施例28c和28d:[(2s,8r)-4-甲氧基-2,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸和
[1214]
[(2s,8s)-4-甲氧基-2,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸
[1215][1216]
步骤1:3-{3-[(1r)-1-羟基乙基]-4-甲氧基苯基}-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯的制备
[1217]
采用通用方法6,用(2e)-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙-2-烯酸乙酯(1当量)和(1r)-1-[2-甲氧基-5-(4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷-2-基)苯基]乙-1-醇(1.1当量)作为起始试剂,得到标题化合物(81%收率)。
[1218]1h-nmr(400mhz,dmso-d6)δppm:7.6(2d,1h),7.45(2d,1h),7.35(d,1h),7.2(d,2h),7.12(dd,1h),6.88(d,2h),6.81(d,1h),4.9(d,1h),4.9(m,1h),4.8(m,1h),4.65(t,2h),4.32(s,2h),3.91(q,2h),3.71(2s,6h),3.4(t,2h),3.1(2d,2h),2.79(2s,3h),1.92(m,2h),1.48(m,2h),1.2(2d,3h),1(t,3h)。
[1219]
步骤2:3-(3-{(1s)-1-[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]乙基}-4-甲氧基苯基)-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯的制备
[1220]
采用通用方法7,用3-{3-[(1r)-1-羟基乙基]-4-甲氧基苯基}-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯(1当量)和6-苄氧基-3,4-二氢-1,2λ6,3-噁噻嗪2,2-二氧化物(1.1eq.)作为起始试剂,得到标题化合物(60%收率)。
[1221]1h-nmr(400mhz,dmso-d6)δppm:7.6(d,1h),7.5(2d,1h),7.45-7.3(m,6h),7.2(d,2h),7.11(dd,1h),6.9(m,2h),6.88(d,2h),6.78(m,2h),5.39(m,1h),5.05(m,2h),4.81(m,1h),4.65-4.5(m,2h),4.61(2t,2h),4.3(s,2h),3.92(q,2h),3.71/3.65(2s,6h),3.38(m,2h),3.15(m,2h),2.78(s,3h),1.9(m,2h),1.48(m+d,5h),0.99(t,3h)。
[1222]
步骤3:3-[1-(4-羟基丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(1s)-1-(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)乙基]-4-甲氧基苯基}丙酸乙酯的制备
[1223]
采用通用方法8,用3-(3-{(1s)-1-[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]乙基}-4-甲氧基苯基)-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯(1当量)作为起始试剂,得到标题化合物(70%收率)。
[1224]1h-nmr(400mhz,dmso-d6)δppm:0.95-1.03(m,3h)1.30-1.47(m,5h)1.85-1.97(m,2h)2.76(d,j=3.55hz,3h)3.18(d,j=8.19hz,2h)3.34-3.42(m,2h)3.67(s,3h)3.94(q,j=7.13hz,2h)4.33(t,j=5.07hz,1h)4.37-4.58(m,3h)4.65(t,j=6.97hz,2h)4.83(q,j=7.87hz,1h)5.32-5.42(m,1h)6.51(dd,j=13.20,2.81hz,1h)6.64(dd,j=8.86,2.75hz,1h)6.76(d,j=1.59hz,1h)6.79-6.84(m,2h)7.08(d,j=8.31hz,1h)7.13(dd,j=8.56,2.08hz,1h)7.42(dd,j=9.05,1.96hz,1h)7.53(t,j=9.17hz,1h)7.60-7.65(m,1h)9.51(s,1h)9.52(s,1h)。
[1225]
步骤4:3-[1-(4-溴丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(1s)-1-(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)乙基]-4-甲氧基苯基}丙酸乙酯的制备
[1226]
采用通用方法9,用3-[1-(4-羟基丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(1s)-1-(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)乙基]-4-甲氧基苯基}丙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体,定量)。
[1227]1h-nmr(400mhz,dmso-d6)δppm:1.00(td,j=7.09,3.79hz,3h)1.42(t,j=6.66hz,3h)1.71-1.82(m,2h)1.92-2.06(m,2h)2.76(d,j=3.91hz,3h)3.10-3.25(m,2h)3.53(t,j=6.66hz,2h)3.67(d,j=1.10hz,3h)3.94(q,j=7.13hz,2h)4.35-4.60(m,2h)4.69(t,j=6.85hz,2h)4.83(q,j=7.83hz,1h)5.36(quin,j=6.94hz,1h)6.51(dd,j=11.37,2.81hz,1h)6.64(dd,j=8.93,2.81hz,1h)6.76(s,1h)6.78(s,1h)6.81(dd,j=8.68,2.93hz,1h)7.13(dd,j=8.50,2.02hz,1h)7.42(dd,j=10.03,2.08hz,1h)7.55(t,j=8.74hz,1h)7.61-7.69(m,1h)9.52(d,j=5.01hz,1h)。
[1228]
步骤5:[(2s)-4-甲氧基-2,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯的制备
[1229]
采用通用方法11,用3-[1-(4-溴丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(1s)-1-(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)乙基]-4-甲氧基苯基}丙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体,60%收率)。
[1230]1h-nmr(400mhz,dmso-d6)δppm:0.98-1.07(m,6h)1.15-1.20(m,4h)1.31(d,j=7.21hz,3h)1.40(d,j=7.46hz,1h)1.48-1.61(m,1h)1.62-1.75(m,1h)1.75-1.87(m,1h)2.00-2.14(m,2h)2.14-2.28(m,2h)2.70(s,3h)2.84(s,2h)3.09(td,j=15.62,7.89hz,2h)3.32-3.38(m,1h)3.46(td,j=9.54,6.11hz,1h)3.54-3.77(m,9h)3.87-3.98(m,5h)3.98-4.02(m,1h)4.05-4.14(m,1h)4.66-4.83(m,5h)4.89(t,j=7.89hz,1h)5.43(dq,j=17.93,7.19hz,2h)5.62(d,j=2.57hz,1h)5.75(d,j=2.81hz,1h)6.62-6.72(m,2h)6.81-6.93(m,4h)6.99(d,j=8.56hz,1h)7.19-7.26(m,2h)7.42(dd,j=8.44,1.96hz,1h)7.50(dd,j=8.56,1.83hz,1h)7.67(d,j=8.68hz,1h)7.74-7.80(m,1h)7.83-7.89(m,1h)。
[1231]
步骤6:实施例28c和28d的制备
[1232]
采用通用方法12,用[(2s)-4-甲氧基-2,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体,89%收率)。
[1233]
通过手性柱色谱分离得到非对映体纯产物。
[1234]
实施例28c(2s,8r)
[1235]c30h32
n4o7s的hrms计算值:592.1992;[m+h]
+
,实测值:593.2065(δ=0.1ppm)。
[1236]
实施例28d(2s,8s)
[1237]c30h32
n4o7s的hrms计算值:592.1992;[m+h]
+
,实测值:593.2070(δ=0.9ppm)。
[1238]1h-nmr(400mhz,dmso-d6)δppm:12.3-11.6(m,1h),7.92(dd,1h),7.82(d,1h),7.77(d,1h),7.18(d,1h),6.9(d,1h),6.88(d,1h),6.69(dd,1h),5.7(d,1h),5.42(q,1h),4.75(m,3h),4.08/3.69(am,2h),3.72(s,3h),3.62/3.45(m,2h),3.2/2.99(dd,2h),2.68(s,3h),2.2/2.1(m,2h),1.8/1.59(m,2h),1.29(d,3h)。
[1239]
实施例29:[(2r,8r)-2,4,24,31-四甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸和
[1240]
[(2r,8s)-2,4,24,31-四甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸
[1241][1242]
步骤1:3-{1-[4-(苄氧基)丁基]-4-甲基-1h-苯并三唑-5-基}-3-{3-[(1s)-1-羟基乙基]-4-甲基苯基}丙酸乙酯的制备
[1243]
采用通用方法6,用(e)-3-[1-(4-苄氧基丁基)-4-甲基-苯并三唑-5-基]丙-2-烯酸乙酯(1当量)和(1s)-1-[2-甲基-5-(4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷-2-基)苯基]乙醇(1.2当量)作为起始试剂,得到标题化合物(50%收率)。
[1244]1h-nmr(400mhz,dmso-d6)δppm:7.58/7.46(2dd,1h),7.41(d,1h),7.35-7.22(m,5h),7.06(dd,1h),6.98(d,1h),4.97/4.96(2d,1h),4.83(m,1h),4.83(m,1h),4.65(t,2h),4.4(s,2h),3.92(q,2h),3.42(t,2h),3.12(m,2h),2.77/2.76(2s,3h),2.19(s,3h),1.94(m,2h),1.5(m,2h),1.23/1.21(2d,3h),1(t,3h)。
[1245]
步骤2:3-{1-[4-(苄氧基)丁基]-4-甲基-1h-苯并三唑-5-基}-3-(3-{(1r)-1-[6-(苄氧基)-8-甲基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]乙基}-4-甲基苯基)丙酸乙酯的制备
[1246]
采用通用方法7,用3-{1-[4-(苄氧基)丁基]-4-甲基-1h-苯并三唑-5-基}-3-{3-[(1s)-1-羟基乙基]-4-甲基苯基}丙酸乙酯(1当量)和6-(苄氧基)-8-甲基-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮(1.1当量)作为起始试剂,得到标题化合物(68%收率)。
[1247]1h-nmr(400mhz,dmso-d6)δppm:0.90-1.03(m,6h)1.41(d,j=6.97hz,5h)1.43-1.53(m,4h)1.81-1.98(m,4h)2.13-2.20(m,6h)2.28(s,6h)2.73-2.80(m,6h)3.11-3.25(m,4h)3.34-3.44(m,4h)3.92(q,j=7.05hz,4h)4.25-4.37(m,2h)4.39(d,j=3.67hz,5h)
[1248]
4.55-4.66(m,4h)4.81-4.91(m,2h)4.99-5.11(m,4h)5.26(q,j=6.93hz,2h)6.63(d,j=2.81hz,1h)6.69(d,j=2.81hz,1h)6.89-6.97(m,2h)7.06-7.15(m,4h)7.20-7.37(m,12h)7.37-7.48(m,10h)7.51-7.56(m,2h)7.56-7.61(m,2h)。
[1249]
步骤3:3-[1-(4-羟基丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(1r)-1-(6-羟基-8-甲基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)乙基]-4-甲基苯基}丙酸乙酯的制备
[1250]
采用通用方法8,用3-{1-[4-(苄氧基)丁基]-4-甲基-1h-苯并三唑-5-基}-3-(3-{(1r)-1-[6-(苄氧基)-8-甲基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]乙基}-4-甲基苯基)丙酸乙酯(1当量)作为起始试剂,得到标题化合物(63%收率)。
[1251]1h-nmr(400mhz,dmso-d6)δppm:9.5/4.4(s+t,2h),7.61(2d,1h),7.58(2d,1h),7.45(2d,1h),7.11(m,2h),6.61(2d,1h),6.41/6.39(2d,1h),5.25(m,1h),4.9(m,1h),4.65(t,2h),4.35/4.29(2m,2h),3.95(q,2h),3.4(q,2h),3.21(d,2h),2.79(s,3h),2.3(s,3h),2.11(2s,3h),1.91(m,2h),1.45(2d,3h),1.38(m,2h),1.01(2t,3h)。
[1252]
步骤4:3-[1-(4-溴丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(1r)-1-(6-羟基-8-甲基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)乙基]-4-甲基苯基}丙酸乙酯的制备
[1253]
采用通用方法9,用3-[1-(4-羟基丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(1r)-1-(6-羟基-8-甲基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)乙基]-4-甲基苯基}丙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体,77%收率)。
[1254]1h-nmr(400mhz,dmso-d6)δppm:9.5(s,1h),7.62(d,1h),7.59(d,1h),7.48/7.41(d,1h),7.1(m,2h),6.61(d,1h),6.4/6.39(d,1h),5.24(m,1h),4.88(m,1h),4.69(t,2h),4.31/4.28(m,2h),3.92(q,2h),3.52(q,2h),3.21(d,2h),2.79(s,3h),2.28(s,3h),2.1(s,2h),2(m,2h),1.78(d,3h),1.41(m,2h),1(t,3h)。
[1255]
步骤5:[(2r)-2,4,24,31-四甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯的制备
[1256]
采用通用方法11,用3-[1-(4-溴丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(1r)-1-(6-羟基-8-甲基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)乙基]-4-甲基苯基}丙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体,61%收率)。
[1257]1h-nmr(400mhz,dmso-d6)δppm:0.97-1.13(m,4h)1.21-1.32(m,2h)1.53-1.76(m,1h)1.77-1.89(m,1h)2.03-2.10(m,3h)2.12-2.25(m,1h)2.31(d,j=11.86hz,3h)2.66(s,2h)2.72-2.80(m,1h)2.81(s,1h)2.95-3.15(m,1h)3.34-3.51(m,2h)3.67(td,j=9.75,5.32hz,1h)3.88-4.01(m,3h)4.62-4.85(m,3h)4.92(t,j=7.76hz,1h)5.24(dq,j=13.89,6.82hz,1h)5.53(d,j=2.93hz,1h)5.69(br.s.,1h)6.56-6.76(m,1h)7.08-7.24(m,2h)
7.30(d,j=7.95hz,1h)7.44(d,j=7.70hz,1h)7.68(d,j=8.80hz,1h)7.74(d,j=8.68hz,1h)7.88(d,j=8.68hz,1h)。
[1258]
步骤6:实施例29的制备
[1259]
采用通用方法12,用[(2r)-2,4,24,31-四甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体,73%收率)。
[1260]
通过手性柱色谱分离得到非对映体纯产物。
[1261]
实施例29a(2r,8r)
[1262]c31h34
n4o6s的hrms计算值:590.2199;[m+h]
+
,实测值:591.2273(δ=0.2ppm)。
[1263]1h-nmr(400mhz,dmso-d6)δppm:12.25(m,1h),7.7(d,1h),7.48(dd,1h),7.3(d,1h),7.1(d,1h),6.72(d,1h),6.61(d,1h),5.7(sl,1h),5.21(q,1h),4.9(t,1h),4.75(m,2h),4.02/3.48(2d,2h),3.75/3.7(2m,2h),3.28/2.9(2dd,2h),2.8(s,3h),2.31(s,3h),2.2/2.02(2m,2h),2.08(s,3h),1.61/1.28(2m,2h),1.11(d,3h)。
[1264]
实施例29b(2r,8s)
[1265]c31h34
n4o6s的hrms计算值:590.2199;[m+h]
+
,实测值:591.2273(δ=0.2ppm)。
[1266]1h-nmr(400mhz,dmso-d6)δppm:12.2(m,1h),7.89(d,1h),7.72(d,1h),7.48(dd,1h),7.2(d,1h),7.11(d,1h),6.69(d,1h),5.51(d,1h),5.28(q,1h),4.8-4.7(2m,2h),4.8(t,1h),4/3.4(2d,2h),3.65/3.47(2m,2h),3.2/2.99(2dd,2h),2.69(s,3h),2.3(s,3h),2.18/2.1(2m,2h),2.1(s,3h),1.82/1.71(2m,2h),1.11(d,3h)。
[1267]
实施例30:[5-甲氧基-4,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸
[1268][1269]
步骤b1:5-溴-3-甲氧基-2-甲基苯甲酸甲酯的制备
[1270]
将5-溴-3-羟基-2-甲基苯甲酸甲酯(1.0eq.,26.0g,106.1mmol)溶于dmf(300ml),然后加入碘甲烷(4eq.,26.5ml,60.2g,424.5mmol)和cs2co3(4eq.,137.9g,424.5mmol)。将反应混合物室温搅拌12小时。反应完成后将混合物倒入冰水中,用etoac萃取,分离后将有机相用硫酸镁干燥并减压浓缩。将粗产物通过正相硅胶色谱纯化,用庚烷-etoac洗脱得到标题化合物(浅黄色固体,19.1g,69%收率)。
[1271]1h-nmr(400mhz,dmso-d6)δppm:7.44(s,1h),7.34(s,1h),3.88(s,3h),3.83(s,3h),2.25(s,3h)。
[1272]
步骤b2:(5-溴-3-甲氧基-2-甲基苯基)甲醇的制备
[1273]
将5-溴-3-甲氧基-2-甲基苯甲酸甲酯(1eq.,19.0g,73mmol)溶于thf(200ml),将溶液冷却至0℃。在30分钟内于n2气氛下加入氢化铝锂(1.2eq.,44ml,2m的thf溶液)。将混合物升温至室温并在室温下搅拌2小时。将反应混合物用饱和nh4cl水溶液淬灭,用etoac萃取,将有机相分离,用硫酸镁干燥,减压浓缩。将粗产物通过正相硅胶色谱纯化,用庚烷-etoac洗脱得到标题化合物(黄色固体,14.7g,87%收率)。
[1274]1h-nmr(400mhz,dmso-d6)δppm:7.16(s,1h),7.03(s,1h),5.23(t,1h),4.46(d,2h),3.34(s,3h),2.00(s,3h)。
[1275]
步骤b3:[3-甲氧基-2-甲基-5-(4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷-2-基)苯基]甲醇的制备
[1276]
采用通用方法3,用(5-溴-3-甲氧基-2-甲基苯基)甲醇(1eq.,14.6g.,63mmol)作为反应试剂,得到标题化合物(12.53g,71%收率)。
[1277]1h-nmr(400mhz,dmso-d6)δppm:7.37(sl,1h),7.06(sl,1h),5.04(t,1h),4.47(d,2h),3.79(s,3h),2.09(s,3h),1.29(s,12h)。
[1278]
步骤1:3-{1-[4-(苄氧基)丁基]-4-甲基-1h-苯并三唑-5-基}-3-[3-(羟基甲基)-5-甲氧基-4-甲基苯基]丙酸乙酯的制备
[1279]
采用通用方法6,用(2e)-3-{1-[4-(苄氧基)丁基]-4-甲基-1h-苯并三唑-5-基}丙-2-烯酸乙酯(1当量)和[3-甲氧基-2-甲基-5-(4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷-2-基)苯基]甲醇(1.15当量)作为起始试剂,得到标题化合物(76%收率)。
[1280]1h-nmr(400mhz,dmso-d6)δppm:7.59(d,1h),7.49(d,1h),7.35-7.2(m,5h),6.89(d,2h),4.95(t,1h),4.82(t,1h),4.67(t,2h),4.41(s,2h),4.4(d,2h),3.91(q,2h),3.75(s,3h),3.45(t,2h),3.15(d,2h),2.8(s,3h),2(s,3h),1.95(m,2h),1.5(m,2h),1(t,3h)。
[1281]
步骤2:3-{1-[4-(苄氧基)丁基]-4-甲基-1h-苯并三唑-5-基}-3-(3-{[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-5-甲氧基-4-甲基苯基)丙酸乙酯的制备
[1282]
采用通用方法7,用3-{1-[4-(苄氧基)丁基]-4-甲基-1h-苯并三唑-5-基}-3-[3-(羟基甲基)-5-甲氧基-4-甲基苯基]丙酸乙酯(1当量)和6-(苄氧基)-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮(1.1当量)作为起始试剂,得到标题化合物(87%收率)。
[1283]1h-nmr(400mhz,dmso-d6)δppm:7.59(d,1h),7.54(d,1h),7.49-7.2(m,10h),7.11(d,1h),7.08(dd,1h),6.96(d,1h),6.9(d,1h),6.8(d,1h),5.1(s,2h),4.87(t,1h),4.61(t,2h),4.39(s,4h),4.19(m,2h),3.92(q,2h),3.74(s,3h),3.39(t,2h),3.19(d,2h),2.79(s,3h),2.03(s,3h),1.9(m,2h),1.48(m,2h),0.99(t,3h)。
[1284]
步骤3:3-[1-(4-羟基丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-5-甲氧基-4-甲基苯基}丙酸乙酯的制备
[1285]
采用通用方法8,用3-{1-[4-(苄氧基)丁基]-4-甲基-1h-苯并三唑-5-基}-3-(3-{[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-5-甲氧基-4-甲基苯基)丙酸乙酯(1当量)作为起始试剂,得到标题化合物(95%收率)。
[1286]1h-nmr(400mhz,dmso-d6)δppm:9.7/4.85(s+t,2h),7.6(d,1h),7.52(d,1h),7(d,1h),6.95(d,1h),6.8(m,2h),6.59(d,1h),4.65(t,2h),4.41(m,1h),4.31(s,2h),4.18(m,
2h),3.95(q,2h),3.78(s,3h),3.4(t,2h),3.2(d,2h),2.8(s,3h),2.05(s,3h),1.91(m,2h),1.38(m,2h),1(t,3h)。
[1287]
步骤4:3-[1-(4-溴丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-5-甲氧基-4-甲基苯基}丙酸乙酯的制备
[1288]
采用通用方法9,用3-[1-(4-羟基丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-5-甲氧基-4-甲基苯基}丙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体,86%收率)。
[1289]1h-nmr(400mhz,dmso-d6)δppm:9.67(s,1h),7.63(d,1h),7.56(d,1h),6.98(d,1h),6.95(d,1h),6.78(m,2h),6.57(d,1h),4.84(t,1h),4.69(t,2h),4.33(s,2h),4.2/4.12(2d,2h),3.94(q,2h),3.75(s,3h),3.53(t,2h),3.19(d,2h),2.78(s,3h),2.05(s,3h),2(quint,2h),1.77(quint,2h),1(t,3h)。
[1290]
步骤5:[5-甲氧基-4,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯的制备
[1291]
采用通用方法11,用3-[1-(4-溴丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-5-甲氧基-4-甲基苯基}丙酸乙酯(1当量)作为起始试剂,得到标题化合物(定量)。
[1292]1h-nmr(400mhz,dmso-d6)δppm:7.67(d,1h),7.45(d,1h),7.23(s,1h),6.98(d,1h),6.79(dd,1h),6.12(d,1h),5.81(d,1h),4.83-4.74(m,3h),4.16-3.78(m,6h),3.9(s,3h),3.64/3.4(dt,2h),3.21/3.07(dd,2h),2.64(s,3h),2.24-2.03(m,2h),2.14(s,3h),1.82/1.65(m,2h),1.02(t,3h)。
[1293]
步骤6:实施例30的制备
[1294]
采用通用方法12,用[5-甲氧基-4,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体,66%收率)。
[1295]
通过手性柱色谱分离得到对映体纯产物。
[1296]
实施例30a(e1)
[1297]c30h32
n4o7s的hrms计算值:592.1992;[m+h]
+
,实测值:593.2069(δ=0.8ppm)。
[1298]
实施例30b(e2)
[1299]c30h32
n4o7s的hrms计算值:592.1992;[m+h]
+
,实测值:593.2066(δ=0.3ppm)。
[1300]1h-nmr(400mhz,dmso-d6)δppm:12.2(m,1h),7.7(d,1h),7.45(d,1h),7.25(d,1h),7(d,1h),6.8(dd,1h),6.11(d,1h),5.8(d,1h),4.8(m,3h),4.12/3.82(d,2h),4.03/3.85(d,2h),3.9(s,3h),3.65/3.4(m,2h),3.1/2.98(dd,2h),2.62(s,3h),2.21/2.1(m,2h),2.18(s,3h),1.88/1.68(m,2h)。
[1301]
实施例31:[(2s,8s)-4-甲氧基-2,32-二甲基-28,28-二氧代-22,27-二氧杂-28λ
6-硫杂-1,14,15,16-四氮杂六环[21.5.3.1
3,7
.1
9,13
.0
12,16
.0
26,30
]三十三碳-3(33),4,6,9(32),10,12,14,23,25,30-十烯-8-基]乙酸,
[1302]
[(2r,8s)-4-甲氧基-2,32-二甲基-28,28-二氧代-22,27-二氧杂-28λ
6-硫杂-1,
14,15,16-四氮杂六环[21.5.3.1
3,7
.1
9,13
.0
12,16
.0
26,30
]三十三碳-3(33),4,6,9(32),10,12,14,23,25,30-十烯-8-基]乙酸,
[1303]
[(2s,8r)-4-甲氧基-2,32-二甲基-28,28-二氧代-22,27-二氧杂-28λ
6-硫杂-1,14,15,16-四氮杂六环[21.5.3.1
3,7
.1
9,13
.0
12,16
.0
26,30
]三十三碳-3(33),4,6,9(32),10,12,14,23,25,30-十烯-8-基]乙酸和
[1304]
[(2r,8r)-4-甲氧基-2,32-二甲基-28,28-二氧代-22,27-二氧杂-28λ
6-硫杂-1,14,15,16-四氮杂六环[21.5.3.1
3,7
.1
9,13
.0
12,16
.0
26,30
]三十三碳-3(33),4,6,9(32),10,12,14,23,25,30-十烯-8-基]乙酸
[1305][1306]
步骤a1:{[(5-碘戊基)氧基]甲基}苯的制备
[1307]
于15℃下,向5-(苄氧基)戊-1-醇(1eq.,1.15kg,5.92mol)的dcm(8l)溶液中加入pph3(1.3eq.,2.02kg,7.70mol)和咪唑(1.3eq.,524g,7.70mol)。于0~15℃将碘(1.3eq.,1.95kg,7.70mol)分批加入到混合物中。将混合物于15℃搅拌0.5小时。反应完成后,将混合物用饱和na2so3水溶液(5l)淬灭。将有机层分离,用无水硫酸钠干燥,过滤并减压浓缩。将残余物缓慢冷却至0℃。将形成的沉淀物滤出,将滤饼用mtbe洗涤(2x1.3 l)并将滤液减压浓缩。将残余物通过正相硅胶色谱纯化,用石油醚/etoac 0至50:1洗脱得到标题化合物(浅黄色油,1.45kg,81%收率)。
[1308]1h-nmr(400mhz,cdcl3)δppm:7.27-7.37(m,5h),4.52(m,2h),3.49(t,j=6.4hz,2h),3.20(t,j=7.2hz,2h),1.84-1.88(m,2h),1.64-1.67(m,2h),1.49-1.53(m,2h)。
[1309]
步骤a2:n-[5-(苄氧基)戊基]-4-溴-3-甲基-2-硝基苯胺的制备
[1310]
于0-5℃下,向4-溴-3-甲基-2-硝基-苯胺(1eq.,25g,108mmol)和{[(5-碘戊基)氧基]甲基}苯(1.5eq.,49.4g,162mmol)的dmf(250ml)溶液中分批加入叔丁醇钾(1.5eq.,
18.2g,162mmol),然后将混合物在室温下搅拌3小时。将反应混合物倒入h2o(520ml)中,用mtbe萃取(3x90ml)。将合并的有机层用硫酸钠干燥,过滤并浓缩至干。将残余物通过正相硅胶色谱纯化,用石油醚/etoac 0至7:1洗脱得到标题化合物(红色油,26.46g,65mmol,60%收率)。
[1311]1h-nmr(400mhz,cdcl3)δppm:7.46(d,j=9.2hz,1h),7.33-7.36(m,5h),6.54(d,j=9.2hz,1h),5.72(s,1h),4.51(s,2h),3.49(t,j=6.4hz,2h),3.13-3.18(m,2h),2.45(s,3h),1.64-1.71(m,4h),1.44-1.52(m,2h)。
[1312]
步骤a3:n
1-[5-(苄氧基)戊基]-4-溴-3-甲基苯-1,2-二胺的制备
[1313]
向n-[5-(苄氧基)戊基]-4-溴-3-甲基-2-硝基苯胺(1eq.,316g,776mmol)的etoh(1.9l)和水(950ml)溶液中加入nh4cl(10eq.,415g,7.76mol)。将混合物加热至70℃,然后分小批加入铁(5eq.,217g,3.88mol)并将混合物于80℃加热1小时。将反应混合物冷却至50℃,加入硅藻土并继续搅拌10分钟。将反应混合物通过硅藻土过滤。将滤饼用热etoac洗涤(2x2.5l,50℃)并将滤液减压浓缩。将水层用etoac萃取(3x1.3l),将有机层用盐水洗涤(3x0.5l),用硫酸钠干燥并减压浓缩。向粗产物(250g)中加入石油醚:etoac 10:1(750ml),将混合物于25℃搅拌16小时。滤出沉淀物并将滤饼用石油醚:etoac 10:1(100ml)洗涤,然后真空干燥。得到浅棕色固体状粗产物(161g,427mmol,55%收率)。
[1314]1h-nmr(400mhz,cdcl3)δppm:7.27-7.36(m,5h),7.01(d,j=8.8hz,1h),6.45(d,j=8.4hz,1h),4.52(s,2h),3.47-3.52(m,4h),3.08(t,j=6.8hz,2h),2.32(s,3h),1.65-1.71(m,4h),1.53-1.57(m,2h)。
[1315]
步骤a4:1-[5-(苄氧基)戊基]-5-溴-4-甲基-1h-苯并三唑的制备
[1316]
在室温下向n
1-[5-(苄氧基)戊基]-4-溴-3-甲基苯-1,2-二胺(1eq.,200g,530mmol)的mecn(1.40l)溶液中加入3-甲基丁基亚硝酸酯(2.5eq.,155g,1.33mol)并将混合物搅拌16小时。反应完成后,将混合物减压浓缩。将残余物溶于etoac(1l),用饱和na2so3洗涤(3x340ml),然后将有机层用盐水洗涤(0.5l)。将水层用etoac萃取(2x170ml),将合并的有机层用硫酸钠干燥,过滤并减压浓缩。将粗产物通过正相硅胶色谱纯化,用石油醚/etoac 0至50:1洗脱得到黑色油状标题化合物(134g,346.7mmol,65%收率)。
[1317]1h-nmr(400mhz,cdcl3)δppm:7.49(d,j=8.8hz,1h),7.20-7.26(m,5h),7.12(d,j=8.8hz,1h),4.52(t,j=6.8hz,2h),4.39(s,2h),3.36(t,j=6.4hz,2h),2.76(s,3h),1.92-1.97(m,2h),1.56-1.60(m,2h),1.33-1.37(m,2h)
[1318]
步骤a5:(2e)-3-{1-[5-(苄氧基)戊基]-4-甲基-1h-苯并三唑-5-基}丙-2-烯酸乙酯的制备
[1319]
采用通用方法2步骤5,用1-[5-(苄氧基)戊基]-5-溴-4-甲基-1h-苯并三唑(1当量)作为起始试剂,得到标题化合物(58%收率)。
[1320]1h-nmr(400mhz,cdcl3)δppm:8.14(d,j=16.4hz,1h),7.68(d,j=9.2hz,1h),7.23-7.40(m,5h),6.42(d,j=15.6hz,1h),4.62(t,j=7.2hz,2h),4.40-4.53(m,2h),4.31(q,j=7.2hz,2h),3.45(t,j=6.4hz,2h),2.92(s,3h),2.03(m,2h),1.62-1.76(m,2h),1.40-1.50(m,2h),1.37(t,j=7.2hz,3h)。
[1321]
步骤1:3-{1-[5-(苄氧基)戊基]-4-甲基-1h-苯并三唑-5-基}-3-[3-(1-羟基乙基)-4-甲氧基苯基]丙酸乙酯的制备
羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)乙基]-4-甲氧基苯基}丙酸乙酯(1当量)作为起始试剂,得到标题化合物(定量)。
[1335]1h-nmr(400mhz,dmso-d6)δppm:1.01(t,j=7.03hz,7h)1.25(d,j=7.34hz,4h)1.35(d,j=4.89hz,5h)1.50(d,j=7.09hz,5h)1.55-1.74(m,5h)1.88-1.97(m,3h)2.70-2.78(m,2h)2.81(s,3h)2.86(s,3h)3.01(dd,j=15.53,7.70hz,1h)3.17(ddd,j=15.62,7.61,4.16hz,4h)3.62(s,4h)3.65-3.74(m,6h)3.76-3.84(m,1h)3.92(quin,j=7.24hz,4h)4.01(d,j=2.32hz,2h)4.14(d,j=17.97hz,1h)4.41(d,j=17.61hz,1h)4.70(d,j=6.24hz,4h)4.83(t,j=8.13hz,1h)4.89(t,j=7.58hz,1h)5.42-5.55(m,2h)5.69(d,j=2.69hz,1h)6.11(d,j=2.81hz,1h)6.66-6.77(m,4h)6.85(dd,j=10.88,9.05hz,2h)6.94(d,j=8.68hz,1h)7.01(d,j=1.96hz,1h)7.15-7.20(m,1h)7.26(d,j=8.80hz,1h)7.47-7.54(m,2h)7.59-7.65(m,2h)7.66-7.73(m,2h)。
[1336]
步骤6:实施例31的制备
[1337]
采用通用方法12,用[4-甲氧基-2,32-二甲基-28,28-二氧代-22,27-二氧杂-28λ
6-硫杂-1,14,15,16-四氮杂六环[21.5.3.1
3,7
.1
9,13
.0
12,16
.0
26,30
]三十三碳-3(33),4,6,9(32),10,12,14,23,25,30-十烯-8-基]乙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体,67%收率)。
[1338]
通过手性柱色谱分离得到非对映体纯产物。
[1339]
实施例31a(2s,8s)
[1340]c31h34
n4o7s的hrms计算值:606.2148;[m+h]
+
,实测值:607.2223(δ=0.3ppm)。
[1341]1h-nmr(400mhz,dmso-d6)δppm:7.61(d,1h),7.51(dd,1h),7.21(d,1h),7(d,1h),6.99(d,1h),6.88(d,1h),6.75(dd,1h),5.75(d,1h),5.49(q,1h),4.9(t,1h),4.7(m,2h),4(s,2h),3.81/3.61(2m,2h),3.72(s,3h),3.09/2.88(2dd,2h),2.81(s,3h),2(m,2h),1.65(m,2h),1.38/1.18(2m,2h),1.28(d,3h)。
[1342]
实施例31b(2r,8s)
[1343]c31h34
n4o7s的hrms计算值:606.2148;[m+h]
+
,实测值:607.2221(δ=0.0ppm)。
[1344]1h-nmr(400mhz,dmso-d6)δppm:7.7(s,2h),7.58(d,1h),7.2(dd,1h),6.82(d,1h),6.71(d,1h),6.7(dd,1h),6.1(d,1h),5.5(q,1h),4.81(t,1h),4.7(t,2h),4.39/4.1(2d,2h),3.7(m,2h),3.61(s,3h),3.15/3.05(2dd,2h),2.8(s,3h),2(m,2h),1.7/1.52(2m,2h),1.48(d,3h),1.39/1.18(2m,2h)。
[1345]
实施例31c(2s,8r)
[1346]c31h34
n4o7s的hrms计算值:606.2148;[m+h]
+
,实测值:607.2232(δ=1.8ppm)。
[1347]1h-nmr(400mhz,dmso-d6)δppm:12.07(sl,1h),7.68(s,2h),7.46(d,1h),7.19(dd,1h),6.84(d,1h),6.73(d,1h),6.71(dd,1h),6.09(d,1h),5.5(q,1h),4.81(t,1h),4.7(t,2h),4.38/4.1(2d,2h),3.71(m,2h),3.63(s,3h),3.15/3.05(2dd,2h),2.8(s,3h),1.99(m,2h),1.69/1.53(2m,2h),1.47(d,3h),1.38/1.18(2m,2h)。
[1348]
实施例31d(2r,8r)
[1349]c31h34
n4o7s的hrms计算值:606.2148;[m+h]
+
,实测值:607.2221(δ=0.0ppm)。
[1350]1h-nmr(400mhz,dmso-d6)δppm:12.2(sl,1h),7.61(d,1h),7.53(dd,1h),7.2(d,1h),6.99/6.97(2d,2h),6.87(d,1h),6.75(dd,1h),5.74(d,1h),5.46(q,1h),4.88(t,1h),
4-甲基苯基}-3-[1-(4-羟基丁基)-4-甲基-1h-苯并三唑-5-基]丙酸乙酯的制备
[1366]
采用通用方法8,用3-{1-[4-(苄氧基)丁基]-4-甲基-1h-苯并三唑-5-基}-3-(3-{[6-(苄氧基)-7-氟-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-甲基苯基)丙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体泡沫,95%收率)。
[1367]1h-nmr(500mhz,dmso-d6)δppm:10.17(s,1h),7.62(d,1h),7.52(d,1h),7.26(d,1h),7.2(dd,1h),7.18(d,1h),7.14(d,1h),6.84(d,1h),4.84(t,1h),4.65(t,2h),4.44(brt.,1h),4.4(s,2h),4.25/4.2(d+d,2h),3.94(q,2h),3.38(m,2h),3.18(d,2h),2.77(s,3h),2.22(s,3h),1.9(m,2h),1.36(m,2h),1(t,3h)。
[1368]
步骤3:3-[1-(4-氯丁基)-4-甲基-苯并三唑-5-基]-3-[3-[(7-氟-6-羟基-2,2-二氧代-4h-1,2λ6,3-噁噻嗪-3-基)甲基]-4-甲基-苯基]丙酸乙酯的制备
[1369]
采用通用方法10,用3-{3-[(7-氟-6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}-3-[1-(4-羟基丁基)-4-甲基-1h-苯并三唑-5-基]丙酸乙酯(1当量)作为起始试剂,得到标题化合物(黄色油,定量)。
[1370]1h-nmr(500mhz,dmso-d6)δppm:10.17(s,1h),7.64(d,1h),7.53(d,1h),7.25(d,1h),7.2(dd,1h),7.18(d,1h),7.14(d,1h),6.84(d,1h),4.85(t,1h),4.7(t,2h),4.4(s,2h),4.25/4.19(d+d,2h),3.94(q,2h),3.65(t,2h),3.18(d,2h),2.77(s,3h),2.22(s,3h),1.99(m,2h),1.68(m,2h),1(t,3h)。
[1371]
步骤4:[23-氟-4,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯的制备
[1372]
采用通用方法11,用3-[1-(4-氯丁基)-4-甲基-苯并三唑-5-基]-3-[3-[(7-氟-6-羟基-2,2-二氧代-4h-1,2λ6,3-噁噻嗪-3-基)甲基]-4-甲基-苯基]丙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体泡沫,69%收率)。
[1373]1h-nmr(500mhz,dmso-d6)δppm:7.69(d,1h),7.47(dd,1h),7.47(d,1h),7.27(d,1h),7.2(d,1h),6.64(d,1h),6.1(d,1h),4.83/4.76(m+m,2h),4.78(t,1h),4.24/3.9(d+d,2h),3.99/3.76(d+d,2h),3.92(q,2h),3.7/3.42(m+m,2h),3.14/3.06(dd+dd,2h),2.64(s,3h),2.32(s,3h),2.21/2.01(m+m,2h),1.8/1.62(m+m,2h),1.01(t,3h)。
[1374]
步骤5:实施例32的制备
[1375]
采用通用方法12,用[23-氟-4,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体,55%收率)。
[1376]
通过手性柱色谱分离得到对映体纯产物。
[1377]
实施例32a(e1)
[1378]c29h29
fn4o6s的hrms计算值:580.1792;[m+h]
+
,实测值:581.1863(δ=-0.3ppm)。
[1379]
实施例32b(e2)
[1380]c29h29
fn4o6s的hrms计算值:580.1792;[m+h]
+
,实测值:581.1867(δ=0.4ppm)。
[1381]1h-nmr(500mhz,dmso-d6)δppm:7.68(d,1h),7.48(s,1h),7.45(d,1h),7.27(s,1h),7.2(d,1h),6.61(s,1h),6.08(d,1h),4.84/4.74(m+m,2h),4.75(t,1h),4.23/3.91(d+
d,2h),3.99/3.76(d+d,2h),3.69/3.4(m+m,2h),3.01/2.94(dd+dd,2h),2.63(s,3h),2.31(s,3h),2.22/2.01(m+m,2h),1.81/1.62(m+m,2h)。
[1382]
13
c-nmr(125mhz,dmso-d6)δppm:131.3,131.3,128.8,127.2,112.6,107.9,107.4,68.7,52,48.5,48.2,41.9,41.1,26.8,25.4,16.5,13.4。
[1383]
实施例33:[5-氯-4,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸
[1384][1385]
步骤b1:(5-溴-3-氯-2-甲基苯基)甲醇的制备
[1386]
将5-溴-3-氯-2-甲基-苯甲酸甲酯(1eq.,20.0g,75.9mmol)溶于etoh(500ml),然后于0℃将硼氢化钠(3eq.,8.6g,227.7mmol)加入到搅拌中的混合物中。将混合物在该温度下搅拌10分钟并在30分钟内加入氯化钙(3eq.,25.3g,227.7mmol)。然后将其升温至室温并在室温下搅拌2小时。将反应混合物用冷的1m hcl水溶液淬灭,用etoac萃取,将有机相分离,用硫酸镁干燥,减压浓缩得到白色固体状粗产物(17.0g,95%收率),其不经进一步纯化直接用于下一步骤。
[1387]1h-nmr(400mhz,dmso-d6)δppm:7.58(s,1h),7.53(s,1h),5.42(t,1h),4.52(d,2h),2.21(s,3h)。
[1388]
步骤b2:[3-氯-2-甲基-5-(4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷-2-基)苯基]甲醇的制备
[1389]
采用通用方法3,用(5-溴-3-氯-2-甲基苯基)甲醇(1eq.,20.0g.,84.9mmol)作为反应试剂,得到标题化合物(11.6g,48%收率)。
[1390]1h-nmr(400mhz,dmso-d6)δppm:7.68(d,1h),7.5(d,1h),5.25(t,1h),4.52(d,2h),2.3(s,3h),1.3(s,12h)。
[1391]
步骤1:3-{1-[4-(苄氧基)丁基]-4-甲基-1h-苯并三唑-5-基}-3-[3-氯-5-(羟基甲基)-4-甲基苯基]丙酸乙酯的制备
[1392]
采用通用方法6,用(2e)-3-{1-[4-(苄氧基)丁基]-4-甲基-1h-苯并三唑-5-基}丙-2-烯酸乙酯(1当量)和[3-氯-2-甲基-5-(4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷-2-基)苯基]甲醇(1.1当量)作为起始试剂,得到标题化合物(98%收率)。
[1393]1h-nmr(400mhz,dmso-d6)δppm:7.6(d,1h),7.49(d,1h),7.29(m,7h),5.16(t,1h),4.84(t,1h),4.66(t,2h),4.44(d,2h),4.4(s,2h),3.94(q,2h),3.42(t,2h),3.16(t,2h),2.76(s,3h),2.19(s,3h),1.95(quint,2h),1.5(quint,2h),1(t,3h)。
[1394]
步骤2:3-{1-[4-(苄氧基)丁基]-4-甲基-1h-苯并三唑-5-基}-3-(3-{[6-(苄氧
基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-5-氯-4-甲基苯基)丙酸乙酯的制备
[1395]
采用通用方法7,用3-{1-[4-(苄氧基)丁基]-4-甲基-1h-苯并三唑-5-基}-3-[3-氯-5-(羟基甲基)-4-甲基苯基]丙酸乙酯(1当量)和6-(苄氧基)-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮(1.1当量)作为起始试剂,得到标题化合物(85%收率)。
[1396]1h-nmr(400mhz,dmso-d6)δppm:7.6(d,1h),7.51(d,1h),7.46(d,2h),7.42-7.22(m,10h),7.13(d,1h),7.06(dd,1h),6.93(d,1h),5.1(s,2h),4.85(t,1h),4.63(t,2h),4.44(sl,2h),4.38(s,2h),4.29(sl,2h),3.93(q,2h),3.4(t,2h),3.2(m,2h),2.76(s,3h),2.26(s,3h),1.92(quint,2h),1.48(quint,2h),0.99(t,3h)。
[1397]
步骤3:3-{3-氯-5-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}-3-[1-(4-羟基丁基)-4-甲基-1h-苯并三唑-5-基]丙酸乙酯的制备
[1398]
采用通用方法8,用3-{1-[4-(苄氧基)丁基]-4-甲基-1h-苯并三唑-5-基}-3-(3-{[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-5-氯-4-甲基苯基)丙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体,81%收率)。
[1399]1h-nmr(400mhz,dmso-d6)δppm:9.7/4.41(s+t,2h),7.65(d,1h),7.55(d,1h),7.4/7.28(2d,2h),7(d,1h),6.8(dd,1h),6.6(d,1h),4.85(t,1h),4.65(t,2h),4.41(s,2h),4.28(d,2h),3.95(q,2h),3.38(q,2h),3.2(m,2h),2.78(s,3h),2.29(s,3h),1.9(m,2h),1.39(m,2h),1.02(t,3h)。
[1400]
步骤4:3-[1-(4-溴丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-氯-5-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}丙酸乙酯的制备
[1401]
采用通用方法9,用3-{3-氯-5-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}-3-[1-(4-羟基丁基)-4-甲基-1h-苯并三唑-5-基]丙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体,74%收率)。
[1402]1h-nmr(400mhz,dmso-d6)δppm:9.68(s,1h),7.65/7.55(2d,2h),7.39/7.26(2d,2h),6.99(d,1h),6.78(dd,1h),6.6(d,1h),4.84(t,1h),4.69(t,2h),4.4(s,2h),4.27(d,2h),3.95(q,2h),3.54(t,2h),3.2(t,2h),2.76(s,3h),2.26(s,3h),2(m,2h),1.78(m,2h),1.01(t,3h)。
[1403]
步骤5:[5-氯-4,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯的制备
[1404]
采用通用方法11,用3-[1-(4-溴丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-氯-5-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}丙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体,45%收率)。
[1405]1h-nmr(400mhz,dmso-d6)δppm:7.68/5.88(m+d,2h),7.67/7.43(2d,2h),6.99(d,1h),6.79(dd,1h),6.6(d,1h),4.82-4.73(m,1h),4.79(t,2h),4.19/4.04(2d,2h),3.97/3.86(2d,2h),3.94(m,2h),3.67/3.45(m+dt,2h),3.21/3.06(2dd,2h),2.65(s,3h),2.35(s,3h),2.21/2.06(2m,2h),1.8/1.6(2m,2h),1.02(t,3h)。
[1406]
步骤6:实施例33的制备
[1407]
采用通用方法12,用[5-氯-4,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫
杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体,90%收率)。
[1408]
通过手性柱色谱分离得到对映体纯产物。
[1409]
实施例33a(e1)
[1410]c29h29
cln4o6s的hrms计算值:596.1496;[m+h]
+
,实测值:597.1573(δ=0.7ppm)。
[1411]
实施例33b(e2)
[1412]c29h29
cln4o6s的hrms计算值:596.1496;[m+h]
+
,实测值:597.1571(δ=0.3ppm)。
[1413]1h-nmr(400mhz,dmso-d6)δppm:12.27(s,1h),7.68(s,1h),7.67(d,1h),7.42(d,1h),6.99(d,1h),6.79(dd,1h),6.58(s,1h),5.86(d,1h),4.82-4.72(m,3h),4.18/4.04(2d,2h),3.98/3.85(d,2h),3.66/3.44(m+dt,2h),3.09/2.94(2dd,2h),2.64(s,3h),2.35(s,3h),2.21/2.06(2m,2h),1.81/1.61(2m,2h)。
[1414]
实施例34:[(2r,8s)-2,4,20,33-四甲基-29,29-二氧代-23,28-二氧杂-29λ
6-硫杂-1,14,15,16,20-五氮杂六环[22.5.3.1
3,7
.1
9,13
.0
12,16
.0
27,31
]三十四碳-3(34),4,6,9(33),10,12,14,24,26,31-十烯-8-基]乙酸和
[1415]
[(2r,8r)-2,4,20,33-四甲基-29,29-二氧代-23,28-二氧杂-29λ
6-硫杂-1,14,15,16,20-五氮杂六环[22.5.3.1
3,7
.1
9,13
.0
12,16
.0
27,31
]三十四碳-3(34),4,6,9(33),10,12,14,24,26,31-十烯-8-基]乙酸
[1416][1417]
步骤a1:(3-{[2-(苄氧基)乙基](甲基)氨基}丙基)氨基甲酸叔丁酯的制备
[1418]
在室温下向[(2-溴乙氧基)甲基]苯(10g,46.5mmol,7.35ml)的mecn(3ml/mmol,139ml)溶液中加入[3-(甲基氨基)丙基]氨基甲酸叔丁酯(1eq.,8.75g,46.5mmol)和k2co3(2eq.,9.22g,93mmol)。将反应混合物加热至50℃并搅拌2小时。反应完成后将混合物用500ml etoac稀释,用500ml水洗涤,然后用500ml盐水洗涤。将有机层用无水硫酸钠干燥,过滤,浓缩至干得到无色油状粗产物,其不经进一步纯化直接用于下一步骤(14.5g,77%收率)。
[1419]1h-nmr(400mhz,dmso-d6)δppm:7.38-7.25(m,5h),6.74(t,1h),4.46(s,2h),3.5(t,2h),2.92(q,2h),2.5(m,2h),2.31(t,2h),2.15(s,3h),1.49(quint,2h),1.37(s,9h)。
[1420]
步骤a2:n
1-[2-(苄氧基)乙基]-n
1-甲基-n
3-(3-甲基-2-硝基苯基)丙-1,3-二胺的制备
[1421]
在室温下向(3-{[2-(苄氧基)乙基](甲基)氨基}丙基)氨基甲酸叔丁酯(14.5g,36mmol)的二氧杂环己烷(5ml/mmol,180ml)溶液中加入hcl(4n的二氧杂环己烷溶液)
(4eq.,36ml)。将反应混合物在室温下搅拌过夜。反应完成后将溶剂减压蒸发至干。粗产物n
1-[2-(苄氧基)乙基]-n
1-甲基丙-1,3-二胺盐酸盐(13.3g,68%收率)不经进一步纯化即可与1-氟-3-甲基-2-硝基苯用通用方法2步骤1进行反应,得到标题化合物(78%收率)。
[1422]1h-nmr(400mhz,dmso-d6)δppm:7.39-7.28(m,5h),7.25(dd,1h),6.78(d,1h),6.58(d,1h),6.55(m,1h),4.5(s,2h),3.67(t,2h),3.22(q,2h),2.98(m,2h),2.82(quint,2h),2.82(m,2h),2.5(-,3h),2.29(s,3h)。
[1423]
步骤a3:n
1-[2-(苄氧基)乙基]-n
3-(4-溴-3-甲基-2-硝基苯基)-n
1-甲基丙-1,3-二胺的制备
[1424]
采用通用方法2步骤2,用n
1-[2-(苄氧基)乙基]-n
1-甲基-n
3-(3-甲基-2-硝基苯基)丙-1,3-二胺(1当量)作为起始试剂,得到标题化合物(65%收率)。
[1425]1h-nmr(400mhz,dmso-d6)δppm:7.5(d,1h),7.3(m,5h),6.7(d,1h),6.55(t,1h),4.45(s,2h),3.52(t,2h),3.15(q,2h),2.55(t,2h),2.45(t,2h),2.22/2.2(2s,6h),1.69(m,2h)。
[1426]
步骤a4:n-[2-(苄氧基)乙基]-3-(5-溴-4-甲基-1h-苯并三唑-1-基)-n-甲基丙-1-胺的制备
[1427]
采用通用方法2步骤3,用n
1-[2-(苄氧基)乙基]-n
3-(4-溴-3-甲基-2-硝基苯基)-n
1-甲基丙-1,3-二胺(1当量)作为反应试剂,得到n
1-(3-{[2-(苄氧基)乙基](甲基)氨基}丙基)-4-溴-3-甲基苯-1,2-二胺(76%收率)。将粗产物用通用方法2步骤4进行反应得到标题化合物(定量)。
[1428]1h-nmr(400mhz,dmso-d6)δppm:7.63(m,2h),7.3(m,5h),4.7(t,2h),4.42(s,2h),3.48(t,2h),2.71(s,3h),2.49(t,2h),2.3(t,2h),2.15(s,3h),2.04(q,2h)。
[1429]
步骤a5:(2e)-3-[1-(3-{[2-(苄氧基)乙基](甲基)氨基}丙基)-4-甲基-1h-苯并三唑-5-基]丙-2-烯酸乙酯的制备
[1430]
采用通用方法2步骤5,用n-[2-(苄氧基)乙基]-3-(5-溴-4-甲基-1h-苯并三唑-1-基)-n-甲基丙-1-胺(1当量)作为起始试剂,得到标题化合物(92%收率)。
[1431]1h-nmr(400mhz,dmso-d6)δppm:8.02(d,1h),7.92/7.69(dd,2h),7.36-7.23(m,5h),6.62(d,1h),4.7(t,2h),4.42(s,2h),4.22(q,2h),3.48(t,2h),2.8(s,3h),2.5(m,2h),2.32(t,2h),2.16(s,3h),2.04(m,2h),1.28(t,3h)。
[1432]
步骤1:3-[1-(3-{[2-(苄氧基)乙基](甲基)氨基}丙基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(1s)-1-羟基乙基]-4-甲基苯基}丙酸乙酯的制备
[1433]
采用通用方法6,用(2e)-3-[1-(3-{[2-(苄氧基)乙基](甲基)氨基}丙基)-4-甲基-1h-苯并三唑-5-基]丙-2-烯酸乙酯(1当量)和(1s)-1-[2-甲基-5-(4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷-2-基)苯基]乙醇(1当量)作为起始试剂,得到标题化合物(30%收率)。
[1434]1h-nmr(400mhz,dmso-d6)δppm:7.57/7.44(d,2h),7.4(d,1h),7.35-7.22(d,5h),7.03(d,1h),6.99(dd,1h),4.98(d,1h),4.82(m,1h),4.82(m,1h),4.63(m,2h),4.4(s,2h),3.92(q,2h),3.49(t,2h),3.11(m,2h),2.77(s,3h),2.5(m,2h),2.32(m,2h),2.17(s,3h),2.17(s,3h),2.01(quint,2h),1.22(d,3h),1(t,3h)。
[1435]
步骤2:3-(3-{(1r)-1-[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]
乙基}-4-甲基苯基)-3-[1-(3-{[2-(苄氧基)乙基](甲基)氨基}丙基)-4-甲基-1h-苯并三唑-5-基]丙酸乙酯的制备
[1436]
采用通用方法7,用3-[1-(3-{[2-(苄氧基)乙基](甲基)氨基}丙基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(1s)-1-羟基乙基]-4-甲基苯基}丙酸乙酯(1当量)和6-(苄氧基)-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮(1.1当量)作为起始试剂,得到标题化合物(92%收率)。
[1437]1h-nmr(400mhz,dmso-d6)δppm:0.97(td,j=7.06,4.95hz,2h)1.41(d,j=6.97hz,2h)2.12(d,j=2.93hz,4h)2.21-2.32(m,4h)2.76(d,j=3.79hz,2h)3.11-3.25(m,2h)3.44(d,j=4.28hz,1h)3.92(d,j=7.09hz,1h)4.38(d,j=4.65hz,3h)4.60(s,1h)4.79-4.95(m,1h)4.98-5.17(m,2h)5.20-5.35(m,1h)6.77-7.65(m,14h)。
[1438]
步骤3:3-{3-[(1r)-1-(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)乙基]-4-甲基苯基}-3-(1-{3-[(2-羟基乙基)(甲基)氨基]丙基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯的制备
[1439]
采用通用方法8,用3-(3-{(1r)-1-[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]乙基}-4-甲基苯基)-3-[1-(3-{[2-(苄氧基)乙基](甲基)氨基}丙基)-4-甲基-1h-苯并三唑-5-基]丙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体,95%收率)。
[1440]1h-nmr(400mhz,dmso-d6)δppm:9.64(s,1h),7.62/7.56(2d+2d,2h),7.46(2s,1h),7.11(m,2h),6.91(2d,1h),6.72(m,1h),6.57(2d,1h),5.25(q,1h),4.87(q,1h),4.66(t,2h),4.36-4.25(m,3h),3.94(2q,2h),3.43(t,2h),3.22(d,2h),2.76(s,3h),2.35(2t,2h),2.31-2.27(m,2h),2.27(s,3h),2.12(2s,3h),2(q,2h),1.42(2d,3h),1(2t,3h)。
[1441]
步骤4:3-(1-{3-[(2-氯乙基)(甲基)氨基]丙基}-4-甲基-1h-苯并三唑-5-基)-3-{3-[(1r)-1-(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)乙基]-4-甲基苯基}丙酸乙酯盐酸盐的制备
[1442]
采用通用方法10,用3-{3-[(1r)-1-(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)乙基]-4-甲基苯基}-3-(1-{3-[(2-羟基乙基)(甲基)氨基]丙基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体,90%收率)。
[1443]1h-nmr(400mhz,dmso-d6)δppm:10.32(2sl,1h),9.7(sl,1h),7.74-7.62(d,2h),7.5(s,1h),7.13-7.08(m,2h),6.92(d,1h),6.74(t,1h),6.66/6.57(d,1h),5.26(quint,1h),4.89(q,1h),4.75(q,2h),4.35(d,2h),3.96(q,4h),3.94(t,2h),3.54-3.38(m,2h),3.3-3.11(m,4h),2.77(m,6h),2.36-2.26(m,2h),2.3(s,3h),1.43(t,3h),1.04(2t,3h)。
[1444]
步骤5:[(2r)-2,4,20,33-四甲基-29,29-二氧代-23,28-二氧杂-29λ
6-硫杂-1,14,15,16,20-五氮杂六环[22.5.3.1
3,7
.1
9,13
.0
12,16
.0
27,31
]三十四碳-3(34),4,6,9(33),10,12,14,24,26,31-十烯-8-基]乙酸乙酯的制备
[1445]
采用通用方法11,用3-(1-{3-[(2-氯乙基)(甲基)氨基]丙基}-4-甲基-1h-苯并三唑-5-基)-3-{3-[(1r)-1-(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)乙基]-4-甲基苯基}丙酸乙酯盐酸盐(1当量)作为起始试剂,得到标题化合物(白色固体,96%收率)。
[1446]1h-nmr(400mhz,dmso-d6)δppm:7.85/7.71(dd,1h),7.63/7.06(dd,1h),7.56/6.85(d,1h),7.45/7.31(dd,1h),7.28/7.11(d,1h),7.05/6.98(d,1h),6.91/6.82(dd,1h),
6.28/6.06(d,1h),5.34-5.21(m,1h),4.95/4.88(t,1h),4.83-4.53(m,2h),4.12/4.03/3.78/3.66(2dd,2h),4.03-3.73(m,2h),3.91(q,2h),3.4-2.91(2ddd,2h),2.83/2.81(2s,3h),2.72-2.38(m,4h),2.35-2.03(m,2h),2.32/2.3/2.27(3s,6h),1.5/1.15(2d,3h),1.03/1(2t,3h)。
[1447]
步骤6:实施例34的制备
[1448]
采用通用方法12,用[(2r)-2,4,20,33-四甲基-29,29-二氧代-23,28-二氧杂-29λ
6-硫杂-1,14,15,16,20-五氮杂六环[22.5.3.1
3,7
.1
9,13
.0
12,16
.0
27,31
]三十四碳-3(34),4,6,9(33),10,12,14,24,26,31-十烯-8-基]乙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体,68%收率)。
[1449]
通过手性柱色谱分离得到非对映体纯产物。
[1450]
实施例34a(2r,8s)
[1451]c32h37
n5o6s的hrms计算值:619.2464;[m+h]
+
,实测值:620.2536(δ=-0.2ppm)。
[1452]1h-nmr(400mhz,dmso-d6)δppm:12.1(m,1h),7.83/7.71(d,2h),7.54(d,1h),7.31(dd,1h),7.11(d,1h),7.04(d,1h),6.91(dd,1h),6.28(d,1h),5.31(q,1h),4.85(t,1h),4.82-4.68(m,2h),4.11/3.65(dd,2h),3.99(t,2h),3.22/3.05(2dd,2h),2.85-2.44(m,4h),2.82(s,3h),2.3/2.28(2s,6h),2.12(m,2h),1.49(d,3h)。
[1453]
实施例34b(2r,8r)
[1454]c32h37
n5o6s的hrms计算值:619.2464;[m+h]
+
,实测值:620.2536(δ=-0.2ppm)。
[1455]1h-nmr(400mhz,dmso-d6)δppm:12.3(m,1h),7.62/7.3(dd,1h),7.46(dd,1h),7.03(d,1h),6.98(d,1h),6.84(d,1h),6.83(dd,1h),6.07(d,1h),5.27(q,1h),4.93(t,1h),4.74/4.58(2m,2h),4.03/3.77(dd,2h),3.88-3.75(m,2h),3.15/2.83(2dd,2h),2.81(s,3h),2.68(m,2h),2.54(m,2h),2.33/2.3(2s,3h),2.2(m,2h),1.15(d,3h)。
[1456]
实施例35:[4,5-二甲氧基-31-甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸
[1457][1458]
步骤b1:[2,3-二甲氧基-5-(4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷-2-基)苯基]甲醇的制备
[1459]
采用通用方法3,用(5-溴-2,3-二甲氧基苯基)甲醇(1eq.,18.0g.,72.9mmol)作为反应试剂,得到标题化合物(11.10g,52%收率)。
[1460]1h-nmr(400mhz,dmso-d6)δppm:7.4(sl,1h),7.13(sl,1h),5.04(t,1h),4.5(d,2h),3.81/3.73(2s,6h),1.29(s,12h)。
[1461]
步骤1:3-{1-[4-(苄氧基)丁基]-4-甲基-1h-苯并三唑-5-基}-3-[3-(羟基甲基)-4,5-二甲氧基苯基]丙酸乙酯的制备
[1462]
采用通用方法6,用(2e)-3-{1-[4-(苄氧基)丁基]-4-甲基-1h-苯并三唑-5-基}丙-2-烯酸乙酯(1当量)和[2,3-二甲氧基-5-(4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷-2-基)苯基]甲醇(1当量)作为起始试剂,得到标题化合物(61%收率)。
[1463]1h-nmr(400mhz,dmso-d6)δppm:7.6/7.52(2d,2h),7.33-7.23(m,5h),6.95(d,1h),6.88(d,1h),4.93(t,1h),4.83(t,1h),4.66(t,2h),4.42(d,2h),4.4(m,2h),3.93(q,2h),3.77/3.63(2s,6h),3.42(t,2h),3.16(d,2h),2.78(s,3h),1.94(quint,2h),1.5(quint,2h),0.99(t,3h)。
[1464]
步骤2:3-{1-[4-(苄氧基)丁基]-4-甲基-1h-苯并三唑-5-基}-3-(3-{[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4,5-二甲氧基苯基)丙酸乙酯的制备
[1465]
采用通用方法7,用3-{1-[4-(苄氧基)丁基]-4-甲基-1h-苯并三唑-5-基}-3-[3-(羟基甲基)-4,5-二甲氧基苯基]丙酸乙酯(1当量)和6-(苄氧基)-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮(1.1当量)作为起始试剂,得到标题化合物(97%收率)。
[1466]1h-nmr(400mhz,dmso-d6)δppm:7.6(d,1h),7.52(d,1h),7.48-7.2(m,10h),7.02(m,3h),6.92(d,1h),6.88(d,1h),5.09(s,2h),4.82(t,1h),4.62(t,2h),4.5(s,2h),4.39(s,2h),4.2(s,2h),3.92(q,2h),3.78(s,3h),3.61(s,3h),3.4(t,2h),3.19(m,2h),2.79(s,3h),1.91(m,2h),1.49(m,2h),0.99(t,3h)。
[1467]
步骤3:3-[1-(4-羟基丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4,5-二甲氧基苯基}丙酸乙酯的制备
[1468]
采用通用方法8,用3-{1-[4-(苄氧基)丁基]-4-甲基-1h-苯并三唑-5-基}-3-(3-{[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4,5-二甲氧基苯基)丙酸乙酯(1当量)作为起始试剂,得到标题化合物(87%收率)。
[1469]1h-nmr(400mhz,dmso-d6)δppm:9.65/4.85(s+t,2h),7.62(d,1h),7.58(d,1h),7.02(d,1h),6.91(d,1h),6.88(d,1h),6.8(m,1h),6.75(dd,1h),4.66(t,2h),4.45(s,2h),4.41(m,1h),4.2(m,2h),3.95(q,2h),3.78(s,3h),3.68(s,3h),3.4(t,2h),3.2(dd,2h),2.8(s,3h),1.91(m,2h),1.39(m,2h),1(t,3h)。
[1470]
步骤4:3-[1-(4-溴丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4,5-二甲氧基苯基}丙酸乙酯的制备
[1471]
采用通用方法9,用3-[1-(4-羟基丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4,5-二甲氧基苯基}丙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体,91%收率)。
[1472]1h-nmr(400mhz,dmso-d6)δppm:9.63(s,1h),7.65(d,1h),7.58(d,1h),7.02(d,1h),6.91(d,1h),6.86(d,1h),6.74(dd,1h),6.6(d,1h),4.84(t,1h),4.69(t,2h),4.45(sl,2h),4.2/4.15(2d,2h),3.94(q,2h),3.76(s,3h),3.63(s,3h),3.54(t,2h),3.19(dd,2h),2.79(s,3h),2(m,2h),1.77(m,2h),1(t,3h)。
[1473]
步骤5:[4,5-二甲氧基-31-甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,
22,24,29-十烯-8-基]乙酸乙酯的制备
[1474]
采用通用方法11,用3-[1-(4-溴丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4,5-二甲氧基苯基}丙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体,70%收率)。
[1475]1h-nmr(400mhz,dmso-d6)δppm:7.68(d,1h),7.47(d,1h),7.34(d,1h),6.97(d,1h),6.79(dd,1h),6.11(d,1h),5.85(d,1h),4.83-4.72(m,3h),4.09-3.63(m,6h),3.92(s,3h),3.76(s,3h),3.69/3.47(2m,2h),3.25/3.09(2dd,2h),2.65(s,3h),2.21/2.07(2m,2h),1.81/1.63(2m,2h),1(t,3h)。
[1476]
步骤6:实施例35的制备
[1477]
采用通用方法12,用[4,5-二甲氧基-31-甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯(1当量)作为起始试剂,得到标题化合物(97%收率)。
[1478]
通过手性柱色谱分离得到对映体纯产物。
[1479]
实施例35a(e2)
[1480]c30h32
n4o8s的hrms计算值:608.1941;[m+h]
+
,实测值:609.2013(δ=-0.1ppm)。
[1481]
实施例35b(e1)
[1482]c30h32
n4o8s的hrms计算值:608.1941;[m+h]
+
,实测值:609.2013(δ=-0.1ppm)。
[1483]1h-nmr(400mhz,dmso-d6)δppm:12.15(m,1h),7.7(d,1h),7.49(d,1h),7.38(d,1h),6.99(d,1h),6.8(dd,1h),6.1(d,1h),5.82(d,1h),4.8(m,3h),4.1(2d,2h),3.92/3.75(2s,6h),3.91/3.85(2d,2h),3.7/3.45(2m,2h),3.15/3(2dd,2h),2.65(s,3h),2.2/2.1(2m,2h),1.82/1.65(2m,2h)。
[1484]
实施例36:[4-氯-5,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸
[1485][1486]
步骤b1:(5-溴-2-氯-3-甲基苯基)甲醇的制备
[1487]
于0℃下将5-溴-2-氯-3-甲基苯甲酸甲酯(1eq.,24.0g,91mmol)溶于etoh(300ml),然后将硼氢化钠(3eq.,10.4g,273mmol)加入到搅拌中的混合物中。将混合物在该温度下搅拌10分钟,然后在30分钟内加入氯化钙(3eq.,30.3g,273mmol),然后升温至室温并搅拌2小时。将反应混合物用冷的1m hcl水溶液淬灭,用etoac萃取,将有机相分离,用硫酸镁干燥,减压浓缩得到白色固体状粗产物(19.0g,88%收率),其不经进一步纯化直接用
于下一步骤。
[1488]1h-nmr(400mhz,dmso-d6)δppm:7.51(s,2h),5.54(t,1h),4.53(d,2h),2.32(s,3h)。
[1489]
步骤b2:[2-氯-3-甲基-5-(4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷-2-基)苯基]甲醇的制备
[1490]
采用通用方法3,用(5-溴-2-氯-3-甲基苯基)甲醇(1eq.,19.0g.,80.7mmol)作为起始试剂,得到标题化合物(15.15g,66%收率)。
[1491]1h-nmr(400mhz,dmso-d6)δppm:7.78(d,1h),7.51(d,1h),5.4(t,1h),4.55(d,2h),2.32(s,3h),1.3(s,12h)。
[1492]
步骤1:3-[4-氯-3-(羟基甲基)-5-甲基苯基]-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯的制备
[1493]
采用通用方法6,用(2e)-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙-2-烯酸乙酯(1当量)和[2-氯-3-甲基-5-(4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷-2-基)苯基]甲醇(1.5当量)作为起始试剂,得到标题化合物(黄色油,50%收率)。
[1494]1h-nmr(400mhz,dmso-d6)δppm:7.6(d,1h),7.45(d,1h),7.3/7.25(2d,2h),7.2(d,2h),6.9(d,2h),5.3(t,1h),4.85(t,1h),4.65(t,2h),4.5(d,2h),4.3(s,2h),3.95(q,2h),3.75(s,3h),3.4(t,2h),3.2(2dd,2h),2.8(s,3h),2.3(s,3h),1.9(quint,2h),1.5(quint,2h),1(t,3h)。
[1495]
步骤2:3-(3-{[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-氯-5-甲基苯基)-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯的制备
[1496]
采用通用方法7,用3-[4-氯-3-(羟基甲基)-5-甲基苯基]-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯(1当量)和6-(苄氧基)-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮(1.1当量)作为起始试剂,得到标题化合物(91%收率)。
[1497]1h-nmr(400mhz,dmso-d6)δppm:7.6/7.5(2d,2h),7.45(dl,2h),7.4(t,2h),7.35(m,3h),7.2(d,2h),7.1(d+dd,2h),6.95(d,1h),6.85(d,2h),5.1(s,2h),4.9(t,1h),4.6(t,2h),4.55(sl,2h),4.35(sl,2h),4.3(s,2h),3.9(q,2h),3.7(s,3h),3.4(t,2h),3.2(2dd,2h),2.8(s,3h),2.3(s,3h),1.9(quint,2h),1.15(quint,2h),1(t,3h)。
[1498]
步骤3:3-[4-氯-3-[(6-羟基-2,2-二氧代-4h-1,2λ6,3-噁噻嗪-3-基)甲基]-5-甲基-苯基]-3-[1-(4-羟基丁基)-4-甲基-苯并三唑-5-基]丙酸乙酯的制备
[1499]
采用通用方法8,用3-(3-{[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-氯-5-甲基苯基)-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯(1当量)作为起始试剂,得到标题化合物(97%收率)。
[1500]1h-nmr(400mhz,dmso-d6)δppm:9.6(m,1h),7.6(d,1h),7.5(d,1h),7.3(2d,2h),6.95(d,1h),6.8(dd,1h),6.6(d,1h),4.95(t,1h),4.65(t,2h),4.5(sl,2h),4.4(m,1h),4.3(sl,2h),3.95(q,2h),3.4(m,2h),3.2(m,2h),2.8(s,3h),2.3(s,3h),1.9(quint,2h),1.4(quint,2h),1(t,3h)。
[1501]
步骤4:3-[1-(4-溴丁基)-4-甲基-1h-苯并三唑-5-基]-3-{4-氯-3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-5-甲基苯基}丙酸乙酯的制备
[1502]
采用通用方法9,用3-[4-氯-3-[(6-羟基-2,2-二氧代-4h-1,2λ6,3-噁噻嗪-3-基)甲基]-5-甲基-苯基]-3-[1-(4-羟基丁基)-4-甲基-苯并三唑-5-基]丙酸乙酯(1当量)作为起始试剂,得到标题化合物(70%收率)。
[1503]1h-nmr(400mhz,dmso-d6)δppm:9.66(s,1h),7.65(d,1h),7.53(d,1h),7.33(2d,2h),6.96(d,1h),6.77(dd,1h),6.61(d,1h),4.85(t,1h),4.69(t,2h),4.5(s,2h),4.32(m,2h),3.95(q,2h),3.54(t,2h),3.19(dd,2h),2.78(s,3h),2.28(s,3h),2(m,2h),1.77(m,2h),1.01(t,3h)。
[1504]
步骤5:[4-氯-5,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯的制备
[1505]
采用通用方法11,用3-[1-(4-溴丁基)-4-甲基-1h-苯并三唑-5-基]-3-{4-氯-3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-5-甲基苯基}丙酸乙酯(1当量)作为起始试剂,得到标题化合物(无色固体,85%收率)。
[1506]1h-nmr(400mhz,dmso-d6)δppm:7.7(d,1h),7.62(s,1h),7.45(d,1h),7(s,1h),6.8(dd,1h),6.7(s,1h),6.6(s,1h),4.8(t,2h),4.8(t,1h),4.25/3.8(d,2h),4.05(d,2h),3.92(q,2h),3.7/3.45(m,2h),3.2/3.1(dd,2h),2.65(s,3h),2.4(s,3h),2.2-2(m,2h),1.8/1.65(m,2h),1(t,3h)。
[1507]
步骤6:实施例36的制备
[1508]
采用通用方法12,用[4-氯-5,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯(1当量)作为起始试剂,得到标题化合物(78%收率)。
[1509]
通过手性柱色谱分离得到对映体纯产物。
[1510]
实施例36a(e1)
[1511]c29h29
cln4o6s的hrms计算值:596.1496;[m+h]
+
,实测值:597.1574(δ=0.8ppm)。
[1512]
实施例36b(e2)
[1513]c29h29
cln4o6s的hrms计算值:596.1496;[m+h]
+
,实测值:597.1573(δ=0.7ppm)。
[1514]1h-nmr(400mhz,dmso-d6)δppm:12.3(m,1h),7.7(d+d,2h),7.45(d,1h),7(d,1h),6.8(dd,1h),6.6(d,1h),5.8(d,1h),4.8(m,3h),4.25/4(d,2h),4/3.8(d,2h),3.65/3.4(m,2h),3.1/2.95(dd,2h),2.65(sl,3h),2.4(s,3h),2.2/2.1(m,2h),1.8/1.65(m,2h)。
[1515]
实施例37:[5-氯-4-甲氧基-31-甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸
[1516][1517]
步骤b1:[3-氯-2-甲氧基-5-(4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷-2-基)苯基]甲醇的制备
[1518]
采用通用方法3,用(5-溴-3-氯-2-甲氧基-苯基)甲醇(1eq.,17.0g.,67.6mmol)作为起始试剂,得到标题化合物(11g,55%收率)。
[1519]1h-nmr(400mhz,dmso-d6)δppm:7.73(d,1h),7.54(d,1h),5.26(t,1h),4.56(d,2h),3.78(s,3h),1.29(s,12h)。
[1520]
步骤1:3-{1-[4-(苄氧基)丁基]-4-甲基-1h-苯并三唑-5-基}-3-[3-氯-5-(羟基甲基)-4-甲氧基苯基]丙酸乙酯的制备
[1521]
采用通用方法6,用(2e)-3-{1-[4-(苄氧基)丁基]-4-甲基-1h-苯并三唑-5-基}丙-2-烯酸乙酯(1当量)和[3-氯-2-甲氧基-5-(4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷-2-基)苯基]甲醇(1.05当量)作为起始试剂,得到标题化合物(60%收率)。
[1522]1h-nmr(400mhz,dmso-d6)δppm:7.61(d,1h),7.5(d,1h),7.38-7.2(m,7h),5.18(t,1h),4.82(t,1h),4.68(t,2h),4.49(d,2h),4.4(s,2h),3.92(q,2h),3.7(s,3h),3.41(t,2h),3.18(m,2h),2.77(s,3h),1.95(m,2h),1.5(m,2h),1(t,3h)。
[1523]
步骤2:3-{1-[4-(苄氧基)丁基]-4-甲基-1h-苯并三唑-5-基}-3-(3-{[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-5-氯-4-甲氧基苯基)丙酸乙酯的制备
[1524]
采用通用方法7,用3-{1-[4-(苄氧基)丁基]-4-甲基-1h-苯并三唑-5-基}-3-[3-氯-5-(羟基甲基)-4-甲氧基苯基]丙酸乙酯(1当量)和6-(苄氧基)-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮(1.1当量)作为起始试剂,得到标题化合物(97%收率)。
[1525]1h-nmr(400mhz,dmso-d6)δppm:7.62(d,1h),7.54(d,1h),7.45-7.25(m,12h),7.03(m,2h),6.96(d,1h),5.08(s,2h),4.85(t,1h),4.65(t,2h),4.57(s,2h),4.39(s,2h),4.29(s,2h),3.94(q,2h),3.7(s,3h),3.41(t,2h),3.2(dd,2h),2.77(s,3h),1.93(quint,2h),1.49(quint,2h),0.99(t,3h)。
[1526]
步骤3:3-{3-氯-5-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲氧基苯基}-3-[1-(4-羟基丁基)-4-甲基-1h-苯并三唑-5-基]丙酸乙酯的制备
[1527]
采用通用方法8,用3-{1-[4-(苄氧基)丁基]-4-甲基-1h-苯并三唑-5-基}-3-(3-{[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-5-氯-4-甲氧基苯基)丙酸乙酯(1当量)作为起始试剂,得到标题化合物(80%收率)。
[1528]1h-nmr(400mhz,dmso-d6)δppm:9.69(sl,1h),7.65(d,1h),7.56(d,1h),7.43/7.35(2d,2h),6.92(d,1h),6.75(dd,1h),6.62(d,1h),4.85(t,1h),4.66(t,2h),4.52(s,2h),4.27(s,2h),3.95(q,2h),3.71(s,3h),3.39(t,2h),3.2(d,2h),2.77(s,3h),1.91
(quint,2h),1.37(quint,2h),1.01(t,3h)。
[1529]
步骤4:3-[1-(4-溴丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-氯-5-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲氧基苯基}丙酸乙酯的制备
[1530]
采用通用方法9,用3-{3-氯-5-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲氧基苯基}-3-[1-(4-羟基丁基)-4-甲基-1h-苯并三唑-5-基]丙酸乙酯(1当量)作为起始试剂,得到标题化合物(89%收率)。
[1531]1h-nmr(400mhz,dmso-d6)δppm:9.65(s,1h),7.67(d,1h),7.57(d,1h),7.43/7.35(2d,2h),6.92(d,1h),6.75(dd,1h),6.62(d,1h),4.85(t,1h),4.7(t,2h),4.52/4.27(2s,4h),3.94(q,2h),3.71(s,3h),3.54(t,2h),3.2(d,2h),2.77(s,3h),2(m,2h),1.78(m,2h),1(t,3h)。
[1532]
步骤5:[5-氯-4-甲氧基-31-甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯的制备
[1533]
采用通用方法11,用3-[1-(4-溴丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-氯-5-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲氧基苯基}丙酸乙酯(1当量)作为起始试剂,得到标题化合物(61%收率)。
[1534]1h-nmr(400mhz,dmso-d6)δppm:7.75(d,1h),7.68(d,1h),7.44(d,1h),6.98(d,1h),6.79(dd,1h),6.63(d,1h),5.93(d,1h),4.79(m,3h),4.14/4.03(2d,2h),4-3.9(m,4h),3.83(s,3h),3.73/3.53(m+dt,2h),3.26/3.07(2dd,2h),2.66(s,3h),2.2/2.06(2m,2h),1.78/1.59(2m,2h),1(t,3h)。
[1535]
步骤6:实施例37的制备
[1536]
采用通用方法12,用[5-氯-4-甲氧基-31-甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体,定量)。
[1537]
通过手性柱色谱分离得到对映体纯产物。
[1538]
实施例37a(e1)
[1539]c29h29
cln4o7s的hrms计算值:612.1445;[m+h]
+
,实测值:613.1523(δ=0.8ppm)。
[1540]
实施例37b(e2)
[1541]c29h29
cln4o7s的hrms计算值:612.1445;[m+h]
+
,实测值:613.1524(δ=0.9ppm)。
[1542]1h-nmr(400mhz,dmso-d6)δppm:12.25(m,1h),7.75(d,1h),7.68(d,1h),7.43(d,1h),7(d,1h),6.8(dd,1h),6.62(d,1h),5.92(d,1h),4.79(m,3h),4.13/4.03(2d,2h),4.02-3.92(dd,2h),3.82(s,3h),3.72/3.52(m+dt,2h),3.12/2.98(2dd,2h),2.65(s,3h),2.21/2.08(2m,2h),1.79/1.6(2m,2h)。
[1543]
实施例38:[4-氯-5-甲氧基-31-甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸
[1544][1545]
步骤b1:[2-氯-3-甲氧基-5-(4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷-2-基)苯基]甲醇的制备
[1546]
采用通用方法3,用(5-溴-2-氯-3-甲氧基苯基)甲醇(1eq.,20.0g.,79.5mmol)作为反应试剂,得到标题化合物(14.6g,62%收率)。
[1547]1h-nmr(400mhz,dmso-d6)δppm:7.52(d,1h),7.19(d,1h),5.4(t,1h),4.55(d,2h),3.89(s,3h),1.3(s,12h)。
[1548]
步骤1:3-[4-氯-3-(羟基甲基)-5-甲氧基苯基]-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯的制备
[1549]
采用通用方法6,用3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯(1当量)和[2-氯-3-甲氧基-5-(4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷-2-基)苯基]甲醇(1.5当量)作为起始试剂,得到标题化合物(黄色油,57%收率)。
[1550]1h-nmr(400mhz,dmso-d6)δppm:7.6(d,1h),7.51(d,1h),7.2(d,2h),7.07/7.02(2d,2h),6.88(d,2h),5.28(t,1h),4.89(t,1h),4.63(t,2h),4.47(d,2h),4.3(s,2h),3.92(q,2h),3.81(s,3h),3.71(s,3h),3.39(t,2h),3.2(d,2h),2.79(s,3h),1.91(m,2h),1.49(m,2h),1(t,3h)。
[1551]
步骤2:3-(3-{[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-氯-5-甲氧基苯基)-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯的制备
[1552]
采用通用方法7,用3-[4-氯-3-(羟基甲基)-5-甲氧基苯基]-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯(1当量)和6-(苄氧基)-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮(1.1当量)作为起始试剂,得到标题化合物(89%收率)。
[1553]1h-nmr(400mhz,dmso-d6)δppm:7.59(d,1h),7.55(d,1h),7.46-7.32(m,5h),7.18(d,2h),7.14(d,1h),7.1-7.02(m,3h),6.93(d,1h),6.85(d,2h),5.08(s,2h),4.9(t,1h),4.62(t,2h),4.53(s,2h),4.31(s,2h),4.3(s,2h),3.94(q,2h),3.83(s,3h),3.72(s,3h),3.36(t,2h),3.23(d,2h),2.8(s,3h),1.9(quint,2h),1.46(m,2h),1(t,3h)。
[1554]
步骤3:3-{4-氯-3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-5-甲氧基苯基}-3-[1-(4-羟基丁基)-4-甲基-1h-苯并三唑-5-基]丙酸乙酯的制备
[1555]
采用通用方法8,用3-(3-{[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-氯-5-甲氧基苯基)-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯(1当量)作为起始试剂,得到标题化合物(97%收率)。
[1556]1h-nmr(400mhz,dmso-d6)δppm:9.67(s,2h),7.62(d,1h),7.57(d,1h),7.12(d,1h),7.01(dd,1h),6.94(d,1h),6.78(dd,1h),6.6(d,1h),4.9(t,1h),4.64(t,2h),4.49(s,
2h),4.4(t,1h),4.29(m,2h),3.93(q,2h),3.8(t,2h),3.39(m,3h),3.21(d,3h),2.79(s,2h),1.9(m,2h),1.37(m,2h),1(t,3h)。
[1557]
步骤4:3-[1-(4-溴丁基)-4-甲基-1h-苯并三唑-5-基]-3-{4-氯-3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-5-甲氧基苯基}丙酸乙酯的制备
[1558]
采用通用方法9,用3-{4-氯-3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-5-甲氧基苯基}-3-[1-(4-羟基丁基)-4-甲基-1h-苯并三唑-5-基]丙酸乙酯(1当量)作为起始试剂,得到标题化合物(76%收率)。
[1559]1h-nmr(400mhz,dmso-d6)δppm:9.66(s,1h),7.65(d,1h),7.59(d,1h),7.14(d,1h),7.02(d,1h),6.95(d,1h),6.76(dd,1h),6.59(d,1h),4.89(t,1h),4.69(t,2h),4.48(s,2h),4.29(m,2h),3.95(q,2h),3.83(s,3h),3.53(t,2h),3.23(d,2h),2.8(s,3h),2(m,2h),1.77(m,2h),1.01(t,3h)。
[1560]
步骤5:[4-氯-5-甲氧基-31-甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯的制备
[1561]
采用通用方法11,用3-[1-(4-溴丁基)-4-甲基-1h-苯并三唑-5-基]-3-{4-氯-3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-5-甲氧基苯基}丙酸乙酯(1当量)作为起始试剂,得到标题化合物(72%收率)。
[1562]1h-nmr(400mhz,dmso-d6)δppm:7.69(d,1h),7.47(d,1h),7.44/6.31(2d,2h),6.98(d,1h),6.79(dd,1h),5.81(d,1h),4.85(m,1h),4.77(m,2h),4.23(d,4h),4.07-3.8(m,4h),3.98(s,3h),3.66/3.42(m+dt,2h),3.26/3.11(2dd,2h),2.65(s,3h),2.2/2.08(2m,2h),1.82/1.65(2m,2h),1.01(t,3h)。
[1563]
步骤6:实施例38的制备
[1564]
采用通用方法12,用[4-氯-5-甲氧基-31-甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体,66%收率)。
[1565]
通过手性柱色谱分离得到对映体纯产物。
[1566]
实施例38a(e1)
[1567]c29h29
cln4o7s的hrms计算值:612.1445;[m+h]
+
,实测值:613.1522(δ=0.6ppm)。
[1568]
实施例38b(e2)
[1569]c29h29
cln4o7s的hrms计算值:612.1445;[m+h]
+
,实测值:613.1522(δ=0.6ppm)。
[1570]1h-nmr(400mhz,dmso-d6)δppm:12.3(m,1h),7.7(d,1h),7.5(m,2h),7(d,1h),6.8(dd,1h),6.3(d,1h),5.8(d,1h),4.8(m,3h),4.25/3.95(2d,2h),4.1/3.8(2d,2h),4(s,3h),3.65/3.4(m,2h),3.15/3(2dd,2h),2.7(sl,3h),2.2/2.1(2m,2h),1.85/1.65(m,2h)。
[1571]
实施例39:[4,26,31-三甲基-27,27-二氧代-21-氧杂-27λ
6-硫杂-1,14,15,16,26-五氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸
[1572][1573]
步骤c1:[5-(苄氧基)-2-硝基苯基]甲醇的制备
[1574]
将3-(羟基甲基)-4-硝基苯酚(1eq.,4.15g,24.5mmol)溶于dmf(75ml),加入nah(1.1eq.,1.08g,27.0mmol)并将混合物在室温下搅拌15分钟。冷却至0℃后滴加(溴甲基)苯(1eq.,2.92ml,4.20g,24.6mmol)并将反应混合物在室温下搅拌过夜。反应完成后将混合物减压浓缩,将残余物用水处理,将沉淀析出的固体过滤,用水洗涤并干燥得到黄色固体状标题化合物(5.77g,91%收率),其不经进一步纯化直接用于下一步骤。
[1575]1h-nmr(500mhz,dmso-d6)δppm:8.14(d,1h),7.52-7.31(m,5h),7.44(d,1h),7.11(dd,1h),5.59(t,1h),5.26(s,2h),4.85(d,2h)。
[1576]
步骤c2:2-{[5-(苄氧基)-2-硝基苯基]甲基}-1h-异吲哚-1,3(2h)-二酮的制备
[1577]
将[5-(苄氧基)-2-硝基苯基]甲醇(1eq.,5.76g,22.2mmol)溶于thf(250ml),加入1h-异吲哚-1,3(2h)-二酮(1eq.,3.27g,22.2mmol)和pph3(2eq.,11.65g,44.42mmol)并将该溶液冷却至5-10℃。滴加diad(2eq.,8.75ml,8.99g,44.4mmol)并将混合物在室温下搅拌1小时。减压浓缩后,将残余物通过正相硅胶色谱纯化,用dcm-meoh(100:0至95:5)作为洗脱剂得到标题化合物(2.89g,34%收率),为黄白色固体。
[1578]1h-nmr(500mhz,dmso-d6)δppm:8.21(d,1h),7.95-7.85(m,4h),7.37-7.25(m,5h),7.19(dd,1h),6.87(d,1h),5.17(s,2h),5.09(s,2h)。
[1579]
步骤c3:1-[5-(苄氧基)-2-硝基苯基]甲胺的制备
[1580]
将2-{[5-(苄氧基)-2-硝基苯基]甲基}-1h-异吲哚-1,3(2h)-二酮(1eq.,2.89g,7.44mmol)溶于etoh(6ml)。加入水合肼(5eq.,1.81ml,1.86g,37.38mmol)并将反应混合物于50℃搅拌过夜。冷却至室温后,滤出固体并将母液减压浓缩。将残余物溶于dcm,用饱和nahco3水溶液洗涤,用硫酸镁干燥,过滤,减压浓缩得到黄色油状标题化合物(1.86g,97%收率),其不经纯化即可用于下一步骤。
[1581]1h-nmr(500mhz,dmso-d6)δppm:8.05(d,1h),7.5-7.32(m,5h),7.44(d,1h),7.07(dd,1h),5.25(s,2h),3.99(s,2h),1.96(brs,2h)。
[1582]
步骤c4:2-(氨基甲基)-4-(苄氧基)苯胺的制备
[1583]
将1-[5-(苄氧基)-2-硝基苯基]甲胺(1eq.,1.86g,7.20mmol)溶于etoh(27ml),然后加入水(8ml)、铁粉(10eq.,4.026g,72.09mmol)和nh4cl(0.5eq.,193mg,3.6081mmol)。将反应混合物回流1小时。冷却至室温后,将混合物用硅藻土垫过滤并减压浓缩。将残余物溶于etoac并用1m naoh水溶液洗涤。将有机相用硫酸镁干燥,过滤,减压浓缩得到棕色油状标题化合物(1.427g,87%收率),其不经纯化直接用于下一步骤。
[1584]1h-nmr(500mhz,dmso-d6)δppm:7.44-7.27(m,5h),6.79(d,1h),6.63(dd,1h),
6.53(d,1h),4.94(s,2h),3.57(s,2h)。
[1585]
步骤c5:6-(苄氧基)-3,4-二氢-2λ6,1,3-苯并噻二嗪-2,2(1h)-二酮的制备
[1586]
将2-(氨基甲基)-4-(苄氧基)苯胺(1eq.,1.42g,6.22mmol)溶于吡啶(45ml)。加入硫酰胺(7eq.,4.18g,43.5mmol)并将混合物回流2小时。将反应混合物减压浓缩并将残余物用60ml 0.5m hcl水溶液处理。将沉淀析出的固体滤出,真空干燥得到黄色-白色固体状标题化合物(1.721g,95%收率),其不经纯化直接用于下一步骤。
[1587]1h-nmr(500mhz,dmso-d6)δppm:9.82(s,1h),7.45-7.28(m,5h),7.17(t,1h),6.87(dd,1h),6.84(d,1h),6.65(d,1h),5.03(s,2h),4.36(d,2h)。
[1588]
步骤c6:6-(苄氧基)-1-甲基-3,4-二氢-2λ6,1,3-苯并噻二嗪-2,2(1h)-二酮的制备
[1589]
将6-(苄氧基)-3,4-二氢-2λ6,1,3-苯并噻二嗪-2,2(1h)-二酮(1eq.,1.57g,5.41mmol)溶于thf(50ml)。加入pph3(2eq.,2.83g,10.82mmol)和meoh(1.1eq.,0.24ml,190mg,5.925mmol)。将反应混合物冷却至0℃并于0℃将diad(2eq.,2.13ml,2.19g,10.8mmol)滴加到搅拌中的反应混合物中,然后在该温度下搅拌2小时。将反应混合物减压浓缩,将残余物通过快速色谱纯化,用dcm作为洗脱剂得到标题化合物(690mg,42%收率),为白色固体。
[1590]1h-nmr(500mhz,dmso-d6)δppm:7.69(brs,1h),7.46-7.29(m,5h),6.98(d,1h),6.94(dd,1h),6.87(d,1h),5.07(s,2h),4.38(s,2h),3.12(s,3h)。
[1591]
步骤1:3-{1-[4-(苄氧基)丁基]-4-甲基-1h-苯并三唑-5-基}-3-(3-{[6-(苄氧基)-1-甲基-2,2-二氧代-1,4-二氢-2λ6,1,3-苯并噻二嗪-3(2h)-基]甲基}-4-甲基苯基)丙酸乙酯的制备
[1592]
采用通用方法7,用3-{1-[4-(苄氧基)丁基]-4-甲基-1h-苯并三唑-5-基}-3-[3-(羟基甲基)-4-甲基苯基]丙酸乙酯(1当量)和6-(苄氧基)-1-甲基-3,4-二氢-2λ6,1,3-苯并噻二嗪-2,2(1h)-二酮(1当量)作为起始试剂,得到标题化合物(57%收率)。
[1593]1h-nmr(500mhz,dmso-d6)δppm:7.57(d,1h),7.47(d,1h),7.45(d,2h),7.39(t,2h),7.33(t,1h),7.3(t,2h),7.25(d,2h),7.24(t,1h),7.19(dd,1h),7.13(d,1h),7.12(d,1h),7.08(d,1h),7.03(dd,1h),6.82(d,1h),5.09(s,2h),4.84(t,1h),4.61(t,2h),4.38(s,2h),4.27(s,2h),4.01(s,2h),3.91(q,2h),3.38(t,2h),3.24(s,3h),3.19/3.14(dd+dd,2h),2.75(s,3h),2.21(s,3h),1.9(qn,2h),1.46(qn,2h),0.97(t,3h)。
[1594]
步骤2:3-[1-(4-羟基丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(6-羟基-1-甲基-2,2-二氧代-1,4-二氢-2λ6,1,3-苯并噻二嗪-3(2h)-基)甲基]-4-甲基苯基}丙酸乙酯的制备
[1595]
采用通用方法8,用3-{1-[4-(苄氧基)丁基]-4-甲基-1h-苯并三唑-5-基}-3-(3-{[6-(苄氧基)-1-甲基-2,2-二氧代-1,4-二氢-2λ6,1,3-苯并噻二嗪-3(2h)-基]甲基}-4-甲基苯基)丙酸乙酯(1当量)作为起始试剂,得到标题化合物(定量)。
[1596]1h-nmr(500mhz,dmso-d6)δppm:9.42(s,1h),7.61(d,1h),7.5(d,1h),7.19(dd,1h),7.13(brs.,1h),7.12(d,1h),6.96(d,1h),6.76(dd,1h),6.49(d,1h),4.83(t,1h),4.64(t,2h),4.43(t,1h),4.23/4.19(d+d,2h),4.04/3.99(d+d,2h),3.93(q,2h),3.38(q,2h),3.19(s,3h),3.16(m,2h),2.74(s,3h),2.22(s,3h),1.9(m,2h),1.36(m,2h),0.99(t,
3h)。
[1597]
步骤3:3-[1-(4-氯丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(6-羟基-1-甲基-2,2-二氧代-1,4-二氢-2λ6,1,3-苯并噻二嗪-3(2h)-基)甲基]-4-甲基苯基}丙酸乙酯盐酸盐的制备
[1598]
采用通用方法10,用3-[1-(4-羟基丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(6-羟基-1-甲基-2,2-二氧代-1,4-二氢-2λ6,1,3-苯并噻二嗪-3(2h)-基)甲基]-4-甲基苯基}丙酸乙酯(1当量)作为起始试剂,得到标题化合物(定量)。
[1599]1h-nmr(500mhz,dmso-d6)δppm:9.43(br.,1h),7.64(d,1h),7.51(d,1h),7.19(dd,1h),7.13(d,1h),7.12(d,1h),6.96(d,1h),6.77(dd,1h),6.49(d,1h),4.83(t,1h),4.69(t,2h),4.23/4.19(d+d,2h),4.04/3.99(d+d,2h),3.93(q,2h),3.64(t,2h),3.19(s,3h),3.17(m,2h),2.74(s,3h),2.22(s,3h),1.99(m,2h),1.68(m,2h),0.99(t,3h)。
[1600]
步骤4:[4,26,31-三甲基-27,27-二氧代-21-氧杂-27λ
6-硫杂-1,14,15,16,26-五氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯的制备
[1601]
采用通用方法11,用3-[1-(4-氯丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(6-羟基-1-甲基-2,2-二氧代-1,4-二氢-2λ6,1,3-苯并噻二嗪-3(2h)-基)甲基]-4-甲基苯基}丙酸乙酯盐酸盐(1当量)作为起始试剂,得到标题化合物(定量)。
[1602]1h-nmr(500mhz,dmso-d6)δppm:7.68(d,1h),7.45(d,1h),7.45(d,1h),7.26(d,1h),6.94(d,1h),6.76(dd,1h),6.51(d,1h),5.71(d,1h),4.78(t,1h),4.76(m,2h),3.95/3.76(d+d,2h),3.92(q,2h),3.9/3.76(d+d,2h),3.62/3.42(m+m,2h),3.18(s,3h),3.16/3.05(dd+dd,2h),2.61(s,3h),2.33(s,3h),2.19/2.09(m+m,2h),1.82/1.64(m+m,2h),1(t,3h)。
[1603]
步骤5:实施例39的制备
[1604]
采用通用方法12,用[4,26,31-三甲基-27,27-二氧代-21-氧杂-27λ
6-硫杂-1,14,15,16,26-五氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体,55%收率)。
[1605]
通过手性柱色谱分离得到对映体纯产物。
[1606]
实施例39a(e1,光学纯度》99.9%)
[1607]c30h33
n5o5s的hrms计算值:575.2202;[m+h]
+
,实测值:576.2273(δ=-0.4ppm)。
[1608]
实施例39b(e2,光学纯度~99.7%)
[1609]c30h33
n5o5s的hrms计算值:575.2202;[m+h]
+
,实测值:576.2252(δ=-4.0ppm)。
[1610]1h-nmr(500mhz,dmso-d6)δppm:7.67(d,1h),7.46(dd,1h),7.43(d,1h),7.26(d,1h),6.94(d,1h),6.76(dd,1h),6.49(d,1h),5.7(d,1h),4.76(t,1h),4.75(m,2h),3.94/3.76(d+d,2h),3.9/3.76(d+d,2h),3.61/3.4(m+m,2h),3.18(s,3h),3.04/2.94(dd+dd,2h),2.6(s,3h),2.33(s,3h),2.2/2.11(m+m,2h),1.82/1.64(m+m,2h)。
[1611]
13
c-nmr(125mhz,dmso-d6)δppm:131.2,130.8,128.2,127.4,118.2,116.3,111.8,108,67.6,51.1,49.6,48.3,41.8,41,33.6,26.7,25.6,18.6,13.4。
[1612]
实施例40:[(2r,8s)-4-甲氧基-2,33-二甲基-29,29-二氧代-23,28-二氧杂-29
λ
6-硫杂-1,14,15,16-四氮杂六环[22.5.3.1
3,7
.1
9,13
.0
12,16
.0
27,31
]三十四碳-3(34),4,6,9(33),10,12,14,24,26,31-十烯-8-基]乙酸和
[1613]
[(2r,8r)-4-甲氧基-2,33-二甲基-29,29-二氧代-23,28-二氧杂-29λ
6-硫杂-1,14,15,16-四氮杂六环[22.5.3.1
3,7
.1
9,13
.0
12,16
.0
27,31
]三十四碳-3(34),4,6,9(33),10,12,14,24,26,31-十烯-8-基]乙酸
[1614][1615]
步骤1:3-{1-[6-(苄氧基)己基]-4-甲基-1h-苯并三唑-5-基}-3-{3-[(1s)-1-羟基乙基]-4-甲氧基苯基}丙酸乙酯的制备
[1616]
采用通用方法6,用(e)-3-[1-(6-苄氧基己基)-4-甲基-苯并三唑-5-基]丙-2-烯酸乙酯(1当量)和(1s)-1-[2-甲氧基-5-(4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷-2-基)苯基]乙醇(1.1当量)作为起始试剂,得到标题化合物(50%收率)。
[1617]1h-nmr(400mhz,dmso-d6)δppm:7.6(d,1h),7.48(d,1h),7.38(d,1h),7.32-7.25(m,5h),7.11(dd,1h),6.81(d,1h),4.9(d,1h),4.9(m,1h),4.8(m,1h),4.62(t,2h),4.4(s,2h),3.91(q,2h),3.71(s,3h),3.38(t,2h),3.1(d,2h),2.78(s,3h),1.88(m,2h),1.5(m,2h),1.35(m,2h),1.2(m+d,5h),1(t,3h)。
[1618]
步骤2:3-(3-{(1r)-1-[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]乙基}-4-甲氧基苯基)-3-{1-[6-(苄氧基)己基]-4-甲基-1h-苯并三唑-5-基}丙酸乙酯的制备
[1619]
采用通用方法7,用3-{1-[6-(苄氧基)己基]-4-甲基-1h-苯并三唑-5-基}-3-{3-[(1s)-1-羟基乙基]-4-甲氧基苯基}丙酸乙酯(1当量)和6-(苄氧基)-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮(1.5当量)作为起始试剂,得到标题化合物(米黄色固体,71%收率)。
[1620]1h-nmr(400mhz,dmso-d6)δppm:0.97(t,j=7.09hz,5h)1.10-1.26(m,7h)1.29(br.s.,3h)1.37-1.53(m,7h)1.75-1.91(m,3h)2.72-2.79(m,4h)3.09-3.21(m,3h)3.33-3.41(m,3h)3.64(d,j=1.71hz,3h)3.91(qd,j=6.95,2.26hz,2h)4.38(d,j=1.47hz,2h)4.46-4.65(m,3h)4.82(q,j=8.15hz,1h)4.86-5.12(m,2h)5.28-5.45(m,1h)6.63-6.82(m,2h)6.82-6.97(m,2h)7.08-7.48(m,12h)7.48-7.55(m,1h)7.57-7.68(m,1h)。
[1621]
步骤3:3-{3-[(1r)-1-(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)乙基]-4-甲氧基苯基}-3-[1-(6-羟基己基)-4-甲基-1h-苯并三唑-5-基]丙酸乙酯的制备
[1622]
采用通用方法8,用3-(3-{(1r)-1-[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]乙基}-4-甲氧基苯基)-3-{1-[6-(苄氧基)己基]-4-甲基-1h-苯并三唑-5-基}丙酸乙酯(1当量)作为起始试剂,得到标题化合物(98%收率)。
[1623]1h-nmr(400mhz,dmso-d6)δppm:0.91-1.04(m,7h)1.11-1.47(m,23h)1.87(quint,
j=7.12hz,4h)2.73-2.78(m,5h)3.13-3.22(m,3h)3.32-3.36(m,3h)3.57-3.59(m,3h)3.67(d,j=0.98hz,6h)3.94(q,j=7.46hz,4h)4.29(t,j=5.07hz,2h)4.37-4.57(m,3h)4.63(t,j=6.91hz,4h)4.78-4.87(m,2h)5.37(quint,j=7.06hz,2h)6.51(dd,j=12.35,2.81hz,2h)6.64(dd,j=8.80,2.69hz,2h)6.76(d,j=1.22hz,1h)6.77-6.84(m,1h)7.13(dd,j=8.56,1.96hz,1h)7.42(dd,j=11.13,2.08hz,1h)7.53(t,j=9.05hz,1h)7.59-7.66(m,1h)9.52(d,j=3.55hz,1h)。
[1624]
步骤4:3-[1-(6-溴己基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(1r)-1-(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)乙基]-4-甲氧基苯基}丙酸乙酯的制备
[1625]
采用通用方法9,用3-{3-[(1r)-1-(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)乙基]-4-甲氧基苯基}-3-[1-(6-羟基己基)-4-甲基-1h-苯并三唑-5-基]丙酸乙酯(1当量)作为起始试剂,得到标题化合物(77%收率)。
[1626]1h-nmr(400mhz,dmso-d6)δppm:9.5(s,1h),7.6(d,1h),7.55(d,1h),7.4(d,1h),7.1(m,1h),6.8(m,1h),6.75(d,1h),6.65(d,1h),6.5(d,1h),5.4(m,1h),4.8(m,1h),4.65(t,2h),4.5(m,2h),3.95(q,2h),3.7(s,3h),3.45(t,2h),3.2(m,2h),2.75(d,3h),1.9(quint,2h),1.75(quint,2h),1.4(t,3h),1.4/1.25(2m,4h),1(m,3h)。
[1627]
步骤5:[(2r)-4-甲氧基-2,33-二甲基-29,29-二氧代-23,28-二氧杂-29λ
6-硫杂-1,14,15,16-四氮杂六环[22.5.3.1
3,7
.1
9,13
.0
12,16
.0
27,31
]三十四碳-3(34),4,6,9(33),10,12,14,24,26,31-十烯-8-基]乙酸乙酯的制备
[1628]
采用通用方法11,用3-[1-(6-溴己基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(1r)-1-(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)乙基]-4-甲氧基苯基}丙酸乙酯(1当量)作为起始试剂,得到标题化合物(65%收率)。
[1629]1h-nmr(400mhz,dmso-d6)δppm:0.93-1.03(m,8h)1.24(d,j=4.65hz,8h)1.32-1.67(m,15h)1.96(d,j=6.85hz,4h)2.85(s,7h)2.97-3.12(m,3h)3.15-3.22(m,3h)3.39-3.48(m,1h)3.62(d,j=18.71hz,8h)3.67-3.78(m,2h)3.91(qd,j=7.05,5.01hz,5h)4.10-4.27(m,2h)4.24-4.38(m,3h)4.59-4.74(m,6h)4.79-4.90(m,3h)5.42(q,j=7.17hz,1h)5.51(q,j=7.13hz,1h)5.86(d,j=2.81hz,1h)6.24(d,j=2.81hz,1h)6.72(d,j=8.56hz,4h)6.84(d,j=8.56hz,1h)6.90(dd,j=9.05,4.16hz,2h)7.12-7.25(m,2h)7.36(d,j=8.80hz,1h)7.46(dd,j=8.56,2.08hz,1h)7.57-7.73(m,5h)。
[1630]
步骤6:实施例40的制备
[1631]
采用通用方法12,用[(2r)-4-甲氧基-2,33-二甲基-29,29-二氧代-23,28-二氧杂-29λ
6-硫杂-1,14,15,16-四氮杂六环[22.5.3.1
3,7
.1
9,13
.0
12,16
.0
27,31
]三十四碳-3(34),4,6,9(33),10,12,14,24,26,31-十烯-8-基]乙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体,79%收率)。
[1632]
通过手性柱色谱分离得到非对映体纯产物。
[1633]
实施例40a(2r,8s)
[1634]c32h36
n4o7s的hrms计算值:620.2305;[m+h]
+
,实测值:621.2378(δ=0.1ppm)。
[1635]1h-nmr(400mhz,dmso-d6)δppm:12.1(m,1h),7.62(d,1h),7.46(dd,1h),7.31(d,1h),7.15(d,1h),6.91(d,1h),6.87(d,1h),6.72(dd,1h),5.87(d,1h),5.42(q,1h),4.84(t,1h),4.67(m,2h),4.16(dd,2h),3.66(s,3h),3.61/3.46(2m,2h),3.01/2.91(2dd,2h),
2.85(s,3h),1.97(m,2h),1.68-1.16(m,6h),1.35(d,3h)。
[1636]
实施例40b(2r,8r)
[1637]c32h36
n4o7s的hrms计算值:620.2305;[m+h]
+
,实测值:621.2377(δ=-0.1ppm)。
[1638]1h-nmr(400mhz,dmso-d6)δppm:12.08(m,1h),7.66(d,1h),7.59(d,1h),7.58(d,1h),7.2(dd,1h),6.9(d,1h),6.73(d,1h),6.72(dd,1h),6.24(d,1h),5.51(q,1h),4.82(t,1h),4.67(m,2h),4.29(dd,2h),3.65(s,3h),3.6/3.5(2m,2h),3.07(d,2h),2.84(s,3h),1.96(m,2h),1.7-1.2(m,6h),1.54(d,3h)。
[1639]
实施例41:[(2r,8s)-4-甲氧基-2,32-二甲基-28,28-二氧代-19,22,27-三氧杂-28λ
6-硫杂-1,14,15,16-四氮杂六环[21.5.3.1
3,7
.1
9,13
.0
12,16
.0
26,30
]三十三碳-3(33),4,6,9(32),10,12,14,23,25,30-十烯-8-基]乙酸和
[1640]
[(2r,8r)-4-甲氧基-2,32-二甲基-28,28-二氧代-19,22,27-三氧杂-28λ
6-硫杂-1,14,15,16-四氮杂六环[21.5.3.1
3,7
.1
9,13
.0
12,16
.0
26,30
]三十三碳-3(33),4,6,9(32),10,12,14,23,25,30-十烯-8-基]乙酸
[1641][1642]
步骤1:3-(1-{2-[2-(苄氧基)乙氧基]乙基}-4-甲基-1h-苯并三唑-5-基)-3-{3-[(1s)-1-羟基乙基]-4-甲氧基苯基}丙酸乙酯的制备
[1643]
采用通用方法6,用(2e)-3-(1-{2-[2-(苄氧基)乙氧基]乙基}-4-甲基-1h-苯并三唑-5-基)丙-2-烯酸乙酯(1当量)和(1s)-1-[2-甲氧基-5-(4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷-2-基)苯基]乙-1-醇(2当量)作为起始试剂,得到标题化合物(无色油,52%收率)。
[1644]1h-nmr(400mhz,dmso-d6)δppm 7.6(d,1h),7.45(d,1h),7.38(s,1h),7.3-7.2(t+d,5h),7.1(d,1h),6.8(d,1h),4.9(d,1h),4.9(m,1h),4.8(t,2h),4.8(t,1h),4.3(s,2h),3.9(t,2h),3.9(q,2h),3.7(s,3h),3.55/3.45(t,4h),3.1(m,2h),2.75(s,3h),1.2(d,3h),1(t,3h)。
[1645]
步骤2:3-(3-{(1r)-1-[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]乙基}-4-甲氧基苯基)-3-(1-{2-[2-(苄氧基)乙氧基]乙基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯的制备
[1646]
采用通用方法7,用3-(1-{2-[2-(苄氧基)乙氧基]乙基}-4-甲基-1h-苯并三唑-5-基)-3-{3-[(1r)-1-羟基乙基]-4-甲氧基苯基}丙酸乙酯(1当量)和6-(苄氧基)-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮(1.1当量)作为起始试剂,得到标题化合物(67%收率)。
[1647]1h-nmr(400mhz,dmso-d6)δppm:7.63-7.45(dd,2h),7.45-7.05(m,12h),6.94-6.71(m,4h),5.36(m,1h),5.08-4.97(dd,2h),4.86-4.75(m,3h),4.54/4.51(dd,2h),4.29
(s,2h),3.95-3.84(m,4h),3.63/3.62(s,3h),3.5/3.4(m,4h),3.17-3.1(m,2h),2.75/2.74(s,3h),1.42/1.4(d,3h),0.98(t,3h)。
[1648]
步骤3:3-{3-[(1r)-1-(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)乙基]-4-甲氧基苯基}-3-{1-[2-(2-羟基乙氧基)乙基]-4-甲基-1h-苯并三唑-5-基}丙酸乙酯的制备
[1649]
采用通用方法8,用3-(3-{(1r)-1-[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]乙基}-4-甲氧基苯基)-3-(1-{2-[2-(苄氧基)乙氧基]乙基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体,69%收率)。
[1650]1h-nmr(400mhz,dmso-d6)δppm:0.96-1.05(m,3h)1.42(t,j=6.64hz,3h)2.76(d,j=5.65hz,3h)3.11-3.21(m,2h)3.38(d,j=2.29hz,4h)3.67(s,3h)3.85-3.91(m,2h)3.94(qd,j=7.12,1.22hz,2h)4.38-4.57(m,3h)4.76-4.88(m,3h)5.37(quin,j=7.02hz,1h)6.51(dd,j=16.02,2.90hz,1h)6.65(dd,j=8.85,2.90hz,1h)6.75-6.84(m,2h)7.13(dd,j=8.54,1.83hz,1h)7.43(dd,j=8.54,1.98hz,1h)7.49-7.58(m,1h)7.61-7.68(m,1h)9.53(br.s.,1h)。
[1651]
步骤4:3-{1-[2-(2-溴乙氧基)乙基]-4-甲基-1h-苯并三唑-5-基}-3-{3-[(1r)-1-(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)乙基]-4-甲氧基苯基}丙酸乙酯的制备
[1652]
采用通用方法9,用3-{3-[(1r)-1-(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)乙基]-4-甲氧基苯基}-3-{1-[2-(2-羟基乙氧基)乙基]-4-甲基-1h-苯并三唑-5-基}丙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体,94%收率)。
[1653]1h-nmr(400mhz,dmso-d6)δppm:1.01(td,j=7.09,3.91hz,3h)1.41(t,j=6.54hz,3h)2.75(d,j=4.77hz,3h)3.08-3.26(m,2h)3.45(t,j=5.99hz,2h)3.64-3.69(m,4h)3.88-3.98(m,6h)4.36-4.59(m,2h)4.76-4.87(m,3h)5.31-5.42(m,1h)6.51(dd,j=11.13,2.81hz,1h)6.65(dd,j=8.86,2.87hz,1h)6.75-6.85(m,2h)7.12(dd,j=8.50,1.90hz,1h)7.42(dd,j=7.03,2.02hz,1h)7.50-7.58(m,1h)7.62-7.68(m,1h)。
[1654]
步骤5:[(2r)-4-甲氧基-2,32-二甲基-28,28-二氧代-19,22,27-三氧杂-28λ
6-硫杂-1,14,15,16-四氮杂六环[21.5.3.1
3,7
.1
9,13
.0
12,16
.0
26,30
]三十三碳-3(33),4,6,9(32),10,12,14,23,25,30-十烯-8-基]乙酸乙酯的制备
[1655]
采用通用方法11,用3-{1-[2-(2-溴乙氧基)乙基]-4-甲基-1h-苯并三唑-5-基}-3-{3-[(1r)-1-(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)乙基]-4-甲氧基苯基}丙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体,96%收率)。
[1656]1h-nmr(400mhz,dmso-d6)δppm:1.01(dt,j=17.58,7.11hz,7h)1.36(d,j=7.09hz,3h)1.61(d,j=7.09hz,4h)2.86(d,j=4.89hz,7h)2.93-3.12(m,3h)3.12-3.27(m,3h)3.45-3.64(m,8h)3.68-3.85(m,8h)3.86-3.98(m,10h)4.04(d,j=11.13hz,1h)4.08-4.26(m,3h)4.53(d,j=17.85hz,1h)4.74-4.97(m,9h)5.43(q,j=6.77hz,1h)5.56(q,j=7.21hz,1h)5.68(d,j=2.57hz,1h)6.45(d,j=2.45hz,1h)6.54(d,j=8.56hz,1h)6.60(dd,j=8.93,2.93hz,1h)6.68-6.78(m,2h)6.85(dd,j=11.19,8.99hz,3h)7.10(s,1h)7.13(d,j=8.68hz,1h)7.27(d,j=8.80hz,1h)7.45(d,j=8.44hz,1h)7.55-7.61(m,2h)7.70(d,j=8.68hz,1h)。
[1657]
步骤6:实施例41的制备
[1658]
采用通用方法12,用[(2r)-4-甲氧基-2,32-二甲基-28,28-二氧代-19,22,27-三氧杂-28λ
6-硫杂-1,14,15,16-四氮杂六环[21.5.3.1
3,7
.1
9,13
.0
12,16
.0
26,30
]三十三碳-3(33),4,6,9(32),10,12,14,23,25,30-十烯-8-基]乙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体,72%收率)。
[1659]
通过手性柱色谱分离得到非对映体纯产物。
[1660]
实施例41a(2r,8s)
[1661]c30h32
n4o8s的hrms计算值:608.1941;[m+h]
+
,实测值:609.2014(δ=0.1ppm)。
[1662]1h-nmr(400mhz,dmso-d6)δppm:12.1(br),7.7(d,1h),7.6(sl,1h),7.27(d,1h),6.87(d,1h),6.76(d,1h),6.61(dd,1h),6.54(d,1h),6.45(d,1h),5.56(q,1h),4.85/4.52(2d,2h),4.85(m,2h),4.8(t,1h),3.92(m,2h),3.9/3.52(2m,2h),3.76(m,2h),3.57(s,3h),3.18/3.05(2dd,2h),2.85(s,3h),1.6(d,3h)。
[1663]
13
c-nmr(100mhz,dmso-d6)δppm:1561,173.7,154.8,146.2,145.4,138.3,135.4,132.6,131.5,127.8,125.2,125.2,124.6,119.6,118.1,114.4,113,111,109.7,70.4,68.8,68.1,55.6,51.3,48.5,46,40.6,39.5,19.6,13.5。
[1664]
15
n-nmr(50mhz,dmso-d6)δppm:-152.9,-290.5。
[1665]
实施例41b(2r,8r)
[1666]c30h32
n4o8s的hrms计算值:608.1941;[m+h]
+
,实测值:609.2014(δ=0.1ppm)。
[1667]1h-nmr(400mhz,dmso-d6)δppm:12.1(br),7.59(d,1h),7.46(d,1h),7.1(d,1h),7.08(sl,1h),6.89(d,1h),6.85(d,1h),6.73(dd,1h),5.71(d,1h),5.43(q,1h),4.85(m,1h),4.82(m,2h),4.17/4.12(m,2h),4.06/3.91(dt+td,2h),3.84/3.71(2m,2h),3.72(s,3h),3.62/3.52(2m,2h),2.97/2.84(2dd,2h),2.86(s,3h),1.35(d,3h)。
[1668]
13
c-nmr(100mhz,dmso-d6)δppm:173,155.8,155.4,146.7,145.2,137.6,136.1,132.4,128.7,128.3,127,126.1,125.5,119.4,118.5,115,113.3,111.3,108.9,69.7,68.7,68.7,55.9,52.4,48.6,46.1,41.3,40.8,17.7,13.3。
[1669]
15
n-nmr(50mhz,dmso-d6)δppm:-3.1,-152.9,-290.5。
[1670]
实施例42:[4,21,31-三甲基-27,27-二氧代-26-氧杂-27λ
6-硫杂-1,14,15,16,21-五氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸
[1671][1672]
步骤c1:6-溴-2h-1,2λ6,3-噁噻嗪-2,2-二酮的制备
[1673]
采用通用方法4步骤2,用5-溴-2-羟基苯甲醛(1当量)作为起始试剂,得到标题化
合物(白色固体,38%收率)。
[1674]1h-nmr(400mhz,dmso-d6)δppm:8.25(d,1h),8.15(s,1h),8.1(dd,1h),7.52(d,1h)。
[1675]
步骤c2:6-溴-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮的制备
[1676]
采用通用方法4步骤3,用6-溴-2h-1,2λ6,3-噁噻嗪-2,2-二酮(1当量)作为起始试剂,得到标题化合物(白色固体,57%收率)。
[1677]1h-nmr(400mhz,dmso-d6)δppm:8.6(m,1h),7.56(d,1h),7.52(dd,1h),7.05(d,1h),4.58(s,2h)。
[1678]
步骤1:3-{3-[(6-溴-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯的制备
[1679]
采用通用方法7,用3-[3-(羟基甲基)-4-甲基-苯基]-3-[1-[4-[(4-甲氧基苯基)甲氧基]丁基]-4-甲基-苯并三唑-5-基]丙酸乙酯(1当量)和6-溴-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮(1.2当量)作为起始试剂,得到标题化合物(91%收率)。
[1680]1h-nmr(400mhz,dmso-d6)δppm:7.62(dd,1h),7.59/7.48(2d,2h),7.53(d,1h),7.24(d,1h),7.22-7.11(m,5h),6.86(d,2h),4.84(t,1h),4.65(t,2h),4.5(m,2h),4.31(s,2h),4.24(m,2h),3.93(q,2h),3.72(s,3h),3.37(t,2h),3.16(d,2h),2.76(s,3h),2.23(s,3h),1.92(quint,2h),1.48(quint,2h),0.99(t,3h)。
[1681]
步骤2:3-[3-({6-[(叔丁氧基羰基)氨基]-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基}甲基)-4-甲基苯基]-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯的制备
[1682]
在氩气流下向装备有干燥管的25ml圆底烧瓶中加入3-{3-[(6-溴-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯(1eq.,100mg,0.126mmol)、氨基甲酸叔丁酯(1.2eq.,17.8mg,0.152mmol)、叔丁醇钠(1.5eq.,18.2mg,0.189mmol)、tbuxphos(0.2eq.,10.7mg,0.0253mmol)和pd2(dba)3(0.1eq.,11.6mg,0.0126mmol)。将混合物悬浮于甲苯(1ml)中并在室温下搅拌过夜。将挥发物减压蒸发。将残余物通过正相硅胶色谱纯化,用己烷-etoac洗脱得到标题化合物(27mg,20%收率)。
[1683]1h-nmr(400mhz,dmso-d6)δppm:0.98(t,j=7.09hz,3h)1.15-1.28(m,13h)1.92(quint,j=7.24hz,2h)2.22(s,3h)2.75(s,3h)3.16(d,j=7.46hz,2h)3.36(t,j=6.30hz,3h)3.72(s,3h)3.86-3.97(m,2h)4.22(s,2h)4.30(s,2h)4.46(s,2h)4.64(t,j=6.91hz,2h)4.84(t,j=8.07hz,1h)6.12(br.s.,2h)6.86(d,j=8.68hz,2h)6.92(s,1h)7.06-7.15(m,2h)7.18(d,j=8.68hz,2h)7.24(s,1h)7.36(dd,j=9.05,2.45hz,1h)7.46-7.56(m,2h)7.59(d,j=8.68hz,1h)9.54(s,1h)。
[1684]
步骤3:3-[3-({6-[(叔丁氧基羰基)(甲基)氨基]-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基}甲基)-4-甲基苯基]-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯的制备
[1685]
在装备有干燥管的100ml圆底烧瓶中将3-[3-({6-[(叔丁氧基羰基)氨基]-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基}甲基)-4-甲基苯基]-3-(1-{4-[(4-甲氧基苯基)甲氧
基]丁基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯(1eq.,260mg,0.289mmol)溶于dmf(2.4ml)。将氢化钠(60%的矿物油溶液(1.5eq.,17.3mg,0.433mmol)分批加入到搅拌中的混合物中。搅拌5分钟后加入碘甲烷(1.5eq.,61.5mg,0.027ml)并在室温下继续搅拌过夜。将反应混合物倒入水(20ml)中并用etoac萃取(2x20ml)。将合并的有机层用盐水(20ml)洗涤,用硫酸钠干燥,过滤,将形成的滤液浓缩至干。将残余物通过正相硅胶色谱纯化,用庚烷-etoac作为洗脱剂得到标题化合物(212mg,87%收率)。
[1686]1h-nmr(400mhz,dmso-d6)δppm:7.58(d,1h),7.48(d,1h),7.38-7.1(m,6h),7.19(d,2h),6.86(d,2h),4.82(t,1h),4.62(t,2h),4.49(d,2h),4.3(s,2h),4.22(s,2h),3.91(q,2h),3.71(s,3h),3.38(t,2h),3.2(s,3h),3.15(m,2h),2.5(s,3h),2.21(s,3h),1.9(m,2h),1.49(m,2h),1.4(s,9h),0.99(t,3h)。
[1687]
步骤4:3-[3-({6-[(叔丁氧基羰基)(甲基)氨基]-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基}甲基)-4-甲基苯基]-3-[1-(4-羟基丁基)-4-甲基-1h-苯并三唑-5-基]丙酸乙酯的制备
[1688]
向装备有干燥管的25ml圆底烧瓶中加入3-[3-({6-[(叔丁氧基羰基)(甲基)氨基]-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基}甲基)-4-甲基苯基]-3-(1-{4-[(4-甲氧基苯基)甲氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯(1eq.,0.262g,0.311mmol)、dcm(1.6ml)和水(0.078ml)。加入ddq(1.5eq.,106mg,0.467mmol)后反应混合物变成黑色,同时在室温下继续搅拌3小时,颜色变成红色。将反应混合物用dcm(20ml)稀释,用饱和nahco3水溶液(20ml)洗涤并将水层用dcm(20ml)萃取。将合并的有机层用硫酸钠干燥,过滤,将滤液浓缩。将残余物通过正相硅胶色谱纯化,用庚烷-etoac作为洗脱剂得到标题化合物(202mg,90%收率)。
[1689]1h-nmr(400mhz,dmso-d6)δppm:7.6(d,1h),7.45(d,1h),7.32(dd,1h),7.22(d,1h),7.17(dd,1h),7.15(d,1h),7.13(d,1h),4.83(t,1h),4.63(t,2h),4.5(m,2h),4.4(t),4.25(s,2h),4.23(d,1h),3.92(q,2h),3.38(q,2h),3.2(s,3h),3.18(m,2h),2.75(s,3h),2.21(s,3h),1.9(m,2h),1.4(s,9h),1.38(m,2h),1(t,3h)。
[1690]
步骤5:3-[1-(4-溴丁基)-4-甲基-1h-苯并三唑-5-基]-3-[3-({6-[(叔丁氧基羰基)(甲基)氨基]-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基}甲基)-4-甲基苯基]丙酸乙酯的制备
[1691]
采用通用方法9,用3-[3-({6-[(叔丁氧基羰基)(甲基)氨基]-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基}甲基)-4-甲基苯基]-3-[1-(4-羟基丁基)-4-甲基-1h-苯并三唑-5-基]丙酸乙酯(1当量)作为起始试剂,得到标题化合物(188mg,83%收率)。
[1692]1h-nmr(400mhz,dmso-d6)δppm:7.6(d,1h),7.5(d,1h),7.33(dd,1h),7.3-7.1(m,5h),4.82(t,1h),4.68(t,2h),4.5(m,2h),4.22(m,2h),3.92(q,2h),3.52(t,2h),3.19(s,3h),3.18(m,2h),2.75(s,3h),2.2(s,3h),1.99(m,2h),1.78(m,2h),1.4(s,9h),1(t,3h)。
[1693]
步骤6:3-[1-(4-溴丁基)-4-甲基-1h-苯并三唑-5-基]-3-(4-甲基-3-{[6-(甲基氨基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}苯基)丙酸乙酯的制备
[1694]
在装备有干燥管的100ml圆底烧瓶中将3-[1-(4-溴丁基)-4-甲基-1h-苯并三唑-5-基]-3-[3-({6-[(叔丁氧基羰基)(甲基)氨基]-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基}甲基)-4-甲基苯基]丙酸乙酯(1eq.,0.181g,0.231mmol)溶于dcm(3.6ml)。滴加tfa
(16eq.,0.282ml,0.420g,3.7mmol)并将混合物在室温下搅拌9小时。反应完成后将ph用饱和na2co3水溶液调节至8-9。分层,将有机层用盐水洗涤(10ml)并将水层用dcm(10ml)洗涤。将合并的有机层用硫酸钠干燥,过滤,并将滤液浓缩至干。将残余物通过正相硅胶色谱纯化,用庚烷-etoac-etoh(100:0:0至100/75/25)作为洗脱剂得到标题化合物(0.117g,70%收率)。
[1695]1h-nmr(400mhz,dmso-d6)δppm:7.62(d,1h),7.51(d,1h),7.21(sl,1h),7.2(d,1h),7.14(d,1h),6.91(d,1h),6.57(dd,1h),6.29(d,1h),5.79(q),4.85(t,1h),4.69(t,2h),4.38/4.32(m,2h),4.22/4.15(m,2h),3.93(q,2h),3.53(t,2h),3.17(m,2h),2.76(s,3h),2.66(d,3h),2.22(s,3h),1.98(m,2h),1.77(m,2h),1(t,3h)。
[1696]
步骤7:[4,21,31-三甲基-27,27-二氧代-26-氧杂-27λ
6-硫杂-1,14,15,16,21-五氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯和
[1697]
[4,21,31-三甲基-20,27,27-三氧代-26-氧杂-27λ
6-硫杂-1,14,15,16,21-五氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯的制备
[1698]
向装备有回流冷凝器和干燥管的100ml圆底烧瓶中加入3-[1-(4-溴丁基)-4-甲基-1h-苯并三唑-5-基]-3-(4-甲基-3-{[6-(甲基氨基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}苯基)丙酸乙酯(1eq.,0.11g,0.161mmol)和mecn(48ml)。加入碘化钾(0.1eq.,2.667mg,0.0161mmol)和cs2co3(2eq.,6.2g,0.322mmol)并将混合物于60℃搅拌24小时。反应完成后,将混合物减压浓缩,将残余物用etoac(40ml)稀释并用水(40ml)洗涤。分层,将有机层用盐水洗涤,将合并的水层用etoac(20ml)洗涤。将合并的有机层用硫酸钠干燥,然后过滤,将滤液浓缩至干。将残余物通过反相色谱纯化,用水-mecn-hcooh(1000:25:1 to 25:1000:1)作为洗脱剂。将含有2种主要产物的级分单独合并并浓缩至只剩下水。将形成的含水混合物冷冻干燥得到标题化合物:
[1699]
[4,21,31-三甲基-27,27-二氧代-26-氧杂-27λ
6-硫杂-1,14,15,16,21-五氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯(28%收率)。
[1700]1h-nmr(400mhz,dmso-d6)δppm:7.66(d,1h),7.43(dd,1h),7.3(d,1h),7.27(d,1h),6.87(d,1h),6.64(d,1h),6.5(dd,1h),5.77(d,1h),4.82/4.72(m,2h),4.72(m,1h),4.24/3.94(d,2h),3.99/3.73(d,2h),3.94(q,2h),3.26/3.02(dd,2h),3.13/2.97(m,2h),2.83(s,3h),2.72(s,3h),2.32(s,3h),2.12/1.81(m,2h),1.47/1.04(m,2h),1.01(t,3h)。
[1701]
[4,21,31-三甲基-20,27,27-三氧代-26-氧杂-27λ
6-硫杂-1,14,15,16,21-五氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯(42%收率)。
[1702]1h-nmr(400mhz,dmso-d6)δppm:7.6(d,1h),7.5(dd,1h),7.33(d,1h),7.29(m,2h),7.08(d,1h),6.97(sl,1h),6.2(sl,1h),4.87/4.58(m,2h),4.87(m,1h),4.3/3.69(m,2h),4.2(m,2h),3.92(q,2h),3.22/3.1(2dd,2h),3.2(s,3h),2.4/2.03(m,2h),2.3(s,3h),2.2(s,3h),2.02/1.75(m,2h),1(t,3h)。
[1703]
步骤8:实施例42的制备
[1704]
采用通用方法12,用[4,21,31-三甲基-27,27-二氧代-26-氧杂-27λ
6-硫杂-1,14,15,16,21-五氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯(1eq.,47mg,0.0779mmol)作为起始试剂,得到标题化合物(25mg,54%收率)。
[1705]c30h33
n5o5s的hrms计算值:575.2202;[m+h]
+
,实测值:576.2277(δ=0.3ppm)。
[1706]1h-nmr(400mhz,dmso-d6)δppm:12.3(m,1h),7.64(d,1h),7.45(dd,1h),7.27(d,1h),7.26(d,1h),6.87(d,1h),6.63(d,1h),6.49(dd,1h),5.77(d,1h),4.82/4.72(2m,2h),4.78(m,1h),4.25/3.91(2d,2h),3.99/3.73(2d,2h),3.14/2.99(2dd,2h),3.1/2.97(2m,2h),2.83(s,3h),2.72(s,3h),2.32(s,3h),2.12/1.81(2m,2h),1.47/1.04(2m,2h)。
[1707]
实施例43:[4,21,31-三甲基-20,27,27-三氧代-26-氧杂-27λ
6-硫杂-1,14,15,16,21-五氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸
[1708][1709]
采用通用方法12,用[4,21,31-三甲基-20,27,27-三氧代-26-氧杂-27λ
6-硫杂-1,14,15,16,21-五氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯(1eq.,71mg,0.1149mmol)作为起始试剂,得到标题化合物(35mg,50%收率)。c
30h31
n5o6s的hrms计算值:589.1995;[m+h]
+
,实测值:590.2074(δ=1.0ppm)。
[1710]1h-nmr(400mhz,dmso-d6)δppm:11.8(m,1h),7.6(d,1h),7.53(dd,1h),7.35(d,1h),7.29(d,1h),7.27(dd,1h),7.07(d,1h),6.94(sl,1h),6.2(sl,1h),4.87/4.58(m,2h),4.87(m,1h),4.27/3.69(m,2h),4.19(m,2h),3.21(s,3h),3.13/3(2dd,2h),2.51(s,3h),2.4/2.03(m,2h),2.31(s,3h),2.02/1.75(m,2h)。
[1711]
实施例44:[(19r)-19-羟基-4,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸
[1712][1713]
步骤a1:1-溴-4-氟-2-甲基-3-硝基苯的制备
[1714]
在装备有恒温器的3-颈圆底烧瓶中将1-氟-3-甲基-2-硝基苯(1eq.,50g,322.31mmol)溶于tfa(200ml,2.611mol)并将反应混合物冷却至-5℃。滴加硫酸(100ml),然后分小批加入1-溴吡咯烷-2,5-二酮(1eq.,57.33g,322.1mmol)。将反应混合物于-5℃搅拌过夜,然后于0℃搅拌72小时,并且于5℃搅拌一夜。将混合物倒入冰/水的1:1混合物中,将沉淀析出的固体滤出并用水洗涤。将得到的固体溶于dcm并用饱和nahco3水溶液和盐水洗涤,用硫酸镁干燥,蒸发并在室温下风干过夜得到47.38g(63%收率)灰白色固体状标题化合物。
[1715]1h-nmr(500mhz,dmso-d6)δppm:7.98(dd,1h),7.49(td,1h),2.37(s,3h)。
[1716]
步骤a2:(2r)-4-(4-溴-3-甲基-2-硝基苯氨基)丁烷-1,2-二醇的制备
[1717]
将1-溴-4-氟-2-甲基-3-硝基苯(1eq.,4g,17mmol)、(2r)-4-氨基丁烷-1,2-二醇盐酸盐(1.5eq.,4.6ml,3.6g,25mmol)和dipea(2eq.,6ml,4.452g,34.45mmol)的n,n-二甲基乙酰胺(38eq.,60ml,56.2g,645.3mmol)溶液于100℃搅拌过夜。补加0.74g(5.22mmol)(2r)-4-氨基丁烷-1,2-二醇盐酸盐和1ml dipea后,将反应混合物于100℃继续搅拌6小时。将反应混合物倒在冰上,用etoac萃取并将水层用etoac反萃取。将合并的有机层用盐水洗涤,用硫酸钠干燥并减压浓缩。将粗产物通过正相硅胶色谱纯化,用庚烷-etoac(100:0至60:40)作为洗脱剂。收集并蒸发含产物的级分得到橙色固体状标题化合物(4.13g,76%收率)。
[1718]1h-nmr(500mhz,dmso-d6)δppm:7.54(d,1h),6.74(d,1h),6.29(t,1h),4.72(d,1h),4.55(t,1h),3.5(m,1h),3.23/3.131(dd+m,2h),3.22(q,2h),2.25(s,3h),1.75/1.45(m+m,2h)。
[1719]
步骤a3:(2r)-4-(4-溴-3-甲基-2-硝基-苯氨基)-1-[叔丁基(二甲基)硅基]氧基-丁-2-醇的制备
[1720]
将(2r)-4-(4-溴-3-甲基-2-硝基苯氨基)丁烷-1,2-二醇(1eq.,3g,9.40mmol)溶于干燥dmf(18ml)并加入dipea(4.2ml,24mmol)。将混合物冷却至0℃,然后滴加叔丁基二甲基氯硅烷(1.5g,10mmol)的dmf(5.5ml)溶液。将温度升温至室温并将混合物在该温度下搅拌过夜。将反应混合物倒在饱和nh4cl溶液上并用dcm萃取。将有机相用盐水洗涤,用硫酸钠干燥,过滤并浓缩。高真空蒸除残余的dmf。将粗产物通过正相硅胶色谱纯化,用庚烷-etoac(100:0至75:25)作为洗脱剂得到橙色固体状标题化合物(3.898g,96%收率)。
[1721]1h-nmr(500mhz,dmso-d6)δppm:7.53(d,1h),6.73(d,1h),6.27(t,1h),4.78(d,1h),3.52(m,1h),3.51/3.36(m+m,2h),3.23(q,2h),2.25(s,3h),1.78/1.44(m+m,2h),0.84
(s,9h),0.02(s,6h)。
[1722]
步骤a4:4-溴-n-[(3r)-4-{[叔丁基(二甲基)硅基]氧基}-3-{[叔丁基(二苯基)硅基]氧基}丁基]-3-甲基-2-硝基苯胺的制备
[1723]
将(2r)-4-(4-溴-3-甲基-2-硝基-苯氨基)-1-[叔丁基(二甲基)硅基]氧基-丁-2-醇(1eq.,3.898g,8.994mmol)溶于干燥的dmf(45ml)并加入咪唑(3eq.,1.83g,26.9mmol),然后加入n,n-二甲基吡啶-4-胺(0.113g,0.925mmol)。将反应混合物冷却至0℃并滴加叔丁基二苯基氯硅烷(2eq.,4.96g,18.0mmol)。将温度升至50℃并将混合物在该温度下搅拌过夜。将反应混合物倒在饱和nh4cl溶液上并用dcm萃取。将有机相用饱和nahco3溶液洗涤,然后用盐水洗涤,用硫酸钠干燥,过滤并蒸发。高真空蒸除残余的dmf。将粗产物通过正相硅胶色谱纯化,用dcm洗脱得到橙色油状标题化合物(5.92g,98%收率)。
[1724]1h-nmr(500mhz,dmso-d6)δppm:7.65-7.35(m,10h),7.44(d,1h),6.52(d,1h),6.06(t,1h),3.82(m,1h),3.46/3.44(dd+dd,2h),3.17/3.13(m+m,2h),2.24(s,3h),1.8/1.7(m+m,2h),0.99(s,3h),0.76(s,3h),-0.12/-0.16(s,6h)。
[1725]
步骤a5:4-溴-n
1-[(3r)-4-{[叔丁基(二甲基)硅基]氧基}-3-{[叔丁基(二苯基)硅基]氧基}丁基]-3-甲基苯-1,2-二胺的制备
[1726]
将4-溴-n-[(3r)-4-{[叔丁基(二甲基)硅基]氧基}-3-{[叔丁基(二苯基)硅基]氧基}丁基]-3-甲基-2-硝基苯胺(1eq.,6.0g,8.9mmol)溶于二氧杂环己烷(30ml)和meoh(5ml)的混合物。加入用二氧杂环己烷洗涤的阮内镍催化剂(0.38g,4.4mmol)并将混合物在不锈钢高压釜中在10巴压力下于室温氢化3小时。反应完成后将混合物通过硅藻土垫过滤,用dcm洗涤并将母液蒸发至干得到棕色稠油状标题化合物(5.63g,98%收率),其不经纯化即可用于下一步骤。
[1727]1h-nmr(500mhz,dmso-d6)δppm:7.69-7.37(m,10h),6.65(d,1h),6.1(d,1h),4.55(s,2h),4.52(t,1h),3.87(m,1h),3.48/3.46(dd+dd,2h),3.04/2.97(m+m,2h),2.15(s,3h),1.87/1.79(m+m,2h),1(s,9h),0.77(s,3h),-0.11(s,3h),-0.14(s,3h)。
[1728]
步骤a6:5-溴-1-[(3r)-4-{[叔丁基(二甲基)硅基]氧基}-3-{[叔丁基(二苯基)硅基]氧基}丁基]-4-甲基-1h-苯并三唑的制备
[1729]
将4-溴-n
1-[(3r)-4-{[叔丁基(二甲基)硅基]氧基}-3-{[叔丁基(二苯基)硅基]氧基}丁基]-3-甲基苯-1,2-二胺(1eq.,5.0g,7.8mmol)溶于无水thf(40ml)并将混合物冷却至0℃。于0℃将tfa(10mg,0.0612mmol)加入到混合物中,然后滴加3-甲基丁基亚硝酸酯(1.66eq.,1.8ml,13mmol)。将反应混合物搅拌3小时,同时将温度升至室温。将混合物用thf稀释并蒸发至硅藻土上。将粗产物通过正相硅胶色谱纯化,用庚烷-etoac(100:0至98:2)作为洗脱剂洗脱得到深棕色稠油状标题化合物(2.46g,48%收率)。
[1730]1h-nmr(500mhz,dmso-d6)δppm:7.64(d,1h),7.6-7.31(m,10h),7.43(d,1h),3.75(m,1h),3.74(t,2h),3.47/3.43(dd+dd,2h),2.7(s,3h),2.19/2.04(m+m,2h),0.98(s,9h),0.7(s,9h),-0.17/-0.23(s+s,6h)。
[1731]
步骤a7:(2e)-3-{1-[(3r)-4-{[叔丁基(二甲基)硅基]氧基}-3-{[叔丁基(二苯基)硅基]氧基}丁基]-4-甲基-1h-苯并三唑-5-基}丙-2-烯酸乙酯的制备
[1732]
在微波试管中将5-溴-1-[(3r)-4-{[叔丁基(二甲基)硅基]氧基}-3-{[叔丁基(二苯基)硅基]氧基}丁基]-4-甲基-1h-苯并三唑(1eq.,2.455g,3.76mmol)溶于无水dmf
(10ml)。加入丙-2-烯酸乙酯(2eq.,0.805ml,7.40mmol),然后加入dipea(1.95ml,11.375mmol)。将反应混合物用n2冲洗,然后加入(乙酸-κo)({2-[二(2-甲基苯基)膦基]苯基}甲基)钯(0.1eq.,0.359g,0.382mmol)。将混合物再次用n2冲洗,将试管密封并置于微波反应器中于150℃反应2小时。将混合物通过硅藻土垫过滤,将滤饼用dcm洗涤并将母液蒸发至硅藻土上。将粗产物通过正相硅胶色谱纯化,用庚烷-etoac(100:0至80:20)作为洗脱剂得到黄色稠油状标题化合物(2.19g,88%收率)。
[1733]1h-nmr(500mhz,dmso-d6)δppm:8.02(d,1h),7.93(d,1h),7.62-7.31(m,10h),7.46(d,1h),6.66(d,1h),4.74(t,2h),4.22(q,2h),3.78(m,1h),3.49/3.45(dd+dd,2h),2.8(s,3h),2.19/2.05(m+m,2h),1.28(t,3h),0.99(s,9h),0.71(s,9h),-0.16/-0.21(s+s,6h)。
[1734]
步骤1:3-{1-[(3r)-4-{[叔丁基(二甲基)硅基]氧基}-3-{[叔丁基(二苯基)硅基]氧基}丁基]-4-甲基-1h-苯并三唑-5-基}-3-[3-(羟基甲基)-4-甲基苯基]丙酸乙酯的制备
[1735]
将(2e)-3-{1-[(3r)-4-{[叔丁基(二甲基)硅基]氧基}-3-{[叔丁基(二苯基)硅基]氧基}丁基]-4-甲基-1h-苯并三唑-5-基}丙-2-烯酸乙酯(1eq.,1.43g,2.13mmol)溶于二氧杂环己烷(10ml)并加入[2-甲基-5-(4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷-2-基)苯基]甲醇(1.55eq.,0.81g,3.3mmol),然后加入tea(1.4eq.,0.42ml,3.0mmol)和水(2ml)。将反应混合物用n2冲洗,然后加入氯(1,5-环辛二烯)铑(i)二聚体催化剂(0.051g,0.10mmol)。于80℃搅拌过夜后混合物通过硅藻土垫过滤,将滤饼用dcm洗涤,将母液蒸发并将残余物溶于庚烷。将混合物通过正相硅胶色谱纯化,用庚烷-etoac(100:0至60:40)作为洗脱剂,得到无色稠油状标题化合物(0.99g,59%收率)。
[1736]1h-nmr(500mhz,dmso-d6)δppm:7.62-7.28(m,10h),7.43(d,1h),7.34(d,1h),7.29/7.27(d/d,1h),7.1/7.08(dd/dd,1h),7.03/7.01(d/d,1h),5/4.99(t/t,1h),4.83(t,1h),4.67(t,2h),4.41/4.4(d/d,2h),3.92(m,2h),3.76(m,1h),3.44(m,2h),3.13(m,2h),2.75(s,3h),2.15(s,3h),2.15/2.02(m+m,2h),1.01/1(t/t,3h),0.97(s,9h),0.7/0.68(s/s,9h),-0.18/-0.19/-0.23/-0.26(s/s/s/s,6h)。
[1737]
步骤2:3-(3-{[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-甲基苯基)-3-{1-[(3r)-4-{[叔丁基(二甲基)硅基]氧基}-3-{[叔丁基(二苯基)硅基]氧基}丁基]-4-甲基-1h-苯并三唑-5-基}丙酸乙酯的制备
[1738]
将3-{1-[(3r)-4-{[叔丁基(二甲基)硅基]氧基}-3-{[叔丁基(二苯基)硅基]氧基}丁基]-4-甲基-1h-苯并三唑-5-基}-3-[3-(羟基甲基)-4-甲基苯基]丙酸乙酯(1eq.,0.882g,1.11mmol)、6-(苄氧基)-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮(0.696g,2.39mmol)和pph3(0.57g,2.2mmol)悬浮于干燥的thf(20ml)并一次性加入diad(0.27g,1.3mmol)。将反应混合物室温搅拌24小时。将混合物用dcm稀释,蒸发至硅藻土上并通过正相硅胶色谱纯化,用庚烷-etoac(100:0至80:20)作为洗脱剂,得到白色固体状标题化合物(0.707g,60%收率)。
[1739]1h-nmr(500mhz,dmso-d6)δppm:7.62-7.28(m,18h),7.45(d,1h),7.34(d,1h),7.13(d,1h),7.06(dd,1h),6.96/6.94(d/d,1h),5.09(s,2h),4.86(t,1h),4.66(m,2h),4.43(m,2h),4.2(s,2h),3.92(m,2h),3.76(m,1h),3.42(m,2h),3.18(m,2h),2.76(s,3h),2.22/2.21(s/s,3h),2.15/2(m+m,2h),0.99/0.98(t/t,3h),0.95(s,9h),0.69/0.66(s/s,
9h),-0.2/-0.22/-0.25/-0.3(s/s/s/s,6h)。
[1740]
步骤3:3-{1-[(3r)-4-{[叔丁基(二甲基)硅基]氧基}-3-{[叔丁基(二苯基)硅基]氧基}丁基]-4-甲基-1h-苯并三唑-5-基}-3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}丙酸乙酯的制备
[1741]
将3-(3-{[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-甲基苯基)-3-{1-[(3r)-4-{[叔丁基(二甲基)硅基]氧基}-3-{[叔丁基(二苯基)硅基]氧基}丁基]-4-甲基-1h-苯并三唑-5-基}丙酸乙酯(1eq.,0.577g,0.541mmol)溶于二氧杂环己烷(2ml)和meoh(6ml)的混合物,然后将pd/c(0.05g,0.05mmol)加入到混合物中,将其在不锈钢高压釜中在2巴下于室温氢化过夜。反应完成后将混合物通过硅藻土垫过滤,将滤饼用dcm洗涤,将母液浓缩,将残余物在室温下高真空干燥以得到白色泡沫状标题化合物(0.485g,92%收率)。该产物不经纯化即可用于下一步骤。
[1742]1h-nmr(500mhz,dmso-d6)δppm:9.7(s,1h),7.61-7.08(m,13h),7.47(d,1h),7.36(d,1h),6.99(d,1h),6.79(dd,1h),6.61(d,1h),4.85(t,1h),4.68(m,2h),4.41/4.36(d+d,2h),4.21/4.16(d+d,2h),3.93(m,2h),3.74(m,1h),3.43(m,2h),3.17(m,2h),2.75(s,3h),2.22/2.21(s/s,3h),2.16/2.02(m+m,2h),1.01/1(t/t,3h),0.96(s,9h),0.69/0.66(s/s,9h),-0.2/-0.21/-0.25/-0.29(s/s/s/s,6h)。
[1743]
步骤4:3-{1-[(3r)-3-{[叔丁基(二苯基)硅基]氧基}-4-羟基丁基]-4-甲基-1h-苯并三唑-5-基}-3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}丙酸乙酯的制备
[1744]
将3-{1-[(3r)-4-{[叔丁基(二甲基)硅基]氧基}-3-{[叔丁基(二苯基)硅基]氧基}丁基]-4-甲基-1h-苯并三唑-5-基}-3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}丙酸乙酯(1eq.,0.47g,0.48mmol)溶于etoh(30ml)。加入2m盐酸水溶液(0.5ml,1mmol)并将混合物在室温下搅拌3小时。反应完成后将混合物冷却至0℃并用0.15ml tea中和。将混合物用dcm稀释,蒸发至硅藻土上并通过正相硅胶色谱纯化,用dcm-meoh(100:0至80:20)作为洗脱剂,得到白色固体状标题化合物(0.335g,81%收率)。
[1745]1h-nmr(500mhz,dmso-d6)δppm:9.7(s,1h),7.61-7.09(m,13h),7.47(d,1h),7.36(d,1h),6.99(d,1h),6.79(dd,1h),6.62/6.61(d,1h),4.84(t,1h),4.74(t,1h),4.66(t,2h),4.41/4.36(d+d,2h),4.22/4.17(d+d,2h),3.93(m,2h),3.74(m,1h),3.38(m,2h),3.17(m,2h),2.76/2.75(s/s,3h),2.22/2.21(s/s,3h),2.15/2.02(m+m,2h),1.01/1(t/t,3h),0.96(s,9h)。
[1746]
步骤5:3-{1-[(3r)-3-{[叔丁基(二苯基)硅基]氧基}-4-氯丁基]-4-甲基-1h-苯并三唑-5-基}-3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}丙酸乙酯的制备
[1747]
采用通用方法10,用3-{1-[(3r)-3-{[叔丁基(二苯基)硅基]氧基}-4-羟基丁基]-4-甲基-1h-苯并三唑-5-基}-3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}丙酸乙酯(1当量)作为起始试剂,得到标题化合物(无色油,33%收率)。
[1748]1h-nmr(500mhz,dmso-d6)δppm:9.72(brs,1h),7.54-7.11(m,15h),6.99(d,1h),6.79(dd,1h),6.6(d,1h),4.85(t,1h),4.63(t,2h),4.4/4.36(d+d,2h),4.21/4.17(d+d,2h),3.93(q,2h),3.93(dd,1h),3.67(d,2h),3.18(m,2h),2.76/2.75(s,3h),2.22(s,3h),
2.2/2.11(m+m,2h),1.01/0.99(t/t,3h),0.96/0.95(s/s,9h)。
[1749]
步骤6:[(19r)-19-{[叔丁基(二苯基)硅基]氧基}-4,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯的制备
[1750]
采用通用方法11,用3-{1-[(3r)-3-{[叔丁基(二苯基)硅基]氧基}-4-氯丁基]-4-甲基-1h-苯并三唑-5-基}-3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}丙酸乙酯(1当量)作为起始试剂,得到标题化合物(39%收率)。
[1751]1h-nmr(500mhz,dmso-d6)δppm:7.75-7.25(m,12h),7.51/7.48(d/d,1h),7.31/7.29(d/d,1h),6.92/6.85(d/d,1h),6.55/6.52(d/d,1h),6.43/6.3(dd/dd,1h),5.36/5.28(d/d,1h),4.92/4.64(m+m,2h),4.8(m,1h),4.32/4.16(m/m,1h),4.29/3.72(d+d,2h),4.01/3.61(d+d,2h),3.94/3.92(q/q,2h),3.41/3.14(dd+m,2h),3.12(m,2h),2.59/2.52(s/s,3h),2.5/2.36(m+m,2h),2.33/2.32(s/s,3h),1.07(s,9h),1.03(t,3h)。
[1752]
步骤7:[(19r)-19-羟基-4,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯的制备
[1753]
将[(19r)-19-{[叔丁基(二苯基)硅基]氧基}-4,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯(1eq.,30mg,0.03550mmol)溶于thf(2ml)并加入1m四丁基氟化铵的thf溶液(1.5eq.,0.053ml,0.053mmol)。将反应混合物室温搅拌24小时。将混合物用dmf稀释并通过直接注射通过制备型反相c18柱色谱纯化,得到15mg(70%收率)白色固体泡沫状标题化合物。
[1754]1h-nmr(500mhz,dmso-d6)δppm:7.66/7.65(d,1h),7.49/7.4(d,1h),7.48(dd,1h),7.3/7.27(d,1h),7.02/7(d,1h),6.84/6.83(dd,1h),6.57/6.46(d,1h),6.03/5.74(d,1h),5.33/5.28(brs,1h),4.94-4.7(m,2h),4.78(m,1h),4.24-3.75(d+d,4h),3.93(q,2h),3.85/3.69(m,1h),3.57/3.34(m,2h),3.24-2.99(dd+dd,2h),2.61/2.6(s,3h),2.41/2.26(m+m,2h),2.33/2.32(s,3h),1.01(t,3h)。
[1755]
步骤8:实施例44的制备
[1756]
采用通用方法12,用[(19r)-19-羟基-4,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯(1当量)作为反应试剂,得到标题化合物(白色固体,92%收率)。
[1757]c29h30
n4o7s的hrms计算值:578.1835;[m+h]
+
,实测值:579.1906(δ=-0.3ppm)。
[1758]1h-nmr(500mhz,dmso-d6)δppm:7.6/7.58(d/d,1h),7.54/7.51(brd/brd.,1h),7.41/7.35(d/d,1h),7.24/7.21(d/d,1h),7/6.99(d/d,1h),6.83/6.82(dd/dd,1h),6.37/6.31(d/d,1h),5.94/5.7(brd/d,1h),5.46/5.29(brd/d,1h),4.9-4.68(m,2h),4.8(m,1h),4.07-3.87(m,2h),3.99/3.87(d+d,2h),3.86/3.72(br/br.,1h),3.55-3.24(m,2h),2.59-2.34(m,2h),2.56/2.55(s/s,3h),2.4/2.3(m+m,2h),2.31/2.3(s/s,3h)。
[1759]
13
c-nmr(125mhz,dmso-d6)δppm:173.4,155.9,144.5,131.3,131.1/131,129.1,128.2,119.7/119.5,117.6/117.3,116.9,111.3/11.1,107.4/107.3,73/72.4,65.9/65.8,
52.2/51.8,48.8/48.6,46.9,43.9/43.6,43.5/43,32.9,18.5/18.4,13.5。
[1760]
实施例45:[(19r)-4,19,31-三甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸
[1761][1762]
步骤a1:(2e)-3-(4-氟-2-甲基-3-硝基苯基)丙-2-烯酸乙酯的制备
[1763]
将1-溴-4-氟-2-甲基-3-硝基苯(1eq.,50g,213.66mmol)、(2e)-3-(4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷-2-基)丙-2-烯酸乙酯(1.15eq.,55.55g,245.71mmol)、碳酸钠(2.5eq.,56.61g,534.14mmol)溶于thf(250ml)和水(250ml)的混合物并用n2净化,然后加入a
ta
phos.pdcl2(0.02eq.,1.9g,4.2731mmol)。将反应混合物在n2气氛下加热回流2小时。加入500ml etoac和250ml水。分层,将水层用2x20ml etoac萃取,将合并的有机层用硫酸镁干燥,过滤并减压蒸发。将残余物在玻璃过滤器中通过用250g硅胶过滤纯化,用4l庚烷-etoac(90:10)作为洗脱剂。收集含产物的级分并减压蒸发。将残余物溶于30ml庚烷并通过超声结晶。将沉淀析出的固体过滤并于40℃真空干燥过夜得到48.48g(89.6%收率)白色固体状标题化合物。
[1764]1h-nmr(500mhz,dmso-d6)δppm:8.06(dd,1h),7.8(d,1h),7.52(t,1h),6.64(d,1h),4.21(q,2h),2.36(s,3h),1.27(t,3h)。
[1765]
步骤1:6-(苄氧基)-3-[(5-溴-2-甲基苯基)甲基]-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮的制备
[1766]
采用通用方法7,用(5-溴-2-甲基苯基)甲醇(1当量)和6-(苄氧基)-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮(0.83当量)作为起始试剂,得到标题化合物(65%收率),为白色固体。
[1767]1h-nmr(500mhz,dmso-d6)δppm:7.47(d,1h),7.46(dd,1h),7.44(d,2h),7.4(t,2h),7.34(t,1h),7.21(d,1h),7.13(d,1h),7.06(d,1h),7.05(dd,1h),5.08(s,2h),4.57(s,2h),4.29(s,2h),2.24(s,3h)。
[1768]
步骤2:6-(苄氧基)-3-{[2-甲基-5-(4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷-2-基)苯基]甲基}-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮的制备
[1769]
采用通用方法3,用6-(苄氧基)-3-[(5-溴-2-甲基苯基)甲基]-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮(1当量)作为起始试剂,得到标题化合物(56%收率),为白色固体。
[1770]1h-nmr(500mhz,dmso-d6)δppm:7.58(d,1h),7.54(s,1h),7.47-7.31(m,5h),7.27(d,1h),7.15(d,1h),7.05(dd,1h),7.04(d,1h),5.07(s,2h),4.5(s,2h),4.29(s,2h),2.29(s,3h),1.29(s,12h)。
4-甲基苯基)-3-{1-[(3r)-4-羟基-3-甲基丁基]-4-甲基-3a,7a-二氢-1h-苯并三唑-5-基}丙酸乙酯的制备
[1781]
向3-(3-氨基-4-{[(3r)-4-羟基-3-甲基丁基]氨基}-2-甲基苯基)-3-(3-{[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-甲基苯基)丙酸乙酯(1eq.,1.10g,1.6mmol)的dcm(25ml)溶液中一次性加入3-甲基丁基亚硝酸酯(3eq.,550mg,4.7mmol,0.63ml)。将反应混合物室温搅拌1天。将反应混合物用dcm(100ml)稀释并用盐水洗涤(100ml)。将有机层用硫酸镁干燥,过滤并蒸发。将残余物通过正相硅胶色谱纯化,用庚烷-etoac作为洗脱剂得到标题化合物(560mg,50%收率)。
[1782]1h-nmr(500mhz,dmso-d6)δppm:7.51(d,1h),7.49(d,1h),7.48-7.32(m,5h),7.24(m,1h),7.19(dd,1h),7.14(d,1h),7.14(d,1h),7.07(dd,1h),6.97(d,1h),5.1(s,2h),4.84(t,1h),4.65(m,2h),4.48(t,1h),4.44(s,2h),4.22(s,2h),3.92(q,2h),3.22(m,2h),3.18(m,2h),2.76(s,3h),2.21(s,3h),1.98/1.59(m+m,2h),1.39(m,1h),0.98(t,3h),0.86(d,3h)
[1783]
步骤7:3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}-3-{1-[(3r)-4-羟基-3-甲基丁基]-4-甲基-3a,7a-二氢-1h-苯并三唑-5-基}丙酸乙酯的制备
[1784]
采用通用方法8,用3-(3-{[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-甲基苯基)-3-{1-[(3r)-4-羟基-3-甲基丁基]-4-甲基-3a,7a-二氢-1h-苯并三唑-5-基}丙酸乙酯(1eq.,560mg,0.7856mmol)作为起始试剂,得到标题化合物(460mg,94%收率)。
[1785]1h-nmr(500mhz,dmso-d6)δppm:9.7(s,1h),7.61(d,1h),7.51(d,1h),7.22(d,1h),7.2(dd,1h),7.13(d,1h),6.99(d,1h),6.79(dd,1h),6.61(d,1h),4.84(t,1h),4.68(t,2h),4.5(brs,1h),4.38(s,2h),4.21/4.17(d+d,2h),3.93(q,2h),3.24(m,2h),3.19/3.15(dd+dd,2h),2.75(s,3h),2.22(s,3h),2/1.61(m+m,2h),1.42(m,1h),1(t,3h),0.88(d,3h)。
[1786]
步骤8:3-{1-[(3r)-4-氯-3-甲基丁基]-4-甲基-3a,7a-二氢-1h-苯并三唑-5-基}-3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}丙酸乙酯的制备
[1787]
采用通用方法10,用3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}-3-{1-[(3r)-4-羟基-3-甲基丁基]-4-甲基-3a,7a-二氢-1h-苯并三唑-5-基}丙酸乙酯(1eq.,460mg,0.7387mmol)作为起始试剂,得到标题化合物(470mg,99%收率)。
[1788]1h-nmr(500mhz,dmso-d6)δppm:9.71(s,1h),7.63(d,1h),7.52(d,1h),7.22(d,1h),7.2(dd,1h),7.13(d,1h),6.99(d,1h),6.79(dd,1h),6.6(d,1h),4.84(t,1h),4.71(t,2h),4.38(s,2h),4.21/4.17(d+d,2h),3.93(q,2h),3.63/3.6(dd+dd,2h),3.17(d,2h),2.76(s,3h),2.22(s,3h),2.04/1.77(m+m,2h),1.74(m,1h),1.01(d,3h),0.99(t,3h)。
[1789]
步骤9:[(19r)-4,19,31-三甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯的制备
[1790]
采用通用方法11,用3-{1-[(3r)-4-氯-3-甲基丁基]-4-甲基-3a,7a-二氢-1h-苯并三唑-5-基}-3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}丙酸乙酯(1eq.,470mg,0.7330mmol)作为起始试剂,得到标题化合物(110mg,25%收率)。
[1791]1h-nmr(500mhz,dmso-d6,非对映异构体的混合物)δppm:7.68/7.65(d/d,1h),7.5/7.35(d/d,1h),7.48(dd,1h),7.3/7.28(d/d,1h),7/6.98(d/d,1h),6.81(dd,1h),6.56/6.53(d/d,1h),5.83/5.77(d/d,1h),4.83/4.79/4.75(m+m/m,2h),4.8/4.79(t/t,1h),4.18/4.09/4/3.87(d/d+d/d,2h),4.03/3.94/3.89/3.75(d/d+d/d,2h),3.92(m,2h),3.67/3.42/3.36(m/dd+dd,2h),3.22/3.14/3.06/3.02(dd+dd/dd+dd,2h),2.64/2.59(s/s,3h),2.33/2.11/2.02/1.95(m+m/m+m,2h),2.32(s,3h),2.11/1.6(m/m,1h),1.1/1.04(d/d,3h),1.01/1(t/t,3h)。
[1792]
步骤10:实施例45的制备
[1793]
采用通用方法12,用[(19r)-4,19,31-三甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯(1eq.,110mg,0.1819mmol)作为起始试剂,得到标题化合物(90mg,86%收率)。
[1794]
通过手性柱色谱分离得到非对映异构体。
[1795]
实施例45a(19r,dia1)
[1796]1h-nmr(500mhz,dmso-d6)δppm:12.22(br.,1h),7.64(d,1h),7.49(d,1h),7.49(d,1h),7.28(d,1h),7(d,1h),6.81(dd,1h),6.54(d,1h),5.75(d,1h),4.82/4.74(dm+m,2h),4.75(t,1h),4.17/3.87(d+d,2h),4.04/3.75(d+d,2h),3.35(m,2h),3.03/2.95(dd+dd,2h),2.58(s,3h),2.32(s,3h),2.12/2.03(m+m,2h),2.12(m,1h),1.1(d,3h)。
[1797]
13
c-nmr(125mhz,dmso-d6)δppm:173.2,131.2,131.2,128.8,127.4,119.5,117.4,111.1,107.7,72.4,51.8,48.7,46.2,42,41,33.8,32.3,18.4,17.1,13.4。
[1798]
实施例45b(19r,dia2)
[1799]c30h32
n4o6s的hrms计算值:576.2042;[m+h]
+
,实测值:577.212(δ=0.8ppm)。
[1800]1h-nmr(500mhz,dmso-d6)δppm:12.2(br.,1h),7.68(d,1h),7.49(dd,1h),7.34(d,1h),7.3(d,1h),6.99(d,1h),6.81(dd,1h),6.51(d,1h),5.83(d,1h),4.79(m,2h),4.78(m,1h),4.1/4(d+d,2h),3.95/3.89(d+d,2h),3.67/3.41(dd+dd,2h),3.11/2.91(dd+dd,2h),2.63(s,3h),2.34/1.96(m+m,2h),2.32(s,3h),1.61(m,1h),1.04(d,3h)。
[1801]
13
c-nmr(125mhz,dmso-d6)δppm:173.3,131.6,131.3,128.1,127.4,119.5,116.8,112,108.2,72.8,51.8,48.6,45.9,41.3,40.7,31.5,29.9,18.4,16.6,13.4。
[1802]
实施例46:[(2r,8rs,19s)-19-羟基-2,4,31-三甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸和
[1803]
[(2r,8rs,19s)-19-羟基-2,4,31-三甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸
[1804][1805]
步骤a1:(2s)-4-(4-溴-3-甲基-2-硝基苯氨基)丁烷-1,2-二醇的制备
[1806]
将1-溴-4-氟-2-甲基-3-硝基苯(1eq.,6g,26mmol)、(2s)-4-氨基丁烷-1,2-二醇盐酸盐(1.5eq.,6.9ml,5.40g,38mmol)和dipea(2eq.,9ml,6.68g,51.67mmol)的混合物在n,n-二甲基乙酰胺(120ml)中于100℃搅拌一个周末。将反应混合物倒在碎冰上,用etoac萃取并将水层用etoac洗涤。将合并的有机层用盐水洗涤,用硫酸钠干燥,减压浓缩。将残余物通过正相硅胶色谱纯化,用dcm-meoh作为洗脱剂得到标题化合物(7.47g,91%收率)。
[1807]1h-nmr(500mhz,dmso-d6)δppm:7.54(d,1h),6.74(d,1h),6.29(t,1h),4.72(d,1h),4.55(t,1h),3.5(m,1h),3.23/3.131(dd+m,2h),3.22(q,2h),2.25(s,3h),1.75/1.45(m+m,2h)。
[1808]
步骤a2:(2s)-4-(4-溴-3-甲基-2-硝基苯氨基)-1-{[叔丁基(二甲基)硅基]氧基}丁-2-醇的制备
[1809]
将(2s)-4-(4-溴-3-甲基-2-硝基苯氨基)丁烷-1,2-二醇(1eq.,7.29g,22.8mmol)溶于干燥的dmf(44ml)并加入dipea(2.51eq.,10ml,7.42g,57.41mmol,2.51equiv)。将反应混合物冷却至0℃,然后滴加溶于干燥dmf(13ml)的叔丁基二甲基氯硅烷(1.06eq.,4.2ml,3.65g,24.2mmol)。将温度升温至室温并将混合物在该温度下搅拌过夜。将反应混合物倒在饱和nh4cl溶液上,用etoac萃取并将水层用etoac洗涤。将合并的有机层用盐水洗涤,用硫酸钠干燥,浓缩。将残余物通过正相硅胶色谱纯化,用庚烷-etoac作为洗脱剂得到标题化合物(8.30g,84%收率)。
[1810]1h-nmr(500mhz,dmso-d6)δppm:7.53(d,1h),6.73(d,1h),6.27(t,1h),4.78(d,1h),3.52(m,1h),3.51/3.36(m+m,2h),3.23(q,2h),2.25(s,3h),1.78/1.44(m+m,2h),0.84(s,9h),0.02(s,6h)。
[1811]
步骤a3:4-溴-n-[(3s)-4-{[叔丁基(二甲基)硅基]氧基}-3-{[叔丁基(二苯基)硅基]氧基}丁基]-3-甲基-2-硝基苯胺的制备
[1812]
将(2s)-4-(4-溴-3-甲基-2-硝基苯氨基)-1-{[叔丁基(二甲基)硅基]氧基}丁-2-醇(1eq.,8.24g,19.0mmol)溶于干燥dmf(95ml)并加入咪唑(3eq.,3.87g,56.8mmol),然后加入n,n-二甲基吡啶-4-胺(0.1eq.,0.238g,1.95mmol)。将反应混合物冷却至0℃,然后滴加叔丁基-二苯基氯硅烷(2eq.,10.5g,38.2mmol)。将温度升温至室温并将混合物在该温度下搅拌过夜。将反应混合物倒在冷的饱和nh4cl溶液上,用dcm萃取。将合并的有机层用盐水洗涤,用硫酸钠干燥,减压浓缩。将残余物通过正相硅胶色谱纯化,用庚烷-etoac作为洗脱剂得到标题化合物(13.37g,定量)。
[1813]1h-nmr(500mhz,dmso-d6)δppm:7.65-7.35(m,10h),7.44(d,1h),6.52(d,1h),6.06(t,1h),3.82(m,1h),3.46/3.44(dd+dd,2h),3.17/3.13(m+m,2h),2.24(s,3h),1.8/
1.7(m+m,2h),0.99(s,3h),0.76(s,3h),-0.12/-0.16(s,6h)。
[1814]
步骤a4:4-溴-n
1-[(3s)-4-{[叔丁基(二甲基)硅基]氧基}-3-{[叔丁基(二苯基)硅基]氧基}丁基]-3-甲基苯-1,2-二胺的制备
[1815]
将4-溴-n-[(3s)-4-{[叔丁基(二甲基)硅基]氧基}-3-{[叔丁基(二苯基)硅基]氧基}丁基]-3-甲基-2-硝基苯胺(1eq.,13.0g,19.35mmol)溶于二氧杂环己烷(10ml)和meoh(50ml)。将用二氧杂环己烷洗涤的阮内镍催化剂(0.5eq.,0.8g,9.00mmol)加入到混合物中,将其在不锈钢高压釜中于10巴压力下于室温氢化3小时。反应完成后将混合物用硅藻土垫过滤,将硅藻土用dcm洗涤,将母液浓缩。将残余物通过正相硅胶色谱纯化,用庚烷-etoac作为洗脱剂得到标题化合物(10.90g,88%收率)。
[1816]1h-nmr(500mhz,dmso-d6)δppm:7.69-7.37(m,10h),6.65(d,1h),6.1(d,1h),4.55(s,2h),4.52(t,1h),3.87(m,1h),3.48/3.46(dd+dd,2h),3.04/2.97(m+m,2h),2.15(s,3h),1.87/1.79(m+m,2h),1(s,9h),0.77(s,3h),-0.11(s,3h),-0.14(s,3h)。
[1817]
步骤a5:5-溴-1-[(3s)-4-{[叔丁基(二甲基)硅基]氧基}-3-{[叔丁基(二苯基)硅基]氧基}丁基]-4-甲基-1h-苯并三唑的制备
[1818]
将4-溴-n
1-[(3s)-4-{[叔丁基(二甲基)硅基]氧基}-3-{[叔丁基(二苯基)硅基]氧基}丁基]-3-甲基苯-1,2-二胺(1eq.,8.50g,13mmol)溶于无水thf(40ml)并将混合物冷却至0℃。将2,2,2-三氯乙酸(0.01eq.,17.4mg,0.106mmol)加入到混合物中,然后滴加3-甲基丁基亚硝酸酯(1.8eq.,3.13ml,2.73g,13mmol)。将反应混合物搅拌3小时,同时将温度升温至室温。将混合物用thf稀释并蒸发到硅藻土上。将粗产物通过正相硅胶色谱纯化,用庚烷-etoac作为洗脱剂得到标题化合物(4.67g,54%收率)。
[1819]1h-nmr(500mhz,dmso-d6)δppm:7.64(d,1h),7.6-7.31(m,10h),7.43(d,1h),3.75(m,1h),3.74(t,2h),3.47/3.43(dd+dd,2h),2.7(s,3h),2.19/2.04(m+m,2h),0.98(s,9h),0.7(s,9h),-0.17/-0.23(s+s,6h)。
[1820]
步骤a6:(2e)-3-{1-[(3s)-4-{[叔丁基(二甲基)硅基]氧基}-3-{[叔丁基(二苯基)硅基]氧基}丁基]-4-甲基-1h-苯并三唑-5-基}丙-2-烯酸乙酯的制备
[1821]
将5-溴-1-[(3s)-4-{[叔丁基(二甲基)硅基]氧基}-3-{[叔丁基(二苯基)硅基]氧基}丁基]-4-甲基-1h-苯并三唑(1eq.,5.09g,7.80mmol)溶于无水dmf(10ml)。加入丙-2-烯酸乙酯(2eq.,1.70ml 1.56g,15.6mmol)和dipea(3eq.,4.07ml,3.02g,23.4mmol)并将反应混合物用n
2.
冲洗。加入乙酰氧基-[[2-(二-邻-甲苯基膦基)苯基]甲基]钯(0.1eq.,731mg,0.780mmol)催化剂并将混合物在微波反应器中于150℃加热7小时。将混合物通过硅藻土垫过滤并将滤液通过反相色谱纯化得到标题化合物(2.58g,49%收率)。
[1822]1h-nmr(500mhz,dmso-d6)δppm:8.02(d,1h),7.93(d,1h),7.62-7.31(m,10h),7.46(d,1h),6.66(d,1h),4.74(t,2h),4.22(q,2h),3.78(m,1h),3.49/3.45(dd+dd,2h),2.8(s,3h),2.19/2.05(m+m,2h),1.28(t,3h),0.99(s,9h),0.71(s,9h),-0.16/-0.21(s+s,6h)。
[1823]
步骤1:6-(苄氧基)-3-[(1r)-1-(5-溴-2-甲基苯基)乙基]-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮的制备
[1824]
采用通用方法7,用(1r)-1-(5-溴-2-甲基苯基)乙-1-醇(1.4eq.,30.08g,139.8mmol)和6-(苄氧基)-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮(1eq.,29.10g,
99.9mmol)作为起始试剂,得到标题化合物(41.6g,85%收率),为白色固体。
[1825]1h-nmr(500mhz,dmso-d6)δppm:7.6(d,1h),7.47-7.31(m,5h),7.44(dd,1h),7.2(d,1h),7.03(d,1h),7.03(d,1h),6.97(dd,1h),5.27(q,1h),5.09/5.06(d+d,2h),4.5(s,2h),2.33(s,3h),1.42(d,3h)。
[1826]
步骤2:6-(苄氧基)-3-{(1r)-1-[2-甲基-5-(4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷-2-基)苯基]乙基}-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮的制备
[1827]
采用通用方法3,用6-(苄氧基)-3-[(1r)-1-(5-溴-2-甲基苯基)乙基]-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮(1eq.,60g,122.9mmol)作为起始试剂,得到标题化合物(60.7g,92%收率)。
[1828]1h-nmr(500mhz,dmso-d6)δppm:7.62(d,1h),7.58(dd,1h),7.43(d,2h),7.39(t,2h),7.33(t,1h),7.27(d,1h),7.04(d,1h),7.02(d,1h),6.98(dd,1h),5.3(q,1h),5.07/5.03(d+d,2h),4.4(s,2h),2.39(s,3h),1.44(d,3h),1.3(s,6h),1.29(s,6h)。
[1829]
步骤3:3-(3-{(1r)-1-[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]乙基}-4-甲基苯基)-3-{1-[(3s)-4-{[叔丁基(二甲基)硅基]氧基}-3-{[叔丁基(二苯基)硅基]氧基}丁基]-4-甲基-1h-苯并三唑-5-基}丙酸乙酯的制备
[1830]
采用通用方法6,用(2e)-3-{1-[(3s)-4-{[叔丁基(二甲基)硅基]氧基}-3-{[叔丁基(二苯基)硅基]氧基}丁基]-4-甲基-1h-苯并三唑-5-基}丙-2-烯酸乙酯(1eq.,2.87g,4.28mmol)和6-(苄氧基)-3-{(1r)-1-[2-甲基-5-(4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷-2-基)苯基]乙基}-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮(1.2eq.,2.75g,5.13mmol)作为起始试剂,得到标题化合物(3.34g,72%收率)。
[1831]1h-nmr(500mhz,dmso-d6,非对映异构体的混合物)δppm:7.61-7.06(m,20h),7.06/7.05(d/d,1h),7.01/6.99(dd/dd,1h),6.9/6.85(d/d,1h),5.27(m,1h),5.09/5.06(d+d,2h),4.88/4.87(t/t,1h),4.66(m,2h),4.53-4.31(m,2h),3.92/3.91(q/q,2h),3.73(m,1h),3.46-3.36(m,2h),3.23(m,2h),2.77(s,3h),2.28/2.27(s/s,3h),2.15/2(m+m,2h),1.42(d,3h),0.99/0.98(t/t,3h),0.96/0.94(s/s,9h),0.68/0.66(s/s,9h),-0.2/-0.21/-0.25/-0.29(s/s/s/s,6h)。
[1832]
步骤4:3-{1-[(3s)-3-{[叔丁基(二苯基)硅基]氧基}-4-羟基丁基]-4-甲基-1h-苯并三唑-5-基}-3-{3-[(1r)-1-(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)乙基]-4-甲基苯基}丙酸乙酯的制备
[1833]
采用通用方法8,用3-(3-{(1r)-1-[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]乙基}-4-甲基苯基)-3-{1-[(3s)-4-{[叔丁基(二甲基)硅基]氧基}-3-{[叔丁基(二苯基)硅基]氧基}丁基]-4-甲基-1h-苯并三唑-5-基}丙酸乙酯(1eq.,3.56g,3.29mmol)作为反应试剂,得到粗产物3-{1-[(3s)-4-{[叔丁基(二甲基)硅基]氧基}-3-{[叔丁基(二苯基)硅基]氧基}丁基]-4-甲基-1h-苯并三唑-5-基}-3-{3-[(1r)-1-(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)乙基]-4-甲基苯基}丙酸乙酯(3.23g)。将粗产物(1当量)溶于etoh(200ml)并加入氯化氢(1m水溶液)(2eq.,7.18ml,7.18mmol)。将混合物在室温下搅拌24小时,然后将混合物用tea(20mmol,2.8ml)中和并将溶剂蒸发。将粗产物通过反相色谱纯化,用5mm nh4hco3水溶液-mecn作为洗脱剂得到标题化合物(1.97g,62%收率)。
[1834]1h-nmr(500mhz,dmso-d6,非对映异构体的混合物)δppm:9.66/9.64(s/s,1h),7.61-7.02(m,15h),6.92(d,1h),6.73(dd,1h),6.61/6.57(d/d,1h),5.26(q,1h),4.89/4.87(t/t,1h),4.75/4.66(t/t,2h),4.44-4.25(m,2h),3.94(q,2h),3.73(m,1h),3.38(m,2h),3.23(m,2h),2.8/2.77(s/s,3h),2.28/2.27(s/s,3h),2.26/2.15/2.02/1.84(m/m+m/m,2h),1.43/1.41(d/d,3h),1.01(t,3h),0.96/0.95/0.87/0.82(s/s+s/s,9h)。
[1835]
步骤5:[(2r,19s)-19-羟基-2,4,31-三甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯的制备
[1836]
采用通用方法10,用3-{1-[(3s)-3-{[叔丁基(二苯基)硅基]氧基}-4-羟基丁基]-4-甲基-1h-苯并三唑-5-基}-3-{3-[(1r)-1-(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)乙基]-4-甲基苯基}丙酸乙酯(1eq.,1.97g,2.24mmol)作为反应试剂,得到粗产物3-{1-[(3s)-3-{[叔丁基(二苯基)硅基]氧基}-4-氯丁基]-4-甲基-1h-苯并三唑-5-基}-3-{3-[(1r)-1-(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)乙基]-4-甲基苯基}丙酸乙酯(2.01g)。将其不经进一步纯化用通用方法11进行反应得到标题化合物(77mg,4%收率)。
[1837]1h-nmr(500mhz,dmso-d6,非对映异构体的混合物)δppm:7.89/7.44(d/d,1h),7.7/7.69(d/d,1h),7.44-6.68(m,3h),7/6.94(d/d,1h),6.84/6.76(dd/dd,1h),5.97/5.93(d/brd,1h),5.39/5.14(d/d,1h),5.25/5.23(q/q,1h),4.94/4.74(t/t,2h),4.92/4.81(t/t,1h),4.04/4.02/3.41/3.31(d+d/d+d,2h),3.98/3.25(m/m,1h),3.95/3.94(q/q,2h),3.81/3.6/3.57/3.53(d+d/d+d,2h),3.41/3.33/3.12/3.01(dd+dd/dd+dd,2h),2.81/2.69(s/s,3h),2.43/1.99/1.98(m+m/m,2h),2.32/2.29(s/s,3h),1.28/1.08(d/d,3h),1.03/1.02(t/t,3h)
[1838]
步骤6:实施例46的制备
[1839]
采用通用方法12,用[(2r,19s)-19-羟基-2,4,31-三甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯(1eq.,69mg,0.1112mmol)作为起始试剂,得到标题化合物(38mg,58%收率)。
[1840]
通过手性柱色谱分离得到对映体纯产物。
[1841]
实施例46a(2r,8s,19s)
[1842]c30h32
n4o7s的hrms计算值:592.1992;[m+h]
+
,实测值:593.2056(δ=-1.4ppm)。
[1843]1h-nmr(500mhz,dmso-d6)δppm:7.86(d,1h),7.67(d,1h),7.43(dd,1h),7.18(d,1h),7.13(brs.,1h),7(d,1h),6.84(dd,1h),5.91(d,1h),5.4(br.,1h),5.23(q,1h),4.8(m,2h),4.78(t,1h),4.03/3.3(d+d,2h),3.98(m,1h),3.6/3.52(dd+dd,2h),3.15/2.93(dd+dd,2h),2.65(s,3h),2.28(s,3h),2(m,2h),1.25(d,3h)。
[1844]
13
c-nmr(125mhz,dmso-d6)δppm:131.2,129.5,126.2,125.7,119.7,118.5,109.2,107.6,72.8,66,55.5,45,44,42.7,42.2,35.3,18.5,14.4,13.4。
[1845]
实施例46b(2r,8r,19s)
[1846]c30h32
n4o7s的hrms计算值:592.1992;[m+h]
+
,实测值:593.2051(δ=-2.3ppm)。
[1847]1h-nmr(500mhz,dmso-d6)δppm:7.67(d,1h),7.46(d,1h),7.28(d,1h),7.06(d,
1h),6.94(d,1h),6.76(dd,1h),6.68(brs.,1h),5.95(brs.,1h),5.22(q,1h),5.15(br.,1h),4.94/4.72(dd+dd,2h),4.91(br.,1h),4.05/3.42(d+d,2h),3.82/3.6(d+d,2h),3.26(br.,1h),3.26/2.81(br+br.,2h),2.8(brs.,3h),2.43/2(br+br.,2h),2.31(s,3h),1.07(d,3h)。
[1848]
13
c-nmr(125mhz,dmso-d6)δppm:131.4,128.4,128.1,125.8,119.9,118,109.2,108.7,73.1,64.2,55.3,44.9,44.4,40.6,39.7,31.1,18.5,14.2,13.3。
[1849]
实施例47:[4-甲氧基-21,34-二甲基-30,30-二氧代-24,29-二氧杂-30λ
6-硫杂-1,14,15,16,21-五氮杂六环[23.5.3.1
3,7
.1
9,13
.0
12,16
.0
28,32
]三十五碳-3(35),4,6,9(34),10,12,14,25,27,32-十烯-8-基]乙酸
[1850][1851]
步骤1:3-[1-(4-氯丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲氧基苯基}丙酸乙酯盐酸盐的制备
[1852]
采用通用方法10,用3-[1-(4-羟基丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲氧基苯基}丙酸乙酯(1当量)作为起始试剂,得到标题化合物(黄色固体泡沫,定量)。
[1853]1h-nmr(500mhz,dmso-d6)δppm:7.65(d,1h),7.51(d,1h),7.26(d,1h),7.23(dd,1h),6.89(d,1h),6.83(d,1h),6.72(dd,1h),6.6(d,1h),4.82(t,1h),4.7(t,2h),4.47(s,2h),4.19(s,2h),3.93(q,2h),3.69(s,3h),3.64(t,2h),3.14(d,2h),2.75(s,3h),1.99(m,2h),1.68(m,2h),1(t,3h)。
[1854]
步骤2:3-(1-{4-[苄基(甲基)氨基]丁基}-4-甲基-1h-苯并三唑-5-基)-3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲氧基苯基}丙酸乙酯的制备
[1855]
在室温下向搅拌中的3-[1-(4-氯丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲氧基苯基}丙酸乙酯盐酸盐(1eq.,1.2g,1.9mmol)的mecn(10ml)溶液中加入n-甲基-1-苯基甲胺(3eq.,0.68g,5.6mmol)并将混合物于80℃加热过夜。将粗产物通过反相色谱纯化,用5mm nh4hco3水溶液-mecn作为洗脱剂得到米黄色固体泡沫状标题化合物(0.82g,61%收率)。
[1856]1h-nmr(500mhz,dmso-d6)δppm:9.63(s,1h),7.6(d,1h),7.49(d,1h),7.29-7.18(m,5h),7.26(d,1h),7.25(dd,1h),6.88(d,1h),6.83(d,1h),6.7(dd,1h),6.58(d,1h),4.82(t,1h),4.64(t,2h),4.47(s,2h),4.19(s,2h),3.93(q,2h),3.69(s,3h),3.37(s,2h),3.14(d,2h),2.75(s,3h),2.3(t,2h),2.01(s,3h),1.9(qn,2h),1.41(qn,2h),1(t,3h)。
[1857]
步骤3:3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲
氧基苯基}-3-{4-甲基-1-[4-(甲基氨基)丁基]-1h-苯并三唑-5-基}丙酸乙酯的制备
[1858]
采用通用方法8,用3-(1-{4-[苄基(甲基)氨基]丁基}-4-甲基-1h-苯并三唑-5-基)-3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲氧基苯基}丙酸乙酯(1eq.,0.83g,1.13mmol)作为起始试剂,得到标题化合物(白色固体泡沫,0.4g,56%收率)。
[1859]1h-nmr(500mhz,dmso-d6)δppm:7.63(d,1h),7.5(d,1h),7.25(d,1h),7.24(dd,1h),6.89(d,1h),6.83(d,1h),6.7(dd,1h),6.57(d,1h),4.81(t,1h),4.64(t,2h),4.47(s,2h),4.2/4.17(d+d,2h),3.94(q,2h),3.69(s,3h),3.14(d,2h),2.75(s,3h),2.42(t,2h),2.19(s,3h),1.89(qn,2h),1.33(qn,2h),1.01(t,3h)。
[1860]
步骤4:[4-甲氧基-21,34-二甲基-30,30-二氧代-24,29-二氧杂-30λ
6-硫杂-1,14,15,16,21-五氮杂六环[23.5.3.1
3,7
.1
9,13
.0
12,16
.0
28,32
]三十五碳-3(35),4,6,9(34),10,12,14,25,27,32-十烯-8-基]乙酸乙酯的制备
[1861]
在室温下向搅拌中的3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲氧基苯基}-3-{4-甲基-1-[4-(甲基氨基)丁基]-1h-苯并三唑-5-基}丙酸乙酯(1eq.,0.286g,0.448mmol)的mecn(6ml)溶液中加入cs2co3(5eq.,0.73g,2.24mmol)和1,2-二溴乙烷(5eq.,0.193ml,2.24mmol)并将混合物于80℃加热5小时。将粗产物通过反相色谱纯化,用5mm nh4hco3水溶液-mecn作为洗脱剂得到白色固体状标题化合物(0.045g,15%收率)。
[1862]1h-nmr(500mhz,dmso-d6)δppm:7.63(d,1h),7.55(d,1h),7.44(dd,1h),7.14(d,1h),7.07(d,1h),7(dd,1h),6.96(d,1h),6.47(d,1h),4.8(t,1h),4.76/4.69(m+m,2h),4.37/3.96(d+d,2h),4.27/3.92(d+d,2h),4.12/4.05(m+m,2h),3.89(q,2h),3.77(s,3h),3.14/3.07(dd+dd,2h),2.76(s,3h),2.73/2.7(m+m,2h),2.59/2.42(m+m,2h),2.22(s,3h),1.96(qn,2h),1.63(m,2h),0.98(t,3h)。
[1863]
步骤5:实施例47的制备
[1864]
采用通用方法12,用[4-甲氧基-21,34-二甲基-30,30-二氧代-24,29-二氧杂-30λ
6-硫杂-1,14,15,16,21-五氮杂六环[23.5.3.1
3,7
.1
9,13
.0
12,16
.0
28,32
]三十五碳-3(35),4,6,9(34),10,12,14,25,27,32-十烯-8-基]乙酸乙酯(1eq.,41mg,0.0617mmol)作为起始试剂,得到标题化合物(白色固体,35mg,89%收率)。
[1865]c32h37
n5o7s的hrms计算值:635.2414;[m+h]
+
实测值=636.2479(δ=-1.2ppm)。
[1866]1h-nmr(500mhz,dmso-d6)δppm 12.42(brs,1h),7.64(d,1h),7.54(d,1h),7.45(dd,1h),7.11(d,1h),7.07(d,1h),7(dd,1h),6.96(d,1h),6.45(d,1h),4.78(t,1h),4.76/4.7(m+m,2h),4.36/3.97(d+d,2h),4.27/3.91(d+d,2h),4.13/4.05(m+m,2h),3.77(s,3h),3.03/2.98(dd+dd,2h),2.75(s,3h),2.74/2.69(m+m,2h),2.6/2.43(m+m,2h),2.23(s,3h),1.96(m,2h),1.63(m,2h)。
[1867]
13
c-nmr(125mhz,dmso-d6)δppm:131.2,130.9,126.8,119.1,114.5,114.4,111.7,108,66.7,56.6,56.2,56.2,48.6,48.6,47.5,42.6,41,41,27.3,23.4,13.3。
[1868]
实施例48:[(8r)-11-溴-4,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸
[1869][1870]
步骤1:[(8r)-11-溴-4,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯的制备
[1871]
在室温下向搅拌中的[(8r)-4,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯(1eq.,1.47g,2.49mmol)的硝基甲烷(15ml)溶液中加入过一硫酸氢钾(3eq.,3.595g,7.466mmol)和溴化钾(0.77eq.,0.23g,1.93mmol),然后将混合物于60℃搅拌2天。将反应混合物溶于etoac(150ml)并将有机层用10%na2s2o3水溶液(150ml)洗涤。将有机层用无水mgso4干燥,过滤并减压浓缩。将残余物通过正相硅胶色谱纯化,用庚烷-etoac梯度洗脱得到白色固体状标题化合物(0.63g,38%收率)。
[1872]1h-nmr(500mhz,dmso-d6)δppm:7.63(s,1h),7.49(dd,1h),7.3(d,1h),7(d,1h),6.81(dd,1h),6.5(d,1h),5.73(d,1h),5.18/4.82(dm+m,2h),4.74(m,1h),4.27/3.83(d+d,2h),4.04/3.76(d+d,2h),3.95(m,2h),3.58/3.12(dt+m,2h),3.11(m,2h),2.59(s,3h),2.33(s,3h),2.27/2.17(m+m,2h),1.91/1.68(m+m,2h),1.03(t,3h)。
[1873]
步骤2:实施例48的制备
[1874]
采用通用方法12,用[(8r)-11-溴-4,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯(1eq.,308mg,0.46mmol)作为起始试剂,得到标题化合物(白色固体,144mg,49%收率)。
[1875]1h-nmr(500mhz,dmso-d6)δppm:12.28(brs,1h),7.6(s,1h),7.5(dd,1h),7.3(d,1h),7(d,1h),6.81(dd,1h),6.49(d,1h),5.73(d,1h),5.19/4.82(m+m,2h),4.82(t,1h),4.26/3.84(d+d,2h),4.03/3.77(d+d,2h),3.58/3.13(m+m,2h),3(d,2h),2.59(s,3h),2.33(s,3h),2.27/2.18(m+m,2h),1.91/1.69(qn+qn,2h)。
[1876]
实施例49:[(8r)-4,31-二甲基-27,27-二氧代-11-苯基-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸
[1877][1878]
步骤1:[(8r)-4,31-二甲基-27,27-二氧代-11-苯基-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯的制备
[1879]
在氮气氛下,将[(8r)-11-溴-4,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯(1eq.,300g,0.448mmol)、苯基硼酸(3eq.,164mg,1.344mmol)、cs2co3(3eq.,438mg,1.344mmol)、a
ta
phos.pdcl2催化剂(0.1eq.,20mg,0.0448mmol)、thf(4ml)和水(4ml)的混合物在微波反应器中于100℃加热1小时。将混合物冷却后,分层,将水层进一步用2x5ml etoac萃取。将合并的有机层用硫酸镁干燥,减压蒸发。粗产物含有2种阻转异构体的混合物(比率:94:6)。将残余物通过反相色谱纯化,用5mm nh4hco3水溶液-mecn作为洗脱剂得到白色固体状标题化合物(非对映异构体1,232mg,78%收率)。
[1880]1h-nmr(500mhz,dmso-d6)δppm:7.49(dd,1h),7.47(t,1h),7.45(t,2h),7.31(s,1h),7.28(d,1h),7.21(br.,2h),7.08(d,1h),6.83(d,1h),6.8(dd,1h),5.82(d,1h),4.79(t,1h),4.77/4.32(dd+dt,2h),4.39/3.95(d+d,2h),4.13/3.83(d+d,2h),3.86(q,2h),3.35/2.95(m+m,2h),3.06(d,2h),2.72(s,3h),2.35(s,3h),1.43/1.1(m+m,2h),1.35/1.1(m+m,2h),0.9(t,3h)。
[1881]
步骤2:实施例49的制备
[1882]
采用通用方法12,用[(8r)-4,31-二甲基-27,27-二氧代-11-苯基-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯(1eq.,228mg,0.342mmol)作为起始试剂,得到标题化合物(白色固体,193mg,88%收率)。
[1883]c35h34
n4o6s的hrms计算值:638.2199;[m+h]
+
,实测值:639.2263(δ=-1.4ppm)。
[1884]1h-nmr(500mhz,dmso-d6)δppm:12.11(brs,1h),7.49(dd,1h),7.47(t,1h),7.45(t,2h),7.29(s,1h),7.28(d,1h),7.22(br,2h),7.08(d,1h),6.82(d,1h),6.79(dd,1h),5.83(d,1h),4.77/4.33(m+m,2h),4.77(t,1h),4.38/3.97(d+d,2h),4.12/3.85(d+d,2h),3.34/2.97(m+m,2h),2.96(d,2h),2.73(s,3h),2.35(s,3h),1.43/1.08(m+m,2h),1.34/1.08(m+m,2h)。
[1885]
13
c-nmr(125mhz,dmso-d6)δppm:173.1,155.9,147.3,144.4,141.7,137.8,136.8,136.4,132,131.3,131.3,129.3,129,128.8,128.6,127.9,127,123.8,119.6,117.8,117.1,110.2,67.4,52.4,50.5,48.8,41.6,41.2,25.6,24.1,18.6,13.3。
[1886]
实施例50:[(8r)-11-氯-4,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸
[1887][1888]
步骤1:[(8r)-11-氯-4,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯和
[1889]
[(8r)-11,30-二氯-4,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯和
[1890]
[(8r)-11,23-二氯-4,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯的制备
[1891]
在室温下向搅拌中的[(8r)-4,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯(1eq.,0.5g,0.846mmol)的硝基甲烷(10ml)溶液中加入过一硫酸氢钾(3eq.,1.223g,2.54mmol)和氯化钾(1.5eq.,95mg,1.269mmol),然后将混合物于60℃搅拌24小时。将反应混合物用dcm(20ml)稀释并将有机层用水(20ml)洗涤。将有机层用无水mgso4干燥,过滤并减压蒸发。将残余物通过反相色谱纯化,用5mm hcooh水溶液-mecn作为洗脱剂得到3种标题化合物:
[1892]
[(8r)-11-氯-4,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯(61mg,12%收率),
[1893]1h-nmr(500mhz,dmso-d6)δppm:7.52(s,1h),7.49(dd,1h),7.3(d,1h),7(d,1h),6.82(dd,1h),6.53(d,1h),5.76(d,1h),5.1/4.89(m+m,2h),4.75(t,1h),4.3/3.83(d+d,2h),4.05/3.76(d+d,2h),3.95(q,2h),3.61/3.17(t+t,2h),3.12(dd,2h),2.61(s,3h),2.33(s,3h),2.22/2.14(m,2h),1.9/1.67(m,2h),1.03(t,3h)。
[1894]
[(8r)-11,30-二氯-4,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯(74mg),
[1895]1h-nmr(500mhz,dmso-d6)δppm:7.48(dd,1h),7.34(s,1h),7.33(d,1h),7.11(d,1h),7.05(d,1h),6.43(d,1h),5.07/4.85(dm+m,2h),4.74(dd,1h),4.27/4(d+d,2h),4.09/
3.87(d+d,2h),4.04/3.78(m+m,2h),3.91(q,2h),3.27/3.09(dd+dd,2h),2.62(s,3h),2.43/2.12(m+m,2h),2.34(s,3h),1.74/1.43(m+m,2h),0.98(t,3h)。
[1896]
[(8r)-11,23-二氯-4,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯(42mg)。
[1897]1h-nmr(500mhz,dmso-d6)δppm:7.57(s,1h),7.48(dd,1h),7.36(s,1h),7.27(d,1h),6.66(d,1h),6.02(s,1h),5.09/4.93(m+m,2h),4.73(t,1h),4.44/3.78(d+d,2h),4.09/3.65(d+d,2h),3.97/3.93(m+m,2h),3.6/3.04(m+m,2h),3.15/3.04(dd+dd,2h),2.62(s,3h),2.32(s,3h),2.28/2.08(m+m,2h),1.9/1.67(m+m,2h),1.03(t,3h)。
[1898]
步骤2:实施例50的制备
[1899]
采用通用方法12,用[(8r)-11-氯-4,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯(1eq.,54mg,0.086mmol)作为起始试剂,得到标题化合物(白色固体,26mg,50%收率)。
[1900]c29h29
cln4o6s的hrms计算值:596.1496;[m+h]
+
,实测值:597.156(δ=-1.5ppm)。
[1901]1h-nmr(500mhz,dmso-d6)δppm:7.5(dd,1h),7.49(s,1h),7.29(d,1h),7(d,1h),6.81(dd,1h),6.5(d,1h),5.74(d,1h),5.09/4.87(m+m,2h),4.72(t,1h),4.28/3.83(d+d,2h),4.04/3.76(d+d,2h),3.6/3.17(dm+dm,2h),3.02/2.98(dd+dd,2h),2.6(s,3h),2.33(s,3h),2.22/2.15(m+m,2h),1.9/1.68(m+m,2h)。
[1902]
13
c-nmr(125mhz,dmso-d6)δppm:131.4,131.1,129,127.6,119.5,117.1,111.3,67.9,51.9,50,48.7,41.6,40.8,26.5,26.3,18.5,13.3。
[1903]
实施例51:[(8r)-11,30-二氯-4,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸
[1904][1905]
采用通用方法12,用[(8r)-11,30-二氯-4,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯(1eq.,69mg,0.1046mmol)作为起始试剂,得到标题化合物(白色固体,57mg,86%收率)。
[1906]c29h28
cl2n4o6s的hrms计算值:630.1107;[m+h]
+
,实测值:631.1179(δ=-0.1ppm)。
[1907]1h-nmr(500mhz,dmso-d6)δppm:7.49(dd,1h),7.32(d,1h),7.3(s,1h),7.11(d,1h),7.04(d,1h),6.43(d,1h),5.07/4.85(dm+m,2h),4.72(t,1h),4.27/4(d+d,2h),4.09/
3.87(d+d,2h),4.03/3.76(m+m,2h),3.17/2.96(dd+dd,2h),2.62(s,3h),2.44/2.13(m+m,2h),2.34(s,3h),1.74/1.45(m+m,2h)。
[1908]
13
c-nmr(125mhz,dmso-d6)δppm:131.5,131.5,127.7,127.6,117.6,117.6,70.3,52.6,49.9,47.4,40.3,39.8,27.2,26.7,18.5,13.2。
[1909]
实施例52:[(8r)-11,23-二氯-4,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸
[1910][1911]
采用通用方法12,用[(8r)-11,23-二氯-4,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯(1eq.,38mg,0.0576mmol)作为起始试剂,得到标题化合物(白色固体,23mg,63%收率)。
[1912]c29h28
cl2n4o6s的hrms计算值:630.1107;[m+h]
+
,实测值:631.1173(δ=-1.0ppm)。
[1913]1h-nmr(500mhz,dmso-d6)δppm:7.55(s,1h),7.49(dd,1h),7.36(s,1h),7.27(d,1h),6.64(d,1h),6.01(s,1h),5.09/4.93(m+m,2h),4.71(t,1h),4.43/3.78(d+d,2h),4.09/3.66(d+d,2h),3.6/3.04(m+m,2h),3.04/2.94(dd+dd,2h),2.61(s,3h),2.32(s,3h),2.28/2.08(m+m,2h),1.9/1.66(m+m,2h)。
[1914]
13
c-nmr(125mhz,dmso-d6)δppm:151.4,131.3,131.1,129.3,127.5,120,111.4,68.5,52,49.8,48.7,41.9,40.8,26.2,26,18.5,13.4。
[1915]
实施例53:[4-甲氧基-39-甲基-35,35-二氧代-21,29,34-三氧杂-35λ
6-硫杂-1,14,15,16-四氮杂七环[28.5.3.1
3,7
.1
9,13
.0
12,16
.0
22,27
.0
33,37
]四十碳-3(40),4,6,9(39),10,12,14,22,24,26,30,32,37-十三烯-8-基]乙酸
[1916][1917]
步骤1:3-{1-[4-(2-甲酰基苯氧基)丁基]-4-甲基-1h-苯并三唑-5-基}-3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲氧基苯基}丙酸乙酯的制备
[1918]
将3-[1-(4-氯丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲氧基苯基}丙酸乙酯盐酸盐(1eq.,0.5g,0.78mmol)溶于干燥dmf(8ml)并加入2-羟基苯甲醛(24eq.,2ml,19mmol),然后加入cs2co3(0.50g,1.5mmol)。在n2气氛下将反应混合物于120℃搅拌1小时。1小时后补加0.5g(1.5mmol)cs2co3并将混合物于120℃继续搅拌2小时。将混合物冷却至室温,倒在冰上并用dcm萃取。将合并的有机层用硫酸钠干燥,过滤并减压蒸发。将粗产物通过正相硅胶色谱纯化,用dcm-meoh(100:0至97.5:2.5)作为洗脱剂,得到0.426g(75%收率)浅棕色泡沫状标题化合物。
[1919]1h-nmr(500mhz,dmso-d6)δppm:10.32(s,1h),9.62(s,1h),7.66(d,1h),7.66(dd,1h),7.6(ddd,1h),7.5(d,1h),7.26(d,1h),7.23(dd,1h),7.16(d,1h),7.04(t,1h),6.89(d,1h),6.83(d,1h),6.7(dd,1h),6.58(d,1h),4.81(t,1h),4.75(t,2h),4.48(s,2h),4.21/4.17(d+d,2h),4.13(t,2h),3.94(q,2h),3.69(s,3h),3.14(d,2h),2.75(s,3h),2.1(m,2h),1.74(m,2h),1.01(t,3h)。
[1920]
步骤2:3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲氧基苯基}-3-(1-{4-[2-(羟基甲基)苯氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯的制备
[1921]
将3-{1-[4-(2-甲酰基苯氧基)丁基]-4-甲基-1h-苯并三唑-5-基}-3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲氧基苯基}丙酸乙酯(1eq.,0.350g,0.480mmol)溶于etoh(2ml)并加入硼氢化钠(2.75eq.,50mg,1.322mmol)。将反应混合物室温搅拌1小时。将混合物倒在碎冰上并减压蒸发。将残余物在水和etoac之间进行分配,分相,将水相用另一份etoac萃取。将合并的有机相用硫酸钠干燥,过滤并蒸发至硅藻土上。将粗产物通过正相硅胶色谱纯化,用dcm-meoh(100:0至95.2:4.8)作为洗脱剂,得到0.33g(94%收率)米白色状泡沫状标题化合物。
[1922]1h-nmr(500mhz,dmso-d6)δppm:9.62(s,1h),7.66(d,1h),7.51(d,1h),7.35(d,1h),7.26(d,1h),7.23(dd,1h),7.15(t,1h),6.9(t,1h),6.89(d,1h),6.87(d,1h),6.84(d,1h),6.71(dd,1h),6.59(d,1h),4.94(t,1h),4.82(t,1h),4.73(t,2h),4.6(d,2h),4.48(s,2h),4.19(s,2h),3.96(t,2h),3.94(q,2h),3.69(s,3h),3.15(d,2h),2.76(s,3h),2.06(m,2h),1.68(m,2h),1.01(t,3h)。
[1923]
步骤3:3-(1-{4-[2-(氯甲基)苯氧基]丁基}-4-甲基-1h-苯并三唑-5-基)-3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲氧基苯基}丙酸乙酯的制备
[1924]
将3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲氧基苯基}-3-(1-{4-[2-(羟基甲基)苯氧基]丁基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯(1eq.,0.330g,0.452mmol)溶于干燥dcm(2ml)并将混合物冷却至0℃。加入亚硫酰氯(70μl,0.95965mmol)并将反应混合物于0℃搅拌30分钟。反应完成后将挥发物蒸发至干,通过从残余物中蒸发dcm除去过量试剂。将粗产物在室温下高真空干燥得到0.441g(定量)米白色泡沫状标题化合物。
[1925]1h-nmr(500mhz,dmso-d6)δppm:9.66(brs,1h),7.66(d,1h),7.5(d,1h),7.35(dm,1h),7.29(m,1h),7.26(d,1h),7.23(dd,1h),6.97(dm,1h),6.9(m,1h),6.89(d,1h),6.84
(d,1h),6.71(dd,1h),6.59(d,1h),4.82(t,1h),4.75(t,2h),4.64(s,2h),4.48(s,2h),4.19(s,2h),4.04(t,2h),3.93(q,2h),3.69(s,3h),3.15(d,2h),2.75(s,3h),2.1(m,2h),1.71(m,2h),1(t,3h)。
[1926]
步骤4:[4-甲氧基-39-甲基-35,35-二氧代-21,29,34-三氧杂-35λ
6-硫杂-1,14,15,16-四氮杂七环[28.5.3.1
3,7
.1
9,13
.0
12,16
.0
22,27
.0
33,37
]四十碳-3(40),4,6,9(39),10,12,14,22,24,26,30,32,37-十三烯-8-基]乙酸乙酯的制备
[1927]
采用通用方法11,用3-(1-{4-[2-(氯甲基)苯氧基]丁基}-4-甲基-1h-苯并三唑-5-基)-3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲氧基苯基}丙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体,48%收率)。
[1928]1h-nmr(500mhz,dmso-d6)δppm:7.67(d,1h),7.57(d,1h),7.44(dd,1h),7.34(dd,1h),7.29(td,1h),7.26(d,1h),7.01(d,1h),7(dd,1h),6.95(t,1h),6.87(d,1h),6.77(d,1h),6.64(d,1h),5.03(s,2h),4.81(t,1h),4.77(t,2h),4.41/4.34(d+d,2h),4.3/4.2(d+d,2h),4.13/4.06(m+m,2h),3.91(qd,2h),3.73(s,3h),3.2/3.15(dd+dd,2h),2.8(s,3h),2.21/2.02(m+m,2h),1.84(m,2h),1(t,3h)。
[1929]
步骤5:实施例53的制备
[1930]
采用通用方法12,用[4-甲氧基-39-甲基-35,35-二氧代-21,29,34-三氧杂-35λ
6-硫杂-1,14,15,16-四氮杂七环[28.5.3.1
3,7
.1
9,13
.0
12,16
.0
22,27
.0
33,37
]四十碳-3(40),4,6,9(39),10,12,14,22,24,26,30,32,37-十三烯-8-基]乙酸乙酯(1当量)作为起始试剂,得到标题化合物(80%收率)。
[1931]
通过手性柱色谱分离得到对映体纯产物。
[1932]
实施例53a(e1)
[1933]c36h36
n4o8s的hrms计算值:684.2254;[m+h]
+
,实测值:685.2315(δ=-1.7ppm)。
[1934]
实施例53b(e2)
[1935]c36h36
n4o8s的hrms计算值:684.2254;[m+h]
+
,实测值:685.2317(δ=-1.4ppm)。
[1936]1h-nmr(500mhz,dmso-d6)δppm:7.67(d,1h),7.55(d,1h),7.34(dd,1h),7.29(t,1h),7.23(d,1h),7.14(d,1h),7.01(d,1h),7(dd,1h),6.95(t,1h),6.88(d,1h),6.78(d,1h),6.63(d,1h),5.03(s,2h),4.79(t,1h),4.77(t,2h),4.4/4.33(d+d,2h),4.3/4.2(d+d,2h),4.14/4.06(m+m,2h),3.73(s,3h),3.09/3.05(dd+dd,2h),2.8(s,3h),2.21/2.03(m+m,2h),1.84(qn,2h)。
[1937]
13
c-nmr(125mhz,dmso-d6)δppm:173.2,156.4,156.3,155.6,146.4,144.6,137.7,136.1,131.5,130.1,129.7,129.3,129.1,127,126.6,124.8,121.9,120.7,119,118.2,116.3,112.9,111.9,111.5,108.2,67.5,65.1,56.1,49.8,48.5,48.1,40.8,40.4,27.1,26.4,13.3。
[1938]
实施例54:[4-甲氧基-39-甲基-35,35-二氧代-29,34-二氧杂-21,35λ
6-二硫杂-1,14,15,16-四氮杂七环[28.5.3.1
3,7
.1
9,13
.0
12,16
.0
22,27
.0
33,37
]四十碳-3(40),4,6,9(39),10,12,14,22,24,26,30,32,37-十三烯-8-基]乙酸
[1939][1940]
步骤1:3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲氧基苯基}-3-[1-(4-{[2-(羟基甲基)苯基]硫基}丁基)-4-甲基-1h-苯并三唑-5-基]丙酸乙酯的制备
[1941]
将3-[1-(4-氯丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲氧基苯基}丙酸乙酯(1eq.,1g,1.55mmol)和(2-硫基苯基)甲醇(1.2eq.,262mg,1.87mmol)溶于dmf(5ml)并加入k2co3(2eq.,430mg,3.11mmol)。将反应混合物室温搅拌2小时。反应完成后,将混合物倒入10ml水中并用2x30ml dcm萃取。将有机层分离并用硫酸镁干燥。过滤后将母液蒸发至干得到黄色结晶产物(1.15g,99%收率)。
[1942]1h-nmr(500mhz,dmso-d6)δppm:7.63(d,1h),7.5(d,1h),7.41(dm,1h),7.27(d,1h),7.23(dd,1h),7.22(d,1h),7.15(td,1h),7.12(td,1h),6.89(d,1h),6.84(d,1h),6.7(dd,1h),6.58(d,1h),4.82(t,1h),4.67(t,2h),4.48(s,2h),4.48(s,2h),4.21/4.17(d+d,2h),3.93(q,2h),3.69(s,3h),3.15(d,2h),2.94(t,2h),2.75(s,3h),2.01/1.51(m+m,4h),1(t,3h)。
[1943]
步骤2:3-[1-(4-{[2-(氯甲基)苯基]硫基}丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲氧基苯基}丙酸乙酯的制备
[1944]
采用通用方法10,用3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲氧基苯基}-3-[1-(4-{[2-(羟基甲基)苯基]硫基}丁基)-4-甲基-1h-苯并三唑-5-基]丙酸乙酯(1当量)作为起始试剂,得到标题化合物(98%收率)。
[1945]1h-nmr(500mhz,dmso-d6)δppm:7.62(d,1h),7.5(d,1h),7.39(dd,1h),7.34(dd,1h),7.27(d,1h),7.24(td,1h),7.23(dd,1h),7.16(td,1h),6.89(d,1h),6.84(d,1h),6.71(dd,1h),6.59(d,1h),4.82(t,1h),4.74/4.7(d+d,2h),4.67(t,2h),4.48(s,2h),4.21/4.17(d+d,2h),3.93(q,2h),3.69(s,3h),3.15(d,2h),3(t,2h),2.75(s,3h),2.01/1.51(m+m,4h),1(t,3h)。
[1946]
步骤3:[4-甲氧基-39-甲基-35,35-二氧代-29,34-二氧杂-21,35λ
6-二硫杂-1,14,15,16-四氮杂七环[28.5.3.1
3,7
.1
9,13
.0
12,16
.0
22,27
.0
33,37
]四十碳-3(40),4,6,9(39),10,12,14,22,24,26,30,32,37-十三烯-8-基]乙酸乙酯的制备
[1947]
采用通用方法11,用3-[1-(4-{[2-(氯甲基)苯基]硫基}丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲氧基苯基}丙酸乙酯(1当量)作为起始试剂,得到标题化合物(黄色结晶,21%收率)。
[1948]
通过手性柱色谱分离得到对映体纯的最终中间体。
[1949]1h-nmr(500mhz,dmso-d6)δppm:7.58(d,1h),7.53(d,1h),7.51(d,1h),7.38(t,1h),7.34(d,1h),7.34(dd,1h),7.31(d,1h),7.24(t,1h),6.86(d,1h),6.79(dd,1h),6.74(d,1h),6.72(d,1h),4.99/4.92(d+d,2h),4.82(t,1h),4.65(t,2h),4.47/4.4(d+d,2h),4.34/4.26(d+d,2h),3.9(qd,2h),3.72(s,3h),3.16/3.07(m+m,2h),3.14(m,2h),2.81(s,3h),2.04/1.9(m+m,2h),1.62(m,2h),0.99(t,3h)。
[1950]
步骤4:实施例54的制备
[1951]
采用通用方法12,用[4-甲氧基-39-甲基-35,35-二氧代-29,34-二氧杂-21,35λ
6-二硫杂-1,14,15,16-四氮杂七环[28.5.3.1
3,7
.1
9,13
.0
12,16
.0
22,27
.0
33,37
]四十碳-3(40),4,6,9(39),10,12,14,22,24,26,30,32,37-十三烯-8-基]乙酸乙酯e1(1当量)或e2(1当量)作为起始试剂,得到标题化合物(收率分别为18%-73%)。
[1952]
实施例54a(e1)
[1953]c36h36
n4o7s
2的
hrms计算值:700.2025;[m+h]
+
,实测值:701.2100(δ=0.3ppm)。
[1954]
实施例54b(e2)
[1955]c36h36
n4o7s2的hrms计算值
:
700.2025;[m+h]
+
,实测值:701.2101(δ=0.4ppm)。
[1956]1h-nmr(500mhz,dmso-d6)δppm:7.57(d,1h),7.53-7.21(m,4h),7.49(d,1h),7.33(dd,1h),7.26(d,1h),6.85(d,1h),6.79(dd,1h),6.76(d,1h),6.71(d,1h),4.98/4.91(d+d,2h),4.81(t,1h),4.64(t,2h),4.46/4.39(d+d,2h),4.33/4.26(d+d,2h),3.72(s,3h),3.16/3.06(m+m,2h),2.97(d,2h),2.8(s,3h),2.04/1.9(m+m,2h),1.61(m,2h)。
[1957]
13
c-nmr(125mhz,dmso-d6)δppm:130.3,129.5,127.2,119,116.4,112.7,111.4,107.9,68.4,56,49.9,48.6,47.4,41.4,41.1,32.4,28.5,25.1,13.4。
[1958]
实施例55a:[(8r)-4,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基](2h2)乙酸
[1959][1960]
在室温下向搅拌中的[(8r)-4,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯(1eq.,100mg,0.1693mmol)的甲醇-d4(四氘代甲醇,(2h3)甲(2h)醇)(2ml)溶液中缓慢加入nah(60%的矿物油溶液,10eq.,68mg,1.6936mmol)。将混合物搅拌5分钟后,将反应器封闭并将混合物于65℃搅拌18小时。将反应混合物用2ml 1m hcl水溶液中和,滤出白色沉淀,用2x5ml水洗涤,真空干燥。将粗产物通过反相色谱纯化,用5mm hcooh水溶液-mecn作为洗脱剂得到标题化合物(米黄色固体,82mg,86%收率)。c
29
d2h
28
n4o6s的hrms计算值:564.2012;[m+h]
+
,实测值:565.2086(δ=0.3ppm)。
[1961]1h-nmr(500mhz,dmso-d6)δppm:12.19(br.,1h),7.68(d,1h),7.49(dd,1h),7.43(d,1h),7.29(d,1h),6.99(d,1h),6.79(dd,1h),6.54(d,1h),5.85(d,1h),4.77(m,2h),4.74(s,1h),4.13/3.94(d+d,2h),3.99/3.84(d+d,2h),3.64/3.42(m+m,2h),2.62(s,3h),2.32(s,3h),2.21/2.06(m+m,2h),1.82/1.62(m+m,2h)。
[1962]
13
c-nmr(125mhz,dmso-d6)δppm:173.3,131.3,131.3,128.6,127.3,119.5,117.5,111.2,108,67.8,51.9,48.8,48.2,41.6,40.1,26.7,25.5,18.5,13.4。
[1963]
实施例55b:[(8s)-4,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基](2h2)乙酸
[1964][1965]
在室温下向搅拌中的[(8r)-4,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯(1eq.,200mg,0.338mmol)的甲醇-d4(四氘代甲醇,(2h3)甲(2h)醇)(4ml)溶液中缓慢加入nah(60%的矿物油溶液,10eq.,135mg,3.38mmol)。将混合物搅拌5分钟后,将反应器封闭并将混合物于65℃搅拌过夜。将反应混合物用2ml 1m hcl水溶液中和,滤出白色沉淀,用2x5ml水洗涤,真空干燥。将粗产物通过反相色谱纯化,用5mm hcooh水溶液-mecn作为洗脱剂得到标题化合物(白色固体,82mg,43%收率)。
[1966]c29
d2h
28
n4o6s的hrms计算值:564.2012;[m+h]
+
,实测值:565.2081(δ=-0.6ppm)。
[1967]1h-nmr(500mhz,dmso-d6)δppm:12.19(br.,1h),7.68(d,1h),7.49(dd,1h),7.43(d,1h),7.29(d,1h),6.99(d,1h),6.79(dd,1h),6.54(d,1h),5.85(d,1h),4.77(m,2h),4.74(s,1h),4.13/3.94(d+d,2h),3.99/3.84(d+d,2h),3.64/3.42(m+m,2h),2.62(s,3h),2.32(s,3h),2.21/2.06(m+m,2h),1.82/1.62(m+m,2h)。
[1968]
13
c-nmr(125mhz,dmso-d6)δppm:173.3,131.3,131.3,128.6,127.3,119.5,117.5,111.2,108,67.8,51.9,48.8,48.2,41.6,40.1,26.7,25.5,18.5,13.4。
[1969]
实施例56:[(2r,8r)-2,4,32-三甲基-28,28-二氧代-19,22,27-三氧杂-28λ
6-硫杂-1,14,15,16-四氮杂六环[21.5.3.1
3,7
.1
9,13
.0
12,16
.0
26,30
]三十三碳-3(33),4,6,9(32),10,12,14,23,25,30-十烯-8-基](2h2)乙酸
[1970][1971]
在室温下向搅拌中的[(2r,8r)-2,4,32-三甲基-28,28-二氧代-19,22,27-三氧杂-28λ
6-硫杂-1,14,15,16-四氮杂六环[21.5.3.1
3,7
.1
9,13
.0
12,16
.0
26,30
]三十三碳-3(33),4,6,9(32),10,12,14,23,25,30-十烯-8-基]乙酸乙酯(1eq.,150mg,0.2417mmol)的甲醇-d4(四氘代甲醇,(2h3)甲(2h)醇)(3ml)溶液中缓慢加入nah(60%的矿物油溶液,10eq.,97mg,2.417mmol)。将混合物搅拌5分钟后,将反应器封闭并将混合物于65℃搅拌18小时。将反应混合物用2.5ml 1m hcl水溶液中和,滤出白色沉淀,用2x5ml水洗涤,真空干燥。将粗产物通过反相色谱纯化,用5mmhcooh水溶液-mecn作为洗脱剂得到标题化合物(米黄色固体,82mg,86%)。
[1972]c30
d2h
30
n4o7s的hrms计算值:594.2117;[m+h]
+
,实测值:595.2192(δ=0.3ppm)。
[1973]1h-nmr(500mhz,dmso-d6)δppm:12.23(brs,1h),7.65(d,1h),7.46(dd,1h),7.29(d,1h),7.12(d,1h),6.94(d,1h),6.9(d,1h),6.8(dd,1h),6.01(d,1h),5.25(q,1h),4.9(s,1h),4.82(t,2h),4.15/3.79(d+d,2h),4.11/4.03(dt+dt,2h),3.95/3.8(m+m,2h),3.7/3.68(m+m,2h),2.79(s,3h),2.33(s,3h),1.16(d,3h)。
[1974]
13
c-nmr(125mhz,dmso-d6)δppm:173.4,155.5,146.5,145,141.5,137.7,135.9,135.5,132.3,131.6,128.3,127.9,127,126.6,120,119,115.4,114.1,108.6,69.3,69.1,68.5,55.4,48.8,45.1,41.1,39.4,18.6,15.6,13.4。
[1975]
实施例57:[4,38-二甲基-34,34-二氧代-20,28,33-三氧杂-34λ
6-硫杂-1,14,15,16-四氮杂七环[27.5.3.1
3,7
.1
9,13
.0
12,16
.0
21,26
.0
32,36
]三十九碳-3(39),4,6,9(38),10,12,14,21,23,25,29,31,36-十三烯-8-基]乙酸
[1976][1977]
步骤a1:3-(4-溴-3-甲基-2-硝基苯氨基)丙-1-醇的制备
[1978]
在n2下于室温下将1-溴-4-氟-2-甲基-3-硝基苯(1eq.,90g,385mmol)溶于3-氨基丙-1-醇(2.2eq,64g,847mmol)。将混合物于80℃加热1小时。反应完成后,将混合物冷却至室温并用dcm稀释。将该溶液用水洗涤。将有机层用硫酸镁干燥,过滤并蒸发至干得到粗产
物,通过用石油醚研制而纯化(104g,94%收率)。
[1979]1h-nmr(500mhz,dmso-d6)δppm:7.54(d,1h),6.74(d,1h),6.24(t,1h),4.61(t,1h),3.47(q,2h),3.19(q,2h),2.25(s,3h),1.67(m,2h)。
[1980]
步骤a2:3-(2-氨基-4-溴-3-甲基苯氨基)丙-1-醇的制备
[1981]
向搅拌中的3-(4-溴-3-甲基-2-硝基苯氨基)丙-1-醇(1eq.,104g,360mmol)的etoh(1000ml)和水(200ml)溶液中加入nh4cl(5eq.,97.2g,1800mmol)和铁粉(5eq.,100.8g,1800mmol)并将混合物于90℃加热过夜。反应完成后,将混合物冷却至室温并用硅藻土垫过滤。将滤液蒸发至只剩下水并用etoac萃取。分离出有机层并用硫酸钠干燥。将母液过滤并蒸发得到粗产物,将其通过正相硅胶色谱纯化,用etoac-石油醚(0:100至50:50%)作为洗脱剂(80g,86%收率)。
[1982]1h-nmr(500mhz,dmso-d6)δppm:6.71(d,1h),6.26(d,1h),4.58(br,3h),4.48(br,1h),3.52(q,2h),3.04(q,2h),2.16(s,3h),1.73(m,2h)。
[1983]
步骤a3:3-(5-溴-4-甲基-1h-苯并三唑-1-基)丙-1-醇的制备
[1984]
在室温下向搅拌中的3-(2-氨基-4-溴-3-甲基苯氨基)丙-1-醇(1eq.,10g,0.038mol)的thf(150ml)和acoh(15ml)溶液中加入3-甲基丁基亚硝酸酯(3eq.,13.6g,0.115mol)。将反应混合物室温搅拌1小时。反应完成后,将混合物倒入冰水中。用etoac萃取,将有机层用mgso4干燥,过滤并蒸发至干得到粗产物,将其通过正相硅胶色谱纯化,用etoac-石油醚洗脱(0:100至40:60%)得到标题化合物(4g,38%收率)。
[1985]1h-nmr(500mhz,dmso-d6)δppm:7.70(d,2h),7.68(d,2h),4.74(t,2h),4.67(t,1h),3.40(q,2h),2.72(s,3h),2.05(m,2h)。
[1986]
步骤a4:(2e)-3-[1-(3-羟基丙基)-4-甲基-1h-苯并三唑-5-基]丙-2-烯酸乙酯的制备
[1987]
向搅拌中的3-(5-溴-4-甲基-1h-苯并三唑-1-基)丙-1-醇(1eq.,8g,0.029mol)的thf(120ml)和水(20ml)的混合物溶液中加入na2co3(2.5eq.,7.85g,0.079mol)和(2e)-3-(4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷-2-基)丙-2-烯酸乙酯(1.2eq.,8.04g,0.035mol)并将混合物用n2脱气30分钟。最后加入a
ta
phos.pdcl2催化剂(0.02eq.,0.52g,0.0007mol)并将混合物于70℃加热2小时。反应完成后将混合物倒入冰水中并用etoac萃取。将有机相干燥并蒸发。将得到粗产物通过用et2o研制进行纯化,得到标题化合物(12.6g,47%收率)。
[1988]1h-nmr(500mhz,dmso-d6)δppm:8.03(d,1h),7.98(d,1h),7,71(d,1h),6.66(d,1h),4.75(t,2h),4.68(t,1h),4.22(q,2h),3.39(q,2h),2.81(s,3h),2.04(m,2h),1.28(t,3h)。
[1989]
步骤1:3-(3-{[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-甲基苯基)-3-[1-(3-羟基丙基)-4-甲基-1h-苯并三唑-5-基]丙酸乙酯的制备
[1990]
采用通用方法6,用(2e)-3-[1-(3-羟基丙基)-4-甲基-1h-苯并三唑-5-基]丙-2-烯酸乙酯(1当量)和6-(苄氧基)-3-{[2-甲基-5-(4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷-2-基)苯基]甲基}-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮(2当量)作为起始试剂,得到标题化合物(黄色固体泡沫,77%收率)。
[1991]1h-nmr(500mhz,dmso-d6)δppm:7.58(d,1h),7.49-7.31(m,5h),7.49(d,1h),7.23
(d,1h),7.19(dd,1h),7.13(d,1h),7.13(d,1h),7.07(dd,1h),6.97(d,1h),5.11(s,2h),4.85(t,1h),4.65(t,2h),4.65(t,1h),4.44(s,2h),4.22(s,2h),3.92(q,2h),3.36(m,2h),3.19/3.15(dd+dd,2h),2.77(s,3h),2.21(s,3h),1.99(m,2h),0.99(t,3h)。
[1992]
步骤2:3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}-3-[1-(3-羟基丙基)-4-甲基-1h-苯并三唑-5-基]丙酸乙酯的制备
[1993]
采用通用方法8,用3-(3-{[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-甲基苯基)-3-[1-(3-羟基丙基)-4-甲基-1h-苯并三唑-5-基]丙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体泡沫,93%收率)。
[1994]1h-nmr(500mhz,dmso-d6)δppm:9.71(brs.,1h),7.6(d,1h),7.5(d,1h),7.22(d,1h),7.19(dd,1h),7.13(d,1h),6.99(d,1h),6.79(dd,1h),6.6(d,1h),4.84(t,1h),4.68(t,2h),4.67(br.,1h),4.4/4.36(d+d,2h),4.21/4.17(d+d,2h),3.94(q,2h),3.38(t,2h),3.19/3.15(dd+dd,2h),2.76(s,3h),2.22(s,3h),2.01(m,2h),1(t,3h)。
[1995]
步骤3:3-[1-(3-氯丙基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}丙酸乙酯的制备
[1996]
采用通用方法10,用3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}-3-[1-(3-羟基丙基)-4-甲基-1h-苯并三唑-5-基]丙酸乙酯(1当量)作为起始试剂,得到标题化合物(黄色固体泡沫,97%收率)。
[1997]1h-nmr(500mhz,dmso-d6)δppm:9.72(brs.,1h),7.62(d,1h),7.53(d,1h),7.22(d,1h),7.2(dd,1h),7.13(d,1h),6.99(d,1h),6.79(dd,1h),6.6(d,1h),4.84(t,1h),4.77(t,2h),4.39/4.35(d+d,2h),4.21/4.17(d+d,2h),3.94(q,2h),3.61(m,2h),3.19/3.15(dd+dd,2h),2.76(s,3h),2.34(m,2h),2.22(s,3h),1(t,3h)。
[1998]
步骤4:3-{1-[3-(2-甲酰基苯氧基)丙基]-4-甲基-1h-苯并三唑-5-基}-3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}丙酸乙酯的制备
[1999]
将3-[1-(3-氯丙基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}丙酸乙酯(1eq.,0.65g,1.1mmol)溶于干燥n,n-二甲基乙酰胺(5ml)并加入2-羟基苯甲醛(34eq.,4ml,37.536mmol),然后加入cs2co3(5.55eq.,2.0g,6.1mmol)。将该溶液于120℃加热2小时。将粗产物通过正相硅胶色谱纯化,用dcm-meoh(100:0至95:5)作为洗脱剂,得到0.49g(66%收率)浅橙色固体状标题化合物。
[2000]1h-nmr(500mhz,dmso-d6)δppm:10.12(d,1h),9.7(brs,1h),7.63(d,1h),7.62(d,1h),7.58(t,1h),7.45(d,1h),7.2(d,1h),7.16(dd,1h),7.12(d,1h),7.1(d,1h),7.03(t,1h),6.99(d,1h),6.78(dd,1h),6.6(d,1h),4.89(t,2h),4.82(t,1h),4.39/4.35(d+d,2h),4.21/4.16(d+d,2h),4.11(t,2h),3.93(q,2h),3.17/3.11(dd+dd,2h),2.73(s,3h),2.41(qn,2h),2.22(s,3h),1(t,3h)。
[2001]
步骤5:3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}-3-(1-{3-[2-(羟基甲基)苯氧基]丙基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯的制备
[2002]
将3-{1-[3-(2-甲酰基苯氧基)丙基]-4-甲基-1h-苯并三唑-5-基}-3-{3-[(6-羟
基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}丙酸乙酯(1eq.,0.48g,0.69mmol)溶于干燥etoh(5ml)并加入硼氢化钠(3.77eq.,0.10g,2.6mmol)。将该溶液在室温下搅拌2小时。将反应混合物倒在碎冰上并浓缩。将残余物在水和etoac之间进行分配,分相并将水相用另一份etoac萃取。将收集的有机相用硫酸钠干燥,过滤并蒸发。将残余物在高真空下室温干燥得到0.466g(97%收率)米白色泡沫状标题化合物。
[2003]1h-nmr(500mhz,dmso-d6)δppm:9.56(brs,1h),7.61(d,1h),7.48(d,1h),7.36(d,1h),7.2(d,1h),7.17(dd,1h),7.14(t,1h),7.13(d,1h),6.96(d,1h),6.91(t,1h),6.82(d,1h),6.76(dd,1h),6.56(d,1h),4.84(t,1h),4.83(t,2h),4.52(s,2h),4.35(s,2h),4.2/4.16(d+d,2h),3.94(m,2h),3.93(q,2h),3.17/3.13(dd+dd,2h),2.75(s,3h),2.33(qn,2h),2.22(s,3h),1(t,3h)。
[2004]
步骤6:[4,38-二甲基-34,34-二氧代-20,28,33-三氧杂-34λ
6-硫杂-1,14,15,16-四氮杂七环[27.5.3.1
3,7
.1
9,13
.0
12,16
.0
21,26
.0
32,36
]三十九碳-3(39),4,6,9(38),10,12,14,21,23,25,29,31,36-十三烯-8-基]乙酸乙酯的制备
[2005]
将3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}-3-(1-{3-[2-(羟基甲基)苯氧基]丙基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯(1eq.,0.66mmol,0.46g)溶于干燥thf(40ml)并加入pph3(3eq.,0.52g,2mmol),然后加入diad(3eq.,0.40g,2.0mmol),同时冷却。将反应混合物室温搅拌1.5小时。将溶剂蒸发并将粗产物通过正相硅胶色谱纯化,用庚烷-etoac(100:0至30:70)作为洗脱剂,得到0.187g(42%收率)白色泡沫状标题化合物。
[2006]
通过手性柱色谱分离得到对映体纯的最终中间体。(ee~99.9%)
[2007]1h-nmr(500mhz,dmso-d6)δppm:7.63(d,1h),7.58(d,1h),7.58(dm,1h),7.36(dd,1h),7.35(d,1h),7.33(m,1h),7.22(dd,1h),7.17(d,1h),7.15(d,1h),7.06(dm,1h),7.02(m,1h),6.91(d,1h),5.27(s,2h),4.9/4.82(m+m,2h),4.85(t,1h),4.43/4.09(d+d,2h),4.29/4.02(d+d,2h),4.18/4.02(m+m,2h),3.88(m,2h),3.19/3.11(dd+dd,2h),2.81(s,3h),2.37/2.27(m+m,2h),2.28(s,3h),0.96(t,3h)。
[2008]
步骤7:实施例57的制备
[2009]
采用通用方法12,用[4,38-二甲基-34,34-二氧代-20,28,33-三氧杂-34λ
6-硫杂-1,14,15,16-四氮杂七环[27.5.3.1
3,7
.1
9,13
.0
12,16
.0
21,26
.0
32,36
]三十九碳-3(39),4,6,9(38),10,12,14,21,23,25,29,31,36-十三烯-8-基]乙酸乙酯e1(1当量)或e2(1当量)作为起始试剂,得到标题化合物(收率分别为75%-83%)。
[2010]
实施例57a(e1)
[2011]c35h34
n4o7s的hrms计算值:654.2148;[m+h]
+
,实测值:655.2224(δ=0.5ppm)。
[2012]
实施例57b(e2)
[2013]c35h34
n4o7s的hrms计算值:654.2148;[m+h]
+
,实测值:655.2231(δ=1.5ppm)。
[2014]1h-nmr(500mhz,dmso-d6)δppm:12.07(brs,1h),7.63(d,1h),7.58(d,1h),7.57(s,1h),7.36(dd,1h),7.34(t,1h),7.33(d,1h),7.21(dd,1h),7.16(d,1h),7.15(d,1h),7.07(d,1h),7.02(t,1h),6.91(d,1h),5.27(s,2h),4.9/4.82(m+m,2h),4.83(t,1h),4.43/4.1(d+d,2h),4.28/4.03(d+d,2h),4.17/4.05(m+m,2h),3.07/3.03(dd+dd,2h),2.81(s,3h),2.37/2.28(m+m,2h),2.28(s,3h)。
[2015]
13
c-nmr(125mhz,dmso-d6)δppm:173.2,156.1,156.1,146.2,144.8,142.2,137.4,136.2,132.4,131.8,131.2,130.1,129.9,129.4,129.3,127.3,126.8,125,120.9,119.6,118.3,117,112.4,111.8,107.7,65.4,64,51.9,49.1,44.3,41.1,40.8,30.1,18.3,13.3。
[2016]
实施例58:[4,32-二甲基-28,28-二氧代-19-苯基-22,27-二氧杂-28λ
6-硫杂-1,14,15,16,19-五氮杂六环[21.5.3.1
3,7
.1
9,13
.0
12,16
.0
26,30
]三十三碳-3(33),4,6,9(32),10,12,14,23,25,30-十烯-8-基]乙酸
[2017][2018]
步骤a1:2-(4-溴-3-甲基-2-硝基苯氨基)乙-1-醇的制备
[2019]
在n2下,于室温下将1-溴-4-氟-2-甲基-3-硝基苯(1eq.,600g,2.56mol)溶于乙醇胺(2.5eq,332g,5.45mol)。于95℃加热1.5小时后,将反应混合物冷却至室温并用dcm稀释。将该溶液用水洗涤。将有机层用mgso4干燥并蒸发至干得到粗产物,将其通过用石油醚研制纯化得到标题化合物(630g,89%收率)。
[2020]1h-nmr(500mhz,dmso-d6)δppm:7.59(d,1h),6.79(d,1h),6.09(t,1h),4.84(t,1h),3.54(q,2h),3.19(q,2h),2.27(s,3h)。
[2021]
步骤a2:2-(2-氨基-4-溴-3-甲基苯氨基)乙-1-醇的制备
[2022]
向搅拌中的2-(4-溴-3-甲基-2-硝基苯氨基)乙-1-醇(1eq.,630g,2.29mol)的etoh(500ml)和水(100ml)溶液中加入nh4cl(5eq.,611g,11.45mol)和锌粉(5eq.,744g,11.45mol)并将混合物于95℃加热12小时。反应完成后,将混合物通过硅藻土垫过滤。将滤液蒸发并将残余物在2l水中搅拌3小时。滤出沉淀产物,干燥并通过用戊烷研制而纯化(430g,77%收率)。
[2023]1h-nmr(500mhz,dmso-d6)δppm:6.72(d,1h),6.28(d,1h),4.67(t,1h),4.58(s,2h),4.51(t,1h),3.59(q,2h),3.06(q,2h),2.17(s,3h)。
[2024]
步骤a3:2-(5-溴-4-甲基-1h-苯并三唑-1-基)乙-1-醇的制备
[2025]
在2.5小时内向搅拌中的2-(2-氨基-4-溴-3-甲基苯氨基)乙-1-醇(1eq.,160g,0.652mol)和四氟硼酸(2eq.,160ml,1.3mol)的mecn(1500ml)溶液中加入3-甲基丁基亚硝酸酯(1.5eq.,114.7g,0.979mol)和四氟硼酸(2eq.,160ml,1.3mol)的mecn溶液。在该过程中内部温度必须保持在5℃以下。反应完成后,将混合物倒入冰水中,用10%naoh溶液碱化并用etoac萃取。将有机层用mgso4干燥并蒸发至干。将粗产物通过柱色谱纯化(90g,48%收率)。
[2026]1h-nmr(500mhz,dmso-d6)δppm:7.67(s,2h),4.98(t,1h),4.74(t,2h),3.86(q,
2h),2.72(s,3h)。
[2027]
步骤a4:(2e)-3-[1-(2-羟基乙基)-4-甲基-1h-苯并三唑-5-基]丙-2-烯酸乙酯的制备
[2028]
向搅拌中的2-(5-溴-4-甲基-1h-苯并三唑-1-基)乙-1-醇(1eq.,50g,0.19mol)的thf(450ml)和水(50ml)的混合物溶液中加入na2co3(2.5eq.,51.2g,0.48mol)和(2e)-3-(4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷-2-基)丙-2-烯酸乙酯(1.2eq.,53g,0.23mol)并将混合物用n2脱气30分钟。加入a
ta
phos.pdcl2催化剂(0.02eq.,2.76g,0.04mol)并将混合物于70℃加热8小时。反应完成后将混合物倒入冰水中并用etoac萃取。将有机相干燥并蒸发。将得到的粗产物通过用et2o研制而纯化(46g,86%收率)。
[2029]1h-nmr(500mhz,dmso-d6)δppm:8.03(d,1h),7.95(d,1h),7,70(d,1h),6,65(d,1h),4,98(t,1h),4,74(t,2h),4,22(q,2h),3.87(q,2h),2,82(s,3h),1.28(t,3h)。
[2030]
步骤1:3-(3-{[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-甲基苯基)-3-[1-(2-羟基乙基)-4-甲基-1h-苯并三唑-5-基]丙酸乙酯的制备
[2031]
采用通用方法6,用(2e)-3-[1-(2-羟基乙基)-4-甲基-1h-苯并三唑-5-基]丙-2-烯酸乙酯(1当量)和6-(苄氧基)-3-{[2-甲基-5-(4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷-2-基)苯基]甲基}-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮(1.3当量)作为起始试剂,得到标题化合物(黄色固体泡沫,82%收率)。
[2032]1h-nmr(500mhz,dmso-d6)δppm:7.58(d,1h),7.47(m,2h),7.47(d,1h),7.41(tm,2h),7.35(tm,1h),7.24(d,1h),7.18(dd,1h),7.14(d,1h),7.13(d,1h),7.07(dd,1h),6.97(d,1h),5.11(s,2h),4.95(t,1h),4.85(t,1h),4.64(t,2h),4.46/4.42(d+d,2h),4.24/4.2(d+d,2h),3.93(q,2h),3.81(q,2h),3.2/3.15(dd+dd,2h),2.77(s,3h),2.21(s,3h),1.01(t,3h)。
[2033]
步骤2:3-(3-{[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-甲基苯基)-3-[1-(2-氯乙基)-4-甲基-1h-苯并三唑-5-基]丙酸乙酯的制备
[2034]
采用通用方法10,用3-(3-{[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-甲基苯基)-3-[1-(2-羟基乙基)-4-甲基-1h-苯并三唑-5-基]丙酸乙酯(1当量)作为起始试剂,得到标题化合物(米黄色固体泡沫,88%收率)。产物不经进一步纯化用于下一步。
[2035]1h-nmr(500mhz,dmso-d6)δppm:7.65(d,1h),7.52(d,1h),7.46(d,2h),7.44(t,2h),7.35(t,1h),7.25(d,1h),7.2(dd,1h),7.14(d,1h),7.14(d,1h),7.07(dd,1h),6.96(d,1h),5.1(s,2h),4.99(t,2h),4.85(t,1h),4.46/4.42(d+d,2h),4.23/4.2(d+d,2h),4.12(t,2h),3.93(q,2h),3.2/3.16(dd+dd,2h),2.78(s,3h),2.21(s,3h),0.98(t,3h)。
[2036]
步骤3:3-(3-{[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-甲基苯基)-3-(1-{2-[(2-羟基乙基)(苯基)氨基]乙基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯的制备
[2037]
将3-(3-{[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-甲基苯基)-3-[1-(2-氯乙基)-4-甲基-1h-苯并三唑-5-基]丙酸乙酯(1eq.,1g,1.378mmol)溶于2-苯氨基乙醇(20eq.,3.78g,27.56mmol)。将反应混合物于130℃加热13小时。冷却至室温后,将混合物用水稀释并用etoac萃取。将有机相用硫酸镁干燥,过滤并浓缩至干得到粗
产物,将其通过正相硅胶色谱纯化,用庚烷-acoet(0至50:50)作为洗脱剂得到标题化合物(643mg,白色固体,59%收率)。
[2038]1h-nmr(500mhz,dmso-d6)δppm:7.48(s,1h),7.48(s,1h),7.48-7.31(m,5h),7.22(d,1h),7.17(dd,1h),7.15-6.55(m,5h),7.14(d,1h),7.14(d,1h),7.07(dd,1h),6.96(d,1h),5.1(s,2h),4.84(t,1h),4.78(t,2h),4.65(t,1h),4.46/4.42(d+d,2h),4.23/4.2(d+d,2h),3.92(q,2h),3.84(m,2h),3.36(m,2h),3.16(m,2h),3.09(m,2h),2.75(s,3h),2.21(s,3h),0.99(t,3h)。
[2039]
步骤4:3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}-3-(1-{2-[(2-羟基乙基)(苯基)氨基]乙基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯的制备
[2040]
将3-(3-{[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-甲基苯基)-3-(1-{2-[(2-羟基乙基)(苯基)氨基]乙基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯(1eq.,637mg,0.806mmol)和pd/c催化剂(230mg)悬浮于etoh(25ml)和二氧杂环己烷(5ml)中。将混合物在不锈钢反应器中在2巴压力下于室温氢化18小时。通过硅藻土垫过滤并蒸发至干得到粗产物,用et2o研制,然后溶于etoh并蒸发得到标题化合物(530mg,白色固体,94%收率)。
[2041]1h-nmr(500mhz,dmso-d6)δppm:9.7(s,1h),7.6(d,1h),7.5(d,1h),7.21(d,1h),7.17(dd,1h),7.13-6.59(m,5h),7.13(d,1h),6.99(d,1h),6.79(dd,1h),6.61(d,1h),4.83(t,1h),4.81(t,2h),4.66(t,1h),4.4/4.36(d+d,2h),4.21/4.17(d+d,2h),3.93(q,2h),3.85(m,2h),3.38(q,2h),3.17(d,2h),3.11(t,2h),2.74(s,3h),2.22(s,3h),1(t,3h)。
[2042]
步骤5:[4,32-二甲基-28,28-二氧代-19-苯基-22,27-二氧杂-28λ
6-硫杂-1,14,15,16,19-五氮杂六环[21.5.3.1
3,7
.1
9,13
.0
12,16
.0
26,30
]三十三碳-3(33),4,6,9(32),10,12,14,23,25,30-十烯-8-基]乙酸乙酯的制备
[2043]
将3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}-3-(1-{2-[(2-羟基乙基)(苯基)氨基]乙基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯(1eq.,248mg,0.3540mmol)溶于thf(50ml)并加入pph3(4eq.,371mg,1.416mmol)。将混合物冷却至~5℃并滴加diad(4eq.,286mg,1.416mmol)。将混合物于回流温度下加热1小时。反应完成后将溶剂蒸发,将粗产物通过正相硅胶色谱纯化,用庚烷-acoet(60:40)作为洗脱剂得到标题化合物(157mg,白色固体,65%收率)。
[2044]
通过手性柱色谱分离得到对映体纯的最终中间体。
[2045]1h-nmr(500mhz,dmso-d6)δppm:7.67(d,1h),7.46(d,1h),7.45(dd,1h),7.26(d,1h),7.25-6.67(m,5h),7.07(d,1h),6.9(dd,1h),6.88(d,1h),6.1(d,1h),4.89/4.85(m+m,2h),4.82(t,1h),4.13(s,2h),4.13/3.94(m+m,2h),4.01/3.93(d+d,2h),3.9(q,2h),3.8/3.58(m+m,2h),3.67/3.42(m+m,2h),3.1/3.03(dd+dd,2h),2.72(s,3h),2.32(s,3h),0.99(t,3h)。
[2046]
步骤6:实施例58的制备
[2047]
采用通用方法12,用[4,32-二甲基-28,28-二氧代-19-苯基-22,27-二氧杂-28λ
6-硫杂-1,14,15,16,19-五氮杂六环[21.5.3.1
3,7
.1
9,13
.0
12,16
.0
26,30
]三十三碳-3(33),4,6,9(32),10,12,14,23,25,30-十烯-8-基]乙酸乙酯e1(1当量)或e2(1当量)作为起始试剂,得
到标题化合物(收率分别为68%-82%)。
[2048]
实施例58a(e1)
[2049]c35h35
n5o6s的hrms计算值:653.2308;[m+h]
+
,实测值:654.236(δ=-3.2ppm)。
[2050]
实施例58b(e2)
[2051]c35h35
n5o6s的hrms计算值:653.2308;[m+h]
+
,实测值:654.2359(δ=-3.3ppm)。
[2052]1h-nmr(500mhz,dmso-d6)δppm:12.13(brs,1h),7.66(d,1h),7.46(dd,1h),7.43(d,1h),7.27(d,1h),7.23(t,2h),7.06(d,1h),6.89(dd,1h),6.86(d,2h),6.84(d,1h),6.71(t,1h),6.07(d,1h),4.88/4.86(m+m,2h),4.8(t,1h),4.17/4.09(d+d,2h),4.15/3.95(m+m,2h),3.99/3.96(d+d,2h),3.77/3.55(m+m,2h),3.65/3.4(m+m,2h),3.02/2.91(dd+dd,2h),2.72(s,3h),2.32(s,3h)。
[2053]
13
c-nmr(125mhz,dmso-d6)δppm:173.2,155.6,147.9,146.4,144.9,141.8,137.3,136.3,132,132,131.6,131.3,129.8,128.5,127.5,127.3,119.5,117.5,117.4,116.4,113.2,112.5,108.1,66.6,51.9,50.6,49.8,48.5,46.2,41.3,41,18.4,13.4。
[2054]
实施例59:[4-甲氧基-32-甲基-28,28-二氧代-19,22,27-三氧杂-28λ
6-硫杂-1,14,15,16-四氮杂六环[21.5.3.1
3,7
.1
9,13
.0
12,16
.0
26,30
]三十三碳-3(33),4,6,9(32),10,12,14,23,25,30-十烯-8-基]乙酸
[2055][2056]
步骤1:6-(苄氧基)-3-[(5-溴-2-甲氧基苯基)甲基]-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮的制备
[2057]
采用通用方法7,用(5-溴-2-甲氧基苯基)甲醇(1当量)和6-(苄氧基)-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮(0.77当量)作为起始试剂,得到标题化合物(82%收率),为白色固体。
[2058]1h-nmr(500mhz,dmso-d6)δppm:7.49(dd,1h),7.48-7.29(m,5h),7.45(d,1h),7.06(m,1h),7.01(m,1h),7.01(m,1h),6.96(d,1h),5.08(s,2h),4.65(s,2h),4.26(s,2h),3.72(s,3h)。
[2059]
步骤2:6-(苄氧基)-3-{[2-甲氧基-5-(4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷-2-基)苯基]甲基}-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮的制备
[2060]
采用通用方法3,用6-(苄氧基)-3-[(5-溴-2-甲氧基苯基)甲基]-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮(1当量)作为起始试剂,得到标题化合物(87%收率),为米黄色固体。
[2061]1h-nmr(500mhz,dmso-d6)δppm:7.66(dd,1h),7.6(d,1h),7.44(d,2h),7.4(t,2h),7.34(t,1h),7.08(d,1h),7.02(dd,1h),7.02(d,1h),7(d,1h),5.07(s,2h),4.59(s,
2h),4.26(s,2h),3.75(s,3h),1.28(s,12h)。
[2062]
步骤3:3-(3-{[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-甲氧基苯基)-3-(1-{2-[2-(苄氧基)乙氧基]乙基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯的制备
[2063]
采用通用方法6,用(2e)-3-(1-{2-[2-(苄氧基)乙氧基]乙基}-4-甲基-1h-苯并三唑-5-基)丙-2-烯酸乙酯(1当量)和6-(苄氧基)-3-{[2-甲氧基-5-(4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷-2-基)苯基]甲基}-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮(1.3当量)作为起始试剂,得到标题化合物(52%收率)。
[2064]1h-nmr(500mhz,dmso-d6)δppm:7.62(d,1h),7.47-7.14(m,12h),7.42(d,1h),6.98(dd,1h),6.96(d,1h),6.92(d,1h),6.84(d,1h),5.07(s,2h),4.81(m,2h),4.81(t,1h),4.52(s,2h),4.3(s,2h),4.19(s,2h),3.92(q,2h),3.88(t,2h),3.64(s,3h),3.51(m,2h),3.41(m,2h),3.13/3.09(dd+dd,2h),2.75(s,3h),1(t,3h)。
[2065]
步骤4:3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲氧基苯基}-3-{1-[2-(2-羟基乙氧基)乙基]-4-甲基-1h-苯并三唑-5-基}丙酸乙酯的制备采用通用方法8,用3-(3-{[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-甲氧基苯基)-3-(1-{2-[2-(苄氧基)乙氧基]乙基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体,定量)。
[2066]1h-nmr(500mhz,dmso-d6)δppm:9.62(s,1h),7.64(d,1h),7.48(d,1h),7.26(d,1h),7.23(dd,1h),6.89(d,1h),6.85(d,1h),6.71(dd,1h),6.59(d,1h),4.82(t,1h),4.81(t,2h),4.55(m,1h),4.48(s,2h),4.21/4.17(d+d,2h),3.94(q,2h),3.89(t,2h),3.69(s,3h),3.38(m,4h),3.14(m,2h),2.75(s,3h),1.02(t,3h)。
[2067]
步骤5:3-{1-[2-(2-氯乙氧基)乙基]-4-甲基-1h-苯并三唑-5-基}-3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲氧基苯基}丙酸乙酯盐酸盐的制备
[2068]
采用通用方法10,用3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲氧基苯基}-3-{1-[2-(2-羟基乙氧基)乙基]-4-甲基-1h-苯并三唑-5-基}丙酸乙酯(1当量)作为起始试剂,得到标题化合物(固体泡沫,96%收率)。
[2069]1h-nmr(500mhz,dmso-d6)δppm:9.64(brs,1h),7.64(d,1h),7.49(d,1h),7.26(d,1h),7.22(dd,1h),6.89(d,1h),6.84(d,1h),6.71(dd,1h),6.59(d,1h),4.83(t,2h),4.81(t,1h),4.47(s,2h),4.2/4.17(d+d,2h),3.94(q,2h),3.93(t,2h),3.69(s,3h),3.6(t,2h),3.59(t,2h),3.14(d,2h),2.75(s,3h),1.02(t,3h)。
[2070]
步骤6:[4-甲氧基-32-甲基-28,28-二氧代-19,22,27-三氧杂-28λ
6-硫杂-1,14,15,16-四氮杂六环[21.5.3.1
3,7
.1
9,13
.0
12,16
.0
26,30
]三十三碳-3(33),4,6,9(32),10,12,14,23,25,30-十烯-8-基]乙酸乙酯的制备
[2071]
采用通用方法11,用3-{1-[2-(2-氯乙氧基)乙基]-4-甲基-1h-苯并三唑-5-基}-3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲氧基苯基}丙酸乙酯盐酸盐(1当量)作为起始试剂,得到标题化合物(59%收率)。
[2072]
通过手性柱色谱分离得到对映体纯的最终中间体。
[2073]1h-nmr(500mhz,dmso-d6)δppm:7.71(d,1h),7.38(dd,1h),7.35(d,1h),6.96(d,
1h),6.95(d,1h),6.94(d,1h),6.82(dd,1h),6.46(d,1h),4.86/4.83(m+m,2h),4.79(t,1h),4.4/4.23(d+d,2h),4.18(s,2h),3.99/3.94(m+m,2h),3.94(m,2h),3.89(m,2h),3.81/3.68(m+m,2h),3.76(s,3h),3.09/3.04(dd+dd,2h),2.7(s,3h),0.98(t,3h)
[2074]
步骤7:实施例59的制备
[2075]
采用通用方法12,用[4-甲氧基-32-甲基-28,28-二氧代-19,22,27-三氧杂-28λ
6-硫杂-1,14,15,16-四氮杂六环[21.5.3.1
3,7
.1
9,13
.0
12,16
.0
26,30
]三十三碳-3(33),4,6,9(32),10,12,14,23,25,30-十烯-8-基]乙酸乙酯e1(1当量)或e2(1当量)作为起始试剂,得到标题化合物(收率分别为91%-93%)。
[2076]
实施例59a(e1)
[2077]c29h30
n4o8s的hrms计算值:594.1784;[m+h]
+
,实测值:595.1843(δ=-2.4ppm)。
[2078]
实施例59b(e2)
[2079]c29h30
n4o8s的hrms计算值:594.1784;[m+h]
+
,实测值:595.1849(δ=-1.4ppm)。
[2080]1h-nmr(500mhz,dmso-d6)δppm:12.05(brs,1h),7.71(d,1h),7.4(dd,1h),7.34(d,1h),6.96(d,1h),6.95(d,1h),6.92(d,1h),6.82(dd,1h),6.44(d,1h),4.84(m,2h),4.77(t,1h),4.39/4.22(d+d,2h),4.18(s,2h),4/3.95(m+m,2h),3.94(m,2h),3.81/3.68(m+m,2h),3.77(s,3h),2.96(d,2h),2.7(s,3h)。
[2081]
13
c-nmr(125mhz,dmso-d6)δppm:173.2,157,155.6,146.5,145.2,136.7,135.7,132.5,131,131,127.1,126.6,121.3,118.7,118.2,115,114.4,111.8,109.2,69.9,68.6,68.3,56.1,48.9,48.8,48.5,41.3,41.1,13.3。
[2082]
实施例60:[4,36-二甲基-30,30-二氧代-24,29-二氧杂-30λ
6-硫杂-1,14,15,16,19-五氮杂七环[23.5.3.2
19,22
.1
3,7
.1
9,13
.0
12,16
.0
28,32
]三十七碳-3(37),4,6,9(36),10,12,14,25,27,32-十烯-8-基]乙酸
[2083][2084]
步骤1:3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}-3-[1-(2-羟基乙基)-4-甲基-1h-苯并三唑-5-基]丙酸乙酯的制备
[2085]
采用通用方法8,用3-(3-{[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-甲基苯基)-3-[1-(2-羟基乙基)-4-甲基-1h-苯并三唑-5-基]丙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体,94%收率)。
[2086]1h-nmr(500mhz,dmso-d6)δppm:9.71(s,1h),7.6(d,1h),7.49(d,1h),7.23(d,1h),7.18(dd,1h),7.13(d,1h),7(d,1h),6.79(dd,1h),6.62(d,1h),4.96(t,1h),4.84(t,1h),4.67(t,2h),4.41/4.36(d+d,2h),4.21/4.17(d+d,2h),3.94(q,2h),3.84(q,2h),3.19/3.15(dd+dd,2h),2.76(s,3h),2.22(s,3h),1.03(t,3h)。
[2087]
步骤2:3-[1-(2-氯乙基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}丙酸乙酯盐酸盐的制备
[2088]
采用通用方法10,用3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}-3-[1-(2-羟基乙基)-4-甲基-1h-苯并三唑-5-基]丙酸乙酯(1当量)作为起始试剂,得到标题化合物(灰白色固体泡沫,96%收率)。产物不经进一步纯化用于下一步。
[2089]1h-nmr(500mhz,dmso-d6)δppm:9.72(br.,1h),7.67(d,1h),7.53(d,1h),7.24(d,1h),7.2(dd,1h),7.13(d,1h),6.99(d,1h),6.79(dd,1h),6.61(d,1h),5.02(t,2h),4.84(t,1h),4.4/4.36(d+d,2h),4.22/4.17(d+d,2h),4.15(t,2h),3.93(q,2h),3.18(d,2h),2.77(s,3h),2.22(s,3h),1(t,3h)。
[2090]
步骤3:3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}-3-(1-{2-[4-(羟基甲基)哌啶-1-基]乙基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯的制备
[2091]
在室温下向搅拌中的3-[1-(2-氯乙基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}丙酸乙酯盐酸盐(1eq.,0.8g,1.335mmol)的dmf(8ml)混合物中加入(哌啶-4-基)甲醇(10eq.,1.538g,13.35mmol)。将反应混合物加热至80℃并在该温度下搅拌24小时。反应完成后将混合物冷却至室温并直接注射到c18柱上并通过反相色谱纯化,用5mm nh4hco3水溶液-mecn梯度洗脱得到标题化合物(393mg,白色固体,43%收率)。
[2092]1h-nmr(500mhz,dmso-d6)δppm:9.73(brs,1h),7.62(d,1h),7.5(d,1h),7.22(d,1h),7.19(dd,1h),7.13(d,1h),6.99(d,1h),6.79(dd,1h),6.6(d,1h),4.83(t,1h),4.74(t,2h),4.56/0.96(m+m,4h),4.4/4.35(d+d,2h),4.37(brs,1h),4.22/4.17(d+d,2h),3.93(q,2h),3.17(d,2h),3.17(d,2h),2.9/2.85/1.92(d/d+t,4h),2.77(t,2h),2.75(s,3h),2.22(s,3h),1.27(m,1h),0.99(t,3h)。
[2093]
步骤4:[4,36-二甲基-30,30-二氧代-24,29-二氧杂-30λ
6-硫杂-1,14,15,16,19-五氮杂七环[23.5.3.2
19,22
.1
3,7
.1
9,13
.0
12,16
.0
28,32
]三十七碳-3(37),4,6,9(36),10,12,14,25,27,32-十烯-8-基]乙酸乙酯的制备
[2094]
将3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}-3-(1-{2-[4-(羟基甲基)哌啶-1-基]乙基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯(1eq.,287mg,0.4237mmol)溶于thf(60ml)并加入pph3(4eq.,444mg,1.694mmol)。将混合物冷却至~5℃并滴加diad(4eq.,343mg,1.694mmol)。在回流温度下加热1.5小时。然后将溶剂蒸发,将粗产物溶于dmf并将混合物直接注射到c18柱上并通过反相色谱纯化,用5mm nh4hco3水溶液-mecn梯度洗脱得到标题化合物(100mg,36%收率)。
[2095]
通过手性柱色谱分离得到对映体纯的最终中间体。
[2096]1h-nmr(500mhz,dmso-d6)δppm:7.68(d,1h),7.61(d,1h),7.42(dd,1h),7.25(d,1h),7.04(d,1h),7.01(d,1h),6.99(d,1h),6.96(dd,1h),4.84/4.61(td+dd,2h),4.8(t,1h),4.35/4.24(d+d,2h),4.24/4.12(d+d,2h),4.07/3.93(dd+dd,2h),3.88(q,2h),3.14/2.99(dd+dd,2h),3.02/2.76(t+dd,2h),3.01/2.64/2.06/1.72(dd+t+dd+t,4h),2.67(s,3h),2.33(s,3h),1.57(m,1h),1.47/1.42/1.28/1.12(d+dd+d+dd,4h),0.97(t,3h)。
[2097]
步骤5:实施例60的制备
[2098]
采用通用方法12,用[4,36-二甲基-30,30-二氧代-24,29-二氧杂-30λ
6-硫杂-1,14,15,16,19-五氮杂七环[23.5.3.2
19,22
.1
3,7
.1
9,13
.0
12,16
.0
28,32
]三十七碳-3(37),4,6,9(36),10,12,14,25,27,32-十烯-8-基]乙酸乙酯e1(1当量)或e2(1当量)作为起始试剂,得到标题化合物(收率分别为48%-44%)。
[2099]
实施例60a(e1)
[2100]c33h37
n5o6s的hrms计算值:631.2464;[m+h]
+
,实测值:632.2538(δ=0.1ppm)。
[2101]
实施例60b(e2)
[2102]c33h37
n5o6s的hrms计算值:631.2464;[m+h]
+
,实测值:632.2542(δ=0.7ppm)。
[2103]1h-nmr(500mhz,dmso-d6)δppm:12.29(brs,1h),7.69(d,1h),7.6(d,1h),7.43(dd,1h),7.25(d,1h),7.04(d,1h),7.01(d,1h),6.97(d,1h),6.95(dd,1h),4.84/4.6(dd+d,2h),4.78(t,1h),4.34/4.24(d+d,2h),4.25/4.11(d+d,2h),4.06/3.93(dd+dd,2h),3.04/2.77(t+dd,2h),3.03/2.9(dd+dd,2h),3.01/2.64/2.07/1.72(dd+t+dd+t,4h),2.66(s,3h),2.34(s,3h),1.57(m,1h),1.47/1.43/1.28/1.12(d+dd+d+dd,4h)。
[2104]
13
c-nmr(125mhz,dmso-d6)δppm:173,157.1,146.4,144.4,141.9,136.6,136.2,132.7,132.5,131.6,129.9,129.8,126.9,126.6,119.2,118.1,116.1,113.7,109.2,71.5,57.9,53.4/51.9,52.3,49.2,46,42.2,41.7,36.5,28.9/28.2,18.9,13.3。
[2105]
实施例61:[(17e)-4,36-二甲基-32,32-二氧代-26,31-二氧杂-32λ
6-硫杂-1,14,15,16-四氮杂七环[25.5.3.1
3,7
.1
9,13
.0
12,16
.0
19,24
.0
30,34
]三十七碳-3(37),4,6,9(36),10,12,14,17,19,21,23,27,29,34-十四烯-8-基]乙酸
[2106][2107]
步骤1:3-(1-乙炔基-4-甲基-1h-苯并三唑-5-基)-3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}丙酸乙酯的制备
[2108]
向搅拌中的3-[1-(2-氯乙基)-4-甲基-苯并三唑-5-基]-3-[3-[(6-羟基-2,2-二氧代-4h-1,2λ6,3-噁噻嗪-3-基)甲基]-4-甲基-苯基]丙酸乙酯盐酸盐(1eq.,1.5g,2.36mmol)的mecn(25ml)溶液中加入cs2co3(3eq.,2.31g,7.08mmol)并将混合物于80℃搅拌过夜。反应完成后将溶剂减压蒸发。将残余物在50ml dcm/50ml水之间进行分配,分层,将水层进一步用2x30ml dcm萃取。将合并的有机层用硫酸镁干燥,过滤并将滤液浓缩至干。将粗产物通过反相色谱纯化,用5mm nh4hco3水溶液-mecn梯度洗脱得到标题化合物(848mg,64%收率)。
[2109]1h-nmr(500mhz,dmso-d6)δppm:9.7(s,1h),7.82(d,1h),7.82(dd,1h),7.62(d,1h),7.23(d,1h),7.2(dd,1h),7.14(d,1h),6.99(d,1h),6.78(dd,1h),6.61(d,1h),5.97/5.29(dd+dd,2h),4.85(t,1h),4.41/4.36(d+d,2h),4.22/4.17(d+d,2h),3.94(q,2h),3.19
(d,2h),2.79(s,3h),2.22(s,3h),1.01(t,3h)。
[2110]
步骤2:3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}-3-(1-{(e)-2-[2-(羟基甲基)苯基]乙炔基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯的制备
[2111]
向搅拌中的3-(1-乙炔基-4-甲基-1h-苯并三唑-5-基)-3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}丙酸乙酯(1eq.,0.844g,1.5mmol)的mecn(8ml)溶液中加入tea(38eq.,8ml,57.4mmol)、(2-碘苯基)甲醇(2eq.,702mg,3mmol)、pph3(0.2eq.,79mg,0.3mmol)和乙酸钯(ii)催化剂(0.1eq.,34mg,0.15mmol)。将混合物用氮气冲洗并在微波反应器中于110℃加热4小时。反应完成后将溶剂减压蒸发。将残余物在50ml dcm/50ml水之间进行分配,分层,然后将水层用50ml dcm萃取。将合并的有机层用硫酸镁干燥,过滤并将滤液浓缩至干。将粗产物通过正相硅胶色谱纯化,用dcm-meoh(100:0至99:1)作为洗脱剂得到标题化合物(808mg,81%收率)。
[2112]1h-nmr(500mhz,dmso-d6)δppm:9.69(s,1h),8.29(d,1h),7.94(d,1h),7.86(dd,1h),7.76(d,1h),7.65(d,1h),7.43(dd,1h),7.36(td,1h),7.33(td,1h),7.26(d,1h),7.21(dd,1h),7.15(d,1h),6.99(d,1h),6.79(dd,1h),6.61(d,1h),5.3(t,1h),4.87(t,1h),4.66(d,2h),4.42/4.38(d+d,2h),4.23/4.19(d+d,2h),3.95(q,2h),3.21(d,2h),2.81(s,3h),2.23(s,3h),1.02(t,3h)。
[2113]
步骤3:3-(1-{(e)-2-[2-(氯甲基)苯基]乙炔基}-4-甲基-1h-苯并三唑-5-基)-3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}丙酸乙酯盐酸盐的制备
[2114]
采用通用方法10,用3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}-3-(1-{(e)-2-[2-(羟基甲基)苯基]乙炔基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯(1当量)作为起始试剂,得到标题化合物(黄色固体泡沫,定量)。产物不经进一步纯化用于下一步。
[2115]1h-nmr(500mhz,dmso-d6)δppm:9.71(brs,1h),8.39(d,1h),7.98(d,1h),7.96(dm,1h),7.78(d,1h),7.68(d,1h),7.51(dm,1h),7.46(m,1h),7.36(m,1h),7.27(d,1h),7.22(dd,1h),7.15(d,1h),6.99(d,1h),6.79(dd,1h),6.61(d,1h),5(s,2h),4.87(t,1h),4.41/4.38(d+d,2h),4.23/4.18(d+d,2h),3.95(q,2h),3.21(d,2h),2.82(s,3h),2.23(s,3h),1.02(t,3h)。
[2116]
步骤4:[(17e)-4,36-二甲基-32,32-二氧代-26,31-二氧杂-32λ
6-硫杂-1,14,15,16-四氮杂七环[25.5.3.1
3,7
.1
9,13
.0
12,16
.0
19,24
.0
30,34
]三十七碳-3(37),4,6,9(36),10,12,14,17,19,21,23,27,29,34-十四烯-8-基]乙酸乙酯的制备
[2117]
采用通用方法11,用3-(1-{(e)-2-[2-(氯甲基)苯基]乙炔基}-4-甲基-1h-苯并三唑-5-基)-3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}丙酸乙酯盐酸盐(1当量)作为起始试剂,得到标题化合物(13%收率)。
[2118]
通过手性柱色谱分离得到对映体纯的最终中间体。
[2119]1h-nmr(500mhz,dmso-d6)δppm:8.42(d,1h),8(d,1h),7.83(d,1h),7.66(d,1h),7.64(d,1h),7.55(d,1h),7.51(t,1h),7.45(dd,1h),7.41(t,1h),7.24(dd,1h),7.23(d,1h),7.21(d,1h),7.02(d,1h),6.92(d,1h),5.26/5.16(d+d,2h),4.89(dd,1h),4.32/4.11
(d+d,2h),4.28/4.08(d+d,2h),3.89(q,2h),3.23/3.08(dd+dd,2h),2.8(s,3h),2.31(s,3h),0.96(t,3h)。
[2120]
步骤5:实施例61的制备
[2121]
采用通用方法12,用[(17e)-4,36-二甲基-32,32-二氧代-26,31-二氧杂-32λ
6-硫杂-1,14,15,16-四氮杂七环[25.5.3.1
3,7
.1
9,13
.0
12,16
.0
19,24
.0
30,34
]三十七碳-3(37),4,6,9(36),10,12,14,17,19,21,23,27,29,34-十四烯-8-基]乙酸乙酯e1(1当量)或e2(1当量)作为起始试剂,得到标题化合物(收率分别为89%-73%)。
[2122]
实施例61a(e1)
[2123]c34h30
n4o6s的hrms计算值:622.1886;[m+h]
+
,实测值:623.1956(δ=-0.5ppm)。
[2124]
实施例61b(e2)
[2125]c34h30
n4o6s的hrms计算值:622.1886;[m+h]
+
,实测值:623.1955(δ=-0.6ppm)。
[2126]1h-nmr(500mhz,dmso-d6)δppm:8.42(d,1h),8(d,1h),7.81(d,1h),7.63(d,1h),7.6(d,1h),7.55(d,1h),7.51(t,1h),7.44(dd,1h),7.41(t,1h),7.24(dd,1h),7.22(d,1h),7.2(d,1h),6.99(d,1h),6.92(d,1h),5.26/5.15(d+d,2h),4.87(t,1h),4.34/4.11(d+d,2h),4.28/4.09(d+d,2h),3.09/2.94(dd+dd,2h),2.8(s,3h),2.31(s,3h)。
[2127]
13
c-nmr(125mhz,dmso-d6)δppm:173.4,156,146.9,145.5,141.7,138.3,136.2,135,134.4,132.1,131.3,131.3,130.5,129.9,129.6,129.2,128.9,128.8,128.2,126.3,125.6,119.9,119.5,118.6,116.1,115.4,109.4,70.8,52,48.7,41.9,40.9,18.5,13.3。
[2128]
实施例62:[4,36-二甲基-32,32-二氧代-26,31-二氧杂-32λ
6-硫杂-1,14,15,16-四氮杂七环[25.5.3.1
3,7
.1
9,13
.0
12,16
.0
19,24
.0
30,34
]三十七碳-3(37),4,6,9(36),10,12,14,19,21,23,27,29,34-十三烯-8-基]乙酸
[2129][2130]
将[(17e)-4,36-二甲基-32,32-二氧代-26,31-二氧杂-32λ
6-硫杂-1,14,15,16-四氮杂七环[25.5.3.1
3,7
.1
9,13
.0
12,16
.0
19,24
.0
30,34
]三十七碳-3(37),4,6,9(36),10,12,14,17,19,21,23,27,29,34-十四烯-8-基]乙酸乙酯(1eq.,49mg,0.075mmol)和pd/c催化剂(0.1eq.,4mg)悬浮于二氧杂环己烷(5ml)中并在不锈钢反应器中在常压下于室温氢化3.5小时。将混合物用硅藻土垫过滤并蒸发至干。将粗产物用通用方法12进行反应得到标题化合物(白色固体,61%收率)。
[2131]
通过手性柱色谱分离得到对映体纯产物。
[2132]
实施例62a(e1)
[2133]c34h32
n4o6s的hrms计算值:624.2042;[m+h]
+
,实测值:625.2141(δ=4.1ppm)。
[2134]
实施例62b(e2)
[2135]c34h32
n4o6s的hrms计算值:624.2042;[m+h]
+
,实测值:625.2128(δ=2.0ppm)。
[2136]1h-nmr(500mhz,dmso-d6)δppm:7.75(d,1h),7.62(d,1h),7.48(d,1h),7.48(d,1h),7.46(t,1h),7.38(d,1h),7.33(t,1h),7.27(d,1h),7.1(d,1h),7.03(dd,1h),6.71(brs.,1h),6.53(d,1h),4.92(m,2h),4.83(t,1h),4.74/4.69(d+d,2h),4.3/3.96(d+d,2h),4.18/4.02(d+d,2h),3.43/3.16(m+m,2h),3.11/2.85(dd+dd,2h),2.71(s,3h),2.33(s,3h)。
[2137]
13
c-nmr(125mhz,dmso-d6)δppm:131.5,131.3,130.5,130.2,129.5,128.4,127.8,127.3,119.6,116,112.8,108,69.2,52,48.8,48.8,41.4,40.9,32.2,18.4,13.3。
[2138]
实施例63:[4,32-二甲基-28,28-二氧代-22,27-二氧杂-19,28λ
6-二硫杂-1,14,15,16-四氮杂六环[21.5.3.1
3,7
.1
9,13
.0
12,16
.0
26,30
]三十三碳-3(33),4,6,9(32),10,12,14,23,25,30-十烯-8-基]乙酸
[2139][2140]
步骤1:3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}-3-(1-{2-[(2-羟基乙基)硫基]乙基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯的制备
[2141]
将3-[1-(2-氯乙基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}丙酸乙酯盐酸盐(1eq.,0.836g,1.395mmol)和k2co3(2.2eq.,424mg,3.070mmol)悬浮于etoh(50ml)。在室温下加入碘化钾(0.1eq.,23mg,0.1395mmol)和2-硫基乙-1-醇(15eq.,1.64g,20.93mmol)并将混合物于60℃加热6天。冷却至室温后,将反应混合物过滤并浓缩至干得到粗产物,将其通过正相硅胶色谱纯化,用dcm-meoh(100:0至95:5)作为洗脱剂得到标题化合物(黄色油,400mg,45%收率)。
[2142]1h-nmr(500mhz,dmso-d6)δppm:9.71(s,1h),7.65(d,1h),7.51(d,1h),7.23(d,1h),7.19(dd,1h),7.13(d,1h),6.99(d,1h),6.79(dd,1h),6.6(d,1h),4.86(t,1h),4.84(dd,1h),4.83(t,2h),4.4/4.36(d+d,2h),4.22/4.17(d+d,2h),3.94(q,2h),3.52(q,2h),3.19/3.15(dd+dd,2h),3.09(t,2h),2.76(s,3h),2.58(t,2h),2.22(s,3h),1.01(t,3h)
[2143]
步骤2:[4,32-二甲基-28,28-二氧代-22,27-二氧杂-19,28λ
6-二硫杂-1,14,15,16-四氮杂六环[21.5.3.1
3,7
.1
9,13
.0
12,16
.0
26,30
]三十三碳-3(33),4,6,9(32),10,12,14,23,25,30-十烯-8-基]乙酸乙酯的制备
[2144]
将3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}-3-(1-{2-[(2-羟基乙基)硫基]乙基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯(1eq.,400mg,0.624mmol)溶于thf(20ml)。加入pph3(4eq.,655mg,2.497mmol)并将混合物冷却至
~5℃。滴加diad(4eq.,504.9mg,2.497mmol)并将混合物在室温下搅拌2小时。反应完成后将混合物浓缩至干得到粗产物,将其通过制备型反相色谱纯化,用5mm nh4hco3水溶液-mecn作为洗脱剂得到标题化合物(215mg,白色固体,55%收率)。
[2145]
通过手性柱色谱分离得到对映体纯的最终中间体。
[2146]1h-nmr(500mhz,dmso-d6)δppm:7.72(d,1h),7.65(d,1h),7.45(dd,1h),7.23(d,1h),7.12(d,1h),7.07(d,1h),6.99(dd,1h),6.11(d,1h),5.04/4.84(m+m,2h),4.81(t,1h),4.36/3.99(m+m,2h),4.35/3.94(d+d,2h),4.14/3.68(d+d,2h),3.88(q,2h),3.41/3.14(m+m,2h),3.36/2.85(m+m,2h),3.12/3.08(dd+dd,2h),2.74(s,3h),2.31(s,3h),0.98(t,3h)。
[2147]
步骤3:[4,32-二甲基-28,28-二氧代-22,27-二氧杂-19,28λ
6-二硫杂-1,14,15,16-四氮杂六环[21.5.3.1
3,7
.1
9,13
.0
12,16
.0
26,30
]三十三碳-3(33),4,6,9(32),10,12,14,23,25,30-十烯-8-基]乙酸的制备
[2148]
采用通用方法12,用[4,32-二甲基-28,28-二氧代-22,27-二氧杂-19,28λ
6-二硫杂-1,14,15,16-四氮杂六环[21.5.3.1
3,7
.1
9,13
.0
12,16
.0
26,30
]三十三碳-3(33),4,6,9(32),10,12,14,23,25,30-十烯-8-基]乙酸乙酯e1(1当量)或e2(1当量)作为起始试剂,得到标题化合物(收率分别为77%-74%)。
[2149]
实施例63a(e1)
[2150]c29h30
n4o6s2的hrms计算值:594.1607;[m+h]
+
,实测值:595.1686(δ=1.1ppm)。
[2151]
实施例63b(e2)
[2152]c29h30
n4o6s2的hrms计算值:594.1607;[m+h]
+
,实测值:595.1681(δ=0.2ppm)。
[2153]1h-nmr(500mhz,dmso-d6)δppm:12.08(br.,1h),7.72(d,1h),7.62(d,1h),7.44(dd,1h),7.23(d,1h),7.11(d,1h),7.04(d,1h),6.98(dd,1h),6.11(d,1h),5.03/4.84(m+m,2h),4.78(t,1h),4.33/3.96(d+d,2h),4.33/3.97(m+m,2h),4.13/3.71(d+d,2h),3.4/3.16(m+m,2h),3.33/2.85(m+m,2h),3(d,2h),2.73(s,3h),2.31(s,3h)。
[2154]
13
c-nmr(125mhz,dmso-d6)δppm:131.4,131.2,129.3,127,119.2,114.9,114.3,108.2,71.5,51.8,48.4,47.2,41.6,41.2,31.3,28.8,18.3,13.3。
[2155]
实施例64:[(2r,8s)-4-氯-2,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸和
[2156]
[(2r,8r)-4-氯-2,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸
[2157][2158]
步骤b1:(1s)-1-[2-氯-5-(4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷-2-基)苯基]乙-1-醇的制备
[2159]
采用通用方法3,用(1s)-1-(5-溴-2-氯苯基)乙-1-醇(1eq.,7.8g.,33.1mmol)作为反应试剂,得到标题化合物(7.1g,76%收率)。
[2160]1h-nmr(400mhz,dmso-d6)δppm:7.98(d,1h),7.5(dd,1h),7.38(dd,1h),5.4(d,1h),5.01(m,1h),1.3(d+s,15h)。
[2161]
步骤1:3-{1-[4-(苄氧基)丁基]-4-甲基-1h-苯并三唑-5-基}-3-{4-氯-3-[(1s)-1-羟基乙基]苯基}丙酸乙酯的制备
[2162]
采用通用方法6,用(2e)-3-{1-[4-(苄氧基)丁基]-4-甲基-1h-苯并三唑-5-基}丙-2-烯酸乙酯(1当量)和(1s)-1-[2-氯-5-(4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷-2-基)苯基]乙-1-醇(2当量)作为起始试剂,得到标题化合物(87%收率)。
[2163]1h-nmr(400mhz,dmso-d6)δppm:7.61/7.47(2dd,2h),7.56/7.33-7.19(s+m,8h),5.32/5.3(2d,1h),4.94(m,1h),4.86(m,1h),4.66(2t,2h),4.4(s,2h),3.93(q,2h),3.42(t,2h),3.17(m,2h),2.77/2.76(2s,3h),1.94(quint,2h),1.5(quint,2h),1.27/1.24(2d,3h),1(t,3h)。
[2164]
步骤2:3-{1-[4-(苄氧基)丁基]-4-甲基-1h-苯并三唑-5-基}-3-(3-{(1r)-1-[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]乙基}-4-氯苯基)丙酸乙酯的制备
[2165]
采用通用方法7,用3-{1-[4-(苄氧基)丁基]-4-甲基-1h-苯并三唑-5-基}-3-{4-氯-3-[(1s)-1-羟基乙基]苯基}丙酸乙酯(1当量)和6-(苄氧基)-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮(1.1当量)作为起始试剂,得到标题化合物(82%收率)。
[2166]1h-nmr(400mhz,dmso-d6)δppm:0.93-1.01(m,3h)1.40-1.54(m,5h)1.86-1.98(m,2h)2.77(s,3h)3.19-3.26(m,2h)3.36-3.45(m,2h)3.85-3.98(m,2h)4.36-4.41(m,2h)4.43-4.60(m,2h)4.60-4.70(m,2h)4.84-4.95(m,1h)5.03-5.13(m,2h)5.35-5.43(m,1h)6.81-6.94(m,1h)6.98-7.07(m,1h)7.17-7.31(m,5h)7.36(s,1h)7.37-7.47(m,5h)7.51-7.57(m,1h)7.62(d,j=8.56hz,1h)。
[2167]
步骤3:3-{4-氯-3-[(1r)-1-(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)乙基]苯基}-3-[1-(4-羟基丁基)-4-甲基-1h-苯并三唑-5-基]丙酸乙酯的制备
[2168]
采用通用方法8,用3-{1-[4-(苄氧基)丁基]-4-甲基-1h-苯并三唑-5-基}-3-(3-{(1r)-1-[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]乙基}-4-氯苯基)丙酸乙酯(1当量)作为起始试剂,得到标题化合物(48%收率)。
[2169]1h-nmr(400mhz,dmso-d6)δppm:9.6(s,1h),7.65(m,2h),7.6(d,1h),7.35(d,1h),
7.2(dd,1h),6.9(d,1h),6.7(dd,1h),6.6(d,1h),5.4(m,1h),4.9(m,1h),4.65(t,2h),4.45(m,3h),3.95(q,2h),3.4(q,2h),3.25(d,2h),2.8(s,3h),1.9(m,2h),1.5(m,3h),1.4(m,2h),1(2t,3h)。
[2170]
步骤4:3-[1-(4-溴丁基)-4-甲基-1h-苯并三唑-5-基]-3-{4-氯-3-[(1r)-1-(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)乙基]苯基}丙酸乙酯的制备
[2171]
采用通用方法9,用3-{4-氯-3-[(1r)-1-(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)乙基]苯基}-3-[1-(4-羟基丁基)-4-甲基-1h-苯并三唑-5-基]丙酸乙酯(1当量)作为起始试剂,得到标题化合物(黄色油,70%收率)。
[2172]1h-nmr(400mhz,dmso-d6)δppm:9.63/9.62(2m,1h),7.67(d,1h),7.66/7.58(dd,2h),7.36(d,1h),7.25(dd,1h),6.9(d,1h),6.72(m,1h),6.62/6.59(d,1h),5.37(m,1h),4.94-4.87(m,1h),4.7(t,2h),4.51-4.39(m,2h),3.94(q,2h),3.54(q,2h),3.25(d,2h),2.77(s,3h),2(m,2h),1.77(m,2h),1.46(m,3h),1(t,3h)。
[2173]
步骤5:[(2r)-4-氯-2,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯的制备
[2174]
采用通用方法11,用3-[1-(4-溴丁基)-4-甲基-1h-苯并三唑-5-基]-3-{4-氯-3-[(1r)-1-(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)乙基]苯基}丙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体,98%收率)。
[2175]1h-nmr(400mhz,dmso-d6)δppm:0.96-1.08(m,5h)1.14(d,j=6.85hz,2h)1.29(d,j=6.97hz,4h)1.55-1.77(m,2h)1.77-1.90(m,1h)1.92-2.27(m,3h)2.61-2.86(m,5h)2.98-3.20(m,2h)3.34-3.53(m,4h)3.59-3.80(m,2h)3.86-4.03(m,3h)4.03-4.17(m,2h)4.66-4.80(m,3h)4.86(t,j=7.95hz,1h)4.95(t,j=7.76hz,1h)5.28-5.47(m,2h)5.72(d,j=2.81hz,1h)5.85(br.s.,1h)6.66-6.80(m,2h)6.87-6.98(m,2h)7.15(d,j=8.80hz,1h)7.31(d,j=1.96hz,1h)7.48(d,j=8.19hz,1h)7.57-7.63(m,2h)7.71(d,j=8.68hz,1h)7.78(d,j=8.68hz,1h)7.91(d,j=8.80hz,1h)。
[2176]
步骤6:实施例64的制备
[2177]
采用通用方法12,用[(2r)-4-氯-2,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体,定量)。
[2178]
通过手性柱色谱分离得到非对映体纯产物。
[2179]
实施例64a(2r,8s)
[2180]c29h29
cln4o6s的hrms计算值:596.1496;[m+h]
+
,实测值:597.1572(δ=0.5ppm)。
[2181]1h-nmr(400mhz,dmso-d6)δppm:12.16(m,1h),7.9(d,1h),7.78(d,1h),7.61(dd,1h),7.49(d,1h),7.27(d,1h),6.94(d,1h),6.75(dd,1h),5.69(d,1h),5.4(m,1h),4.83(m,1h),4.82-4.68(m,2h),4.1/3.38(dd,2h),3.67/3.47(2m,2h),3.24/3.05(2dd,2h),2.66(s,3h),2.18/2.1(2m,2h),1.86/1.74(2m,2h),1.28(d,3h)。
[2182]
实施例64b(2r,8r)
[2183]c29h29
cln4o6s的hrms计算值:596.1496;[m+h]
+
,实测值:597.1573(δ=0.7ppm)。
[2184]1h-nmr(400mhz,dmso-d6)δppm:12.33(m,1h),7.71(d,1h),7.6/6.9(2s,3h),7.11(d,1h),6.92(d,1h),6.73(dd,1h),5.86(d,1h),5.36(q,1h),4.93(m,1h),4.76(m,2h),4.1/3.49(dd,2h),3.76/3.65(2m,2h),3.28/2.91(2dd,2h),2.66(s,3h),2.21/2.04(2m,2h),1.66/1.32(2m,2h),1.14(d,3h)。
[2185]
实施例65:{4,31-二甲基-27,27-二氧代-18-[4-(三氟甲基)苯基]-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基}乙酸
[2186][2187]
步骤1:3-(3-{[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-甲基苯基)-3-[4-({4-羟基-2-[4-(三氟甲基)苯基]丁基}氨基)-2-甲基-3-硝基苯基]丙酸乙酯的制备
[2188]
将3-(3-{[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-甲基苯基)-3-(4-氟-2-甲基-3-硝基苯基)丙酸乙酯(1eq.,2g,3.1mmol)和4-氨基-3-[4-(三氟甲基)苯基]丁-1-醇(1.5eq.,1.078g,4.622mmol)溶于n,n-二甲基乙酰胺(5ml)。加入dipea(1.85eq.,1ml,5.741mmol)并将混合物在n2下于100℃搅拌过夜。加入过量4-氨基-3-[4-(三氟甲基)苯基]丁-1-醇(0.25g,1.072mmol),然后加入dipea(0.3ml,1.72mmol)并将混合物于100℃继续搅拌24小时。冷却后倒在冰冷的盐水上并用dcm萃取,将收集的有机相用硫酸钠干燥并蒸发到硅藻土上。将粗产物通过正相硅胶色谱纯化,用dcm-meoh(100:0至95.2:4.8)作为洗脱剂,经高真空室温下干燥后得到2.334g(88%收率)标题化合物。
[2189]1h-nmr(500mhz,dmso-d6)δppm:7.63/7.62(d/d,2h),7.43(d,2h),7.41(d/d,2h),7.39(t,2h),7.34(t,1h),7.33(d,1h),7.16(db,1h),7.15(d,1h),7.14(d,1h),7.11(dd,1h),7.07(dd,1h),6.99/6.98(d/d,1h),6.75(d,1h),5.62(t,1h),5.09(s,2h),4.53(t,1h),4.46/4.42(d+d,2h),4.45(t,1h),4.24/4.23/4.19/4.19(d+d/d+d,2h),3.97/3.95(q/q,2h),3.39/3.27(m+m,2h),3.28/3.27/3.18/3.16(m+m/m+m,2h),3.13(m,1h),3.05/3.04/3.01/3(dd+dd/dd+dd,2h),2.22/2.21(s/s,3h),2.11(s,3h),1.88/1.7(m+m,2h),1.04/1.03(t/t,3h)。
[2190]
步骤2:3-[3-氨基-4-({4-羟基-2-[4-(三氟甲基)苯基]丁基}氨基)-2-甲基苯基]-3-(3-{[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-甲基苯基)
丙酸乙酯的制备
[2191]
向3-(3-{[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-甲基苯基)-3-[4-({4-羟基-2-[4-(三氟甲基)苯基]丁基}氨基)-2-甲基-3-硝基苯基]丙酸乙酯(1eq.,2.327g,2.7p mmol)的1,2-二氯乙烷(7ml)和ipa(7ml)溶液中加入阮内镍催化剂(0.65g,7.6mmol)。在60分钟内滴加水合肼(0.8109g,0.7858ml,8.100mmol)(放热反应!)并将反应混合物室温继续搅拌30分钟。将反应混合物通过硅藻土垫过滤,将硅藻土用dcm(3x15ml)和thf(2x15ml)洗涤。将滤液蒸发得到2.267g(定量)浅黄色泡沫状标题化合物。
[2192]1h-nmr(500mhz,dmso-d6)δppm:7.63(m,2h),7.48-7.3(m,5h),7.46(m,2h),7.14(d,1h),7.09(d,1h),7.07(dd,1h),7.06(d,1h),7.02/7.01(dd,1h),6.98(d,1h),6.35(d,1h),5.1(s,2h),4.51(t,1h),4.43(t,1h),4.42(s,2h),4.32(t,1h),4.21/4.14(d+d,2h),4.12(s,2h),3.96/3.93(m+m,2h),3.48(d,1h),3.29/3.19(m+m,2h),3.23/3.16(m+m,2h),3.15(m,1h),2.9(d,2h),2.2(s,3h),1.98-1.72(m+m,2h),1.94(s,3h),1.05(t,3h)
[2193]
步骤3:3-(3-{[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-甲基苯基)-3-(1-{4-羟基-2-[4-(三氟甲基)苯基]丁基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯的制备
[2194]
将3-[3-氨基-4-({4-羟基-2-[4-(三氟甲基)苯基]丁基}氨基)-2-甲基苯基]-3-(3-{[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-甲基苯基)丙酸乙酯(1eq.,2.24g,2.69mmol)溶于thf(15ml)和acoh(1.5ml)的混合物。在0℃下向其中加入澄清的3-甲基丁基亚硝酸酯溶液(3eq.,0.946g,1.09ml,8.08mmol)并将混合物在室温下搅拌3小时。将混合物倒在饱和nahco3溶液上并用etoac萃取。将水层进一步用etoac部分洗涤,将合并的有机层用硫酸钠干燥,过滤并减压蒸发。将粗产物通过制备型hplc在反相c18柱上纯化,用nh4hco3水溶液-mecn(100:0至30:70)作为洗脱剂得到0.80g(40%收率)浅黄色泡沫状标题化合物。
[2195]1h-nmr(500mhz,dmso-d6)δppm:7.53(d,2h),7.47(d,1h),7.46(m,2h),7.44/7.43(d/d,1h),7.41(m,2h),7.4(m,2h),7.34(tm,1h),7.22(brs.,1h),7.17/7.11(dd/m,1h),7.14(d,1h),7.11(m,1h),7.07(dd,1h),6.96/6.95(d/d,1h),5.11/5.08(d+d,2h),4.89(m,2h),4.8(t,1h),4.48/4.47(t/t,1h),4.44(m,2h),4.21(m,2h),3.92/3.89(q/q,2h),3.58(m,1h),3.27/3.14(m+m,2h),3.14(m,2h),2.7(s,3h),2.21(s,3h),1.82(m,2h),0.96/0.92(t/t,3h)。
[2196]
步骤4:3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}-3-(1-{4-羟基-2-[4-(三氟甲基)苯基]丁基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯的制备
[2197]
采用通用方法8,用3-(3-{[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-甲基苯基)-3-(1-{4-羟基-2-[4-(三氟甲基)苯基]丁基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色泡沫状物质,96%收率)。
[2198]1h-nmr(500mhz,dmso-d6)δppm:9.71(s,1h),7.55(d,2h),7.5/7.48(d/d,1h),7.45(d,1h),7.43(d,2h),7.21(brs.,1h),7.17/7.11(d/d,1h),7.12(m,1h),7(d,1h),6.79(dd,1h),6.61/6.6(d/d,1h),4.92(m,2h),4.79(t,1h),4.38(s,2h),4.21/4.17(d+d,2h),3.91(m,2h),3.6(m,1h),3.28/3.15(m+m,2h),3.14(m,2h),2.7/2.69(s/s,3h),2.22(s,
3h),1.83(m,2h),0.97/0.94(t/t,3h)
[2199]
步骤5:3-(1-{4-氯-2-[4-(三氟甲基)苯基]丁基}-4-甲基-1h-苯并三唑-5-基)-3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}丙酸乙酯的制备
[2200]
采用通用方法10,用3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}-3-(1-{4-羟基-2-[4-(三氟甲基)苯基]丁基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯(1当量)作为起始试剂,得到标题化合物(黄色固体泡沫,定量)。产物不经进一步纯化用于下一步。1h-nmr(500mhz,dmso-d6)δppm:9.72(br.,1h),7.58(d,2h),7.5/7.49(d/d,1h),7.47/7.45(d/d,1h),7.4(d,2h),7.21(brs.,1h),7.17/7.11(d/d,1h),7.12(m,1h),6.99(d,1h),6.79(dd,1h),6.61(brs.,1h),4.97(m,2h),4.79(t,1h),4.38(s,2h),4.21/4.17(d+d,2h),3.91(m,2h),3.66(m,1h),3.53/3.31(m+m,2h),3.14(m,2h),2.69(s/s,3h),2.24/2.12(m+m,2h),2.22(s,3h),0.97/0.93(t/t,3h)。
[2201]
步骤6:{4,31-二甲基-27,27-二氧代-18-[4-(三氟甲基)苯基]-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基}乙酸乙酯的制备
[2202]
将3-(1-{4-氯-2-[4-(三氟甲基)苯基]丁基}-4-甲基-1h-苯并三唑-5-基)-3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}丙酸乙酯(1eq.,0.55g,0.71mmol)溶于n,n-二甲基乙酰胺(5ml)。加入cs2co3(1.7eq.,0.50g,1.5mmol)并将混合物于120℃搅拌3小时。反应完成后将混合物通过硅藻土垫过滤,用dcm洗涤。蒸发母液并将粗产物通过反相c18柱色谱纯化,用nh4hco3水溶液-mecn(100:0至0:100)洗脱得到0.23g(44%收率)黄色泡沫状所需化合物。
[2203]1h-nmr(500mhz,dmso-d6,非对映异构体的混合物)δppm:7.87/7.84(d/d,1h),7.8/7.78(s/d,2h),7.8/7.67(s/d,2h),7.58/7.5(d/d,1h),7.51/7.49(dd/dd,1h),7.31/7.29(d/d,1h),7(d,1h),6.79/6.77(dd/dd,1h),6.61/6.55(d/d,1h),6.02/5.82(d/d,1h),5.16/5.04/4.86/4.77(dd/dd+dd/dd,2h),4.8(t,1h),4.22/4.15/3.97/3.87(d/d+d/d,2h),4.08/4.04/3.85/3.82(d/d+d/d,2h),3.93/3.92(q/q,2h),3.78/3.6(m/m,1h),3.61/3.53/3.53/3.06(m/m+m/m,2h),3.22-3.03(m,2h),2.64/2.62(s/s,3h),2.35-2(m,2h),2.34/2.33(s/s,3h),1.02/1.01(t/t,3h)。
[2204]
步骤7:实施例65的制备
[2205]
采用通用方法12,用{4,31-二甲基-27,27-二氧代-18-[4-(三氟甲基)苯基]-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基}乙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体,29%收率)。
[2206]c36h33
f3n4o6s的hrms计算值:706.2073;[m+h]
+
,实测值:707.2142(δ=-0.5ppm)。
[2207]1h-nmr(500mhz,dmso-d6,非对映异构体的混合物)δppm:12.13(br.,1h),7.86/7.84(d/d,1h),7.8/7.68(s/d,2h),7.8/7.78(s/d,2h),7.56/7.5(d/d,1h),7.52/7.5(dd/dd,1h),7.31/7.3(d/d,1h),6.99(d,1h),6.79/6.77(dd/dd,1h),6.59/6.53(d/d,1h),6/5.81(d/d,1h),5.15/5.04/4.85/4.77(dd/dd+dd/dd,2h),4.78(t,1h),4.22/4.14/3.98/3.87(d/d+d/d,2h),4.07/4.04/3.86/3.82(d/d+d/d,2h),3.78/3.63(m/m,1h),3.67-3.02
(m,2h),3.06/2.99(m+m,2h),2.63/2.62(s/s,3h),2.38-2.02(m,2h),2.34/2.33(s/s,3h)。
[2208]
13
c-nmr(125mhz,dmso-d6)δppm:173.2,131.4/131.3,131.1,129.5/129.2,128.8,127.6/127.4,126.1,119.6/119.4,117.7/117.3,111.7/111.3,108.3/108,66.5/66.3,54/52.5,51.9,48.8/48.7,43.7/41.2,41.9/41.8,40.9,34.2/32.7,18.5/18.4,13.5/13.4。
[2209]
实施例66:[30-氯-4,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸
[2210][2211]
步骤1:6-(苄氧基)-3-[(5-溴-2-甲基苯基)甲基]-5-氯-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮的制备
[2212]
将6-(苄氧基)-3-[(5-溴-2-甲基苯基)甲基]-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮(1eq.,2g,4.2mmol)溶于硝基甲烷(40ml),然后加入(3eq.,7.78g,12.7mmol)和氯化钾(1.8eq.,5.66g,7.5921mmol)。将反应混合物于60℃搅拌2天。减压浓缩后,将残余物溶于dcm并将溶液用水洗涤。将有机相用硫酸镁干燥,过滤并减压浓缩得到2.078g粗产物,将其通过快速色谱纯化,用庚烷-etoac作为洗脱剂得到黄色油状标题化合物(1.404g,2.759mmol,65%收率)。
[2213]1h-nmr(500mhz,dmso-d6)δppm:7.51-7.32(m,5h),7.5(d,1h),7.47(dd,1h),7.34(d,1h),7.22(d,1h),7.21(d,1h),5.25(s,2h),4.59(s,2h),4.36(s,2h),2.26(s,3h)。
[2214]
步骤2:6-(苄氧基)-5-氯-3-{[2-甲基-5-(4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷-2-基)苯基]甲基}-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮的制备
[2215]
采用通用方法3,用6-(苄氧基)-3-[(5-溴-2-甲基苯基)甲基]-5-氯-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮(1eq.,1.40g,2.75mmol)作为起始试剂,得到标题化合物(1.33g,87%收率)。
[2216]1h-nmr(500mhz,dmso-d6)δppm:7.58(dd,1h),7.51(d,1h),7.49-7.33(m,5h),7.35(s,1h),7.28(d,1h),7.22(d,1h),5.25(s,2h),4.5(s,2h),4.34(s,2h),2.33(s,3h),1.28(s,12h)。
[2217]
步骤3:3-{1-[4-(苄氧基)丁基]-4-甲基-1h-苯并三唑-5-基}-3-(3-{[6-(苄氧基)-5-氯-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-甲基苯基)丙酸乙酯的制备
[2218]
采用通用方法6,用(2e)-3-{1-[4-(苄氧基)丁基]-4-甲基-1h-苯并三唑-5-基}丙-2-烯酸乙酯(1eq.,0.92g,2.34mmol)和6-(苄氧基)-5-氯-3-{[2-甲基-5-(4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷-2-基)苯基]甲基}-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮
(1eq.,1.30g,2.34mmol)作为起始试剂,得到标题化合物(638mg,33%收率)。
[2219]1h-nmr(500mhz,dmso-d6)δppm:7.56(d,1h),7.51-7.21(m,10h),7.46(d,1h),7.33(d,1h),7.25(m,1h),7.24(m,1h),7.2(d,1h),7.16(d,1h),5.24(s,2h),4.84(t,1h),4.63(t,2h),4.39(s,2h),4.37(s,2h),4.26(s,2h),3.91(q,2h),3.38(t,2h),3.15(d,2h),2.76(s,3h),2.25(s,3h),1.91(m,2h),1.47(m,2h),0.97(t,3h)。
[2220]
步骤4:3-{3-[(5-氯-6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}-3-[1-(4-羟基丁基)-4-甲基-1h-苯并三唑-5-基]丙酸乙酯的制备
[2221]
采用通用方法8,用3-{1-[4-(苄氧基)丁基]-4-甲基-1h-苯并三唑-5-基}-3-(3-{[6-(苄氧基)-5-氯-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-甲基苯基)丙酸乙酯(1eq.,755mg,0.9169mmol)作为起始试剂,得到标题化合物(423mg,72%收率)。
[2222]1h-nmr(500mhz,dmso-d6)δppm:10.5(br.,1h),7.58(d,1h),7.48(d,1h),7.24(m,1h),7.24(m,1h),7.16(d,1h),7.04(d,1h),7.02(d,1h),4.84(t,1h),4.64(t,2h),4.43(br.,1h),4.36(s,2h),4.26/4.22(d+d,2h),3.92(q,2h),3.38(t,2h),3.15(d,2h),2.76(s,3h),2.24(s,3h),1.9(m,2h),1.36(m,2h),0.99(t,3h)。
[2223]
步骤5:3-[1-(4-氯丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(5-氯-6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}丙酸乙酯的制备
[2224]
采用通用方法10,用3-{3-[(5-氯-6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}-3-[1-(4-羟基丁基)-4-甲基-1h-苯并三唑-5-基]丙酸乙酯(1eq.,420mg,0.6530mmol)作为起始试剂,得到标题化合物(444mg,99%收率)。
[2225]1h-nmr(500mhz,dmso-d6)δppm:10.52(s,1h),7.6(d,1h),7.49(d,1h),7.24(dd,1h),7.23(d,1h),7.16(d,1h),7.04(d,1h),7.02(d,1h),4.84(t,1h),4.68(t,2h),4.35(s,2h),4.25/4.22(d+d,2h),3.92(q,2h),3.64(t,2h),3.15(d,2h),2.75(s,3h),2.24(s,3h),1.99/1.68(m+m,4h),0.98(t,3h)。
[2226]
步骤6:[30-氯-4,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯的制备
[2227]
采用通用方法11,用3-[1-(4-氯丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(5-氯-6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}丙酸乙酯(1eq.,432mg,0.6530mmol)作为起始试剂,得到标题化合物(372mg,91%收率)。
[2228]1h-nmr(500mhz,dmso-d6)δppm:7.55(d,1h),7.5(dd,1h),7.31(d,1h),7.31(d,1h),7.15(d,1h),7.06(d,1h),6.41(d,1h),4.78/4.73(dm+dm,2h),4.78(t,1h),4.12/4.01(d+d,2h),4.1/4.01(m+m,2h),4.05/3.98(d+d,2h),3.9(m,2h),3.23/3.01(dd+dd,2h),2.6(s,3h),2.33(s,3h),2.23/2.06(m+m,2h),1.67/1.53(m+m,2h),0.97(t,3h)。
[2229]
步骤7:实施例66的制备
[2230]
采用通用方法12,用[30-氯-4,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯(1eq.,370mg,0.5919mmol)作为起始试剂,得到标题化合物(221mg,63%收率)。
[2231]
通过手性柱色谱分离得到对映体纯产物。
[2232]
实施例66a(e1)
[2233]c29h29
cln4o6s的hrms计算值:596.1496;[m+h]
+
,实测值:597.1565(δ=-0.7ppm)。
[2234]
实施例66b(e2)
[2235]c29h29
cln4o6s的hrms计算值:596.1496;[m+h]
+
,实测值:597.1567(δ=-0.4ppm)。
[2236]1h-nmr(500mhz,dmso-d6)δppm:7.55(d,1h),7.51(d,1h),7.31(d,1h),7.29(d,1h),7.15(d,1h),7.05(d,1h),6.39(s,1h),4.79/4.71(m+m,2h),4.79/4.71(d+d,2h),4.76(t,1h),4.12/4.01(d+d,2h),4.09/4.01(m+m,2h),3.1/2.88(dd+dd,2h),2.6(s,3h),2.33(s,3h),2.24/2.07(m+m,2h),1.67/1.52(m+m,2h)。
[2237]
13
c-nmr(125mhz,dmso-d6)δppm:131.4,131.3,128.4,127,118,117.7,108.5,71.4,52.7,48,48,41.1,41.1,27.2,26.5,18.5,13.3。
[2238]
实施例67:[4,38-二甲基-34,34-二氧代-28,33-二氧杂-20,34λ
6-二硫杂-1,14,15,16-四氮杂七环[27.5.3.1
3,7
.1
9,13
.0
12,16
.0
21,26
.0
32,36
]三十九碳-3(39),4,6,9(38),10,12,14,21,23,25,29,31,36-十三烯-8-基]乙酸
[2239][2240]
步骤a1:(2e)-3-(4-甲基-1-{3-[(氧杂环己烷-2-基)氧基]丙基}-1h-苯并三唑-5-基)丙-2-烯酸乙酯的制备
[2241]
于0℃向(2e)-3-[1-(3-羟基丙基)-4-甲基-1h-苯并三唑-5-基]丙-2-烯酸乙酯(1eq.,4.34g,15mmol)的dcm(50ml)溶液中加入4-甲基苯-1-磺酸一水合物(0.01eq.,38mg,0.15mmol),然后加入3,4-二氢-2h-吡喃(1.1equiv.,1.39g,16.5mmol)。将反应混合物升温至室温并搅拌1小时,然后用饱和nahco3(30ml)淬灭。分相。将水相用dcm(30ml)萃取,并将合并的有机相用mgso4干燥。减压除去溶剂得到标题化合物(5.5g,98%收率)。
[2242]1h-nmr(500mhz,dmso-d6)δppm:8.02(d,1h),7.97(d,1h),7.71(d,1h),6.65(d,1h),4.77(t,2h),4.47(dd,1h),4.22(q,2h),3.65/3.36(m+m,2h),3.62/3.29(m+m,2h),2.81(s,3h),2.16(m,2h),1.71-1.32(m,6h),1.28(t,3h)。
[2243]
步骤1:3-[3-(羟基甲基)-4-甲基苯基]-3-(4-甲基-1-{3-[(氧杂环己烷-2-基)氧基]丙基}-1h-苯并三唑-5-基)丙酸乙酯的制备
[2244]
将(2e)-3-(4-甲基-1-{3-[(氧杂环己烷-2-基)氧基]丙基}-1h-苯并三唑-5-基)丙-2-烯酸乙酯(1eq.,5.5g,0.015mol)加入到二氧杂环己烷(90ml)和水(45ml)中并将该悬浮液用氮气脱气。加入[2-甲基-5-(4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷-2-基)苯基]甲醇(1.5当量,5.5g,0.022mol)和tea(1.6eq.,2.4g,0.024mol),然后加入氯(1,5-环辛二烯)铑(i)二聚体催化剂(0.05当量,0.36g,0.00074mol)。将反应混合物于80℃加热30分钟,然后升温搅拌过夜。反应完成后,将混合物用水(50ml)稀释。将溶液用etoac萃取(2x50ml)。将合并的有机层用盐水(50ml)洗涤并用mgso4干燥。将溶剂蒸发得到深色油,将其通过快速
色谱纯化,用庚烷/etoac(50:50)作为洗脱剂得到标题化合物(7.3g,定量)。
[2245]1h-nmr(500mhz,dmso-d6)δppm:7.6(d,1h),7.47(d,1h),7.26(d,1h),7.1(dd,1h),7.02(d,1h),4.99(t,1h),4.83(t,1h),4.71(t,2h),4.45(dd,1h),4.4(d,2h),3.92(q,2h),3.62/3.33(m+m,2h),3.59/3.26(m+m,2h),3.13(m,2h),2.76(s,3h),2.15(s,3h),2.13(m,2h),1.7-1.3(m,6h),1.01(t,3h)。
[2246]
步骤2:3-(3-{[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-甲基苯基)-3-(4-甲基-1-{3-[(氧杂环己烷-2-基)氧基]丙基}-1h-苯并三唑-5-基)丙酸乙酯的制备
[2247]
将3-[3-(羟基甲基)-4-甲基苯基]-3-(4-甲基-1-{3-[(氧杂环己烷-2-基)氧基]丙基}-1h-苯并三唑-5-基)丙酸乙酯(1eq.,3.0g,6.1mmol)溶于thf(20ml),然后加入6-(苄氧基)-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮(1eq.,1.80g,6.18mmol)和pph3(2eq.,3.20g,12.2mmol)。将混合物冷却至5℃,滴加diad(2eq.,2.40g,11.9mmol)并将反应混合物室温搅拌2小时。将溶剂蒸发至干。将粗产物通过正相硅胶色谱纯化,用庚烷-etoac(100:0至50:50)作为洗脱剂得到标题化合物(2.8g,60%收率)。
[2248]1h-nmr(500mhz,dmso-d6)δppm:7.58(d,1h),7.49-7.31(m,5h),7.49(d,1h),7.22(d,1h),7.19(dd,1h),7.13(d,1h),7.13(d,1h),7.07(dd,1h),6.96(d,1h),5.1(s,2h),4.85(t,1h),4.68(t,2h),4.43(s,2h),4.42(dd,1h),4.21(s,2h),3.92(q,2h),3.6/3.31(m+m,2h),3.57/3.24(m+m,2h),3.2/3.15(dd+dd,2h),2.77(s,3h),2.22(s,3h),2.11(m,2h),1.69-1.26(m,6h),0.99(t,3h)。
[2249]
步骤3:3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}-3-(4-甲基-1-{3-[(氧杂环己烷-2-基)氧基]丙基}-1h-苯并三唑-5-基)丙酸乙酯的制备
[2250]
在装备有ptfe涂覆的磁力搅拌棒的烘箱干燥的容器中将3-(3-{[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-甲基苯基)-3-(4-甲基-1-{3-[(氧杂环己烷-2-基)氧基]丙基}-1h-苯并三唑-5-基)丙酸乙酯(1eq.,2.80g,3.6mmol)溶于thf(45ml)。加入pd/c并将混合物在4巴压力下室温氢化12小时。反应完成后滤出催化剂。将母液蒸发至干得到标题化合物(2.45g,99%收率)。
[2251]1h-nmr(500mhz,dmso-d6)δppm:9.7(s,1h),7.6(d,1h),7.51(d,1h),7.21(d,1h),7.19(dd,1h),7.13(d,1h),6.99(d,1h),6.79(dd,1h),6.6(d,1h),4.84(t,1h),4.71(t,2h),4.43(m,1h),4.38(s,2h),4.21/4.17(d+d,2h),3.93(q,2h),3.61/3.33(m+m,2h),3.59/3.27(m+m,2h),3.19/3.15(dd+dd,2h),2.75(s,3h),2.22(s,3h),2.14(qn,2h),1.66-1.31(m,6h),1(t,3h)。
[2252]
步骤4:3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}-3-[1-(3-羟基丙基)-4-甲基-1h-苯并三唑-5-基]丙酸乙酯的制备
[2253]
将3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}-3-(4-甲基-1-{3-[(氧杂环己烷-2-基)氧基]丙基}-1h-苯并三唑-5-基)丙酸乙酯(1eq.,2.40g,3.60mmol)溶于etoh(25.0ml)并加入4-甲基苯-1-磺酸吡啶复合物(0.05eq.,45.3mg,0.180mmol)。将反应混合物于55℃搅拌2小时。将反应混合物浓缩,将残余物溶于dcm,用2x20ml nahco3洗涤,然后用20ml盐水洗涤,用硫酸镁干燥,过滤并蒸发至干得到标
题化合物(1.90g,88%收率)。
[2254]1h-nmr(500mhz,dmso-d6)δppm:9.71(brs.,1h),7.6(d,1h),7.5(d,1h),7.22(d,1h),7.19(dd,1h),7.13(d,1h),6.99(d,1h),6.79(dd,1h),6.6(d,1h),4.84(t,1h),4.68(t,2h),4.67(br.,1h),4.4/4.36(d+d,2h),4.21/4.17(d+d,2h),3.94(q,2h),3.38(t,2h),3.19/3.15(dd+dd,2h),2.76(s,3h),2.22(s,3h),2.01(m,2h),1(t,3h)。
[2255]
步骤5:3-[1-(3-氯丙基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}丙酸乙酯的制备
[2256]
采用通用方法10,用3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}-3-[1-(3-羟基丙基)-4-甲基-1h-苯并三唑-5-基]丙酸乙酯(1当量)作为起始试剂,得到标题化合物(97%收率)。
[2257]1h-nmr(500mhz,dmso-d6)δppm:9.76(brs,1h),7.63(d,1h),7.53(d,1h),7.22(d,1h),7.2(dd,1h),7.13(d,1h),6.99(d,1h),6.8(dd,1h),6.6(d,1h),4.84(t,1h),4.77(t,2h),4.37(s,2h),4.21/4.17(d+d,2h),3.93(q,2h),3.61(t,2h),3.19/3.15(dd+dd,2h),2.76(s,3h),2.33(qn,2h),2.22(s,3h),1(t,3h)。
[2258]
步骤6:3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}-3-[1-(3-{[2-(羟基甲基)苯基]硫基}丙基)-4-甲基-1h-苯并三唑-5-基]丙酸乙酯的制备
[2259]
将3-[1-(3-氯丙基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}丙酸乙酯(1eq.,1.61g,2.63mmol)和(2-硫基苯基)甲醇(1.2eq.,442mg,3.15mmol)溶于dmf(9ml)并加入k2co3,(2eq.,726mg,5.25mmol)。将反应混合物室温搅拌2小时。倒入10ml水中后,将混合物用2x30ml dcm萃取。将合并的有机层用硫酸镁干燥,过滤并蒸发至干得到黄色结晶产物(1.5g,79%收率)。
[2260]1h-nmr(500mhz,dmso-d6)δppm:9.7(s,1h),7.59(d,1h),7.51(d,1h),7.43(d,1h),7.22(d,1h),7.19(dd,1h),7.19(d,1h),7.17(t,1h),7.13(d,1h),7.12(t,1h),6.99(d,1h),6.79(dd,1h),6.6(d,1h),5.22(t,1h),4.84(t,1h),4.76(t,2h),4.52(d,2h),4.4/4.35(d+d,2h),4.21/4.17(d+d,2h),3.93(q,2h),3.19/3.13(dd+dd,2h),2.9(t,2h),2.76(s,3h),2.22(s,3h),2.13(qn,2h),1(t,3h)。
[2261]
步骤7:3-[1-(3-{[2-(氯甲基)苯基]硫基}丙基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}丙酸乙酯的制备
[2262]
采用通用方法10,用3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}-3-[1-(3-{[2-(羟基甲基)苯基]硫基}丙基)-4-甲基-1h-苯并三唑-5-基]丙酸乙酯(1当量)作为起始试剂,得到标题化合物(98%收率)。
[2263]c37h39
cln4o6s2的hrms计算值:734.2000;[m+h]
+
,实测值:735.2057(δ=-2.1ppm)。
[2264]
步骤8:[4,38-二甲基-34,34-二氧代-28,33-二氧杂-20,34λ
6-二硫杂-1,14,15,16-四氮杂七环[27.5.3.1
3,7
.1
9,13
.0
12,16
.0
21,26
.0
32,36
]三十九碳-3(39),4,6,9(38),10,12,14,21,23,25,29,31,36-十三烯-8-基]乙酸乙酯的制备
[2265]
采用通用方法11,用3-[1-(3-{[2-(氯甲基)苯基]硫基}丙基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯
基}丙酸乙酯(1eq.,1.56g,2.12mmol)作为起始试剂,得到标题化合物(1.375g,黄色结晶,93%收率)。
[2266]c37h38
n4o6s2的hrms计算值:698.2233;[m+h]
+
,实测值:699.229(δ=-2.2ppm)。
[2267]
步骤9:实施例67的制备
[2268]
采用通用方法12,用[4,38-二甲基-34,34-二氧代-28,33-二氧杂-20,34λ
6-二硫杂-1,14,15,16-四氮杂七环[27.5.3.1
3,7
.1
9,13
.0
12,16
.0
21,26
.0
32,36
]三十九碳-3(39),4,6,9(38),10,12,14,21,23,25,29,31,36-十三烯-8-基]乙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体,22%收率)。
[2269]
通过手性柱色谱分离得到对映体纯产物。
[2270]
实施例67a(e1)
[2271]c35h34
n4o6s2的hrms计算值:670.1920;[m+h]
+
,实测值:671.1992(δ=-0.1ppm)。实施例67b(e2)
[2272]c35h34
n4o6s2的hrms计算值:670.1920;[m+h]
+
,实测值:671.1992(δ=-0.1ppm)。
[2273]1h-nmr(500mhz,dmso-d6)δppm:12.12(br.,1h),7.61(dd,1h),7.57(dd,1h),7.54(d,1h),7.46(d,1h),7.41(td,1h),7.36(dd,1h),7.33(td,1h),7.18(d,1h),7.15(m,1h),7.15(m,1h),7.15(d,1h),6.77(brs.,1h),5.26/5.14(d+d,2h),4.81(t,1h),4.64(m,2h),4.34/4.17(d+d,2h),4.25/4.11(d+d,2h),3.04(m,2h),3.01(m,2h),2.75(s,3h),2.29(s,3h),2.24/2.14(m+m,2h)。
[2274]
13
c-nmr(125mhz,dmso-d6)δppm:173.2,131.3,131.2,130.2,130,129.7,129.2,127.3,127.1,119.6,116.4,113.4,107.8,68.9,51.8,49.2,45.8,41.3,40.8,30.6,28.6,18.4,13.3。
[2275]
实施例68:[(2r)-2,4,31-三甲基-27,27-二氧代-27λ
6-螺[21,26-二氧杂-27-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-18,4'-氧杂环己烷]-8-基]乙酸
[2276][2277]
步骤a1:4-[2-(苄氧基)乙基]氧杂环己烷-4-甲腈的制备
[2278]
于-78℃向氧杂环己烷-4-甲腈(1eq.,10g,90mmol)的无水thf(20ml/g,200ml)溶液中滴加二(三甲基硅基)氨化锂(1.2eq.,1m的thf溶液,108ml,108mmol),同时继续搅拌并将混合物在该温度下继续搅拌2小时。于-78℃滴加溶于100ml thf的[(2-碘乙氧基)甲基]苯(1eq.,23.58g,90mmol)。将反应混合物升温至室温并在室温下继续搅拌一个周末。反应完成后将混合物用100ml水淬灭。加入500ml etoac并分层。将有机层进一步用300ml盐水洗
涤,用无水硫酸钠干燥,过滤并浓缩至干得到粗产物,将其通过正相硅胶色谱纯化,用庚烷-etoac(0至60:40)作为洗脱剂得到标题化合物(12.3g,56%收率)。
[2279]1h-nmr(400mhz,dmso-d6)δppm:7.3(m,5h),4.49(s,2h),3.84/3.49(m,4h),3.62(t,2h),1.9(t,2h),1.83/1.6(2m,4h)。
[2280]
步骤a2:1-{4-[2-(苄氧基)乙基]氧杂环己烷-4-基}甲胺的制备
[2281]
将氢化铝锂(1.5eq.,2.85g,75mmol)置于圆底烧瓶中。加入无水thf(10ml/g,123ml)后将混合物冷却至10℃。于10℃在20分钟内滴加4-[2-(苄氧基)乙基]氧杂环己烷-4-甲腈(1eq.,12.3g,50mmol)的无水thf溶液(10ml/g,123ml),同时继续搅拌。将反应混合物升温至室温并继续搅拌5小时。反应完成后将混合物冷却至0℃,用naoh水溶液淬灭,然后用na2so4水溶液淬灭。室温搅拌过夜后,将混合物过滤,用etoac洗涤并将母液浓缩至干得到标题化合物(12.1g,90%收率)。
[2282]1h-nmr(400mhz,dmso-d6)δppm:7.37-7.23(m,4h),4.44(s,2h),3.57-3.49(m,4h),3.48(t,2h),2.48(s,2h),1.66(t,2h),1.41-1.26(m,4h)。
[2283]
步骤a3:n-({4-[2-(苄氧基)乙基]氧杂环己烷-4-基}甲基)-3-甲基-2-硝基苯胺的制备
[2284]
采用通用方法2步骤1,用1-{4-[2-(苄氧基)乙基]氧杂环己烷-4-基}甲胺(1当量)作为起始试剂,得到标题化合物(橙色油,52%收率)。
[2285]1h-nmr(400mhz,dmso-d6)δppm:7.38-7.24(m,5h),7.27(m,1h),6.82(d,1h),6.59(d,1h),6.46(t,1h),4.42(s,2h),3.57(t,2h),3.52-3.47(m,4h),3.33(dt,2h),2.31(s,3h),1.79(quint,2h)。
[2286]
步骤a4:n-({4-[2-(苄氧基)乙基]氧杂环己烷-4-基}甲基)-4-溴-3-甲基-2-硝基苯胺的制备
[2287]
采用通用方法2步骤2,用n-({4-[2-(苄氧基)乙基]氧杂环己烷-4-基}甲基)-3-甲基-2-硝基苯胺(1当量)作为起始试剂,得到标题化合物(78%收率)。
[2288]1h-nmr(400mhz,dmso-d6)δppm:7.49(d,1h),7.35-7.22(m,5h),6.91(d,1h),5.99(t,1h),4.43(s,2h),3.62-3.5(m,4h),3.51(t,2h),3.19(g,2h),2.28(s,3h),2.28(t,2h),1.45/1.33(m,4h)。
[2289]
步骤a5:n
1-({4-[2-(苄氧基)乙基]氧杂环己烷-4-基}甲基)-4-溴-3-甲基苯-1,2-二胺的制备
[2290]
采用通用方法2步骤3,用n-({4-[2-(苄氧基)乙基]氧杂环己烷-4-基}甲基)-4-溴-3-甲基-2-硝基苯胺(1当量)作为起始试剂,得到标题化合物(97%收率)。
[2291]1h-nmr(400mhz,dmso-d6)δppm:7.29(m,5h),6.7(d,1h),6.35(d,1h),4.7(m,2h),4.4(s,2h),4.1(m,1h),3.6(m,4h),3.5(t,2h),2.99(s,2h),2.2(s,3h),1.87(t,2h),1.6-1.4(m,4h)。
[2292]
步骤a6:1-({4-[2-(苄氧基)乙基]氧杂环己烷-4-基}甲基)-5-溴-4-甲基-1h-苯并三唑的制备
[2293]
采用通用方法2步骤4,用n
1-({4-[2-(苄氧基)乙基]氧杂环己烷-4-基}甲基)-4-溴-3-甲基苯-1,2-二胺(1当量)作为起始试剂,得到标题化合物(棕色固体,80%收率)。
[2294]1h-nmr(400mhz,dmso-d6)δppm:7.69(m,2h),7.4-7.3(m,5h),4.7(s,2h),4.48(s,
6.76(m,3h)6.85-6.96(m,4h)7.14(s,2h)7.19(d,j=7.82hz,2h)7.31(d,j=7.95hz,1h)7.39-7.50(m,2h)7.73(d,j=8.80hz,1h)7.78(d,j=8.68hz,1h)7.85-7.93(m,1h)12.28(br.s.,1h)。
[2317]
实施例69:[4,31-二甲基-19,27,27-三氧代-26-氧杂-27λ
6-硫杂-1,14,15,16,20-五氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸
[2318][2319]
步骤a1:3-{5-[(1e)-3-乙氧基-3-氧代丙-1-烯-1-基]-4-甲基-1h-苯并三唑-1-基}丙酸的制备
[2320]
将(2e)-3-[1-(3-羟基丙基)-4-甲基-1h-苯并三唑-5-基]丙-2-烯酸乙酯(1eq.,2g,6.91mmol)溶于mecn(10ml)和水(10ml),然后加入3-碘-1,2-亚苯基二乙酸酯(2.2eq.,4.90g,15.2mmol)和(2,2,6,6-四甲基哌啶-1-基)oxidanyl(0.2eq.,0.216g,1.38mmol)并将混合物在室温下搅拌1小时。反应完成后将混合物用na2s2o3水溶液和na2co3水溶液(25-25ml)淬灭,然后用etoac洗涤。分层并将水相的ph用柠檬酸调节至3-4。将混合物用etoac萃取,分层,将有机层用硫酸镁干燥,过滤并减压浓缩。将固体残余物用水处理,滤出沉淀并干燥得到标题化合物(1.731g,83%收率)。
[2321]1h-nmr(400mhz,dmso-d6)δppm:12.6(m,1h),8(d,1h),7.95(d,1h),7.7(d,1h),6.65(d,1h),4.9(t,2h),4.2(q,2h),3(t,2h),2.8(sl,3h),1.3(t,3h)。
[2322]
步骤a2:(2e)-3-{1-[3-(苄氧基)-3-氧代丙基]-4-甲基-1h-苯并三唑-5-基}丙-2-烯酸乙酯的制备
[2323]
在氩气下将3-{5-[(1e)-3-乙氧基-3-氧代丙-1-烯-1-基]-4-甲基-1h-苯并三唑-1-基}丙酸(1eq.,1.724g,5.684mmol)溶于dcm(70ml),然后将dmf(0.2eq.,0.09ml,1.1mmol)加入到该溶液中。将混合物冷却至0℃,然后加入草酰氯(9eq.,6.49g,4.33ml,51.1mmol)。将反应混合物于0℃搅拌15分钟,然后在室温下继续搅拌1小时。将反应混合物浓缩并将残余物悬浮于dcm(15ml)。在氩气氛下,将苯甲醇(1.2eq.,0.74g,0.71ml,6.82mmol)溶于dcm(20ml)。滴加酰氯的dcm悬浮液并将反应混合物室温搅拌过夜。将混合物用水洗涤,然后用盐水洗涤。分离出有机相并用硫酸镁干燥,过滤并减压浓缩。将残余物通过正相硅胶色谱纯化,用庚烷-etoac作为洗脱剂得到标题化合物(1.607g,72%收率)。
[2324]1h-nmr(400mhz,dmso-d6)δppm:8.05(d,1h),7.95(d,1h),7.7(d,1h),7.25(2m,5h),6.65(d,1h),5(s,2h),4.9(t,2h),4.2(q,2h),3.2(t,2h),2.8(s,3h),1.3(t,3h)
[2325]
步骤1:3-{1-[3-(苄氧基)-3-氧代丙基]-4-甲基-1h-苯并三唑-5-基}-3-[3-(羟基甲基)-4-甲基苯基]丙酸乙酯的制备
[2326]
采用通用方法6,用(2e)-3-{1-[3-(苄氧基)-3-氧代丙基]-4-甲基-1h-苯并三唑-5-基}丙-2-烯酸乙酯(1eq.,0.859g,2.18mmol)和[2-甲基-5-(4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷-2-基)苯基]甲醇(1.1eq.,0.596g,2.40mmol)作为起始试剂,得到标题化合物(0.729g,62%收率)。
[2327]1h-nmr(400mhz,dmso-d6)δppm:7.6(d,1h),7.5(d,1h),7.3/7.2(m,5h),7.3(d,1h),7.1(dd,1h),7(d,1h),5.05(s,2h),5(t,1h),4.85(t,3h),4.4(d,2h),3.9(q,2h),3.1(m,4h),2.8(s,3h),2.2(s,3h),1(t,3h)。
[2328]
步骤c1:6-氰基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-甲酸叔丁酯的制备
[2329]
将6-溴-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮(1eq.,5.95g,22.5mmol)溶于dcm(225ml),然后加入tea(1.1eq.,2.51g,3.45ml,24.8mmol)、n,n-二甲基吡啶-4-胺(0.1eq.,275mg,2.25mmol)和二碳酸二叔丁酯(1.1eq.,5.41g,24.8mmol)。将反应混合物室温搅拌2小时。将混合物倒入500ml 0.1m hcl溶液中。将有机相分离,用500ml 0.1m hcl溶液洗涤(2x),用硫酸镁干燥,过滤并浓缩得到6-溴-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-甲酸叔丁酯(定量)。将粗产物(1eq.,5g,13.73mmol)溶于n,n-二甲基乙酰胺(80ml),然后加入锌(0.5eq.,449mg,6.86mmol)和氰化锌(1eq.,1.612g,13.73mmol)。将混合物用氩气脱气,然后加入二(三-叔丁基膦)钯(0)催化剂(0.1eq.,424mg,1.73mmol)。将反应混合物于80℃搅拌4小时。将混合物过滤,将过滤的固体用etoac洗涤,将滤液高真空浓缩。将残余物溶于etoac,然后用盐水洗涤。将有机相用硫酸镁干燥,过滤并减压浓缩得到粗产物,将其通过正相硅胶色谱纯化,用庚烷-etoac作为洗脱剂得到标题化合物(2.704g,63%收率)。
[2330]1h-nmr(400mhz,dmso-d6)δppm:8.15(d,1h),8(dd,1h),7.6(d,1h),5.2(s,2h),1.5(s,9h)。
[2331]
步骤c2:[(2,2-二氧代-3,4-二氢-2h-1,2λ6,3-噁噻嗪-6-基)甲基]氨基甲酸苄酯的制备
[2332]
将6-氰基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-甲酸叔丁酯(1eq.,1g,3.22mmol)溶于7mnh3的meoh(10ml)溶液并加入阮内镍催化剂(5eq.,945mg,16.11mmol)。将反应混合物在常压下氢化4小时。反应完成后将混合物过滤,将滤液浓缩得到粗产物6-(氨基甲基)-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮(66%收率),将其溶于thf(2.5ml)。加入nahco3(1.1当量),然后滴加氯甲酸苄酯(1.1当量)并将混合物在室温下搅拌2小时。将混合物用水和etoac稀释,将分离出的有机相用盐水洗涤,用硫酸镁干燥,过滤,浓缩得到粗产物,将其通过正相硅胶色谱纯化,用庚烷-etoac作为洗脱剂得到标题化合物(46%收率)。
[2333]1h-nmr(400mhz,dmso-d6)δppm:8.5(m,1h),7.8(t,1h),7.35(m,5h),7.2(dd,1h),7.15(d,1h),7(d,1h),5.05(s,2h),4.5(s,2h),4.2(d,2h)。
[2334]
步骤2:3-(3-{[6-({[(苄氧基)羰基]氨基}甲基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-甲基苯基)-3-{1-[3-(苄氧基)-3-氧代丙基]-4-甲基-1h-苯并三唑-5-基}丙酸乙酯的制备
[2335]
采用通用方法7,用[(2,2-二氧代-3,4-二氢-2h-1,2λ6,3-噁噻嗪-6-基)甲基]氨基甲酸苄基酯(1eq.,571mg,1.64mmol)和3-{1-[3-(苄氧基)-3-氧代丙基]-4-甲基-1h-苯并三唑-5-基}-3-[3-(羟基甲基)-4-甲基苯基]丙酸乙酯(1.1eq.,930mg,1.80mmol)作为起始试剂,得到标题化合物(1.017g,73%收率)。
[2336]1h-nmr(400mhz,dmso-d6)δppm:7.85(t,1h),7.6(d,1h),7.5(d,1h),7.4-7.1(m,16h),5.05/5(2s,4h),4.9(t,2h),4.85(m,1h),4.5(2d,2h),4.2(m,4h),3.9(q,2h),3.2(d,2h),3.1(t,1h),2.8(s,3h),2.2(s,3h),1(t,3h)。
[2337]
步骤3:3-{5-[1-(3-{[6-(氨基甲基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-甲基苯基)-3-乙氧基-3-氧代丙基]-4-甲基-1h-苯并三唑-1-基}丙酸的制备
[2338]
采用通用方法8,用3-(3-{[6-({[(苄氧基)羰基]氨基}甲基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-甲基苯基)-3-{1-[3-(苄氧基)-3-氧代丙基]-4-甲基-1h-苯并三唑-5-基}丙酸乙酯(1eq.,1.01g,1.19mmol)作为起始试剂,得到标题化合物(844mg,97%收率)。
[2339]1h-nmr(400mhz,dmso-d6)δppm:7.8(d,1h),7.5(d,1h),7.4(dd,1h),7.3(dd,1h),7.2(m,4h),4.8(m,3h),4.3/4.15(2d,2h),4.25(m,2h),4/3.8(2d,2h),3.95(q,2h),3.2(d,2h),2.8/2.65(s+2m,5h),2.2(sl,3h),1(t,3h)。
[2340]
步骤4:实施例69的制备
[2341]
将3-{5-[1-(3-{[6-(氨基甲基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-甲基苯基)-3-乙氧基-3-氧代丙基]-4-甲基-1h-苯并三唑-1-基}丙酸(1eq.,830mg,1.13mmol)溶于dcm(340ml),然后加入tea(5eq.,574mg,0.791ml,5.67mmol)、1h-苯并三唑-1-醇(1.5eq.,256mg,1.7mmol)和3-{[(乙基亚氨基)亚甲基]氨基}-n,n-二甲基丙-1-胺盐酸盐(1.5eq.,326mg,1.7mmol)。将反应混合物室温搅拌过夜。将混合物浓缩至50ml并用饱和nahco3水溶液和盐水洗涤。将水相用dcm萃取。将合并的有机相用10%柠檬酸水溶液洗涤,用水洗涤,然后用盐水洗涤。将有机层用硫酸镁干燥,过滤,浓缩得到粗产物[4,31-二甲基-19,27,27-三氧代-26-氧杂-27λ
6-硫杂-1,14,15,16,20-五氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸乙酯(53%收率),将其用通用方法12进行反应得到外消旋混合物形式的标题化合物(45mg,13%)。
[2342]c29h29
n5o6s的hrms计算值:575.1838;[m+h]
+
,实测值:576.1913(δ=0.3ppm)。
[2343]1h-nmr(400mhz,dmso-d6)δppm:12.1(m,1h),8.35(m,1h),7.65/7.6(d,2h),7.45(dd,1h),7.25(d+dd,2h),7.1(d,1h),6.75(d,1h),6.3(d,1h),5.05/4.95(m,2h),4.8(t,1h),4.7/4dd,2h),4.3/3.9(2d,2h),4.1/3.7(d,2h),3/2.8(m,2h),3(m,2h),2.6(s,3h),2.3(sl,3h)。
[2344]
实施例70:[4,36-二甲基-32,32-二氧代-26,31-二氧杂-32λ
6-硫杂-1,14,15,16,19-五氮杂七环[25.5.3.1
3,7
.1
9,13
.0
12,16
.0
20,25
.0
30,34
]三十七碳-3(37),4,6,9(36),10,12,14,20,22,24,27,29,34-十三烯-8-基]乙酸
[2345]
[2346]
步骤c1:1-(4-甲氧基苯氧基)-2-硝基苯的制备
[2347]
将4-甲氧基苯酚(1eq.,6.207g,50mmol)和1-氟-2-硝基苯(1eq.,7.055g,0.05mol)溶于二氧杂环己烷(50ml)并将k2co3(2eq.,13.821g,0.1mol)加入到该溶液中。将混合物于100℃搅拌23小时。反应完成后将混合物冷却至室温并滤出有机盐。将滤液减压浓缩并将残余物通过用庚烷研制进行纯化得到标题化合物(黄色结晶,11.96g,98%收率)。
[2348]1h-nmr(500mhz,dmso-d6)δppm:8.02(dd,1h),7.63(t,1h),7.29(t,1h),7.07(m,2h),7.00(m,3h),3.76(s,3h)。
[2349]
步骤c2:4-(2-硝基苯氧基)苯酚的制备
[2350]
于0℃将1-(4-甲氧基苯氧基)-2-硝基苯(1eq.,11.96g,0.04878mol)溶于dcm(300ml,4.680mol)。滴加三溴硼烷(1.2eq.,14.66g,0.05853mol)的20ml dcm溶液。将反应混合物在室温下搅拌过夜。将混合物倒入水(100ml)中。将有机层用盐水洗涤,用硫酸镁干燥,过滤并减压浓缩。将残余物用etoac稀释并通过正相硅胶色谱纯化,用庚烷-etoac(100:0至66:33)作为洗脱剂得到标题化合物(11.11g,黄色结晶,98%收率)。
[2351]1h-nmr(500mhz,dmso-d6)δppm:9.52(s,1h),7.99(dd,1h),7.61(m,1h),7.24(t,1h),6.96(m,3h),6.82(m,2h)。
[2352]
步骤c3:2-羟基-5-(2-硝基苯氧基)苯甲醛的制备
[2353]
将4-(2-硝基苯氧基)苯酚(1eq.,11.11g,0.04805mol)溶于1,2-二氯乙烷(150ml),然后加入二氯化镁(5eq.,22.88g,0.2403mol)和tea(6eq.,29.18g,0.2883mol,40.19ml)。加入多聚甲醛(10eq.,14.42g,0.4805mol)并将混合物于40℃搅拌1小时,然后于70℃搅拌12小时。将冷却的混合物用dcm(300ml)稀释并用3x50ml 1m hcl水溶液洗涤。将有机层用硫酸镁干燥,过滤并蒸发得到棕色结晶状标题化合物(11.89g,95%收率)。
[2354]1h-nmr(500mhz,dmso-d6)δppm:10.8(br.,1h),10.24(s,1h),8.04(dd,1h),7.66(ddd,1h),7.36(dd,1h),7.33(td,1h),7.27(d,1h),7.09(d,1h),7.09(dd,1h)。
[2355]
步骤c4:6-(2-硝基苯氧基)-2h-1,2λ6,3-噁噻嗪-2,2-二酮的制备
[2356]
将氯磺酰异氰酸酯(4eq.,25.20g,15.50ml,0.1781mol)冷却至0℃并于0℃下在30分钟内滴加hcooh(4eq.,8.196g,6.72ml,0.1781mol)。形成白色沉淀。将反应混合物在30分钟内升温至室温并在室温下搅拌1小时。将混合物再次冷却至0℃并滴加2-羟基-5-(2-硝基苯氧基)苯甲醛(1eq.,11.54g,0.04452mol)的nmp(75ml)溶液。将混合物在室温下搅拌过夜。小心地倒入100ml浓nh4cl溶液中,形成橙色沉淀,过滤并真空干燥后得到橙色结晶状标题化合物(6.71g,47%收率)。
[2357]1h-nmr(500mhz,dmso-d6)δppm:9.15(s,1h),8.15(dd,1h),7.78(td,1h),7.71(d,1h),7.69(dd,1h),7.63(d,1h),7.48(td,1h),7.36(dd,1h)。
[2358]
步骤c5:6-(2-硝基苯氧基)-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮的制备
[2359]
将6-(2-硝基苯氧基)-2h-1,2λ6,3-噁噻嗪-2,2-二酮(1eq.,7.65g,23.9mmol)溶于etoh(250ml)并于0℃下将氰基硼氢化钠(1.2eq.,1.8g,28.7mmol)分批加入到该溶液中。将混合物在室温下搅拌30分钟。将溶剂蒸发至干。将黄色油在etoac和水之间进行分配。分离出有机层并将水相用etoac萃取(2x30ml)。将合并的有机相用硫酸镁干燥,过滤并浓缩。将残余物通过正相快速硅胶柱色谱纯化,用庚烷-etoac(100:0至50:50)作为洗脱剂得到黄色油状标题化合物(1.25g,16%收率)。
[2360]1h-nmr(500mhz,dmso-d6)δppm:8.54(t,1h),8.08(dm,1h),7.71(m,1h),7.39(m,1h),7.18(dm,1h),7.16(d,1h),7.09(dd,1h),7.07(d,1h),4.55(d,2h)。
[2361]
步骤a1:(2e)-3-(4-甲基-1-{2-[(氧杂环己烷-2-基)氧基]乙基}-1h-苯并三唑-5-基)丙-2-烯酸乙酯的制备
[2362]
于0℃下向6-(2-硝基苯氧基)-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮(1eq.,1.38g,5mmol)的dcm(25ml)溶液中加入4-甲基苯-1-磺酸一水合物(0.01eq.,9.5mg,0.05mmol),然后加入3,4-二氢-2h-吡喃(1.1当量,0.463g,5.5mmol)。将反应混合物升温至室温并搅拌1小时。将混合物用饱和nahco3(30ml)淬灭并分相。将水相用dcm(30ml)萃取,将合并的有机相用硫酸镁干燥,过滤并减压蒸发得到标题化合物(1.7g,95%收率)。
[2363]1h-nmr(500mhz,dmso-d6)δppm:8.01(d,1h),7.96(d,1h),7.72(d,1h),6.64(d,1h),4.93/4.88(m+m,2h),4.53(dd,1h),4.21(q,2h),4.05/3.84(m+m,2h),3.36/3.29(m+m,2h),2.8(s,3h),1.58-1.19(m,6h),1.27(t,3h)。
[2364]
步骤1:3-[3-(羟基甲基)-4-甲基苯基]-3-(4-甲基-1-{2-[(氧杂环己烷-2-基)氧基]乙基}-1h-苯并三唑-5-基)丙酸的制备
[2365]
将(2e)-3-(4-甲基-1-{2-[(氧杂环己烷-2-基)氧基]乙基}-1h-苯并三唑-5-基)丙-2-烯酸乙酯(1eq.,4.85g,13.5mmol)的二氧杂环己烷(80ml)和水(40ml)悬浮液用n2脱气,然后加入[2-甲基-5-(4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷-2-基)苯基]甲醇(1.4eq.,4.69g,18.9mmol)和tea(1.6eq.,2.18g,21.6mmol)。加入氯(1,5-环辛二烯)铑(i)二聚体催化剂(0.05eq.,0.333g,0.675mmol)并将反应混合物于80℃加热30分钟,然后室温加热过夜。将反应混合物用水和etoac稀释,将有机相分离,用硫酸镁干燥,过滤并浓缩至干得到粗产物,将其通过正相硅胶色谱纯化,用庚烷-etoac(50:50)作为洗脱剂得到标题化合物(深色油,5.11g,79%收率)。1h-nmr(500mhz,dmso-d6)δppm:7.62(d,1h),7.47(d,1h),7.25(brs.,1h),7.09/7.07(dd/dd,1h),7.02/7.01(d/d,1h),4.99/4.98(t/t,1h),4.9-4.78(m,2h),4.83(m,1h),4.51(dm,1h),4.4(d,2h),4.01/3.82(m+m,2h),3.92(q,2h),3.33-3.2(m,2h),3.13(d,2h),2.74(s,3h),2.15(s,3h),1.54-1.18(m,6h),1(t,3h)。
[2366]
步骤2:3-(4-甲基-3-{[6-(2-硝基苯氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}苯基)-3-(4-甲基-1-{2-[(氧杂环己烷-2-基)氧基]乙基}-1h-苯并三唑-5-基)丙酸乙酯的制备
[2367]
将3-[3-(羟基甲基)-4-甲基苯基]-3-(4-甲基-1-{2-[(氧杂环己烷-2-基)氧基]乙基}-1h-苯并三唑-5-基)丙酸(1eq.,3.277g,6.804mmol)溶于thf(30ml)。向该溶液中加入溶于thf(10ml)的6-(2-硝基苯氧基)-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮(1.39eq.,3.04g,9.43mmol)和pph3(2eq.,3.570g,13.61mmol)。将混合物冷却至~5℃,滴加diad(2eq.,2.897g,2.821ml,13.61mmol)并将混合物于45℃加热1小时。将反应混合物浓缩至干得到粗产物,将其通过正相硅胶色谱纯化,用dcm-meoh(99:1)作为洗脱剂得到标题化合物(橙色固体,5.3g,99%收率)。
[2368]1h-nmr(500mhz,dmso-d6)δppm:8.09(dd,1h),7.72(td,1h),7.58(d,1h),7.48(d,1h),7.38(t,1h),7.27(dd,1h),7.25(m,1h),7.24(dm,1h),7.17(d,1h),7.16(m,1h),7.12(d,1h),7.11(m,1h),4.82(m,1h),4.82(m,2h),4.48(m,2h),4.48(m,1h),4.26/4.23(d+d,2h),3.99/3.8(m+m,2h),3.89(q,2h),3.23(m,2h),3.15(d,2h),2.73/2.72(s/s,3h),2.22
(s,3h),1.5-1.13(m,6h),0.97(t,3h)。
[2369]
步骤3:3-[1-(2-羟基乙基)-4-甲基-1h-苯并三唑-5-基]-3-(4-甲基-3-{[6-(2-硝基苯氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}苯基)丙酸乙酯的制备
[2370]
将3-(4-甲基-3-{[6-(2-硝基苯氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}苯基)-3-(4-甲基-1-{2-[(氧杂环己烷-2-基)氧基]乙基}-1h-苯并三唑-5-基)丙酸乙酯(1eq.,3.091g,3.933mmol)溶于thf(16ml)和etoh(2ml)。加入水合磷钨酸(0.1eq.,0.1368g,0.3933mmol)并将反应混合物室温搅拌24小时。反应完成后将混合物浓缩至干。将粗固体产物在etoac和水之间进行分配。将分离出的有机层用碳酸氢钠溶液洗涤两次,用硫酸镁干燥,过滤并蒸发至干得到标题化合物(棕色固体,2.8g,定量)。
[2371]1h-nmr(500mhz,dmso-d6)δppm:8.09(dd,1h),7.71(td,1h),7.53(d,1h),7.45(d,1h),7.38(td,1h),7.27(d,1h),7.27(d,1h),7.24(dd,1h),7.18(dd,1h),7.17(dd,1h),7.12(d,1h),7.12(d,1h),4.94(t,1h),4.83(t,1h),4.64(t,2h),4.48(s,2h),4.26(s,2h),3.91(q,2h),3.81(q,2h),3.15(m,2h),2.74(s,3h),2.22(s,3h),1(t,3h)。
[2372]
步骤4:3-[1-(2-氯乙基)-4-甲基-1h-苯并三唑-5-基]-3-(4-甲基-3-{[6-(2-硝基苯氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}苯基)丙酸乙酯的制备
[2373]
将3-[1-(2-羟基乙基)-4-甲基-1h-苯并三唑-5-基]-3-(4-甲基-3-{[6-(2-硝基苯氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}苯基)丙酸乙酯(1eq.,2.8g,4.0mmol)溶于dcm(30ml)。在室温下缓慢加入亚硫酰氯(3eq.,1.4g,12mmol)。将反应混合物于45℃加热1.5小时。反应完成后将混合物浓缩至干。将粗产物在etoac和水之间进行分配,将有机相用饱和碳酸氢钠溶液洗涤两次,用硫酸镁干燥,过滤并蒸发至干得到标题化合物(2.9g,棕色固体,97%收率)。
[2374]1h-nmr(500mhz,dmso-d6)δppm:8.09(dm,1h),7.71(m,1h),7.62(d,1h),7.5(d,1h),7.38(m,1h),7.28(d,1h),7.27(d,1h),7.24(dm,1h),7.19(dd,1h),7.18(dd,1h),7.13(d,1h),7.11(d,1h),4.99(t,2h),4.83(t,1h),4.48(s,2h),4.26(s,2h),4.12(t,2h),3.9(q,2h),3.16(d,2h),2.76(s,3h),2.23(s,3h),0.97(t,3h)。
[2375]
步骤5:3-(3-{[6-(2-氨基苯氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-甲基苯基)-3-[1-(2-氯乙基)-4-甲基-1h-苯并三唑-5-基]丙酸乙酯的制备
[2376]
将3-[1-(2-氯乙基)-4-甲基-1h-苯并三唑-5-基]-3-(4-甲基-3-{[6-(2-硝基苯氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}苯基)丙酸乙酯(1eq.,2.78g,3.86mmol)、铁粉(10eq.,2160mg,38.6mmol)和nh4cl(0.5eq.,103mg,1.93mmol)溶于etoh(10ml)和水(3ml)的混合物于80℃加热1.5小时。冷却至室温后,将混合物过滤并减压浓缩。将残余物溶于etoac,用饱和na2co3水溶液洗涤,用硫酸镁干燥,过滤,减压蒸发并真空干燥过夜得到标题化合物(2.314g,棕色固体,87%收率)。
[2377]1h-nmr(500mhz,dmso-d6)δppm:7.63(d,1h),7.52(d,1h),7.25(d,1h),7.18(dd,1h),7.16(d,1h),7.12(d,1h),6.93(m,1h),6.92(dd,1h),6.85(d,1h),6.84(dm,1h),6.81(dm,1h),6.56(m,1h),5(t,2h),4.97(s,2h),4.83(t,1h),4.45(s,2h),4.23(s,2h),4.13(t,2h),3.91(q,2h),3.16(d,2h),2.76(s,3h),2.22(s,3h),0.99(t,3h)。
[2378]
步骤6:[4,36-二甲基-32,32-二氧代-26,31-二氧杂-32λ
6-硫杂-1,14,15,16,19-五氮杂七环[25.5.3.1
3,7
.1
9,13
.0
12,16
.0
20,25
.0
30,34
]三十七碳-3(37),4,6,9(36),10,12,14,
20,22,24,27,29,34-十三烯-8-基]乙酸乙酯的制备
[2379]
在室温下将3-(3-{[6-(2-氨基苯氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-甲基苯基)-3-[1-(2-氯乙基)-4-甲基-1h-苯并三唑-5-基]丙酸乙酯(1eq.,1.12g,1.62mmol)溶于丙腈(50ml)并加入碘化钠(5eq.,1.22g,8.11mmol)。将反应混合物于100℃加热35小时。将混合物浓缩至干,然后在水和etoac之间进行分配。分离出有机相并用硫酸镁干燥,过滤并浓缩至干得到粗产物,将其通过制备型反相色谱纯化,用水tfa溶液-mecn作为洗脱剂得到标题化合物(360mg,黄色粉末,34%收率)。
[2380]
通过手性柱色谱分离得到对映体纯的最终中间体。
[2381]1h-nmr(500mhz,dmso-d6)δppm:7.39(d,1h),7.37(dd,1h),7.34(d,1h),7.21(d,1h),7.16(d,1h),7.06(dd,1h),7(t,1h),6.9(d,1h),6.86(d,1h),6.69(d,1h),6.56(t,1h),6.37(d,1h),5.47(dd,1h),4.95/4.83(dt+dt,2h),4.8(t,1h),4.27/4.1(d+d,2h),4.21/4.15(d+d,2h),3.87(q,2h),3.79/3.68(m+m,2h),3.08/2.99(dd+dd,2h),2.7(s,3h),2.3(s,3h),0.95(t,3h)。
[2382]
步骤7:实施例70的制备
[2383]
采用通用方法12,用[4,36-二甲基-32,32-二氧代-26,31-二氧杂-32λ
6-硫杂-1,14,15,16,19-五氮杂七环[25.5.3.1
3,7
.1
9,13
.0
12,16
.0
20,25
.0
30,34
]三十七碳-3(37),4,6,9(36),10,12,14,20,22,24,27,29,34-十三烯-8-基]乙酸乙酯e1(1当量)或e2(1当量)作为起始试剂,得到标题化合物(收率分别为58%-92%)。
[2384]
实施例70a(e1)
[2385]c33h31
n5o6s的hrms计算值:625.1995;[m+h]
+
,实测值:626.2062(δ=-0.9ppm)。
[2386]
实施例70b(e2)
[2387]c33h31
n5o6s的hrms计算值:625.1995;[m+h]
+
,实测值:626.2062(δ=-0.9ppm)。
[2388]1h-nmr(500mhz,dmso-d6)δppm:12.07(brs,1h),7.38(dd,1h),7.38(d,1h),7.32(d,1h),7.21(d,1h),7.16(d,1h),7.06(dd,1h),7(t,1h),6.9(d,1h),6.84(d,1h),6.69(d,1h),6.56(t,1h),6.37(d,1h),5.47(brs,1h),4.95/4.82(t+d,2h),4.77(t,1h),4.27/4.09(d+d,2h),4.2/4.14(d+d,2h),3.79/3.68(t+d,2h),2.99/2.87(dd+dd,2h),2.7(s,3h),2.3(s,3h)。
[2389]
13
c-nmr(125mhz,dmso-d6)δppm:173.1,155,146.3,146.2,143.8,141.6,140.2,136.4,136.1,133.1,132.1,131.4,130.2,129,127.2,127.1,125.4,120.1,119.7,119.3,118.6,117,116.1,111.8,108.1,51.9,48.8,47.6,44.3,41.2,41.2,18.6,13.3。
[2390]
实施例71:[4,37-二甲基-33,33-二氧代-27,32-二氧杂-33λ
6-硫杂-1,14,15,16,20-五氮杂七环[26.5.3.1
3,7
.1
9,13
.0
12,16
.0
21,26
.0
31,35
]三十八碳-3(38),4,6,9(37),10,12,14,21,23,25,28,30,35-十三烯-8-基]乙酸
[2391][2392]
步骤1:3-[4-甲基-3-[[6-(2-硝基苯氧基)-2,2-二氧代-4h-1,2λ6,3-噁噻嗪-3-基]甲基]苯基]-3-[4-甲基-1-(3-四氢吡喃-2-基氧基丙基)苯并三唑-5-基]丙酸乙酯的制备
[2393]
将3-[3-(羟基甲基)-4-甲基苯基]-3-(4-甲基-1-{3-[(氧杂环己烷-2-基)氧基]丙基}-1h-苯并三唑-5-基)丙酸乙酯(1eq.,1890mg,3.81mmol)溶于thf(25ml),然后加入6-(2-硝基苯氧基)-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮(1.5eq.,1.8g,5.58mmol)和pph3(3.2eq.,3.2g,12.2mmol)。将混合物在惰性气氛(n2)下冷却至5℃并滴加diad(3.11eq.,2.4g,11.9mmol)。将反应混合物室温搅拌2小时。反应完成后将溶剂减压蒸发,将粗产物通过正相快速硅胶色谱纯化,用庚烷-etoac(50:50)作为洗脱剂,得到黄色固体状标题化合物(2.04g,67%收率)。
[2394]1h-nmr(500mhz,dmso-d6)δppm:8.09(dd,1h),7.71(td,1h),7.54(d,1h),7.48(d,1h),7.42(m,1h),7.38(td,1h),7.27(d,1h),7.25(d,1h),7.24(dd,1h),7.18(dd,1h),7.18(dd,1h),7.12(d,1h),7.1(d,1h),4.83(t,1h),4.68(t,2h),4.47(s,2h),4.25(s,2h),3.9(q,2h),3.6/3.31(m+m,2h),3.57/3.24(m+m,2h),3.15(d,2h),2.74(s,3h),2.23(s,3h),2.11(m,2h),1.67-1.29(m,6h),0.98(t,3h)。
[2395]
步骤2:3-[1-(3-羟基丙基)-4-甲基-1h-苯并三唑-5-基]-3-(4-甲基-3-{[6-(2-硝基苯氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}苯基)丙酸乙酯的制备
[2396]
将3-[4-甲基-3-[[6-(2-硝基苯氧基)-2,2-二氧代-4h-1,2λ6,3-噁噻嗪-3-基]甲基]苯基]-3-[4-甲基-1-(3-四氢吡喃-2-基氧基丙基)苯并三唑-5-基]丙酸乙酯(1eq.,2.03g,2.54mmol)溶于etoh(40ml)和thf(25ml),然后将吡啶对甲苯磺酸盐(0.1eq.,64mg,0.127mmol)加入到该溶液中。将反应混合物于55℃搅拌过夜。反应完成后蒸发溶剂,将混合物用dcm稀释并用饱和nahco3水溶液洗涤。分层,将有机层用mgso4干燥。过滤后将滤液浓缩以得到白色固体状标题化合物(1.8g,定量)。
[2397]1h-nmr(500mhz,dmso-d6)δppm:8.09(dd,1h),7.71(td,1h),7.54(d,1h),7.47(d,1h),7.38(td,1h),7.27(d,1h),7.25(d,1h),7.24(dd,1h),7.18(dd,1h),7.18(dd,1h),7.12(d,1h),7.1(d,1h),4.82(t,1h),4.65(t,1h),4.65(m,2h),4.47(s,2h),4.25(s,2h),3.9(q,2h),3.35(q,2h),3.15(m,2h),2.74(s,3h),2.23(s,3h),1.98(m,2h),0.98(t,3h)。
[2398]
步骤3:3-[1-(3-氯丙基)-4-甲基-1h-苯并三唑-5-基]-3-(4-甲基-3-{[6-(2-硝基苯氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}苯基)丙酸乙酯的制备
[2399]
采用通用方法10,用3-[1-(3-羟基丙基)-4-甲基-1h-苯并三唑-5-基]-3-(4-甲基-3-{[6-(2-硝基苯氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}苯基)丙酸乙酯(1eq.,1.8g,2.5mmol)作为起始试剂,得到标题化合物(1.8g,定量,棕色油)。
[2400]1h-nmr(500mhz,dmso-d6)δppm:8.09(dd,1h),7.71(td,1h),7.56(d,1h),7.5(d,1h),7.38(td,1h),7.27(d,1h),7.27(d,1h),7.24(dd,1h),7.18(dd,1h),7.18(dd,1h),7.13(d,1h),7.1(d,1h),4.82(t,1h),4.74(t,2h),4.48(s,2h),4.26(s,2h),3.9(q,2h),3.58(t,2h),3.15(d,2h),2.75(s,3h),2.31(quint.,2h),2.23(s,3h),0.98(t,3h)。
[2401]
步骤4:3-(3-{[6-(2-氨基苯氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-甲基苯基)-3-[1-(3-氯丙基)-4-甲基-1h-苯并三唑-5-基]丙酸乙酯的制备
[2402]
采用通用方法1步骤3,用3-[1-(3-氯丙基)-4-甲基-1h-苯并三唑-5-基]-3-(4-甲基-3-{[6-(2-硝基苯氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}苯基)丙酸乙酯(1eq.,1.8g,2.5mmol)作为起始试剂,得到标题化合物(1.41g,82%收率,棕色固体)。
[2403]c36h38
cln5o6s的hrms计算值:703.2231;[m+h]
+
,实测值:704.2301(δ=-0.4ppm)。
[2404]
步骤5:[4,37-二甲基-33,33-二氧代-27,32-二氧杂-33λ
6-硫杂-1,14,15,16,20-五氮杂七环[26.5.3.1
3,7
.1
9,13
.0
12,16
.0
21,26
.0
31,35
]三十八碳-3(38),4,6,9(37),10,12,14,21,23,25,28,30,35-十三烯-8-基]乙酸乙酯的制备
[2405]
在室温下将3-(3-{[6-(2-氨基苯氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-甲基苯基)-3-[1-(3-氯丙基)-4-甲基-1h-苯并三唑-5-基]丙酸乙酯(1eq.,500mg,0.7100mmol)溶于丙腈(25ml)并加入碘化钠(2eq.,213mg,1.420mmol)。将混合物加热至100℃并回流5小时。加入k2co3(2eq.,196mg,1.420mmol)并将混合物于100℃搅拌6小时。将溶剂减压蒸发并将残余物在dcm和水之间进行分配。分离出有机层并用1m水hcl溶液洗涤,然后用饱和nahco3水溶液洗涤。将有机相用硫酸镁干燥,过滤后减压蒸发。将粗产物通过反相色谱纯化,用水-mecn作为洗脱剂得到白色固体状标题化合物(125mg,0.187mmol,26%收率)。
[2406]1h-nmr(500mhz,dmso-d6)δppm:7.6(d,1h),7.4(dd,1h),7.36(d,1h),7.2(d,1h),7.13(d,1h),7.04(t,1h),6.91(d,1h),6.89(dd,1h),6.88(d,1h),6.86(d,1h),6.85(d,1h),6.64(t,1h),5.05(brt,1h),4.85(t,1h),4.74/4.56(dt+dt,2h),4.29/4.11(d+d,2h),4.21/4.09(d+d,2h),3.9(q,2h),3.29/3.01(m+m,2h),3.16(d,2h),2.69(s,3h),2.27(s,3h),2.19(qn,2h),0.99(t,3h)。
[2407]
步骤6:实施例71的制备
[2408]
采用通用方法12,用[4,37-二甲基-33,33-二氧代-27,32-二氧杂-33λ
6-硫杂-1,14,15,16,20-五氮杂七环[26.5.3.1
3,7
.1
9,13
.0
12,16
.0
21,26
.0
31,35
]三十八碳-3(38),4,6,9(37),10,12,14,21,23,25,28,30,35-十三烯-8-基]乙酸乙酯(1eq.,170mg,0.25mmol)作为起始试剂,得到标题化合物(135mg,83%收率,白色固体)。
[2409]
手性柱色谱分离得到对映体纯产物。
[2410]
实施例71a(e1,光学纯度:97.9%)
[2411]c34h33
n5o6s的hrms计算值:639.2151;[m+h]
+
,实测值:640.2231(δ=1.0ppm)。
[2412]
实施例71b(e2,光学纯度》99.9%)
[2413]c34h33
n5o6s的hrms计算值:639.2151;[m+h]
+
,实测值:640.2226(δ=0.3ppm)。1h-nmr(500mhz,dmso-d6)δppm:12.32(brs,1h),7.56(d,1h),7.39(dd,1h),7.34(d,1h),7.17(d,1h),7.12(d,1h),7.04(t,1h),6.88(dd,1h),6.87(d,1h),6.86(d,1h),6.85(d,1h),6.82(d,1h),6.63(t,1h),5.04(t,1h),4.84(t,1h),4.73/4.55(dt+dt,2h),4.28/4.14(d+
d,2h),4.2/4.09(d+d,2h),3.28/3.02(m+m,2h),2.96(m,2h),2.68(s,3h),2.27(s,3h),2.19(qn,2h)。
[2414]
13
c-nmr(125mhz,dmso-d6)δppm:154.7,146.5,146.1,143.1,142.4,140.4,137,135.7,132,131.7,131.3,129.8,129.3,127.7,127.3,126,120.1,119.5,118.9,118.1,117.2,116.7,113,107.3,51.5,49.1,45,42.5,41.6,39.6,28.3,18.4,13.3。
[2415]
实施例72:[4-甲基-10,25,25-三氧代-19,24-二氧杂-25λ
6-硫杂-1,9,12,13,14-五氮杂五环[18.5.3.1
3,7
.1
11,14
.0
23,27
]三十碳-3(30),4,6,11(29),12,20,22,27-八烯-8-基]乙酸
[2416][2417]
步骤1:[(5-溴-2-甲基苯基)甲氧基](叔丁基)二苯基硅烷的制备
[2418]
将(5-溴-2-甲基苯基)甲醇(1eq.,20g,99mmol)、咪唑(3eq.,20g,297mmol)和dcm(250ml)的混合物于10℃进行搅拌。加入叔丁基二苯基氯硅烷并将混合物在该温度下搅拌1小时。反应完成后,将混合物用水(300ml)淬灭,将形成的混合物用dcm萃取,分层。将有机层用无水硫酸钠干燥,过滤并将滤液减压蒸发。将粗产物通过正相硅胶色谱纯化,用庚烷-dcm(100:0至50:50)作为洗脱剂。得到无色固体状标题化合物(44g,定量)。
[2419]1h-nmr(400mhz,dmso-d6)δppm:7.63(m,4h),7.55(d,1h),7.44(m,6h),7.37(dd,1h),7.11(d,1h),4.73(s,2h),2.09(s,3h),1.04(s,9h)。
[2420]
步骤2:1-[3-({[叔丁基(二苯基)硅基]氧基}甲基)-4-甲基苯基]乙-1-酮的制备
[2421]
于-78℃在惰性气氛下向搅拌中的[(5-溴-2-甲基苯基)甲氧基](叔丁基)二苯基硅烷(1eq.,20g,45.5mmol)的thf(364ml,8ml/mmol)溶液中滴加丁基锂(2.6m,2eq.,35ml,91mmol)并将混合物在该温度下搅拌过夜。于-78℃滴加n,n-二甲基乙酰胺(3eq.,14.1g,137mmol)并将混合物于-78℃继续搅拌1小时。将混合物升温至室温并搅拌过夜。反应完成后,将混合物用水淬灭,用etoac萃取,分层。将有机层用硫酸钠干燥,过滤并将滤液减压蒸发。将粗产物通过正相硅胶色谱纯化,用庚烷-etoac-etoh(100:0:0至70:22.5:7.5)作为洗脱剂。得到无色固体状标题化合物(9.5g,47%收率)。
[2422]1h-nmr(400mhz,cdcl3)δppm:8.1(d,1h),7.8(dd,1h),7.7(dd,4h),7.4(td+d,6h),7.2(d,1h),4.8(s,2h),2.6(s,3h),2.2(s,3h),1.1(q,9h)。
[2423]
步骤3:3-[3-({[叔丁基(二苯基)硅基]氧基}甲基)-4-甲基苯基]-3-氧代丙酸甲酯的制备
[2424]
在室温下向搅拌中的1-[3-({[叔丁基(二苯基)硅基]氧基}甲基)-4-甲基苯基]乙-1-酮(1eq.,9.5g,23.6mmol)的碳酸二甲酯(11eq.,23.4g,259.6mmol)溶液中加入nah(2eq.,1.88g,12mmol,47.2mmol,60wt%的矿物油溶液)。将混合物于95℃加热4小时。反应完成后,将混合物冷却至室温,用水稀释,将形成的混合物用etoac萃取。分层,将有机层用
硫酸钠干燥,过滤并将滤液减压蒸发。将粗产物通过正相硅胶色谱纯化,用庚烷-dcm(100:0至0:100)作为洗脱剂。得到无色油状标题化合物(7.9g,73%收率)。
[2425]1h-nmr(400mhz,dmso-d6)δppm:8.05(d,1h),7.8(dd,1h),7.65(m,4h),7.51-7.4(m,6h),7.33(d,1h),4.8(s,2h),4.13(s,2h),3.64(s,3h),2.22(s,3h),1.05(s,9h)。
[2426]
步骤4:3-氨基-3-[3-({[叔丁基(二苯基)硅基]氧基}甲基)-4-甲基苯基]丙酸甲酯的制备
[2427]
将3-[3-({[叔丁基(二苯基)硅基]氧基}甲基)-4-甲基苯基]-3-氧代丙酸甲酯(1eq.,7.9g,17mmol)、乙酸铵(5eq.,6.6g,86mmol)和meoh(86ml,5ml/mmol)的混合物在回流温度下搅拌过夜。反应完成后,将溶剂减压蒸发得到油状的3-[3-({[叔丁基(二苯基)硅基]氧基}甲基)-4-甲基苯基]-3-亚氨基丙酸甲酯。于10℃将粗产物溶于acoh(43ml,2.5ml/mmol)并将硼氢化钠缓慢加入到该混合物中。将混合物升温至室温并搅拌过夜。将混合物用饱和k2co3水溶液淬灭,将形成的混合物用etoac萃取。分层,将有机层用硫酸钠干燥,过滤并将滤液减压蒸发。将粗产物不经进一步纯化即可用于下一步骤(7.4g油,75%收率)。
[2428]1h-nmr(400mhz,dmso-d6)δppm:7.65(dd,4h),7.4(m,7h),7.2(dd,1h),7.1(d,1h),4.7(s,2h),4.25(m,1h),3.55(s,3h),2.65(2dd,2h),2.15(s,3h),1(s,9h)。
[2429]
步骤5:3-[(叔丁氧基羰基)氨基]-3-[3-({[叔丁基(二苯基)硅基]氧基}甲基)-4-甲基苯基]丙酸甲酯的制备
[2430]
在室温下向搅拌中的3-氨基-3-[3-({[叔丁基(二苯基)硅基]氧基}甲基)-4-甲基苯基]丙酸甲酯(1eq.,4g,7.02mmol)的dcm(56ml,8ml/mmol)溶液中加入tea(1.2eq.,2.5ml,18mmol)和二碳酸二叔丁酯(1.2eq.,1.84g,8.42mmol)。将混合物在室温下搅拌4小时。反应完成后将混合物用水稀释,然后用etoac萃取。分离出有机层并用无水硫酸钠干燥,过滤,浓缩至干。将粗产物通过正相硅胶色谱纯化,用庚烷-etoac-etoh(100:0:0至70:22.5:7.5)作为洗脱剂。得到无色油状标题化合物(3.7g,92%收率)。
[2431]1h-nmr(400mhz,dmso-d6)δppm:7.65(m,4h),7.4(m,9h),7.1(dd+d,2h),4.9(m,1h),4.7(s,2h),3.55(s,3h),2.7(2dd,2h),2.1(s,3h),1.3(m,9h),1(s,9h)。
[2432]
步骤6:3-[(叔丁氧基羰基)氨基]-3-[3-(羟基甲基)-4-甲基苯基]丙酸甲酯的制备
[2433]
将3-[(叔丁氧基羰基)氨基]-3-[3-({[叔丁基(二苯基)硅基]氧基}甲基)-4-甲基苯基]丙酸甲酯(1eq.,16.4g,29.3mmol)、四丁基氟化铵(1eq.,26.4g,29.3mmol)和thf(234ml,8ml/mmol)的混合物在室温下搅拌1小时。反应完成后,将混合物用饱和nahco3水溶液淬灭,将形成的混合物用etoac萃取。分层,将有机层用硫酸钠干燥,过滤并减压蒸发。将粗产物通过正相硅胶色谱纯化,用庚烷-etoac(80:20至30:70)作为洗脱剂。得到无色油状标题化合物(8.55g,90%收率)。
[2434]1h-nmr(400mhz,dmso-d6)δppm:7.42(d,1h),7.29(s,1h),7.08-7.02(m,2h),5.05(t,1h),4.88(m,1h),4.45(d,2h),3.55(s,3h),2.73/2.62(2dd,2h),2.19(s,3h),1.35(s,9h)。
[2435]
步骤7:3-(3-{[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-甲基苯基)-3-[(叔丁氧基羰基)氨基]丙酸甲酯的制备
[2436]
采用通用方法7,用3-[(叔丁氧基羰基)氨基]-3-[3-(羟基甲基)-4-甲基苯基]丙
酸甲酯(1当量)和6-(苄氧基)-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮(1.1当量)作为起始试剂,得到标题化合物(9g,81%收率)。
[2437]1h-nmr(400mhz,dmso-d6)δppm:7.45(d,1h),7.45(d,2h),7.42(t,2h),7.38(t,1h),7.2(m,3h),7.18(d,1h),7.1(dd,1h),7(d,1h),5.09(s,2h),4.9(m,1h),4.48(s,2h),4.22(m,2h),3.55(s,3h),2.76/2.7(2dd,2h),2.23(s,3h),1.38(s,9h)。
[2438]
步骤8:3-(3-{[6-(4-溴丁氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-甲基苯基)-3-[(叔丁氧基羰基)氨基]丙酸甲酯的制备
[2439]
采用通用方法8,用3-(3-{[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-甲基苯基)-3-[(叔丁氧基羰基)氨基]丙酸甲酯(1当量)作为反应试剂,得到3-[(叔丁氧基羰基)氨基]-3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}丙酸甲酯(4.3g,62%收率)。在室温下向该粗产物(0.5g,1mmol,7.35ml)的mecn(10ml/mmol,10ml)溶液中加入1,4-二溴丁烷(1.5eq.,0.2ml,46.5mmol)和cs2co3(3eq.,0.6g,3mmol)并将混合物搅拌过夜。反应完成后将溶剂蒸发。将粗产物通过反相色谱纯化,用水-mecn梯度洗脱(59:41至5:95)得到标题化合物(345mg白色固体,50%收率)。
[2440]1h-nmr(400mhz,dmso-d6)δppm:7.45(d,1h),7.25-7.15(m,3h),7.11(d,1h),7(dd,1h),6.89(d,1h),4.88(m,1h),4.45/4.2(s+m,4h),4(t,2h),3.6(t,2h),3.55(s,3h),2.77/2.68(2dd,2h),2.22(s,3h),1.95(m,2h),1.8(m,2h),1.35(s,9h)。
[2441]
步骤9:3-(3-{[6-(4-叠氮基丁氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-甲基苯基)-3-[(叔丁氧基羰基)氨基]丙酸甲酯的制备
[2442]
将3-(3-{[6-(4-溴丁氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-甲基苯基)-3-[(叔丁氧基羰基)氨基]丙酸甲酯(1eq.,345mg,0.538mmol)、叠氮化钠(2.3eq.,80mg,1.23mmol)和dmf(10ml)的混合物在室温下搅拌过夜。反应完成后,将混合物用冰水淬灭,将形成的混合物用etoac萃取。分层,将有机层用硫酸钠干燥并过滤。将溶剂减压蒸发。将粗产物通过反相色谱纯化,用水-mecn梯度洗脱(100:0至0:100)得到标题化合物(290mg白色固体,50%收率)。
[2443]1h-nmr(400mhz,dmso-d6)δppm:7.42(d,1h),7.25-7.15(m,3h),7.12(d,1h),6.99(dd,1h),6.9(d,1h),4.88(m,1h),4.45(s,2h),4.2(2d,2h),4(t,2h),3.57(s,3h),3.4(t,2h),2.77/2.68(2dd,2h),2.25(s,3h),1.8-1.65(m,4h),1.35(s,9h)。
[2444]
步骤10:1-[4-({3-[(5-{1-[(叔丁氧基羰基)氨基]-3-甲氧基-3-氧代丙基}-2-甲基苯基)甲基]-2,2-二氧代-3,4-二氢-2h-1,2λ6,3-噁噻嗪-6-基}氧基)丁基]-1h-1,2,3-三唑-4-甲酸叔丁酯的制备
[2445]
在室温下向搅拌中的3-(3-{[6-(4-叠氮基丁氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-甲基苯基)-3-[(叔丁氧基羰基)氨基]丙酸甲酯(1eq.,225mg,0.372mmol)的叔丁醇(1.86ml,5ml/mmol)和水(0.75ml,2ml/mmol)溶液中加入丙-2-炔酸叔丁酯(1eq.,47mg,0.372mmol)、硫酸铜(0.06eq.,3.6mg,0.022mmol)和抗坏血酸钠(0.2eq.,15mg,0.075mmol)并将混合物搅拌24小时。用0.1m水hcl淬灭反应,将形成的混合物用etoac萃取。分层,将有机层用硫酸钠干燥并过滤。将溶剂减压蒸发。将粗产物通过正相硅胶色谱纯化,用dcm-etoac(100:0至80:20)作为洗脱剂。得到无色树胶状标题化合物(263mg,96%收率)。
[2446]1h-nmr(400mhz,dmso-d6)δppm:8.68(s,1h),7.45(d,1h),7.2(m,3h),7.15(d,1h),7(dd,1h),6.9(d,1h),4.9(m,1h),4.5(t,2h),4.45(s,2h),4.2(m,2h),3.98(t,2h),3.55(s,3h),2.7(m,2h),2.25(s,3h),2(m,2h),1.7(m,2h),1.5(s,9h),1.3(s,9h)。
[2447]
步骤11:1-{4-[(3-{[5-(1-氨基-3-甲氧基-3-氧代丙基)-2-甲基苯基]甲基}-2,2-二氧代-3,4-二氢-2h-1,2λ6,3-噁噻嗪-6-基)氧基]丁基}-1h-1,2,3-三唑-4-甲酸盐酸盐的制备
[2448]
于0℃向1-[4-({3-[(5-{1-[(叔丁氧基羰基)氨基]-3-甲氧基-3-氧代丙基}-2-甲基苯基)甲基]-2,2-二氧代-3,4-二氢-2h-1,2λ6,3-噁噻嗪-6-基}氧基)丁基]-1h-1,2,3-三唑-4-甲酸叔丁酯(1eq.,200mg,0.274mmol)的二氧杂环己烷(10ml/mmol,2.74ml)溶液中加入hcl(4m的二氧杂环己烷溶液)(5.5eq.,0.377ml)。将反应混合物升温至室温并在室温下搅拌4小时。反应完成后将挥发物减压蒸发至干。粗产物不经纯化即可使用(174mg,定量)。
[2449]1h-nmr(400mhz,dmso-d6)δppm:8.8-8.4(m,3h),8.71(s,1h),7.4(dd+d,2h),7.3(d,1h),7.15(d,1h),7(dd+d,2h),4.62(t,1h),4.52(s,2h),4.5(t,2h),4.25(m,2h),4(t,2h),3.6(s,3h),3.12/2.98(2dd,2h),2.3(s,3h),2.02(m,2h),1.7(m,2h)。
[2450]
步骤12:[4-甲基-10,25,25-三氧代-19,24-二氧杂-25λ
6-硫杂-1,9,12,13,14-五氮杂五环[18.5.3.1
3,7
.1
11,14
.0
23,27
]三十碳-3(30),4,6,11(29),12,20,22,27-八烯-8-基]乙酸甲酯的制备
[2451]
将1-{4-[(3-{[5-(1-氨基-3-甲氧基-3-氧代丙基)-2-甲基苯基]甲基}-2,2-二氧代-3,4-二氢-2h-1,2λ6,3-噁噻嗪-6-基)氧基]丁基}-1h-1,2,3-三唑-4-甲酸盐酸盐(1eq.,154mg,0.252mmol)溶于dcm(126ml,500ml/mmol),然后加入tea(5eq.,0.176ml,1.262mmol)、苯并三唑-1-醇(1.2eq.,41mg,0.303mmol)和n-(3-二甲基氨基丙基)-n
’‑
乙基碳二亚胺盐酸盐(1.2eq.,58mg,0.303mmol)。将混合物室温搅拌过夜,用30ml水淬灭并用dcm萃取。将有机相分离,用盐水洗涤,用硫酸钠干燥,过滤并浓缩得到粗产物,将其通过反相色谱纯化,用水-mecn梯度洗脱(64:36至28:72)得到标题化合物(43mg白色固体,31%收率)。
[2452]1h-nmr(400mhz,dmso-d6)δppm:8.2(d,1h),8.11(s,1h),7.21(m,2h),6.98(d,1h),6.91(d,1h),6.75(dd,1h),6(d,1h),5.61(m,1h),4.7/4.38(2m,2h),4.3(2d,2h),4.18/4.05(2d,2h),4/3.61(2m,2h),3.65(s,3h),3.2/3.1(2m,2h),2.45(s,3h),2.4-1.9(m,4h)。
[2453]
步骤13:实施例72的制备
[2454]
采用通用方法12,用[4-甲基-10,25,25-三氧代-19,24-二氧杂-25λ
6-硫杂-1,9,12,13,14-五氮杂五环[18.5.3.1
3,7
.1
11,14
.0
23,27
]三十碳-3(30),4,6,11(29),12,20,22,27-八烯-8-基]乙酸甲酯(1当量)作为起始试剂,得到标题化合物(白色固体,定量)。
[2455]
通过手性柱色谱分离得到对映体纯产物。
[2456]
实施例72a(e1)
[2457]c25h27
n5o7s的hrms计算值:541.1631;[m+h]
+
,实测值:542.1709(δ=0.9ppm)。
[2458]
实施例72b(e2)
[2459]c25h27
n5o7s的hrms计算值:541.1631;[m+h]
+
,实测值:542.1708(δ=0.7ppm)。
[2460]1h-nmr(400mhz,dmso-d6)δppm:12.3(m,1h),9.15(d,1h),8.66(s,1h),7.31(dd,1h),7.25(d,1h),7.11(d,1h),7.06(d,1h),6.86(dd,1h),6.2(d,1h),5.41(m,1h),4.53(m,2h),4.53/3.99(dd,2h),4.39/3.77(dd,2h),3.39/2.81(2m,2h),2.84/2.72(2dd,2h),2.35(s,3h),2.16-1.7(m,4h)。
[2461]
实施例73:[4,10,14-三甲基-29,29-二氧代-17,23,28-三氧杂-29λ
6-硫杂-1,12,13,14-四氮杂六环[22.5.3.1
3,7
.1
9,16
.0
11,15
.0
27,31
]三十四碳-3(34),4,6,9(33),10,12,15,24,26,31-十烯-8-基]乙酸
[2462][2463]
步骤a1:3-(1,4-二甲基-1h-苯并三唑-5-基)-3-[3-(羟基甲基)-4-甲基苯基]丙酸甲酯的制备
[2464]
采用通用方法6,用(2e)-3-(1,4-二甲基-1h-苯并三唑-5-基)丙-2-烯酸甲酯(1当量)和[2-甲基-5-(4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷-2-基)苯基]甲醇(1.3当量)作为起始试剂,得到标题化合物(橙色油,88%收率)。
[2465]1h-nmr(500mhz,dmso-d6)δppm:7.57(d,1h),7.47(d,1h),7.24(d,1h),7.1(dd,1h),7.02(d,1h),4.99(t,1h),4.84(t,1h),4.4(d,2h),4.23(s,3h),3.48(s,3h),3.18/3.13(dd+dd,2h),2.75(s,3h),2.15(s,3h)。
[2466]
步骤1:3-(3-{[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-甲基苯基)-3-(1,4-二甲基-1h-苯并三唑-5-基)丙酸甲酯的制备
[2467]
采用通用方法7,用3-(1,4-二甲基-1h-苯并三唑-5-基)-3-[3-(羟基甲基)-4-甲基苯基]丙酸甲酯(1当量)和6-(苄氧基)-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮(1.2当量)作为起始试剂,得到标题化合物(米黄色固体泡沫,84%收率)。
[2468]1h-nmr(500mhz,dmso-d6)δppm:7.56(d,1h),7.49(d,1h),7.48-7.32(m,5h),7.21(d,1h),7.18(dd,1h),7.13(d,1h),7.13(d,1h),7.07(dd,1h),6.94(d,1h),5.1(s,2h),4.85(t,1h),4.42(s,2h),4.22/4.19(d+d,2h),4.2(s,3h),3.48(s,3h),3.22/3.17(dd+dd,2h),2.75(s,3h),2.22(s,3h)。
[2469]
步骤2:3-(3-{[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-甲基苯基)-3-(7-溴-1,4-二甲基-1h-苯并三唑-5-基)丙酸甲酯的制备
[2470]
将3-(3-{[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-甲基苯基)-3-(1,4-二甲基-1h-苯并三唑-5-基)丙酸甲酯(1eq.,1g,1.59mmol)溶于硝基甲烷(20ml),然后加入(3eq.,2.31g,4.79mmol)和溴化钾(1.2eq.,0.23g,1.92mmol)。将反应混合物于60℃搅拌过夜,用dcm(30ml)稀释并用水(50ml)洗涤。将有机相用硫酸镁干燥,过滤并减压浓缩得到粗产物,将其通过制备型反相色谱纯化,用5mm水nh4hco
3-mecn梯度
洗脱(95:5至0:100)得到标题化合物(35%收率)。
[2471]1h-nmr(500mhz,dmso-d6)δppm:7.68(s,1h),7.49-7.31(m,5h),7.25(d,1h),7.21(dd,1h),7.16(d,1h),7.13(d,1h),7.06(dd,1h),6.96(d,1h),5.1(s,2h),4.83(t,1h),4.47/4.42(d+d,2h),4.41(s,3h),4.22(s,2h),3.49(s,3h),3.24(d,2h),2.73(s,3h),2.23(s,3h)。
[2472]
步骤3:3-(3-{[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-甲基苯基)-3-(7-{[5-(苄氧基)戊基]氧基}-1,4-二甲基-1h-苯并三唑-5-基)丙酸甲酯的制备
[2473]
将3-(3-{[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-甲基苯基)-3-(7-溴-1,4-二甲基-1h-苯并三唑-5-基)丙酸甲酯(1eq.,391mg,0.554mmol)溶于甲苯(20ml),然后加入5-苄氧基戊-1-醇(10eq.,1.07g,5.54mmol)、cs2co3(10eq.,1.81g,5.54mmol)、2-(二-叔丁基膦)-1,1
’‑
联萘(0.1eq.,22mg,0.055mmol)和二乙酸钯催化剂(0.08eq.,10mg,0.044mmol)。将反应混合物于70℃在惰性气氛下搅拌3天。将溶剂蒸发,然后将混合物用etoac(20ml)和水(20ml)稀释。将有机相分离,将水相进一步用3x20ml etoac萃取。将合并的有机相用硫酸镁干燥,过滤,减压浓缩得到粗产物,将其通过制备型反相色谱纯化,用5mm水nh4hco
3-mecn梯度洗脱(95:5至0:100)得到标题化合物(无色油,11%收率)。
[2474]1h-nmr(500mhz,dmso-d6)δppm:7.47-7.19(m,12h),7.13(d,1h),7.13(d,1h),7.06(dd,1h),6.93(d,1h),6.88(s,1h),5.08(s,2h),4.8(t,1h),4.47/4.42(d+d,2h),4.42(s,2h),4.29(s,3h),4.24/4.19(d+d,2h),4.15/4.06(m+m,2h),3.49(s,3h),3.43(t,2h),3.22(m,2h),2.62(s,3h),2.21(s,3h),1.84-1.03(m,6h)。
[2475]
步骤4:3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}-3-{7-[(5-羟基戊基)氧基]-1,4-二甲基-1h-苯并三唑-5-基}丙酸甲酯的制备
[2476]
采用通用方法8,用3-(3-{[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-甲基苯基)-3-(7-{[5-(苄氧基)戊基]氧基}-1,4-二甲基-1h-苯并三唑-5-基)丙酸甲酯(1当量)作为起始试剂,得到标题化合物(白色固体泡沫,82%收率)。
[2477]1h-nmr(500mhz,dmso-d6)δppm:9.69(s,1h),7.24(d,1h),7.21(dd,1h),7.13(d,1h),6.99(d,1h),6.88(s,1h),6.78(dd,1h),6.58(d,1h),4.79(t,1h),4.42/4.36(d+d,2h),4.39(brs,1h),4.35(s,3h),4.23/4.16(d+d,2h),4.16/4.07(m+m,2h),3.51(s,3h),3.42(m,2h),3.23/3.19(m+m,2h),2.61(s,3h),2.22(s,3h),1.85-1.43(m,6h)。
[2478]
步骤5:3-{7-[(5-氯戊基)氧基]-1,4-二甲基-1h-苯并三唑-5-基}-3-{3-[(6-羟基-2,2-二氧代
[2479]-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}丙酸甲酯盐酸盐的制备
[2480]
采用通用方法10,用3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}-3-{7-[(5-羟基戊基)氧基]-1,4-二甲基-1h-苯并三唑-5-基}丙酸甲酯(1当量)作为起始试剂,得到标题化合物(灰白色固体泡沫,定量)。
[2481]1h-nmr(500mhz,dmso-d6)δppm:9.71(brs,1h),7.24(d,1h),7.21(dd,1h),7.13(d,1h),6.99(d,1h),6.89(s,1h),6.79(dd,1h),6.58(d,1h),4.79(t,1h),4.42/4.37(d+d,2h),4.35(s,3h),4.23/4.17(d+d,2h),4.17/4.07(m+m,2h),3.66(t,2h),3.51(s,3h),
3.24/3.19(dd+dd,2h),2.61(s,3h),2.22(s,3h),1.81(m,2h),1.79(m,2h),1.59(m,2h)。
[2482]
步骤6:[4,10,14-三甲基-29,29-二氧代-17,23,28-三氧杂-29λ
6-硫杂-1,12,13,14-四氮杂六环[22.5.3.1
3,7
.1
9,16
.0
11,15
.0
27,31
]三十四碳-3(34),4,6,9(33),10,12,15,24,26,31-十烯-8-基]乙酸甲酯的制备
[2483]
采用通用方法11,用3-{7-[(5-氯戊基)氧基]-1,4-二甲基-1h-苯并三唑-5-基}-3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}丙酸甲酯盐酸盐(1当量)作为起始试剂,得到标题化合物(米黄色固体,19%)。
[2484]1h-nmr(500mhz,dmso-d6)δppm:7.4(dd,1h),7.2(d,1h),7.1(s,1h),7.07(m,1h),7.07(d,1h),6.97(m,1h),6.96(m,1h),4.77(t,1h),4.42/4.26(d+d,2h),4.35(s,3h),4.29/4.07(m+m,2h),4.18(t,2h),4.11/4.05(d+d,2h),3.49(s,3h),3.32/3.18(dd+dd,2h),2.52(s,3h),2.31(s,3h),2.1-1.58(m,6h)。
[2485]
步骤7:实施例73的制备
[2486]
采用通用方法12,用[4,10,14-三甲基-29,29-二氧代-17,23,28-三氧杂-29λ
6-硫杂-1,12,13,14-四氮杂六环[22.5.3.1
3,7
.1
9,16
.0
11,15
.0
27,31
]三十四碳-3(34),4,6,9(33),10,12,15,24,26,31-十烯-8-基]乙酸甲酯(1当量)作为起始试剂,得到标题化合物(白色固体,72%收率)。
[2487]
通过手性柱色谱分离得到对映体纯产物。
[2488]
实施例73a(e1)
[2489]c31h34
n4o7s的hrms计算值:606.2148;[m+h]
+
,实测值:607.2223(δ=0.3ppm)。
[2490]
实施例73b(e2)
[2491]c31h34
n4o7s的hrms计算值:606.2148;[m+h]
+
,实测值:607.2223(δ=0.3ppm)。
[2492]1h-nmr(500mhz,dmso-d6)δppm 7.4(d,1h),7.19(d,1h),7.13(s,1h),7.06(d,1h),7.02(d,1h),6.99(d,1h),6.96(dd,1h),4.73(t,1h),4.41/4.29(d+d,2h),4.35(s,3h),4.28/4.08(m+m,2h),4.17(t,2h),4.14/3.99(d+d,2h),3.16/3.02(dd+dd,2h),2.5(s,3h),2.31(s,3h),2/1.92(m+m,2h),1.9/1.74(m+m,2h),1.73/1.63(m+m,2h)。
[2493]
13
c-nmr(125mhz,dmso-d6)δppm:173.5,155.7,148.3,144.8,143.6,142.3,137.6,136.4,132.8,131.2,129.9,129.8,123.9,119.4,118.1,117.9,117.6,113.8,107,68.3,68.1,51.9,49.8,42.2,41.7,36.9,27.4,26.7,21.1,18.7,12.8。
[2494]
实施例74:2-[4,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]-2-甲基丙酸
[2495][2496]
步骤1:2-[(5-溴-2-甲基苯基)甲氧基]氧杂环己烷的制备
[2497]
于0℃下向(5-溴-2-甲基苯基)甲醇(1eq.,7.05g,35.1mmol)的dcm(50ml)溶液中加入4-甲基苯-1-磺酸一水合物(0.01当量,0.07g,0.351mmol),然后加入3,4-二氢-2h-吡喃(1.1当量,3.52ml,38.6mmol)。将反应混合物升温至室温并搅拌1小时,然后用饱和nahco3(30ml)淬灭。分相。将水相用dcm(30ml)萃取,将合并的有机相用mgso4干燥并过滤。减压除去溶剂得到标题化合物(10g,定量)。
[2498]1h-nmr(500mhz,dmso-d6)δppm:7.49(d,1h),7.38(dd,1h),7.15(d,1h),4.7(t,1h),4.66/4.42(d+d,2h),3.77/3.49(m+m,2h),2.22(s,3h),1.82-1.41(m,6h)。
[2499]
步骤2:4-甲基-3-{[(氧杂环己烷-2-基)氧基]甲基}苯甲醛的制备
[2500]
向搅拌中的2-[(5-溴-2-甲基苯基)甲氧基]氧杂环己烷(1eq.,5g,18mmol)的thf(40ml)溶液中加入n1,n1,n2,n
2-四甲基乙烷-1,2-二胺(1.5eq.,3.1g,26mmol)。将混合物冷却至-75℃,滴加丁基锂(1.5eq.,26mmol)并将混合物于-75℃继续搅拌30分钟。滴加dmf(2eq.,2.6g,35mmol),将温度升温至室温并将混合物在室温下继续搅拌1小时。反应完成后将混合物倒入80ml水中并用etoac萃取。将分离出的有机层用硫酸镁干燥,过滤并蒸发至干。将粗品油通过正相硅胶色谱纯化,用庚烷-etoac(100:0至0:100)作为洗脱剂得到标题化合物(4g,97%收率)。
[2501]1h-nmr(500mhz,dmso-d6)δppm:9.97(s,1h),7.87(d,1h),7.75(dd,1h),7.42(d,1h),4.76/4.51(d+d,2h),4.73(dd,1h),3.79/3.5(m+m,2h),2.36(s,3h),1.83-1.41(m,6h)。
[2502]
步骤3:{1-[4-(苄氧基)丁基]-4-甲基-1h-苯并三唑-5-基}(4-甲基-3-{[(氧杂环己烷-2-基)氧基]甲基}苯基)甲醇的制备
[2503]
将1-[4-(苄氧基)丁基]-5-溴-4-甲基-1h-苯并三唑(1eq.,1.04g,2.78mmol)溶于thf(40ml)并加入n1,n1,n2,n
2-四甲基乙烷-1,2-二胺(1.5eq.,484mg,4.17mmol)。将混合物冷却至-75℃,滴加丁基锂(3eq.,8.34mmol)并将混合物于-75℃搅拌30分钟。加入溶于thf(10ml)的4-甲基-3-{[(氧杂环己烷-2-基)氧基]甲基}苯甲醛(2eq.,1.3g,5.5mmol)并将反应混合物室温搅拌2小时。反应完成后将混合物倒入100ml水中,用2x50ml etoac萃取,将合并的有机层用硫酸镁干燥,过滤,减压蒸发至干。将粗品油通过正相硅胶色谱纯化,用庚烷-etoac(100:0至0:100)作为洗脱剂得到标题化合物(0.4g,27%收率)。
[2504]1h-nmr(500mhz,dmso-d6)δppm:7.61(d,1h),7.59(d,1h),7.35-7.23(m,5h),7.25(d,1h),7.17(dd,1h),7.09(d,1h),6.05(d,1h),5.89(d,1h),4.67(t,2h),4.61/4.37(d+d,2h),4.59(dd,1h),4.4(s,2h),3.67/3.37(m+m,2h),3.42(t,2h),2.67/2.66(s,3h),2.21(s,3h),1.94(m,2h),1.7-1.3(m,6h),1.49(m,2h)。
[2505]
步骤4:3-{1-[4-(苄氧基)丁基]-4-甲基-1h-苯并三唑-5-基}-2,2-二甲基-3-(4-甲基-3-{[(氧杂环己烷-2-基)氧基]甲基}苯基)丙酸甲酯的制备
[2506]
将{1-[4-(苄氧基)丁基]-4-甲基-1h-苯并三唑-5-基}(4-甲基-3-{[(氧杂环己烷-2-基)氧基]甲基}苯基)甲醇(1eq.,4.04g,7.62mmol)溶于mecn(50ml)并加入2,2,2-三氯乙腈(2eq.,2.2g,15.25mmol)和2,3,4,6,7,8,9,10-八氢嘧啶并[1,2-a]吖庚因(0.05eq.,58.06mg,0.38mmol)。将混合物在室温下搅拌45分钟,然后加入[(1-甲氧基-2-甲基丙-1-烯-1-基)氧基](三甲基)硅烷(2.5eq.,3.32g,19.07mmol)和1,1,1-三氟-n-(三氟甲磺酰基)-甲磺酰胺(0.1eq.,0.21g,0.76mmol)。将反应混合物室温搅拌2小时。反应完成
后加入40ml饱和nahco3水溶液并分层。将水层用2x50ml etoac萃取,将合并的有机层用硫酸镁干燥,过滤并减压蒸发得到标题化合物(4.6g,98%收率)。
[2507]1h-nmr(500mhz,dmso-d6)δppm:7.61-7.54(d,1h),7.61-7.54(d,1h),7.35-7.23(m,5h),7.22(d,1h),7.13(dd,1h),7.06(d,1h),4.77(s,1h),4.66(t,2h),4.58/4.38(d+d,2h),4.57(m,1h),4.4(s,2h),3.67/3.35(m+m,2h),3.43(s,3h),3.42(t,2h),2.7/2.69(s,3h),2.19(s,3h),1.94(m,2h),1.75-1.31(m,6h),1.52(m,2h),1.3(s,3h),1.23(s,3h)。
[2508]
步骤5:3-{1-[4-(苄氧基)丁基]-4-甲基-1h-苯并三唑-5-基}-3-[3-(羟基甲基)-4-甲基苯基]-2,2-二甲基丙酸甲酯的制备
[2509]
将3-{1-[4-(苄氧基)丁基]-4-甲基-1h-苯并三唑-5-基}-2,2-二甲基-3-(4-甲基-3-{[(氧杂环己烷-2-基)氧基]甲基}苯基)丙酸甲酯(1eq.,4.6g,7.49mmol)溶于meoh(80ml)并加入4-甲基苯磺酸吡啶复合物(0.05eq.,94.2mg,0.375mmol)。于55℃搅拌2小时后将反应混合物冷却至室温,减压蒸发至干,溶于dcm,用2x50ml饱和水溶液nahco3萃取,然后用50ml盐水萃取。将有机层用硫酸镁干燥,过滤并减压蒸发得到标题化合物(3.93g,99%收率)。
[2510]1h-nmr(500mhz,dmso-d6)δppm:7.61(d,1h),7.59(d,1h),7.36-7.23(m,5h),7.28(d,1h),7.09(dd,1h),7.01(d,1h),5.01(t,1h),4.76(s,1h),4.66(t,2h),4.41(d,2h),4.4(s,2h),3.43(t,2h),3.42(s,3h),2.7(s,3h),2.15(s,3h),1.95(m,2h),1.52(m,2h),1.3(s,3h),1.24(s,3h)。
[2511]
步骤6:3-{1-[4-(苄氧基)丁基]-4-甲基-1h-苯并三唑-5-基}-3-(3-{[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-甲基苯基)-2,2-二甲基丙酸甲酯的制备
[2512]
采用通用方法7,用3-{1-[4-(苄氧基)丁基]-4-甲基-1h-苯并三唑-5-基}-3-[3-(羟基甲基)-4-甲基苯基]-2,2-二甲基丙酸甲酯(1当量)和6-(苄氧基)-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮(1当量)作为起始试剂,得到标题化合物(62%收率)。
[2513]1h-nmr(500mhz,dmso-d6)δppm:7.59(d,1h),7.57(d,1h),7.46(dm,2h),7.41(tm,2h),7.34(tm,1h),7.3(tm,2h),7.25(tm,1h),7.25(dm,2h),7.23(d,1h),7.19(dd,1h),7.14(d,1h),7.12(d,1h),7.08(dd,1h),6.89(d,1h),5.1(s,2h),4.77(s,1h),4.63(t,2h),4.42(s,2h),4.38(s,2h),4.28/4.17(d+d,2h),3.44(s,3h),3.4(t,2h),2.71(s,3h),2.22(s,3h),1.93(m,2h),1.49(m,2h),1.29/1.25(s+s,6h)。
[2514]
步骤7:3-[1-(4-羟基丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}-2,2-二甲基丙酸甲酯的制备
[2515]
采用通用方法8,用3-{1-[4-(苄氧基)丁基]-4-甲基-1h-苯并三唑-5-基}-3-(3-{[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-甲基苯基)-2,2-二甲基丙酸甲酯(1当量)作为起始试剂,得到标题化合物(99%收率)。
[2516]1h-nmr(500mhz,dmso-d6)δppm:9.71(s,1h),7.61(m,1h),7.61(m,1h),7.21(d,1h),7.19(dd,1h),7.13(d,1h),7(d,1h),6.8(dd,1h),6.57(d,1h),4.76(s,1h),4.65(t,2h),4.44(brs,1h),4.37(s,2h),4.26/4.15(d+d,2h),3.45(s,3h),3.39(t,2h),2.71(s,3h),2.23(s,3h),1.91(qn,2h),1.38(qn,2h),1.3(s,3h),1.25(s,3h)。
[2517]
步骤8:3-[1-(4-氯丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(6-羟基-2,2-二氧
代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}-2,2-二甲基丙酸甲酯的制备
[2518]
采用通用方法10,用3-[1-(4-羟基丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}-2,2-二甲基丙酸甲酯(1当量)作为起始试剂,得到标题化合物(98%收率)。
[2519]1h-nmr(500mhz,dmso-d6)δppm:9.6(brs,1h),7.65(d,1h),7.62(d,1h),7.21(d,1h),7.2(dd,1h),7.13(d,1h),7.01(d,1h),6.81(dd,1h),6.58(d,1h),4.77(s,1h),4.7(t,2h),4.37(s,2h),4.27/4.15(d+d,2h),3.65(t,2h),3.45(s,3h),2.71(s,3h),2.23(s,3h),2.01(qn,2h),1.71(qn,2h),1.3(s,3h),1.26(s,3h)。
[2520]
步骤9:2-[4,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]-2-甲基丙酸甲酯的制备
[2521]
采用通用方法11,用3-[1-(4-氯丁基)-4-甲基-1h-苯并三唑-5-基]-3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}-2,2-二甲基丙酸甲酯(1eq.,3.2g,4.99mmol)作为起始试剂,得到标题化合物(2.95g,97%收率)。
[2522]1h-nmr(500mhz,dmso-d6)δppm:7.6(d,1h),7.5(d,1h),7.38(dd,1h),7.27(d,1h),7.01(d,1h),6.81(dd,1h),6.67(d,1h),5.85(br.,1h),4.81(s,1h),4.8/4.73(m+m,2h),4.35/3.84(brd+brd,2h),4.08/3.65(d+d,2h),3.7/3.43(br+m,2h),3.43(s,3h),2.63(s,3h),2.33(s,3h),2.21/2.06(m+m,2h),1.84/1.64(m+m,2h),1.27/1.13(s+s,6h)。
[2523]
步骤10:实施例74的制备
[2524]
采用通用方法12,用2-[4,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]-2-甲基丙酸甲酯作为反应试剂,得到标题化合物。
[2525]
通过手性柱色谱分离得到对映体纯产物。
[2526]
实施例74a(e1)
[2527]c31h34
n4o6s的hrms计算值:590.2199;[m+h]
+
,实测值:591.2272(δ=0.0ppm)。
[2528]
实施例74b(e2)
[2529]c31h34
n4o6s的hrms计算值:590.2199;[m+h]
+
,实测值:591.2277(δ=0.9ppm)。
[2530]1h-nmr(500mhz,dmso-d6)δppm:12.34(brs,1h),7.61(d,1h),7.53(d,1h),7.46(dd,1h),7.26(d,1h),7(d,1h),6.81(dd,1h),6.61(brs,1h),5.85(brs,1h),4.84(s,1h),
[2531]
4.79/4.73(m+m,2h),4.27/3.87(brd+brd,2h),4.06/3.71(brd+brd,2h),3.71/3.43(m+m,2h),2.62(s,3h),2.33(s,3h),2.22/2.08(m+m,2h),1.83/1.64(m+m,2h),1.25(s,3h),1.07(s,3h)。
[2532]
13
c-nmr(125mhz,dmso-d6)δppm:133.3,130.9,130.6,128.3,119.6,117.6,111.1,107.2,67.9,52,51.6,48.7,48.2,26.6,25.6,25.3,24.7,18.5,14.2。
[2533]
实施例75:[24-氯-4,32-二甲基-28,28-二氧代-19,22,27-三氧杂-28λ
6-硫杂-1,14,15,16-四氮杂六环[21.5.3.1
3,7
.1
9,13
.0
12,16
.0
26,30
]三十三碳-3(33),4,6,9(32),10,12,14,23,25,30-十烯-8-基]乙酸
[2534][2535]
步骤1:3-(1-{2-[2-(苄氧基)乙氧基]乙基}-4-甲基-1h-苯并三唑-5-基)-3-[3-(羟基甲基)-4-甲基苯基]丙酸乙酯的制备
[2536]
采用通用方法6,用(2e)-3-(1-{2-[2-(苄氧基)乙氧基]乙基}-4-甲基-1h-苯并三唑-5-基)丙-2-烯酸乙酯(1当量)和[2-甲基-5-(4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷-2-基)苯基]甲醇(1.3当量)作为起始试剂,得到标题化合物(黄色油,71%收率)。
[2537]1h-nmr(500mhz,dmso-d6)δppm:7.61(d,1h),7.4(d,1h),7.33-7.17(m,5h),7.26(d,1h),7.08(dd,1h),7.01(d,1h),4.99(t,1h),4.82(t,1h),4.81(t,2h),4.39(d,2h),4.32(s,2h),3.92(q,2h),3.89(t,2h),3.52(m,2h),3.43(m,2h),3.12/3.07(dd+dd,2h),2.75(s,3h),2.14(s,3h),1.01(t,3h)。
[2538]
步骤2:3-(3-{[6-(苄氧基)-7-氯-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-甲基苯基)-3-(1-{2-[2-(苄氧基)乙氧基]乙基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯的制备
[2539]
采用通用方法7,用3-(1-{2-[2-(苄氧基)乙氧基]乙基}-4-甲基-1h-苯并三唑-5-基)-3-[3-(羟基甲基)-4-甲基苯基]丙酸乙酯(1当量)和6-(苄氧基)-7-氯-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮(0.83当量)作为起始试剂,得到标题化合物(灰白色固体,95%收率)。
[2540]1h-nmr(500mhz,dmso-d6)δppm:7.6(d,1h),7.51-7.13(m,10h),7.46(s,1h),7.43(d,1h),7.26(s,1h),7.25(d,1h),7.17(dd,1h),7.11(d,1h),5.16(s,2h),4.84(t,1h),4.8(t,2h),4.48/4.44(d+d,2h),4.28(s,2h),4.24/4.19(d+d,2h),3.91(q,2h),3.87(t,2h),3.5(m,2h),3.4(m,2h),3.18/3.12(dd+dd,2h),2.76(s,3h),2.19(s,3h),0.97(t,3h)。
[2541]
步骤3:3-{3-[(7-氯-6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}-3-{1-[2-(2-羟基乙氧基)乙基]-4-甲基-1h-苯并三唑-5-基}丙酸乙酯的制备
[2542]
采用通用方法8,用3-(3-{[6-(苄氧基)-7-氯-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-甲基苯基)-3-(1-{2-[2-(苄氧基)乙氧基]乙基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体泡沫,定量)。
[2543]1h-nmr(500mhz,dmso-d6)δppm:10.48(s,1h),7.62(d,1h),7.5(d,1h),7.31(s,1h),7.28(d,1h),7.18(dd,1h),7.13(d,1h),6.85(s,1h),4.83(t,1h),4.8(t,2h),4.54(m,1h),4.46/4.41(d+d,2h),4.25/4.2(d+d,2h),3.93(q,2h),3.88(t,2h),3.37(m,2h),3.37(m,2h),3.17(d,2h),2.76(s,3h),2.22(s,3h),1(t,3h)。
[2544]
步骤4:[24-氯-4,32-二甲基-28,28-二氧代-19,22,27-三氧杂-28λ
6-硫杂-1,14,15,16-四氮杂六环[21.5.3.1
3,7
.1
9,13
.0
12,16
.0
26,30
]三十三碳-3(33),4,6,9(32),10,12,14,23,25,30-十烯-8-基]乙酸乙酯的制备
[2545]
将3-{3-[(7-氯-6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}-3-{1-[2-(2-羟基乙氧基)乙基]-4-甲基-1h-苯并三唑-5-基}丙酸乙酯(1eq.,855mg,1.3mmol)溶于thf(80ml)并加入pph3(3eq.,1020mg,3.89mmol)。在室温下滴加diad(3eq.,787mg,3.89mmol)并将混合物在室温下继续搅拌1.5小时。反应完成后将溶剂蒸发,将粗产物通过正相硅胶色谱纯化,用庚烷-acoet(100:0至35:65)作为洗脱剂得到标题化合物(白色固体,定量)。
[2546]1h-nmr(500mhz,dmso-d6)δppm:7.65(d,1h),7.46(d,1h),7.42(dd,1h),7.42(s,1h),7.23(d,1h),7.13(d,1h),6.61(s,1h),4.86(m,2h),4.78(t,1h),4.36/4.08(d+d,2h),4.21/3.9(d+d,2h),4.01/3.94(m+m,2h),3.97/3.86(m+m,2h),3.86(q,2h),3.85/3.62(m+m,2h),3.09/3.02(dd+dd,2h),2.74(s,3h),2.3(s,3h),0.96(t,3h)。
[2547]
步骤5:实施例75的制备
[2548]
采用通用方法12,用[24-氯-4,32-二甲基-28,28-二氧代-19,22,27-三氧杂-28λ
6-硫杂-1,14,15,16-四氮杂六环[21.5.3.1
3,7
.1
9,13
.0
12,16
.0
26,30
]三十三碳-3(33),4,6,9(32),10,12,14,23,25,30-十烯-8-基]乙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体,93%收率)。
[2549]c29h29
cln4o7s的hrms计算值:612.1445;[m+h]
+
,实测值:613.1505(δ=-2.2ppm)。1h-nmr(500mhz,dmso-d6)δppm:(m,6h),12.08(brs.,1h),7.65(d,1h),7.45(d,1h),7.43(d,1h),7.42(s,1h),7.23(d,1h),7.1(s,1h),6.6(s,1h),4.86(m,2h),4.76(t,1h),4.35/4.1(d+d,2h),4.2/3.9(d+d,2h),2.95(d,2h),2.74(s,3h),2.31(s,3h)。
[2550]
13
c-nmr(125mhz,dmso-d6)δppm:173.1,131.2,130.8,129.4,126.8,119.8,116,108.9,71.3/69.9/68.3,52,48.6,48.4,41.7,41.1,18.6,13.4。
[2551]
实施例76:[31-氯-4,32-二甲基-28,28-二氧代-19,22,27-三氧杂-28λ
6-硫杂-1,14,15,16-四氮杂六环[21.5.3.1
3,7
.1
9,13
.0
12,16
.0
26,30
]三十三碳-3(33),4,6,9(32),10,12,14,23,25,30-十烯-8-基]乙酸
[2552][2553]
步骤1:3-(3-{[6-(苄氧基)-5-氯-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-甲基苯基)-3-(1-{2-[2-(苄氧基)乙氧基]乙基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯的制备
[2554]
采用通用方法6,用(e)-3-[1-[2-(2-苄氧基乙氧基)乙基]-4-甲基-苯并三唑-5-基]丙-2-烯酸乙酯(1当量)和6-苄氧基-5-氯-3-[[2-甲基-5-(4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷-2-基)苯基]甲基]-4h-1,2λ6,3-噁噻嗪2,2-二氧化物(1.2当量)作为反应试剂,得到标题化合物(白色固体泡沫,27%收率)。
[2555]1h-nmr(500mhz,dmso-d6)δppm:7.59(d,1h),7.51-7.12(m,10h),7.42(d,1h),7.34(d,1h),7.24(d,1h),7.21(dd,1h),7.21(d,1h),7.14(d,1h),5.25(s,2h),4.83(t,
1h),4.78(t,2h),4.4(s,2h),4.28(s,2h),4.24(s,2h),3.9(q,2h),3.87(t,2h),3.5(m,2h),3.4(m,2h),3.12(m,2h),2.75(s,3h),2.23(s,3h),0.98(t,3h)。
[2556]
步骤2:3-{3-[(5-氯-6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}-3-{1-[2-(2-羟基乙氧基)乙基]-4-甲基-1h-苯并三唑-5-基}丙酸乙酯的制备
[2557]
采用通用方法8,用3-(3-{[6-(苄氧基)-5-氯-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-甲基苯基)-3-(1-{2-[2-(苄氧基)乙氧基]乙基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体泡沫,定量)。
[2558]1h-nmr(500mhz,dmso-d6)δppm:10.51(s,1h),7.6(d,1h),7.47(d,1h),7.25(d,1h),7.24(dd,1h),7.16(d,1h),7.05(d,1h),7.02(d,1h),4.84(t,1h),4.8(t,2h),4.54(m,1h),4.37(s,2h),4.24(s,2h),3.92(q,2h),3.88(t,2h),3.38(m,2h),3.38(m,2h),3.15(m,2h),2.76(s,3h),2.24(s,3h),1(t,3h)。
[2559]
步骤3:[31-氯-4,32-二甲基-28,28-二氧代-19,22,27-三氧杂-28λ
6-硫杂-1,14,15,16-四氮杂六环[21.5.3.1
3,7
.1
9,13
.0
12,16
.0
26,30
]三十三碳-3(33),4,6,9(32),10,12,14,23,25,30-十烯-8-基]乙酸乙酯的制备
[2560]
将3-{3-[(5-氯-6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}-3-{1-[2-(2-羟基乙氧基)乙基]-4-甲基-1h-苯并三唑-5-基}丙酸乙酯(1eq.,385mg,0.584mmol)溶于thf(10ml)并加入pph3(3eq.,460mg,1.75mmol)。在室温下滴加diad(3eq.,354mg,1.75mmol)并将混合物在该温度下继续搅拌1.5小时。反应完成后将溶剂蒸发,将粗产物通过正相硅胶色谱纯化,用庚烷-acoet(100:0至35:65)作为洗脱剂得到标题化合物(白色固体泡沫,64%收率)。
[2561]1h-nmr(500mhz,dmso-d6)δppm:7.59(d,1h),7.47(dd,1h),7.32(d,1h),7.29(d,1h),7.09(d,1h),7.07(d,1h),6.61(d,1h),4.83(m,2h),4.78(t,1h),4.28/3.9(d+d,2h),4.21/4.03(d+d,2h),4.17-3.98(m,4h),3.9(m,2h),3.76(m,2h),3.04/2.99(dd+dd,2h),2.59(s,3h),2.34(s,3h),0.99(t,3h)。
[2562]
步骤4:实施例76的制备
[2563]
采用通用方法12,用[31-氯-4,32-二甲基-28,28-二氧代-19,22,27-三氧杂-28λ
6-硫杂-1,14,15,16-四氮杂六环[21.5.3.1
3,7
.1
9,13
.0
12,16
.0
26,30
]三十三碳-3(33),4,6,9(32),10,12,14,23,25,30-十烯-8-基]乙酸乙酯(1当量)作为起始试剂,得到标题化合物(白色固体,86%收率)。
[2564]
通过手性柱色谱分离得到对映体纯产物。
[2565]
实施例76a(e1)
[2566]c29h29
cln4o7s的hrms计算值:612.1445;[m+h]
+
,实测值:613.1499(δ=-3.1ppm)。
[2567]
实施例76b(e2)
[2568]c29h29
cln4o7s的hrms计算值:612.1445;[m+h]
+
,实测值:613.1515(δ=-0.5ppm)。
[2569]1h-nmr(500mhz,dmso-d6)δppm:11.83(brs,1h),7.59(d,1h),7.49(dd,1h),7.33(d,1h),7.29(d,1h),7.1(d,1h),7.07(d,1h),6.58(d,1h),4.85/4.8(m+m,2h),4.75(t,1h),4.26/3.89(d+d,2h),4.2/4.03(d+d,2h),4.14/4.09(m+m,2h),4.09/4.01(m+m,2h),3.77(m,2h),2.88/2.82(dd+dd,2h),2.58(s,3h),2.34(s,3h)。
[2570]
13
c-nmr(125mhz,dmso-d6)δppm:131.6,130.7,129.5,126.8,117.1,114.4,108.5,69.5,68.9,68.3,52.2,48.8,47.4,42.1,41.9,18.5,13.3。
[2571]
实施例77:[4,29-二甲基-25,25-二氧代-19,24-二氧杂-25λ
6-硫杂-1,14,15,16-四氮杂六环[18.5.3.1
3,7
.1
9,13
.0
12,16
.0
23,27
]三十碳-3(30),4,6,9(29),10,12,14,20,22,27-十烯-8-基]乙酸
[2572][2573]
步骤1:[4,29-二甲基-25,25-二氧代-19,24-二氧杂-25λ
6-硫杂-1,14,15,16-四氮杂六环[18.5.3.1
3,7
.1
9,13
.0
12,16
.0
23,27
]三十碳-3(30),4,6,9(29),10,12,14,20,22,27-十烯-8-基]乙酸乙酯的制备
[2574]
将3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}-3-[1-(2-羟基乙基)-4-甲基-1h-苯并三唑-5-基]丙酸乙酯(1eq.,320mg,0.5512mmol)溶于thf(60ml)并加入pph3(2eq.,289mg,1.10mmol)。将diad(2eq.,0.217ml,222.86mg,1.1mmol)加入到搅拌中的溶液中并将反应混合物于70℃搅拌2小时。将混合物减压浓缩并将残余物通过反相色谱纯化,用5mm nh4hco3水溶液-mecn梯度洗脱得到标题化合物(230mg,74%收率),为白色固体泡沫。
[2575]1h-nmr(500mhz,dmso-d6)δppm:7.79(d,1h),7.51(dd,1h),7.36(d,1h),7.3(d,1h),6.92(d,1h),6.87(dd,1h),5.89(d,1h),5.88(d,1h),5.15/5.04(m+m,2h),4.79(dd,1h),4.68/4.33(m+m,2h),4.15/3.54(d+d,2h),3.98/3.69(d+d,2h),3.94/3.91(m+m,2h),3.43/3.04(dd+dd,2h),2.61(s,3h),2.29(s,3h),0.99(t,3h)。
[2576]
步骤2:实施例77的制备
[2577]
采用通用方法12,用[4,29-二甲基-25,25-二氧代-19,24-二氧杂-25λ
6-硫杂-1,14,15,16-四氮杂六环[18.5.3.1
3,7
.1
9,13
.0
12,16
.0
23,27
]三十碳-3(30),4,6,9(29),10,12,14,20,22,27-十烯-8-基]乙酸乙酯(1eq.,265mg,0.4710mmol)作为反应试剂,得到标题化合物(175mg,69%收率)。
[2578]
通过手性柱色谱分离得到对映体纯产物。
[2579]
实施例77a(e1)
[2580]c27h26
n4o6s的hrms计算值:534.1573;[m+h]
+
,实测值:535.1646(δ=0.0ppm)。
[2581]
实施例77b(e2)
[2582]c27h26
n4o6s的hrms计算值:534.1573;[m+h]
+
,实测值:535.1646(δ=0.0ppm)。
[2583]1h-nmr(500mhz,dmso-d6)δppm:12.21(brs,1h),7.79(d,1h),7.51(dd,1h),7.34(d,1h),7.3(d,1h),6.92(d,1h),6.87(dd,1h),5.88(d,1h),5.88(d,1h),5.15/5.03(m+m,2h),4.77(t,1h),4.67/4.34(m+m,2h),4.14/3.55(d+d,2h),3.97/3.7(d+d,2h),3.31/2.94
(dd+dd,2h),2.6(s,3h),2.29(s,3h)。
[2584]
13
c-nmr(125mhz,dmso-d6)δppm:132.2,131.2,127.8,127.1,118.9,116.4,115.7,109.8,69.8,51.6,49.2,48,40.1,40,18.1,13.1。
[2585]
实施例78:[4,32-二甲基-28,28-二氧代-19,22,27-三氧杂-28λ
6-硫杂-1,14,15,16-四氮杂六环[21.5.3.1
3,7
.1
9,13
.0
12,16
.0
26,30
]三十三碳-3(33),4,6,9(32),10,12,14,23,25,30-十烯-8-基]乙酸
[2586][2587]
步骤1:3-(3-{[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-甲基苯基)-3-(1-{2-[2-(苄氧基)乙氧基]乙基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯的制备
[2588]
采用通用方法7,用3-(1-{2-[2-(苄氧基)乙氧基]乙基}-4-甲基-1h-苯并三唑-5-基)-3-[3-(羟基甲基)-4-甲基苯基]丙酸乙酯(1eq.,2.19g,4.12mmol)和6-(苄氧基)-3,4-二氢-2h-1,2λ6,3-噁噻嗪-2,2-二酮(1.2eq.,1.44g,4.94mmol)作为起始试剂,得到标题化合物(2.604g,79%收率)。
[2589]1h-nmr(500mhz,dmso-d6)δppm:(m,5h),(m,5h),7.6(d,1h),7.43(d,1h),7.21(d,1h),7.16(dd,1h),7.14(d,1h),7.11(d,1h),7.07(dd,1h),6.95(d,1h),5.1(s,2h),4.83(t,1h),4.78(t,2h),4.43/4.39(d+d,2h),4.28(s,2h),4.21/4.18(d+d,2h),3.91(q,2h),3.86(t,2h),3.49(m,2h),3.4(m,2h),3.17/3.11(dd+dd,2h),2.75(s,3h),2.2(s,3h),0.98(t,3h)。
[2590]
步骤2:3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)甲基]-4-甲基苯基}-3-{1-[2-(2-羟基乙氧基)乙基]-4-甲基-1h-苯并三唑-5-基}丙酸乙酯的制备
[2591]
采用通用方法8,用3-(3-{[6-(苄氧基)-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基]甲基}-4-甲基苯基)-3-(1-{2-[2-(苄氧基)乙氧基]乙基}-4-甲基-1h-苯并三唑-5-基)丙酸乙酯(1eq.,2.60mg,3.23mmol)作为起始试剂,得到标题化合物(2.604g,79%收率)。
[2592]1h-nmr(500mhz,dmso-d6)δppm:9.71(s,1h),7.63(d,1h),7.49(d,1h),7.23(d,1h),7.19(dd,1h),7.13(d,1h),6.99(d,1h),6.79(dd,1h),6.61(d,1h),4.84(t,1h),4.8(t,2h),4.54(m,1h),4.4/4.36(d+d,2h),4.22/4.17(d+d,2h),3.94(q,2h),3.88(t,2h),3.38(m,2h),3.37(m,2h),3.17(m,2h),2.76(s,3h),2.22(s,3h),1.01(t,3h)。
[2593]
步骤3:[4,32-二甲基-28,28-二氧代-19,22,27-三氧杂-28λ
6-硫杂-1,14,15,16-四氮杂六环[21.5.3.1
3,7
.1
9,13
.0
12,16
.0
26,30
]三十三碳-3(33),4,6,9(32),10,12,14,23,25,30-十烯-8-基]乙酸乙酯的制备
[2594]
采用通用方法7,用3-{3-[(6-羟基-2,2-二氧代-2h-1,2λ6,3-噁噻嗪-3(4h)-基)
甲基]-4-甲基苯基}-3-{1-[2-(2-羟基乙氧基)乙基]-4-甲基-1h-苯并三唑-5-基}丙酸乙酯(1eq.,2.10mg,3.36mmol)作为反应试剂在120ml/mmol thf中进行反应,得到标题化合物(1.65g,81%收率)。1h-nmr(500mhz,dmso-d6)δppm:(m,6h),7.73(d,1h),7.44(d,1h),7.43(dd,1h),7.25(d,1h),7.06(d,1h),6.92(dd,1h),6.81(d,1h),6.46(d,1h),4.84(m,2h),4.81(t,1h),4.27/4.06(d+d,2h),4.15/4.07(d+d,2h),3.88(q,2h),3.08/3.03(dd+dd,2h),2.67(s,3h),2.32(s,3h),0.97(t,3h)。
[2595]
步骤4:实施例78的制备
[2596]
采用通用方法12,用[4,32-二甲基-28,28-二氧代-19,22,27-三氧杂-28λ
6-硫杂-1,14,15,16-四氮杂六环[21.5.3.1
3,7
.1
9,13
.0
12,16
.0
26,30
]三十三碳-3(33),4,6,9(32),10,12,14,23,25,30-十烯-8-基]乙酸乙酯(1eq.,1.645g,2.72mmol)作为起始试剂,得到标题化合物(83%收率)。
[2597]
通过手性柱色谱分离得到对映体纯产物。
[2598]
实施例78a(e1)
[2599]c29h30
n4o7s的hrms计算值:578.1835;[m+h]
+
,实测值:579.1915(δ=1.2ppm)。
[2600]
实施例78b(e2)
[2601]c29h30
n4o7s的hrms计算值:578.1835;[m+h]
+
,实测值:579.1917(δ=1.6ppm)。
[2602]1h-nmr(500mhz,dmso-d6)δppm:12.28(brs,1h),7.72(d,1h),7.43(dd,1h),7.42(d,1h),7.25(d,1h),7.06(d,1h),6.92(dd,1h),6.78(d,1h),6.44(d,1h),4.85/4.82(m+m,2h),4.79(t,1h),4.25/4.05(d+d,2h),4.15/4.06(d+d,2h),4.03/3.98(m+m,2h),4(m,2h),3.8/3.74(m+m,2h),2.93(d,2h),2.66(s,3h),2.32(s,3h)。
[2603]
13
c-nmr(125mhz,dmso-d6)δppm:131.4,130.7,129.4,127.2,118.9,115.3,114.7,109,69.8,68.5,68.4,51.8,49,48.4,41.8,41.7,18.5,13.3。
[2604]
实施例79:2-[(8r)-4,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]-n-(嘧啶-5-基)乙酰胺和
[2605]
2-[(8s)-4,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]-n-(嘧啶-5-基)乙酰胺
[2606][2607]
在室温下向搅拌中的[(8r)-4,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸或[(8s)-4,31-二甲基-27,27-二氧代-21,26-二氧
杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸(1eq.,250mg,0.444mmol)的干燥dmf(3ml)溶液中加入1-[二(二甲基氨基)亚甲基]-1h-1,2,3-三唑并[4,5-b]吡啶翁3-氧化物六氟磷酸盐(1.48eq.,250mg,0.657mmol)和dipea(3.2eq.,0.25ml,1.4mmol)。将混合物在室温下搅拌3分钟,然后加入嘧啶-5-胺(2.37eq.,100mg,1.05mmol)并将混合物在室温下搅拌过夜。反应完成后将混合物过滤,将滤液用dmf稀释并通过反相色谱纯化,用水25mm nh4hco3溶液-mecn作为洗脱剂得到标题化合物(白色固体,48%收率)。
[2608]
实施例79a(8r)
[2609]c33h33
n7o5s的hrms计算值:639.2264;[m+h]
+
,实测值:640.2335(δ=-0.3ppm)。实施例79b(8s)
[2610]c33h33
n7o5s的hrms计算值:639.2264;[m+h]
+
,实测值:640.2332(δ=-0.7ppm)。
[2611]1h-nmr(500mhz,dmso-d6)δppm:10.45(s,1h),8.88(s,2h),8.83(s,1h),7.68(d,1h),7.52(dd,1h),7.43(d,1h),7.31(d,1h),7(d,1h),6.8(dd,1h),6.54(d,1h),5.82(d,1h),4.94(t,1h),4.78/4.73(m+m,2h),4.11/3.98(d+d,2h),3.99/3.87(d+d,2h),3.61/3.4(m+m,2h),3.24/3.11(dd+dd,2h),2.63(s,3h),2.33(s,3h),2.2/2.08(m+m,2h),1.82/1.62(m+m,2h)。
[2612]
13
c-nmr(125mhz,dmso-d6)δppm:153.5,147.4,131.5,131.3,128.4,127.4,119.6,117.5,111.2,108.1,67.9,51.9,48.8,48.3,42.7,41.7,26.7,25.5,18.5,13.5。
[2613]
实施例80:2-[(8s)-4,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]-n-(吡啶-3-基)乙酰胺和
[2614]
2-[(8r)-4,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]-n-(吡啶-3-基)乙酰胺
[2615][2616]
在室温下向搅拌中的[(8s)-4,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸或[(8r)-4,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]乙酸(1eq.,250mg,0.444mmol)的干燥dmf(3ml)溶液中加入1-[二(二甲基氨基)亚甲基]-1h-1,2λ6,3-三唑并[4,5-b]吡啶翁3-氧化物六氟磷酸盐(1.48eq.,250mg,0.657mmol)和dipea(3.2eq.,0.25ml,1.4mmol)。将混合物
在室温下搅拌3分钟,然后加入吡啶-3-胺(2.39eq.,100mg,1.06mmol)并将混合物在室温下搅拌过夜。反应完成后将混合物过滤,将滤液用dmf稀释并通过反相色谱纯化,用水25mm nh4hco3溶液-mecn作为洗脱剂得到标题化合物(白色固体,44%收率)。
[2617]
实施例80a(8s)
[2618]c34h34
n6o5s的hrms计算值:638.2311;[m+h]
+
,实测值:639.2382(δ=-0.3ppm)。
[2619]
实施例80b(8r)
[2620]c34h34
n6o5s的hrms计算值:638.2311;[m+h]
+
,实测值:639.2381(δ=-0.5ppm)。
[2621]1h-nmr(500mhz,dmso-d6)δppm:10.22(s,1h),8.6(s,1h),8.2(dd,1h),7.91(dm,1h),7.68(d,1h),7.53(dd,1h),7.42(d,1h),7.31(d,1h),7.27(m,1h),7(d,1h),6.8(dd,1h),6.53(d,1h),5.83(d,1h),4.94(t,1h),4.77/4.74(m+m,2h),4.1/3.98(d+d,2h),3.99/3.88(d+d,2h),3.62/3.41(m+m,2h),3.21/3.08(dd+dd,2h),2.63(s,3h),2.33(s,3h),2.2/2.07(m+m,2h),1.82/1.62(m+m,2h)。
[2622]
13
c-nmr(125mhz,dmso-d6)δppm144.6,141,131.4,131.3,128.4,127.4,126.4,124.1,119.5,117.5,111.2,108,67.8,51.9,48.8,48.3,42.8,41.7,26.7,25.5,18.5,13.4。
[2623]
实施例81:2-[4,31-二甲基-27,27-二氧化-21,26-二氧杂-27-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]-2-甲基-n-(嘧啶-5-基)丙酰胺
[2624][2625]
将搅拌中的2-[4,31-二甲基-27,27-二氧化-21,26-二氧杂-27-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]-2-甲基丙酸e1(1eq.,261mg,0.442mmol)或e2(1当量)的亚硫酰氯(310eq.,16.3g,10ml,0.137mol)溶液在n2气氛下于80℃加热1天。反应完成后,将混合物蒸发至干且不经进一步纯化直接使用。将粗酰氯溶于thf(5ml),然后加入dipea(44mg,0.442mmol)和嘧啶-5-胺(42mg,0.442mmol)并将混合物在室温下搅拌过夜。反应完成后将混合物直接通过反相色谱纯化,用5mm nh4hco3水溶液-mecn作为洗脱剂得到标题化合物(白色固体,收率分别为14%-15%)。
[2626]
实施例81a(e1)
[2627]c35h37
n7o5s的hrms计算值:667.2577;[m+h]
+
,实测值:668.2657(δ=1.1ppm)。
[2628]
实施例81b(e2)
[2629]c35h37
n7o5s的hrms计算值:667.2577;[m+h]
+
,实测值:668.2654(δ=0.7ppm)。
[2630]1h-nmr(500mhz,dmso-d6)δppm:9.71(brs.,1h),8.81(s,1h),8.76(s,2h),7.63(d,1h),7.57(d,1h),7.46(brd.,1h),7.29(d,1h),7.01(d,1h),6.81(dd,1h),6.67(brs.,1h),5.75(brs.,1h),5.03(s,1h),4.76/4.7(dm+dm,2h),4.43/3.75(brd+brd,2h),4.13/
3.57(brd+brd,2h),3.66/3.35(br+m,2h),2.65(brs.,3h),2.34(s,3h),2.18/2.06(m+m,2h),1.83/1.67(m+m,2h),1.38/1.23(s+s,6h)。
[2631]
13
c-nmr(125mhz,dmso-d6)δppm:176.9,153.8,149,133.2,131.2,130.8,128,119.6,117.7,110.8,107,67.9,52,52,48.8,48.2,47,26.8,26.2/24.1,25.6,18.5,14.2。
[2632]
实施例82:2-[4,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]-2-甲基-n-(吡啶-3-基)丙酰胺
[2633][2634]
将搅拌中的2-[4,31-二甲基-27,27-二氧代-21,26-二氧杂-27λ
6-硫杂-1,14,15,16-四氮杂六环[20.5.3.1
3,7
.1
9,13
.0
12,16
.0
25,29
]三十二碳-3(32),4,6,9(31),10,12,14,22,24,29-十烯-8-基]-2-甲基丙酸e1(1eq.,261mg,0.442mmol)或e2(1当量)的亚硫酰氯(310eq.,16.3g,10ml,0.137mol)溶液在n2气氛下于80℃加热1天。反应完成后,将混合物蒸发至干且不经进一步纯化直接使用。将粗酰氯溶于thf(5ml),然后加入dipea(44mg,0.442mmol)和吡啶-3-胺(42mg,0.443mmol)并将混合物在室温下搅拌过夜。反应完成后将混合物直接通过反相色谱纯化,用5mm nh4hco3水溶液-mecn作为洗脱剂得到标题化合物(白色固体,收率分别为41%-46%)。
[2635]
实施例82a(e1)
[2636]c36h38
n6o5s的hrms计算值:666.2625;[m+h]
+
,实测值:667.2697(δ=0.0ppm)。
[2637]
实施例82b(e2)
[2638]c36h38
n6o5s的hrms计算值:666.2625;[m+h]
+
,实测值:667.2700(δ=0.4ppm)。
[2639]1h-nmr(500mhz,dmso-d6)δppm:9.48(s,1h),8.51(d,1h),8.18(d,1h),7.75(d,1h),7.63(d,1h),7.57(d,1h),7.47(d,1h),7.29(d,1h),7.24(dd,1h),7.01(d,1h),6.81(dd,1h),6.65(br,1h),5.74(br,1h),5.05(s,1h),4.75/4.71(m+m,2h),4.43/3.74(d+d,2h),4.13/3.57(d+d,2h),3.66/3.34(m+m,2h),2.65(s,3h),2.34(s,3h),2.18/2.07(m+m,2h),1.83/1.67(m+m,2h),1.37(s,3h),1.22(s,3h)。
[2640]
13
c-nmr(125mhz,dmso-d6)δppm:176.4,156,146.6,144.9,144.6,142.8,139.4,136.4,135.9,135.6,133.3,131.8,131.8,131.2,130.7,128.7,128.3,128.1,123.8,119.6,117.7,117.1,110.8,107,67.9,52.1,51.8,48.8,48.2,46.9,26.8,26.3,25.6,24,18.6,14.2。
[2641]
实施例83:hepg2
–
基因报告测定
[2642]
nrf2转录因子将通过与抗氧化反应元件(are)的结合来激活保护基因免受氧化损伤。我们利用nrf2的转染因子特性开发了一种基因报告测定法,该测定基于在are和nrf2活化控制下的β内酰胺酶报告基因的活化。
[2643] are-bla hepg2细胞系(ref.k1208,invitrogen)含有稳定整合到hepg2细胞中的受抗氧化反应元件(are)控制的β-内酰胺酶报告基因。
[2644] are-bla hepg2细胞在dmem glutamax
tm
(ref.61965-026,thermo fisher)、10%透析的fbs(ref.p30-193306,panbiotech)、12mm hepes(ref.15630-056,gibco)、0.1mm非必需氨基酸(neaa)细胞培养补充剂(ref.11140-35,gibco)、1%丙酮酸钠(ref.s8636,sigma)、2.5μg/ml杀稻瘟菌素(ref.210-01,invitrogen)、1%青霉素/链霉素(15070-063,gibco)中、在胶原蛋白i(50μg/ml,ref.a10483-1,life technologies)包被的烧瓶中,在37℃,5%co2下生长至汇合。
[2645]
实验前18小时,使用tryple xpress(ref.126905,bibco)在37℃下收获细胞10分钟,重悬于dmem glutamax
tm
(ref.61965-026,thermo fisher)、1%透析的fbs(ref.p30-193306,panbiotech)、25mm hepes(ref.15630-056,gibco)、0.1mm neaa(ref.11140-35,gibco)、1%丙酮酸钠(ref.s8636,sigma)、2.5μg/ml杀稻瘟菌素(ref.210-01,invitrogen)、1%青霉素/链霉素(15070-063,gibco)中,然后以32μl中30000个细胞/孔的密度接种到384孔细胞培养微透明板(ref.781091,greiner)中。细胞在使用前储存在37℃、5%co2下。
[2646]
将100%dmso(0.315μl/孔)中的化合物重悬于20μl dmem glutamax
tm
、1%透析的fbs、25mm hepes、0.1mm neaa、1%丙酮酸钠(ref.s8636,sigma)、2.5μg/ml杀稻瘟菌素、3.4%dmso、1%青霉素/链霉素(15070-063,gibco)中。将化合物和作为阳性对照的穿心莲内酯(终浓度为10μm;ref.365645-500mg,aldrich)以8μl/孔分配到细胞上,然后在37℃和5%co2下孵育16小时。第二天将live blazer试剂(live blazer fret b/g(ccf4-am),ref.k1089,invitrogen)分配到细胞上(8μl/孔)并在室温下避光孵育2小时。
[2647]
然后,使用多模式阅读器(ex 409nm/em 460nm和530nm;envision,perkin elmer)测量荧光共振能量转移(fret)信号。数据在1%dmso(基础信号)和10μm穿心莲内酯(阳性信号)之间进行标准化,并使用activity base软件进行分析。
[2648]
实施例84:u2os
–
易位测定
[2649]
将u2os细胞使用mmlv衍生的逆转录病毒载体稳定转导,以在细胞核中过表达nrf2-酶供体融合蛋白和受体酶(u2os keap1-nrf2核易位细胞系,ref.93-0821c3,discoverx)。
[2650]
pathhunter u2os细胞在最低必需培养基(mem)(ref.30-2003,atcc)、10%fbs(ref.p30-193306,panbiotech)、500μg/ml遗传霉、250μg/ml潮霉素、0.25μg/ml嘌呤霉素(分别为10131-027、10687-010和ref.a1113802,life technologies)中生长。
[2651]
实验前一天晚上,使用tryple xpress(ref.126905,bibco)在37℃下收获细胞5分钟,重悬于opti-mem
tm
(ref.31985-047,gibco)、1%fbs(ref.p30-193306,panbiotech),然后以20μl中7500个细胞/孔的密度接种到384孔板(ref.6007680,perkin elmer中。细胞在37℃、5%co2下储存过夜,直至使用。
[2652]
将100%dmso(0.315μl/孔)中的化合物重悬于20μl mem、1%fbs、3.4%dmso中。将化合物和作为阳性对照的穿心莲内酯(终浓度为10μm;ref.365645-500mg,aldrich)以5μl/孔分配到细胞上,然后在37℃和5%co2下孵育3小时。孵育后,将path hunter试剂分配到细胞上(12μl/孔,ref.93-0001,discoverx),室温避光孵育60分钟。
[2653]
然后,使用多模式阅读器(pherastar,bmg labtech)测量发光信号。数据在1%dmso(基础信号)和10μm穿心莲内酯(阳性信号)之间进行标准化,并使用activity base软件进行分析。
[2654]
[2655]
[2656]
[2657]
[2658][2659]
实施例85:表面等离子共振
[2660]
使用cm5芯片在biacore t200(ge healthcare)上在25℃下通过表面等离子共振(spr)进行与keap1的kelch结构域的结合测定。从novalix(批次pu-p01)获得的his-thromb-keap1(a321-c624)使用标准向导协议通过胺偶联共价固定,浓度为20μg/ml在ph 5.5的乙酸钠中。捕获配体直到达到1250ru。使用胺空白作为参考流动池。实时监测分析物与配体的结合,结合时间为180秒,解离时间为720秒。使用biacore t200评估软件(ge healthcare)对结合(ka)和解离(kd)速率进行简单的1:1动力学相互作用模型的拟合。从这些拟合参数计算平衡常数(kd=kd/ka)。在实验中,在单循环动力学(sck)中将半对数稀释的化合物注射到keap1上,每个循环5个递增的浓度,分别为0.316、1、3.16、10和31.6nm。使用10mm hepes(ph 7.4)、150mm nacl、3mm edta、1mm tcep、0.05%p20、5%dmso的运行缓冲液以50μl/min的流速进行biacore结合测定。采用双重减法,减去参考流动池和前一个空白循环(使用运行缓冲液)。应用溶剂校正来校正dmso体效应。
[2661]
[2662]
[2663]
[2664][2665]
实施例86:靶向参与研究(target engagement study)
[2666]
在喂食的db/db小鼠(8周大,janvier labs)中评估靶向参与作用。口服给药30和/或100mg/kg(10ml/kg,在hec 1%中)剂量的化合物或载体。小鼠麻醉后,在给药后4、6和24小时采集血液和肝脏样本。在每个时间点测定血浆和肝脏中的化合物浓度。通过治疗小鼠与对照小鼠相比肝脏中nqo1基因表达的增加来测量化合物对nrf2的激活。
[2667]
实施例87:口服葡萄糖耐量试验研究(ogtt)
[2668]
在ob/ob小鼠(10周,janvier labs)中评估了化合物对葡萄糖耐量的功效。化合物以30和/或100mg/kg(10ml/kg,在hec 1%中)给药10天。最后一次给药后,小鼠立即禁食4小时。然后进行口服葡萄糖耐量试验,测量葡萄糖给药(1.5g/kg,10ml/kg,在水中)前和给药后不同时间点的血糖和血浆胰岛素水平。然后随意给小鼠提供食物。在ogtt后的第二天,处死小鼠并取出肝脏。然后通过测量化合物治疗小鼠与对照小鼠相比肝脏中nqo1基因表达的增加来确认靶向参与。
[2669]
实施例88:使用mcd模型的nash效果研究
[2670]
使用通过甲硫氨酸和胆碱缺乏(mcd)饮食诱导的nash小鼠模型评估化合物在nash中的功效。化合物治疗和通过饮食诱导nash同时开始。将小鼠置于mcd饮食下并立即开始用化合物治疗14天。对小鼠称重并口服给予化合物(10ml/kg,在hec 1%中)。经过14天的治疗和饮食后,禁食4小时的小鼠被安乐死。获得血样用于肝酶测定(丙氨酸氨基转移酶(alt)和天冬氨酸氨基转移酶(ast))。取肝脏进行nash分析和靶向参与测量。定量肝甘油三酯含量。nash通过脂肪变性、炎症的测量和nafld活动评分(nas)的量化来确定。然后通过测量化合物治疗小鼠与对照小鼠相比肝脏中nqo1基因表达的增加来确认靶向参与。
[2671]
实施例89:adpkd的效果研究
[2672]
为了评估nrf2激活剂的功效,我们使用最初描述的条件性和诱导型pkd1基因缺陷小鼠(lantinga-van leeuwen等人,hum mol genet.2007,16(24),3188-96)。在向10天大的小鼠(p10)注射他莫昔芬后,肾上皮细胞中的pkd1基因被特异性缺失。这导致肾单位远端囊肿形成的快速进展。然后小鼠通过管饲法接受测试分子(3至30mg/kg/d)或载体(羟乙基纤
维素1%)2至3周。在治疗结束时,处死所有小鼠并收集血浆和肾脏。血浆样本用于监测研究结束时的药物暴露。按照之前的描述(lu等人,sci.transl.med.12,eaba3613(2020)2020年7月29日,“activation of nrf2 ameliorates oxidative stress and cystogenesis in autosomal dominant polycystic kidney disease”),通过量化治疗对肾脏大小、肾脏重量、肾脏重量与体重比、囊性指数(通过组织学分析确定)和作为肾功能指标的尿体积的影响来确定疗效。nrf2靶向参与可以通过测量nrf2靶基因激活(例如nqo1)或使用标准检测试剂盒直接量化肾脏中的活性氧(ros)来监测。
[2673]
实施例90:药物组合物
[2674]
制备1000片每片含10mg的配方:
[2675]
实施例1至82之一的化合物...................................10g
[2676]
羟丙基纤维素..............................................2g
[2677]
小麦淀粉.................................................10g
[2678]
乳糖......................................................100g
[2679]
硬脂酸镁...................................................3g
[2680]
滑石.......................................................3g
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1