肝样细胞和人工肝组织的制备方法以及应用
发明领域本申请属于生物与新医药,具体地,涉及诱导多能干细胞分化为肝样细胞团的方法以及通过肝样细胞团制备人工肝组织的方法。
背景技术:
0、发明背景
1、肝脏是人体最重要的器官之一并承担着许多重要功能,而肝脏中的肝功能主要是由肝细胞所提供。在大多数肝病中,肝细胞逐渐减少并进一步导致肝衰竭,而肝移植是目前唯一有效的肝衰竭的治疗方式。然而由于肝脏供体数量有限,中国香港特别行政区每年约有40%的人在等待肝移植的过程中死亡。因此,尝试肝细胞移植疗法或构建人工肝组织作为肝移植的替代疗法具有重要的临床意义。除了临床需求,肝细胞也可用于体外药物代谢研究和药物毒理评价。药物性肝损伤是到达临床试验的许多药物的主要障碍,许多创新药因毒性问题而下架。这其中部分是由于用于评估药物肝损伤的体外细胞模型和小鼠毒性模型的限制。然而由于新鲜肝组织中分离的肝细胞数量有限,同时肝细胞在体外具有不可增殖的特点,因此目前工业上和临床上对于优质来源的肝细胞仍然有着迫切需求。
2、目前已经有研究表明多能干细胞可以用于肝方向的分化,然而大部分多能干细胞产生的肝样细胞仅仅表达胎儿肝细胞标志物同时缺乏主要的药物代谢酶细胞色素p450(cyp)活性。因此,迄今为止还没有人工分化的肝样细胞进入临床实验。因此,促进多能干细胞分化的不成熟的胎儿肝样细胞进一步分化为具有成体肝细胞特性的肝样细胞具有重要的临床意义。
3、肝细胞移植疗法的另一个挑战是植入的肝细胞在肝脏中难以留存,而利用成熟的肝样细胞构建人工肝组织从而帮助肝细胞在肝脏中定植是一种可能的解决办法。在传统的构建人工肝组织的方法中(如将干细胞接种到水凝胶或聚合物支架中),由于缺乏血管,营养交换会受到限制,因此构建的人工肝组织的大小具有局限性。虽然3d打印技术可以用于构建血管化的组织,但对用于打印的“生物墨水”(生物材料和细胞的混合物)有着极高要求,这限制了3d打印在构建可植入人体的组织中的应用。使用脱细胞支架也可以构建血管化的人工肝组织,但将细胞注入支架的过程繁琐,并且难以精确控制细胞的接种位置,因此难以建立功能性的血管网络。
4、鉴于可用于临床的成熟的肝样细胞和人工肝组织的缺乏,开发出新的能够产生大量成熟可用的肝样细胞的方法以及构建人工肝组织的方法对于肝脏临床医学和再生医学的研究有着重要的意义。
技术实现思路
0、发明概述
1、第一方面,本申请提供了将多能干细胞诱导为肝样细胞团的方法,其包括将多能干细胞封装在第一微凝胶中进行分化培养,产生具有成熟肝功能的肝样细胞团。
2、在第一方面的一些实施方案中,所述多能干细胞为胚胎干细胞或诱导性多能干细胞。
3、在第一方面的一些实施方案中,所述第一微凝胶包含胶原蛋白。
4、在第一方面的一些实施方案中,所述第一微凝胶的大小为80-120μm。
5、在第一方面的一些实施方案中,所述第一微凝胶包含10-20个所述多能干细胞。
6、在第一方面的一些实施方案中,所述培养的时间为至少17天。
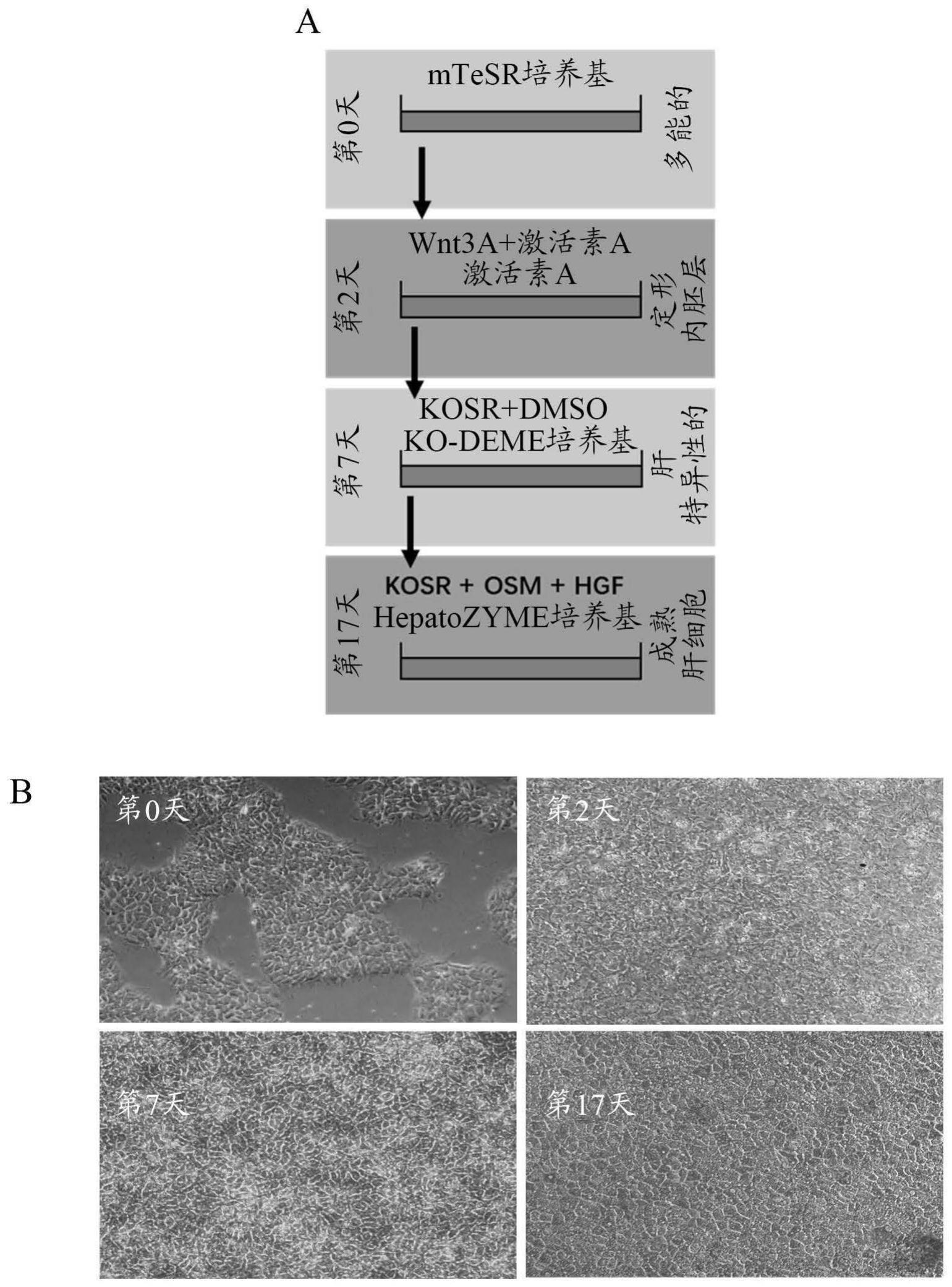
7、在第一方面的一些实施方案中,所述培养包括以下阶段:分化为定形内胚层的阶段;分化为肝母细胞团的阶段;以及肝母细胞团进一步分化和成熟的阶段。
8、第二方面,本申请提供了肝样细胞团,其通过第一方面所述的方法制备。
9、第三方面,本申请提供了人工肝组织的制备方法,其包括将通过第一方面所述的方法制备的肝样细胞团或第二方面所述的肝样细胞团与其它功能细胞封装在第二水凝胶中进行培养,得到所述人工肝组织。
10、第四方面,本申请提供了人工肝组织,其通过第三方面所述的方法制备。
11、第五方面,本申请提供了第二方面所述的肝样细胞团和第四方面所述的人工肝组织在制备用于治疗肝脏相关疾病的产品、药物筛选、毒性测定或再生医学中的用途。
技术特征:
1.将多能干细胞诱导为肝样细胞团的方法,其包括将多能干细胞封装在第一微凝胶中进行分化培养,得到所述肝样细胞团。
2.如权利要求1所述的方法,其中所述多能干细胞为胚胎干细胞或诱导性多能干细胞。
3.如权利要求1或2所述的方法,其中所述第一微凝胶包含胶原蛋白,优选为ⅰ型、ⅱ型、ⅲ型、ⅴ型或ⅺ型胶原蛋白,更优选为ⅰ型胶原蛋白。
4.如权利要求1-3中任一项所述的方法,其中所述第一微凝胶的大小为80-120μm,优选为约100μm;和/或
5.如权利要求1-4中任一项所述的方法,其中所述培养的时间为至少17天。
6.如权利要求1-5中任一项所述的方法,其中所述培养包括以下阶段:
7.肝样细胞团,其通过权利要求1-6中任一项所述的方法制备;
8.人工肝组织的制备方法,其包括将通过权利要求1-6中任一项所述的方法制备的肝样细胞团或权利要求7所述的肝样细胞团与其它功能细胞封装在第二水凝胶中进行培养,得到所述人工肝组织;
9.人工肝组织,其通过权利要求8所述的方法制备。
10.权利要求7所述的肝样细胞团或权利要求9所述的人工肝组织在制备用于治疗肝脏相关疾病的产品、药物筛选、毒性测定或再生医学中的用途。
技术总结
本申请提供了将多能干细胞诱导为肝样细胞团的方法,其包括将多能干细胞封装在第一微凝胶中进行分化培养,得到所述肝样细胞团。本申请还提供了人工肝组织的制备方法,其包括将通过上述方法制备的肝样细胞团与其它功能细胞封装在第二水凝胶中进行培养,得到所述人工肝组织。本申请还提供了通过上述方法制备的肝样细胞团和人工肝组织及其用途。
技术研发人员:陈汉辉,邓帅
受保护的技术使用者:香港中文大学
技术研发日:
技术公布日:2024/1/13
- 还没有人留言评论。精彩留言会获得点赞!