一种具有镇痛作用的双酯型二萜生物碱、制备方法与应用
1.本发明属于中药利用技术领域,进一步属于中药活性成分分离提取技术领域,具体涉及一种具有镇痛作用的来源于乌头属植物黄草乌的具有镇痛作用的双酯型二萜生物碱、制备方法与应用。
背景技术:
2.1986年国际疼痛研究学会定义疼痛为:与组织损伤或潜在的组织损伤相关的一种不愉快的感觉和情感经历。值得注意的是,大多数疾病都会引起疼痛,而急性疼痛随病程的延长有可能转变为慢性疼痛,因此病理性疼痛多为慢性疼痛。
3.慢性疼痛是一个已达到流行病程度的全球性问题。据国际疼痛研究学会统计全球每5个成年人中就有1人受疼痛困扰,每年还有10%的人被诊断为慢性疼痛,其中有17%的患者因不堪忍受而自杀。引起慢性疼痛的原因多样,且引发机制仍有待深入了解。临床常用的镇痛药物多有副作用,如阿片类成瘾性强,且易产生耐受,导致药物滥用;非甾体类具有多脏器损害、消化道溃疡、过敏等副作用。目前对于疼痛的产生机制研究发现疼痛的产生主要与神经系统中枢可塑性变化和外周初级感觉神经元的异位传入电活动有关。同时,与外周初级感觉神经元有密切联系的胶质细胞、血管内皮细胞、免疫细胞及细胞分泌的各类因子都会参与慢性疼痛的发生过程。来自损伤性外周致敏感受器和神经病变轴突的传入电活动(称为异位传入电活动)会导致以痛觉过敏和痛性感觉异常为特征的慢性疼痛,两者机制接近。
4.乌头属植物为传统中医包括民族民间习用的镇痛药,常用于癌痛、神经痛、关节炎性疼痛。但乌头属植物毒性较强,不当使用常引发心脏骤停、休克等严重副反应。乌头属植物主要的活性成分为二萜生物碱。近年来,科技人员试图从乌头属植物来源的二萜生物碱中筛选具有良好镇痛作用且毒性较小的二萜生物碱用于开发新型镇痛药物,但是进展比较缓慢,并没有得到临床应用效果明显优于常用的草乌甲素,且毒性更低的生物碱类新药物资源。
5.黄草乌为云南习用的乌头属植物,目前在云南种植面积较大,在云南红药、虎力散、肿痛气雾剂等云南著名的伤科药物中作为处方药材应用。经研究发现,黄草乌中富含黄草乌碱甲、乙、丙、丁和滇乌碱等二萜生物碱成分。而黄草乌碱甲在多种疼痛模型中表现出的镇痛活性较高,且毒性也低于目前上市的草乌甲素(文献报道草乌甲素小鼠灌胃给药的ld
50
为4.06mg/kg)。
技术实现要素:
6.本发明的目的在于提供一种具有镇痛作用的双酯型二萜生物碱;进一步的目的在于提供一种具有镇痛作用的双酯型二萜生物碱的制备方法;更进一步的目的在于提供具有镇痛作用的双酯型二萜生物碱之黄草乌碱甲的(va)的应用。
7.本发明的第一目的是这样实现的,所述具有镇痛作用的双酯型二萜生物碱,所述
双酯型二萜生物碱来源于毛莨科乌头属植物黄草乌的黄草乌碱甲(vilmorrianine a,va),其分子量为643;结构式为:所述黄草乌碱甲(va)具有镇痛作用,在大鼠福尔马林致痛模型急性疼痛期、慢性疼痛期均具有镇痛作用;在大鼠神经结扎致神经病理性疼痛模型(snl)中和大鼠完全弗氏佐剂致急慢性炎性疼痛模型(cfa)中对神经病理性疼痛、炎性疼痛均有镇痛效果,且在神经病理性疼痛模型中,黄草乌碱甲长期给药不产生耐受性,与吗啡合用不产生交叉耐受,与吗啡合用镇痛效果有叠加或协同作用。
8.所述黄草乌碱甲(va)作为生物碱药物之毒性低于已上市乌头生物碱类药物草乌甲素。小鼠灌胃给药急性毒性的半数致死量,ld50=7.1491mg/kg,95%可信使用限量范围为5.6881~8.9814mg/kg。
9.本发明进一步的目的是这样实现的,所述的具有镇痛作用的双酯型二萜生物碱的提取方法,所述双酯型二萜生物碱通过下列工艺步骤获得:(1)原料处理:以黄草乌干燥块根为原料,粉碎后加入原料3-5质量倍的甲醇室温浸泡4-6次,每次24-48h,将提取液合并减压浓缩后得到浸膏;(2)提取:将总浸膏分散到其3质量倍的水中,用氯仿进行萃取7-8次后,所得萃取液减压回收溶剂,得到总生物碱浸膏;(3)分离:总生物碱浸膏经硅胶柱层析分离,以石油醚-丙酮系统(100:1-1:1)为洗脱剂洗脱,每500毫升收集流份,通过薄层层析检识(条件:石油醚-丙酮1.5:1,氨蒸汽饱和20分钟,碘化铋钾显色),合并为fr.a-i。其中fr.c(比移值0.5-0.6之间的斑点)进一步经氧化铝柱层析,以石油醚-丙酮系统(95:1-10:1)为洗脱剂,每250毫升收集流份,以薄层层析条件检识(石油醚-丙酮1.5:1,氨蒸汽饱和20分钟,碘化铋钾显色),分为fr.c1-9。
10.(4)纯化:流份fr.c7(比移值在0.5附近的一个主要斑点)经硅胶柱层析进一步纯化,以石油醚-丙酮系统(80:1-20:1)为洗脱剂洗脱,得到化合物黄草乌碱甲(va)。
11.本发明更进一步的目的是这样实现的,所述双酯型二萜生物碱之黄草乌碱甲(va)在制备治疗神经病理性疼痛、炎性疼痛药物中的应用;所述双酯型二萜生物碱之黄草乌碱甲(va)作为化学镇痛药物中的应用。
12.本发明从毛莨科乌头属植物黄草乌中获取了一种双酯型二萜生物碱之黄草乌碱甲(vilmorrianinea,va),研究证明黄草乌碱甲(va)毒性小于已上市的乌头类生物碱草乌甲素,对于急、慢性疼痛均有明显的镇痛药效,可用于炎性痛、神经病理性疼痛,且长期使用不产生自身耐受性,与经典镇痛药吗啡合用有叠加或协同作用,其毒性显著低于已上市乌头生物碱类药物,可以作为一种新型生物碱类药物,具有巨大的临床应用价值,潜在的社会效益、经济效益显著。
附图说明
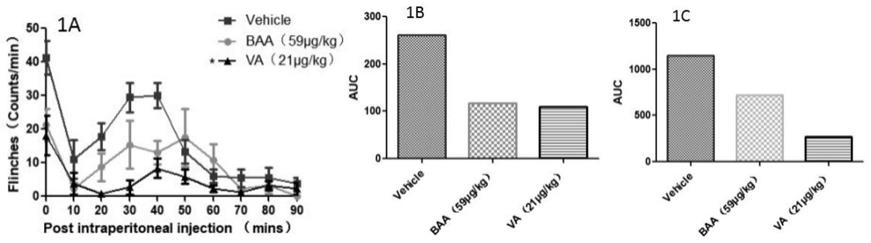
13.图1为黄草乌碱甲在大鼠福尔马林致痛模型中的镇痛效果。其中1a为注射福尔马林后0-90min不同化合物对大鼠疼痛行为发生次数的影响;1b注射福尔马林后0-10min急性疼痛期不同化合物镇痛作用曲线下面积;1c为注射福尔马林后10-90min急性疼痛期不同化合物镇痛作用曲线下面积。根据曲线下面积计算得出黄草乌碱甲的急慢性镇痛率,计算公式为(生理盐水组曲线下面积-给药组曲线下面积)*100/生理盐水组曲线下面积。
14.图2为黄草乌碱甲在大鼠神经结扎致神经病理性疼痛模型中的镇痛效果。
15.图3为黄草乌碱甲在大鼠完全弗氏佐剂致急性炎性疼痛模型中的镇痛效果。其中3a为不同化合物的机械痛抑制效果;3b为不同化合物的热辐射痛抑制效果。
16.图4为黄草乌碱甲在大鼠完全弗氏佐剂致慢性炎性疼痛模型中的镇痛效果。其中4a为不同化合物的机械痛抑制效果;4b为不同化合物的热辐射痛抑制效果。
具体实施方式
17.下面结合与实施例对本发明作进一步的说明,但不以任何方式对本发明加以限制,基于本发明的技术教导所作的任何变换或替换,均属于本发明的保护范围。
18.本发明所述具有镇痛作用的双酯型二萜生物碱,所述双酯型二萜生物碱来源于毛莨科乌头属植物黄草乌的黄草乌碱甲(vilmorrianinea,va),其特性通过下列获得或实现。
19.实施例1,所述双酯型二萜生物碱之黄草乌碱甲的ld50按如下方式获得:(1)动物分组:取昆明种小鼠80只,雌雄各半,分为8组,溶媒对照组(vehicle)、黄草乌碱甲(va)2.45mg/kg、3.5mg/kg、5mg/kg、7.14mg/kg、10.10mg/kg、14.58mg/kg、20mg/kg组,每组10只;(2)实验方法:不同浓度剂量组等体积分别灌胃给药1次,溶媒对照组给予生理盐水。观察给药后各组动物的急性毒性反应和死亡情况,连续14天。对观察期死亡的动物和观察期结束后处死的动物进行解剖,肉眼检查各组织脏器的体积、颜色、质地等有无异常。根据各组动物死亡率,用bliss法计算黄草乌碱甲ld50;(3)ld50计算:黄草乌碱甲(va)的主要中毒表现为痉挛、抽搐、呛咳、呃逆、呕吐和大小便失禁。解剖未见明显的内脏异常现象,应主要为神经或肌肉毒性;黄草乌碱甲(va)给药后小鼠的死亡时间在1-2h内,部分延迟至24h。计算得到黄草乌碱甲ld50为7.1491mg/kg,95%可信限为5.6881-8.9814mg/kg。
20.实施例2,所述双酯型二萜生物碱之黄草乌碱甲(va)对大鼠福尔马林致痛模型的镇痛作用,具体通过下述工艺验证:(1)动物分组:wistar雄性大鼠18只,随机分为3组,溶媒对照组(vehicle)、草乌甲素组(baa)、黄草乌碱甲(va)组,每组6只;(2)模型构建:以腹腔注射的方式给药,baa组剂量为59μg/kg,va组剂量为21μg/kg,vehicle组给予黄草乌碱甲(va)的配置溶媒,给药后在大鼠右侧足部皮下注射5%的福尔马林溶液50μl;注射后立刻将大鼠放入有机玻璃盒内,记录大鼠在注射福尔马林后0,10,20,30,40,50,60,70,80和90min时的疼痛行为次数;将注射5%福尔马林后可产生二相疼痛,分为急性期(0~10minⅰ相)与慢性期(10~90minⅱ相),用于考察黄草乌碱甲的初步镇痛作用;
(3)作用效果:图1示出了黄草乌碱甲在大鼠福尔马林致痛模型中的镇痛效果。vehicle组大鼠在注射福尔马林溶液后表现出明显的急性疼痛反应(0~10min)和慢性疼痛反应(10~90min);而baa组和va组大鼠的疼痛行为次数有一定降低,且va组慢性疼痛期(10-90min)镇痛效果强于baa组;图1b为0-10min急性疼痛期的镇痛效果曲线下面积,计算出黄草乌碱甲(va)急性镇痛率为57.98%;图1c为10-90min慢性疼痛期的镇痛效果曲线下面积,计算出其黄草乌碱甲(va)慢性镇痛率为76.16%。
21.实施例3,所述黄草乌碱甲(va)在大鼠神经结扎致神经病理性疼痛模型中的镇痛作用,具体通过下述工艺验证:(1)动物分组:wistar雄性大鼠,在神经结扎术后第14天选择机械痛阈值《10g的24只动物纳入实验,随机分为4组,溶媒对照组(vehicle)、草乌甲素组(baa)、黄草乌碱甲(va)组和吗啡(morphine)+va组,每组6只;(2)模型构建:除吗啡以皮下注射方式给药,其余化合物和溶媒以腹腔注射方式给药,baa组剂量为21μg/kg,va组剂量为15μg/kg,morphine+va组吗啡剂量为7mg/kg,每日注射一次,vehicle组给予黄草乌碱甲(va)的配置溶媒,除吗啡外其余药物均每日注射两次,两次给药间隔6h;每天在首次给药后1h使用电子测痛仪分别测定各组大鼠的造模侧(ipsilateral)和对侧(contralateral)足部的回避力度阈值;大鼠在神经结扎后,其造模侧足回避力度阈值在5g左右,而对侧足回避力度阈值在50g左右,说明神经病理性疼痛模型制作成功;(3)作用效果:图2示出了黄草乌碱甲在大鼠神经结扎致神经病理性疼痛模型中的镇痛效果。大鼠在神经结扎后,其造模侧足回避力度阈值在5g左右,而对侧足回避力度阈值在50g左右,说明神经病理性疼痛模型制作成功。vehicle组在给药的7天中,其两侧足回避力度阈值保持稳定;而va组和baa组动物造模侧足的回避力度阈值明显升高,且镇痛效果在给药的7天中保持稳定,但对侧足回避力度阈值与溶媒对照组相比没有差异(va组与vehicle组每日对比,连续7天差异p<0.001)。结果说明黄草乌碱甲(va)与草乌甲素的镇痛效果相当,且连续给药无自身耐受性;morphine+va组大鼠的造模侧足及对侧足的回避力度阈值均有一定升高,说明吗啡和黄草乌碱甲(va)合用时有一定的叠加或协同效应,且两者不会产生交叉耐受。图2中###表示baa组与vehicle组相比p<0.001,***表示va组与vehicle组相比p<0.001,^表示morphine+va组与vehicle组相比p<0.05,^^表示morphine+va组与vehicle组相比p<0.01,^^^表示morphine+va组与vehicle组相比p<0.001。
22.实施例4,所述黄草乌碱甲(va)在大鼠完全弗氏佐剂致急慢性炎性疼痛模型中具有镇痛作用,具体通过下述工艺验证:(1)动物分组:wistar雄性大鼠24只,随机分为3组,溶媒对照组(vehicle)、草乌甲素组(baa)、黄草乌碱甲(va)组,每组8只;(2)模型构建:
①
急性炎性疼痛模型构建:各组大鼠右后肢关节腔内注射完全弗氏佐剂(cfa)50μl造模,每日以腹腔注射的方式给药,baa组剂量为21μg/kg,va组剂量为21μg/kg,vehicle组给予黄草乌碱甲(va)的配置溶媒,连续给药7天;记录造模前(0d)和给药的第1d、3d、5d、7d大鼠患侧足和对侧足的热辐射回避潜伏时间和机械刺激回避力度阈值;
②
慢性炎性疼痛模型构建:各组大鼠右后肢关节腔内注射完全弗氏佐剂(cfa)50μ
l造模,造模第19天开始每日以腹腔注射的方式给药,baa组剂量为21μg/kg,va组剂量为21μg/kg,vehicle组给予黄草乌碱甲的配置溶媒,连续给药7天;记录造模前(0d)和给药的第1d、3d、5d、7d大鼠患侧足和对侧足的热辐射回避潜伏时间和机械刺激回避力度阈值;(3)作用效果:
①
图3示出了黄草乌碱甲在大鼠完全弗氏佐剂致急慢性炎性疼痛模型中的镇痛效果。大鼠注射cfa造模后,其造模侧足第一天的机械刺激回避力度阈值在12g左右,热辐射回避潜伏时间在2s左右,均显著低于造模前的基础值及对侧足,说明炎症急性模型造模成功;给予黄草乌碱甲后可明显升高急性炎性疼痛大鼠的机械痛阈值与热辐射痛阈值,且效果好于草乌甲素;
②
图4示出了黄草乌碱甲在大鼠完全弗氏佐剂致急慢性炎性疼痛模型中的镇痛效果。大鼠注射cfa造模后,疼痛持续,至第19天机械刺激回避力度阈值维持在20g左右,热辐射回避潜伏时间维持在5s左右,仍显著低于造模前及对侧足,说明炎症慢性模型造模成功。给予黄草乌碱甲(va)后可明显升高慢性炎性疼痛大鼠的热辐射痛阈值,效果好于草乌甲素。
23.图3和图4中#表示baa组与vehicle组相比p<0.05,##表示baa组与vehicle组相比p<0.01,###表示baa组与vehicle组相比p<0.001,*表示va组与vehicle组相比p<0.05,**表示va组与vehicle组相比p<0.01,***表示va组与vehicle组相比p<0.001。
24.实施例5,所述的具有镇痛作用的双酯型二萜生物碱的提取方法,具体通过下列工艺步骤获得:(1)原料处理:以黄草乌干燥块根为原料,粉碎后加入原料3-5质量倍的甲醇室温浸泡4-6次,每次24-48h,将提取液合并减压浓缩后得到浸膏;(2)提取:将总浸膏分散到其3质量倍的水中,用氯仿进行萃取7-8次后,所得萃取液减压回收溶剂,得到总生物碱浸膏;(3)分离:总生物碱浸膏经硅胶柱层析分离,以石油醚-丙酮系统为洗脱剂洗脱,收集流份,通过薄层层析检识,合并为fr.a-i。其中fr.c进一步经氧化铝柱层析,以石油醚-丙酮系统为洗脱剂,通过薄层层析检识,分为fr.c1-9。
25.(4)纯化:流份fr.c7经硅胶柱层析进一步纯化,以石油醚-丙酮系统为洗脱剂洗脱,得到化合物黄草乌碱甲(va)。
26.其中,所述的具有镇痛作用的双酯型二萜生物碱的提取方法,其特征在于:总生物碱浸膏经硅胶柱层析分离过程中的石油醚-丙酮系统为(100:1-1:1),收集流份体积为500毫升,薄层层析检识条件为石油醚-丙酮(1.5:1),氨蒸汽饱和20分钟,碘化铋钾显色,其中fr.c包含比移值0.5-0.6之间的斑点。
27.fr.c经氧化铝柱层析的石油醚-丙酮系统为(95:1-10:1),收集流份体积为250毫升,薄层层析检识条件为石油醚-丙酮(1.5:1),氨蒸汽饱和20分钟,碘化铋钾显色,其中fr.c7为比移值在0.5附近的一个主要斑点。
28.fr.c7合并浓缩后经过硅胶柱层析进一步纯化,石油醚-丙酮洗脱剂的体积比为80:1-20:1,得到化合物黄草乌碱甲(va)。
29.所述实施例中所用的材料、试剂等,如无特殊说明,均可从商业途径得到。
30.所述实施例中大鼠为wistar雄性大鼠(体重在130-250g范围内),为成都达硕实验动物有限公司的产品。
31.所述实施例中的吗啡(埃法生物)使用时按每1mg加入2.5μl浓盐酸和150μl的无水乙醇溶解,后使用无菌生理盐水稀释并调节至ph4-5后使用。福尔马林(solarbio)用生理盐水稀释至5%皮下注射使用。黄草乌碱甲自黄草乌中分离获得后按每1mg加入2.5μl浓盐酸和150μl的无水乙醇溶解,后使用无菌生理盐水稀释并调节至ph4-5后使用。
32.所述实施例通过记录福尔马林注射后动物的疼痛行为次数(抬脚、舔舐、抖动)、足底机械测痛仪、足底热辐射测痛仪测量动物对伤害性机械刺激和伤害性热刺激的反应三种方式衡量痛觉水平。在进行行为学实验前,首先使受试大鼠适应测试环境和测试方法,每次适应30min。
33.足底热辐射痛阈值检测:使用足底热辐射测痛仪(itclifescience公司)测试受试大鼠对伤害性热辐射刺激反应的潜伏期。实验中需保持周围环境安静,室温25℃。将大鼠置于透明、透气的有机玻璃盒内,玻璃隔板下方放置热辐射测痛仪,辐射强度为45℃,光源照射患侧和正常侧足底部位,记录大鼠足部出现收缩时测痛仪显示的时间(s)。以30秒为最大测量值,防止局部因热辐射受伤。每足需测定3次,每次测量间隔3min,3次测量的平均值即为大鼠该足的回避潜伏时间(pwl,pawwithdrawllatency)。
34.足底机械痛阈值检测:使用vonfrey电子测痛仪(itclifescience公司)测试受试大鼠对伤害性机械刺激反应的回避力度(g)。将大鼠放入透明、透气的有机玻璃盒内,底部为钢丝网。将测痛仪的纤维丝垂直触到大鼠足底部,记录大鼠足部出现收缩时测痛仪显示的力值。每足测量3次,每次测量间隔3min,3次结果的平均值即为大鼠的回避力度阈值(pwt,pawwithdrawthreshold)。
35.所述实施例中的实验结果均采用平均值
±
标准差的方式表示;行为学实验的统计方法采用两组间t检验,检验结果以p<0.05为差异有统计学意义。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1