一种结肠癌肿瘤患者菌群检测诊断营养不良状况的试剂盒的制作方法
1.本发明属于结肠癌患者体内菌群检测技术领域,具体涉及一种结肠癌肿瘤患者菌群检测诊断营养不良状况的试剂盒。
背景技术:
2.结肠癌是原发于结肠黏膜上皮的恶性肿瘤,结直肠癌患者一般有以下表现:1)排便异常:当结肠发生病变异常后,患者会出现腹泻、便秘等不正常的情况,严重时大便中带有血色;2)腹部疼痛:患有结肠癌的病程中,肿瘤会在肠腔内快速生长,进而使得肠腔受到阻塞,引起部分性肠梗阻或完全性肠梗阻,代谢物无法排泄,堆积在肠道中,出现严重的腹部疼痛;3)莫名恶心:肠道受到损伤刺激,出现恶心,腹部发胀等情况;4)营养不良:肿瘤生长需要消耗患者体内的能量,在加上癌细胞的不断刺激,使得患者消化功能和吸收功能变差;机体无法得到更多的养分,体重下降,还会出现头晕心悸等症状;
3.结肠癌患者出现营养不良可严重影响患者的预后和治疗耐受性,极大的降低肿瘤患者的生活质量;所以,对结肠癌患者的营养情况进行诊断并进行干预,对于肿瘤患者的治疗进程是十分重要的;目前对于结肠癌患者的营养情况进行诊断的方式主要为抽血、问诊、体检;如何构建一种准确,快速,无创的结肠癌患者营养情况诊断方式,是现在需要解决的问题。
技术实现要素:
4.为了解决上述技术问题,本发明提供了一种结肠癌肿瘤患者菌群检测诊断营养不良状况的试剂盒;发明人通过临床试验研究发现三种菌株与结肠癌患者营养情况具有直接和间接的相关性,通过这三种菌株的dna作为引物,制作成试剂盒,利用该试剂盒对结肠癌患者的粪便样本进行对应的三种菌株检测,通过菌株检测结果丰度,来诊断结肠癌患者的营养情况;
5.为了达到上述技术目的,本发明是通过以下技术方案实现的:一种结肠癌肿瘤患者菌群检测诊断营养不良状况的试剂盒,其特征在于,包括菌株的dna引物序列,所述菌株分别是:atopobium.vaginae、 selenomonassputigena、faecalibacteriumprausnitzii;三种菌株的dna 特异性引物序列如下:
6.1)atopobium.vaginae dna正向引物:
7.5'-ggtgaagcagtggaaacact-3'
8.atopobium.vaginae dna反向引物:
9.5'-attcgcttctgctcgcgca-3'
10.2)selenomonassputigena dna正向引物:
11.5'-agagtttgatcctggctcag-3'
12.selenomonassputigena dna反向引物:
13.5'-ctcaatattctcaagctcggtt-3'
14.3)faecalibacteriumprausnitziidna正向引物:
15.5'-cccggcatcgggtagag-3'
16.faecalibacteriumprausnitziidna反向引物:
17.5'-ggacgcgaggccatctc-3';
18.所述试剂盒还包括:粪便样本保存试剂、pcr反应试剂、pcr产物纯化试剂、测序反应试剂;
19.优选的,所述粪便样本保存试剂为dnahelper保护液,且粪便样本与dnahelper保护液的比例为1:2;
20.优选的,所述pcr反应试剂包括:10xpcr反应缓冲液、25mmdntp混合液、5u/ultaqdna聚合酶、20um引物对、ddh2o;
21.优选的,所述pcr产物纯化试剂包括:1u/ulsap酶、10u/ulexoi酶、ddh2o;
22.优选的,所述测序反应体系包括:25%bigdyemix1ul、3.2umdna测序引物、125mmedta溶液、100%乙醇溶液、70%乙醇溶液、hidi溶液、ddh2o;
23.优选的,所述dna测序引物序列如下:
24.atopobium.vaginaedna测序引物:
25.5'-ggtgaagcagtggaaacact-3';
26.selenomonassputigenadna测序引物:
27.5'-agagtttgatcctggctcag-3';
28.faecalibacteriumprausnitziidna测序引物:
29.5'-cccggcatcgggtagag-3';
30.优选的,所述atopobium.vaginae在经过测序后其所获得的结果与内参基因相比,超过2.98倍即表示患者可能存在中重度营养不良需要干预;selenomonassputigena的结果与内参基因相比,超过2.66倍即表示可能存在中重度营养不良;而faecalibacteriumprausnitzii的结果与内参基因相比,超过1.96倍即表示可能存在中重度营养不良。
31.本发明的有益效果是:
32.利用本发明提供的试剂盒,采集患者粪便样本,对粪便样本的dna进行提取,pcr扩增和产物纯化后,由试剂盒内与结肠癌营养情况相关的三种菌株dna测序序列对患者粪便关于三种菌株的dna进行测序后比对;根据患者体内三种菌株尤其是atopobium.vaginae的丰度来定性的诊断患者营养情况;利用该试剂盒实现了对结肠癌患者体内atopobium.vaginae、selenomonassputigena、faecalibacteriumprausnitzii菌群无创,准确检测,为结肠癌患者的营养状况检测提供了针对的新思路和方式。
附图说明
33.图1中a、b是roc曲线结合约登指数分析明确atopobium、selenomonas和faecalibacterium三个菌属的诊断性作用;
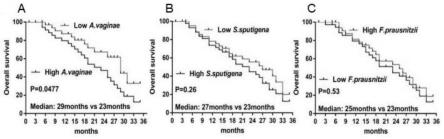
34.图2中a、b、c是通过cox回归分析探索atopobium、selenomonas和faecalibacterium下属菌种在患者总生存时间中的作用。
具体实施方式
35.下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有作出创造性劳动前提下所获得的所有其它实施例,都属于本发明保护的范围。
36.实施例1
37.不同营养状态下结肠癌肠道菌群探究;
38.营养状况评估方式及标准:通过pg-sga评估工具来评估营养状况,pg-sga包括病人自我评估部分(包括体重、食物摄入、症状、活动和身体功能)和医务人员评估部分(包括与营养有关的疾病状况、代谢状况和体检);定性评分的结果如下;0-1分为营养良好(pg-sga1), 2-3分为疑似营养不良(pg-sga2),4-8分为中度营养不良(pg-sga3),≥9分为严重营养不良(pg-sga4);
39.根据roc曲线来检查不同微生物群物种的分类和预测的诊断能力,结果如图1a、1b所示;得到结果显示,atopobium.vaginae、 selenomonassputigena及faecalibacteriumprausnitzii的作为诊断的精准性而言,atopobium.vaginae最高为13.5,selenomonassputigena及 faecalibacteriumprausnitzii分别为6.5和7.4,而准确性越高意味着诊断的特异性越强。
40.菌属选择:atopobium、selenomonas、faecalibacterium;
41.探究结果:根据roc结果,我们评估了这三个属的能力,以预测 crc的预后;在所考虑的三个物种中,即topobium vaginae(a. vaginae)、selenomonas sputigena(s.sputigena)和 faecalibacterium prausnitzii(f.prausnitzii),a.vaginae最有能力区分中重度营养不良状态,即pg-sga 3和pg-sga 4组(p《0.01); atopobium.vaginae在经过测序后其所获得的结果与内参基因相比,超过2.98倍即表示患者可能存在中重度营养不良需要干预。
42.selenomonassputigena的结果与内参基因相比,超过2.66倍即表示可能存在中重度营养不良。而faecalibacteriumprausnitzii的结果与内参基因相比,超过1.96倍即表示可能存在中重度营养不良。
43.实施例2
44.结肠癌肿瘤患者菌群检测诊断营养不良状况的试剂盒的使用:
45.1、抽提dna模板
46.对结肠癌患者粪便进行采样并保存于dnahelper保护液中,粪便样本与dnahelper保护液比例为1:2;抽提基因组dna。
47.2、pcr扩增反应
48.使用检测试剂盒中的pcr反应组件,其中含有下列引物对:
49.1)atopobium.vaginae dna正向引物:
50.5'-ggtgaagcagtggaaacact-3'
51.atopobium.vaginae dna反向引物:
52.5'-attcgcttctgctcgcgca-3'
53.2)selenomonassputigena dna正向引物:
54.5'-agagtttgatcctggctcag-3'
55.selenomonassputigenadna反向引物:
56.5'-ctcaatattctcaagctcggtt-3'
57.3)faecalibacteriumprausnitziidna正向引物:
58.5'-cccggcatcgggtagag-3'
59.faecalibacteriumprausnitziidna反向引物:
60.5'-ggacgcgaggccatctc-3';
61.pcr扩增的反应体系为:10
×
pcr反应缓冲液2.5μl;25mm的dntp混合液0.2μl、5u/ultaq酶0.125μl、dna模板1μl(12-15ng左右)、20um正向引物反向引物各0.25μl、ddh2o19.175μl;
62.在特定的反应条件参数下,对atopobium.vaginaedna、selenomonassputigenadna、faecalibacteriumprausnitziidna进行pcr扩增反应。
63.3、pcr扩增产物纯化
64.使用检测试剂盒中的pcr产物纯化组件,反应体系为总体积25ul,包含pcr产物20ul,1u/ulsap酶0.75ul,10u/ulexoi酶0.375ul,去离子水3.875ul;
65.在pcr扩增仪上进行反应,反应条件为37℃、15min,72℃、20min。
66.4、dna测序反应
67.使用检测试剂盒中的测序反应组件,其中,含有下列dna测序引物:
68.atopobium.vaginaedna测序引物:
69.5'-ggtgaagcagtggaaacact-3';
70.selenomonassputigenadna测序引物:
71.5'-agagtttgatcctggctcag-3';
72.faecalibacteriumprausnitziidna测序引物:
73.5'-cccggcatcgggtagag-3';
74.反应的体系为总体积5ul,包含pcr纯化产物1ul,25%bigdyemix1ul,3.2umdna测序引物1ul,去离子水2ul;
75.在pcr扩增仪上在特定条件下进行pcr扩增反应;
76.反应结束后加入125mmedta溶液1ul和100%乙醇溶液15ul,于室温下沉淀15min;在4℃,3600rpm/min的转速离心30min,轻轻倒去上清液;加入70%乙醇溶液30ul,3600rpm/min离心15min,轻轻倒去上清液;室温放置20min后加入hidi溶液8ul,放入测序仪中。
77.结果分析:在经过测序后其所获得的结果与内参基因相比,atopobium.vaginae超过2.98倍即表示患者可能存在中重度营养不良需要干预。selenomonassputigena超过2.66倍即表示可能存在中重度营养不良。而faecalibacteriumprausnitzii超过1.96倍即表示可能存在中重度营养不良。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1