一管法检测乙型肝炎病毒DNA的试剂盒及其应用的制作方法
一管法检测乙型肝炎病毒dna的试剂盒及其应用
技术领域
1.本发明涉及试剂盒技术领域,尤其涉及一管法检测乙型肝炎病毒dna的试剂盒及其应用。
背景技术:
2.目前应用于实时荧光定量pcr检测的dna提取方法主要有四种,即碱裂解法、煮沸裂解法、层析柱法和磁珠法。磁珠法提取dna是通过细胞裂解液裂解细胞,从细胞中游离出来的dna分子被特异的吸附到磁性颗粒表面,而蛋白质等杂质不被吸附,而留在溶液中。反应一定时间之后,再在磁场作用下,使磁性颗粒与液体分开,回收颗粒(即磁珠-dna混合物),再用洗脱液洗脱,从而得到纯净的dna。再将纯净dna加入到pcr反应液中进行荧光定量pcr反应。
3.目前常用的磁珠法提取的过程中所用的提取剂种类繁杂,有机溶剂的大量使用也容易对操作者带来伤害。且在整个洗脱过程中需要多步洗涤,才能够相对彻底地去除蛋白和盐分子,进而增加了整个实时荧光定量pcr检测过程的耗时,不仅增加了操作的工作量,还容易出现污染,进而影响最终的检测精度。此外,由于dna提取与pcr扩增不在同一载体中进行,在提取物转移的过程中操作不当也会影响最终的结果,并且洗涤次数的增加也容易导致的实验室污染以及dna丢失。
4.因此,如何开发一种在一管中实现dna的提取和扩增的试剂盒,通过引物探针的特异性序列来识别hbv的片段进行扩增,这样的好处是磁珠法提取的产物与pcr扩增在同一载体中进行,不需经过多次洗脱和洗涤导致的dna丢失,对提高临床检测质量具有重要意义。
技术实现要素:
5.本发明的目的在于提供一管法检测乙型肝炎病毒dna的试剂盒及其应用,本发明的提取试剂,使用磁珠法提取乙型肝炎病毒核酸(dna),将整体磁珠加入到反应液中进行荧光定量pcr检测,减少因为几次洗涤而带来的核酸丢失和间接的污染,大大提高检测的灵敏度,可以达到5iu/ml的最低检测限。
6.为了实现上述发明目的,本发明提供以下技术方案:本发明提供了一种乙型肝炎病毒dna定量检测试剂盒,所述试剂盒包括上游引物、下游引物、探针和乙型肝炎病毒dna提取液;所述上游引物的序列为:a-1:actgttcaagcctccaag;b-1:taggaggctgtaggcataaat;或c-1:ttgttggttcttctggacta;所述下游引物的序列为:a-2:agagtaactccacagaagc;b-2:agatgattaggcagaggtgaa;
或c-2:gtgctggtggttgatgat;所述探针的序列为:a-3:tgtgccttgggtggctttggggcat;b-3:aggcataaattggtctgttcaccagcaccat;或c-3:tcaaggtatgttgcccgtttgt。
7.作为优选,所述乙型肝炎病毒dna提取液包括提取液1~4,所述提取液1为曲拉通x-100、异硫氰酸胍盐、盐酸胍、tris、sds、edta和氯化钠中的一种或多种。
8.作为优选,所述提取液2为4-羟乙基哌嗪乙磺酸、氯化钠、磁珠、ctba缓冲液、1
×
te缓冲液中的一种或多种。
9.作为优选,所述提取液3为4-羟乙基哌嗪乙磺酸、曲拉通x-100、tris、sds和氯化钠中的一种或多种。
10.作为优选,所述提取液4为矿物油、石蜡油中的一种或多种。
11.作为优选,所述提取液1~4的体积比为1~3:2~4:4~8:1~3。
12.作为优选,所述试剂盒在提取血清时提取液1、血清和提取液2的体积比为3~5:2~4:0.5~1.5;所述提取液3和提取液4的体积比为2~4:0.5~1.5。
13.作为优选,所述试剂盒对b、c、d基因的最低检出限为5iu/ml;所述试剂盒对b、c、d基因的扩增效率达95%以上。
14.作为优选,所述试剂盒扩增时的程序为:48~52℃,4~10min;93~97℃,1~3min;(92~98℃,10~20s;55~65℃,30~38s)42~48个循环;22~28℃,8~12s。
15.本发明还提供了所述试剂盒在制备乙型肝炎病毒dna检测产品中的应用。
16.本发明提供了一种乙型肝炎病毒dna定量检测试剂盒,所述试剂盒包括上游引物、下游引物、探针和乙型肝炎病毒dna提取液,所述上游引物的序列如seq id no:1所示,所述下游引物的序列如seq id no:2所示,所述探针的序列如seq id no:3所示。本发明的试剂盒操作步骤简单,不使用有机溶液,对于操作者来说减少有机试剂的伤害,对于环境来说减少污染。同时,只需要3步就可以将血清中的hbv病毒提取至磁珠上。设计的引物探针可以特异性识别b、c、d基因的共同的片段,扩增效率达95%以上。特异性很强,可以特异性识别乙型肝炎病毒b、c、d基因片段可以在一管中实现dna的提取和扩增,方便快捷,灵敏度高。本发明的试剂盒可以将磁珠上吸附的dna混合物,直接加入到pcr反应体系中进行检测,通过引物探针的特异性序列来识别hbv的片段进行扩增,这样的好处是磁珠法提取的产物与pcr扩增在同一载体中进行,不需经过多次洗脱和洗涤导致的dna丢失,从而提高了检测的灵敏度,对提高临床检测质量具有重要意义。
附图说明
17.图1为实施例1中c基因国参标曲图;图2为实施例2中c基因国参标曲图;图3为实施例4中c基因定量限实验标曲图;图4为实施例4中c基因定量限扩增图;图5为实施例5中b基因定量限实验标曲图;图6为实施例5中b基因定量限扩增图;
图7为实施例6中d基因定量限国参c基因标曲图;图8为实施例6中d基因型定量限扩增图;图9为实施例7中使用两种标曲对4个阳性样本赋值后的拟合曲线;图10为实施例7中国参b基因标曲;图11为实施例7中自制企业参考品标曲;图12为实施例3中c基因型最低检出峰情况12出12;图13为实施例3中c基因最低检测限出峰情况12出12;图14为实施例3中b基因最低检测限出峰情况12出12;图15为实施例3中b基因最低检测限出峰情况12出12;图16为实施例3中d基因最低检测限出峰情况12出12;图17为实施例3中d基因最低检测限出峰情况12出12。
具体实施方式
18.在本发明中,所述b、c、d基因为乙肝的b、c、d基因分型的基因。
19.下面结合实施例对本发明提供的技术方案进行详细的说明,但是不能把它们理解为对本发明保护范围的限定。
20.实施例1 样品dna的提取和扩增(1)将400μl的提取液1(由曲拉通x-100和5m的异硫氰酸胍盐按照体积比1:80配制而成)、300μl的血清和100μl的提取液2(由4-羟乙基哌嗪乙磺酸20mm的、2m的氯化钠和磁珠按照体积比7:1:2配制而成)在离心管中混合,静置10min后500rpm离心30秒;(2)离心后将离心管放置到磁珠分离器上,静置1min,去除废液;(3)在离心管中加入600μl的提取液3(由曲拉通x-100和2m的氯化钠按照体积比1:100配制而成)和200μl的矿物油,混匀后500rpm离心30秒;(4)离心后将离心管放置到磁珠分离器上,静置1min,去除废液后500rpm离心20秒;(5)离心后将离心管放置到磁珠分离器上,静置1min,再次去除废液,加入反应液40ul混合后,得混合液备用;(反应液为引物、探针混合液共10.4μl、水4.6μl、酶混合液25μl(taq酶、ung酶、镁离子、脱氧核糖核苷三磷酸)共40ul);(6)混合液按照表1的过程进行pcr。
21.表1
实施例2 提取效率计算使用已知浓度的国家参考品c基因样本,使用实施例1的方法将其进行提取后,代入标曲计算出来的值,与标示值的对比。即代入标曲计算的浓度/样本浓度*100=提取效率%。国家参考品c基因标准曲线如图2所示,结果如表2所示。
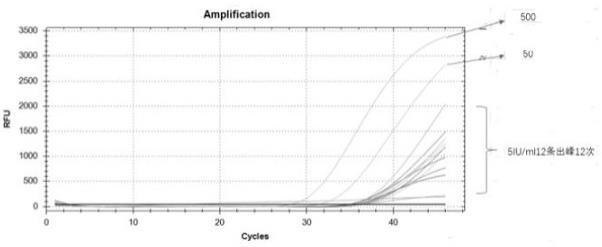
22.表2实施例3 b、c、d基因最低检出限使用国家参考品标示的浓度如表2中所示,梯度稀释至5iu/ml后,进行24次重复性检测,如果23次均出峰,即符合药监局规定的95%的阳性检出率。23/24=95.8% 如图12和图13所示为c基因的最低检测限出峰个数,5iu/ml的样本24次检测均出峰,如图14和图15为b基因的最低检测限出峰个数,5iu/ml的样本24次检测均出峰。如图16和图17为d基因的最低检测限出峰个数,5iu/ml的样本24次检测均出峰。即符合最低检测限要求。故b、c、d基因的最低检测限为5iu/ml。
23.实施例4 c基因定量限使用c基因国参5*107iu/ml的样本进行10倍梯度稀释,稀释后的模板浓度分别为5*106iu/ml、5*105iu/ml、5*104iu/ml、5*103iu/ml、5*102iu/ml等5个浓度,并将其继续稀释至10iu/ml模板,将上述样本均经过提取后扩增实验,得到如下表3数据,将上述5个梯度的ct值对应浓度logc制作标曲后,将10iu/ml模板检测的11次的ct值代入标曲计算得到的logc值与标示logc值的差值均≤0.4,即检测的浓度10iu/ml符合准确度要求,得到c基因型定量限为10iu/ml。同时计算标曲的扩增效率为105.96%,符合标曲的制作要求。计算10iu/ml模板的ct值的变异系数为0.54%,符合规定的要求。见图2和图3。
24.表3
实施例5 b基因定量限使用b基因国参5*106iu/ml的样本进行10倍梯度稀释,稀释后的模板浓度分别为5*105iu/ml、5*104iu/ml、5*103iu/ml、5*102iu/ml、5*101iu/ml等5个浓度,并将其继续稀释至10iu/ml模板,将上述样本均经过提取后扩增实验,得到如下数据,将上述5个梯度的ct值对应浓度logc制作标曲后,将10iu/ml模板检测的11次的ct值代入标曲计算得到的logc值与标示log值的差值均≤0.4,即检测的浓度10iu/ml符合准确度要求,得到b基因型定量限为10iu/ml。同时计算标曲的扩增效率为103.58%,符合标曲的制作要求。计算10iu/ml模板的ct值的变异系数为1.334%,符合规定的要求。见图4和图5。
25.表4
实施例6 d基因定量限由于d基因为稀有基因型,中检院的国参并没有提供,所以本研发自合成d基因质粒,合成后进行定量浓度为6.57*1013copy/ml,将其进行10倍梯度稀释成d3(6.57*103copy/ml)后,使用国家参考品c基因制作标曲,对d3进行浓度定量为51.28iu/ml,然后将d3进行5倍稀释即为10iu/ml,进行11次的样本重复提取和扩增,数据如下表所示。将11次的ct值代入到国参标曲中计算出的logc与标示值差值均≤0.4。即检测的浓度10iu/ml符合准确度要求,得到d基因型定量限为10iu/ml。同时计算标曲的扩增效率为108.63%,符合标曲的制作
要求。计算10iu/ml模板的ct值的变异系数为0.691%,符合规定的要求。见图6和图7。
26.表5实施例7 准确度实验使用阳性样本高、中、中低、低共4个浓度样本,分别使用国参和企业自制的参考品对其进行检测,使用本研究中开发的提取试剂和扩增试剂,4个样本重复2次检测,将ct均值分别代入到国参标曲和企业参考品的标曲中进行计算,两者计算出来的logc值进行线性拟合,拟合r2=1,线性很好,说明完全可以使用企业参考品代替国参对样本进行赋值。同时两者计算差值均≤0.4,符合要求。见图8~11。
27.表6
表7由以上实施例可知,本发明提供了一管法检测乙型肝炎病毒dna的试剂盒及其应用。该试剂盒包含两个组份。一种是高效率的提取试剂:比现有的提取试剂操作更简单、使用更方便;不含有机溶液,保护操作人员和减少环境污染。只需要3步操作就可将血清中的乙肝病毒dna高效地结合至磁珠上。另一种组分是扩增试剂:用于扩增的引物和探针互补结合b,c,d基因型的共同片段,扩增效率高达95%以上;但不结合其它病毒(如eb病毒、丙型肝炎病毒、甲型肝炎病毒等)的核酸序列,特异性高。对血清样本的最低检测限为5国际单位/
毫升。
28.以上所述仅是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以做出若干改进和润饰,这些改进和润饰也应视为本发明的保护范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1