一类1,6-二炔化合物的结构及其应用
本技术属于有机合成领域,涉及1,6-二炔基化合物的结构及其在合成大共轭稠环化合物中的应用。
背景技术:
1、多元稠环化合物广泛存在于天然产物、药物和材料领域当中。由于多元稠环化合物具有大共轭结构,有比较好的发光性质,在发光材料领域有着广泛的应用,因此多元稠环化合物的合成方法及其应用研究备受有机合成化学家的关注。目前制备稠环化合物的主要途径有两种:1、通过已有的环状化合物进行进一步修饰,从而得到需要的结构;2、利用高度不饱和化合物比如1,n-烯炔、1,n-二烯、1,n-二炔等,在一定的条件下发生环化反应,从而构建稠环化合物。前者具有更高的目的性,但需要对底物进行预先设计合成。后者具有更高的效率,可以同时构建多根化学键。
2、1,6-二炔类化合物是一类具有高度不饱和的化合物,含有两个碳碳三键,在反应过程中能够协同作用,可发生多种串联环化反应,有着多种多样的反应性质,得到不同结构的环状化合物。1,6-二炔化合物合成简便,通过炔烃分子的简单亲核进攻、取代或者偶联等就可以合成结构多样性的1,6-二炔化合物。在亲电试剂、过渡金属或者碱的作用下,1,6-二炔可经过不同的途径,得到结构多样性的稠环化合物。也就是说,1,6-二炔本身的结构具有多样性,且不同的反应条件下产物业具有多样性。因此1,6-二炔是一类非常有用的有机合成中间体。
技术实现思路
1、根据本技术的一个方面,提供了一种1,6-二炔类化合物,所述1,6-二炔就是一类具有结构多样性的化合物,能够作为一种重要的化合物来合成在荧光材料上具有很大应用价值的化合物。
2、一种通式(i)所示的化合物,及其互变异构体、多晶型物、溶剂化物、或它们的盐,
3、
4、其中,x选自氮原子、磷原子、砷原子、碲原子、硼原子;
5、r’选自c1–c30烷基、取代的c1–c30烷基、c6–c30芳基、取代的c6–c30芳基、c3–c30杂芳基、取代的c3–c30杂芳基、氨基、取代的氨基以及可选地被选自以下的杂原子基团插入任意位置:co、o、s、so、so2、nra、-n=、=n-;,
6、其中,r1a、r4a独立地选自氢、氘、c1–c30烷基、取代的c1–c30烷基、c6–c30芳基、取代的c6–c30芳基、c3–c30杂芳基、取代的c3–c30杂芳基、膦基、取代的膦基、硼基、取代的硼基、硅基、取代的硅基、卤素、氨基、取代的氨基以及可选地被选自以下的杂原子基团插入任意位置:co、o、s、so、so2、nra、-n=、=n-;
7、r2a选自c6–c30芳基、取代的c6–c30芳基、c3–c30杂芳基、取代的c3–c30杂芳基、c1–c10烯基、c1–c10取代的烯基,
8、r3a为氢、氘、c1–c30烷基、取代的c1–c30烷基、c1–c30烯基、取代的c1–c30烯基、c1–c30炔基、取代的c1–c30炔基、c6–c30芳基、取代的c6–c30芳基、c3–c30杂芳基、取代的c3–c30杂芳基、c1–c30环烷基、取代的c1–c30环烷基、c1–c30杂环烷基、取代的c1–c30杂环烷基、膦基、卤素、硅基、硼基、锗、砷、硒以及可选地被选自以下的杂原子基团插入任意位置:co、o、s、so、so2、nra、-n=、=n-;
9、ra独立地选自h、烷基或芳基。
10、可选地,取代的c6–c30芳基、取代的c3–c30杂芳基中的取代基选自烷基、烯基、醛基、卤素、卤代烷基、酯基插入的烷基、烷氧基、烷硫基、取代的氨基。
11、可选地,取代的c6–c30芳基、取代的c3–c30杂芳基中的取代基选自c1–c30烷基、c1–c30烯基、c1–c30醛基、卤素、卤代c1–c30烷基、酯基插入的c1–c30的烷基、c1–c30烷氧基、c1–c30烷硫基、苯基取代的氨基。
12、可选地,r’选自c6–c30芳基、c6–c10的烷基取代的c6–c30芳基、“卤素取代的c6–c10的烷基”取代的c6–c30芳基、c3–c30杂芳基、c6–c10的烷基取代的c3–c30杂芳基、“卤素取代的c6–c10的烷基”取代的c3–c30杂芳基;
13、优选地,r’选自c6–c30芳基、c3–c30杂芳基。
14、可选地,r1a、r4a独立地选自氢、芳基、烷基取代的c6–c30芳基、“s原子插入的烷基”取代的c6–c30芳基、“o原子插入的烷基”取代的c6–c30芳基、卤素取代的c6–c30芳基、芳基取代的c6–c30芳基、“卤素取代的烷基”取代的c6–c30芳基、“芳基取代的氨基”取代的c6–c30芳基、“酯基插入的烷基”取代的c6–c30芳基、c3–c30杂芳基;
15、优选地,r1a独立地选自苯基、叔丁基取代的苯基、ch3s-取代的苯基、ch3o-取代的苯基、萘基、苯基取代的苯基、至少一个甲基取代的苯基、cf3o-取代的苯基、br取代的苯基、“二苯基取代的氨基”取代的苯基、“酯基插入的甲基”取代的苯基、二苯并噻吩基。
16、可选地,r2a选自c6–c30芳基、“酯基插入的烷基”取代的c6–c30芳基、烷基取代的c6–c30芳基、“氧原子插入的烷基”取代的c6–c30芳基、芳基取代的c6–c30芳基、c3–c30杂芳基、醛基取代的c6–c30芳基、卤素取代的c6–c30芳基、烯基取代的c6–c30芳基;
17、优选地,r2a选自苯基、萘基、“酯基插入的甲基”取代的苯基、丙基取代的苯基、菲基、“氧原子插入的甲基”取代的苯基、联苯基、噻吩基、甲醛基取代的苯基、cl取代的苯基、乙烯基取代的苯基。
18、可选地,r3a选自氢原子、氘原子、c6–c30芳基、“酯基插入的烷基”取代的c6–c30芳基、至少一个烷基取代的c6–c30芳基;
19、优选地,r3a选自氢原子、氘原子、苯基、“酯基插入的甲基”取代的苯基、至少一个甲基取代的苯基。
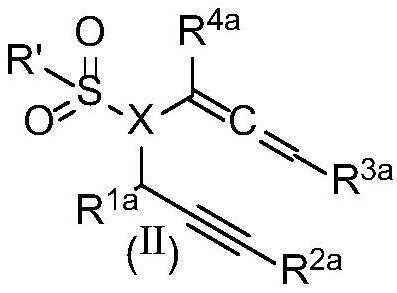
20、可选地,所述互变异构体具有通式(ii)、(iii)或(iv);
21、或者或者
22、根据本技术的另一个方面,提供上述任一项所述的化合物的制备方法,包括以下步骤:
23、含有通式(v)和(vi)所示的化合物的原料进行反应,得到通式(i)所示的化合物;
24、
25、可选地,通式(v)和(vi)所示的化合物的摩尔比为1:1-5;
26、优选地,所述反应在酸试剂的存在下进行反应;所述酸试剂包括对甲基苯磺酸、对硝基苯磺酸、甲基磺酸、三氯化铁、三氯化铝;
27、优选地,所述反应的温度为25-100℃;所述反应的时间为0.1-48小时。
28、可选地,通式(v)所示的化合物的制备方法包括以下步骤:
29、含有通式(vii)和(viii)所示的化合物的原料进行反应,得到通式(v)所示的化合物;
30、
31、可选地,通式(vii)和(viii)所示的化合物的摩尔比为1:1-5;
32、优选地,所述反应在亲核取代试剂的存在下进行反应;所述亲核取代试剂包括正丁基锂、仲丁基锂、叔丁基锂、甲基锂、二异丙基氨基锂、双三甲基硅基胺基锂;
33、优选地,所述反应的温度为-78-25℃;所述反应的时间为0.1-24小时。
34、作为一种实施方式,所述化合物的制备方法包括以下步骤:
35、
36、主要步骤为炔烃对醛类化合物进行亲核取代,得到炔丙醇类化合物。炔丙醇类化合物在与n-炔丙基磺酰胺类化合物偶联,从而合成所需化合物。
37、根据本技术的另一个方面,提供上述任一项所述的化合物在制备异吲哚二聚化合物中的应用,其中所述异吲哚二聚化合物具有下式所示的结构;
38、
39、其中,
40、x和y独立地选自氮原子、磷原子、砷原子、碲原子、硼原子;
41、r1、r4相同或不同;r1、r4独立地选自氢、c1–c30烷基、取代的c1–c30烷基、c6–c30芳基、取代的c6–c30芳基、c3–c30杂芳基、取代的c3–c30杂芳基、膦基、取代的膦基、硼基、取代的硼基、硅基、取代的硅基、卤素、氨基、取代的氨基以及可选地被选自以下的杂原子基团插入任意位置:co、o、s、so、so2、nra、-n=、=n-;
42、r2、r5相同或不同;r2、r5独立地选自c6–c30芳基、取代的c6–c30芳基、c3–c30杂芳基、取代的c3–c30杂芳基;
43、r3、r6相同或不同;r7、r8相同或不同;r3、r6、r7、r8独立地选自氢原子、c1–c30烷基、取代的c1–c30烷基、c1–c30烯基、取代的c1–c30烯基、c1–c30炔基、取代的c1–c30炔基、c6–c30芳基、取代的c6–c30芳基、c3–c30杂芳基、取代的c3–c30杂芳基、c1–c30环烷基、取代的c1–c30环烷基、c1–c30杂环烷基、取代的c1–c30杂环烷基、膦基、卤素、硅基、硼基、锗、砷、硒以及可选地被选自以下的杂原子基团插入任意位置:co、o、s、so、so2、nra、-n=、=n-;
44、ra独立地选自h、烷基或芳基。
45、根据本技术的另一个方面,提供上述任一项所述的化合物在检测含有活性氧的物质中的应用。
46、可选地,所述活性氧包括次氯酸钠、过氧化氢、臭氧中的至少一种。
47、可选地,将将上述通式(i)化合物涂抹于硅胶板、陶瓷片、聚四氟片、蓝宝石基底、玻璃或者二氧化硅基底等载体上,然后将有活性氧的化合物(次氯酸钠、过氧化氢、臭氧等)滴在载体上。然后用加热30秒。载体将会有无色变成红色,并且在365nm的紫外灯照射下荧光会从没有荧光到逐渐显现出强烈的荧光。
48、根据本技术的另一个方面,提供上述任一项所述的化合物在细胞成像中的应用。
49、本技术中,“烷基”,是指烷烃失去一个h原子得到的基团。
50、“烯基”,是指烯烃失去一个h原子得到的基团。
51、“炔基”,是指炔烃失去一个h原子得到的基团。
52、“环烷基”,是指环烷烃失去一个h原子得到的基团。
53、“杂环烷基”,是指杂环烷烃失去一个h原子得到的基团。
54、“芳基”,是指芳烃失去一个h原子得到的基团。
55、“杂芳基”,是指杂芳烃失去一个h原子得到的基团。
56、“取代的烷基”、“取代的芳基”等,分别指任意基团取代的烷基、任意基团取代的芳基。
57、“杂原子基团插入任意位置”是指杂原子基团可以以取代h原子的方式或者是取代c原子的方式插入基团中,例如“o原子插入甲基为ch3o-”、“s原子插入甲基为ch3s-”、“nh插入甲基为ch3nh-”、“n原子插入苯基为吡啶基”等。
58、“烷基取代的芳基”、“芳基取代的芳基”等分别表示含有烷基取代基的芳基和含有芳基取代基的芳基,例如等;其中“*”处代表基团的连接点。
59、本技术中,“烷基”、“芳基”等如无特别说明,均可有任意个连接点;一般为1个连接点,2个连接点,3个连接点,4个连接点或5个连接点。
60、“c1–c30”等均值c原子的个数。
61、“卤代c1–c30烷基”等是指卤素取代的c原子数为1-30的烷基。
62、“卤素”是指氟、氯、溴、碘。
63、“盐”表示与无机和/或有机酸和碱形成的酸性和/或碱性盐。此外,当本发明的化合物包含碱性部分(例如但不限于吡啶或咪唑)和酸性部分(例如但不限于羧酸)时,两性离子(“内盐”)可以是形成并包括在本文所用的术语“盐”中。
64、“溶剂化物”包括例如水合物。
65、本技术所描述的结构式意在包括所有的同分异构形式(如对映异构,非对映异构和几何异构体(或构象异构体)):例如含有不对称中心的r~s构型,双键的(z)、(e)异构体等。因此,本技术化合物的单个立体化学异构体或其对映异构体、非对映异构体或几何异构体(或构象异构体)的混合物都属于本技术的范围。
66、“互变异构体”表示具有不同能量的结构同分异构体可以超过低能垒,从而互相转化。比如,质子互变异构体(即质子移变)包括通过质子迁移进行互变。化合价互变异构体包括通过一些成键电子重组而进行互变。
67、“溶剂化物”是指本发明化合物与溶剂分子配位形成特定比例的配合物。
68、本技术能产生的有益效果包括:
69、1)本技术所提供的1,6-二炔类化合物,具有多变的结构合成方便,适用于工业化生产。
70、2)本技术所提供的1,6-二炔类化合物,用于合成一类苯并异吲哚二聚化合物及其衍生物。
71、3)本技术所提供的1,6-二炔类化合物,用于细胞成像的用途
72、4)本技术所提供的1,6-二炔类化合物,用于检测含有活性氧(次氯酸钠、过氧化氢、臭氧等)的用途。
- 还没有人留言评论。精彩留言会获得点赞!