制备含磷配体的方法
1.本发明涉及含磷配体技术领域,特别是涉及制备含磷配体的方法。
背景技术:
2.亚磷酸酯类化合物作为烯烃的氢氰化有关的催化体系是本领域已知的。现有公开技术通常采用r-oh与磷氯化合物以惰性气体吹扫或者添加有机碱缚酸剂的方式制备亚磷酸酯类化合物。如,中国专利cn101250200a提及一种双(2,4-二叔丁基苯基)季戊四醇二亚磷酸酯的合成方法,反应过程中通入氮气搅拌,反应生成的氯化氢用氢氧化钠溶液吸收。中国专利cn106220681a提及一种亚磷酸酯抗氧化剂的制备方法,反应过程中保持体系微正压,产生的氯化氢均被排入氯化氢吸收系统,生成盐酸。
3.中国专利cn102875599a公开了2,2
′
,6-三羟基联苯与二吡咯氯化磷在无水三乙胺的条件下制备三齿含磷配体,反应结束后过滤除三乙胺盐酸盐,除溶剂、柱层析粗提纯、甲醇重结晶得目标产品,收率为64%。中国专利cn101331144b公开了2,2
′
,6,6
′‑
四羟基-1,1
′‑
联苯与二吡咯氯化磷在三乙胺的条件下制备四齿含磷配体,反应结束后过滤、除溶剂、柱层析得目标产物,收率为36%。
4.现有技术关于双齿及以上多齿含磷配体制备过程,通常需要加入液体胺类化合物作为缚酸剂与产生的氯化氢反应生成铵盐酸盐,反应结束后,经过滤、除溶剂、柱层析提纯目标产物。但是,这种方法普遍存在缚酸剂用量大、反应体系粘度过高、缚酸剂后处理困难且回收利用工序复杂等问题,增加三废处理成本。
5.中国专利cn100441584c公开了一种季戊四醇亚磷酸酯抗氧化剂的制备,以季戊四醇、溶剂、三氯化磷和2,6-二叔丁基对甲酚为原料,在弱碱型大孔离子交换树脂作为催化剂的作用下,制备季戊四醇亚磷酸酯,产生的氯化氢气体及时排除体系,反应后的催化剂易分离回收,可再生重复使用。但是,弱碱型大孔离子交换树脂作为催化剂成本较高,使用量较大,再生处理复杂,需要经过酸洗、碱洗、蒸馏水洗至中性,干燥,整个过程操作复杂、能耗大,且产生大量废水、废盐。
6.因此,如何解决含磷配体类化合物制备过程中使用缚酸剂后体系含盐量过高,粘度大,后处理困难的问题,以及如何解决制备过程的选择性低、转化率低是本领域面临的难题。同时,对于一些含有敏感型基团(如双键等)的含磷配体类化合物,以条件更加温和、反应更加快速的方式来制备也是本领域的迫切需求。
技术实现要素:
7.基于此,有必要针对上述问题,提供一种制备含磷配体的方法,所述制备方法采用聚吡啶离子液体多孔微球作为催化剂,并将反应产生的氯化氢移出反应装置,使得制备方法具有优异的反应选择性和收率。
8.一种制备含磷配体的方法,包括以下步骤:
9.将结构式如式(e)所示的磷氯化合物、聚吡啶离子液体多孔微球与有机溶剂混合
得到第一配制物,将结构式如式(f)所示的化合物与有机溶剂混合得到第二配制物;以及
10.将所述第一配制物与所述第二配制物于反应装置中混合进行反应,并将反应产生的氯化氢移出所述反应装置,反应结束后将反应液进行过滤,滤液经过后处理得到含磷配体;
[0011][0012]
式(e)中,x和y分别独立的选自取代芳氧基或者含氮杂环基团,式(f)中,z为含一个或多个取代基的脂肪烃或芳烃的多价基团,其中,取代基选自氢原子、卤素原子、c
1-c
10
的烷基、c
1-c
10
的烷氧基、c
1-c
10
的烷酰基、芳基、杂芳基、氰基或者硝基,n为1至8的整数。
[0013]
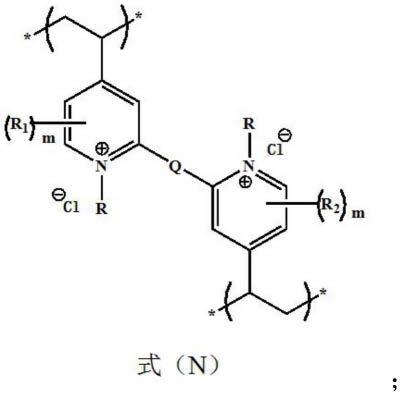
在其中一个实施例中,所述聚吡啶离子液体多孔微球中聚吡啶离子液体的结构式如式(n)所示,
[0014][0015]
式(n)中,r选自c
1-c
10
的直链烷基或者支链烷基,r1和r2分别独立的选自氢原子、卤素原子、c
1-c
10
的烷基、c
1-c
10
的烷氧基、c
1-c
10
的烷酰基、芳基、杂芳基、氰基或者硝基,m为0至3的整数,q为直接键或者二价连接基团。
[0016]
在其中一个实施例中,q选自在其中一个实施例中,q选自或者
[0017]
其中,r3、r4、r5、r6分别独立的选自氢原子、卤素原子、c
1-c
10
的烷基、c
1-c
10
的烷氧
基、c
1-c
10
的烷酰基、芳基、杂芳基、氰基或者硝基,q0选自直接键或者二价连接基团,m0为0至3的整数,m1为0至2的整数。
[0018]
在其中一个实施例中,q0选自-(ch2)n
1-、-(ch2o)n
2-、取代芳基或者未取代芳基,n1、n2分别独立的为1至50的整数。
[0019]
在其中一个实施例中,所述聚吡啶离子液体多孔微球中聚苯乙烯种子微球的粒度为50nm-100nm,尺寸相对标准偏差《3%。
[0020]
在其中一个实施例中,所述聚吡啶离子液体多孔微球的bet比表面积为50m2/g-500m2/g,平均孔径为10nm-50nm。
[0021]
在其中一个实施例中,式(e)中,所述取代芳氧基的结构式为:其中,rx和ry分别独立的选自氢原子、卤素原子、腈基、c
1-c
10
的烷基、c
1-c
10
的烷氧基、c
1-c
10
的烷酰基、c
1-c
10
的酯基、c
1-c
10
的磺酸酯基、乙烯基、丙烯基、丙烯酰基、丙烯酸酯或者甲基丙烯酰基。
[0022]
在其中一个实施例中,x和y均选自时,x和y不成环;
[0023]
或者,x和y均选自含氮杂环基团时,x和y不成环或者x和y经由单键或亚甲基成环;
[0024]
或者,x选自和y选自含氮杂环基团时,x和y经由亚甲基成环。
[0025]
在其中一个实施例中,所述含氮杂环基团选自在其中一个实施例中,所述含氮杂环基团选自或者其中,rx和ry分别独立的选自氢原子、卤素原子、腈基、c
1-c
10
的烷基、c
1-c
10
的烷氧基、c
1-c
10
的烷酰基、c
1-c
10
的酯基、c
1-c
10
的磺酸酯基、乙烯基、丙烯基、丙烯酰基、丙烯酸酯或者甲基丙烯酰基。
[0026]
在其中一个实施例中,x和y均选自含氮杂环基团且二者经由单键或亚甲基成环的结构部位选自以下任意一种:
[0027][0028]
或者
[0029]
在其中一个实施例中,式(f)中,z选自在其中一个实施例中,式(f)中,z选自在其中一个实施例中,式(f)中,z选自或者
[0030]
其中,r1和r2分别独立的选自氢原子、卤素原子、腈基、c
1-c
10
的烷基、c
1-c
10
的烷氧基、c
1-c
10
的烷酰基、c
1-c
10
的酯基、c
1-c
10
的磺酸酯基、乙烯基、丙烯基、丙烯酰基、丙烯酸酯或者甲基丙烯酰基。
[0031]
在其中一个实施例中,式(f)中,n为2至4的整数。
[0032]
在其中一个实施例中,将所述第一配制物与所述第二配制物混合进行反应的步骤中,所述磷氯化合物与所述式(f)所示的化合物的摩尔比为1.0:1/x-1.3:1/x,x与式(f)化合物中的n相等,所述聚吡啶离子液体多孔微球中氮元素与式(f)所示的化合物中羟基的摩尔比为0.01:1-0.1:1。
[0033]
在其中一个实施例中,所述第一配制物中磷氯化合物的浓度为0.05mol/l-5.0mol/l,所述第二配制物中式(f)所示的化合物的浓度为0.05mol/l-5.0mol/l。
[0034]
在其中一个实施例中,将所述第一配制物与所述第二配制物混合进行反应的步骤中,反应温度为0℃-50℃,反应时间为1h-5h。
[0035]
在其中一个实施例中,将所述第一配制物与所述第二配制物混合进行反应的步骤中,将所述第二配制物分批加入所述第一配制物中。
[0036]
在其中一个实施例中,所述第二配制物分批加入所述第一配制物中时,时间控制在2h-10h。
[0037]
在其中一个实施例中,反应结束后将反应液进行过滤的步骤中,还回收得到聚吡啶离子液体多孔微球。
[0038]
在其中一个实施例中,回收得到的聚吡啶离子液体多孔微球经过洗涤和干燥后,循环套用于所述第一配制物中。
[0039]
在其中一个实施例中,将所述第一配制物与所述第二配制物于反应装置中混合进行反应的步骤中,通入保护气体进行吹扫,以将反应产生的氯化氢移出所述反应装置,联产获得盐酸。
[0040]
本发明的制备方法中,采用聚吡啶离子液体多孔微球作为催化剂,其多孔结构可以增加反应的催化活性位点,从而可以提高反应选择性和收率,同时催化作用降低了反应所需活化能,一方面能降低反应温度,另一方面可以加快化学反应速率,更加适用于制备含有敏感型基团(如双键等)的含磷配体类化合物。再者,该催化剂性质稳定、后处理简单、循环性能好,易于回收再利用。
[0041]
另外,本发明在反应过程中将反应产生的氯化氢移出反应装置,可以解决体系粘稠、后处理困难的问题,进而也能有助于提高反应选择性和收率。
具体实施方式
[0042]
为了便于理解本发明,下面将对本发明进行更详细的描述。但是,应当理解,本发明可以以许多不同的形式来实现,并不限于本文所描述的实施方式或实施例。相反地,提供这些实施方式或实施例的目的是使对本发明的公开内容的理解更加透彻全面。
[0043]
除非另有定义,本文所使用的所有的技术和科学术语与属于本发明的技术领域的技术人员通常理解的含义相同。本文中在本发明的说明书中所使用的术语只是为了描述具体的实施方式或实施例的目的,不是旨在于限制本发明。
[0044]
本发明提供的制备含磷配体的方法,包括以下步骤:
[0045]
s1,将结构式如式(e)所示的磷氯化合物、聚吡啶离子液体多孔微球与有机溶剂混合得到第一配制物,将结构式如式(f)所示的化合物与有机溶剂混合得到第二配制物;
[0046][0047]
式(e)中,x和y分别独立的选自取代芳氧基或者含氮杂环基团,式(f)中,z为含一个或多个取代基的脂肪烃或芳烃的多价基团,其中,取代基选自氢原子、卤素原子、c
1-c
10
的烷基、c
1-c
10
的烷氧基、c
1-c
10
的烷酰基、芳基、杂芳基、氰基或者硝基,n为1至8的整数;
[0048]
s2,将所述第一配制物与所述第二配制物于反应装置中混合进行反应,并将反应产生的氯化氢移出所述反应装置,反应结束后将反应液进行过滤,滤液经过后处理得到含磷配体。
[0049]
应予说明的是,聚吡啶离子液体多孔微球包括聚苯乙烯种子微球以及负载于所述聚苯乙烯种子微球中的聚吡啶离子液体。在制备聚吡啶离子液体多孔微球时,聚苯乙烯种子微球类似于“晶种”的存在,吡啶单体通过物理作用吸附在聚苯乙烯种子微球上,并借助于聚苯乙烯种子微球的孔道聚合生长成聚吡啶离子液体,进而,形成的聚吡啶离子液体多孔微球中具有更多的活性位点。
[0050]
所以,本发明采用聚吡啶离子液体多孔微球作为催化剂时,其更多的活性位点可以有效提高反应选择性和收率,同时,由于聚吡啶离子液体多孔微球呈球状,后处理简单,且性质更稳定、循环性能好,易于回收再利用。
[0051]
可选的,所述聚吡啶离子液体的结构式如式(n)所示,
[0052][0053]
式(n)中,r选自c
1-c
10
的直链烷基或者支链烷基。
[0054]
式(n)中,r1和r2分别独立的选自氢原子、卤素原子、c
1-c
10
的烷基、c
1-c
10
的烷氧基、c
1-c
10
的烷酰基、芳基、杂芳基、氰基或者硝基,m为0至3的整数,进一步的,r1和r2分别独立的选自氢原子、氟原子、氯原子、溴原子、甲基、乙基、正丙基、异丙基、甲氧基、乙氧基、正丙氧基、异丙氧基、氰基、乙酰基或者丙酰基。
[0055]
式(n)中,q为直接键或者二价连接基团,进一步的,q选自
或者
[0056]
其中,r3、r4、r5、r6分别独立的选自氢原子、卤素原子、c
1-c
10
的烷基、c
1-c
10
的烷氧基、c
1-c
10
的烷酰基、芳基、杂芳基、氰基或者硝基,m0为0至3的整数,m1为0至2的整数,进一步的,r3、r4、r5、r6分别独立的选自氢原子、氟原子、氯原子、溴原子、甲基、乙基、正丙基、异丙基、甲氧基、乙氧基、正丙氧基、异丙氧基、氰基、乙酰基或者丙酰基。
[0057]
其中,q0选自直接键或者二价连接基团,进一步的,q0选自-(ch2)n
1-、-(ch2o)n
2-、取代芳基或者未取代芳基,n1、n2分别独立的为1至50的整数。
[0058]
可选的,所述聚吡啶离子液体多孔微球中聚苯乙烯种子微球的粒度为50nm-100nm,尺寸相对标准偏差《3%。
[0059]
可选的,所述聚吡啶离子液体多孔微球具有孔结构,bet比表面积为50m2/g-500m2/g,平均孔径为10nm-50nm。
[0060]
可选的,所述聚吡啶离子液体多孔微球的制备方法包括以下步骤:
[0061]
(1)取聚苯乙烯种子微球超声分散于表面活性剂水溶液中,得到第一乳液;另取一定体积第一有机溶剂超声分散于表面活性剂水溶液中,得到第二乳液,在室温下,将第二乳液迅速加入到第一乳液中并震荡混合一段时间,得到含聚苯乙烯种子微球的第一混合液;
[0062]
(2)将一定量吡啶单体和引发剂溶于第二有机溶剂中,然后分散于含有表面活性剂水溶液中,超声乳化后,迅速加入到第一混合液中,并继续震荡混合,得到第二混合液;
[0063]
(3)通过惰性气氛置换,除去第二混合液中的空气,然后进行聚合反应,聚合反应结束后,聚合反应液经固液分离和第三有机溶剂洗涤后,在真空条件下进行干燥,得到交联聚乙烯基吡啶多孔微球;
[0064]
(4)将交联聚乙烯基吡啶多孔微球与第四有机溶剂、卤代烷烃混合,然后在一定温度下搅拌反应,反应结束后,反应液经固液分离和第五有机溶剂洗涤后,干燥得到聚吡啶离子液体多孔微球。
[0065]
步骤(1)和步骤(2)中,表面活性剂水溶液的浓度为0.2wt%-1.5wt%,优选为0.5wt%-1.0wt%,震荡混合的时间为6h-18h,优选为10h-12h。
[0066]
其中,表面活性剂选自阳离子表面活性剂、阴离子表面活性剂、非离子表面活性剂中的至少一种,进一步选自十六烷基三甲基季铵溴化物、十八烷基二甲基苄基季铵氯化物、十二烷基硫酸铵、十二烷基硫酸钠、十二烷基苯磺酸钠、十二烷基磷酸酯钾、聚乙烯醇、吐温-80中的至少一种。
[0067]
步骤(1)的第一乳液中,聚苯乙烯微球的质量与表面活性剂水溶液的体积比为1g:20ml-1g:100ml,步骤(1)的第二乳液中,第一有机溶剂与表面活性剂水溶液的体积比为1:10-1:30。
[0068]
其中,所述第一有机溶剂选自乙酸乙酯、四氢呋喃、n,n-二甲基甲酰胺、二甲基亚砜、甲醇、乙醇、丙醇、叔丁醇、乙二醇、丙二醇、丙三醇、丙酮中的至少一种。
[0069]
步骤(2)中,吡啶单体与引发剂的摩尔比为20:1-50:1,吡啶单体与步骤(1)中聚苯乙烯种子微球的质量比为50:1-100:1。
[0070]
其中,所述吡啶单体的通式为所述引发剂选自偶氮类引发剂,进一步选自偶氮二异丁腈(aibn)、偶氮二异庚腈(abvn)、偶氮二异丁酸二甲酯(aibme)、偶氮二异丁脒盐酸盐(aiba)、偶氮二异丁咪唑啉盐酸盐(aibi)中的至少一种;所述第二有机溶剂选自脂肪或脂环烃、卤代脂肪或脂环烃、取代或未取代的芳香烃、脂肪醚、环状醚中的至少一种,进一步选自苯、甲苯、二甲苯、二氯甲烷、环己烷、正己烷、四氢呋喃中的至少一种。
[0071]
步骤(3)中,所述聚合反应的温度为40℃-120℃,进一步优选为60℃-80℃,时间为6h-36h,进一步优选为20h-24h。
[0072]
步骤(3)中,所述第三有机溶剂选自乙酸乙酯、四氢呋喃、n,n-二甲基甲酰胺、二甲基亚砜、甲醇、乙醇、丙醇、叔丁醇、乙二醇、丙二醇、丙三醇、丙酮中的至少一种。
[0073]
步骤(3)获得的所述交联聚苯乙烯吡啶多孔微球的氮元素的含量ωn为5%-20%。
[0074]
步骤(4)中,所述交联聚苯乙烯吡啶多孔微球中氮元素的摩尔量nn=mc*ωn/14,其中,mc指交联聚苯乙烯吡啶多孔微球的质量。进一步地,交联聚苯乙烯吡啶多孔微球与卤代烷烃的摩尔比为nn:n
卤代烷烃
=1:1.0-1:1.5。
[0075]
步骤(4)中,所述第四有机溶剂选自甲苯、苯、二甲苯、四氢呋喃、环己烷、正己烷、二氯甲烷中的至少一种,所述卤代烷烃选自c
1-c
10
的卤代烷烃,进一步优选自1-氯丙烷、2-氯丙烷、1-溴丙烷、1-溴丁烷、2-溴丁烷、1-碘戊烷、2-碘戊烷中的至少一种,所述第五有机溶剂选自乙酸乙酯、四氢呋喃、n,n-二甲基甲酰胺、二甲基亚砜、甲醇、乙醇、丙醇、叔丁醇、乙二醇、丙二醇、丙三醇、丙酮中的至少一种。
[0076]
步骤(4)中,反应的温度为60℃-150℃,优选为80℃-120℃,反应的时间为6h-36h,优选为18h-24h。
[0077]
为了获得不同的含磷配体化合物,可选的,结构式如式(e)所示的磷氯化合物中,x和y分别独立的选自取代芳氧基或者含氮杂环基团。
[0078]
其中,所述取代芳氧基的结构式为:中,rx和ry分别独立的选自氢原子、卤素原子、腈基、c
1-c
10
的烷基、c
1-c
10
的烷氧基、c
1-c
10
的烷酰基、c
1-c
10
的酯基、c
1-c
10
的磺酸酯基、乙烯基、丙烯基、丙烯酰基、丙烯酸酯或者甲基丙烯酰基。
[0079]
可选的,所述含氮杂环基团选自可选的,所述含氮杂环基团选自或者其中,rx和ry分别独立的选自氢原子、卤素原子、腈基、c
1-c
10
的烷基、c
1-c
10
的烷氧基、c
1-c
10
的烷酰基、c
1-c
10
的酯基、c
1-c
10
的磺酸酯基、乙烯基、丙烯基、丙烯酰基、丙烯酸酯或者甲基丙烯酰基。
[0080]
进一步的,当x和y均选自时,x和y不成环;当x和y均选自含氮杂环基团时,x和y不成环或者x和y经由单键或亚甲基成环;当x选自y选自含氮杂环基团时,x和y经由亚甲基成环。
[0081]
进一步的,当x和y均选自含氮杂环基团且二者经由单键或亚甲基成环的结构部位选自以下任意一种:
[0082][0082]
或者
[0083]
可选的,式(f)中,z选自
或者
[0084]
其中,r1和r2分别独立的选自氢原子、卤素原子、腈基、c
1-c
10
的烷基、c
1-c
10
的烷氧基、c
1-c
10
的烷酰基、c
1-c
10
的酯基、c
1-c
10
的磺酸酯基、乙烯基、丙烯基、丙烯酰基、丙烯酸酯或者甲基丙烯酰基。
[0085]
进一步的,式(f)中,n为2至8的整数,更进一步的,式(f)中,n为2至4的整数。
[0086]
可选的,第一配制物和第二配制物中的有机溶剂选自c
4-c8的烷烃、酯类、醚类或者c
3-c6的酮中的至少一种,进一步的,选自苯、甲苯、二甲苯、戊烷、正己烷、正庚烷、环己烷、甲基环己烷、乙醚、二异丙醚、甲基叔丁基醚、四氢呋喃、二氯甲烷、1,4-二噁烷、1,3-二氧戊环、乙酸乙酯、乙酸异丁酯、乙酸叔丁基酯、丙酮、2-丁酮、3,3-二甲基-2-丁酮、苄腈、丙腈或者乙腈中的至少一种,更进一步的,选自四氢呋喃、甲苯或者乙酸乙酯中的至少一种。
[0087]
可选的,所述第一配制物中磷氯化合物的浓度为0.05mol/l-5.0mol/l,进一步优选为0.5mol/l-2.0mol/l。
[0088]
可选的,所述第二配制物中式(f)所示的化合物的浓度为0.05mol/l-5.0mol/l,进一步优选为0.2mol/l-1.5mol/l。
[0089]
步骤s2将所述第一配制物与所述第二配制物混合进行反应的步骤中,反应温度为0℃-50℃,优选为20℃-30℃,反应时间为1h-5h,优选为3h-3.5h,同时,控制所述磷氯化合物与所述式(f)所示的化合物的摩尔比为1.0:1/x-1.3:1/x,其中,x与式(f)化合物中的n相等,控制所述聚吡啶离子液体多孔微球中氮元素与式(f)所示的化合物中羟基的摩尔比为0.01:1-0.1:1,优选为0.02:1-0.05:1。
[0090]
可选的,将所述第一配制物与所述第二配制物混合进行反应的步骤中,将所述第二配制物采用滴加等方式分批加入所述第一配制物中,进一步的,所述第二配制物持续、匀速的滴加至所述第一配制物中,时间控制在2h-10h,优选为3h-5h。
[0091]
本发明的步骤s2中,在反应过程中还将反应产生的氯化氢移出反应装置,从而解决体系粘稠、后处理困难的问题,同时,也能有助于提高反应选择性和收率。
[0092]
可选的,可以采用保护气体吹扫、减压、超声等物理方式将产生的氯化氢移出反应
装置,排入至氯化氢吸收系统,生成盐酸。
[0093]
由于在反应过程中持续通入保护气体进行吹扫,还能够增加反应的混合效果,优选的,步骤s2将所述第一配制物与所述第二配制物于反应装置中混合进行反应的步骤中,通入保护气体进行吹扫,以将反应产生的氯化氢移出所述反应装置。
[0094]
可以理解,只要不影响反应的气体均可以作为保护气体使用,可选的,所述保护气体选自氮气、氩气、氖气、氦气、一氧化碳或者二氧化碳中的至少一种。
[0095]
在实际操作中,可以先向反应装置中持续通入干燥的保护气体,置换掉反应装置内部的空气和水汽,然后将第一配制物置于反应装置中,然后采用滴加等方式将第二配制物分批加入第一配制物中,加入过程中,持续通入干燥的保护气体进行吹扫。
[0096]
反应结束后,将反应液进行过滤,滤液先经过浓缩除去有机溶剂,浓缩液经过后处理分离纯化,得到含磷配体。典型地,可以通过柱层析、模拟移动床、结晶、萃取、精馏等后处理手段对含磷配体进行分离纯化。
[0097]
同时,将反应液进行过滤的步骤中,还回收得到聚吡啶离子液体多孔微球,可选的,回收得到的聚吡啶离子液体多孔微球经过洗涤和干燥后,可循环套用于步骤s1中的第一配制物中。
[0098]
以下,将通过以下具体实施例对所述制备含磷配体的方法做进一步的说明。
[0099]
以下聚吡啶离子液体多孔微球的制备方法中,吡啶单体的结构式如n
0-1至n
0-10所示。
[0100]
[0101][0102]
聚吡啶离子液体多孔微球d1的制备
[0103]
(1)取1g聚苯乙烯种子微球(粒度为55nm,尺寸相对标准偏差为1.6%)超声分散于20ml、0.5wt%的十二烷基硫酸钠溶液中,得到第一乳液;另取2ml的乙酸丁酯超声分散于20ml、0.5wt%的十二烷基硫酸钠溶液中,得到第二乳液。将第二乳液迅速加入到第一乳液中震荡混合,并在室温下震荡12小时,得到含聚苯乙烯种子微球的第一混合液。
[0104]
(2)将50g结构式如n
0-1所示的联吡啶单体和1.97g的aibn引发剂溶于40ml的甲苯中,然后分散于0.5wt%的十二烷基硫酸钠溶液中,超声乳化后,迅速加入到第一混合液中,并在相同条件下继续震荡12小时,得到第二混合液。
[0105]
(3)通过氮气置换,除去第二混合液中的空气,然后置于65℃下震荡聚合24小时,聚合结束后,聚合反应液经离心、乙醇洗涤后,在室温下真空干燥,得到49.98g的交联聚乙烯基吡啶多孔微球c1,并采用元素分析法确定其氮元素的含量。
[0106]
(4)将45g的交联聚乙烯基吡啶多孔微球置于反应瓶中,加入一定量甲苯和34.94g的1-氯丙烷,经充分混合均匀后,在100℃下搅拌反应24小时。然后,将反应液离心、乙醇洗
涤后,在室温下真空干燥,得到78.9g的聚吡啶离子液体多孔微球d1,收率为98.7%,并采用元素分析法确定其氮元素的含量。
[0107]
聚吡啶离子液体多孔微球d2至d12的制备方法与上述相同,区别在于反应控制参数不同,具体反应参数如表1所示,反应结果如表2所示。
[0108]
表1
[0109][0110]
表2
[0111][0112][0113]
以下实施例1-实施例12的含磷配体的制备方法中,磷氯化合物的结构式如e1至e12所示,式(f)所示的化合物的结构式如f1至f12所示,含磷配体的结构式如l1至l12所示。
[0114]
[0115]
[0116]
[0117][0118]
实施例1
[0119]
将磷氯化合物e1(86.17g,0.341mol)、聚吡啶离子液体多孔微球d1(3.68g,含氮量
0.0195mol)与甲苯混合成200ml的第一配制物。
[0120]
将4,5-二甲基-2,2',6,6'-四羟基联苯f1(20g,0.081mol)与甲苯混合成100ml的第二配制物。
[0121]
向反应装置持续通入30min干燥的氮气,置换反应装置内部的空气和水汽,然后将第一配制物转移至反应装置中,将第二配制物转移至高位滴加装置中,启动反应装置中的搅拌器,并运行氯化氢吸收系统。
[0122]
在25℃下,从高位滴加装置将第二配制物持续匀速滴加至反应装置中,控制滴加时间为3h,滴加过程中持续通入干燥的氮气,滴加结束后,继续搅拌反应4h。随后,将反应液过滤,除去聚吡啶离子液体多孔微球d1,滤液经过浓缩除去甲苯,浓缩液通过柱层析分离纯化后得到70.65g的含磷配体l1,收率为78.3%。
[0123]
含磷配体l2至l12的制备方法与上述相同,区别在于反应控制参数不同,具体反应参数如表3所示,反应结果如表4所示。
[0124]
表3
[0125][0126]
表4
[0127][0128]
聚吡啶离子液体多孔微球套用实验:
[0129]
将实施例1中过滤出的聚吡啶离子液体多孔微球d1进行制备含磷配体l1的套用实
验,数据如下表5所示,具体制备含磷配体l1的步骤同实施例1。
[0130]
表5
[0131][0132]
由表5可知,本发明的聚吡啶离子液体多孔微球可以重复套用多次,套用20次回收率仍大于95%,且反应活性无明显降低。
[0133]
对比例1
[0134]
与实施例1的区别仅在于,将实施例1中的催化剂替换成弱碱型大孔离子交换树脂(3.68g,型号d301),其余制备方法均与实施例1相同。反应结束后分离提纯得到48.45g的含磷配体l1,选择性为59.2%,收率为53.7%。
[0135]
对比例2
[0136]
与实施例1的区别仅在于,将实施例中的催化剂替换成81ml无水三乙胺,反应过程中不需要持续通入干燥的氮气,也不需要运行氯化氢吸收系统,其余制备方法均与实施例1相同。反应结束后分离提纯得到38.35g的含磷配体l1,选择性为47.3%,收率为42.5%。
[0137]
以上所述实施例的各技术特征可以进行任意的组合,为使描述简洁,未对上述实施例中的各个技术特征所有可能的组合都进行描述,然而,只要这些技术特征的组合不存在矛盾,都应当认为是本说明书记载的范围。
[0138]
以上所述实施例仅表达了本发明的几种实施方式,其描述较为具体和详细,但并不能因此而理解为对发明专利范围的限制。应当指出的是,对于本领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干变形和改进,这些都属于本发明的保护范围。因此,本发明专利的保护范围应以所附权利要求为准。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1