用于检测H4亚型禽流感病毒的特异性引物和探针及其应用的制作方法
用于检测h4亚型禽流感病毒的特异性引物和探针及其应用
技术领域
1.本发明属于分子生物学诊断技术领域,涉及快速检测h4亚型禽流感病毒的荧光定量rt-pcr方法的引物与探针组合,及利用该组合来快速鉴定h4亚型禽流感病毒的应用。
背景技术:
2.1956年,h4亚型禽流感病毒第一次在捷克斯洛伐克的鸭子中分离出来,随后在亚洲、欧洲和北美等国家的野生和家养禽类中广泛传播。近年来,在中国华中、华东和华南等地的活禽市场中发现同一宿主共同感染h4与其他亚型禽流感病毒事件,另外在家鸭中发现h4亚型病毒与其他亚型禽流感病毒(如h3亚型)之间发生了重组。除禽类外,哺乳动物(如海豹和猪)中也能分离出h4亚型流感病毒。有研究表明h4亚型禽流感病毒无需事先适应即可在小鼠体内复制,并可通过密切接触在豚鼠之间传播。值得注意的是,h4n8亚型病毒(a/slaty-backed gull/japan/6ks0185/2006)可以导致小鼠出现严重的呼吸道症状,最终死亡。1999年,从加拿大的猪中分离出的两株h4n6低致病性流感病毒株,其血凝素蛋白中出现了q226l和g228s氨基酸突变,提示这两株病毒与人类受体结合的亲和力有所提高。此外,血清流行病学研究表明,经常接触活家禽的人群,包括家禽养殖者、工人和兽医,感染h4亚型禽流感病毒的风险更大。以上研究都清楚地揭示了h4亚型禽流感病毒对公众健康构成的潜在威胁。
3.目前禽流感病毒感染的诊断方法主要包括病毒分离鉴定、血清学方法和分子生物学方法,如逆转录酶聚合酶链反应和实时定量聚合酶链反应。当前逆转录酶聚合酶链反应和实时定量聚合酶链反应检测技术现在已经足够成熟,并广泛应用于流感病毒的快速诊断。目前商用的流感病毒检测试剂盒主要包括用于检测病毒核蛋白抗原的酶联免疫分析法,以及用于检测甲型流感病毒基质基因的实时逆转录定量聚合酶链反应。但当前并未有快速、有效的特异性检测h4亚型禽流感病毒方法,因而开发一种快速、灵敏、有效的h4亚型禽流感病毒检测产品势在必行,这能促进更早更广泛的发现h4亚型禽流感病毒感染,控制疫情扩散。
技术实现要素:
4.本发明的目的是提供一组针对h4亚型禽流感病毒血凝素基因的特异性引物和探针,能特异性检测h4亚型禽流感病毒。
5.本发明的第二个目的提供一种h4亚型禽流感病毒荧光定量rt-pcr检测试剂盒,具有特异性好、灵敏度高、准确性好、检测速度快、操作简便等特点。通过以下步骤和技术方案实现:
6.设计特异性引物与探针:根据h4血凝素基因保守区域设计了一组针对h4亚型禽流感病毒血凝素基因的检测引物与探针,包括两条引物和一条探针,序列分别是:
7.上游引物:h4-f:5
’‑
gacccarggatacaaggaca-3’(seq id no.1),
8.下游引物:h4-r:5
’‑
aaatgcaaatctggcacc-3’(seq id no.2);
9.探针:h4-p:5
’‑
cy5-ttgtgggcttgtc-mgb-3’(seq id no.3),h4-p的5’端进行报告荧光染料cy5标记, 3’端进行荧光淬灭基团mgb标记。
10.h4亚型禽流感病毒荧光定量rt-pcr检测试剂盒(探针法)包括两条引物和一条探针,序列分别是:
11.上游引物:h4-f:5
’‑
gacccarggatacaaggaca-3’(seq id no.1),
12.下游引物:h4-r:5
’‑
aaatgcaaatctggcacc-3’(seq id no.2);
13.探针:h4-p:5
’‑
cy5-ttgtgggcttgtc-mgb-3’(seq id no.3),h4-p的5’端进行报告荧光染料cy5标记, 3’端进行荧光淬灭基团mgb标记。
14.h4亚型禽流感病毒荧光定量rt-pcr检测试剂盒(探针法)除包含上述特异性引物和探针外,还包括一步法荧光定量pcr反应缓冲液、一步法荧光定量pcr反应混合酶和无核酸酶水。
15.具体的,试剂盒包括10微升一步法荧光定量pcr反应缓冲液、1微升一步法荧光定量pcr反应混合酶、0.5 微升10微摩尔的h4-f、0.5微升10微摩尔的h4-r、0.5微升10微摩尔的h4-p、2微升模板、5.5微升无核酸酶水,总反应体系为20微升,其中模板为阳性对照、阴性对照或待检样本。
16.h4亚型禽流感病毒荧光定量rt-pcr检测试剂盒(探针法)的检测方法如下:
17.1)利用核酸提取试剂从待测样本中提取rna。
18.2)利用检测试剂盒中提供的引物与探针、一步法荧光定量pcr反应缓冲液、一步法荧光定量pcr反应混合酶和无核酸酶水进行荧光定量rt-pcr反应,扩增核酸。
19.3)荧光定量rt-pcr反应扩增条件:第一阶段,反转录:55摄氏度,15分钟;第二阶段,预变性:95摄氏度, 30秒;第三阶段,pcr扩增:95摄氏度,5秒;60摄氏度,34秒,40个循环,每次循环第三阶段60摄氏度扩增后采集荧光信号,选择荧光通道cy5。
20.4)根据ct值判断荧光定量rt-pcr检测结果,判定样品中是否含有h4亚型禽流感病毒。
21.本发明的另一个目的是提供含检测h4亚型禽流感病毒的特异性引物和探针的特异性检测试剂盒的应用,在含有h4亚型禽流感病毒的体液、尿囊液或其他环境样本中的检测。
22.本发明的优点在于提供了一种检测h4亚型禽流感病毒的荧光定量rt-pcr试剂盒。使用h4亚型禽流感病毒血凝素基因特异性引物和探针,通过一步法荧光定量rt-pcr快速检测h4亚型禽流感病毒,反应在一管内完成,操作方便,并降低了污染风险,实现h4亚型禽流感病毒的快速检测。该荧光定量rt-pcr试剂盒对h4禽流感病毒具有良好的特异性、敏感性和重复性,为临床诊断、检验检疫等领域的流感疫情早期预警机制提供了可行的技术支持。
23.本发明具有操作简单、检测时间短、特异性强、准确率高等优点。本发明为临床样本中h4亚型禽流感病毒感染的辅助诊断提供了有效的工具,并可推广应用于临床和实验研究。
24.说明书附图
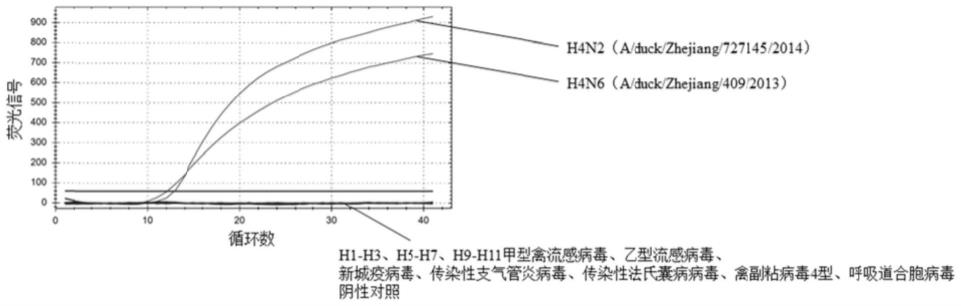
25.图1为h4亚型禽流感病毒荧光定量rt-pcr检测试剂盒的特异性。
26.图2为h4亚型禽流感病毒荧光定量rt-pcr检测试剂盒的灵敏度。
27.图3为h4亚型禽流感病毒荧光定量rt-pcr检测试剂盒的重复性。
具体实施方式
28.下面结合具体实施例,进一步阐述本发明。应理解,这些实施例仅用于说明本发明而不用于限制本发明的范围。下述实施例中,如无特殊说明,所使用的实验方法均为常规方法;所采用试剂为市购。
29.实施例1.用该荧光定量rt-pcr进行h4亚型禽流感病毒的定性检测
30.本发明制备的h4亚型禽流感病毒荧光定量rt-pcr检测法可以用来检测h4亚型禽流感病毒,鉴定方法可以通过下述方法实现:
31.h4亚型禽流感病毒荧光定量rt-pcr检测法:
32.(1)设计特异性引物与探针:从美国国立卫生研究院genbank数据库(http://www.ncbi.nlm.nih.gov/genomes/flu/)中下载了3000条h4亚型禽流感病毒血凝素基因序列,根据保守区域设计了一组针对h4亚型禽流感病毒血凝素基因的检测引物与探针,包括两条引物和一条探针,序列分别是:
33.上游引物:h4-f:5
’‑
gacccarggatacaaggaca-3’(seq id no.1),
34.下游引物:h4-r:5
’‑
aaatgcaaatctggcacc-3’(seq id no.2);
35.探针:h4-p:5
’‑
cy5-ttgtgggcttgtc-mgb-3’(seq id no.3),h4-p的5’端进行报告荧光染料cy5标记, 3’端进行荧光淬灭基团mgb标记。
36.以上引物与探针均委托北京擎科生物科技有限公司合成。
37.(2)荧光定量rt-pcr反应体系建立:包括一步法荧光定量pcr反应缓冲液10微升、一步法荧光定量pcr 反应混合酶1微升、10微摩尔的h4-f 0.5微升、10微摩尔的h4-r 0.5微升、10微摩尔的h4-p 0.5微升、模板2微升、无核酸酶水5.5微升,总反应体系为20微升,其中模板可以为阳性对照、阴性对照或待检样本。
38.荧光定量rt-pcr反应条件:第一阶段,第一阶段,反转录:55摄氏度,15分钟;第二阶段,预变性:95 摄氏度,30秒;第三阶段,pcr扩增:95摄氏度,5秒;60摄氏度,34秒,40个循环,每次循环第三阶段60 摄氏度扩增后采集荧光信号,选择荧光通道cy5。
39.(3)荧光定量rt-pcr检测方法:
①
按之江生物核酸提取试剂盒(磁珠法)说明书要求从待检样本中提取rna;
②
荧光定量rt-pcr试剂准备:取出pcr反应缓冲液、pcr反应混合酶、探针、引物、模板和水,室温融化后震荡,离心数秒后按上述比例进行配置;
③
将20微升的反应混合液震荡离心后上机,按上述反应条件进行检测;
④
收集荧光信号,记录实验结果
40.(4)结果判读:
①
基线与阈值设定:基线通常按照仪器自动设置的基线即可,或者选择刚好超过阴性对照品检测荧光曲线的最高点作为基线;
②
质控标准:阴性对照无明显扩增曲线,阳性对照的cy5检测通道有明显的s型扩增曲线,同时满足以上两个条件,实验结果有效可进行结果判定,否则实验无效;
③
结果判定:阳性: ct值≤36,且有s型扩增曲线;阴性:无ct值或未检出;可疑:36<ct值≤40,可将样品重新进行实验,或重新采样进行实验。
41.(5)确定荧光定量rt-pcr试剂盒检测h4亚型禽流感病毒的特异性:取不同亚型的禽流感病毒,包括 a/duck/zhejiang/d1/2013(h1n2)、a/duck/zhejiang/465/2013(h2n7)、a/duck/zhejiang/4613/2013(h3n2)、 a/duck/zhejiang/727145/2014(h4n2)、a/duck/zhejiang/409/2013(h4n6)、a/duck/zhejiang/224/2011(h5n1)、 a/chicken/zhejiang/1664/2017(h6n1)、a/chicken/zhejiang/92752/2015(h7n3)、 a/duck/zhejiang/1026120/
2015(h7n9)、a/chicken/zhejiang/221/2016(h9n2)、 a/chicken/zhejiang/2cp8/2014(h10n7)、a/duck/zhejiang/727d2/2013(h11n3),乙型流感病毒(b/phuket/3073/2013),新城疫病毒,传染性支气管炎病毒,传染性法氏囊病病毒,禽副粘病毒4型和呼吸道合胞病毒并提取rna。检测结果表明,荧光定量rt-pcr检测对h4亚型禽流感病毒具有较好的特异性。
42.结果见附图1。
43.(6)确定荧光定量rt-pcr试剂盒检测h4亚型禽流感病毒的灵敏度:使用合成的h4n2亚型(a/duck/zhejiang/727145/2014)禽流感病毒的dna质粒为模板,并进行10倍倍比稀释(108、107、106、105、 104、103、102、101、100拷贝每微升),并进行荧光定量rt-pcr检测。结果显示:本发明的荧光定量rt-pcr方法的检测限为10拷贝每微升,具有较高的灵敏度。
44.结果见附图2。
45.(7)评估荧光定量rt-pcr试剂盒检测h4亚型禽流感病毒的重复性:
①
使用三个不同浓度的dna质粒模板(106、104、102拷贝每微升),在一次实验中设置三个复孔以评估荧光定量rt-pcr试剂盒的批内差异。
②
使用三个不同浓度的dna质粒模板(106、104、102拷贝每微升),重复进行三次实验评估荧光定量rt-pcr试剂盒的批间差异。结果显示:本发明的荧光定量rt-pcr方法具有较好的重复性。
46.结果见附图3。
47.本发明的荧光定量rt-pcr检测方法具有快速、特异、便捷等优点,具有良好的临床应用前景。
48.应理解,本发明是结合最佳实施例进行描述的,然而在阅读了本发明的上述内容后,本领域技术人员可以对本发明作各种改动或修改,这些等价形式同样落于本技术所附权利要求书所限定的范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1