一种对甲状腺微小乳头状癌进行分子分型的方法以及分子标志物应用与流程
本发明涉及精准医疗,具体地,涉及一种对甲状腺微小乳头状癌进行分子分型的方法以及分子标志物应用。
背景技术:
1、甲状腺微小乳头状癌是指最大径小于等于10mm的甲状腺乳头状癌,近年来甲状腺癌发病率的急剧上升主要是因为甲状腺微小乳头状癌的检出。2015年, ata指南建议对低危的甲状腺微小乳头状癌进行随访以避免不必要的手术,但部分患者会出现淋巴结甚至远处转移,导致大部分临床医生和患者并不主张进行随访。因此,对甲状腺微小乳头状癌患者的处理现阶段仍存在挑战。
2、甲状腺微小乳头状癌是一种受环境和基因影响的多因素疾病,目前已知的主要因素包括电离辐射暴露、肥胖、基因以及表观遗传学的变异等。目前发现的 braf、ras、ret等基因主要聚焦于甲状腺乳头状癌,单独以甲状腺微小乳头状癌作为研究对象的研究极少,尚不足以较为完整地揭示甲状腺微小乳头状癌发生发展等病理生理过程。此外,免疫治疗近年来在临床上受到越来越多的关注,在甲状腺乳头状癌中也有所进展。有研究对晚期甲状腺乳头状癌患者进行了帕博丽珠单抗治疗,部分患者治疗效果令人欣喜,但这些患者占比并不大,这可能是患者的免疫异质性造成的,需要更多的分子标志物来筛选对免疫治疗敏感的患者。
技术实现思路
1、本发明克服了现有技术的不足,提供了一种甲状腺微小乳头状癌分型的分类方法和分子标志物应用。
2、为了达到上述目的,本发明采用的技术方案为:
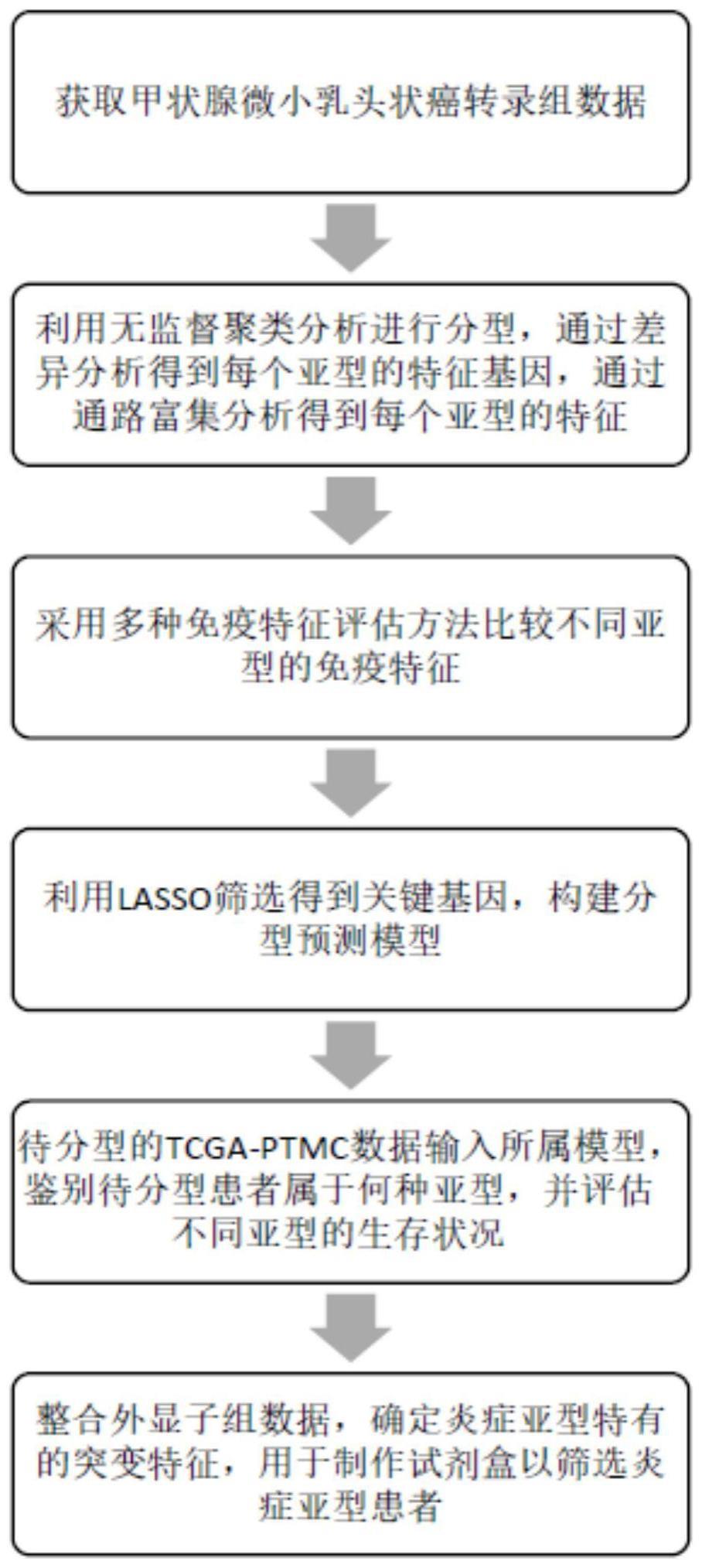
3、一种对甲状腺微小乳头状癌进行分子分型的方法,包括以下步骤:
4、s1数据获取:对甲状腺微小乳头状癌组织进行全转录组测序,得到甲状腺微小乳头状癌基因表达数据集,下载28例甲状腺微小乳头状癌患者的临床数据和转录组数据,下载58例正常甲状腺组织的转录组数据;
5、s2分子分型:通过无监督聚类算法进行分子分型,根据轮廓分数确定最佳分类为2,通过差异分析,得到每个亚型的特征基因;
6、s3分型定义:对每个亚型的特征基因进行通路富集分析,根据其功能将两种亚型定义为炎症型和侵袭型;
7、s4免疫评估:利用不同免疫相关基因集进行单样本富集分析来评估两种亚型的免疫状态,并采用反卷积法对两种亚型的免疫细胞浸润丰度进行评估,最后对免疫检查点治疗相关基因的表达情况进行分析来评估两种亚型对免疫检查点治疗的敏感性;
8、s5模型构建:利用lasso筛选得到符合预设条件的关键基因,构建分型预测模型;
9、s6模型评估:利用roc曲线和auc值评估模型的预测能力,并根据约登指数确定分类最佳截断值;
10、s7模型验证:将待分类的甲状腺微小乳头状癌患者数据输入s5构建的模型中,鉴别待分类患者的亚型种类并再次通过免疫评估步骤评估分类的准确性,最后通过生存分析评估不同亚型的生存状态。
11、在本发明的一个较佳实施例中,进一步包括,在s2中,分型的过程中采用的数据通过r语言deseq2包标准化并进行对数转换,方法是r语言sc3包,所用基因为标准差排序前5000个基因,每个亚型的特征基因定义为校正p值小于 0.05。
12、在本发明的一个较佳实施例中,进一步包括,在s3中,分型定义的过程中采用的是r语言clusterprofiler包,所用基因为每个亚型的特征基因,采用默认的参数,以校正p值小于0.05作为其显著通路的截断值。
13、在本发明的一个较佳实施例中,进一步包括,在s4中,免疫评估的过程中采用r语言estimate包、immunedeconv包、gsva包,并采用秩和检验对比两种亚型免疫特征得分和免疫相关基因的表达量,以p值小于0.05作为两组具有统计学显著差异的截断值。
14、在本发明的一个较佳实施例中,进一步包括,在s5中,两个数据集经过标准化和对数转换后的基因表达量采用r语言sva包进行批次效应的去除,然后将所有亚型的特征基因的经过处理的表达量纳入lasso回归分析,通过r语言 glmnet包选择系数不为0的基因构建筛选模型并计算诊断风险得分;
15、其中公式为:风险得分=28.09977752- 0.98758679*ccni-1.53712485*pg rmc2-0.52919630*synpo-0.43810986*rab27a -1.00260392*rasa1 -0.06439753*lamc1 -0.28431350*eh d2 +0.16597787*igkv4-1+0.34026915*igkv1d-39 +0.10677938*igkv3-11 +0.58545336*ighv3-21 +0.16645968*ighv3-30 +0.41399296*st6gal1 +0.68858130*cxcr4+0.17401608*rgs1+0.37281935*oas2+0.03731571*ifi44l。
16、在本发明的一个较佳实施例中,进一步包括,s6中,依据s5风险评分公式计算各患者的风险评分,并利用r语言predict函数预测患者为炎症型的概率,然后使用roc曲线分析以评估模型的预测能力,最后通过约登指数来确定分类最佳截断值,最佳截断值为0.494。
17、在本发明的一个较佳实施例中,进一步包括,s7中,将待分类的甲状腺微小乳头状癌患者的处理过的基因表达量输入所述模型计算每个患者的得分,并根据最佳截断值将其分为炎症型和非炎症型,然后对两组进行免疫评估,其采用的是r语言estimate包、immunedeconv包、gsva包,并采用秩和检验对比两组免疫特征得分和免疫相关基因的表达量,以p值小于0.05作为两组具有统计学显著差异的截断值,然后采用r语言survival包对两组患者无进展生存进行分析,计算两组的5年无进展生存率。
18、在本发明的一个较佳实施例中,进一步包括,一组用于筛选甲状腺微小乳头状癌炎症亚型的分子标志物,其特征在于,所述分子标志物包括:afp突变、 igh@ext融合、tg融合、tpte2融合、ifrd1融合;
19、所述分子标志物按照如下方法对甲状腺微小乳头状癌免疫亚型进行筛选: s 101数据获取:对甲状腺微小乳头状癌患者癌和癌旁组织进行全外显子组测序和全转录组测序,得到甲状腺微小乳头状癌体细胞突变数据集和基因融合数据集;s102驱动基因筛选:采用mutsigcv算法选择显著突变的基因作为驱动突变基因,并采用star-fusion流程选择可信度高的融合基因并采用rt–pcr对其进行验证; s103炎症亚型分子标志物确定:对驱动基因和分子分型进行关联型分析,将只出现在炎症亚型的驱动基因作为甲状腺微小乳头状癌炎症亚型的分子标志物;当甲状腺微小乳头状癌患者出现afp突变、igh@ext融合、tg融合、tpte2融合、 ifrd1融合任一种情况时,其对免疫抑制剂治疗敏感。
20、在本发明的一个较佳实施例中,进一步包括,s102中,所述驱动基因筛选的过程中,显著突变基因的确定采用的是mutsigcv(v.1.41)算法,输入的数据为每个患者的体细胞突变数据(maf文件),以q小于0.1作为截断值;融合基因的确定采用的是star-fusion(v.1.6.0)算法,输入的数据为每个患者的转录组测序数据,过滤标准包括:含有线粒体或hla伴侣基因、涉及两个免疫球蛋白基因片段、在正常样本中被检测到、每m reads中支持融合的片段数小于0.1,过滤后并采用rt-pcr方法对筛选的融合基因进行验证;
21、在本发明的一个较佳实施例中,进一步包括,一种甲状腺微小乳头状癌炎症亚型评估试剂盒,其特征在于,所述试剂盒包括权利要求9-11中任一项所述的甲状腺微小乳头状癌炎症亚型评估试剂。
22、优选的,步骤2)中,所述驱动基因筛选的过程中,显著突变基因的确定采用的是mutsigcv(v.1.41)算法,输入的数据为每个患者的体细胞突变数据(maf 文件),以q小于0.1作为截断值;融合基因的确定采用的是star-fusion(v.1.6.0) 算法,输入的数据为每个患者的转录组测序数据,过滤标准包括:含有线粒体或 hla伴侣基因、涉及两个免疫球蛋白基因片段、在正常样本中被检测到、每m reads中支持融合的片段数小于0.1,过滤后并采用rt-pcr方法对筛选的融合基因进行验证。
23、本发明还提供了前面所述的分子标志物在制备甲状腺微小乳头状癌分型评估试剂或试剂盒中的应用。
24、本发明还提供了一种甲状腺微小乳头状癌分型评估试剂,所述试剂能够检测样本中前面所述的分子标志物的突变情况。
25、本发明还提供了一种甲状腺微小乳头状癌分型评估试剂盒,所述试剂盒包括前面任一所述的评估试剂。
26、本发明的有益效果:
27、本发明首先运用无监督聚类分析方法对转录组测序数据进行分析,得到了一个免疫激活且对干扰素γ敏感的炎症亚型,其相对于另一个亚型,表现为pd1、 pdl1、calt4的高表达以及cd8+t细胞的浸润,有助于为个体化治疗提供参考。然后利用lasso分析筛选得到符合预设条件的关键基因,建立预测分型的模型。并将待分类的tcga-ptmc患者数据输入所述模型,鉴别待分类的tcga-ptmc患者的亚型,并评估不同亚型的生存状况。本发明进一步采用联合分析的方法,结合体细胞突变数据,构建了一组基因集合来筛选甲状腺微小乳头状癌炎症亚型患者,其只在炎症亚型患者中存在突变或者融合,包括afp、igh@ext、tg、tpte2、ifrd1 5个基因,可用于制作试剂盒以筛选对ici治疗敏感的甲状腺微小乳头状癌患者。
- 还没有人留言评论。精彩留言会获得点赞!