一种金属有机框架材料及其制备方法和应用与流程
1.本发明涉及一种金属有机框架材料及其制备方法和应用,属于生物传感器技术领域。
背景技术:
2.癌胚胎抗原检测作为结直肠癌诊疗的一个重要指标,对结直肠癌的诊断、治疗、转移、复发具有重要的指导价值,因此建立一种迅速、灵敏、可靠的癌胚胎抗原检测方法至关重要。目前针对癌胚胎抗原的检测方法主要有酶联免疫吸附法、放射性免疫法以及化学发光免疫法,但这些方法检测时间长、不易操作、有放射性污染问题,使癌胚胎抗原的检测受到了很大制约。于是人们将免疫分析法的稳健性和简单性与电化学方法固有的高灵敏度相结合,提供了一种可靠的生物传感器开发的策略。
3.电化学免疫传感器作为一种新型的生物传感器,以其鉴定物质的高度敏感性、特异性和稳定性受到人们的关注,此外,电化学免疫传感器将传统的免疫测试和生物传感技术融为一体,减少了分析时间,提高了测试的灵敏度和精度,兼具测定过程简单,特异性强等优势,已经在临床诊断、环境监测、食品安全等领域得到广泛应用。但目前的电化学免疫传感器仍需解决多目标同时检测能力的问题,并进一步排除生物样品中干扰组分在电极表面的非特异性吸附会带来的干扰。因此,聚焦解决电化学免疫传感器的重现性差、抗干扰能力弱等问题是该研究领域面临的重要课题。
4.金属有机框架材料(metal organic frameworks,mofs)是由金属离子和有机配体高度有序地连接而成的多孔有序纳米材料,在气体储存、生物医学、催化等领域具有广泛的应用前景。在作为电极材料使用时,其多孔、高比表面积和优异的导电性等使mofs在传感应用中具有非常大的发展潜力。因此,提供一种金属有机框架材料,并将其作为电化学免疫传感器的核心材料,实现电化学免疫传感器对癌胚胎抗原的高灵敏度的检测,并展现出优异的重现性和抗干扰力,在临床诊断以及生物测定分析中是十分必要的。
技术实现要素:
5.本发明为了解决现有电化学免疫传感器的重现性差、抗干扰能力弱等问题,提供一种金属有机框架材料及其制备方法,并将其作为电化学免疫传感器的核心材料,实现电化学免疫传感器对癌胚胎抗原的高灵敏度的检测,并展现出优异的重现性和抗干扰力。
6.本发明的技术方案:本发明的目的之一是提供一种金属有机框架材料,该材料简称为mof-et4,化学式为[sm2(l)3],式中l为c
92h58
o8。
[0007]
本发明的目的之二是提供上述金属有机框架材料的制备方法,该方法为:将smcl3•
6h2o、配体和苯甲酸加入到n, n-二甲基甲酰胺中,超声处理10min,再在120℃下加热12h,依次经过离心、洗涤和干燥处理,得到mof-et4。
[0008]
进一步限定,smcl3•6h2o、配体、苯甲酸和n, n-二甲基甲酰胺的配比为44mg:48mg:
500mg:5ml。
[0009]
进一步限定,smcl3•
6h2o的浓度为0.172mmol/l。
[0010]
进一步限定,配体的结构为: 。
[0011]
进一步限定,配体的制备方法包括以下步骤:s1,将1,3,6,8-四(频哪酯基)芘、4,4
’‑
二溴联苯、四(三苯基膦)钯和碳酸钾加入到混合溶液中,在氩气保护下,加热反应,反应完成后,将有机相旋干,再使用洗脱剂进行硅胶柱层析,得到黄色固体,命名为中间体1;s2,将4-甲氧羰基苯硼酸、中间体1、四(三苯基膦)钯、磷酸三钾和二氧六环混合,在氮气的保护下密封,然后放置在油浴中搅拌反应,反应结束后分离有机相并用水洗涤,再用氯仿萃取3次,然后将有机相旋干,得到的残渣在四氢呋喃中加热煮沸2h并趁热过滤,得到的黄色固体,命名为中间体2;s3,将中间体2加入到含有氢氧化钠的四氢呋喃/水混合液中,回流搅拌反应5h,反应结束后旋干溶剂,向残留物中加入水,在25℃下搅拌2h,然后调节ph至1,过滤,使用水洗涤后将粗产物用n, n-二甲基甲酰胺重结晶,过滤,真空干燥,得到黄色固体即为配体。
[0012]
更进一步限定,s1中1,3,6,8-四(频哪酯基)芘、4,4
’‑
二溴联苯、四(三苯基膦)钯和碳酸钾的摩尔比为0.71:7.05:0.04:14.5。
[0013]
更进一步限定,s1中混合溶液由甲苯和水按照体积比为1:1的比例混合制成。
[0014]
更进一步限定,s1中加热反应温度为105℃,时间为24h。
[0015]
更进一步限定,s1中洗脱剂由正己烷和甲苯按照体积比为3:1的比例混合制成。
[0016]
更进一步限定,s2中4-甲氧羰基苯硼酸、中间体1、四(三苯基膦)钯、磷酸三钾和二氧六环的配比为5.8mmol:5.8mmol:0.02mmol:10ml:2.65mmol。
[0017]
更进一步限定,s2中油浴中反应温度为130℃,时间为72h。
[0018]
更进一步限定,s3中四氢呋喃/水混合液中四氢呋喃和水的体积比为1:1。
[0019]
更进一步限定,s3中中间体2、氢氧化钠和四氢呋喃/水溶液的配比为0.39mmol:18.75mmol:100ml。
[0020]
本发明的目的之三是提供上述金属有机框架材料的应用,具体的用于电化学免疫传感器用电极材料。
[0021]
本发明的目的之四是提供一种电化学免疫传感器,包括电极基体和修饰在电极基体表面的上述金属有机框架材料,金属有机框架材料上涂覆有癌胚抗原特异性单克隆抗体。
[0022]
进一步下限定,电化学免疫传感器的线性范围为0.005至100 u ml-1
,最低的检测限值为0.0029 u ml
−1(s/n=3)。
[0023]
本发明具有以下有益效果:本发明提供一种新型金属有机框架材料,将其作为电化学免疫传感器的电极材料用于癌胚胎抗原检测,该电化学免疫传感器的线性范围为0.005至100 u ml-1
,最低的检测限值为0.0029 u ml
−1(s/n=3)。该传感器重复检测的相对标准偏差仅为0.69%,而且加入干扰物质后的响应电流值与单一癌胚胎抗原的响应电流基本一致,相对标准偏差为0.72%,是目前金属有机框架材料在癌胚胎抗原检测的相关报道中灵敏度最高、重现性以及抗干扰力最好的电化学免疫传感器材料,具有良好的应用前景。此外,本发明提供的金属有机框架材料合成方法还具有工艺简单、条件温和等优点。
附图说明
[0024]
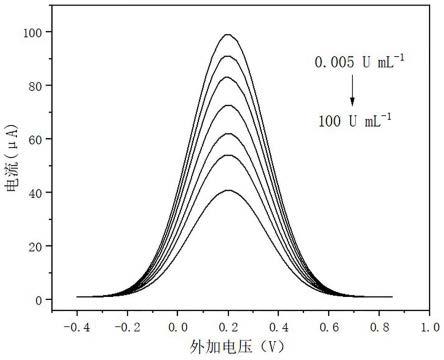
图1为制备金属有机框架材料的配体的合成路线;图2为电化学免疫传感器的响应性测试结果;图3为dpv峰值电流与浓度的校对曲线;图4为电化学免疫传感器的重现性测试结果;图5为电化学免疫传感器的抗干扰性测试结果。
具体实施方式
[0025]
为了使本发明的目的、技术方案及优点更加清楚明白,以下结合附图及实施例,对本发明进行进一步详细说明。应当理解,此处所描述的具体实施例仅仅用以解释本发明,并不用于限定本发明。下面将结合附图对本发明的技术方案进行清楚、完整地描述,显然,所描述的实施例是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
[0026]
此外,下面所描述的本发明不同实施方式中所涉及的技术特征只要彼此之间未构成冲突就可以相互结合。
[0027]
下述实施例中所使用的实验方法如无特殊说明均为常规方法。所用材料、试剂、方法和仪器,未经特殊说明,均为本领域常规材料、试剂、方法和仪器,本领域技术人员均可通过商业渠道获得。
[0028]
下述实施例使用的原料1,3,6,8-四(频哪酯基)芘(cas:1398053-00-3)、4,4
’‑
二溴联苯(cas:92-86-4)、4-甲氧羰基苯硼酸(cas:99768-12-4)均从sigma-aldrich公司直接
采购获得。
[0029]
实施例1:本实施例制备金属有机框架材料cof-et4的过程如下:(1)如图1所示,合成配体1:
①
合成中间体1:向20毫升甲苯和20毫升水的混合溶液中依次加入1,3,6,8-四(频哪酯基)芘(原料1,0.5克,0.71毫摩尔)、4,4
’‑
二溴联苯(原料2,2.2克,7.05毫摩尔)、四(三苯基膦)钯(46毫克,0.04毫摩尔)和碳酸钾(0.2克,14.5毫摩尔),在氩气保护下105℃加热反应24小时。然后将有机相旋干,以正己烷:甲苯(v/v=3:1)为洗脱剂进行硅胶柱层析,得到黄色固体0.69克,即为中间体1,收率为86%。
[0030]
对获得的中间体1进行结构表征:《1》核磁表征鉴定结果:氢谱:1h nmr (400 mhz, cdcl3): δ 8.03 (m, 10 h), 7.72 (d, 8 h), 7.55 (d, 4 h), 7.45 (m, 16 h)。
[0031]
碳谱:
13
c nmr (100 mhz, cdcl3): δ 140.55, 139.63, 137.80, 137.79, 136.82, 135.98, 133.17, 131.94, 131.85, 131.50, 129.63, 128.62, 128.46, 128.03, 126.92, 125.13, 124.99, 124.78, 122.04。
[0032]
《2》质谱表征结果:esi(m/z): [m+h]
+ calcd. for c
64h38
br4, 1126.62; found, 1127.14。
[0033]
《3》元素分析测试结果:calcd. for c
64h38
br4, c, 68.23, h, 3.4; found, c, 69.15, h, 4.1。
[0034]
综上可知,获得的中间体1的结构如下: 。
[0035]
②
合成中间体2:向30毫升密封管中依次加入4-甲氧羰基苯硼酸(1.04克,5.8毫摩尔)、中间体1
(0.55克,0.485毫摩尔)、四(三苯基膦)钯(原料3,0.02克,0.02毫摩尔)和磷酸三钾(0.55克,10毫升)、二氧六环(15毫升,2.65毫摩尔),并在氮气的保护下密封。然后将该混合物放置在油浴中,在130
°
c下搅拌反应72小时,反应结束后有机相用水洗涤,再用氯仿萃取3次,每次50毫升,有机相旋干后得到的残渣在四氢呋喃中加热煮沸2小时并趁热过滤,得到的黄色固体0.53克,即为中间体2,收率为82%。
[0036]
对获得的中间体2进行结构表征:《1》核磁表征鉴定结果:氢谱:1h nmr (400 mhz, cdcl3): δ 8.12 (m, 16 h), 7.88 (d, 8 h), 7.74 (d, 8 h), 7.5 (d, 2 h), 7.33 (d, 8 h), 7.22 (m, 12 h)。
[0037]
碳谱:
13
c nmr (100 mhz, cdcl3): δ 166.66, 144.41, 140.93, 137.80, 137.79, 136.82, 135.98, 133.17, 131.85, 131.50, 130.39, 130.13, 129.83, 129.63, 128.62, 128.03, 126.92, 125.13, 124.99, 124.78, 52.07。
[0038]
《2》质谱表征结果:esi(m/z): [m+h]
+ calcd. for c
96h66
o8, 1347.58; found, 1348.14。
[0039]
《3》元素分析测试结果:calcd. for c
96h66
o8, c, 85.57, h, 4.94, o, 9.5; found, c, 85.12, h, 5.3, o, 9.1。
[0040]
综上可知,获得的中间体2的结构如下: 。
[0041]
③
合成配体1:向250毫升圆底瓶中依次加入中间体2(0.5克,0.39毫摩尔),再加入100毫升含有氢氧化钠(0.75克,18.75毫摩尔)的四氢呋喃/水(v/v=1:1)混合溶液,并回流搅拌5小时。旋
干溶剂后向残留物中加入50毫升水, 25℃下搅拌2小时,再用1摩尔/升的盐酸调整ph值至1。过滤,并用水洗涤。然后将粗产物用n, n-二甲基甲酰胺重结晶,过滤后真空干燥,得到黄色固体0.46克,即为所需配体,收率为91%。
[0042]
对获得的配体1进行结构表征:《1》核磁表征鉴定结果:氢谱:1h nmr (400 mhz, dmso): δ 8.23 (d, 8 h), 8.13 (d, 8 h), 7.88 (d, 8 h), 7.72 (d, 8 h), 7.5 (d, 2 h), 7.32 (d, 8 h), 7.21 (m, 12 h)。
[0043]
碳谱:
13
c nmr (100 mhz, dmso): δ 167.69, 144.13, 140.93, 137.68, 137.60, 136.38, 135.32, 132.44, 131.07, 130.86, 130.23, 129.63, 129.61, 128.55, 127.91, 126.71, 126.66, 125.08, 124.99, 124.95。
[0044]
《2》质谱表征结果:esi(m/z): [m+h]
+ calcd. for c
92h58
o8, 1291.47; found, 1292.03。
[0045]
《3》元素分析测试结果:calcd. for c
92h58
o8, c, 85.56, h, 4.53, o, 9.91; found, c, 85.12, h, 4.9, o, 9.1。
[0046]
综上可知,获得的配体1的结构如下: 。
[0047]
(2)合成金属有机框架材料mof-et4:将smcl3•
6h2o(44毫克,0.172毫摩尔/升)、配体(48毫克,0.037毫摩尔)和500毫克苯甲酸加入到5毫升的n, n-二甲基甲酰胺中,然后将混合物超声处理10分钟,再在高压釜中以120℃进行溶剂热处理12小时,反应体系使用离心机以10000转/分钟的转速离心20分钟,固体过滤后在30毫升的乙醇中浸泡12小时,然后用丙酮洗涤3次,每次10毫升。最后在100℃下真空干燥,得到mof-et4。
[0048]
对获得的mof-et4进行结构表征:《1》将合成的mof-et4晶体存在玻璃毛细管中,采用单晶体x射线进行了晶体结构的测试,仪器为bruker-apexⅱ型ccd探测器,用cu kα (λ=1.54178
åꢀ
)x射线源采集。数据是sadabs程序对吸收进行校正,没有对消光或衰变进行校正。用shelxtl软件包直接求解,测试结果见表1。
[0049]
表1
(3)采用上述制备获得的金属有机框架材料mof-et4制备电化学免疫传感器:将裸玻璃碳电极(gce)用粒径为0.3微米的氧化铝粉末抛光,并在水中超声5分钟,然后将10微升5毫克/毫升的mof-et4分散在5%的壳聚糖溶液中,滴在清洗过的裸玻璃碳电极上,干燥。再将10微升(0.1 u ml
−1)的癌胚抗原特异性单克隆抗体(anti-cea)涂覆在mof-et4/gce电极表面,在4℃下孵育25分钟,用磷酸盐缓冲液(ph=7)洗涤。为了阻断传感器上的
非特异性结合位点,加入5微升的1%牛血清白蛋白(bsa),在4℃下孵育30分钟,再用磷酸盐缓冲液(ph=7)洗涤,即制备得到电化学免疫传感器。
[0050]
对获得的电化学免疫传感器进行性能表征:《1》电化学免疫传感器的响应性测试:采用差分脉冲伏安法研究电化学免疫传感器对癌胚胎抗原(cea)的响应,电位范围为-0.2 v~0.6 v,电位增量为0.004 v,脉冲幅值为0.05 v,脉冲宽度为0.2 s,样品宽度为0.0167 s,脉冲周期为0.5 s。
[0051]
将电化学免疫传感器插入到待测不同浓度的癌胚胎抗原中,当电极中的抗体与待测的癌胚胎抗原(cea)结合后,会引起电极表面膜和溶液交界面电荷密度的改变,产生膜电位的变化。
[0052]
响应性测试结果如图2所示,由图2可知,当抗原浓度增加时,峰值电流反而减小,这是由于额外的蛋白质分子阻碍了电子的转移。
[0053]
图3是电化学免疫传感器与cea浓度之间的线性关系,线性范围为0.005至100 u ml-1
,相应的线性方程分别为i=-3.8033
×ccea
+98.895(r2=0.9932)和i=-0.5941
×ccea
+96.542(r2=0.9913),最低的检测限(lod)值为0.0029 u ml
−1(s/n=3),可以证明,该电化学免疫传感器具有更宽的检测范围和更低的检测限,这是由于mof-et4材料具有良好的导电性,为抗原提供了更多的结合位点,所以该电化学免疫传感器具有优异的灵敏度。
[0054]
《2》电化学免疫传感器的重现性测试:重现性是电化学免疫传感器的重要性能指标,采用与(3)相同的方法制备了5个电化学免疫传感器,将电化学免疫传感器插入到0.1 u ml-1
的cea中,并且对每个传感器进行5次重复检测。
[0055]
测试结果如图4所示,通过计算可得到其相对标准偏差为0.69%,可以证明,采用金属有机框架材料mof-et4制备的电化学免疫传感器具有良好的重现性。
[0056]
《3》电化学免疫传感器的抗干扰性测试:以癌抗原-125(ca-125),癌抗原19-9(ca 19-9),免疫球蛋白(lgg),甲胎蛋白(afp)为干扰物质,先在1 u ml
−1的cea中分别加入100 u ml
−1上述干扰物质,然后插入电化学免疫传感器进行检测。
[0057]
测试结果如图5所示,可以看出加入干扰物质的响应电流值与单一cea的响应电流基本一致,相对标准偏差为0.72%,说明其他分析物的干扰可以忽略不计,这证明该电化学免疫传感器具有良好的抗干扰能力。
[0058]
显然,上述实施例仅仅是为清楚地说明所作的举例,而并非对实施方式的限定。对于所属领域的普通技术人员来说,在上述说明的基础上还可以做出其它不同形式的变化或变动。这里无需也无法对所有的实施方式予以穷举。而由此所引伸出的显而易见的变化或变动仍处于本发明创造的保护范围之中。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1