一种基于β-乳糖苷酶响应的近红外一区多功能荧光链接体及制备方法和应用
一种基于
β-乳糖苷酶响应的近红外一区多功能荧光链接体及制备方法和应用
技术领域
1.本发明属于药物制备技术领域,涉及一种基于β-乳糖苷酶响应的近红外一区多功能荧光链接体及制备方法和应用
背景技术:
2.卵巢癌是妇科肿瘤中死亡率最高的,全世界每年有超过220,000名女性罹患该病。被称为“无声杀手”,这是由于其早期无明显症状而容易被忽视而得名。其中,靶向治疗是卵巢癌的经典治疗方法,但预后较差。因此,对卵巢癌的早期诊断和有效治疗对于延长患者的寿命至关重要。
3.荧光标记技术因其具有高灵敏度以及低毒性的特点而被广泛应用于生物体的标记示踪成像分析。因此,可以通过荧光标记技术实现对卵巢癌的标记成像分析。而当前的荧光标记技术通常是直接在靶向识别分子中引入荧光团构建荧光探针来实现标记示踪分析的。这样,必然会由于需要满足标记示踪条件所进行过量荧光探针引入的问题,往往会造成需要多次洗涤避免假阳性结果。与此同时,由于多次洗涤步骤的存在使得无法实现实时在体的监测示踪分析。
技术实现要素:
4.本发明的目的在于提供一种基于β-乳糖苷酶响应的近红外一区多功能荧光链接体及制备方法和应用,该基于β-乳糖苷酶响应的近红外一区多功能荧光链接体用于化学修饰靶向抗肿瘤药物分子,并且可以用于验证基于β-乳糖苷酶响应的近红外一区多功能荧光链接体构建的探针实现“诊疗一体化”的可行性。
5.为达到上述目的,本发明采用以下技术方案:
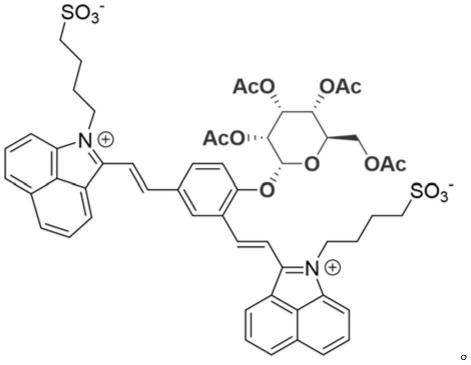
6.一种基于β-乳糖苷酶响应的多功能近红外一区荧光链接体,该荧光链接体结构式如下:
[0007][0008]
一种基于β-乳糖苷酶响应的多功能近红外一区荧光链接体的制备方法,包括以下
步骤:
[0009]
a)2,3,4,6-四-o-乙酰基-α-d-吡喃半乳糖与5-醛基水杨醛在k2co3的作用下,得到带有二醛基的中间体;
[0010]
b)4-(2-甲基-4-苯并[cd]吲哚-1-基)丁烷-1-磺酸盐与带有二醛基的中间体在(ch3co)2o作用下,得到基于β-乳糖苷酶响应的近红外一区多功能链接体,结构式如下:
[0011][0012]
进一步的,步骤a)的具体过程为:将2,3,4,6-四-o-乙酰基-α-d-吡喃半乳糖,5-醛基水杨醛和k2co3在dmf中于0℃下混合,然后在n2气氛下,进行反应,反应完成后,加入h2o,得到带有二醛基的中间体;
[0013]
步骤b)的具体过程为:将带有二醛基的中间体,4-(2-甲基-4-苯并[cd]吲哚-1-基)丁烷-1-磺酸盐以及乙酸钠溶于乙酸酐溶液中,于50℃下搅拌3h,得到基于β-乳糖苷酶响应的近红外一区多功能荧光链接体。
[0014]
进一步的,4-(2-甲基-4-苯并[cd]吲哚-1-基)丁烷-1-磺酸盐通过以下过程制得:
[0015]
1)1,2-氧硫烷2,2-二氧化物与环己酮苯并[cd]吲哚-2(1h)-酮在koh的作用下,得到4-(2-氧代-1,2-二氢苯并[cd]吲哚-1-鎓-1-基)丁烷-1-磺酸钠;
[0016]
2)4-(2-氧代-1,2-二氢苯并[cd]吲哚-1-鎓-1-基)丁烷-1-磺酸钠在四丁基氯化铵的作用下,得到4-(2-氧代-1,2-二氢苯并[cd]吲哚-1-鎓-1-基)丁烷-1-磺酸-四丁基铵盐;
[0017]
3)4-(2-氧代-1,2-二氢苯并[cd]吲哚-1-鎓-1-基)丁烷-1-磺酸-四丁基铵盐在ch3mgcl作用下,得到4-(2-甲基-4-苯并[cd]吲哚-1-基)丁烷-1-磺酸盐。
[0018]
进一步的,步骤1)的具体过程为:将1,2-氧硫烷2,2-二氧化物与koh溶于n-甲基-2-吡咯烷酮中,室温条件下搅拌30min,然后加入环己酮苯并[cd]吲哚-2(1h)-酮,然后于90℃下加热搅拌10h,得到4-(2-氧代-1,2-二氢苯并[cd]吲哚-1-鎓-1-基)丁烷-1-磺酸钠。
[0019]
进一步的,步骤2)的具体过程为:将4-(2-氧代-1,2-二氢苯并[cd]吲哚-1-鎓-1-基)丁烷-1-磺酸钠与四丁基氯化铵溶于乙酸溶液中,于90℃搅拌30min,然后滴加乙酸乙酯,滴毕后过滤,浓缩,得到4-(2-氧代-1,2-二氢苯并[cd]吲哚-1-鎓-1-基)丁烷-1-磺酸-四丁基氯化铵盐。
[0020]
进一步的,步骤3)的具体过程为:将4-(2-氧代-1,2-二氢苯并[cd]吲哚-1-鎓-1-基)丁烷-1-磺酸-四丁基氯化铵盐与ch3mgcl溶于无水四氢呋喃中,然后在氮气保护下,于60℃中搅拌1h,得到4-(2-甲基-4-苯并[cd]吲哚-1-基)丁烷-1-磺酸盐。
[0021]
一种如上所述的基于β-乳糖苷酶特异性响应的近红外一区荧光链接体在制备用于治疗肿瘤的诊疗一体化药物方面的应用。
[0022]
进一步的,抗肿瘤药物为抗肺癌、肝癌、卵巢癌或黑色素瘤的药物。
[0023]
一种如上所述的基于β-乳糖苷酶特异性响应的近红外一区荧光链接体在构建药物探针中的应用。
[0024]
与现有技术相比,本发明具有以下有益效果:
[0025]
本发明通过使用2,3,4,6-四-o-乙酰基-α-d-吡喃半乳糖、5-亚硝基水杨醛、1,2-氧硫烷-2,2-二氧化物与环己酮苯并[cd]吲哚-2(1h)-酮合成基于β-乳糖苷酶响应的多功能荧光链接体,该链接体分子能够化学修饰靶向抗肿瘤药物分子进而构建“诊疗一体化”药物,其进入体内,在肿瘤β-乳糖苷酶的催化下,荧光开启进行标记示踪,同时二硫键在肿瘤高还原条件下释放靶向抗肿瘤药物,从而实现诊疗一体化的目的。本发明的基于β-乳糖苷酶响应的近红外一区多功能荧光链接体制备方法简单,易于实现,并且应用范围广。
[0026]
本发明中的基于β-乳糖苷酶响应的近红外一区多功能荧光链接体可以对靶向抗肿瘤药物分子进行化学共价修饰构建“诊疗一体化”药物,进而通过肿瘤(肝癌、肺癌、乳腺癌、宫颈癌、黑色素瘤、神经胶质瘤)微环境的刺激,触发荧光点亮进行肿瘤部位的荧光标记,同时释放靶向抗肿瘤药物分子,从而达到对肿瘤的标记示踪以及治疗。利用该链接体所构建的探针分子可以改善纳米递送药物体系在诊疗一体化概念应用方面的生物毒性,同时扩充诊疗一体化概念的应用多元性。本发明的基于β-乳糖苷酶响应的近红外一区多功能荧光链接体能够用于构建“诊疗一体化”药物以及验证该药物在实现诊断与治疗一体化的可行性。
附图说明
[0027]
图1为本发明提供的基于β-乳糖苷酶响应的近红外一区多功能荧光链接体的合成路线图;
[0028]
其中,化合物1为2,3,4,6-四-o-乙酰基-α-d-吡喃半乳糖,化合物2为5-羟基水杨醛,化合物3为(2r,3r,4r,5r,6r)-2-(乙酰氧基甲基)-6-(2,4-二甲酰基苯氧基)四氢-2h-吡喃-3,4,5-三乙酸三酯,化合物4为环己酮苯并[cd]吲哚-2(1h)-酮,化合物5为1,2-氧硫烷2,2-二氧化物,化合物6为4-(2-氧代-1,2-二氢苯并[cd]吲哚-1-鎓-1-基)丁烷-1-磺酸钠,化合物7为4-(2-氧代-1,2-二氢苯并[cd]吲哚-1-鎓-1-基)丁烷-1-磺酸-四丁基铵盐,化合物8为试剂4-(2-甲基-4-苯并[cd]吲哚-1-基)丁烷-1-磺酸盐。试剂与条件:(a)tea,dcm,n2,0℃to 50℃,2h;(b)koh,rt,30min to 50℃,10h;(c)90℃,30min;(d)ch3mgcl,thf,n2,60℃,1h。
[0029]
图2为本发明提供的基于β-乳糖苷酶响应的近红外一区多功能bd7分子的合成路线图;
[0030]
图3为细胞成像图;其中,(a)为红光下双功能分子对卵巢癌细胞成像图,(b)为绿光下双功能分子对卵巢癌细胞成像图,(c)为蓝光下双功能分子对卵巢癌细胞成像图,(d)为图(a)-(c)三幅图的叠加,(e)为红光下双功能分子对人脐静脉血管内皮细胞成像图,(f)为绿光下双功能分子对人脐静脉血管内皮细胞成像图,(g)为蓝光下双功能分子对人脐静脉血管内皮细胞成像图,(h)为图(e)-(g)三幅图的叠加。
[0031]
图4为细胞增殖抑制效果考察图。
具体实施方式
[0032]
下面结合附图和具体的实施例对本发明做进一步的详细说明,所述是对本发明的解释而不是限定。
[0033]
为了实现对卵巢癌的高效特异性标记分子,可利用荧光特异性点亮的手段对其实现特异性标记。β-半乳糖苷酶(β-gal)是一种糖苷水解酶,可以水解半乳糖与其他部分形成的β-糖苷键。近年来,β-gal作为一种在原发性卵巢癌细胞和衰老细胞中过度表达的重要生物标志物已被广泛研究。据报道,β-gal的酶活性在卵巢癌细胞(如skov3细胞)中比在其他癌细胞和正常细胞中显着增强。因此,用于内源性β-gal可视化的荧光探针对于原发性卵巢癌细胞的诊断和监测具有重要价值。
[0034]
本发明中的室温为25℃,过夜为12h。
[0035]
本发明在小分子的基础上构建诊疗一体化分子,利用其实现标记及治疗的作用,以扩充诊疗一体化在癌症治疗方面的实现手段。
[0036]
本发明通过使用2,3,4,6-四-o-乙酰基-α-d-吡喃半乳糖、5-亚硝基水杨醛、1,2-氧硫烷-2,2-二氧化物与环己酮苯并[cd]吲哚-2(1h)-酮合成基于β-乳糖苷酶响应的近红外一区多功能荧光链接体,该链接体可以用于化学修饰靶向抗肿瘤药物分子构建“诊疗一体化”药物。
[0037]
本发明提供的基于β-乳糖苷酶响应的近红外一区多功能荧光链接体,其结构如下:
[0038][0039]
本发明所述的基于β-乳糖苷酶响应的近红外一区多功能荧光链接体名称如下:
[0040]
4,4'-(((1e,1'e)-(4-(((2r,3r,4r,5r,6r)-3,4,5-三乙酰氧基-6(乙酰氧基甲基)四氢-2h-吡喃-2-基)氧基)-1,3-亚苯基)双(乙烯-2,1-二基))双(苯并[cd]吲哚-1-铵-2,1二基))双(丁烷-1-磺酸盐)。
[0041]
下面结合图1中所示的合成路线和具体的合成实施例来详细说明本发明提供的具有构建“诊疗一体化”药物的基于β-乳糖苷酶响应的近红外一区多功能荧光链接体的制备方法。
[0042]
参见图1,一种基于β-乳糖苷酶响应的多功能近红外一区荧光链接体的制备方法,包括以下步骤:
[0043]
a)2,3,4,6-四-o-乙酰基-α-d-吡喃半乳糖与5-醛基水杨醛在k2co3的作用下,得到带有二醛基的中间体;
[0044]
所述步骤a)的具体操作为:
[0045]
将2,3,4,6-四-o-乙酰基-α-d-吡喃半乳糖,5-醛基水杨醛和k2co3在dmf中于0℃混合n2气氛。将反应在室温下搅拌过夜,向混合物中加入h2o,得到带有二醛基的中间体;
[0046]
b)1,2-氧硫烷2,2-二氧化物与环己酮苯并[cd]吲哚-2(1h)-酮在koh的作用下,得到4-(2-氧代-1,2-二氢苯并[cd]吲哚-1-鎓-1-基)丁烷-1-磺酸钠;
[0047]
所述步骤b)的具体操作为:
[0048]
将1,2-氧硫烷2,2-二氧化物,koh溶于n-甲基-2-吡咯烷酮中,室温条件下搅拌30min,然后向反应体系中加入环己酮苯并[cd]吲哚-2(1h)-酮。接下来,将上述反应体系置于90℃下加热搅拌10h。待反应完全后,体系冷却至室温然后加入丙酮进行处理,体系析出结晶即可得到4-(2-氧代-1,2-二氢苯并[cd]吲哚-1-鎓-1-基)丁烷-1-磺酸钠。
[0049]
c)4-(2-氧代-1,2-二氢苯并[cd]吲哚-1-鎓-1-基)丁烷-1-磺酸钠在四丁基氯化铵的作用下,得到4-(2-氧代-1,2-二氢苯并[cd]吲哚-1-鎓-1-基)丁烷-1-磺酸-四丁基铵盐;
[0050]
所述步骤c)的具体操作为:
[0051]
将4-(2-氧代-1,2-二氢苯并[cd]吲哚-1-鎓-1-基)丁烷-1-磺酸钠,四丁基氯化铵溶于乙酸溶液中,将反应体系置于90℃搅拌30min。然后向上述反应体系中缓慢滴加乙酸乙酯,过滤除去kcl,将反应体系浓缩即可得到4-(2-氧代-1,2-二氢苯并[cd]吲哚-1-鎓-1-基)丁烷-1-磺酸-四丁基氯化铵盐。
[0052]
d)4-(2-氧代-1,2-二氢苯并[cd]吲哚-1-鎓-1-基)丁烷-1-磺酸-四丁基铵盐在ch3mgcl作用下,得到4-(2-甲基-4-苯并[cd]吲哚-1-基)丁烷-1-磺酸盐;
[0053]
所述步骤d)的具体操作为:
[0054]
将4-(2-氧代-1,2-二氢苯并[cd]吲哚-1-鎓-1-基)丁烷-1-磺酸-四丁基氯化铵盐,ch3mgcl溶于无水四氢呋喃中。在氮气保护下,将上述反应体系置于60℃中搅拌1h,待反应体系冷却后加入1mol/l盐酸进行中和,并利用乙醇和乙醚对上述反应体系进行稀释。接下来,将上述反应体系冷却至0℃至过夜析出,该析出的结晶即为4-(2-甲基-4-苯并[cd]吲哚-1-基)丁烷-1-磺酸盐。
[0055]
e)4-(2-甲基-4-苯并[cd]吲哚-1-基)丁烷-1-磺酸盐与带有二醛基的中间体在(ch3co)2o作用下得到基于β-乳糖苷酶响应的多功能近红外一区荧光链接体。
[0056]
所述步骤e)的具体操作为:
[0057]
在室温条件下,将带有二醛基的中间体,4-(2-甲基-4-苯并[cd]吲哚-1-基)丁烷-1-磺酸盐以及乙酸钠溶于乙酸酐溶液中,将反应体系置于50℃油浴中搅拌3h。待反应完成后,向上述反应体系中加入10倍体积的h2o,然后通过ch2cl2进行萃取,收集有机相。然后,向体系中加入饱和nahco3进行洗涤,收集有机相,然后利用饱和nacl(进行洗涤,收集有机相。最后,加入适量na2so4室温搅拌4h,利用旋转蒸发仪进行浓缩,进而利用60-100目硅胶进行拌样,经色谱柱纯化(二氯甲烷:甲醇(v:v)=10:1)即可得到基于β-乳糖苷酶响应的近红外
一区多功能荧光链接体。
[0058]
上述含有基于β-乳糖苷酶响应的近红外一区多功能荧光链接体在构建“诊疗一体化”药物方面的应用。
[0059]
实施例1
[0060]
一种基于β-乳糖苷酶响应的近红外一区多功能荧光链接体的制备方法,如图1所示,包括如下步骤:
[0061]
a)2,3,4,6-四-o-乙酰基-α-d-吡喃半乳糖与5-醛基水杨醛在k2co3的作用下,得到带有二醛基的中间体,具体过程如下:
[0062]
将2,3,4,6-四-o-乙酰基-α-d-吡喃半乳糖(2.00g,4.86mmol),5-醛基水杨醛(0.82g,4.86mmol)和k2co3(1.02g,7.29mmol)在dmf(20ml)中于0℃下,在n2气氛下,将反应在室温下搅拌过夜,向混合物中加入h2o(40ml),得到带有二醛基的中间体。
[0063]
b)1,2-氧硫烷2,2-二氧化物与环己酮苯并[cd]吲哚-2(1h)-酮在koh的作用下,得到4-(2-氧代-1,2-二氢苯并[cd]吲哚-1-鎓-1-基)丁烷-1-磺酸钠,具体过程如下:
[0064]
将1,2-氧硫烷2,2-二氧化物(0.85g,0.0050mol),koh(0.56g,0.0100mol)溶于10ml n-甲基-2-吡咯烷酮中,室温条件下搅拌30min,然后向反应体系中加入环己酮苯并[cd]吲哚-2(1h)-酮(0.75g,0.0055mol)。接下来,将上述反应体系置于90℃下加热搅拌10h。待反应完全后,体系冷却至室温然后加入丙酮进行处理,体系析出结晶即可得到4-(2-氧代-1,2-二氢苯并[cd]吲哚-1-鎓-1-基)丁烷-1-磺酸钠。
[0065]
c)4-(2-氧代-1,2-二氢苯并[cd]吲哚-1-鎓-1-基)丁烷-1-磺酸钠在四丁基氯化铵的作用下,得到4-(2-氧代-1,2-二氢苯并[cd]吲哚-1-鎓-1-基)丁烷-1-磺酸-四丁基铵盐,具体过程如下:
[0066]
将4-(2-氧代-1,2-二氢苯并[cd]吲哚-1-鎓-1-基)丁烷-1-磺酸钠(1.50g,5mmol),四丁基氯化铵(1.51g,5.5mmol)溶于8ml乙酸溶液中,将反应体系置于90℃搅拌30min。然后向上述反应体系中缓慢滴加乙酸乙酯,过滤除去kcl,将反应体系浓缩即可得到4-(2-氧代-1,2-二氢苯并[cd]吲哚-1-鎓-1-基)丁烷-1-磺酸-四丁基氯化铵盐
[0067]
d)4-(2-氧代-1,2-二氢苯并[cd]吲哚-1-鎓-1-基)丁烷-1-磺酸-四丁基铵盐在ch3mgcl作用下,得到4-(2-甲基-4-苯并[cd]吲哚-1-基)丁烷-1-磺酸盐,具体过程如下:
[0068]
将4-(2-氧代-1,2-二氢苯并[cd]吲哚-1-鎓-1-基)丁烷-1-磺酸-四丁基氯化铵盐(2.32g,5mmol),ch3mgcl(7.5ml,22.5mmol)溶于20ml无水四氢呋喃中。在氮气保护下,将上述反应体系置于60℃中搅拌1h,待反应体系冷却后加入1mol/l盐酸进行中和,并利用乙醇(15ml)和乙醚(20ml)对上述反应体系进行稀释。接下来,将上述反应体系冷却至0℃至过夜析出,该析出的结晶即为4-(2-甲基-4-苯并[cd]吲哚-1-基)丁烷-1-磺酸盐。。
[0069]
e)4-(2-甲基-4-苯并[cd]吲哚-1-基)丁烷-1-磺酸盐与带有二醛基的中间体在(ch3co)2o作用下得到基于β-乳糖苷酶响应的多功能链接体,具体过程如下:
[0070]
在室温条件下,将带有二醛基的中间体(0.92g,1.915mmol),4-(2-甲基-4-苯并[cd]吲哚-1-基)丁烷-1-磺酸盐(1.23g,4.059mmol)以及乙酸钠(0.19g,2.317mmol)溶于5ml乙酸酐溶液中,将反应体系置于50℃油浴中搅拌3h。待反应完成后,向上述反应体系中加入10倍体积的h2o(50ml),然后通过ch2cl2(20ml
×
3)进行萃取,收集有机相。然后,向体系中加入饱和nahco3(20ml
×
3)进行洗涤,收集有机相,然后利用饱和nacl(20ml
×
3)进行洗
涤,收集有机相。最后,加入适量na2so4室温搅拌4h,利用旋转蒸发仪进行浓缩,进而利用60-100目硅胶进行拌样,经色谱柱纯化(二氯甲烷:甲醇(v:v)=10:1)即可得到基于β-乳糖苷酶特异性响应的荧光链接体。重0.56g,收率28.61%,得到基于β-乳糖苷酶响应的近红外一区多功能荧光链接体。
[0071]
lc-ms(esi,m/z):1023.34[m+h]
+
,1021.69[m-h]
‑‑
。
[0072]
基于β-乳糖苷酶特异性响应的近红外一区荧光链接体在制备用于治疗肿瘤的诊疗一体化药物方面的应用。其应用范围较广,为一类通用型的基于β-乳糖苷酶特异性响应的近红外一区多功能荧光链接体,可以用于修饰具有抗肿瘤活性的活性生物小分子如索拉菲尼,索拉菲尼等,也可以用于修饰具有治疗作用的单克隆抗体药物分子,例如抗血管生成类单克隆抗体药物贝伐珠单抗等,pd1/pdl1单克隆抗体药物阿替珠单抗等。在本发明中应用实施例验证只考察了索拉菲尼,其具有显著的抗血管生成作用,对神经胶质瘤表现出较强的杀伤作用。
[0073]
本发明利用基于β-乳糖苷酶响应的近红外一区多功能荧光链接体化学修饰靶向抗肿瘤药物分子bd7,构建了bd7“诊疗一体化”药物分子,并且利用其对一些肿瘤细胞进行示踪定位成像分析及活性筛选。
[0074]
bd7“诊疗一体化”药物分子的构建,如图2所示:
[0075]
在0℃条件下,将二硫基二乙酸(1.27g,7.00mmol),edc
·
hcl(0.64g,3.36mmol),hobt(0.45g,3.36mmol)溶于无水二氯甲烷中(20ml),搅拌30min。然后,向上述混合体系中加入bd7(0.50g,1.40mmol)。接下来,将其置于室温下搅拌过夜,期间利用tlc进行监测反应进程直至反应完全。最后,分别通过h2o(20ml
×
3),饱和nahco3(20ml
×
3)进行洗涤,收集有机相,然后利用饱和nacl(20ml
×
3)进行洗涤,收集有机相。最后,加入适量na2so4室温搅拌4h,利用旋转蒸发仪进行浓缩,进而利用60-100目硅胶进行拌样,经色谱柱纯化(石油醚:乙酸乙酯(v:v)=1:3)即可得到中间体1。
[0076]
冰浴条件下,将中间体1(0.24g,0.46mmol),pybop(0.24g,0.46mmol)溶于无水二氯甲烷中(20ml)中,缓慢滴加三乙胺(0.094g,0.92mmol)后搅拌3min,然后向反应体系中加入乙二胺(13μl,0.23mmol),接下来,将其置于室温下搅拌过夜,期间利用tlc进行监测反应进程直至反应完全。最后,分别通过h2o(20ml
×
3),饱和nahco3(20ml
×
3)进行洗涤,收集有机相,然后利用饱和nacl(20ml
×
3)进行洗涤,收集有机相。最后,加入适量na2so4室温搅拌4h,利用旋转蒸发仪进行浓缩,进而利用60-100目硅胶进行拌样,经色谱柱纯化(石油醚:乙酸乙酯(v:v)=1:3)即可得到中间体2。
[0077]
将中间体2(0.05g,0.09mmol),荧光链接体(0.18g,0.18mmol),dmap(0.02g,0.18mmo)溶于无水dmf(5ml)中。接下来,将上述反应混合物置于40℃油浴锅中搅拌反应12h,tlc检测反应直至反应完全。进而,加入10倍体积的h2o(50ml),然后通过ch2cl2(20ml
×
3)进行萃取,收集有机相。然后,向体系中加入饱和nahco3(20ml
×
3)进行洗涤,收集有机相,然后利用饱和nacl(20ml
×
3)进行洗涤,收集有机相。最后,加入适量na2so4室温搅拌4h,利用旋转蒸发仪进行浓缩,进而利用60-100目硅胶进行拌样,经色谱柱纯化(乙酸乙酯:甲醇(v:v)=1:1)即可得到bd7双功能分子,即bd7“诊疗一体化”药物分子。
[0078]
含有基于β-乳糖苷酶响应的近红外一区多功能荧光链接体构建的“诊疗一体化”靶向抗肿瘤药物分子在特异性标记方面的应用。
[0079]
在此,通过细胞成像实验,对其特异性标记β-乳糖苷酶高表达的细胞(skov3,卵巢癌细胞)以及低表达的细胞(ea.hy926,人脐血管内皮细胞)进行成像分析。
[0080]
具体实操步骤:
[0081]
1)细胞种板:每孔细胞密度为4.3*105细胞/ml,37℃孵育过夜;
[0082]
2)细胞给药:每孔探针浓度为4μmol/l,37℃孵育2h;
[0083]
3)洗涤:利用pbs洗涤三次细胞,除去过量探针分子;
[0084]
4)细胞固定:洗涤完成后,在室温下,在细胞中加入1ml 3.7%多聚甲醛(925μl 4%多聚甲醛+75μl pbs),固定30min,用pbs洗涤两次(轻微搅拌1-2分钟),并在室温下用含有0.1%triton x-100的pbs溶液透化10min。然后用pbs将细胞洗涤两次,缓慢搅拌1min,在室温下,用含2%bsa的pbs(含0.05%tween-20)封闭30min,并用pbs(含0.05%tween-20)洗涤两次。每次5min,轻轻晃动。
[0085]
5)封片:在各组加入5μl抗荧光淬灭封片剂,周围加指甲油封片。
[0086]
6)荧光显微镜进行检测:细胞成像结果如图2所示,探针浓度为0.1μmol/l,从图3中的(a)-(h),可以看出,skov3细胞(β-乳糖苷酶高表达)被荧光特异性标记,说明构建的探针可以实现“诊疗一体化”中的标记即诊断一步。
[0087]
含有基于β-乳糖苷酶响应的近红外一区多功能荧光链接体构建的“诊疗一体化”靶向抗肿瘤药物分子在抗肿瘤活性方面的应用。
[0088]
利用上述设计合成的bd7“诊疗一体化”药物分子对ea.hy926细胞(人脐血管静脉细胞)、a549(肺癌细胞)、hepg2(人肝癌细胞)、skov3(人卵巢癌细胞)、b16细胞(黑色素瘤细胞)进行增殖抑制分析评价。
[0089]
利用mtt对其进行活性评价:
[0090]
1)细胞种板:96孔板种板,每孔细胞密度为1*105细胞/ml,每孔加入180μl细胞悬液,37℃孵育过夜。
[0091]
2)细胞给药:设置6个浓度梯度,分别为20μmol/l,4μmol/l,0.8μmol/l,0.16μmol/l,0.032μmol/l,0.0064μmol/l,每孔加入20μl,37℃孵育24h;
[0092]
3)细胞给mtt:每孔加入22μmol/l,37℃孵育4h;
[0093]
4)细胞处理:吸去每孔液体,加入150μl dmso,室温于摇床上孵育10min。
[0094]
5)吸光度测定:将96孔板置于酶标仪上测定其在490nm处的吸光度。
[0095]
6)抑制率计算:抑制率=阴性孔od-给孔od/阴性孔od-空孔白od
[0096]
细胞增殖抑制结果如图4所示,构建的探针分子表现出与阳性药物分子近似的抗细胞增殖活性,即可表明构建的药物探针分子可以实现“诊疗一体化”概念中治疗一步。
[0097]
本发明通过引入靶向药物作为靶向分子,同时,为了保证药物分子的治疗活力,引入基于肿瘤微环境高还原响应的二硫键作为可释放性基团构建“诊疗一体化”的双功能分子,便可实现对卵巢癌的高效标记以及治疗于一体的目的。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1